La reumatología es una subespecialidad de la medicina interna que estudia y trata pacientes con problemas músculo esqueléticos, así como también enfermedades autoinmunes que comprometen el mesenquima y diferentes órganos, teniendo en común un rol patogénico del sistema inmune.
El laboratorio juega un papel importante en el proceso diagnóstico de estas condiciones. Sin embargo, a pesar del progreso y refinamiento de algunos exámenes, la baja sensibilidad y especificidad que muchos de ellos tienen, hacen que la interpretación sea ocasionalmente muy difícil.
En este artículo se revisan algunas características de los exámenes más comúnmente usados en reumatología, así como su sensibilidad y especificidad en el diagnóstico de estas enfermedades. Ya que la correcta interpretación de un examen requiere una compresión de conceptos estadísticos subyacentes, se revisan en forma muy somera algunos aspectos de ellos.
Como conclusión, se remarca la necesidad de cuidar la interpretación de estos resultados, para evitar lo más que se pueda el costo económico, el stress psicológico y el problema médico derivado de la mala interpretación de estos exámenes.
Rheumatology is a medical subspecialty that takes care of some non traumatic musculoskeletal problems as well as many autoimmune diseases that involves the integuments and different organs, having as a common issue a pathogenic role of the immune system.
Laboratory plays an important role in the diagnosis process of these conditions. However, despite the progress and refinement of some test, lack sensitivity and specificity makes interpretation of them occasionally quite difficult.
Some characteristic, disease association as well as sensitivity and specificity are reviewed here for the most common rheumatic test. Since part of a correct interpretation of a test, needs an understanding of statistical principles underneath it, in a very simple way some of them are also considered in this review.
As a conclusion, an underscoring of the need to process cautiously the rheumatic test results is made, to avoid as much as it can, unnecessary test and the burden both economically, psychological and medically an incorrect diagnosis, based on a misinterpretation of a test.
La reumatología es una rama de la medicina interna, que tiene varias particularidades que la hacen especialmente compleja, entre ellas:
- 1.
Existe una gran sobreexposición de síntomas y signos entre las distintas enfermedades.
- 2.
Muchas enfermedades de etiología distintas pueden dar la misma constelación de síntomas y signos.
- 3.
Los exámenes de apoyo diagnóstico en su gran mayoría no son patognomónicos de la enfermedad, son difíciles de realizar y de interpretar y no están disponibles en todas partes.
- 4.
La prevalencia de un número importante de las patologías reumatológicas son de baja prevalencia, lo que hace que la experiencia individual en el diagnóstico y manejo para aquellos no dedicados a la especialidad sea baja y por otro lado el comportamiento estadístico de los exámenes diagnósticos es pobre.
- 5.
El diagnóstico de un importante grupo de patologías reumatológicas se hace mediante criterios de diagnóstico establecidos por grupos o sociedades científicas, lo que requiere conocer estos criterios y el comportamiento de estos criterios de diagnóstico (vale decir su sensibilidad, especificidad, etc.).
Tomando en consideración lo anterior, en este artículo revisaremos los exámenes diagnósticos más usados en reumatología y veremos algunos aspectos generales de su aplicación en el proceso de diagnóstico de estas enfermedades.
Factor reumatoide (FR)Este examen es posiblemente uno de los más antiguos en el diagnóstico reumatológico. Se basa en la detección de inmunoglobulina, generalmente de tipo IgM dirigidos contra fragmento Fc de la IgG. Se han descrito también factor reumatoide IgA e IgG cuyo rol diagnóstico no es claro. Las técnicas mediante las cuales se realiza han ido evolucionando con el tiempo y hoy día se realizan mediante técnicas de ELISA cuantitativas o mediante técnicas de precipitación, las cuales se expresan como dilución (títulos de dilución). El FR tiene una sensibilidad en enfermedad establecida del orden de 70% y en enfermedad precoz del orden de 50%. El gran problema del FR en el diagnóstico de AR es que existen un número importante de situaciones en las cuales puede haber un falso positivo. En general cualquier situación en la que hay estímulo persistente para la producción de complejos inmunes e hipergamaglobulinemia, puede producir un FR, como por ejemplo:
- -
Enfermedades inflamatorias crónicas
- -
Infecciones
- -
Neoplasias
- -
Enfermedades linfoproliferativas
- -
Crioglobulinemia
- -
Edad
Adicionalmente y para hacer el proceso diagnóstico más complejo en muchas de estas situaciones puede haber artritis que simula una AR:
- -
Tuberculosis
- -
Endocarditis Bacteriana
- -
Crioglobulinemia Mixta Esencial por infección por Virus Hepatitis C
En consecuencia el valor diagnóstico de un FR es bajo y requiere un buena suma de sospecha clínica, examen físico e historia bien realizados para poder hacer el diagnóstico.
Una vez establecido el diagnóstico de AR, el FR no tiene un rol importante en el seguimiento de la enfermedad y no hay buenas razones para solicitar este examen más allá de establecer el diagnóstico. En otra enfermedad en que frecuentemente se ve elevado el FR, como es el síndrome de Sjögren, una caída en los títulos de FR puede ser un aviso de la aparición de una enfermedad linfoproliferativa en este contexto.
Anticuerpos anti péptido cíclico citrulinado (CCP)Desde hace algunos años se cuenta con un nuevo test diagnóstico para AR, que se basa en determinación de proteínas citrulinadas. Se ha especulado que al citrulización de algunas proteínas como la filagrina podría hacer que éstas se volvieran antigénicas y eventualmente jugar un rol patogénico en esta enfermedad. Independiente, sin embargo de lo anterior, la determinación de la presencia de anticuerpos dirigidos contra péptidos citrulinados ha demostrado ser una potente herramienta diagnóstica en AR, especialmente en aquellos cuadros de presentación temprana. La sensibilidad del examen es de 60 a 70% en etapa temprana, aumentando a 60 a 80% en pacientes con la enfermedad establecida y con una especificidad de 80 a 95%.
Una observación muy interesante es que la presencia de ambos test positivos, FR y anti-CCP tiene un valor positivo predictivo de casi 100%, por lo que su valor en el diagnóstico es muy importante y según algunos autores la presencia de ambos marcadores podría ocurrir antes que la aparición clínica de la enfermedad, lo que abriría la oportunidad potencial de tratar la enfermedad antes de su aparición clínica.
Anticuerpos antinuclearesEstos anticuerpos se detectan normalmente usando inmunofluorescencia indirecta. Pretenden identificar la presencia en suero del paciente de anticuerpos dirigidos contra componentes del núcleo de células. Actualmente las células en uso son de una línea denominada Hep-2. Utilizando estas células y la técnica de IFI se pueden definir varios patrones o tipos de fluorescencia y se puede determinar la concentración de éstos mediante diluciones progresivas.
Los patrones mejor reconocidos, aunque existen muchos cuyas asociaciones con enfermedades no es muy clara o poco conocida, son:
Homogéneo: Que es el más inespecífico, pero el más común de observar.
Periférico: Es infrecuente, pero su presencia debe orientar fuertemente a un lupus eritematoso sistémico.
Moteado: El cual orienta a la presencia de anticuerpos dirigidos contra proteínas no DNA del núcleo, y asociado muchas veces con la presencia de otros anticuerpos denominados anticuerpos contra antígeno extractables nucleares o ENA. Se pueden observar en muchas condiciones pero su asociación más habitual es con lupus o síndrome de Sjögren.
Nucleolar: Es infrecuente y su presencia orienta a cuadros como las polidermatomiositis.
Adicionalmente se pueden identificar patrón anticentrómero, el cual es característico de la esclerodermia limitada o enfermedad de CREST.
Este examen tiene la ventaja de tener un bajo costo, pero la desventaja de depender del observador y de la poca especificidad. En títulos bajos hasta un 30% de población sana puede tener un falso positivo de estos exámenes. Mientras mayor es el título, se gana especificidad en el sentido que la presencia de una enfermedad autoinmune es más probable. Con la excepción de los anticuerpos anticentrómero y el patrón periférico, la asociación con enfermedades específicas no es muy buena, y pueden verse en tiroiditis autoinmune, enfermedades hepáticas, uso de medicamentos, infecciones, fibromialgia, etc. En consecuencia la presencia de estos anticuerpos, especialmente cuando los títulos son menores a 1/80 debe interpretarse con precaución y tener presente la alta tasa de falsos positivos.
Anticuerpos anti antígenos extractables nucleares (ENA)Estos anticuerpos se detectan actualmente por una técnica de ELISA, y permite identificar los siguientes antígenos:
Anti Ro, asociado a Sjögren y Lupus
Anti La asociado a Sjögren y Lupus
Anti Sm muy especifico de Lupus
Anti RNP marcador de la Enfermedad Mixta del Tejido Conectivo
Anti SCL-70 se asocia fuertemente con esclerodermia difusa.
Anti Jo-1, asociado a una variante de las dermatomiositis denominado síndrome antisintetasa.
La presencia de estos anticuerpos tiene mayor valor diagnóstico que los ANA, ya que la presencia de falsos positivos es mucho más rara.
Anticuerpos anti DNALa presencia de estos anticuerpos se hace generalmente por medio de IFI. Sin embargo existen otras dos técnicas en uso, la de ELISA y la por radioinmunoensayo, denominada para este caso técnica de Farr. La IFI ha sido validada ampliamente y es la técnica standard en la determinación de los anti-DNA. Es un examen relativamente barato, pero muy operador dependiente. La presencia de estos anticuerpos orienta fuertemente a un lupus.
Anticuerpos anticitoplasma de neutrófilos (ANCA)Estos anticuerpos se determinaron inicialmente en relación a vasculitis sistémica tipo Granulomatosis de Wegener o poliangeitis microscópica.
Se pueden determinar por medio de IFI, técnica que permite identificar dos patrones de fluorescencia, un patrón perinuclear, denominado consecuentemente ANCAp y uno citoplasmático denominado ANCAc. Ambos patrones reflejan la presencia de anticuerpos dirigidos contra diferentes antígenos: el ANCAc contra una serin proteasa de los gránulos primarios de los neutrófilos, denominada serin proteasa 3, y en consecuencia este anticuerpo se conoce como anti PR3 y el ANCAp dirigido contra una pleyada de proteínas intracitoplasmáticas residentes de los gránulos de los neutrófilos. El ANCAp asociado a vasculitis se dirige contra la mielperoxidasa y se le conoce como anti MPO. Sin embargo otros antígenos también pueden dar el aspecto de ANCAp o de una fluorescencia mixta denominado ANCA atípico, el cual se asocia entre otras con enfermedades inflamatorias intestinales, especialmente la colitis ulcerosa. Los antígenos asociado son catepsina G, lactoferrina, elastasa y BPI.
Estos anticuerpos particularmente el ANCAp tiene una especificidad baja y aparecen positivos en numerosas situaciones, no solo en vasculitis. Estos anticuerpos se pueden detectar no solo mediante IFI sino también por ELISA, lo que permite identificar antígenos específicos, lo que evidentemente aumenta el rol diagnóstico del examen. La técnica de IFI es muy difícil de interpretar y requiere un observador entrenado. Este hecho, sumado a la sobreposición que se ha descrito entre el patrón de fluorescencia y los diversos antígenos, es que se sugiere que un ANCA positivo por IFI deba ser evaluado siempre con un ANCA por ELISA, de esta forma se puede tener mayor certeza que existen anticuerpos dirigidos contra los antígenos esperados en estos cuadros clínicos. Los cuadros asociados a ANCA PR3 y MPO son principalmente vasculitis sistémica del tipo de Granulomatosis de Wegener (PR3), poliangeitis microscópica (MPO), glomerulonefritis rápidamente progresiva (MPO) y menos común en Churg-Strauss y muy raro en poliarteritis nodosa clásica. Debe tenerse presente que dado que en estas enfermedades en especial en relación con GW de tipo localizado, la sensibilidad de los ANCA es mala, no superando el 50%, por lo tanto la ausencia de ANCA no descarta el diagnóstico. Por otro lado un cuadro sistémico con compromiso renal y ANCA negativo debe hacer sospechar otra etiología.
El rol del seguimiento de estos anticuerpos ha sido materia de controversia a lo largo del tiempo. En algunos pacientes es evidente que los títulos de los ANCA siguen la actividad clínica de la enfermedad y el aumento de éstos es seguido por un rebrote de la enfermedad. Para algunos el aumento de título de estos anticuerpos debiera llevar a un cambio de conducta terapéutica, sin embargo sobre este punto no hay un acuerdo universal, y parece más prudente la sugerencia de un control más cercano en aquellos individuos en los cuales se identifica un aumento de los títulos de los anticuerpos.
ComplementoEl complemento es una parte del sistema inmune, el cual interviene en los mecanismos de defensa frente a agresiones de diversas índoles. El complemento está formado por una serie de proteínas las cuales se activan en forma secuencial, dando finalmente origen a proteínas con acción deletérea sobre membranas plasmáticas, pero adicionalmente el complemento al unirse a anticuerpos forma complejos inmunes, los cuales son reconocidos por células del sistema retículo-macrofágico y “retirados” de circulación. El depósito tisular, sin embargo puede dar comienzo a un proceso inflamatorio, el cual es parte de los mecanismos involucrados en la patogénesis de algunas de las enfermedades autoinmunes. Es interesante desde punto de vista recordar que alteraciones genéticas asociadas a un mal “funcionamiento” de este sistema proteico y por ende a un defectuoso aclaramiento de complejo inmunes, se asocia con la aparición de fenómenos mediados por anticuerpos como lupus. El complemento se puede activar por dos vías principales: la denominada vía alterna o de la properdina, dentro de cuyos mecanismos de activación incluye a proteínas y componente de las membranas bacterianas y la vía clásica la cual es activada por la presencia de complejos inmunes. En la práctica cotidiana, se determina la concentración de C4 y C3. C3 es una vía final común a la activación del complemento por ambas vías tanto la clásica como la alterna y por lo tanto puede disminuir tanto en infecciones como en activación por complejos inmunes. C4 es una proteína propia de la vía clásica y su disminución implica una activación por la vía de complejos inmunes. En otras situaciones clínicas puede ser de interés la determinación de otros componente del complemento, tal como el CH50, el cual es un reflejo del “funcionamiento” global del complemento, ya que mide la capacidad de hemolizar el 50% del sustrato usada para su determinación, el cual depende de haber formado la cascada terminal C5-C9 para que ocurra. En enfermedades autoinmunes es raramente solicitado, sin embargo en estudio de algunas inmunodeficiencias puede ser más importante.
El lupus es sin duda el estereotipo de las enfermedades en las cuales el complemento juega un papel patogénico y también aquella en que la determinación de los niveles de complemento es más importante en el diagnóstico y seguimiento. Es frecuente que mientras más activa la enfermedad (y por ende mayor concentración de complejo inmunes) menor sea la concentración de los niveles de complemento en sangre. Sin embargo al igual que en otras situaciones clínicas, esto no es siempre así y no es inhabitual encontrar pacientes en los cuales los niveles de complemento están permanentemente disminuidos. Una potencial explicación es que se trate de pacientes con defectos genéticos del complemento. En situaciones en las cuales se logra correlacionar la actividad clínica de la enfermedad con los niveles de complemento, el seguimiento de estos puede ser útil.
Si bien en cualquier situación en la cual aumente la concentración de complejos inmunes puede haber un descenso de los niveles de complemento, es en lupus que la determinación de éstos tiene utilidad clínica. En otros cuadros su utilidad es más limitada. Una condición interesante a considerar es en aquellos pacientes con síndrome de Sjögren, en los cuales la disminución persistente de C4 se asocia con la evolución a linfoma.
Sindrome antifosfolipídicoEl síndrome antifosfolipídico es la trombofilia adquirida más frecuente. Sus manifestaciones clínicas pueden ser variadas e incluir trombosis venosa o arteria, pérdidas fetales recurrentes, infertilidad, livedo reticularis, trombocitopenia y otras alteraciones menos comunes incluyendo la dramática presentación del síndrome antifosfolipídico catastrófico. Este último es un cuadro clínico de alta mortalidad, caracterizado por trombosis en 3 órganos en forma simultanea, generalmente incluyendo falla renal, anemia hemolítica y trombocitopenia.
El diagnóstico se establece por la detección de anticuerpos y por pruebas funcionales de coagulación.
Los anticuerpos más comúnmente detectados son las anticardiolipinas de clase IgG e IgM en títulos moderados o elevados. Este examen se realiza mediante un técnica de ELISA y detecta los anticuerpos dirigidos contra fosfolípidos de membrana asociados a un cofactor. El test permite cuantificar la cantidad de anticuerpos, lo cual se expresa como unidades estandarizadas. Se define como títulos moderados sobre 40 U y altos sobre 80 U. Títulos menores tienen una baja asociación con el síndrome antifosfolipídico, sin embargo esto debe ser analizado paciente a paciente. De acuerdo a los criterios de diagnóstico actualmente en uso se requieren al menos dos determinaciones distanciadas por 3 meses para considerar el examen como positivo. Esto dado que la detección de anticuerpos en forma transitoria no es infrecuente, más aun en títulos bajos y no son suficientes para definir un síndrome antifosfolipídico.
Otro test de utilidad diagnóstico es la detección de anticuerpos contra beta glicoproteína I. También se determina por medio de una técnica de ELISA, sin embargo no hay un nivel de corte que defina significancia, como si la hay para las anticardiolipinas, por lo que cualquier positivo debe considerarse positivo.
El otro test que completa la trilogía de elementos que define un síndrome antifosfolipidos es el denominado anticoagulante lúpico. El nombre de este test se presta para confusiones, ya que su presencia confiere, al igual que los otros exámenes, un riesgo de trombosis. Este es un examen cualitativo en el cual se mide indirectamente la presencia de anticuerpos contra fosfolípidos por su capacidad de interferir con la cascada de coagulación y dar tiempo de sangría prolongado el cual no se corrige al agregar plasma normal (lo cual ocurriría si hubiera in déficit de algún factor de la coagulación alterado).
En suma, el cuadro de síndrome antifosfolipídico se define por la presencia de uno o más de los test mencionados. La presencia de dos o más en forma simultánea aumenta el riesgo de manifestaciones clínicas.
Algunos conceptos acerca de la interpretación de los exámenesTal como se mencionó anteriormente, una de las dificultades que tiene el uso de los exámenes en reumatología es que no son infrecuentes en la población sana y por otro lado las enfermedades autoinmunes son infrecuentes en la población.
Para comprender este problema, vale la pena recordar algunos conceptos básicos de estadística.
La sensibilidad se refiere a la capacidad de un test de detectar a individuos enfermos y la especifcidad se refere a la capacidad del test de detectar sanos. Es decir mientras más sensible un test quiere decir que es más frecuente en la población enferma… pero no discrimina a los sanos de enfermos de tal forma que ambos grupos podrían tener el examen positivo. Dicho de otra forma, es improbable que alguien esté enfermo si el test es negativo y muy sensible. Por otro lado, mientras más específico un test quiere decir que menos probable que resulte positivo en los sanos o dicho de otra forma es poco probable que alguien esté sano, teniendo el test positivo. Ambas condiciones, sensibilidad y especificidad, son propias del test y dependen del comportamiento de éste independiente de la población en que se estudie. Normalmente estos datos son provistos por los “fabricantes” del examen.
En la práctica médica, sin embargo lo que nos interesa contestar es si el paciente sentado frente a mi tiene o no tiene la condición que le estoy estudiando. La extrapolación de la sensibilidad y especificidad al paciente individual es lo que se conoce como valor predictivo (positivo o negativo). Para poder contestar esta pregunta me falta un dato muy importante: cuan frecuente o probable (prevalente) es la enfermedad que estoy pensando en la población que yo veo. Por ejemplo, supongamos que en una determinada población no existe la diabetes (solo una utopía), la presencia de un examen de glucosa alterado, representa un error… un falso positivo. Si por el contrario el 100% de esa población sufre de diabetes, entonces un examen normal es un falso negativo. Y ¿cómo relacionamos entonces, la sensibilidad y especificidad de un test con la prevalencia de la enfermedad?
Existen varias formas de relacionar estas variables:
- 1.-
a través de lo que se denomina valor positivo predictivo (o negativo) y
- 2.-
a través de los “likelihood ratios” o razones de verosimilitud (LR).
Valor Predictivo:
Podríamos definir el valor positivo predictivo (VPP) como la probabilidad que dado que el examen es positivo y considerando la probabilidad (prevalencia) de la enfermedad, el paciente tenga la enfermedad en estudio.
A la inversa, lo mismo aplica para el valor predictivo negativo (VPN).
Aunque siempre incomodan los números, la mejor forma de recordar estos conceptos es con un ejemplo:
De esta forma usemos un ejemplo de la vida real.
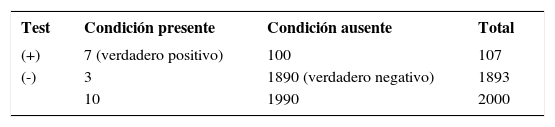
EL anti CCP tiene una sensibilidad de 70% y una especificidad de 95% y los datos poblaciones estiman que en Chile la Artritis Reumatoide tiene una prevalencia del orden de 0.5%.
Veamos entonces como se vería esta tabla si tomamos al azar 2000 personas chilenas (este número solo para hacer la tabla con enteros).
Es decir si tomo al azar 2000 chilenos y les hago un anti CCP y sale positivo, la probabilidad de que estén enfermos es de 0.06%. Por eso los exámenes reumatológicos, dada la baja prevalencia, son malos exámenes de screening (tamizaje).
Otra forma más sencilla de mirar los números es usar los denominados likelihood ratios o LR. Estos se estiman a través de la formula:
LR(+)= (sens)/(1-especificidad) o (a/(a+c))/(d(d+b))
El LR(-) es la contraparte= (1-sensibilidad)/especificidad.
Una de las virtudes de los LR es que un solo número reúnen la sensibilidad, especificidad y prevalencia.
Para el uso diagnóstico de los LR debemos recordar a Thomas Bayes, monje franciscano, que quiso probar matemáticamente la probabilidad de la existencia de Dios y se topó con una suerte de paradoja: la probabilidad de la existencia de Dios depende de la probabilidad a priori que se crea en Dios, de lo contrario no se puede. Es decir, solo aquellos que creen en Dios a priori pueden creer a posteriori. Siendo evidente su frustración, descartó sus estudios probabilísticos. Sin embargo, después de su muerte el prior del Monasterio, encontró que en los trabajos de Bayes, había elementos rescatables y los hizo públicos. Así nace, para fortuna nuestra, uno de los hechos, a mi modo de ver, más importante del proceso de diagnóstico médico: la capacidad que tengo de hacer de hacer un diagnóstico utilizando exámenes complementarios, depende de la capacidad de constituir una probabilidad a priori suficientemente elevada. Lo interesante de esto, es que solo se puede lograr a través de una buena anamnesis, examen físico y capacidad clínica. Es decir volvemos a nuestros años de semiología. No hay test disponible (al menos en reumatología) que permita elaborar un diagnóstico si no hemos mejorado nuestra probabilidad a priori de la enfermedad. ¿Cómo se relacionan estas variables? (en el fondo cual es Teorema de Bayes): Teorema de Bayes: P(E|+)= P(+|E)*P(E)/ P(S|+)/P(+|S)*P(S) En forma abreviada y llevándolo a nuestro tema de hoy: Probabilidad a posteriori= probabilidad a priori*LR Veamos un ejemplo: Supongamos el mismo test, antiCCP con el mismo ejercicio de tomar 2000 chilenos al azar.
Para un test con 70% de sensibilidad y una especificidad de 95%, el LR(+) es 14 y LR(-) es 0.3
La probabilidad a priori de alguien tomado al azar es la prevalencia de la enfermedad en el lugar en que estoy, por lo tanto asumiendo una prevalencia igual para todo Chile de 0,5%, entonces un CCP + es
Probabilidad a posteriori=0.005 x 14= 0.07 o 7% que es el mismo número al que llegamos con el ejercicio de cálculo a través de sensibilidad y especificidad, solo que aquí debemos recordar un numero… el LR. En distintos sitios de medicina basada en la evidencia encontraran LR para muchas condiciones.
Vean entonces que el LR (así como la sensibilidad y especificidad) son características propias del test y no se puede extrapolar directamente a su capacidad de diagnostico. Por lo tanto la única forma de mejorar la capacidad diagnóstica es aumentando la probabilidad a priori… ¿y cómo se hace esto? Bueno esta es la parte de “arte” de la medicina. Depende que yo pueda buscar elementos clínicos que me permitan asumir que determinado paciente tiene características que hacen más probable una artritis reumatoide, con lo cual, la probabilidad a posteriori será mayor. Y esto no es más que nuestra vieja amiga la historia clínica y la semiología.
Asociación de exámenes y diagnósticos en reumatología
| Examen | Patología |
|---|---|
| ANA | LES* |
| DNA | LES |
| Anti Ro | Sjögren, LES |
| Anti La | Sjögren, LES |
| Anti Sm | LES |
| Anti Scl-70 | Esclerodermia difusa |
| Anti RNP | Enfermedad Mixta del Tejido Conectivo |
| Anti Jo-1 | Dermatomiositis variedad anti-sintetasa |
| ANCAp o (MPO por ELISA) | PAM, GNRP |
| ANCAc o (PR3 por ELISA) | Granulomatosis de Wegener** |
| FR | Artritis Reumatoide* |
| Anti CCP | Artritis Reumatoide |
Como espero haberlo podido demostrar, los exámenes, al menos en reumatología, contienen la paradoja que necesitamos una clínica muy buena para que tengan valor diagnóstico.
El autor declara no tener conflictos de interés, con relación a este artículo.