En nuestra práctica nos resultan muy cercanos y familiares los programas estructurados de inmunizaciones para lactantes, preescolares y escolares (PNI=Programa Nacional de Inmunizaciones). Sin embargo, para la población adolescente y adultos jóvenes, no existe conciencia, ni menos un programa estatal de inmunizaciones para esta población. Por ello, están desprovistos de prestaciones organizadas y estructuradas en relación a vacunas.
El desarrollo de nuevas vacunas, acompañado de un avance tecnológico indiscutible, ha hecho posible contar hoy en día con nuevas vacunas plausibles de usar en adolescentes y adultos; tanto para reforzar la inmunidad adquirida por el PNI, como es el caso de difteria, tétanos, pertussis, o inmunizar para aquellas que no recibieron en la primera infancia como hepatitis B, parotiditis, rubéola, sarampión, polio etc.; o nuevas vacunas como hepatitis A o varicela y otras más recientes dirigidas espacia/mente a este grupo etáreo, como la vacuna para prevención de la infección por virus papiloma humano, la anti pertussis (a dosis adecuada para esta edad), y la anti menin-gocócica conjugada, según sea la necesidad epidemiológica.
Se agregan vacunas especiales en caso de viaje a zonas endémicas, como es el caso de rabia, encefalitis japonesa o fiebre amarilla; tema que no se incluye en este artículo, propio de la medicina del viajero, o tampoco el de aquellos con mayor susceptibilidad a infecciones específicas como las vacunas anti neumocócica 23 valente, anti meningocócica no conjugada o anti Hemophilus influenza b (Ej., Asplénicos, Hipogamaglobulinemia, S. nefrótico etc.).
In our clinical practice we are very close and familiar to the structured program of immunizations for infants, preschool and school children (NIP=National Immunization Program) but for teenagers and young adults, there is no awareness, let alone a state program of immunizations for this population, and therefore, there is the need to develop an organized and structured program in relation to vaccines for them.
The development of new vaccines, accompanied by an undeniable technological advance has made it possible to have today potential use in adolescents and adults, both to strengthen the Immunity acquired buy the NIP, as is the case of diphtheria, tetanus, pertussis or immunization for those who did not receive it at early childhood as hepatitis B, mumps, rubella, measles, polio etc., or new vaccines such as hepatitis A and chickenpox and other more recent, specially targeted for this age group, as is the vaccine for prevention of infection with human papilloma virus, anti pertussis, a suitable dose for this age, and meningococcal conjugate vaccine, depending on the epidemiological need. Added special vaccinations when traveling to endemic areas, such as rabies, Japanese encephalitis and yellow fever; issue not included in this article, typical of the travel medicine or either of those with increased susceptibility to specific infections, such as 23-valent pneumococcal vaccine, anti meningococcal unconjugated or anti Haemophilus influenzae b unconjugated vaccine (eg, asplenic, hypogammaglobulinemia, nephrotic syndrome etc)
Las vacunas han demostrado ser uno de los avances más sobresalientes en la medicina contemporánea y uno de los diez logros más relevantes en salud, en los dos últimos siglos. La mayoría de los países que se agrupan en la Organización Mundial de la Salud (OMS) han hecho enormes esfuerzos para introducir y aplicar programas de inmunizaciones especialmente dirigidos a recién nacidos, lactantes, preescolares y escolares (1).
Los adolescentes, que según la Academia Americana de Pediatría (AAP), la Academia de Médicos Americanos (AMA) y la Sociedad Chilena de Pediatría corresponden al grupo etáreo comprendido entre los 11 a 18 años e incluso hasta los 21 años de edad, han estado relegados, hasta hace algunos pocos años, a estos programas estructurados de inmunizaciones (1).
Hoy en día la atención integral de estos, debe incluir la utilización de vacunas que permitan la prevención de diversas enfermedades infecciosas, por ello, desde hace más de una década, numerosos países, especialmente desarrollados, están estableciendo programas organizados de inmunizaciones dirigidos a esta población en particular (2).
Es importante destacar entonces, que cuando asistimos a un adolescente, hay que concientizarlo sobre la importancia de recibir vacunas durante esa edad y posteriormente en la adultez; enfatizar acerca de la susceptibilidad que presenta el adolescente a numerosas enfermedades inmunoprevenibles, reafirmar su potencialidad como reservorio y estimular la indicación de vacunar según estos parámetros, tanto en forma individual como en la elaboración de programas en salud pública.
Es interesante recalcar que la aplicación de determinadas vacunas a un adolescente, especialmente si es mujer, también lleva implícito la potencial protección a su descendencia. (Ej: rubéola, tétanos, hepatitis B, etc.). En América Latina 100 de cada 1.000 mujeres adolescentes son madres cada año (2).
El análisis de los calendarios actuales de vacunación nos permite deducir que los adolescentes se encuentran a mitad de camino entre los calendarios de vacunación infantil y el de los del adulto. Esta indefinición, junto con las especiales características psicosociales de los mismos, y la falta de programas universales definidos, en la mayoría de los países, son probablemente los factores que condicionan las bajas tasas de cobertura en esta población.
La dificultad que supone captar adolescentes para cualquier programa sanitario obliga a ser flexibles tanto en los horarios como en las citaciones, ser creativos en la puesta en práctica de programas de vacunación a adolescentes y que ellos resulten atractivos para tener una mejor adherencia y cobertura.
Tener presente que cuando sea necesario, es deseable administrar múltiples vacunas, planificar, priorizando, cuáles son las que se pondrán en cada visita. Procurando siempre no desaprovechar las oportunidades de vacunar, las cuales podrían estar condicionadas al cumplimiento de un determinado programa, como por ejemplo, para postular, ya sea a un trabajo laboral, a la entrada a una determinada institución o al ingreso a un centro de estudios superiores.
En Chile no existe un programa establecido para adolescentes; pero comercialmente se distribuyen la mayoría de ellas. Es importante destacar que es necesario introducir la necesidad de estas inmunizaciones en esta población y disminuir la falencia que ello representa, especialmente referido a los refuerzos (Booster) para tétanos cada diez años, inmunizar para hepatitis a y b, aquellos que no la recibieron en el periodo de lactante y ofrecer las nuevas como es el caso de pertussis y papiloma humano.
El objetivo del presente artículo tiene como razón principal insistir en la necesidad de introducir, en nuestro medio, el concepto y la necesidad de programar vacunas en la población adolescente, analizar las actuales recomendaciones de inmunización en estos pacientes y profundizar en las indicaciones, los riesgos y beneficios de las más representativas e importantes de ellas, especialmente la anti pertussis a dosis adecuada, la anti virus del papiloma humano y según epidemiología, la anti meningocócica; para poder entender y prescribirlas en futuras indicaciones, tanto personales como de salud pública.
Vacunas en la adolescenciaLas vacunas internacionalmente recomendadas a esta edad por la OMS son la vacuna anti hepatitis B, si no ha sido aplicada anteriormente, los refuerzos de la tresvírica (parotiditis, rubéola y sarampión), la anti varicela (dosis inicial y según epidemiología en el futuro, probable refuerzo, cinco años después), toxoíde diftérico-tetánico y la antipertussis en la dosis adecuada para esta edad (Tdap) (3).
Para casos especiales la antineumocócica no conjugada 23 valente, la anti-influenza anual, la anti-hepatitis A, si no ha sido administrada y dos nuevas vacunas, la antimeningocócica conjugada cuadrivalente y la anti virus papiloma humano (3).
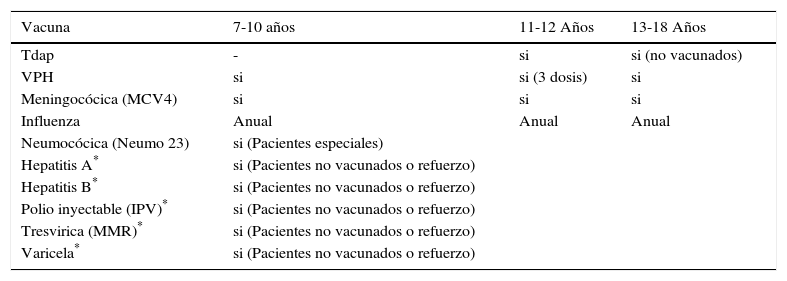
Frente a estas recomendaciones varios países, en su mayoría desarrollados, han incorporado esquemas oficiales para adolescentes, como parte de sus programas nacionales, como por Ej., el programa de vacunación de adolescentes en EEUU (cuadro 1) (3).
Programa recomendado de inmunizaciones entre 7 a 18 años E.E.U.U 2010**
| Vacuna | 7-10 años | 11-12 Años | 13-18 Años |
|---|---|---|---|
| Tdap | - | si | si (no vacunados) |
| VPH | si | si (3 dosis) | si |
| Meningocócica (MCV4) | si | si | si |
| Influenza | Anual | Anual | Anual |
| Neumocócica (Neumo 23) | si (Pacientes especiales) | ||
| Hepatitis A* | si (Pacientes no vacunados o refuerzo) | ||
| Hepatitis B* | si (Pacientes no vacunados o refuerzo) | ||
| Polio inyectable (IPV)* | si (Pacientes no vacunados o refuerzo) | ||
| Tresvirica (MMR)* | si (Pacientes no vacunados o refuerzo) | ||
| Varicela* | si (Pacientes no vacunados o refuerzo) |
Se estima que en Chile más del 90% de la población infantil recibe cinco dosis de DPT (difteria, pertussis a células enteras, tétanos) y una dosis de dT (toxoíde tetánico, diftérico) en segundo año básico. Esto ha dado como resultado una baja sustancial de casos y una drástica disminución de las tasas de difteria, tétanos y coqueluche en la población chilena (4).
De más de 10.000 casos de coqueluche entre los años 76-77, con tasas de 101,5 a 95,4 por 100.000 habitantes se produce una importante disminución a 1.200 casos el año 2006 con una tasa de 7,7. En difteria, desde el año 1997 que no se reporta ningún caso y en tétanos desde al año 2002 se reportan entre 7 a 11 casos anuales (4).
La inmunogenicidad para la tos ferina, conferida por esta vacuna, la DPT, es superior al 80% con la administración de 3 dosis. Sus niveles protectores no están bien establecidos y no está claro cual o cuales de los componentes inducen inmunoprotección. Con cuatro dosis disminuye hasta en un 50% después de cinco años del último refuerzo (2o año básico) y casi ausente a los 12 años (21, 22).
La eficacia de esta vacuna, para la tos convulsiva, se ha calculado entre 70-85% durante los tres primeros años después de recibir 3 dosis (21). Se ha demostrado que hay pérdida de inmunidad en los vacunados con DPT, seis a 10 años después de la última dosis, además de observar reinfecciones a pesar de haber tenido la enfermedad natural (22); sin embargo hasta ahora no hay un conocimiento exacto de cómo, tanto las vacunas tradicionales como las nuevas, protegen (16, 17).
Algo parecido ocurre en relación a la protección contra el tétanos y la difteria, inicialmente extraordinario con niveles de protección (>0,001UI/mL) en casi el 100% de los vacunados, para ambos agentes, permaneciendo niveles aceptables o mínimos entre 10 a 15 años post vacuna, por ello que se hace indispensable refuerzos cada 10 años, especialmente dirigido a mantener una excelente inmunidad frente al tétanos (20).
La coqueluche es una enfermedad que aún permanece endémica en numerosas regiones del planeta, a pesar de los programas de vacunación, como ha sido el caso del brote epidémico durante el año 2010 en California (5). La inmunidad protectora dura alrededor de 5-10 años en los pacientes con programas completos de inmunizaciones, por ello los adolescentes son un grupo susceptible de presentar una enfermedad clásica, leve e incluso asintomática y ser causa de cuadros clínicos difíciles de diagnosticar (21), por tal razón ellos pasan a se un reservorio muy significativo en el abordaje epidemiológico y clínico de esta enfermedad.
El año 2003, en Estados Unidos, el número de casos reportados de coqueluche fue superior a los de los últimos 30 años y en el 64% de ellos ocurrió en adolescentes y adultos (5). La tos convulsiva es causa importante de morbilidad respiratoria en adolescentes y adultos (6). Padres, cuidadoras, abuelos y bisabuelos han demostrado ser una fuente significativa de infección por B. pertussis, especialmente para menores de un año (6). Eliminando o disminuyendo significativamente este reservorio, se espera que disminuya significativamente las tasas de infección en estos niños, donde se concentra el mayor número de casos de morbilidad y mortalidad por este agente (5, 6).
En nuestro país, el uso de vacuna anti pertussis (DPT) ha permitido una reducción muy significativa de la incidencia de esta patología, especialmente en niños menores de cinco años, con la salvedad que esta vacuna no se puede seguir indicando más allá de los siete años, por los potenciales efectos adversos que se podrían presentar como fiebre sobre 39-40° C, acompañado de persistente calofrío, letargo importante, severo y doloroso enrojecimiento en la zona de punción, intenso malestar general, anafilaxia (2 por 100.00 dosis) y/o complicaciones neurológicas como episodios de colapso, e incluso síntomas que aparentan shock endotóxico (21); por tal razón pasa a ser indispensable contar con una vacuna para poder ser aplicada a edades mayores sin riesgo de estos potenciales efectos adversos.
Desde el año 2005 se han licenciado e incorporado a programas oficiales, en algunos países desarrollados, nuevas vacunas para este grupo poblacional Tdap (toxoide tetánico, diftérico, más algunos antígenos de B. pertussis (componentes acelulares); en dosis menores que la DPaT o vacuna acelular de la infancia).
Así el 15 de marzo de 2005 fue aprobada por la FDA de los EE.UU., ADA-CEL® como vacuna aplicable a adolescentes y adultos hasta 64 años y el 3 de mayo de 2006 aprobó BOOSTRIX® para el mismo grupo etáreo (6, 7). Repevax ® (Sanofi Pasteur) aún no aprobada por la FDA, contiene además de los componentes que tiene ADACEL, vacuna anti poliomielitis (Tdap/IPV).
En nuestro país se han licenciado y autorizado ambas vacunas Tdap: ADACEL® (Sanofi Pasteur) y BOOSTRIX® (GlaxoSmithKline).
Ambas vacunas contienen toxoide diftérico y tetánico más antígenos inmunoestimulantes y protectores para B. pertussis, como son: Pertusinógeno, hemaglutinina filamentosa y pertactina, más aglutinógenos de fimbrias, en el caso de ADACEL®; los componentes de esta vacunas están en dosis bastante más bajas que en las vacunas acelulares que se usan en niños menores de 7 años (6, 7).
Todos los estudios de reactogenicidad, inmunogenicidad y eficacia son comparables para ambas vacunas (8, 9).
Las dos vacunas están comercialmente disponibles en Chile y recomendable para usarlas, cualquiera de ellas, especialmente en adolescentes después de 10 años de haber recibido la vacuna del PNI en 2o año básico (dT) y agregar refuerzos cada 10 años, para mantener una buena inmunidad para tétanos, difteria y coqueluche.
Tener presente su utilidad en pacientes que hicieron reacciones adversas severas a vacuna pertussis a células enteras y/o que es necesario inmunizar después de los 6 años (completar PNI) o en adolescentes y adultos en probables campañas para controlar un brote epidémico.
Vacuna contra el virus del papiloma humano (VPH)Los virus del papiloma humano (VPH), o papilomavirus, son un grupo de más de 100 virus ADN relacionados. Pueden causar verrugas, papilomas benignos y lesiones cancerígenas. Sólo algunos tipos están relacionados con ciertos tipos de cáncer, por lo que son denominados VPH oncogénicos y son alrededor de 13 serotipos diferentes, que pueden causar tanto cáncer cervicouterino como anorectal. Se sabe que alrededor de 37 tipos de VPH se transmiten por contacto sexual y muchos de ellos son causa de verrugas anogenitales (10, 11).
Los VPH oncogénicos más prevalentes son el 16 y 18, causantes de más del 70% de los casos y los serotipos 31, 33, 35, 45, 52 y 58 que causa el otro 10-30%; en conjunto son causa de cerca del 100% de los casos, especialmente en infecciones persistentes. Algunos serotipos, como el 16 pueden causar, además, cáncer laríngeo.
En Chile el cáncer cérvico-uterino (CCU) ocupa el cuarto lugar entre las neoplasias malignas, con una tasa de mortalidad de 8,7 por 100.000 mujeres mayores de 15 años (18).
Tanto en estudios nacionales como internacionales los genotipos predominantes son el VPH 16 y 18. En diferentes estudios chilenos, el VPH 16 ocupa el 81% de los adeno carcinomas cervicales y el VPH 18, un 13% (19).
Los virus VPH son altamente transmisibles y son la causa más frecuente de infección del tracto genital en todos los países del mundo. Son transmitidos a través de contacto sexual, penetrante o no, y generalmente adquiridos en los primeros años de inicio de la actividad sexual, por ello la mayor incidencia ocurre entre los 16 y 20 años. Tanto la incidencia como la prevalencia están directamente relacionadas con el aumento de la actividad sexual (11).
Los factores de riesgo más relevantes son el número de parejas sexuales, la falta de uso de condón, uso prolongado de anticonceptivos orales, estado inmunitario (Ej. infección por VIH), multiparidad, tabaquismo, drogadicción y coinfección con otras infecciones de transmisión sexual, como el virus de la inmunodeficiencia humana (VIH).
Los VPH son virus que afectas sólo los epitelios de las mucosas sin fase hematógena, alrededor de la mitad de las mujeres infectadas desarrollan anticuerpos séricos, los cuales no son protectores para infecciones por otros serotipos. La mayoría de las infecciones son asintomáticas e indetectables, incluso por métodos moleculares, hasta más allá de 2 años de adquiridos. Sólo una pequeña proporción de mujeres infectadas hace una infección persistente y si corresponden a serotipos oncogénicos, pueden desarrollar cáncer. El tiempo entre la adquisición del agente y el desarrollo de neoplasia puede ser de varias décadas.
Desde el punto de vista epidemiológico se presentan más de 500.000 casos nuevos anualmente en el mundo y cerca del 80% de las muertes por este diagnóstico ocurren en mujeres de países en vías de desarrollo.
En Chile se presentan alrededor de 1.200 casos nuevos, anualmente de CCU, con una tasa de 28,8 por 100.000 mujeres mayores de 15 años. El año 2004 ocurrieron 676 muertes por esta causa, constituyendo la quinta causa de muerte por cáncer en mujeres chilenas (20).
No se dispone de datos epidemiológicos, chilenos, de la frecuencia de infecciones por VPH 6 y 11. En centros centinelas de enfermedades de transmisión sexual (ETS) se notificaron 427 casos de condilomas acuminados el año 1999 (19,7% del total de las ETS notificadas ese año) y 2309 casos durante los años 1999-2003 (21,9% del total de la ETS) (20).
En encuestas realizadas en nuestro país, los años 2003 y 2004 muestra que un tercio de los jóvenes inician actividad sexual antes de los 15 años y que entre un 7 a 12% de los varones y 1 a 3% de las mujeres inician actividad sexual antes de los 13 años (20).
El desarrollo de vacunas ha llevado a contar con dos vacunas anti VPH, efectivas para la prevención de la infección y no para el tratamiento de la infección crónica. Ambas vacunas son el producto de tecnología recombinante, por lo tanto no están constituidas con partículas infectantes, ni material genético, son partículas proteicas formadoras del virus (VLPs) muy antigénicas, pero no infectantes (12, 13).
Cervarix® vacuna bivalente producida por los laboratorios GlaxoShmithKline contiene antígenos VLP de los serotipos 16 y 18 con un coadyuvante ASO4 que incluye un lípido A monofosforilado. Está indicada en tres dosis intramusculares, 0, 1 y 6 meses.
Gardasil® vacuna cuadrivalente manufacturada por laboratorio Merck contiene antígenos VLP de los serotipos 6, 11, 16 y 18 con un adyuvante hidrofosfato de aluminio. Está indicada en tres dosis 0, 1 y 6 meses.
Numerosos estudios comparativos de seguridad, inmunogenicidad y eficacia en diferentes países y continentes señalan que ambas vacunas muestran resultados comparables en relación a la prevención de infección por VPH 16 y 18, y por ende CCU.
En mujeres, antes de tener contacto con virus silvestre, ambas vacunas demuestran una efectividad de más del 90% para neoplasia intracervical (CIN 2/3) o adenocarcinoma in situ (AIS). Ambas vacunas producen protección parcial para serotipos oncogénicos diferentes al 16 y 18.
Ambas vacunas inducen altos niveles de anticuerpos relacionados a los serotipos, anticuerpos IgG neutralizantes que trasudan el epitelio y neutralizan al virus.
Para ambas vacunas el seguimiento de los niveles de protección ha demostrado efectividad por más de 16 años y se pueden administrar concomitantemente con otras vacunas como Tdap, hepatitis A y/o B, varicela, etc. La estrategia de vacunación anti VPH en adolescentes está dirigida especialmente a la prevención del cáncer cervicouterino y en menor importancia a verrugas genitales, por eso están indicadas en mujeres de 9 a 12 años o inicio tardío entre 13 a 26 años. Otra posible indicación es la disminución de cáncer de pene, recto, orofaringeo y laríngeo asociado especialmente al serotipo 16.
En esta dirección el 16 de octubre de 2009 la FDA autorizó el uso de vacuna cuadrivalente en varones de 9 a 26 años (13).
En Chile existen ambas vacunas en forma comercial, no han sido incorporadas, por ahora, a ningún programa de salud pública. Se recomienda su uso en niñas entre 9 a 13 años, idealmente antes del inicio de la actividad sexual, a pesar de que se pueden colocar e indicar a cualquier edad, incluso después de iniciada la actividad sexual, sin embargo su efectividad puede verse disminuida si la paciente se ha infectado con un serotipo vaccinal (11, 12).
Vacuna cuadrivalente antimeningocócica (MCV4)La enfermedad meningocócica es una patología endémica grave, con brotes epidémicos periódicos a lo largo del tiempo que ocurren en todos los países del mundo. La población más susceptible y el principal reservorio se ubican en la población adolescente, especialmente en lugares cerrados, frecuentados por ellos, como son las universidades, internados, regimientos, etc.
El año 2009 se notificaron en Chile 93 casos de enfermedad meningocócica, cifra inferior al año anterior (103 casos). La incidencia ha tendido a estabilizarse permaneciendo como una enfermedad de baja endemia. El 57% corresponde a pacientes mayores de 5 años con una mortalidad de 9%. El 59% de los casos se confirmó por el ISP; 64% corresponden al serogrupo B, 25% corresponden al C, 4% al Y y 2% al W135 (14).
Entre las numerosas vacunas antimeningocócicas comerciales que existen, están la antiserotipo(s) A; C;Ay C; W135; Y; yA, C, Y, W135 no conjugada (MPSV4). Recientemente aparece la cuadrivalente conjugada A, C, Y W135 (MCV4), delineada inicialmente para adolescentes, actualmente aprobada también para niños desde los dos años (15).
MCV4 fue certificada en Estados Unidos en enero del año 2005, contiene antígenos purificados capsulares de cuatro serotipos de N. meningitidis y conjugados con una proteína no tóxica del toxoíde diftérico. Estos antígenos al ser conjugados son más antigénicos, T dependientes, e inducen por ello una mucho mejor respuesta inmune de memoria.
Esta vacuna MCV4 (Menactra® de Sanofi Pasteur) aprobada y recomendada por el FDA y el Comité Asesor de Inmunizaciones de Estados Unidos en junio del 2009 para uso en adolescentes, está indicada en una dosis en pacientes entre 11 y 16 años, y en las poblaciones de riesgo hasta los 55 años. Si la persona sigue siendo de riesgo debe ser revacunada cada cinco años. A partir del año 2007 esta vacuna fue autorizada para su uso en niños de 2-10 años, con riesgo de enfermedad meningocócica (15).
La única contraindicación relativa de esta vacuna es en pacientes que tienen historia de Guillan-Barré, por el mayor riesgo de reactivación (18).
En Chile aún no ha sido certificada ni aprobada por el Instituto de Salud Pública, sin embargo dada nuestra vigilancia para enfermedad meningocócica, actualmente no parece una vacuna indispensable en las presentes condiciones epidemiológicas; si en un futuro se demostraran brotes en centros cerrados u otros graves problemas con esta bacteria, que potencialmente podrían afectar, en especial a esta población adolescente, la indicación podría cambiar y ser necesario e imperioso su uso.
ConclusiónComo se aprecia, existen en varios países Programas de Inmunización dirigidos a los adolescentes, con miras a mejorar la salud de esta población tanto en lo particular como en lo general.
Como medida de Salud Pública nacional y dada la experiencia internacional, son indispensables y hacen que miremos al futuro inmediato para incorporarlas a programas estructurados en nuestro país. Por ahora y dado nuestros recursos, son de uso privado, en la mayoría de los casos y recomendables según lo expuesto.
Una propuesta de calendario optativo de inmunizaciones para adolescentes en Chile que podría ser una alternativa a considerar en un futuro próximo (Cuadro 2).
| Vacunas | Edad | Dosis | Protección | Ocasión |
|---|---|---|---|---|
| Tpad | 11-21 años | 1 | Difteria-Tétanos-Pertussis | Rutina |
| Anti-VPH | 9-18 años (niñas) | 3 | Virus papiloma humano | Rutina |
| Influenza | 9-21 años | anual | Influenza | Casos especiales o campaña |
| Antineumocócica (23v) | 9-21 años | 1 | Neumococos | Casos especiales |
| Hepatitia A y/o B | 9-21 años | 2 | Hepatitis A o B | No vacunados o casos especiales |
| Tresvirica | 9-21 años | 1 | Parotiditis- Rubéola-Sarampión | No vacunados o casos especiales |
| Anti Varicela | 9-21 años | 1 | Varicela | No vacunados o Refuerzo |
El autor declara no tener conflictos de interés, en relación a este artículo.