La enfermedad tiroidea subclínica (ETS) es una condición asintomática de alta prevalencia que incluye el hipertiroidismo subclínico (HiperSC) y el hipotiroidismo subclínico (HipoSC). Ambas formas no tienen síntomas ni signos específicos y solamente pueden ser detectados mediante exámenes hormonales. Las causas más frecuentes de HiperSC son la enfermedad de Graves y el bocio multinodular. De HipoSC la causa más frecuente es la tiroiditis crónica autoinmune (enfermedad de Hashimoto). El criterio diagnóstico para HiperSC es TSH sérica de ≤0.4mU/L y valores normales deT4 total o libre. El criterio diagnóstico para HipoSC es TSH sérica de 4.5-10mU/L junto con valores normales de T4 total o libre. Ambas se consideran más severas cuando los valores de TSH se alejan del valor normal: <0.1mU/L HiperSC y >10mU/L en HipoSC. En la ETS las alteraciones cardiovasculares son frecuentes, pero de distinta índole, así en el HiperSC hay mayor riesgo de arritmias supraventriculares mientras en el HipoSC hay un riesgo aumentado de dislipidemia y ateroesclerosis. En este artículo se analizan los aspectos diagnósticos de la ETS, sus complicaciones y se propone un plan de manejo desde una perspectiva clínica.
Subclinical thyroid disease is a highly prevalent asymptomatic entity that includes subclinical hyperthyroidism and subclinical hypothyroidism. Both forms lack of specific signs and symptoms and only can be detected by hormonal tests. The most frequent etiologies for subclinical hyperthyroidism are Graves’ disease and multinodular goiter, and for subclinical hypothyroidism is Chronic autoimmune thyroiditis. Accepted diagnostic criteria for subclinical hyper and hypothyroidism are a TSH ≤ 0.4mU/L with normal T3, T4 or FT4 and a TSH ≥ 4.5mU/L with a normal T4 or FT4 respectively. Both conditions have frequent cardiovascular and metabolic complications such as supraventricular arrhythmia (subclinical hyperthyroidism) and hyperlipidemia with atherogenesis (subclinical hypothyroidism). Diagnostic criteria and abnormalities associated with this conditions are reviewed. In addition, a clinical treatment approach is proposed.
La ETS es un trastorno funcional de la glándula tiroidea de alta prevalencia, asintomática y solo detectable mediante exámenes hormonales de laboratorio. Puede corresponder a una enfermedad tiroidea en su etapa inicial, manifestándose por concentraciones levemente alteradas de TSH y normales de T3 y T4 o T4 libre.
El rango normal de TSH está situado entre 0.5-4.5mU/L. Estos valores corresponden a los encontrados en el 95% de la población general, sin que ello signifique que el 5% restante tenga un trastorno o anormalidad tiroidea.
Aún hay muchas controversias en el diagnóstico y manejo de estas condiciones. Sin embargo, se han planteado algunas recomendaciones diagnósticas y terapéuticas válidas para ciertos grupos poblacionales. Los pacientes con hipertiroidismo subclínico (HiperSC) tienen niveles de TSH menores de 0.5mU/L. En el hipotiroidismo subclínico (HipoSC) los niveles de TSH están entre 4.5-10mU/L. A diferencia de las enfermedades clínicas o definitivas, en la ETS los niveles de hormonas tiroideas (T3, T4, T4 libre) son normales (1).
Lo anterior surge del hecho que los niveles séricos de TSH son más sensibles que los niveles de hormonas tiroideas para evaluar el grado de función de la glándula tiroidea.
Ambas formas subclínicas pueden acompañarse de diversas complicaciones cardiovasculares, esqueléticas y cognitivas, y/o pueden evolucionar en un período variable (meses o años) y llegar a constituirse en una enfermedad tiroidea definitiva.
PrevalenciaLa prevalencia de la enfermedad tiroidea subclínica en nuestro país no ha sido estudiada.
En el laboratorio del Hospital Clínico de la Universidad se analizaron 7.627 muestras de exámenes de personas sin antecedentes previos de enfermedad tiroidea, encontrándose 1.6% de TSH ≤0.5mU/L y 3.4% entre 5-10mU/L. Estas cifras son comparables a las reportadas en estudios internacionales. En el Estudio de Salud Nacional y Encuesta de Salud Nutricional de Estados Unidos (NHANES III) (2) se reportó una TSH <0.4mU/L en el 1.8 % de los casos. De este grupo solo el 0.7% presentaba niveles <0.1mU/L (TSH suprimida); esto permite concluir que aproximadamente el 75% de los HiperSC tienen niveles de TSH entre 0.1-0.4mU/L (2, 3).
El HipoSC tiene mayor prevalencia en países con ingesta elevada de yodo alcanzando a afectar al 4-9.5% de la población adulta (4). Esta cifra aumenta en la población de adultos mayores (>65 años) reportándose cifras de 8.2% en hombres y 16.9% en mujeres (5).
Hipertiroidismo subclinico (hipersc)Habitualmente estos pacientes no presentan síntomas ni signos de hipertiroidismo, aunque en algunos pueden detectarse aumentos de frecuencia cardíaca promedio en mediciones de 24 horas.
Según la causa se distinguen dos tipos:
- •
Exógeno: causado por administración excesiva de levotiroxina sódica (L-T4) en casos de tratamiento para bocio, supresión de TSH en el post operado de cáncer tiroideo o dosis de sustitución mayores a las requeridas en casos de hipotiroidismo.
- •
Endógeno: causado por las mismas condiciones que originan el hipertiroidismo clínico, es decir: la enfermedad de Graves y el bocio multinodular tóxico.
El HiperSC puede causar arritmias y/o insuficiencia cardíaca. En mayores de 60 años con TSH <0.1mU/L (suprimida) se reporta 28% de incidencia de fibrilación auricular en comparación con 11% en pacientes con TSH entre 0.1-0.4mU/L. Estos resultados demuestran que a menores concentraciones TSH mayores son los riesgos de arritmia (5).
DiagnósticoEl HiperSC debe sospecharse cuando TSH está bajo el rango inferior de normalidad (<0.4mU/L) junto con niveles normales de hormonas tiroideas. Cuando los niveles de TSH están entre 0.1-0.4mU/L se considera leve, si está bajo 0.1mU/L se considera severo.
Sin embargo, no todos los casos de TSH bajo el límite normal corresponden a HiperSC. Existen otras condiciones (no tiroideas) que pueden causar disminución de los niveles de TSH. En Tabla 1 se muestran algunas de estas condiciones. Entre ellas, la enfermedad no tiroidea del paciente enfermo en que ocurre una disminución en el estímulo de TRH hipotalámico destinado a reducir los niveles de hormona tiroidea, y por ende del gasto energético, como forma de respuesta metabólica a la enfermedad grave sistémica. Una vez que el paciente supera la condición de gravedad, la TSH se normaliza e incluso puede sobrepasar el rango de normalidad dentro de las 2-4 semanas posteriores a la recuperación. Algunos fármacos como los corticoides y la dopamina pueden bajar los niveles de TSH y hacer sospechar erróneamente un hipertiroidismo.
Diagnóstico diferencial de la enfermedad tiroidea subclinica
| TSH ELEVADO |
| • Fase posterior a enfermedad no - tiroidea severa |
| • Elevación nocturna de TSH |
| • Error de laboratorio |
| • Anticuerpos heterófilos |
| • Fármacos (metoclopropamida, domperidona) |
| • Resistencia a las hormonas tiroideas |
| • Obesidad severa |
| TSH SUBNORMAL |
| • Enfermedad no-tiroidea severa |
| • Hipotiroidismo central |
| • Fármacos (glucorticoides, dopamina) |
| • Supresión post tratamiento de hipertiroidismo |
| • Interferencia de HCG en altas concentraciones |
| • Error de laboratorio |
| • Tratamiento con dosis altas de glucocorticoides o dopamina |
Como se ha mencionado, las causas de HiperSC son las mismas del hipertiroidismo clínico o definitivo. En jóvenes la etiología más frecuente es la enfermedad de Graves. En pacientes mayores de 65 años predomina como etiología el bocio multinodular. El HiperSC también puede ser inducido por fármacos. Entre estos, la amiodarona, fármaco muy usado en el tratamiento de arritmias supraventriculares que tiene un alto contenido de yodo (6mg de yodo por comprimido de 200mg). Considerando que la recomendación de ingesta diaria de yodo en el adulto normal es aproximadamente 150-300 ug/día, cada comprimido de amiodarona aporta unas 20-40 veces la dosis diaria total de yodo. La tirotoxicosis secundaria a este fármaco ocurre en 1-23% de los pacientes que la utilizan, siendo muy frecuente el HiperSC (6). En algunos casos se debe a mayor secreción de hormona tiroidea en áreas autónomas de la glándula que son gatilladas por el aporte de yodo. En otros casos el fármaco induce una tiroiditis destructiva en pacientes sin patología tiroidea previa (7).
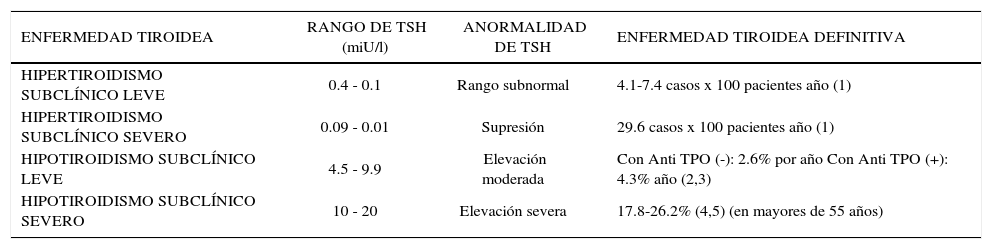
Efectos sistemicosEs importante considerar que tanto el HiperSC exógeno como endógeno, pueden provocar efectos cardiovasculares (8). Por otra parte, el riesgo de conversión a hipertiroidismo definitivo, aumenta significativamente cuando la TSH está suprimida (<0.1mU/L). En la Tabla 2 se muestran los riesgos de estas complicaciones de acuerdo a la edad del paciente y el nivel de TSH basal.
Enfermedad tiroidea subclinica: evolución a enfermedad definitiva
| ENFERMEDAD TIROIDEA | RANGO DE TSH (miU/l) | ANORMALIDAD DE TSH | ENFERMEDAD TIROIDEA DEFINITIVA |
|---|---|---|---|
| HIPERTIROIDISMO SUBCLÍNICO LEVE | 0.4 - 0.1 | Rango subnormal | 4.1-7.4 casos x 100 pacientes año (1) |
| HIPERTIROIDISMO SUBCLÍNICO SEVERO | 0.09 - 0.01 | Supresión | 29.6 casos x 100 pacientes año (1) |
| HIPOTIROIDISMO SUBCLÍNICO LEVE | 4.5 - 9.9 | Elevación moderada | Con Anti TPO (-): 2.6% por año Con Anti TPO (+): 4.3% año (2,3) |
| HIPOTIROIDISMO SUBCLÍNICO SEVERO | 10 - 20 | Elevación severa | 17.8-26.2% (4,5) (en mayores de 55 años) |
Se sabe que las hormonas tiroideas aumentan la frecuencia cardíaca, la fuerza de eyección y la relajación ventricular diastólica. Estos efectos suelen estar presentes en el HiperSC, aunque en menor grado que en el hipertiroidismo definitivo. También se ha reportado aumento de la morbilidad y mortalidad por enfermedad cardiovascular (9). Los estudios demuestran mayor frecuencia de taquicardia, extrasístoles auriculares y ventriculares. En general las arritmias tienden a controlarse cuando se logra llevar al paciente al eutiroidismo (9).
En general los cambios observados son similares al hipertiroidismo definitivo, pero son más frecuentes en adultos mayores. Algunos trabajos han mostrado algunas alteraciones eco-cardiográficas en pacientes jóvenes con HiperSC que tienden a ser más frecuentes en enfermedades de Graves de larga duración y con alto grado de supresión de TSH (10).
Tanto en el hipertiroidismo clínico como subclínico tienen mayor frecuencia de enfermedad ateroesclerótica. En ambos se ha reportado hipercoagulabilidad, mayor tendencia a la trombosis y aumento del grosor de la capa íntima-media de la carótida (11, 12).
Un estudio reciente reportó aumento de la mortalidad en pacientes con HiperSC reportándose mayor riesgo relativo de mortalidad por cualquier causa o por enfermedad cardiovascular en 1.3 (95% IC; 1.02-1.66) y 1.68 (1.02-2.76) respectivamente (13).
Los adultos mayores (>65 años) además de mayor arritmia tienen mayor riesgo de sufrir un evento cardiovascular o de morir por esta causa. Es probable que la presencia de una cardiopatía asociada, aumente aún más el riesgo de morbilidad y mortalidad en esta población. Por tal motivo se recomienda en este grupo un tratamiento precoz y efectivo del HiperSC.
Hueso y esqueletoLas hormonas tiroideas aumentan la acción resortiva del osteoclasto. En el hipertiroidismo definitivo el riesgo de osteoporosis y de fractura está aumentado. En mujeres postmenopáusicas con HiperSC endógeno se ha reportado una disminución de la densidad mineral ósea, especialmente a nivel del hueso cortical (región distal del radio). Sin embargo, esto no se ha objetivado en el hombre ni en mujeres premenopáusicas. Al parecer, el efecto resortivo de las hormonas tiroideas se hace más evidente después de los 65 años. En una cohorte seguida por cuatro años, se observó un riesgo de fractura de cadera tres veces mayor y de fractura vertebral cuatro veces mayor cuando TSH estaba en rango <0.1mU/L(14).
TratamientoEl manejo del HiperSC debe ser indicado por un equipo multidisciplinario. Este debe incluir un endocrinólogo, un médico de medicina nuclear (si se va a usar yodo 131) y otros especialistas que correspondan a las complicaciones del paciente. En general se usa el yodo 131 para producir una ablación radioactiva de la glándula tiroidea. Los pacientes que tienen un bocio de gran tamaño (>50 gr) o sospecha de neoplasia tiroidea deben ser tratados con cirugía. Las drogas antitiroideas pueden ser usadas, pero habitualmente sus efectos solo duran mientras se les utilice. Estas opciones deben ser evaluadas cuidadosamente de acuerdo a los riesgos y beneficios involucrados en cada caso.
Hipotiroidismo subclinico (hiposc)Esta condición es considerada asintomática por la mayor parte de los autores, algunos estudios le han atribuido alteraciones clínicas como astenia, hipoacusia, dislipidemia y/o depresión. Sin embargo, no hay certeza de que estas asociaciones sean reales.
La historia natural del HipoSC en el adulto mayor ha sido recientemente analizada en el Estudio de Salud Cardiovascular de Estados Unidos (15). Los autores evaluaron 459 adultos mayores de 65 años con HipoSC, y los siguieron durante cuatro años (15). La función tiroidea fue evaluada a los 2 y 4 años, observándose que solo un 56% de los pacientes seguían con valores altos de TSH después de cuatro años de seguimiento. La normalización del examen ocurrió en el 46% de los pacientes con TSH basal entre 4.5 y 6.9mU/L, en el 10% con valores entre 7 y 9.9mU/L y 7% cuando éstos eran >10mU/L (15).
Efectos cardiovascularesEl hipotiroidismo definitivo afecta la función y el metabolismo cardiovascular. En la actualidad se considera que estos efectos son producidos por la falta de hormona tiroidea a nivel de la célula miocárdica y pared vascular. Sin embargo, todavía hay controversias respecto a los efectos cardiovasculares del HipoSC. En cuanto a los lípidos, se han reportado cambios en los niveles de LDL, los que tienden a ser mayores que en sujetos eutiroideos (16). Por otra parte, se ha destacado el rol de las hormonas tiroideas en la fase diastólica de la contracción miocárdica, es decir aquella relacionada con la activación de la ATPasa dependiente de calcio (17). Las hormonas tiroideas activan sitios específicos del DNA nuclear estimulando la síntesis de RNA particular y de proteínas específicas del músculo cardíaco. La disminución de las concentraciones de hormonas tiroideas puede alterar la función cardíaca normal (18). Las hormonas tiroideas también estimulan el sistema adrenérgico vascular a través de vías alternativas a las génicas (19, 20). Junto con lo anterior se han reportado efectos de estas hormonas en la adaptación a la isquemia cardíaca y en el proceso de remodelación post infarto. Esto puede explicar la mayor mortalidad que presentan los pacientes infartados cuando tienen niveles bajos de T3 (21).
El hipotiroidismo subclínico se asocia a trastornos cardíacos e incremento de la ateroesclerosis. Una gran cantidad de estudios epidemiológicos muestran mayor riesgo de mortalidad cardiovascular tanto en hipotiroidismo clínico como subclínico (22, 23), pero no todos los estudios lo demuestran (25, 26).
Efectos en los lípidosVarios trabajos han reportado niveles consistentemente elevados de colesterol total, LDL-C, apolipoproteína B, lipoproteína (a) y triglicéridos en pacientes con hipotiroidismo definitivo (27). En general estos cambios tienden a revertirse con la corrección del hipotiroidismo. Algunos pacientes siguen teniendo valores alterados y en ellos se debe sospechar una dislipidemia primaria concomitante. Por otra parte, la influencia del HipoSC en los niveles séricos de lípidos es menos evidente, pero los niveles de apoliproteína B suelen estar aumentados (27) y algunos estudios también han demostrado elevación de los niveles de LDL-C (28). En la actualidad se acepta que el evento determinante en la elevación de LDL es una disminución de la síntesis proteica intracelular lo que lleva a una menor expresión del receptor de LDL (29). Con el tratamiento del HipoSC (L-T4) se revierte este proceso y bajan los niveles del LDL sérico.
En estudios experimentales se ha demostrado que la administración de T3 aumenta la expresión de genes relacionados con los canales de calcio, eleva la captación de O2 y disminuye la resistencia vascular (30).
Una revisión actualizada concluye que no hay suficientes evidencias para apoyar o negar el rol patogénico del HipoSC en la dislipidemia asociada a esta condición (16).
Manejo del HipoSCLa decisión de indicar un tratamiento con L-T4 es difícil y se recomienda que sea efectuada por un endocrinólogo. Estudios recientes han demostrado normalización espontánea de la TSH a los 2 a 4 años de observación en aproximadamente un tercio de los casos de TSH elevada. Cuando los valores iniciales de TSH son >6.9mU/L, la probabilidad de normalización baja del 32% al 10%; si el paciente tiene anticuerpos anti TPO(+) la normalización de TSH es mucho menos frecuente (15).
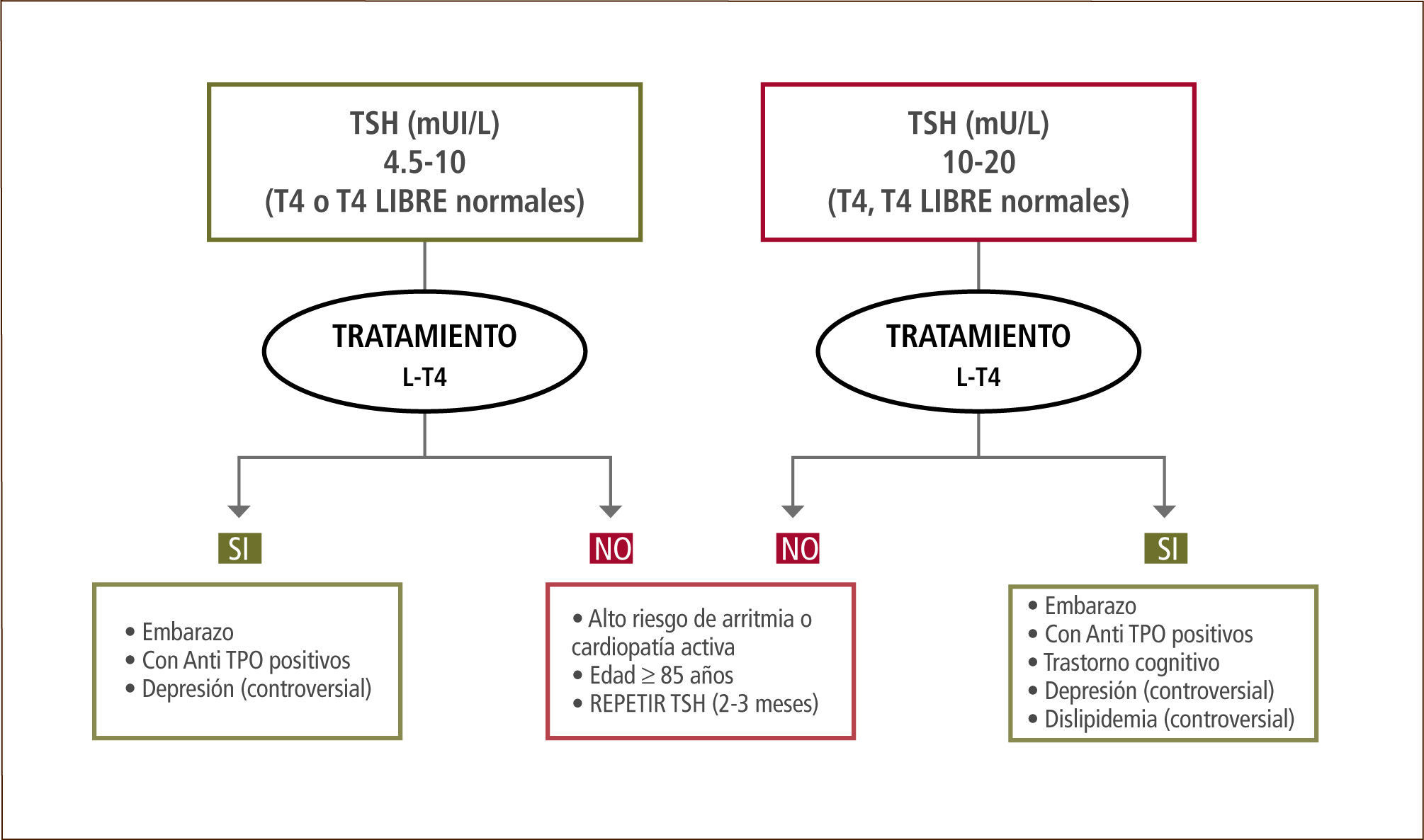
Aún no hay consenso respecto a la conducta terapéutica en pacientes con HipoSC. Considerando las últimas publicaciones se propone un esquema de manejo que considera el valor inicial de TSH (Figura 2). Si este valor está entre 4.5 y 10mU/L se considera que el HipoSC es leve y más frecuentemente transitorio; si está entre 10 y 20 se considera más severo y debe ser corregido con mayor frecuencia. De acuerdo a las últimas evidencias se recomienda iniciar L-T4 en pacientes embarazadas (primer trimestre) y en pacientes con anticuerpos anti TPO positivos. Hay controversia respecto a indicar esta terapia en pacientes con depresión: Al respecto hay una extensa literatura que apoya el uso de hormonas tiroideas para potenciar o acelerar el efecto de los fármacos antidepresivos. En cuanto a síntomas neuropsicológicos inespecíficos que han sido asociados al HipoSC (Ej. alteraciones de memoria, concentración, ánimo) el tratamiento con levotiroxina no ha demostrado ser superior al placebo.
Se sugiere iniciar terapia con levotiroxina en dosis bajas (12.5-25 ug/día) para luego ajustarla.
ScreeningLas recomendaciones actuales en general son contrarias al screening universal para HipoSC (31). Sin embargo, se recomienda un screening selectivo para ciertos grupos específicos como por ejemplo mujeres en edad reproductiva, sujetos con antecedentes familiares de hipotiroidismo, portadores de enfermedades autoinmunes (DM tipo 1, vitiligo, enfermedad celíaca), pacientes con depresión y adultos mayores (32, 33). Recientemente se publicó un estudio de screening en población adulta normal demostrándose que el 95% de las personas tenían valores normales de TSH (0.35-5.5mU/L). El 3.0% tenía valores levemente elevados (5.5-10mU/L), el 0.7% valores >10mU/L y el 1.2% tenía valores <0.35mU/L). Posteriormente se hizo un segundo examen de TSH a los cinco años observándose que el 62% de los pacientes con TSH inicial elevada se normalizaban y el 2.9% mantenía los niveles elevados o la elevaban aún más. Por otra parte el 50% de las TSH disminuidas (<0.35mU/L) también normalizaban los niveles (34).
El autor declara no tener conflictos de interés, relacionados a este artículo.