La distrofia fascioescapulohumeral (DFEH) es una de las formas más comunes de distrofia muscular. Afecta principalmente los músculos de la cara, el hombro y de la parte superior del brazo. Los síntomas suelen aparecer mayoritariamente entre los 10 y 26 años. A menudo son leves y empeoran muy lentamente.
El presente artículo describe las características morfológicas y funcionales, evaluaciones e intervenciones realizadas a una persona mayor octogenaria con DFEH.
Se realizaron evaluaciones en los sistemas musculoesquelético, respiratorio y neurológico, además de análisis de sangre, espirometría, fuerza de agarre palmar y bioimpedancia. Las intervenciones incluyeron sesiones de kinesioterapia, dos o tres veces por semana, durante siete años, centradas en mantener la fuerza muscular, la flexibilidad y la capacidad aeróbica.
La evaluación inicial y la reevaluación mostraron una disminución progresiva de la fuerza muscular y movilidad articular, atrofia muscular y complicaciones respiratorias.
La kinesioterapia sistemática permitió mantener niveles de actividad muscular, prevenir rigidez articular y mejorar la funcionalidad general del paciente. Los resultados indicaron una mantención de la funcionalidad y calidad de vida, aunque limitado por la naturaleza progresiva de la DFEH.
Fascioscapulohumeral dystrophy (FSHD) is one of the most common forms of muscular dystrophy. It mainly affects the muscles of the face, shoulder and upper arm. Symptoms usually appear between the ages of 10 and 26. They are often mild and worsen very slowly.
This article describes the morphologic and functional characteristics, evaluations, and interventions performed on an octogenarian older adult with DFEH.
Assessments were performed on the musculoskeletal, respiratory, and neurological systems, in addition to blood work, spirometry, palmar grip strength, and bioimpedance. Interventions included kinesiotherapy sessions two to three times per week for seven years, focusing on maintaining muscle strength, flexibility and aerobic capacity.
Initial assessment and reassessment showed a progressive decrease in muscle strength and joint mobility, muscle atrophy, as well as respiratory complications.
Systematic kinesiotherapy allowed maintaining muscle activity levels, preventing joint stiffness, and improving the patient's overall functionality. The results indicated a maintenance of functionality and quality of life, although limited by the progressive nature of FSHD.
La distrofia muscular (DM) es un grupo heterogéneo de patologías del músculo, causado por una mutación genética hereditaria o de novo, que determina la ausencia, destrucción o disfunción de proteínas esenciales para la estructura y funcionalidad de las fibras musculares estriadas. Clínicamente, las distrofias musculares se caracterizan por una debilidad muscular progresiva de los miembros, el tronco y la cara, en proporciones y grados variables1,2. A nivel histopatológico, la DM se define por una combinación de necrosis y regeneración con un aumento del tejido conectivo intersticial en el músculo esquelético. Estas características permiten diferenciar a las DM de otras miopatías no distróficas, como las miopatías congénitas, metabólicas o inflamatorias. Este fenómeno de destrucción muscular lleva, con el tiempo, a un reemplazo del músculo por tejido fibroadiposo2,3.
A nivel mundial se estima que entre el 19,8-25,1/100 000 habitantes, de todas las edades, presentan algún tipo de DM confirmada por biopsia muscular3,4. Encontrar estudios epidemiológicos sobre la DM se dificulta debido a la superposición de la semiología con otros tipos de miopatías. En la mayoría de los estudios, la prevalencia lleva a desórdenes en el cromosoma X, siendo la población masculina la más afectada4. A la fecha, no existe un estudio que haya explorado la prevalencia de esta enfermedad en Sudamérica4,5. En Chile las estadísticas no son precisas, las cifras de prevalencia hablan de 3,5 pacientes por cada 100 000 varones sólo para la DM de Duchenne6,7 y se estima, que existan alrededor de 5 000 pacientes afectados3, quedando alrededor de un 15% de los casos fuera de la estadística6,7.
En la clínica, como característica común de las DM se observa la pérdida progresiva del músculo estriado, que puede ser de los miembros, tronco y cara, de severidades variables, llegando a involucrar la musculatura respiratoria estriada, la musculatura cardíaca, los pares craneales (V,VII) y otros órganos. Las manifestaciones clínicas dependen de la mutación genética que presente el paciente3. La disfunción del músculo estriado es progresiva e indolora, y afecta a los grupos musculares de forma no uniforme. Esta disfunción genera compensaciones para realizar los diferentes tipos de movimiento1–3. Se puede observar intolerancia al ejercicio, trastornos musculares, rigidez articular, disminución en los rangos de movimiento, malformaciones esqueléticas, infecciones respiratorias recurrentes, disfagia, somnolencia diurna, problemas cardíacos, alteraciones de la marcha y síndrome de la cabeza caída (dropped head)1,3. En algunos pacientes también existen alteraciones de la musculatura lisa, lo que genera hipertensión, diabetes, endocrinopatías, alteraciones cutáneas y del colágeno tipo VI, entre otras patologías1,3,6,8.
En los últimos años se han descubierto distintos tipos de DM que se pueden manifestar en la niñez o en etapas adultas. Entre ellos se encuentra la distrofia facioescapulohumeral (DFEH). La DFEH presenta una prevalencia estimada de 3,95 casos por cada 100 000 personas2,9,10. La expresión clínica es altamente variable, el 70% de las personas se diagnostica antes de los 15 años y el 95% a los 20 años2,9,10.
Desde el punto de vista clínico, los síntomas más frecuentes incluyen debilidad progresiva de la musculatura facial y del cíngulo escapular, siendo el síntoma inicial la dificultad para realizar una abducción de hombro y flexión de hombro sobre los 90 grados2,9–11.
No obstante, la manifestación de síntomas entre las personas afectadas por distrofia facioescapulohumeral varía entre un 10% y un 30% de los portadores2,10. Es por esto, que podemos ver comprometidos grupos musculares como los abdominales, extensores de los dedos del pie y tibial anterior provocando la caída del pie (dropped foot) y alteraciones de la marcha. Por último, podemos encontrar debilidad de los músculos del cíngulo pélvico2,10–12.
En cuanto a la musculatura facial, es frecuente que los músculos orbiculares de la boca y de los ojos se vean afectados, lo que conlleva dificultad para realizar expresiones faciales, tales como el soplar o el cierre completo de los párpados2,10–12.
Otros síntomas secundarios asociados a la FSDH incluyen la pérdida de la audición y alteraciones vasculares de la retina, las que pueden presentarse de forma bilateral y progresiva. En casos menos frecuentes, se puede encontrar ptosis palpebral, dropped head, contracturas musculares, cardiomiopatías e incluso insuficiencia respiratoria2,10–12.
Si bien la tecnología ha permitido avanzar en el diagnóstico y tratamiento de esta enfermedad, el pronóstico para estos pacientes aún es reservado3. En este contexto, la kinesioterapia y el trabajo multidisciplinario de distintos profesionales de la salud permite controlar los síntomas y contribuir a una mejor calidad de vida del paciente y su familia. El objetivo de este reporte de caso fue describir las características morfológicas, las evaluaciones e intervenciones realizadas a una persona mayor octogenaria diagnosticada con DM.
Presentación del casoAntecedentes generalesPaciente de género masculino, de 82 años, con antecedentes mórbidos de hipertensión arterial, cardiomegalia, hernias inguinales/abdominales y fractura de patela resuelta con osteosíntesis. El paciente realiza seguimiento de su DM a través de análisis de laboratorio una vez al año. Su tratamiento farmacológico es el siguiente: prednisona 5g/día, probióticos (1 cápsula diaria), ezetrol 10mg (tres veces a la semana), losartán 50mg (medio comprimido diario), melatonina 3mg/día y bromuro de ipratropio dos puffs cada 12h todos los días.
Anamnesis remotaA la edad de 29 años, el paciente sufre un accidente de tránsito de trayecto a su trabajo. Por protocolo fue enviado al hospital para un chequeo de rutina. Al ser evaluado, se detectó una disminución del rango articular de movimiento activo y de fuerza en ambos miembros superiores. Sumado a esto, presentaba ptosis palpebral bilateral. Se realizaron exámenes de laboratorio y radiografías con resultados normales. Como estudio complementario se realizó una biopsia del músculo deltoides derecho. El resultado de este examen fue compatible con el diagnóstico de DM. A los 39 años se le diagnosticó glaucoma bilateral, con avance progresivo, presentando desde hace dos años un 30% de visión tubular, pérdida de la vista periférica y de profundidad. El paciente no se realizó exámenes genéticos y a la fecha es el único con DM en su familia.
Anamnesis próximaA los 75 años, debido a infecciones respiratorias recurrentes, asistió a consulta médica donde se le diagnosticó una neumonía lobular derecha, quedando con tratamiento médico y derivación a kinesioterapia. Desde el 2016 al 2023, el paciente realizó sesiones de kinesioterapia, dos a tres veces por semana. Esto lo complementaba con treinta minutos al día de actividad física (bicicleta o caminata) y entrenamiento de fuerza en gimnasio cuatro veces por semana, rutina que ya realizaba previo al inicio de las sesiones de kinesioterapia.
El usuario falleció en octubre del año 2023 (a los 84 años) debido a una neumonía lobular izquierda.
EvaluaciónA continuación se presenta la evaluación del paciente con comparaciones entre la primera evaluación del 2016 y la reevaluación del año 2023.
Inspección2016: a la observación, el paciente se encuentra sedente en su cama, sin dificultad para comunicarse. Presenta tos eficiente con secreciones, normotermia, sobrecarga respiratoria leve (saturación 92%), a la movilidad activa se observan rangos de movimientos disminuidos en miembros superiores. A la palpación se percibe atrofia muscular generalizada, con mayor énfasis en la musculatura flexora y abductora de hombro, extensora del cuello y de músculos faciales.
Postural2016: en el plano frontal se observa la cabeza en flexión (dropped head) logrando posición anatómica con dificultad. En el plano sagital se observa una disminución de la lordosis cervical, hipercifosis torácica, hiperlordosis lumbar, antepulsión pélvica y retropulsión de cintura escapular.
2023: a lo reportado anteriormente se suma cabeza en flexión completa, logrando la posición anatómica con asistencia (afirmándose de una silla o del terapeuta), hombro derecho elevado, curvatura toracolumbar con giba costal derecha (figura 1A y 1B). Al realizar el movimiento voluntario de elevación de la cabeza para mantener la posición anatómica, las desviaciones posturales observadas en el plano sagital aumentan (figura 2A y 2B).
2016: La primera evaluación de la musculatura facial fue a través de la movilidad activa (gestos emocionales) y movimientos mandibulares (elevación, depresión, protrusión y retracción). Se observaron los párpados superiores caídos (ptosis palpebral), debido a esto utiliza una prótesis con lentes ópticos para levantarlos. Además, existe una pérdida leve de la movilidad mandibular (presenta dificultad para la elevación de la mandíbula). No presenta dificultad para la deglución (realiza bien los gestos de masticación y deglución). En el resto de los grupos musculares se evaluó la fuerza muscular funcional según la escala de Daniels (tabla 1).
Comparación de la evaluación de la fuerza muscular por grupos musculares con la escala de Daniels
| Grupo Muscular | 2016 | 2023 |
|---|---|---|
| Flexores de hombro | M3 | M2 |
| Abductores de hombro | M3 | M2 |
| Extensores de hombro | M3 | M2 |
| Rotadores de hombro | M3 | M3 |
| Flexores de cuello | M3 | M2 |
| Extensores de cuello | M3 | M2 |
| Inclinadores y rotadores de cuello | M3 | M2 |
| Flexores y extensores de codo | M4 | M3 |
| Flexores y extensores del carpo y dedos | M4 | M3 |
| Flexores y extensores de cadera | M4 | M4 |
| Abductores y aductores de cadera | M4 | M4 |
| Rotadores de cadera | M4 | M4 |
| Flexores y extensores de rodilla | M4 | M4 |
| Flexores y extensores de tobillo | M4 | M4 |
| Eversores e inversores de tobillo | M4 | M4 |
| Flexores de tronco | M4 | M4 |
| Extensores de tronco | M3 | M3 |
| Inclinadores de tronco | M4 | M4 |
M0: Sin contracción.
M1: Contracción visible y palpable. Sin movimiento activo.
M2: Contracción voluntaria y completa. Movimiento activo, sin vencer la gravedad.
M3: Contracción voluntaria y completa. Movimiento activo, vence la gravedad.
M4: Contracción voluntaria y completa. Movimiento activo, vence la gravedad y resistencia moderada.
M5: Contracción voluntaria y completa. Movimiento activo, vence la gravedad y resistencia.
2023: se observa mayor debilidad de la musculatura facial (figura 3), aumento de la atrofia muscular, además de mayor dificultad para masticar y deglutir alimentos.
Flexibilidad2016: se observó una disminución de la movilidad pasiva en la flexión y abducción de hombro, presentan con end feel firme. Rotación y extensión de hombro, flexores y extensores de codo y carpo normales. En miembro inferior sólo se observó acortamiento muscular de la flexión de rodilla con end feel firme.
2023: no se observaron mayores cambios con respecto a la flexibilidad.
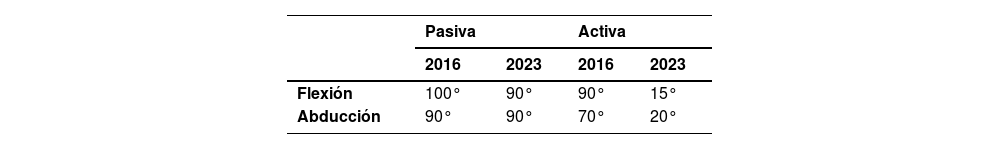
Sistema musculoesquelético2016: se evaluó el rango de movimiento activo y pasivo a través de goniometría. Los rangos de movimiento, tanto pasivos como activos, de flexión y abducción de hombro están disminuidos (tabla 2). La rotación medial-lateral y extensión de hombro están conservadas. Flexión y extensión de codo, manos, dedos y prono-supinación de antebrazo, conservadas. En miembros inferiores los rangos de movimiento pasivos y activos están conservados para movimientos funcionales.
2023: hubo una disminución en la flexión de cadera con rodilla extendida (60°) con end feel firme, la cual se completa al flectar la rodilla. En la columna cervical se observó una progresión en la limitación de la extensión e inclinación bilateral del cabeza-cuello. En la reevaluación se realizó goniometría de la movilidad pasiva de cuello, en donde la flexión está completa, la extensión llega a 10° y las inclinaciones a 30° ambas con end feel firme.
Sistema respiratorioSe le solicitó realizar una radiografía de tórax el año 2023, la cual muestra ascenso del hemidiafragma izquierdo (figura 4). A la auscultación respiratoria; murmullo pulmonar normal en el hemitórax derecho y disminuido en el hemitórax izquierdo. Entre los años 2016 y 2023, presentó infecciones respiratorias a repetición. El murmullo pulmonar en el hemitórax derecho disminuyó progresivamente durante los 7 años de kinesioterapia y la tos ineficiente con dificultad para eliminar secreciones.
Sistema neurológicoEncontramos hipotonía leve en miembros superiores e inferiores según la escala de Campbell, reflejos osteotendinosos disminuidos, sensibilidad superficial normal (sensibilidad táctil de los dermatomas), sin observar mayores cambios entre los años 2016 y 2023. Por otro lado, hay alteración de la sensibilidad profunda propioceptiva (alteraciones posturales), encontrándose un cambio el año 2023 por el aumento de algunas alteraciones posturales, tales como, la escoliosis.
Se le realizó una evaluación cognitiva con el Test Mini Addenbrooke's13 con puntuación máxima (30 puntos), resultado incompatible con deterioro cognitivo.
Marcha y equilibrio2016: en la marcha se observó una base de sustentación amplia y asistencia de ayuda técnica, bastón, a lado izquierdo. Destaca la antepulsión de pelvis, lo que genera una proyección del centro de gravedad hacia posterior y una disminución en su basculación pélvica, su extensión de tronco y la flexión de cuello. En las fases de la marcha, realiza un apoyo completo del pie con extensión completa del miembro inferior. En la fase de balanceo, tiene una mayor flexión de cadera al momento del paso, compensada con la ayuda del bastón. Fase de impulso sin alteraciones. Con respecto a la simetría, rota hacia derecha la cintura escapular, balanceo de los brazos disminuido, el paso del pie derecho es más corto y desviado hacia lateral. Con la asistencia del bastón, en superficies lisas, se observa un balance y equilibrio acorde a su edad. Sin embargo, frente a obstáculos y/o desniveles, pierde estabilidad.
2023: a su reevaluación se constata un aumento de la base de sustentación, la elevación de rodilla en la fase de balanceo y el desplazamiento hacia posterior del centro de gravedad. La estabilidad, por otro lado, se midió a través de test de estación unipodal, el cual salió alterado en ambas evaluaciones. Además, se aplicó la Escala de Tinetti14,15, con puntaje 6 para marcha y equilibrio, 12 puntos en total, lo que indica un riesgo grave de caídas. En el índice de Barthel16, obtuvo 50 puntos, en rango de dependencia severa.
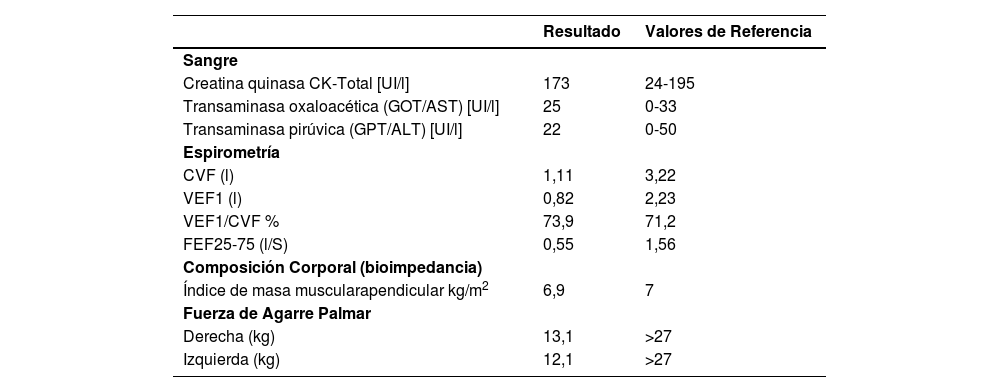
Integración sistémicaEl usuario se realizó exámenes de sangre cada 6 meses, para determinar valores de creatina quinasa (CK) en el tiempo (tabla 3). Para completar la evaluación se realizó una espirometría con el equipo MIR (Minispir, USA), la prueba de fuerza de agarre palmar (Jamar Plus+; Sammons Preston, Rolyon, Bolingbrook, IL, USA) y una bioimpedancia (Tanita MC780 MA, Tokio, Japón) (tabla 3).
Exámenes
| Resultado | Valores de Referencia | |
|---|---|---|
| Sangre | ||
| Creatina quinasa CK-Total [UI/l] | 173 | 24-195 |
| Transaminasa oxaloacética (GOT/AST) [UI/l] | 25 | 0-33 |
| Transaminasa pirúvica (GPT/ALT) [UI/l] | 22 | 0-50 |
| Espirometría | ||
| CVF (l) | 1,11 | 3,22 |
| VEF1 (l) | 0,82 | 2,23 |
| VEF1/CVF % | 73,9 | 71,2 |
| FEF25-75 (l/S) | 0,55 | 1,56 |
| Composición Corporal (bioimpedancia) | ||
| Índice de masa muscularapendicular kg/m2 | 6,9 | 7 |
| Fuerza de Agarre Palmar | ||
| Derecha (kg) | 13,1 | >27 |
| Izquierda (kg) | 12,1 | >27 |
CVF: Capacidad vital forzada.
VEF1: Volumen espirado forzado en el primer segundo.
FEF25-75: Flujo espiratorio forzado entre el 25% y 75%.
Alteración de la funcionalidad muscular global secundaria al diagnóstico médico de DM.
ObjetivoFavorecer la funcionalidad y mejorar la calidad de vida, facilitando una mayor independencia.
Objetivos específicos
- -
Mantener los rangos de movimiento pasivos y activos globales.
- -
Mantener la fuerza muscular global.
- -
Mejorar la flexibilidad.
- -
Mejorar el equilibrio y estabilidad estática y dinámica.
- -
Educar la concientización de posturas corporales correctas.
- -
Mejorar y/o mantener la capacidad aeróbica.
- -
Reeducar la marcha.
La terapia kinésica fue realizada por el mismo equipo durante los 7 años que el paciente permaneció en control. Se realizaron de dos a tres sesiones semanales de una hora de duración, las sesiones se estructuraron de la siguiente manera: preparación-desarrollo del objetivo-vuelta a la calma. Se planteó complementar los niveles de actividad física que el usuario realizaba previamente al inicio de las sesiones, integrando las actividades tanto en sesiones supervisadas por el kinesiólogo, como mediante pautas individualizadas para ser ejecutadas por el usuario los días que no asistía a terapia. La base de la intervención fue la mantención de los rangos de movimiento de miembros superiores, de columna vertebral y corrección del patrón de marcha. En detalle, los rangos de movimiento se trabajaron con el método Maitland, facilitación neuromuscular propioceptiva (FNP), movimiento terapéutico pasivo y activo. Para la fuerza muscular se realizaron ejercicios isométricos, concéntricos y excéntricos con Theraband® (color azul y verde) y mancuernas de 0,5 y 1kg. Los ejercicios de marcha y equilibrio fueron realizados en un entorno real, con el objetivo de corregir patrones posturales y optimizar las distintas fases de la marcha. A pesar del aumento progresivo de la DFEH, el usuario era capaz de mantener el tronco erguido en distintas posturas, sobre todo en bipedestación y en sedente, controlando su hiperlordosis lumbar. Para lograr esto, se trabajó la educación postural con retroalimentación táctil y verbal para corregir las alteraciones presentes en posición sedente y bípedo.
En relación a la marcha, se enfatizó el entrenamiento de la dorsiflexión de tobillo con el fin de prevenir la caída del pie en la fase de apoyo de talón. El ejercicio aeróbico se estructuró mediante sesiones de marcha con duración entre 20 a 30 minutos, controlando la frecuencia cardiaca mediante un pulsómetro, manteniendo frecuencias entre 120 y 145, según la fórmula de frecuencia cardíaca máxima18. Posteriormente, se incorporaron tareas funcionales, tales cómo trabajo específico con obstáculos, superficies irregulares y escaleras.
La vuelta a la calma se realizó con bicicleta estática, movilidad articular y elongaciones. Todas las series y repeticiones de los ejercicios se basaron en la escala de repetición máxima y tolerancia del usuario (Escala de Borg). Los ejercicios debieron ser adaptados según necesidad.
DiscusiónEs difícil diagnosticar la DM debido a que es poco frecuente y por la superposición clínica que presentan sus signos y síntomas. La biopsia muscular y los exámenes genéticos son la base de la confirmación diagnóstica, mientras que los análisis de sangre, con la CK como principal indicador, censan cómo evoluciona la destrucción muscular, además de su grado de severidad1–3.
Los últimos avances de exámenes genéticos han demostrado que existen distintos tipos de DM clasificada según los grupos musculares comprometidos2,3. En relación a esto, podemos hipotetizar que el paciente de este reporte de caso presenta una distrofia fascioescapohumeral. Esto concuerda con la historia clínica, las evaluaciones musculoesqueléticas (tabla 1) y la presencia de atrofia muscular en la musculatura de cuello, cara y miembros superiores (figuras 2 y 3). En complemento a lo anterior, las distrofias fascioescapohumerales se caracterizan por no permitir la flexión, abducción y elevación del hombro por encima de su altura; signos clínicos presentes en nuestro paciente (tabla 2)10,11,19. Adicionalmente, presentaba signos clínicos secundarios presentes en algunos casos de DFEH tales como hiperlordosis lumbar por debilidad de los abdominales, dropped foot por debilidad de los dorsiflexores, hipoacusia bilateral, ptosis palpebral, cardiopatía e insuficiencia respiratoria. Al comparar los signos clínicos presentados por nuestro paciente con los descritos en el estudio de Cea y Jiménez realizado en Chile en el año 201519, que incluyó a siete usuarios, se observa una concordancia significativa.
La evaluación realizada nos permitió objetivar la debilidad progresiva del músculo esquelético y también su atrofia. En la actualidad se sabe que estos fenómenos se relacionan con una disminución en la funcionalidad y aumento en la dependencia. En relación al caso clínico, este hecho es comprobable al observar su fuerza muscular (tabla 1), las características de su marcha y equilibrio (Escala de Tinetti) y la puntuación de su índice de Barthel (50 puntos).
La mayoría de los estudios y revisiones hacen referencia a las DM en la niñez, son escasos los reportes donde se describe el desarrollo de la DM en adultos y personas mayores3. El estudio de Cea y Jiménez enfatiza la ausencia de seguimiento clínico de la evolución de la DFEH de estos usuarios en nuestro país, atribuidos principalmente al subdiagnóstico o superposición diagnóstica19. En este contexto, se debe resaltar la relevancia del diagnóstico diferencial y el estudio genético, el cual no se realiza en todos los casos, y que no estuvieron disponibles para nuestro paciente.
Si bien la literatura indica que la DFEH no afecta al sistema nervioso, en nuestras evaluaciones encontramos alteración de los reflejos, del tono muscular y de la sensibilidad profunda, vinculados, según la literatura, a la disfunción del efector, en este caso el músculo esquelético y no a una lesión neurológica.
Es importante destacar que el paciente, sumado a la DFEH, presentaba sarcopenia, según sus resultados en fuerza de agarre palmar y masa muscular17,20. En el primer ítem, el usuario logró en ambas manos valores inferiores al punto de corte (≥27kg). A esto se suma el análisis de la bioimpedancia (tabla 3), donde el cálculo del índice de masa muscular esquelética apendicular (IMMA=MMA/altura al cuadrado) arrojó un valor de 6,9kg/m2 estando por debajo del punto de corte para el diagnóstico de sarcopenia (7,0kg/m2 en hombres). En este contexto, mantener la fuerza muscular global fue un objetivo importante a desarrollar en cada sesión, debido al estrés sobre el músculo esquelético de ambas condiciones fisiopatológicas.
Los efectos del ejercicio en personas mayores son conocidos21,22. Sin embargo, en el caso de la DFEH en una persona mayor la prescripción del ejercicio debe tener ciertas consideraciones. Algunos estudios sostienen que el ejercicio aeróbico ayuda a disminuir la sintomatología de pacientes con DM22–25. Por otro lado, los ejercicios de fuerza muscular de los miembros superiores tienen una respuesta que depende de cada paciente. En este contexto, no existe evidencia sobre la frecuencia, volumen e intensidad del ejercicio que se debe considerar en la DFEH, y se debe trabajar acorde a las características, necesidades y evolución individual de cada paciente23.
Un estudio llevó a cabo un programa de entrenamiento de fuerza isométrica y dinámica en usuarios con DFEH26. Los resultados sugieren que el ejercicio de fuerza dinámica podría contribuir a la mejoría de la sintomatología, no obstante, la evidencia no es suficiente para respaldar esta hipótesis22,23. Por otra parte, algunos estudios han evaluado distintas intervenciones farmacológicas, sin lograr los resultados esperados25,27. Entonces la DFEH está limitada por su carácter genético, lo que resalta la necesidad de encontrar enfoques terapéuticos integrales y personalizados.
La kinesioterapia tiene un rol fundamental para retrasar el avance de las manifestaciones clínicas de la DFEH23,24. El paciente permaneció siete años realizando kinesioterapia de forma sistemática, donde se alternaron ejercicios de fuerza muscular, flexibilidad, propioceptivos, correcciones posturales, siempre en concordancia con el objetivo general y las expectativas del usuario. Esto permitió mantener la actividad muscular, prevenir contracturas musculares, rigidez articular y disminución en los rangos de movimiento. Estas condiciones básicas permitieron conservar y optimizar el remanente de marcha existente, hecho que repercutió positivamente en sus actividades cotidianas. En este contexto, el mantenimiento de un tratamiento médico actualizado, junto con la kinesioterapia sistemática, permitieron mejorar el pronóstico funcional en este usuario. Actualmente, existe un manual de evaluación, seguimiento y tratamiento para la DFEH, el cual identifica diversas problemáticas relacionadas con el tratamiento adecuado27. Dicho documento concluye que la mejora de la fuerza muscular y la función muscular representan un objetivo terapéutico fundamental en el manejo de estos pacientes27. En consecuencia, persiste la necesidad de profundizar en la investigación respecto a los efectos del ejercicio físico y la terapia kinésica en personas con diagnóstico de DFEH, con el fin de generar evidencia que respalde intervenciones efectivas y basadas en resultados clínicos concretos.
Se reconoce, además, que el abordaje multidisciplinario adquiere particular relevancia en estos casos. La literatura respalda que un enfoque transdisciplinario es el modelo idóneo para la atención de personas con DM3. Por ello, se enfatiza la comunicación efectiva y una interacción fluida entre los distintos profesionales del equipo de salud, con el fin de brindar una atención integral, coordinada y centrada en las múltiples necesidades del paciente.
ConclusiónSe presentó un reporte de caso de un paciente octogenario con DM, donde se describieron características morfo-clínicas, evaluaciones e intervenciones realizadas. La kinesioterapia permitió mantener la funcionalidad y calidad de vida del paciente, a pesar del progreso en la disminución de la fuerza muscular. El ejercicio físico en pacientes con DM es una herramienta que podría reducir las complicaciones derivadas de la DM.
Conflictos de interésLos autores declaran no tener ningún conflicto de interés asociado a la elaboración de este artículo.
Aspectos éticosEl siguiente caso clínico fue aprobado por el Comité de Ética de la Pontificia Universidad Católica de Valparaíso, Chile (Código BIOEPUCV-H 671-2023). Se obtuvo el consentimiento informado firmado por el usuario para la publicación de este artículo.
FinanciamientoDI Asociativo 039.302/2024, Vicerrectoría de Investigación, Creación e Innovación, Pontificia Universidad Católica de Valparaíso, Chile.