La constipación crónica es una causa frecuente de consulta tanto a nivel de medicina general como de especialistas, con una prevalencia que varía entre el 2 y el 27% de la población. Es más frecuente en mujeres, en sujetos de edad avanzada y si bien no es una condición grave, altera significativamente la calidad de vida de los pacientes.
Puede ser primaria o secundaria a diversas patologías médicas. Su fisiopatología es multifactorial existiendo pacientes con tránsito colónico normal, con tránsito colónico prolongado o con alteraciones del defecatorias.
Su tratamiento tradicional se basa en cambios en la dieta y en el uso de laxantes de diferentes tipos. En los últimos años se han descubierto nuevos fármacos que mediante el aumento de la secreción de fluidos hacia el intestino o a través de un aumento de la motilidad colónica representan nuevas herramientas terapéuticas.
La cirugía tiene un rol importante en el manejo en un grupo seleccionados de pacientes, refractarios a la terapia tradicional.
Chronic constipation is a very common complaint encountered by both primary care physicians and specialists, with a prevalence ranging from 2 to 27% of the population. It is more commonly reported in women and elderly patients, with a significant impairment in quality of life.
Constipation may be primary or secondary to different diseases. Has a multifactorial pathophysiology and can be subclassified into normal transit constipation, slow transit constipation and defecation disorders.
Current treatment is based on dietary changes and different types of laxatives. New pharmacological treatments have been developed in the last years, which stimulate intestinal fluid secretion or colonic motility.
Surgery has an important role in selected patients who do not respond to current medical treatment.
La constipación es un motivo frecuente de consulta tanto a nivel de medicina general como en la consulta del especialista, que implica un costo no menor en salud y que impacta negativamente en la calidad de vida de quienes la portan (1).
Es una alteración basada en síntomas, con una definición muy subjetiva. Frecuentemente existe discrepancia entre lo que los médicos y lo que los pacientes llaman constipación (2, 3). Los médicos conciben la constipación como un fenómeno objetivo, basado fundamentalmente en una disminución del número de movimientos intestinales, considerando como normal una frecuencia entre tres movimientos intestinales por día hasta tres movimientos intestinales por semana. Los criterios de Roma III consideran como constipación la presencia de menos de tres movimientos intestinales por semana, asociados a la presencia de diversas molestias defecatorias (2).
Los pacientes perciben como constipación la presencia de dificultad para “obrar”, es decir una mayor consistencia de las deposiciones, deposiciones duras o la presencia de esfuerzo, más que el número de deposiciones en un determinado tiempo (1).
La constipación es una condición bastante prevalente en la población general, con valores variables dependiendo de la definición utilizada, es decir si es que se aplican los criterios de Roma III (Tabla 1) o prevalencias basadas en reportes de sintomatología por pacientes. Una revisión sistemática realizada en Estados Unidos, mostró una prevalencia entre un 1,9 a un 27,8% con un promedio de 14,8% de la población, utilizando diferentes criterios diagnósticos (4). Una revisión sistemática y metanálisis que determinó la prevalencia de constipación crónica en diferentes regiones del mundo utilizando diversos criterios, reporta una prevalencia de 18% en Sudamérica (5).
Criterios de roma III para constipación crónica
| Los criterios deben haber estado presentes en los últimos 3 meses con inicio de los síntomas al menos 6 meses antes del diagnóstico. |
| Presencia de 2 o más de los siguientes síntomas: |
| • Deposiciones duras en >25% de las defecaciones |
| • Esfuerzo defecatorio en >25% de las defecaciones |
| • Sensación de evacuación incompleta en >25% de las defecaciones |
| • Sensación de obstrucción anorectal y/o bloqueo en >25% de las defecaciones. |
| • Maniobras digitales para facilitar la defecación en >25% de las defecaciones |
| • < 3 evacuaciones por semana. |
| Rara vez presencia de deposiciones sueltas sin el uso de laxantes |
| Criterios insuficientes para la presencia de síndrome de intestino irritable. |
Es una condición que ocurre más frecuentemente en el sexo femenino que en los hombres con una relación hombre/mujer que va de 1.01 a 3.77, con una media de 2.2 (6). Esta diferencia por género ocurre principalmente en los menores de 50 años equiparándose en los mayores de 70 años con tasas de 20,6 y 25% respectivamente (6). El mecanismo exacto por el cual se produce esta diferencia no está claro, pero la evidencia acumulada sugiere un rol de las hormonas sexuales femeninas. A su vez la constipación aumenta en la medida que avanza la edad, particularmente después de los 65 años (6).
A pesar de lo frecuente que es como problema, sólo un pequeño porcentaje de los pacientes sintomáticos solicita atención médica y de aquellos que lo solicitan un buen número se siente insatisfecho con el tratamiento que recibe.
Diversos estudios han encontrado que la constipación impacta negativamente en la calidad de vida. Estos pacientes tiene puntajes más bajos en los ítemes de salud mental y física en el cuestionario SF 36 en comparación con sujetos controles.
En este escrito revisaremos el manejo actual de la constipación, enfatizando algunos puntos relacionados con la fisiopatología, métodos de estudio, tratamiento médico, incluyendo el uso de nuevos fármacos y tratamiento quirúrgico.
FisiopatologíaLa fisiopatología de la constipación crónica es multifactorial. Conceptualmente se divide en primaria o idiopática, en la cual existe una alteración intrínseca de la función colónica y/o anorrectal, y secundaria a diversas condiciones médicas y al uso de medicamentos (Tabla 2).
Causas de constipación secundaria
| A) Causas orgánicas: cáncer colorectal, masas extraintestinales, estenosis de colon quirúrgicas, postinflamatorias o isquémicas |
| b) Endocrinas o Metabólicas: diabetes mellitus, hipotiroidismo, hipercalcemia, insuficiencia renal crónica, porfiria |
| C) Neurológicas: injuria de la médula espinal, enfermedad de Parkinson, paraplejia, esclerosis múltiple, neuropatía autonómica, enfermedad de Hirschsprung, pseudoobstrucción intestinal crónica. |
| D) Miogénica: distrofias miotónicas, dermatomiositis, esclerodermia, amiloidosis, pseudoobstrucción intestinal crónica idiopática |
| E) Anorectal: fisuras anales, estenosis anal, enfermedad inflamatoria intestinal, proctitis |
| F) Fármacos: opioides, fármacos antihipertensivos, antidepresivos tricíclicos, hierro, anticonvulsivantes. |
| G) Dieta: baja ingesta de fibra. |
La más frecuente es la constipación primaria y en este grupo se pueden reconocer diferentes subtipos desde el punto de vista fisiopatológico. La constipación puede ser de tránsito lento (pasaje prolongado de las deposiciones a través del colon), puede ser con tránsito normal o puede existir una obstrucción funcional del tracto de salida, es decir la presencia de una disfunción del piso pélvico y de los esfínteres anales, generando una dificultad para evacuar las deposiciones desde el rectosigmoides (7).
La constipación con tránsito colónico normal, también llamada constipación funcional, es probablemente la forma más frecuente de constipación vista por los médicos generales. El paso de las deposiciones a través del colon y la frecuencia defecatoria son normales, pero los pacientes se sienten constipados. Estos pacientes reportan dificultad para evacuar, distensión abdominal, dolor abdominal o disconfort y deposiciones duras. Algunas investigaciones han demostrado que estos sujetos pueden presentar un aumento de la distensibilidad rectal y/o disminución de la sensación a este nivel. Existe una importante sobreposición entre este subgrupo de constipación con el síndrome de intestino irritable constipado (7, 8).
La constipación con tránsito lento representa aproximadamente la mitad de los pacientes con síntomas refractarios a la suplementación con fibra. Estos pacientes presentan movimientos intestinales infrecuentes (clásicamente menos de una vez por semana), y pueden presentar distensión y disconfort abdominal asociados. Las ganas de defecar son infrecuentes y rara vez presentan urgencia (8). Como lo dice su nombre tienen un tiempo de tránsito intestinal prolongado debido a alteraciones significativas de la actividad motora propulsiva del colon.
Diversos estudios han mostrado en estos sujetos una disminución de las HAPCs (high amplitude propagated contractions), las cuales son ondas propulsivas, de amplitud importante, que se inician en diversos puntos del colon y se propagan hacia el recto. Entre otras explicaciones, se piensa que la constipación de tránsito lento es una alteración neuromuscular del colon dado que se han encontrado anormalidades en el plexo mioentérico y alteraciones en las células de Cajal, cuyo volumen está significativamente reducido en estos pacientes. Las células de Cajal son fundamentales para la generación del ritmo eléctrico basal, el cual determina la actividad contráctil del colon. En ausencia de un ritmo eléctrico basal normal, la actividad contráctil del colon se reduce y se vuelve irregular, generándose una disminución del tránsito intestinal (8, 9).
Las alteraciones defecatorias o del tracto de salida son un grupo de anormalidades funcionales y anatómicas del anorecto que llevan a síntomas de constipación. Estos pacientes presentan importante esfuerzo defecatorio, pasan un largo período de tiempo en el inodoro, a veces requieren de maniobras digitales, de cambios de posición o del uso de enemas para lograr defecar.
Esta sintomatología puede deberse a una alteración de la contracción rectal, a una contracción paradojal del puborrectal, o a una inadecuada relajación anal, siendo la falta de coordinación o la disinergia de los músculos involucrados en la defecación la causa más importante. También son frecuentes anormalidades estructurales como por ejemplo: prolapso rectal, intususcepción rectal, rectocele (herniación usualmente de la pared rectal anterior hacia la vagina) y descenso excesivo del periné (7-9).
Evaluación diagnósticaUna cuidadosa historia clínica y un buen examen físico son los puntos más importantes de la evaluación de un paciente que sufre de constipación.
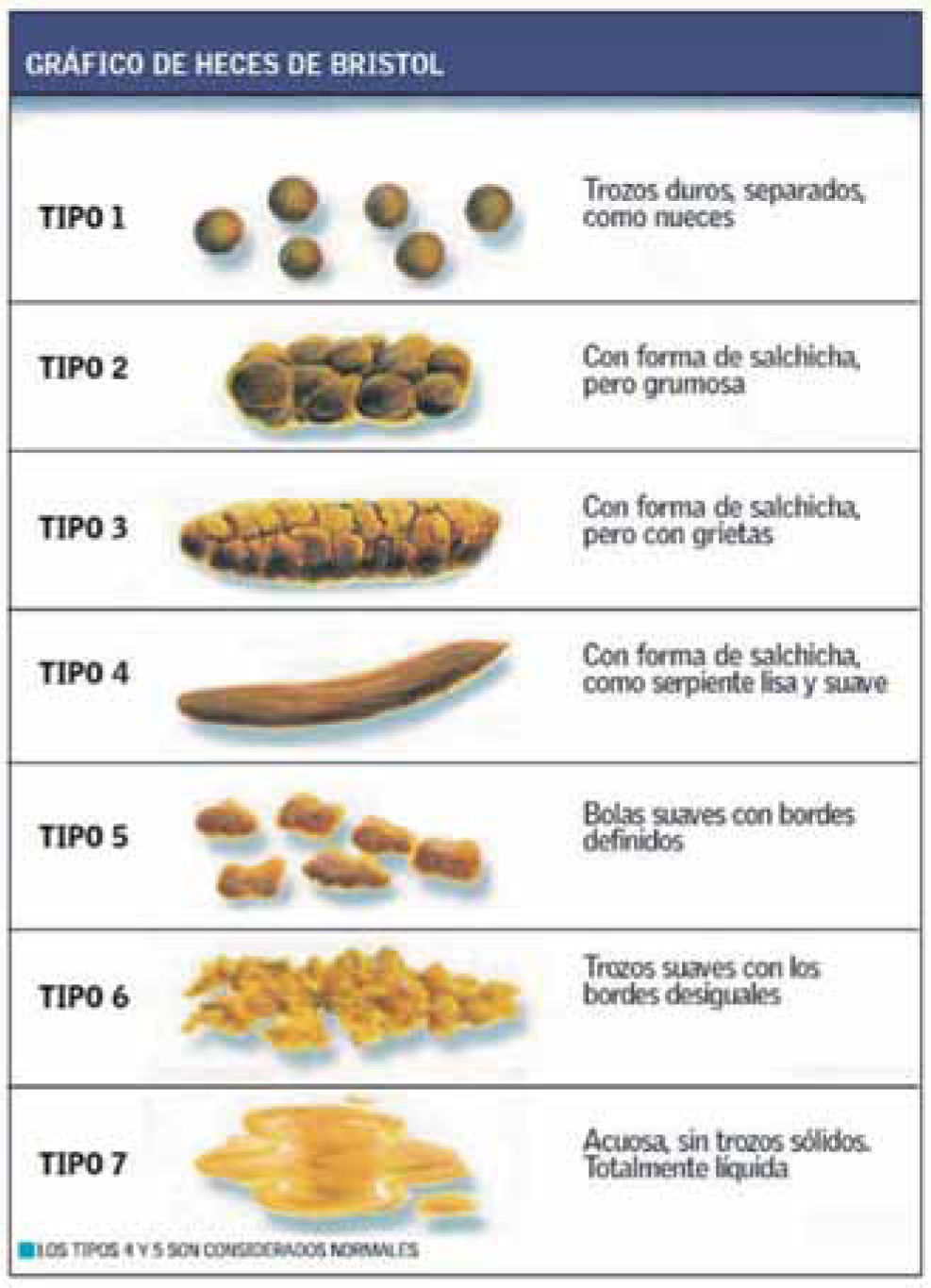
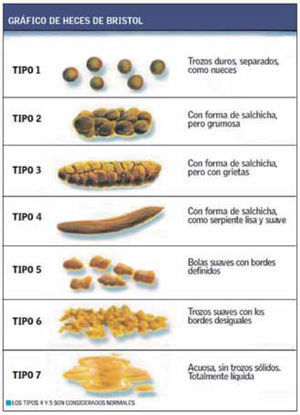
En la historia es fundamental comprender claramente la molestia del paciente. El uso de la escala de Bristol (figura 1) puede ser de utilidad para el que paciente describa la forma y la consistencia de sus deposiciones.
También es de suma importancia tener en claro cuales son las medidas generales que el paciente ha tomado por su cuenta para tratar de aliviar esta molestia, incluyendo información acerca del tipo, dosis y tiempo de uso de diferentes laxantes.
Es fundamental el buscar signos de alarma o banderas rojas, sugerentes de una enfermedad gastrointestinal más seria que requiere una investigación más profunda. Estos signos de alarma incluyen: baja de peso no intencionada, sangre en las deposiciones, anemia, cambio brusco del hábito intestinal luego de los 50 años de edad, dolor abdominal significativo e historia familiar de cáncer de colon o de enfermedad inflamatoria intestinal (10).
El examen físico debe incluir la palpación del abdomen en la búsqueda de deposiciones palpables que impliquen una retención estercorácea.
Un examen rectal cuidadoso es crítico ya que permite la detección de patología anal como estenosis, fisuras, inflamación, rectocele o masas. La falta de descenso del periné al pujar sugiere la presencia de disfunción del piso pélvico (10).
En cuanto a exámenes, numerosos pruebas diagnósticas, incluyendo exámenes de laboratorio (hemograma, hormonas tiroideas, calcemia) y test estructurales del colon (ej: colonoscopía, sigmoidoscopía flexible o enema baritado) han sido recomendados para excluir causas secundarias de constipación crónica, aunque no hay datos que avalen esta medida. El American College of Gastroenterology no recomienda el uso de colonoscopía de rutina en todos los pacientes que consultan por constipación aunque sí se recomienda la colonoscopía como screening de cáncer de colon en todos los pacientes mayores de 50 años (11) y en los pacientes que presentan signos de alarma.
En aquellos pacientes con síntomas de constipación crónica que no responden a la terapia convencional, los diagnósticos de constipación de tránsito lento, disinergia del piso pelviano y otras alteraciones de la musculatura ano-rectal deben ser considerados. El diagnóstico de estas alteraciones es posible a través de exámenes radiológicos y fisiológicos. En general, recomendamos que el estudio funcional específico sea dirigido por un especialista, pues puede significar incomodidad y costos importantes para el paciente, y los resultados de estas pruebas son de compleja interpretación.
El tiempo de tránsito colónico, es un estudio simple, relativamente barato y no invasivo que permite objetivar el tiempo de tránsito intestinal. Los movimientos colónicos, de segmentación, retrógrados y de propulsión, son los determinantes de aproximadamente el 90% del tiempo de tránsito digestivo total. De esta forma, la ingesta de 20-24 marcadores radio-opacos y una radiografía de abdomen simple al tercer y quinto día es la manera más fácil de medir el tiempo de tránsito colónico. En sujetos normales, el 80% de los marcadores habrán sido eliminados para el quinto día. Además de objetivar los trastornos del tránsito, permite agrupar a los pacientes en dos categorías, según el patrón de distribución de los marcadores: Inercia colónica, cuando los marcadores están difusamente distribuidos por el colon, y obstrucción defecatoria, en los pacientes que demuestran persistencia de marcadores en el recto o rectosigmoides.
La manometría anorrectal, si bien es un examen intuitivamente asociado al estudio de la incontinencia anal, la manometría anorrectal es de importancia para descartar Chagas o enfermedad de Hirschsprung de segmento corto, que aunque raro, puede alterar significativamente el manejo de pacientes constipados. Se miden presiones de reposo y de contracción voluntaria a diferentes niveles del margen anal para establecer un canal anal funcional. También se pueden medir volúmenes de sensación rectal para intentar establecer la sensibilidad rectal y su capacitancia. Sin embargo, en pacientes constipados la búsqueda de reflejo rectoanal inhibitorio es escencial para definir dos grupos: aquellos que relajan el esfínter después de una dilatación rectal (reflejo presente, normal) y aquellos con ausencia de reflejo, sugerente de Chagas o enfermedad de Hirschsprung de segmento corto. El Test de Expulsión de Balón consiste en evacuar un balón inflado con 50 cc de agua. Su utilidad para diagnosticar disinergias de piso pelviano y trastornos evacuatorios es controversial, siendo de primera importancia en algunos grupos (12, 13) y de poco valor en otros (14, 15). No se recomienda como método único de diagnóstico en para pacientes con obstrucción defecatoria.
La defecografía o cinedefecografía permite objetivar los cambios dinámicos de los órganos pelvianos durante la defecación. Se puede realizar mediante una resonancia magnética de pelvis o con radiología convencional y contrastes baritados. Es especialmente útil en pacientes con historia de pujo crónico, digitación para evacuar, patrón obstructivo en tiempo de tránsito colónico o con úlcera solitaria de recto en la endoscopía, pues puede revelar la causa de la obstrucción defecatoria, como una contracción paradojal del puborrectal, invaginación recto-rectal, rectoceles, sigmoido o enteroceles o prolapso rectal. La principal ventaja de la cinedefecografía por resonancia magnética es la posibilidad de evaluar el piso pelviano completo en un solo examen, incluyendo los compartimientos ginecológicos y urológicos, pues es frecuente observar trastornos asociados. Además, permite obtener múltiples imágenes en un plano sagital que se pueden ver secuencialmente en modalidad “cine” permitiendo una mejor comprensión de la dinámica de los órganos pelvianos.
Tratamiento médicoOpciones de tratamiento tradicionalesLas opciones tradicionales del manejo de la constipación incluyen la suplementación con fibra y el uso de diversos tipos de laxantes.
En general una de las primeras aproximaciones de tratamiento es el uso de fibra y/o de agentes formadores de masa. Se recomienda el consumo de al menos 20 a 25 gramos de fibra por día, pudiendo utilizarse algunas sustancias como el salvado de trigo en la dieta.
Además productos comerciales como el mucílago hidrofílico de psyllium (plantago ovata) y la metilcelulosa pueden ser de utilidad. Su uso se basa en que estas sustancias al atraer agua hacia el lumen intestinal, aumentan el volumen de las deposiciones y disminuyen su consistencia. Desafortunadamente la suplementación con estos productos puede tener algunas limitaciones, dadas principalmente por la presencia de flatulencia y distensión abdominal (7, 16).
Revisiones recientes avalan la utilidad del uso de fibra soluble (psyllium). Comparada con placebo la fibra soluble mejora en forma global los síntomas (86.5% vs 47.4%), mejora el esfuerzo defecatorio (55.6% vs 28.6%), mejora la consistencia de las deposiciones y aumenta el número de movimientos intestinales por semana. La evidencia actual del uso de fibra insoluble (salvado de trigo) es conflictiva (17).
Laxantes osmóticos: contienen sustancias pobremente absorbibles que sirven como agentes osmóticos, atrayendo agua hacia el lumen intestinal. Dentro de estos se encuentran la lactulosa, el sorbitol, el polietilenglicol, el citrato de magnesio, al sulfato de magnesio y el hidróxido de magnesio o “leche de magnesia”.
Aunque no hay estudios randomizados controlados que demuestren la eficacia de las sales de magnesio, la opinión de expertos y la experiencia clínica avalan su uso (16). Debido a que el magnesio es excretado por vía renal no se recomienda su uso en pacientes con insuficiencia renal. La lactulosa es segura y efectiva en normalizar la frecuencia defecatoria. Tres estudios randomizados controlados (2 en pacientes con constipación funcional y uno en pacientes con constipación asociada a opiáceos) muestran una significativa mejoría de la frecuencia de los movimientos intestinales con un número necesario a tratar (NNT) de 3.9 (11, 16).
El polietilenglicol o PEG es un polímero no absorbible que también atrae fluidos hacia el lumen intestinal. Tanto su fórmula enriquecida con electrolitos (comúnmente usada para la preparación de colonoscopía) como su fórmula sin electrolitos (PEG 3350), son efectivas en mejorar la frecuencia y la consistencia de las deposiciones en estudios randomizados controlados (ERC) (11). Habitualmente una dosis de 17 gramos por día disuelta en 250 ml de agua, es de utilidad.
Un metanálisis reciente que incluyó 5 ERC, reportó que el NNT para mejorar la constipación usando agentes osmóticos (lactulosa en un estudio, PEG en 4) fue de 3 (IC 95% 2-4) (18).
Laxantes estimuladores: son sustancias que actúan a nivel del lumen alterando el transporte de electrolitos y aumentando la secreción intraluminal de fluidos. Además en contacto con la mucosa indirectamente estimulan las terminaciones nerviosas sensoriales lo que lleva a un aumento de la motilidad colónica.
En este grupo se incluye al bisacodyl, el picosulfato de sodio, al senna, el aloe y la cáscara sagrada (7). A pesar de que diversos estudios antiguos han demostrado que son superiores a placebo, debe tenerse especial cuidado dado que pueden producir disconfort y dolor abdominal. Este tipo de laxantes deben ser recomendados sólo para uso ocasional (11).
Nuevos tratamientos farmacológicosLubiprostoneLos canales de cloro (CIC) son proteínas que están localizadas en muchas de las células de nuestro organismo. Tienen diversas funciones entre ellas: el transporte de fluidos a través de las membranas epiteliales, la regulación del volumen celular y del pH y la mantención del potencial de membrana. Nueve diferentes canales han sido identificados. Este tipo de canales están involucrados en la secreción de cloro (19).
El canal de cloro tipo 2 (CIC-2) es de particular interés dado que cuando es activado se promueve la secreción intestinal de fluidos. La secreción intestinal de fluidos hacia el tracto gastrointestinal mejora la consistencia de las deposiciones y puede contribuir a normalizar el tránsito intestinal (19).
El lubiprostone es un activador de los canales de cloro, el que genera un aumento de la secreción intestinal. Su mecanismo exacto aún está en estudio, pudiendo activar a los CIC-2, a canales relacionados con el regulador transmembrana de la conductancia de la fibrosis quística (CFTR) y/o a receptores de prostaglandinas acoplados a la proteína G. Este nuevo fármaco no tiene efecto sobre el tránsito colónico.
Fue aprobado por la FDA en el año 2006 para el tratamiento de la constipación crónica idiopática, tanto en hombres como en mujeres, a una dosis de 24 mcg dos veces al día, y en 2008 fue aprobado para el tratamiento del Síndrome de Intestino Irritable con predominio de constipación en mujeres (8 mcg por 2 veces al día).
Diversos estudios han mostrado que aumenta significativamente el número de movimientos intestinales por semana en relación al placebo. Además recientemente se ha visto que su uso crónico (48 semanas) es seguro y bien tolerado. Su uso a largo plazo disminuye la severidad de la constipación, la distensión abdominal y el disconfort en relación con el basal (20). Su principal efecto adverso es la nausea, la cual se observa en un 19% de los pacientes.
LinaclotideEl linaclotide es un péptido sintético de 14 aminoácidos que es capaz de unirse y activar al receptor de la guanilato ciclasa C en la superficie luminal del epitelio intestinal. La activación de la guanilato ciclasa C genera GMP cíclico, el que a su vez genera una cascada de transducción que activa al regulador transmembrana de conductancia de la fibrosis quística. La activación de este canal genera secreción de cloro y bicarbonato hacia el lumen intestinal, aumentado la secreción intestinal de fluidos y acelerando el tránsito (21).
Al menos dos ERC publicados en el 2011 que determinaron su utilidad por un período de 12 semanas, en dos diferentes dosis (145 o 290 mcg/día) (21), demostraron que este fármaco disminuye significativamente las molestias intestinales y abdominales en paciente con constipación crónica.
PrucaloprideEl prucalopride es un agonista de los receptores 5HT4 de la serotonina. La serotonina es un neurotransmisor ampliamente involucrado en la regulación de la motilidad, de la sensibilidad visceral y de la secreción intestinal. La estimulación de los receptores 5HT4 mediante sustancias agonistas, activando así la peristalsis, ha sido previamente demostrado como un blanco terapéutico efectivo. Fármacos como la cisaprida y el tegaserod forman parte de esta familia, los que dado su baja selectividad para estos receptores han visto limitado su uso clínico por la presencia de efectos adversos especialmente de tipo cardiovascular (7).
Prucalopride es un agonista altamente selectivo de los receptores 5HT4. En pacientes con constipación crónica, el prucalopride aumenta la frecuencia de los movimientos intestinales y disminuye la consistencia de las deposiciones, dado que estimula la motilidad gastrointestinal y colónica (22). Un metanálisis de 7 ERC comparando prucalopride (2 o 4mg por via oral al día) con placebo en 2639 pacientes con constipación crónica reportó un NNT =6 (22).
Se ha recomendado una dosis de 2mg/día, vía oral, excepto en los mayores de 65 años en los que se recomienda 1mg/día.
En octubre del 2009 fue aprobado en Estados Unidos para el tratamien-to de la constipación crónica en mujeres.
En estos momentos este fármaco es considerado como un tratamiento de segunda línea, siendo utilizado en pacientes con constipación severa. Parece ser seguro, con escasos efectos secundarios (22) y además dado su acción en el tracto gastrointestinal alto y bajo, tiene un rol en alteraciones caracterizadas por la presencia de hipomotilidad.
Tratamiento quirúrgicoLa cirugía de la constipación comienza a principios del 1900 con la descripción de Sir Arbuthnot Lane (23) sobre colectomías totales e ileorrectoanastomosis en pacientes con “estasia intestinal”. Inicialmente descrita para todo paciente con “estasia”, los resultados funcionales y la morbimortalidad del procedimiento hicieron que esta técnica cayera en descrédito. Sin embargo, con la aparición de diferentes exámenes y la disminución de la morbimortalidad quirúrgica, reaparece el interés por tratar esta patología, lo que se ve reflejado en un aumento de publicaciones en los últimos 20-25 años reevaluando el rol de este procedimiento en el manejo de los pacientes constipados.
La mejor comprensión de mecanismos defecatorios y la mejor sensibilidad de estudios preoperatorios, han ampliado el tratamiento quirúrgico no solo a pacientes con inercia, sino en gran medida a pacientes con obstrucción defecatoria. Incluso, algunos trabajos sugieren que de los pacientes que fracasan a tratamiento médico, son pocos los que tienen una inercia colónica aislada y la gran mayoría correspondería a trastornos evacuatorios, o la mezcla de ambos fenómenos (24).
Indicaciones de manejo quirúrgicoInercia colónicaLa inercia colónica se caracteriza clínicamente por la baja frecuencia de eliminación de heces duras, casi siempre con ayuda de laxante, y ausencia de maniobras digitales para facilitar la evacuación. Entre los exámenes destaca una retención mayor al 20% de los marcadores radioopacos en el estudio de tiempo de tránsito colónico, con una distribución uniforme de marcadores radiópacos a lo largo del colon.
Se observa más frecuentemente en mujeres jóvenes y su etiología es desconocida, aunque se asocia a alteraciones de los ganglios en el plexo mientérico y a alteraciones del contenido y distribución de neurotransmisores en este plexo.
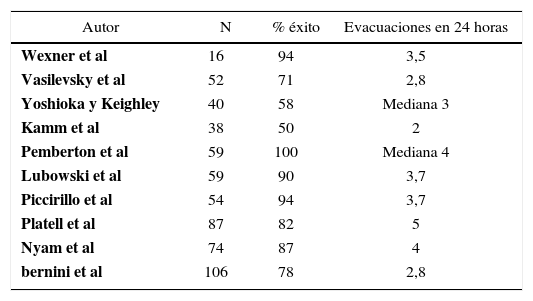
La colectomía subtotal e íleo-recto anastomosis propuesta por Lane hace casi 100 años ha sido en los últimos años el tratamiento de elección de estos pacientes. Entre un 70 a 90% de los pacientes reportan disminución significativa de los síntomas, que se mantiene en el largo plazo. La frecuencia defecatoria aumenta significativamente a cerca de 3-4 evacuaciones por día (tabla 3). Sin embargo, el procedimiento no está exento de complicaciones, siendo la obstrucción intestinal la más frecuentemente reportada, en un 7 a 50% de los pacientes, algunos de los cuales requieren una re-intervención (25). La vía laparoscópica ha mostrado resultados similares a la cirugía abierta en lo funcional, con los beneficios cosméticos y de recuperación para el paciente. Aún está por demostrarse una reducción de la incidencia de obstrucción intestinal en el postoperatorio (tabla 3).
Resultado de colectomías subtotales e íleo-rectoanastomosis en pacientes con inercia colónica
| Autor | N | % éxito | Evacuaciones en 24 horas |
|---|---|---|---|
| Wexner et al | 16 | 94 | 3,5 |
| Vasilevsky et al | 52 | 71 | 2,8 |
| Yoshioka y Keighley | 40 | 58 | Mediana 3 |
| Kamm et al | 38 | 50 | 2 |
| Pemberton et al | 59 | 100 | Mediana 4 |
| Lubowski et al | 59 | 90 | 3,7 |
| Piccirillo et al | 54 | 94 | 3,7 |
| Platell et al | 87 | 82 | 5 |
| Nyam et al | 74 | 87 | 4 |
| bernini et al | 106 | 78 | 2,8 |
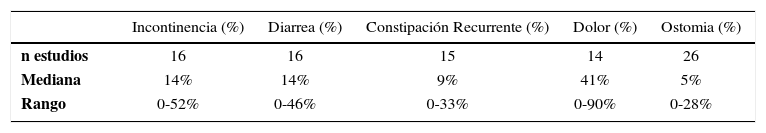
Por otra parte, la persistencia de dolor abdominal y distensión no es infrecuente, lo que debe ser conversado con el paciente para manejar sus reales expectativas (tabla 4).
Revisión de resultados adversos en colectomía total para constipación en 27 estudios de 1988-1998 (25)
| Incontinencia (%) | Diarrea (%) | Constipación Recurrente (%) | Dolor (%) | Ostomia (%) | |
|---|---|---|---|---|---|
| n estudios | 16 | 16 | 15 | 14 | 26 |
| Mediana | 14% | 14% | 9% | 41% | 5% |
| Rango | 0-52% | 0-46% | 0-33% | 0-90% | 0-28% |
Dada la significativa morbilidad asociada al procedimiento, consideramos que la colectomía es el tratamiento de última instancia para los pacientes portadores de inercia colónica, y que se justifica en pacientes altamente seleccionados, con evaluación previa por gastroenterólogo, fracaso a medidas convencionales y farmacológicas, y demostración clara de alteración de motilidad colónica por tiempo de tránsito colónico (en 2 oportunidades), y sin alteración de motilidad intestinal ni evidencias de Hirschsprung o síndrome de obstrucción defecatoria.
El uso de colectomías segmentarias permanece como una opción controversial, debido a que múltiples publicaciones demuestran una alta tasa de recurrencia de la constipación a mediano plazo. Sin embargo, en los últimos años han aparecido grupos que reportan colectomías segmentarias en pacientes bien seleccionados con estudios de motilidad segmentaria del colon y resultados aceptables en el mediano plazo (36).
La neuromodulación periférica y el implante definitivo de marcapasos para estimulación de raíces sacras (S2 y S3) han ganado un importante espacio en los últimos 5 años. Aparentemente la estimulación de S2 induce secuencias de propagación retrógradas y S3 induce secuencias de propagación anterógradas. Sin embargo, el efecto neto es que aumenta la frecuencia defecatoria en un 75% de los pacientes. Existen reportes de disminución de dolor abdominal y pelviano, disensión abdominal y sensación defecatoria que además sugieren que la neuroestimulación no solo juega un rol en la motilidad gastrointestinal, sino también afecta la sensibilidad. No está claro si esto ocurre a nivel central o periférico
Utilizando neuroestimulación periférica del nervio tibial posterior, se logró aumentar el número de evacuaciones mensuales de 9 a 16 en un grupo de 18 pacientes, con mejoría significativa de la calidad de vida y mínimos efectos adversos (26).
La neuroestimulación central ha sido la más estudiada. La técnica es simple y con mínimos efectos adversos y complicaciones, casi todas reversibles. Consiste en implantar por vía percutánea un electrodo cerca de las raíces sacras (S2 y S3), a través del tercer foramen sacro. Se conecta el electrodo a un marcapaso externo por un período corto y de haber respuesta, se conecta a un marcapaso definitivo. El principal inconveniente es el costo de la técnica y la imposibilidad de predecir respuesta en grupos predeterminados de pacientes. Cabe mencionar que existe una gran paradoja en relación a la neuroestimulacion, y es que se ha demostrado utilidad en incontinencia fecal y urinaria, en algunas uropatías obstructivas y en constipación, lo que demuestra la poca evidencia científica sólida de sus mecanismos de acción.
Mediante esta técnica, diferentes grupos han mostrado tasas de éxito variable, algunas incluso sobre un 75% en pacientes implantados (27). El trabajo de mayor tamaño corresponde a Kamm (28), quien realizó una prueba de neuroestimulación en 65 pacientes, de los cuales 45 presentaron mejoría y fueron a implante definitivo de marcapasos. De estos, a los 28 meses de media de seguimiento, un 87% de los pacientes aún presentaba una mejoría significativa en el número de evacuaciones.
Megacolon y megarectoEn pacientes con dilatación anormal del colon, ya sea segmentaria o difusa, la manometría ano-rectal define 2 grupos según el reflejo rectoanal inhibitorio: si está ausente, la etiología puede ser de origen congénito (Hirschspung) o adquirido (Chagas). Si está presente orienta a un megacolon idiopático, cuyo tratamiento es similar al de la inercia colónica. La enfermedad de Hirschsprung en adultos es rara y se diagnostica por la ausencia de ganglios en una biopsia de pared completa rectal o por aumento de la actividad de acetilcolinesterasa, en la muscularis mucosae o lámina propria en una biopsia por aspiración. Su tratamiento depende de la extensión de la enfermedad, aunque la mayoría de los casos en adultos, con compromiso de segmentos corto o ultracortos, se tratan con una miomectomía interna, posterior, de unos 6 x 1cm de ancho, empezando desde la línea dentada o 2cm hacia proximal. El éxito es cercano a 90-100% de los pacientes, aunque está descrita la persistencia de constipación y la incontinencia postoperatoria.
La Enfermedad de Chagas es endémica en muchas áreas de Sudamé-rica, causada por el Tripanosoma cruzi, transmitida a humanos por la picadura de la vinchuca. El diagnóstico se confirma por serología (ELISA, IFI) o mediante técnicas de PCR.
Las alternativas quirúrgicas para el tratamiento el megacolon Chagásico apuntan a la remoción o exclusión del segmento diskinético, realizando una operación de Duhamel-Haddad modificada o una rectosigmoidectomía más anastomosis colorrectal.
Obstrucción defecatoriaExisten múltiples trastornos del piso pelviano que se asocian a constipación como rectoceles, invaginaciones rectoanales o recto-rectales, sigmoidoceles, prolapso rectal, contracción paradojal del puborrectal, etc. Muchas de estas alteraciones, evidenciadas especialmente en la cinedefecografía son también frecuentes en pacientes asintomáticos, por lo que a excepción del prolapso rectal, cuyo diagnóstico es clínico y su tratamiento de primera línea es quirúrgico, se recomienda tratar a estos pacientes con medidas generales, aporte de fibra y biofeedback (29). Frente al fracaso de las medidas conservadoras, han aparecido en los últimos años múltiples técnicas quirúrgicas que apuntan a corregir la obstrucción defecatoria.
La técnica de STARR (por sus siglas en inglés, stapled transanal rectal resection), consiste en una resección en manguito de unos 3cm aproxi-madamente del recto inferior, con el uso de grapadoras. Inicialmente fue concebida para corregir el rectocele, sin embargo, ha ganado aceptación en otros trastornos defecatorios como invaginación recto-rectal. Sus resultados son variables, pues los grupos son heterogéneos. Sin embargo, múltiples reportes de EE.UU. y Europa sugieren una efectividad cercana al 85% en la sintomatología de obstrucción defecatoria asociada a rectocele e invaginación recto rectal (30).
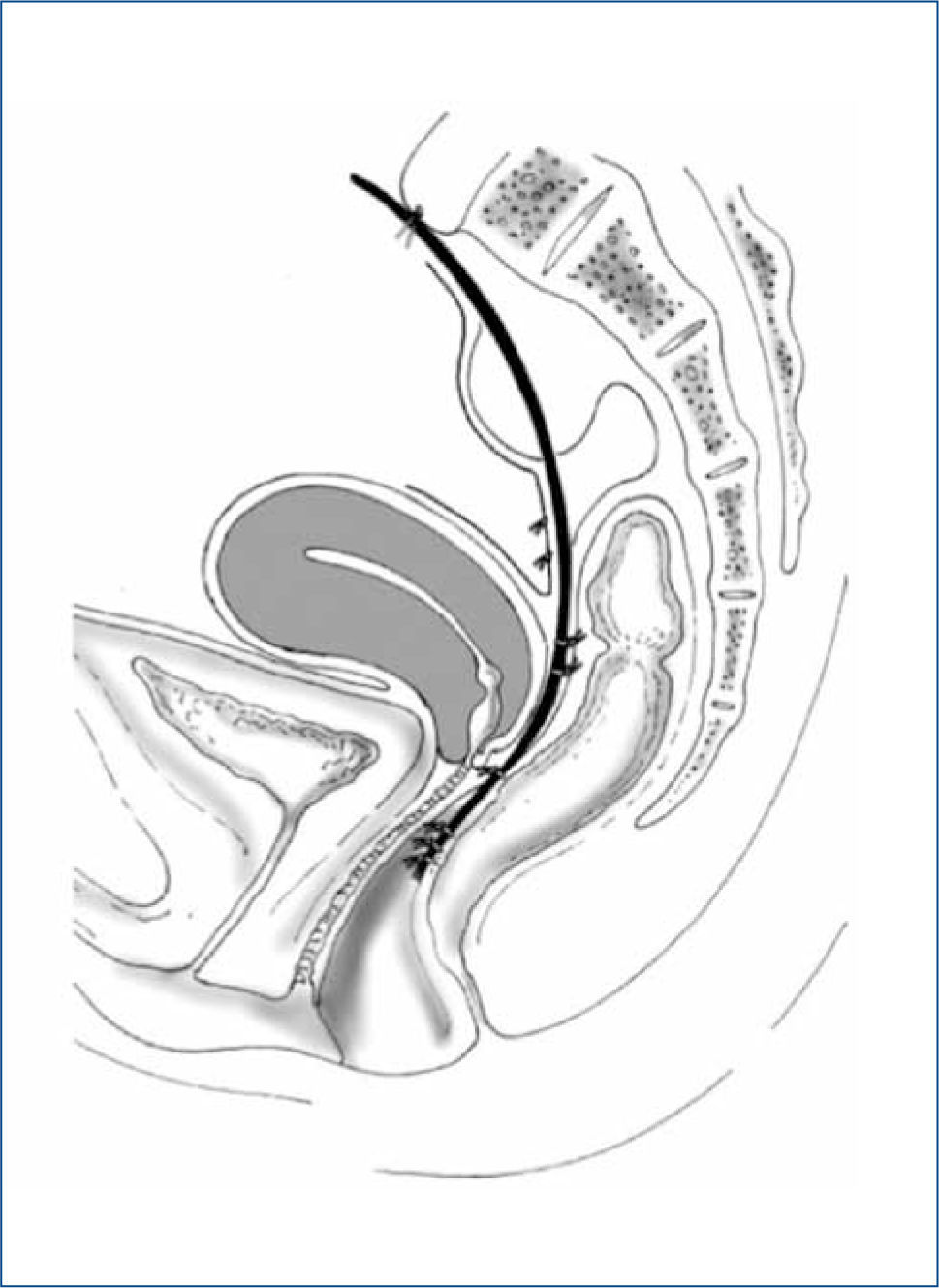
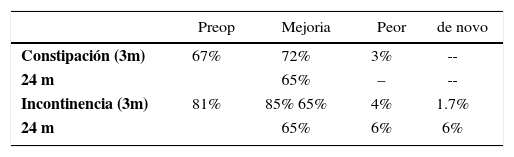
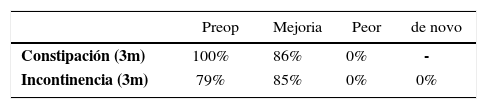
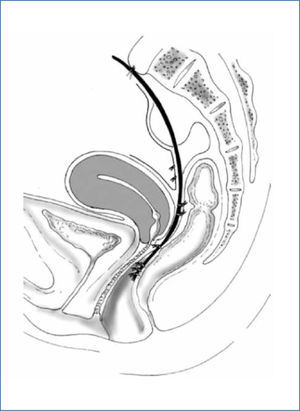
La Rectopexia Ventral es una técnica descrita en 2004 por D´Hoore (27) que consiste en fijar con una malla libre de tensión la pared anterior del recto y posterior de la vagina, al promontorio sacro (Figura 2). Su utilidad se ha descrito en pacientes con prolapso rectal externo (28) y en pacientes con sintomatología de obstrucción defecatoria (29,30) sin prolapso rectal externo, pero con invaginación recto-rectal significativa demostrada por cinedefecografía. En pacientes con prolapso rectal externo ha demostrado ser una técnica segura, aún en ancianos (35). La técnica tiene buenos resultados en recurrencia del prolapso y excelentes resultados funcionales, con disminución significativa de la sintomatología de constipación e incontinencia y baja tasa de constipación de novo (Tablas 5 y 6) frecuente en algunos tipos de correcciones de prolapso. En obstrucción defecatoria, los resultados funcionales son similares.
Esquema Rectopexia Ventral (tomado de D´Hoore et al, referencia 31)
Resultados funcionales post rectopexia ventral en prolapso externo
| Preop | Mejoria | Peor | de novo | |
|---|---|---|---|---|
| Constipación (3m) | 67% | 72% | 3% | -- |
| 24 m | 65% | – | -- | |
| Incontinencia (3m) | 81% | 85% 65% | 4% | 1.7% |
| 24 m | 65% | 6% | 6% |
(Referencia 32)
Resultados funcionales post rectopexia ventral en invaginación recto-rectal
| Preop | Mejoria | Peor | de novo | |
|---|---|---|---|---|
| Constipación (3m) | 100% | 86% | 0% | - |
| Incontinencia (3m) | 79% | 85% | 0% | 0% |
(Referencia 30)
Por lo tanto la cirugía es una alternativa para el manejo de pacientes con constipación crónica. Sin embargo, los resultados funcionales no siempre son perfectos y existe el riesgo de complicaciones. Por lo tanto, se sugiere evaluar cuidadosamente a los pacientes candidatos a cirugía, idealmente en el contexto de un equipo multidisciplinario que involucre activamente a un gastroenterólogo. La adecuada selección de los pacientes es la mejor manera de optimizar los resultados funcionales y minimizar la morbilidad.
SíntesisLa constipación crónica es una patología altamente prevalente cuyos síntomas pueden ser severos alterando en forma importante la calidad de vida del paciente.
Aunque existen diversos laxantes disponibles, tanto de venta libre como de prescripción médica, los pacientes frecuentemente requieren de terapias adicionales para lograr un óptimo alivio de su sintomatología.
La base del tratamiento reside en cambios en la dieta y en el uso de laxantes considerados como tradicionales. Si este tipo de terapia falla, el uso de agentes promotores de la motilidad y/o de activadores de los canales de cloro pueden ser de utilidad, aunque hasta el momento no disponemos de estos nuevos fármacos en nuestro medio.
En casos refractarios, especialmente secundarios a inercia colónica y/o a megacolon o megarecto, la cirugía es una opción terapéutica, que requiere una adecuada evaluación funcional de los pacientes.
El conocer la fisiopatología de la constipación y el espectro de presentación clínica nos permite ajustar nuestro tratamiento, logrando mejores resultados con nuestros pacientes.
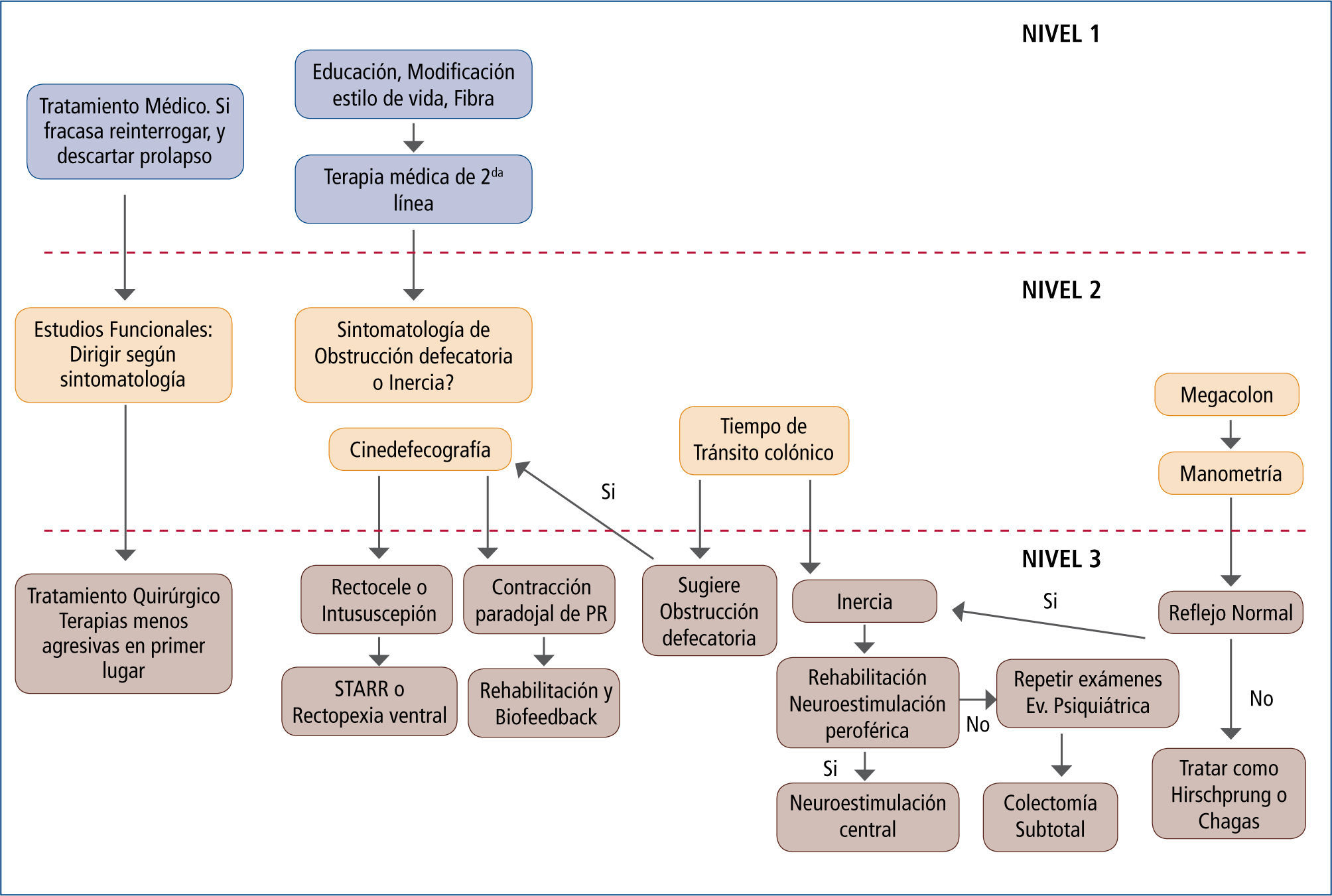
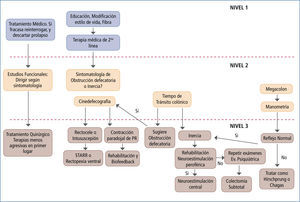
*En la figura 3 los autores presentan una propuesta para estudio y tratamiento de la constipación crónica.
Los autores declaran no tener conflictos de interés, con relación a este artículo.