La prevención y detección temprana de las patologías neoplásicas constituyen una prioridad epidemiológica de primer orden en el mundo actual. Dentro de éstas, el cáncer de próstata (CP) es el tercer más frecuente en Chile, con una tasa de incidencia de 145.3 x 100.000 habitantes masculinos, y la segunda causa de muerte por cáncer. Esta incidencia probablemente seguirá en alza por el desarrollo y mayor disponibilidad de mejores métodos diagnósticos.
Si bien se han identificado muchos factores potencialmente modificables relacionados con la aparición y desarrollo de tumores malignos en la próstata, no existe aún evidencia de estrategias que logren reducir su incidencia de manera significativa.
Estas características sumadas a la baja incidencia de síntomas en los estadíos tempranos de la enfermedad, impone la necesidad de modificar e idealmente detener su progresión una vez detectada. Para lograr este objetivo, el principal recurso con el que se cuenta hoy en día es el screening o tamizaje, estrategia que ha demostrado su utilidad en reducir las muertes por CP. El tamizaje incluye el tacto rectal, antígeno prostático específico y otros biomarcadores.
Los pacientes con sospecha de CP deben ir confirmación diagnóstica, siendo el estándar actual la biopsia transrectal de próstata. Algunos métodos clínicos y de laboratorio para caracterizar y etapificar la enfermedad una vez diagnosticada son el tacto rectal (realizado por un urólogo) y estudio de imágenes como la ecografía, TAC, RNM y el cintigrama óseo.
Una vez realizada la etapificación clínica puede iniciarse el plan terapéutico. Éste debe acordarse entre el médico y su paciente, y en algunas oportunidades por un equipo multidisciplinario. Alternativas curativas hoy en día van desde la cirugía o radioterapia, hasta otros métodos en desarrollo actualmente con resultados promisorios. En pacientes no candidatos a tratamiento curativo, existen también buenas opciones paliativas como la hormonoterapia, quimioterapia y radioterapia, entre otros.
El variado espectro de alternativas terapéuticas y el buen pronóstico en caso de detección precoz del CP, hace vital desarrollar políticas de difusión sobre los alcances de esta enfermedad, y la importancia de su búsqueda en la población masculina de nuestro país.
Early detection and prevention of neoplastic diseases constitute a first order priority in the world today. In Chile, prostate cancer (PC) is the third most frecuent neoplastic pathology, with an incidence of 145.3 per 100.000 men, and the second cause of death by cancer. New and better detection methods will probably make this incidence rise even further in the future.
Many potentially modifiable factors related to the appearence and growth of malignant tumors in the prostate have been identified; however, there’s still no evidence of strategies that would succesfully reduce its incidence. This added to the asymptomatic course of early disease makes imperative the need to modify and ideally stop the progression once detected. To achieve this goal the primary resource available is screening, a strategy that has been proven to reduce mortality by PC. This includes digital rectal exam (DRE), prostate specific antigen and other biomarkers.
Positive screening should undergo diagnostic confirmation, the current gold standard being the transrectal biopsy of the prostate. Some clinical and lab resources available to define and stage this disease once a diagnosis is made are the DRE and imaging studies such as ultrasound, CT scan, MRI and a radionucleotide bone scan.
A therapeutical plan can be initiated once a clinical staging is achieved. The decision must be reached between the patient and urologist, and in some cases with the help of a multidisciplinary team. Surgery and radiotherapy constitute curative alternatives, with other methods still in development with promising results. Paliation options are also available, like hormonal deprivation, chemotherapy and radiotherapy amongst others.
The broad spectrum of therapeutic alternatives and the good prognosis in early stages of PC, makes the development of awareness policies and widespread screening in our country a necessity.
Las enfermedades neoplásicas son hoy en día una de las principales causas de mortalidad, morbilidad y pérdida de años de vida potencial en todo el mundo, y esta realidad se acentúa en países con un mayor grado de desarrollo. Por esto medidas tendientes a la prevención y detección temprana de estas patologías con el fin de llevar a un máximo posible las posibilidades de ofrecer una alternativa terapéutica eficaz, se constituyen en una prioridad epidemiológica de primer orden (1, 2).
Dentro de las enfermedades neoplásicas más frecuentes se encuentra el cáncer de próstata (CP), siendo el tercero en frecuencia entre los hombres españoles, y el primero en Estados Unidos y Chile con una tasa de incidencia de 145.3/100.000 habitantes masculinos el 2009. En nuestro país el CP es además la segunda causa de muerte por cáncer entre hombres tras el cáncer gástrico con 2023 defunciones secundarias a esta etiología el 2008.
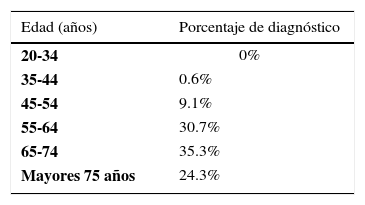
Otra característica importante del CP es que si bien es una patología más frecuente en pacientes añosos, con una mediana de edad en el momento del diagnóstico de 67.3 años, en Estados Unidos, el 0.6% de los diagnósticos se realizan en pacientes entre 35 y 44 años, y el 30.7% en pacientes entre 55 y 64 años (Tabla 1). La incidencia del CP es muy probable que continúe en alza en la medida que mejoran los métodos diagnósticos y su disponibilidad (3, 4, 5).
PrevenciónAnte esta realidad lo ideal sería encontrar mecanismos para reducir significativamente las cifras expuestas, y en este sentido se han intentado desarrollar diversas estrategias dirigidas a modificar diferentes factores que teóricamente favorecen el desarrollo de neoplasias en la glándula prostática como por ejemplo:
- •
Factores de riesgo inherentes al paciente y al medio ambiente en el que se desenvuelven: tales como consumo de alcohol, sedentarismo, sobrepeso y obesidad, dieta rica en grasas y pobre en verduras, frutas y cereales, síndrome metabólico y consumo de tabaco. Si bien está indiscutiblemente demostrado atenuar o eliminar factores como los descritos impactará positivamente en la morbilidad y mortalidad del grupo estudiado, y reducirá significativamente la incidencia de algunas neoplasias como el cáncer gástrico, de colon o de vía aérea, no hay evidencia que el impacto sobre el CP sea significativo (6).
- •
Factores de riesgo relacionados con la biología molecular del CP:
- -
Fitoterapia: desde los 70 se investigó ávidamente la relación entre el consumo de licopenos, pigmento liposoluble presente especialmente en tomates, y le reducción de la incidencia del CP, y si bien los primeros estudios resultaron prometedores, la evidencia actual ha presentado resultados decepcionantes (7).
- -
Dihidrotestosterona: existen medicamentos capaces de reducir la concentración intraprostática del andrógeno metabólicamente más activo a través de la inhibición de la enzima 5 α reductasa, recurso usado por años en el manejo de la hiperplasia prostática benigna. Basado en la andrógeno dependencia del desarrollo del cáncer prostático, se ha intentado probar que el uso de esta familia de fármacos podría reducir la incidencia de CP en pacientes de alto riesgo, sin que hasta hoy existan resultados concluyentes, lo que sumado al alto costo de estos medicamentos hacen que su uso en este sentido no esté hoy dentro de la práctica urológica (8).
- -
Testosterona: Está comprobado que el desarrollo de tumores prostáticos depende de la presencia de testosterona, y por décadas se planteó que a mayor concentración plasmática de esta hormona, existía un riesgo mayor de la ocurrencia de CP, desalentando el uso de tratamientos de sustitución hormonal en pacientes hipogonádicos con factores de riesgo para CP o con antecedente de CP tratado. Sin embargo lo anterior se basaba en evidencia estadísticamente muy débil y hoy se sabe que la concentración plasmática de testosterona no está relacionada ni con la incidencia ni con la agresividad del CP y que para poder prevenir la su aparición mediante la manipulación hormonal, se tendría que mantener niveles de castración desde antes de la pubertad (9, 10).
- -
Vitaminas y oligoelementos: existen estudios aún en curso que buscan demostrar una relación entre el consumo de Vitamina A, vitamina E y Selenio y una reducción en la incidencia de CP. Se esperan sus conclusiones no antes de 2 años (11).
- -
Antinflamatorios no esteroidales: existen estudios que sugieren una reducción de la incidencia del CP en pacientes que consumen aspirina diaria desde los 50 años (12).
- -
En resumen, si bien se han identificado muchos factores potencialmente modificables, relacionados con la aparición y desarrollo de tumores malignos en la próstata, no existe aún evidencia de estrategias que logren reducir su incidencia de manera significativa.
Diagnóstico precozAl encontrarnos entonces ante una patología muy frecuente, responsable de la mortalidad de muchos hombres en todo el mundo, y sin herramientas para modificar su ocurrencia, se impone la necesidad de modificar, e idealmente detener su progresión una vez detectada, y para lograr este objetivo, el principal recurso con el que se cuenta hoy en día es el diagnóstico precoz, es decir, detectar a pacientes con CP clínicamente significativo, con enfermedad órgano localizada, y susceptible de ser sometido a un esquema terapéutico con intenciones curativas. Lamentablemente este paciente es totalmente asintomático, por lo que debemos ir en su búsqueda a través de un screening o tamizaje, estrategia que ha demostrado su utilidad en reducir las muertes por CP (3, 13, 14).
Para orientar esta búsqueda hay que enfocar los esfuerzos en los grupos de riesgo (Tabla 2).
Grupos de riesgo y tamizaje para cáncer prostático
| Variable | Nivel |
|---|---|
| Edad | Más frecuente desde la quinta década de la vida; ausente en menores de 35 años. |
| Raza | Ancestros africanos: doble incidencia que blancos (asiáticos y nativos de Alaska: factor protector). |
| Genética | Antecedentes familiares por rama paterna. |
| Oncogenes | Antecedentes de otras patologías oncológicas. |
| Dieta | Dieta rica en grasas y pobre en verduras, frutas y cereales. |
| Otros | PREVENCIÓN, párrafo 2. |
Screening for prostate cancer: an updated Cochrane systematic review.
Una vez identificado el grupo de riesgo se cuenta hoy con muchos métodos para aproximación y confirmación diagnóstica. De ellos los que debemos utilizar en la etapa de tamizaje están extensamente disponibles en toda la red de salud chilena:
- •
Tacto rectal: Parte del examen físico segmentario que todo médico está capacitado para realizar, y que además de informar sobre una aproximación del volumen de la glándula prostática, es capaz de detectar anomalías tales como asimetría, nodulaciones, relación con estructuras vecinas y variaciones en la consistencia de la glándula, que pueden estar asociadas al CP. Si bien el rendimiento de este examen depende de la experiencia y práctica del examinador, es frecuente el hallazgo de lesiones evidentes que permiten iniciar un búsqueda dirigida, estimándose que con sólo esta exploración es factible el diagnóstico de un 65% de los CP en etapas precoces. Este examen cobra particular importancia en el diagnóstico de los tumores más agresivos, que debido a lo indiferenciado de su tejido, no es infrecuente que no exprese un aumento del Antígeno Prostático Específico (APE)
- •
Antígeno Prostático Específico: glicoproteína de síntesis exclusiva por parte de la próstata y utilizado como marcador tumoral en clínica por muchos años, y que presenta una gran sensibilidad (sólo no eleva sus niveles en tumores de alta indiferenciación) y de baja especificidad, ya que existen otras patologías (prostatitis) y condiciones (sonda uretrovesical) que también pueden elevar los niveles. El nivel de APE debe inquietar al médico si sobrepasa el nivel de 4.0ng/ml, si presenta una aumento significativo sobre el nivel histórico del paciente, o si la densidad del APE (nivel de APE/ volumen próstata en ecotomografía transpélvica) es mayor a 0.15 (ng/ml)/cc de próstata. Ante estas situaciones es recomendable la derivación del paciente al Urólogo para confirmar la sospecha diagnóstica.
- •
Fracción libre APE: Existen isoformas de esta molécula que el tejido tumoral es incapaz de sintetizar, y estas isoformas se desplazan por el torrente sanguíneo sin estar asociadas a carrier alguno. La relación porcentual de estas formas sobre el total del APE constituye la fracción libre APE, que al presentar niveles inferiores a 16% sugieren un origen neoplásico. Este examen presenta utilidad más en la instancia de la confirmación diagnóstica que en el tamizaje.
- •
Otros biomarcadores: se han desarrollado en los últimos años biomarcadores que buscan mejorar la especificidad y la sensibilidad del APE, así como entregar información respecto a la agresividad y el riego de progresión del CP. De ellos el más conocido (y disponible en Chile), y que gradualmente está encontrando su lugar en la práctica clínica es el PCA3, determinación que se realiza en orina, y que no actualmente no tiene papel en el tamizaje.
Las epidemiología nos muestra que se reportan casos entre población menor de 45 años, por lo que existe acuerdo que el tamizaje debe ser considerado ya desde los 40 años de edad (desde los 35 años en pacientes de alto riesgo), y que por las bajas probabilidades de morir de CP debe considerarse su suspensión tras los 75 años. Sin embargo no hay consenso sobre el intervalo, existiendo publicaciones de grupos serios que recomiendan desde el control anual hasta intervalos de 8 años.
BConfirmación diagnóstica (19, 20)El especialista dispone de una serie numerosa de recursos para confirmar o descartar el CP en los pacientes previamente seleccionados en el proceso de tamizaje:
- •
Tacto rectal: El examen rectal de la próstata realizado por urólogo, que presente hallazgos sugerentes de CP, cuenta con una especificidad y sensibilidad tan alta, que se le considera una indicación absoluta para realizar una biopsia de próstata.
- •
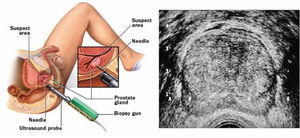
Biopsia de próstata: Hoy es la única herramienta que nos otorga información definitiva e incuestionable, y un resultado positivo en un análisis anatomopatológico de tejido es un requisito fundamental previo a la aplicación de cualquier esquema terapéutico. Existen diferentes técnicas para la obtención de tejido, siendo la más utilizada hoy en día la biopsia de próstata por sextantes transrectal ecoguiada (Figura 1), que permite anestesiar toda la glándula de forma óptima y obtener muestras de forma estandarizada y reproducible y con un bajo índice de complicaciones, lo que permite lograr un nivel bajo de falsos negativos. Sin embargo sigue siendo un examen invasivo y no exento de complicaciones e incluso de mortalidad, por lo que el resto de los exámenes descritos tienen su utilidad en seleccionar los pacientes con la mayor precisión posible, con el fin de evitar indicación de biopsias innecesarias.
- •
Imágenes
- -
Ecografía transrectal: Tiene papel como recurso para dirigir la biopsia transrectal. Y aunque se ha descrito que el hallazgo de zonas hipoecogénicas tiene sugiere la presencia de tejido tumoral, esto no se ha comprobado.
- -
Ecotomografía pélvica: Entrega información sobre volumen prostático, información necesaria para el cálculo de la densidad del APE, pero no entrega información imagenológica que nos aproxime de forma directa al diagnóstico de CP.
- -
Tomografía axial computada: Presta utilidad en la etapificación del CP, en especial identificando enfermedad regional.
- -
Resonancia magnética (RM) de próstata: examen que permite localizar zonas sospechosas de neoplasia en la próstata, con sensibilidad y especificidad alta, aunque para lograr un rendimiento adecuado, se necesita de un resonador de última generación, de un operador especialmente capacitado, y de un radiólogo altamente capacitado. Existen algunos reportes de prostatectomía radical indicada sólo con RM sugerente con resultados prometedores, aunque hoy este examen presta ayuda dirigiendo la realización de una biopsia transrectal hacia zonas sospechosas. La RM también ha demostrado utilidad en la detección de metástasis óseas por CP.
- -
Tomografía por emisión de positrones (PET), y PET CT: no presentan utilidad.
- -
- •
Medicina nuclear: El cintigrama óseo es utilizado rutinariamente en la etapificación del CP.
- •
Marcadores: El APE y su fracción libre, así como nuevos marcadores son de ayuda en la selección de pacientes candidatos a biopsia de próstata. Ya se hizo referencia sobre ellos en el punto 3A.
Una vez realizado el diagnóstico, el plan terapéutico será decidido entre el urólogo, el paciente y, en algunas oportunidades, el radioterapeuta y el oncólogo médico. Las variables a tener en cuenta serán la edad del paciente, las condiciones generales este, la etapificación y la agresividad de la enfermedad. Es decir es una decisión individual.
Las alternativas terapéuticas disponibles actualmente son las siguientes:
Alternativas con intención curativa- •
Cirugía: La prostatectomía radical es una cirugía que ofrece un muy buen control oncológico en enfermedad organolocalizada, y que cada vez presenta menos morbilidad y mortalidad, en especial en concepto de continencia urinaria y potencia sexual. Esta técnica se puede realizar abierta retropúbica, laparoscópica y laparoscópica robot asistida, siendo estas dos últimas aproximaciones, técnicas mínimamente invasiva, que presentan algunas ventajas en cuanto a dolor postoperatorio y hospitalización postquirúrgica, aunque no han demostrado ventajas oncológicas ni en la incidencia de complicaciones y morbilidad quirúrgica respecto a la cirugía abierta.
- •
Radioterapia (RT): constituye una muy buena alternativa curativa. Se encuentra disponible en nuestro país la RT externa, idealmente conformal y de intensidad modulada con el fin de reducir la toxicidad y efectos adversos (rectitis y cistitis actínica) que se puede indicar como alternativa curativa primaria o como tratamiento de rescate; también se dispone de la braquiterapia, mediante el implante de semillas radioactivas (yodo 125) en la glándula prostática, procedimiento de muy buen rendimiento en pacientes bien seleccionados, y con muy bajos índices de morbilidad.
- •
Ultrasonido de alta intensidad focalizado (Hi-fu): método de baja morbilidad, con resultados prometedores en paciente de bajo riesgo, utilizado en Francia, aunque aún no es aprobado por la FDA en Estados Unidos. Se encuentra disponible en Chile.
- •
Criocirugía: Ablación del tejido prostático mediante congelación a -40°C. Utilizado en algunos grupos como alternativa curativa primaria y de rescate. Se le considera aún experimental. No disponible en Chile.
- •
Terapias focales: tratamientos experimentales en fases tempranas de investigación
- •
Hormonoterapia: El bloqueo hormonal, ya sea quirúrgico (orquiectomía bilateral), central (inhibiendo el eje hipotálamo-hipófisis-gónada a través de análogos LhRh) o periférico (antiandrógenos o estrógenos) produce una detención en la progresión del tejido tumoral y promueve su apoptosis. Esta estrategia terapéutica cumple un rol como adyuvancia tras una cirugía o radioterapia y como tratamiento paliativo en pacientes no candidatos a un tratamiento curativo y enfermedad metastásica.
- •
Quimioterapia: el uso de citotóxicos (docetaxel, mitoxantrona) está reservado para enfermedad avanzada refractaria al tratamiento hormonal.
- •
Ketoconazol: Antifúngico que en dosis altas presenta respuesta en CP hormonoresistentes.
- •
Zalendronato: agente ósteoprotector antiosteoclástico. Se utiliza en CP metastático para prevenir fracturas patológicas y corregir la eventual aparición de hipercalcemia.
- •
Otros: existen otros agentes como la estramustina, la ciclofosfamida y el carboplatino, de uso limitado en clínica y dirigidos a CP avanzado como esquema paliativo de tercera línea.
El CP es una enfermedad muy frecuente, segunda causa de mortalidad por cáncer en hombres chilenos, y oligosintomática en sus etapas iniciales. Dado los pobres resultados en esquemas preventivos, es importante buscar y encontrar esta enfermedad, que esta “al alcance de la mano del médico”, en etapas precoces, con el fin de lograr reducir, mediante la utilización de los numerosos recursos curativos disponibles, una reducción en la alta mortalidad que esta patología presenta en la actualidad.
Es vital entonces, para lograr este objetivo, desarrollar políticas públicas y privadas de difusión con el fin de crear una concientización de parte de médicos y pacientes sobre los alcances de esta enfermedad, y la importancia de su búsqueda en la población masculina de nuestro país.
Los autores declaran no tener conflictos de interés, en relación a este artículo.