La cefalea por uso excesivo de medicamentos (MOH, por sus siglas en inglés) es una entidad compleja y aún en desarrollo, con criterios diagnósticos establecidos en la III edición de la clasificación internacional de las cefaleas (ICHD-3). Tiene una prevalencia del 2,2% en la población general y produce una severa carga de enfermedad en quienes la padecen. Los pacientes son heterogéneos por varios aspectos, no se ha determinado si genéticamente el paciente desencadena una cefalea crónica y por esa razón consume en exceso los medicamentos o los medicamentos son los causantes únicos de la cronificación de la cefalea primaria de base del paciente. Existe la MOH complicada y no complicada. El tratamiento debe ser multidisciplinario y tiene varias aristas. La desintoxicación abrupta, asociado al inicio precoz de terapia preventiva es lo que ha demostrado mayor efectividad. Las nuevas terapias para el tratamiento preventivo de la migraña han generado nuevos paradigmas en el manejo de la MOH, existiendo actualmente una serie de alternativas terapéuticas. Existen tres regímenes de desintoxicación: régimen ambulatorio, internación en centro de salud y hospitalización diurna. El pronóstico a mediano y largo plazo es positivo, pero se requiere un programa de seguimiento de estos pacientes en el tiempo por su alta tasa de recaídas, en especial durante el primer año.
Medication overuse headache (MOH) is a complex and still-developing entity, with diagnostic criteria established in the 3rd edition of the International Classification of Headache Disorders (ICHD-3). It has a prevalence of 2.2% in the general population and produces a severe burden of disease in those who suffer from it. Patients are heterogeneous in several respects; it has not been determined whether the patient's genetic makeup triggers a chronic headache, or if the medications themselves are the sole cause of the chronicity of the patient's primary baseline headache. There are complicated and uncomplicated MOH. Treatment must be multidisciplinary. Abrupt detoxification, associated with the early initiation of preventive therapy, has been shown to be most effective. New therapies for the preventive treatment of migraine have generated new paradigms in the management of MOH, and there are currently several therapeutic alternatives. There are three detoxification regimens: outpatient regimen, hospitalization in a health center, and day hospitalization. The medium and long-term prognosis is positive, but a follow-up program is required for these patients over time due to their high relapse rate, especially during the first year.
La cefalea por uso excesivo de fármacos, (MOH, medication overuse headache) es una cefalea secundaria debido a la ingesta mensual elevada de fármacos analgésicos indicados para aliviar una cefalea aguda en una persona que sufre de cefalea primaria de base. Esta entidad ha sido descrita ya desde 1951 por Horton y Peters, quienes publicaron casos de pacientes migrañosos que empeoraban con el uso de tartrato de ergotamina1. Aproximadamente 30 años después, en 1982, Kudrow et al.2, plantearon que el tratamiento profiláctico con amitriptilina era inefectivo en pacientes con MOH; al comparar pacientes con amitriptilina sin MOH tenía 72% de efectividad vs. 30% de efectividad en pacientes con amitriptilina y MOH, planteando “the paradoxical effects to frequent analgesic use”. Por su parte, Mathew3 observó que, si se les realizaba un tratamiento adecuado a pacientes con MOH, regresaban a su patrón previo de dolor.
Se acuñaron diferentes términos para denominar esta entidad, como cefalea de rebote, cefalea por uso indebido de medicamentos, cefalea por adaptación a medicamentos, cefalea inducida por drogas, entre otros4, hasta que en el año 1988 se publicó la primera clasificación internacional de desórdenes de cefalea (ICHD-1, International Classification of Headache Disorders-1) en la cual se acuñó el término “medication overuse headache”. Se planteó que correspondía a una cefalea secundaria, definiendo una serie de criterios diagnósticos que con el paso de los años y acumulación de experiencia en el manejo de estos pacientes se fueron modificando, quedando los cambios plasmados en las subsecuentes clasificaciones hasta llegar a los actuales criterios diagnósticos de la clasificación ICHD-35 y la actual definición de uso excesivo de medicamentos.
Criterios diagnósticos ICHD-3 para MOH
- 1.
Cefalea que se presenta =15 días al mes en un paciente con un trastorno de cefalea preexistente.
- 2.
Uso excesivo regular durante>3 meses de uno o más medicamentos analgésicos para el tratamiento agudo y/o sintomático de las cefaleas
- 3.
No se explica mejor por otro diagnóstico de la ICHD-3
¿Cómo se define el uso excesivo de analgésicos?
- a.
≥10 días al mes para triptanes, ergotamínicos, opioides, analgésicos combinados
- b.
≥15 días al mes para analgésicos simples (como paracetamol o antiinflamatorios no esteroidales (AINEs))
- c.
≥10 días al mes para combinaciones de múltiples clases de fármacos.
Cabe mencionar que para el manejo agudo de la migraña los gepantes (rimagepante y ubrogepante) y ditanes (lasmiditan) representan una nueva generación de tratamientos para la migraña, ofreciendo alternativas a los triptanes tradicionales. Los gepantes no han demostrado generar MOH al utilizar frecuentemente6,7 y si bien no hay estudios clínicos que vinculen lasmiditan8 con MOH si estudios preclínicos en modelos de MOH en ratas han determinado que induce sensibilización central y alodinia cutánea determinando eventual riesgo de MOH, lo cual debe ser confirmado por estudios clínicos y por otra parte, la definición de uso excesivo de analgésicos no tiene relación con la dosis específica del fármaco en cuestión, ni con la frecuencia diaria en que se administró, sino que tiene relación con cuantos días al mes fue ingerido.
Al diagnosticar MOH estamos atribuyendo la causalidad del aumento de la frecuencia de la cefalea del paciente al uso excesivo de analgésicos, pero cuando hay un uso excesivo de analgésicos sin causalidad directa en el incremento de la frecuencia de la cefalea se denomina uso excesivo de medicación, en inglés medication overuse (MO)9. Al respecto, es muy interesante destacar un estudio observacional en 120 pacientes con migraña crónica que encontró que aquellos con uso excesivo de fármacos tenían puntajes significativamente más altos en cuestionarios como HIT-6 y MIDAS (que miden discapacidad y pérdida de funcionalidad) en comparación con pacientes con migraña crónica y bajo uso de medicamentos10.
Para lograr un mejor entendimiento de las diferentes definiciones debemos hacer algunas distinciones.
El término “cefalea crónica diaria” (CCD), es un síndrome que se define como cefaleas =15 días al mes por más de 3 meses seguidos independiente de la causa y de las características clínicas de la cefalea. CCD se subclasifica en corta duración, si la cefalea diariamente tiene una duración menor a 4 horas y de larga duración, si tiene una duración diaria de más de 4 horas. Frente a una CCD de corta duración y que se asocia a síntomas neuroautonómicos craneofaciales se debe sospechar una cefalea en racimos crónica entre otras entidades trigémino-autonómicas. Frente a una CCD de larga duración y descartando causa secundaria, la etiología más frecuente es la migraña crónica (MC) definida en la clasificación ICHD-35 (tabla 1).
Definición de migraña crónica
| Cefalea durante ≥15 días al mes, por al menos 3 meses seguidos, con historia previa de ≥5 crisis de migraña y de esos 15 días al menos ≥8 días al mes la cefalea cumple los criterios de migraña tales como: | |
| Al menos ≥2 de los siguientes: | a) unilateral;b) pulsátil; c) dolor moderado o severo;d) agravado por actividad física |
| Y ≥1 de los siguientes: | a) náusea o vómitos;b) fotofobia y fonofobia |
| Y/o que las crisis se alivien con terapia antimigrañosa específica como triptanes o ergotamínicos. | |
| No atribuible a otro trastorno como causa. | |
Otras causas primarias de CCD de larga duración es la cefalea tipo tensional crónica (CTTC), la cefalea diaria persistente de novo y la hemicránea continua. Esta última se diferencia de las anteriores por presentar síntomas neuroautonómicos hemicraneales. Para sospechar una cefalea diaria persistente de novo, un elemento clínico sugerente es que la cefalea haya iniciado en un día e incluso en un horario recordado en detalle por el paciente y después de su debut, a los 3 días se torna crónica, hecho muy raro de ver en pacientes con MC o CTTC.
La MOH es una de las causas secundarias más importante de CCD y es muy frecuente la presencia de MOH en pacientes con MC. Alrededor del 90% de los pacientes que sufren de MOH tienen de base MC o CTTC11.
Aquellos pacientes que no sufren de una cefalea primaria de base y consumen una elevada cantidad mensual de analgésicos por otras etiologías de dolor crónico no desarrollan MOH12.
EPIDEMIOLOGÍACon respecto a la incidencia de MOH, el estudio HUNT (The Nord-Trøndelag Health Survey), estudio noruego de cohorte longitudinal basado en la población, con seguimiento de 11 años de 26197 respondedores (63% de 41766 elegibles), encontró una incidencia de 0,72 casos de MOH por 1000 personas/año13.
Con respecto a la prevalencia, el Global Burden of Disease Study (GBD) con reportes de 16 países, sitúa la prevalencia de MOH entre el 1 a 2% de la población general14, lo cual extrapolado a 8 billones de habitantes equivale a entre 50-100 millones de personas que sufren de esta condición en el mundo. Existe gran variabilidad en lo reportado en distintos países, por ejemplo, un estudio pakistaní del 2017 realizado en 4 223 pacientes reportó una prevalencia del 0,7% en hombres y 0,8% en mujeres15 y en Mongolia en el año 2019 en un seguimiento de 2 043 pacientes se pesquisó prevalencia del 5,7% (con tendencia a ser más alta en mujeres)16. Estas diferencias tienen una serie de explicaciones que van desde el modelo de sistema de salud de cada país, los seguros sociales, el tipo de seguimiento de los pacientes, la metodología, heterogeneidad de los pacientes y temas culturales en la relación con la salud, medicamentos, entre otros. Asimismo, se reportan distintas cifras de proporción mujeres: hombres afectados por MOH, entre 1,3:115 (Pakistán) a 5:1 en India y 3:1 en China en un estudio del año 2012 en 5 041 personas17. El GBD hasta el 2015 evaluaba MOH como una entidad independiente (ahora está considerada dentro de las complicaciones de migraña y cefalea tipo tensional)18 informando que alrededor de 59 millones de personas en el mundo la padecían y situándola en el sexto lugar de las enfermedades neurológicas que producían más años vividos con discapacidad en el mundo14.
En datos regionales, en la sección latinoamericana del proyecto COMOESTAS, con datos de Chile y Argentina, la edad media de MOH fue de 38,7 años (rango 18-72 años), 80,4% fueron mujeres, 75% nivel educacional técnico o profesional, la migraña fue la cefalea de base más frecuente (77,8%) en pacientes con MOH y en menor proporción la cefalea tipo tensional crónica (15,9%), y el fármaco con mayor uso excesivo fue la ergotamina sola (70%) o en combinación con antiinflamatorios no esteroidales (AINES)19.
En relación a los factores de riesgo asociados a MOH, en distintos estudios transversales se ha observado el sexo femenino, bajo nivel educacional, adultez (en torno a los 40 años) y bajos ingresos familiares20 y en un estudio longitudinal se confirma el sexo femenino y el bajo nivel educacional como factores de riesgo para la incidencia de MOH (OR 1,9), la cefalea de base con mayor riesgo es la migraña (migraña vs no migraña OR 8,1), otras asociaciones con doble riesgo es: historia de latigazo (whiplash), enfermedades musculoesqueléticas crónicas, ansiedad y depresión13. En el American Migraine Study II se confirman los mismos factores riesgos, pero se agregan mujer blanca y ser dueña de casa21.
Dentro de las comorbilidades con MOH, las más frecuentes son ansiedad y depresión, los cuales constituyen fuertes factores de riesgo de cronificación de una cefalea primaria y de MO. Se asocian a mayor discapacidad de la MOH y son predictores de mala evolución, pobre respuesta terapéutica y mayor riesgo de ideación suicida22. Otras comorbilidades existentes son enfermedades musculoesqueléticas crónicas, insomnio, hipotiroidismo, trastornos gastrointestinales (úlcera, síndrome de intestino irritable), síndrome metabólico, hipertensión arterial esencial, y tabaquismo23.
Con respecto a la carga de enfermedad que produce la MOH, la GBD en el año 2013 la situó en el lugar decimoctavo entre las enfermedades que más años vividos con discapacidad existen en el mundo24, generando severa discapacidad y pérdida de funcionalidad en las personas que lo padecen y en el estudio Eurolight en la Unión Europea se estimó un gasto anual el 2011 en MOH de 37 billones de euros, siendo el 92% de ese monto por pérdida de productividad25.
CLÍNICACuando un paciente consulta por cefalea presente todos o casi todos los días durante más de tres meses consecutivos, cumpliendo los criterios ICHD-3 y descartando causas secundarias como hipertensión intracraneana idiopática, cefalea por hipotensión de líquido céfalo-raquídeo, hidrocefalia o cefalea post traumatismo encefalocraneano, entre otras (se recomienda el esquema de trabajo que acuña la sigla SNOOP1026 para banderas rojas en cefalea), lo más probable es que se encuentre frente a una persona que padece de MOH. En centros de cefalea especializados en EE.UU., alrededor del 50-80% de los pacientes con migraña crónica tienen concomitantemente una MOH27. En esta situación, además de realizar la anamnesis habitual, se debe preguntar dirigidamente cuál o cuáles medicamentos analgésicos consume al mes, detallando principios activos, dosis, tiempo de uso, frecuencia diaria y sobretodo la cantidad de días al mes que los consume para confirmar el diagnóstico de MOH.
Con respecto a las características específicas de la cefalea, los criterios diagnósticos ICHD-3 no aportan mayores luces, sólo hacen mención del número de días de cefalea y su relación directa con el uso excesivo de analgésicos. En general, las características clínicas son muy variables, pero lo observado en la práctica clínica es que las características de la cefalea de MOH depende en gran medida de la cefalea primaria que padece el paciente y del fármaco usado en exceso28. En este sentido, un estudio prospectivo de pacientes con migraña con o sin aura o cefalea tipo tensional o ambas, cuando se usan excesivamente los AINES, la cefalea de MOH tiende a ser sorda, opresiva, holocraneana, a menudo sin muchos síntomas “migrañosos” asociados. En cambio, en pacientes de similares características que usan excesivamente de triptanes, la cefalea de MOH tiende a tener claros elementos migrañosos como náuseas, vómitos, foto o sonofobia, propenden a ser matinales en su presentación y responder relativamente rápido al uso de otros triptanes, pero característicamente la cefalea retorna a las pocas horas o al día siguiente28. La situación geográfica y económica de los países también impactan en los fármacos sobre usados, por ejemplo, en EE.UU. existe un alto uso de fármacos opioides y barbitúricos, en el este de Europa de fármacos ergotamínicos, en el oeste de Europa de fármacos triptanes y en países en vías de desarrollo, como Latinoamérica, de ergotamínicos y AINES29,30.
En la evaluación clínica de estos pacientes es fundamental contar con un calendario de cefalea ya sea manual o electrónico. Está demostrado la infra o sobrevaloración que el paciente puede tener con respecto a sus cefaleas en intensidad y frecuencia mensual llevando a errores diagnósticos y por ende indicación de tratamientos no adecuados por parte del médico tratante, bajo 8 días al mes de dolor, el reporte tiende a ser infravalorado y sobre esa cifra, ser supravalorado por los pacientes31. Llevar el registro también evita el efecto “telescoping” (fenómeno descrito en donde los pacientes evalúan un período de tiempo en base a la última crisis sufrida antes del control médico sin sopesar realmente como evolucionaron durante todo el período).
Recomendaciones clínicas para sospechar MOH:
- -
Cefalea que se torna refractaria con frecuencia diaria o casi diaria.
- -
Antecedentes de cefalea primaria preexistente.
- -
La cefalea varía en sus características generales habituales.
- -
Disminución del umbral al dolor.
- -
Astenia, síntomas gastrointestinales, irritabilidad, ansiedad, dificultad concentración.
- -
Taquicardia, frío en extremidades, parestesias, hipertensión arterial en caso de uso de ergotamínicos o combinaciones con cafeína.
- -
Ritmicidad droga-dependiente, rebote REM.
- -
Tolerancia farmacológica a la terapia preventiva y abortiva de crisis de cefalea.
- -
Síntomas de abstinencia al suspender el fármaco usado en exceso.
- -
Mejoría con la discontinuación del fármaco usado en exceso.
- -
Disminución de efecto de preventivos mientras mantiene el uso excesivo de analgésicos.
En adición al aumento de frecuencia de la cefalea y de cambios en sus características habituales, muchos pacientes comienzan a presentar una ritmicidad droga-dependiente, con crisis de dolor o rebote durante el sueño REM. Una característica clínica relevante de la cefalea en estos pacientes es que tienden a despertarse en la noche después del primer o segundo ciclo de sueño REM con una cefalea de gran intensidad y/o despertarse a primera hora de la mañana con una intensa cefalea, posiblemente, por la abstinencia de varias horas del fármaco debido al tiempo transcurrido en el sueño. Otra de las características clínicas es que la terapia preventiva habitual comienza a no tener la misma efectividad que previo a la MOH.
Con respecto al fármaco usado en exceso, el estudio AMPP (American Migraine Prevalence and Prevention) informó que la cronificación (es decir, la transformación de migraña episódica [EM, por sus siglas en inglés] a migraña crónica [CM, por sus siglas en inglés]) ocurre a una tasa de ∼ 2,5% por año32. De los medicamentos agudos evaluados, el uso de opioides y analgésicos que contienen barbitúricos se asoció con un riesgo significativamente mayor de cronificación a CM (opioides: OR=1,44 [IC95% 1,10-2,08]; barbitúricos: OR=1,73 [IC95% 1,10-2,73])32,33. Los resultados fueron similares para mujeres y hombres, excepto que el riesgo de cronificación con el uso de opioides fue mayor en hombres (OR=2,76, IC95% 1,20-6,38) versus mujeres (OR=1,28, IC95% 0,81-1,97)32.
En aquellos pacientes que sufren de una cefalea primaria y tiene un MO sin desarrollar aún una MOH, estudios han demostrado que tenían puntajes significativamente más altos en cuestionarios como HIT-6 y MIDAS (mayor discapacidad y menos funcionalidad por la cefalea), en comparación con los pacientes con bajo uso frecuente de medicamentos34.
Existen dos grupos de pacientes con MOH: MOH complicada y MOH no complicada (tabla 2). Los pacientes con MOH complicada tienden a tener más riesgos de recaídas y mala respuesta al tratamiento vs pacientes con MOH no complicada.
MOH complicada y MOH no complicada
| MOH complicada | MOH no complicada |
|---|---|
| Uso excesivo de opioides y barbitúricos | Uso excesivo de AINEs, analgésicos simples, triptanes y/o ergotamina |
| Uso concomitante de fármacos sedantes o tranquilizantes | No uso de fármacos sedantes o tranquilizantes |
| Comorbilidad psiquiátrica relevante | Sin comorbilidad psiquiátrica relevante |
| Antecedentes de fallas previas de desintoxicación | Sin antecedentes previos de falla de desintoxicación |
| Pobre red de apoyo | Buena red de apoyo |
| Uso excesivo de múltiples fármacos y por tiempos prolongados | Uso excesivo de un fármaco y uso previo no prolongado |
Abreviaciones: AINEs:antinflamatorios no esteroidales; MOH: medication overuse headache.
Por último, hay evidencia científica que demuestra que muchos pacientes con MOH tienen antecedentes de traumas o eventos estresantes en su vida35.
TRATAMIENTOConceptos generales: el primer punto relevante en el tratamiento y que siempre vale la pena recalcar, es desarrollar la sospecha clínica sobre este cuadro para realizar acertadamente el diagnóstico de MOH y así poder indicar el tratamiento correcto. Sin un correcto diagnóstico nunca se le podrá ofrecer a estos pacientes una solución a su problema de salud; hay estudios que evidencian que solo entre el 5 a 15% de pacientes con MOH reciben un tratamiento adecuado36,37. La educación a los pacientes sobre el riesgo de MOH es fundamental para su prevención, lo que contrasta con hallazgos de un reciente estudio que evidenció que cerca del 40% de los pacientes con cefalea crónica no conocían el concepto de MOH38. Se debe ser enfáticos en la educación continua y concientización al cuerpo médico en su conjunto, a nuestros pacientes y a la población en general sobre los riesgos de automedicarse o de una toma excesiva de analgésicos para el manejo de sus cefaleas.
El manejo de MOH tiene una serie de aristas: educación al paciente, discontinuación o desintoxicación del fármaco utilizado en exceso, manejo cognitivo-conductual, tratamiento farmacológico preventivo para MOH y la cefalea primaria de base y planificación de estrategias de tratamiento abortivo para el manejo agudo de crisis de cefalea. A lo anterior se agrega el seguimiento y monitoreo a largo plazo de los pacientes mediante, entre otras cosas, un calendario de cefalea, manejo por equipo multidisciplinario, manejo de comorbilidades y complicaciones de las terapias, idealmente en un centro con expertise en el manejo de cefalea y que ofrezca la posibilidad de hospitalizar al paciente en caso de necesidad.
Dentro de la educación al paciente es necesario plantearles lo siguiente38:
- •
La comprensión de que el uso frecuente de medicamentos agudos para tratar el dolor de cabeza puede contribuir a más dolores de cabeza
- •
La eliminación de la medicación aguda es probable que mejore los dolores de cabeza a largo plazo
- •
Es poco probable que la mejoría del dolor de cabeza sea completa
- •
El uso de medicamentos preventivos para la migraña en paralelo puede reducir la MOH
- •
El tratamiento de la condición de salud mental coexistente (por ejemplo, depresión y ansiedad) puede ofrecer beneficios adicionales
- •
La reexposición a la medicación para el dolor agudo después de una retirada exitosa puede causar la recaída de una MOH
- •
Después de la retirada exitosa de la medicación para el dolor agudo, es necesario tratar el dolor de cabeza subyacente
- •
El tratamiento exitoso de la MOH puede llevar muchas semanas o meses.
Para el tratamiento farmacológico preventivo y abortivo de crisis de dolor en MOH no existen claras directrices de ensayos clínicos referente a la elección de los pacientes, end points primarios y secundarios, extensión del seguimiento, entre otros; siendo los ensayos son muy heterogéneos entre sí, lo que hace difícil sistematizar la información disponible39.
Lo primero es centrarse en la educación al paciente, su diagnóstico de MOH, los riesgos de complicaciones médicas y eventualmente quirúrgicas por el sobreuso de analgésicos. Es necesario dedicar tiempo ya que para muchos pacientes sonará paradójico que lo mejor para su estado de salud actual es el retiro del analgésico que le ayuda a su dolor, aunque sea momentáneamente. Por otro lado, se debe explicar que es esperable que, de manera inicial y transitoria, secundario a la desintoxicación del fármaco analgésico sus cefaleas podrían empeorar. Este punto es muy importante, sobre todo por un estudio que evidencia que el solo consejo médico de los puntos antes mencionados, en ambiente de atención primaria, puede ser tan efectivo como indicar tratamiento farmacológico a pacientes con MOH no complicada40.
Posterior al diagnóstico y a la educación del paciente, se debe realizar la desintoxicación del fármaco usado en exceso, la cual se puede realizar de forma brusca e inmediata o de forma escalonada. Aún existe debate sobre este punto. Un ensayo multicéntrico demostró que iniciar el tratamiento preventivo sin una desintoxicación brusca inicial fue más eficaz para reducir la carga total de cefaleas. Sin embargo, la disminución en el número de días con cefalea respecto al basal fue significativa en el grupo que discontinuó el fármaco utilizado en exceso41.
En este sentido se dispone de varios posibles esquemas terapéuticos:
- -
Discontinuación precoz del fármaco usado en exceso sin terapia preventiva.
- -
Discontinuación precoz del fármaco usado en exceso+terapia preventiva.
- -
Terapia preventiva con restricciones en el uso del fármaco sobre usado.
- -
Terapia preventiva sin discontinuación ni restricciones en el uso del fármaco usado en exceso.
Una revisión sistemática comparó las primeras dos estrategias y evidenció que la discontinuación precoz+terapia preventiva fue superior que la sola discontinuación del fármaco usado en exceso42. Esto fue apoyado por subsecuentes ensayos, uno de ellos muy interesante del Centro de Cefalea Danés Glostrup. Los pacientes se aleatorizaron 1:1:1 a desintoxicación+tratamiento preventivo, tratamiento preventivo sin desintoxicación o desintoxicación con opcional tratamiento preventivo a los dos meses de la desintoxicación. El endpoint primario fue el cambio del número de días de cefalea al mes después de 6 meses, junto a una serie de endpoints secundarios como cambios en los días mensuales de migraña, uso de medicación analgésica, intensidad del dolor, número de respondedores, pacientes con remisión a cefalea episódica y MOH superada. No hubo mayores diferencias en el endpoint primario entre los 3 esquemas, pero en el endpoint secundario de pacientes con reversión a cefalea episódica a los 6 meses, el grupo de desintoxicación+preventivo fue de un 74,2% vs. 60% sólo preventivo vs. 41,7% en sólo desintoxicación, riesgo relativo (RR) de reversión 1,8, lo que corresponde a un 80% mayor probabilidad de revertir la cefalea en el grupo de desintoxicación+prevención vs. sólo desintoxicación. Con respecto a MOH superada a los 6 meses: RR de 1,3 para desintoxicación+preventivo (30% por sobre desintoxicación)43, por lo que, si bien los 3 esquemas fueron efectivos, la desintoxicación precoz del medicamento usado en exceso+la terapia preventiva desde el inicio es el esquema recomendado para el manejo de MOH43. En su estudio, Engelstoft et al. concluyen que la interrupción abrupta (desintoxicación) del fármaco analgésico usado en exceso es más efectiva y factible que sólo restringir su uso44. Esto corre fundamentalmente para fármacos triptanes, ergotamina, analgésicos simples, AINES y combinación de analgésicos, siendo un proceso relativamente seguro y bien tolerado para los pacientes. En el caso de uso excesivo de fármacos barbitúricos, opioides y benzodiazepinas solos o en combinación, éstos deben reducirse gradualmente para evitar síntomas de abstinencia u otras complicaciones.
Por lo anterior, existen tres regímenes de conducir al menos inicialmente la desintoxicación: régimen ambulatorio, internación en centro de salud y la hospitalización diurna. Existe una serie de estudios prospectivos que comparan estas modalidades, siendo en general la desintoxicación con internación del paciente la con mayor tasa de efectividad (71%)45, pero en definitiva no existen guías clínicas que orienten sobre el régimen de desintoxicación a seguir, ni su duración ni que fármacos utilizar.
TRATAMIENTO FARMACOLÓGICOCon respecto al manejo farmacológico existen categorías que se podrían individualizar de la siguiente manera: tratamiento preventivo, tratamiento puente y tratamiento abortivo de crisis de dolor.
TRATAMIENTO FARMACOLÓGICO PUENTE Y PREVENTIVOEl tratamiento preventivo es un tratamiento orientado a mediano y largo plazo para el manejo de la cefalea primaria de base y apunta fundamentalmente a bajar la frecuencia mensual de crisis, junto con bajar la intensidad y discapacidad producida por las mismas. Es altamente recomendado indicar este tratamiento ya que se ha demostrado que es superior a no tratar41. Este tratamiento puede ser ofrecido antes, durante e incluso después de la desintoxicación, siendo lo aconsejable indicarlo precoz al inicio de la desintoxicación46.
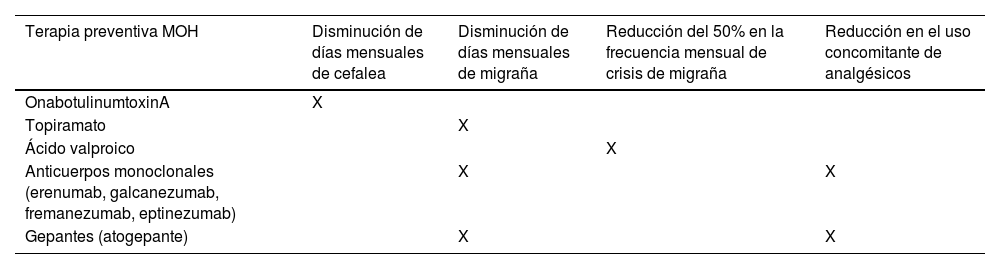
Los medicamentos que han demostrado mayores beneficios en el tratamiento de MOH son topiramato47, ácido valproico48, onabotulinumtoxinA49, anticuerpos monoclonales contra el receptor del péptido relacionado con gen de la calcitonina (CGRP) (erenumab) o directamente contra el ligando CGRP, (fremanezumab, galcanezumab y eptinezumab)50–53 y gepantes (moléculas pequeñas y sintéticas que antagonizan el receptor del CGRP) como el atogepante que fue efectivo en reducir el uso de días de medicación de analgésicos en pacientes con MC y MOH vs placebo54, todos estos estudios con duración de terapia y seguimiento variable entre 3 a 6 meses (tabla 3).
Medición de efectividad de terapia preventiva en MOH
| Terapia preventiva MOH | Disminución de días mensuales de cefalea | Disminución de días mensuales de migraña | Reducción del 50% en la frecuencia mensual de crisis de migraña | Reducción en el uso concomitante de analgésicos |
|---|---|---|---|---|
| OnabotulinumtoxinA | X | |||
| Topiramato | X | |||
| Ácido valproico | X | |||
| Anticuerpos monoclonales (erenumab, galcanezumab, fremanezumab, eptinezumab) | X | X | ||
| Gepantes (atogepante) | X | X |
Lo interesante y que eventualmente podría cambiar el paradigma, es que los ensayos con anticuerpos monoclonales y onabotulinumtoxinA demuestran ser efectivos en los endpoints primarios sin necesariamente realizar un proceso dirigido de desintoxicación del fármaco usado en exceso. Esto plantea una serie de incógnitas que deberán ser resueltas en estudios posteriores sobre la real fisiopatología de esta entidad. Otra alternativa útil es la combinación de terapias preventivas, aunque sin mucha evidencia científica que soporte esta indicación.
No hay estudios aleatorizados ni placebo controlado para otras alternativas de tratamientos preventivos no específicos (bloqueadores de canales de calcio, beta-bloqueadores, antidepresivos tricíclicos, entre otros.).
En casos seleccionados de pacientes es posible intentar una racional combinación de preventivos, por ejemplo: antidepresivo tricíclico+neuromodulador+un anticuerpo mononuclear o que abarquen distintas comorbilidades psiquiátricas u otras, como betabloqueo+topiramato o ácido valproico+onabotulinumtoxinA55.
Por último, si bien no existe mucha evidencia que lo respalde, otra alternativa podría ser la infiltración pericraneal con lidocaína 2% más asociación, o no, a corticoide local en nervios pericraneales.
El tratamiento puente consiste en terapias que permiten controlar las cefaleas de rebote o por desintoxicación que pueden ocurrir sobre todo al inicio de la desintoxicación. En general, las primeras dos semanas son las más críticas y presentan un real desafío al proceso de desintoxicación. Los fármacos que se han utilizado para este efecto son los corticoides orales sistémicos a pesar de que al menos 2 estudios aleatorizados y controlados no encontraron mayor beneficio del uso de corticoide como terapia puente56,57. Nuevamente no hay consenso en cuanto a dosis, fármaco corticoidal en específico, vías de administración ni duración, pero lo más usual es el uso de prednisona 1mg/kg de peso entre 6 días58 a 4 semanas con posterior tapering. Otra alternativa es el uso de celecoxib 400mg al día por 5 días, luego disminuyendo 100mg cada 5 días59. Un fármaco interesante es la tiaprida que, pese a contar con evidencia que apoya su uso en cefaleas crónicas60 y no en MOH, si es utilizada como terapia puente durante el período de desintoxicación. Es un neuroléptico atípico, antagonista selectivo de receptores de dopamina D2/D3, sin afinidad D1, esto tiene implicancias relevantes, ya que D2/D3 se expresan en el núcleo paraventricular hipotalámico participando activamente en el control de la ingesta y saciedad y posiblemente en otros estados de adicción61, uniéndose principalmente a receptores extraestriatales, con pocos efectos sedantes, buen efecto ansiolítico, ideal para pacientes añosos, pero si con algunos efectos adversos como disquinesias precoces, disquinesia tardía, hipotensión ortostática, impotencia, frigidez, amenorrea, galactorrea, ginecomastia, hiperprolactinemia y somnolencia. Existe un estudio aleatorizado y doble ciego que evaluó 39 pacientes (18-65 años) con diagnóstico de MC que fueron asignados a tiaprida 100mg cada 12 horas (21 pacientes) vs topiramato 25mg cada 12 horas por 12 semanas (18 pacientes), el endpoint primario fue el cambio en el número mensual de días de migraña a las 12 semanas. El grupo con tiaprida tuvo una reducción media de 7,2±7,5 días con migrañas por mes en comparación con 7,6±5,8 para el grupo con topiramato (p=0,86), no encontrando diferencias en el resto de endpoints secundarios (cambio en el número mensual de días de cefalea, el porcentaje de sujetos con disminución>50% y>75% de sus días de migraña mensual, y el cambio del impacto de la cefalea medido por el Headache Impact Test-6)62, por lo que si bien no es una evidencia directa en MOH si podría ser útil en MC, que es una de las principales cefaleas primarias de base en contexto de MOH lo que podría explicar su eficacia.
TRATAMIENTO AGUDOAdemás de desintoxicar precozmente al paciente, iniciar terapia puente y eventualmente iniciar terapia preventiva a largo plazo, es necesario planificar un esquema terapéutico abortivo en caso de crisis aguda. Es conocida la presencia de intensas cefaleas de “rebote” al suspender el fármaco usado en exceso siendo necesario indicar un tratamiento analgésico. Se recomienda un esquema estratificado, que consiste en estratificar al paciente con respecto a la frecuencia mensual de crisis, intensidad e impacto en su calidad de vida en: baja necesidad, mediana necesidad o alta necesidad de tratamiento. En caso de baja necesidad de tratamiento, es posible indicar analgésicos simples como acetaminofeno, ácido acetilsalicílico, metamizol o AINES (diclofenaco, ketorolaco, indometacina, naproxeno, etc.) y si no hay respuesta a las 2 horas, indicar fármacos analgésicos específicos como triptanes, ditanes o gepantes, evitando indicar nuevamente el fármaco usado en exceso. En caso de alta necesidad de tratamiento (alta frecuencia mensual de crisis, de gran intensidad y alto impacto en calidad de vida) se recomienda el uso inmediato de fármacos específicos como triptanes, ditanes o gepantes, algunos de ellos por su farmacocinética permiten eventualmente repetir dosis a las 2 horas no sobrepasando el máximo diario recomendado (eletriptán 80mg/día, rizaptriptán 30mg/día) y definir previamente en consenso con el paciente cual será la terapia de rescate si el dolor no cede. También está la posibilidad de utilizar una mezcla de analgésicos que tengan un efecto potenciador entre ellos, disminuyendo los efectos adversos. En aquellos casos de mediana necesidad de tratamiento queda a discreción del tratante en acuerdo con el paciente si se inicia con AINES o terapia específica63. Para evitar caer en nuevo sobreuso de fármacos, la recomendación más importante es educar a los pacientes que la toma de fármacos abortivos no debe exceder la dosis máxima mensual para cada tipo de familia de fármacos mencionada anteriormente (menos de 10 días al mes para triptanes, ergotamínicos, opioides, analgésicos combinados; menos de 15 días al mes para analgésicos simples (como paracetamol o AINES) y menos de 10 días al mes para combinaciones de múltiples clases de fármacos)5. Cabe recordar que el uso de gepantes para el manejo agudo de migraña (rimagepante, zavegepante y ubrogepante)64–66 no desarrollan MOH en los pacientes que los consumen en dosis mensuales elevadas. Con respecto a ditanes (lasmiditan) se deben confirmar estudios clínicos para definir si su uso tiene o no riesgo de MOH.
MANEJO EN INTERNACIÓN VS AMBULATORIOExisten estudios que demuestran una mayor tasa de éxito en desintoxicación en internación vs desintoxicación ambulatoria, entre 48%67 y 71%68.
Un esquema muy interesante de manejo que abarca todas las preferencias de los pacientes y complejidades es el planteado por Sait Ashina y su equipo de trabajo65:
Pacientes con MO y MOH no complicada: después del consejo y educación la pregunta es: ¿Está dispuesto el paciente a desintoxicarse del medicamento usado en exceso?
- -
Si la respuesta es “Sí”: se realiza la desintoxicación aguda de forma ambulatoria bajo la supervisión médica o de enfermería+el uso de terapia preventiva como: anticuerpo monoclonal anti-CGRP o su receptor u onabotulinumtoxinA (sólo en caso de MC de base) o topiramato u otro fármaco, con seguimiento clínico regular junto al uso de un calendario de cefalea.
- -
Si la respuesta es “No”: se comienza con la terapia preventiva con anticuerpo monoclonal anti-CGRP o su receptor u onabotulinumtoxinA (sólo en caso de MC de base) o topiramato u otro. Si la respuesta clínica es inefectiva o incompleta, se procede a la discontinuación del fármaco usado en exceso y seguimiento clínico regular junto al uso de un calendario de cefalea.
Pacientes con MOH complicada: terapia multimodal del dolor (utilizar múltiples fármacos con distintos target en la vía del dolor) e interrupción de la medicación bajo la supervisión de un médico, enfermero o psicólogo de forma no abrupta, siendo manejado el paciente en internación u hospital de día+manejo por equipo de adicciones y seguimiento clínico regular junto al uso de un calendario de cefalea69.
Hay distintas experiencias en distintas partes del mundo con esquema de internación, por ejemplo, 7 días en COMOESTAS70 hasta 2 meses en las guías danesas71. En nuestro centro, la internación se realiza por 5 a 7 días y se indica lo siguiente: hidratación IV con solución glucosalina 80-100ml/hora, omeprazol 20-40mg al día, enoxaparina 40mg SC, clorpromazina 25mg IM cada 8 horas (cuenta con evidencia de utilidad en el manejo de cefaleas crónicas)72, tiaprida 100mg cada 12 horas, analgesia IV SOS+inicio de tratamiento preventivo con onabotulinumtoxinA o topiramato 25mg cada 12 horas, con aumento hasta 50mg cada 12 horas según respuesta clínica y tolerabilidad o anticuerpos monoclonales. Se suma manejo por kinesiología, terapia ocupacional, psicología, psiquiatría y odontología con expertise en trastornos temporo-mandibulares y dolor orofacial.
TRATAMIENTO NO FARMACOLÓGICOEnsayos controlados y aleatorizados aportan evidencia con respecto al biofeedback y mindfulness como terapias asociadas a la terapia farmacológica en el manejo de pacientes con MOH73,74. Un estudio que comparó acupuntura vs. topiramato demostró que era efectiva en pacientes con MC y en el subgrupo de MOH75.
Con respecto a la neuroestimulación del nervio occipital mayor, existe evidencia conflictiva con algunos estudios que plantean una potencial utilidad en MOH y otras series de casos que pesquisaron que pacientes con MO respondieron menos que aquellos con MC y no MO76,77. En el resto de las terapias neuromoduladoras no existe evidencia en pacientes con MOH.
El seguimiento por un equipo multidisciplinario compuesto por neurólogo (idealmente experto en cefaleas), neurólogo general, psiquiatría, psicología, nutriología, odontología con expertise en trastorno temporo-mandibular y dolor orofacial por lo relevante de la comorbilidad con trastornos de la articulación temporo-mandibular. La terapia ocupacional es clave tanto en pacientes manejados de forma ambulatoria o internados. La utilización de un calendario de cefalea es importante para evaluar tolerancia al tratamiento preventivo indicado, adherencia al tratamiento, suspensión real del medicamento usado excesivamente, cambios en los días mensuales de cefaleas, días mensuales de migraña, días de uso de medicación analgésica (idealmente no más de 2 días a la semana), intensidad del dolor y respuesta a la medicación analgésica indicada en caso de crisis aguda de dolor.
El pronóstico es positivo en el corto plazo, con un éxito en torno al 60-100% a los 2 meses de iniciado el tratamiento en cuanto a la reducción del uso de medicación analgésica y entre el 60 a 80% al año de evolución42. No obstante, entre un 10 a 40% de los pacientes puede recaer dentro de los primeros 5 años, siendo el período más crítico el primer año de desintoxicación, lo que subraya la importancia de desarrollar un programa de seguimiento periódico multidisciplinario en estos pacientes78.
Los factores predictivos de mala respuesta y recaída dentro del primer año son los siguientes: cefalea de base migraña+cefalea tipo tensional asociada, sobreuso de opioides, prolongado tiempo de sobreuso de analgésicos, gran número de analgésicos ingeridos, no mejoría a los dos meses del inicio de la desintoxicación, consumo de alcohol, tabaco y trastornos del sueño79,80.
En suma, la MOH es una de las causas más frecuente de cefalea secundaria, es un cuadro complejo, multifactorial, con fisiopatología aún no clara del todo, que genera una alta carga de enfermedad en quienes la padecen con gran impacto en calidad de vida y funcionalidad. Produce una cronificación de la cefalea de base, principalmente migraña, siendo un cuadro eventualmente reversible, para lo cual es fundamental realizar un correcto diagnóstico acompañado de un abordaje multidisciplinario. Se recomienda la desintoxicación abrupta del o los fármacos analgésicos usado en exceso, junto a tratamiento puente y tratamiento preventivo a largo plazo de forma ambulatoria. En aquellos casos de MOH complicada se recomienda el manejo inicial en internación u hospitalización de día junto con una extensa educación al paciente y familia y seguimiento médico estructurado asociado al uso de un calendario de cefalea y terapia no farmacológica si el equipo tratante y el paciente así lo deciden.
Conflictos de interésEl autor declara no tener conflictos de interés.
FinanciamientoEl autor declara no haber recibido financiamiento para la redacción de este manuscrito.