Las enfermedades pulmonares difusas representan un grupo de enfermedades que comparten un mismo criterio radiológico, existiendo más de 200 entidades que se presentan como tal. La clínica es fundamental para aproximar el diagnóstico etiológico que muchas veces resulta complejo. Tos y disnea progresiva son los síntomas clínicos característicos de estas enfermedades y se acompañan de la radiografía de tórax con opacidades difusas como método radiológico inicial. El estudio en general es multi- disciplinario incluyendo patrones radiológicos de la tomografía axial de tórax, estudio de función pulmonar, lavado bronquioal- veolar y biopsia pulmonar en algunos casos.
The diffuse lung diseases are a group of conditions that share common radiological criteria. There are over 200 causes. The clinic skill is essential to approximate the etiologic diagnosis, often complicated. Cough and progressive dyspnea are the clinical features of these diseases and are accompanied by chest radiography with diffuse opacities as the initial radiological method. The study is generally multidisciplinary and including radiological patterns in computer tomography of the chest, lung function study, bronchoalveolar lavage and lung biopsy in some cases.
El concepto de enfermedad pulmonar difusa (EPD) representa una orientación radiológica a un importante número de enfermedades respiratorias que comparten el mismo patrón radiológico en cuanto a extensión de la enfermedad.
Este hecho hace que a través de una simple radiografía de tórax podamos categorizar a los pacientes como portadores de una EPD al presentar opacidades pulmonares. Este hecho hace que a través de una simple radiografía de tórax podamos categorizar a los pacientes como portadores de una EPD al presentar opacidades en uno o más lóbulos pulmonares, en forma uni o bilateral y no necesariamente en forma simétrica1.
Existen más de 200 entidades que pueden presentarse como una EPD, pudiendo comprometerse el intersticio pulmonar, los espacios alveolares, los bronquiolos o los vasos sanguíneos. Cada una de estas patologías tendrá una determinada epidemiología, características clínicas específicas, evolución y tratamiento. Por lo anterior, el tratar de precisar el diagnóstico es de vital importancia para instaurar el manejo oportuno1,2.
El objetivo de esta revisión es delinear en forma general, la aproximación y enfrentamiento de pacientes que se presenten con una EPD, tratando de dar estrategias que nos permitan ir acotando las posibilidades diagnósticas.
PRESENTACIÓN CLÍNICAEl diagnóstico de una EPD puede tener dificultades debido a algunos hechos:
- 1.
Muchas enfermedades se pueden presentar con tos, disnea progresiva y fibrosis pulmonar que es una de las características principales de este grupo de enfermedades.
- 2.
Se pueden presentar con síntomas leves y de lenta progresión en el tiempo.
- 3.
Pueden ser asintomáticas por mucho tiempo antes de presentarse clínicamente.
- 4.
Y pueden no tener una causa identificable, denominándose idiopáticas o criptogénicas3.
En general, la presentación más frecuente de una EPD estará dada por la presencia de tos, predominantemente no productiva y aparición de disnea que puede tener grados variables de progresión en el tiempo, dependiendo de la causa de la enfermedad. Estos síntomas pueden estar acompañados de manifestaciones extrapulmonares como por ejemplo artralgias, debilidad muscular o lesiones cutáneas, lo cual puede orientar a un diagnóstico reumatológico. Se desglosa de lo anterior que una buena anamnesis clínica es fundamental para establecer directrices diagnósticas. De esta forma podremos precisar el tiempo de evolución de la enfermedad, sus síntomas principales, exposiciones ambientales o laborales, tabaquismo, uso de fármacos u otras drogas y antecedentes familiares de EPD.
En varios estudios se ha demostrado que una profunda anamnesis logra acotar en forma considerable las posibilidades diagnósticas de pacientes con sospecha de EPD, pudiéndose llegar en el 60% de los casos a una probable sospecha etiológica. Significa definir grupos etarios y género afectado, relación con el hábito tabáquico y tiempo de aparición de síntomas. Así por ejemplo, pacientes masculinos mayores de 50 años, con tos y disnea progresiva, tabaquismo y sin otras exposiciones conocidas podrían estar cursando con una fibrosis pulmonar idiopática4.
La exploración diagnóstica es de vital importancia en la evaluación de pacientes con EPD.
En la simple inspección del enfermo podremos encontrar hipocratismo digital o dedos en palillos de tambor, acusando por ejemplo una EPD crónica como la fibrosis pulmonar. Un 30% de los pacientes con fibrosis pulmonar idiopática puede tener hipocratismo digital. Sin embargo, también se puede ver este hallazgo semiológico en el cáncer pulmonar o patología cardiovascular. La presencia de lesiones cutáneas como eritema multiforme o lesiones tipo vasculitis también pueden ser manifestaciones de una EPD en el contexto de mesenquimopatias o sarcoidosis4,5.
La arista reumatológica no se puede dejar de lado por lo que la exploración musculoesquelética y articular nunca debe faltar dada la potente asociación de mesenquimopatia y EPD.
Con mucha frecuencia, a nivel pulmonar en la auscultación encontraremos crepitaciones de predominio basal. En algunos casos, como la neumonitis por hipersensibilidad, además auscultaremos sibilancias4,5.
CLASIFICACIÓN DE LAS ENFERMEDADES PULMONARES DIFUSASExisten muchas propuestas de clasificación de la EPD. Se pueden clasificar de acuerdo a su tiempo de presentación en: Agudas, subagudas o crónicas. Sin embargo una forma de agruparlas y que resulta bastante útil en la práctica clínica, es aquella que tiene que ver con la etiología.
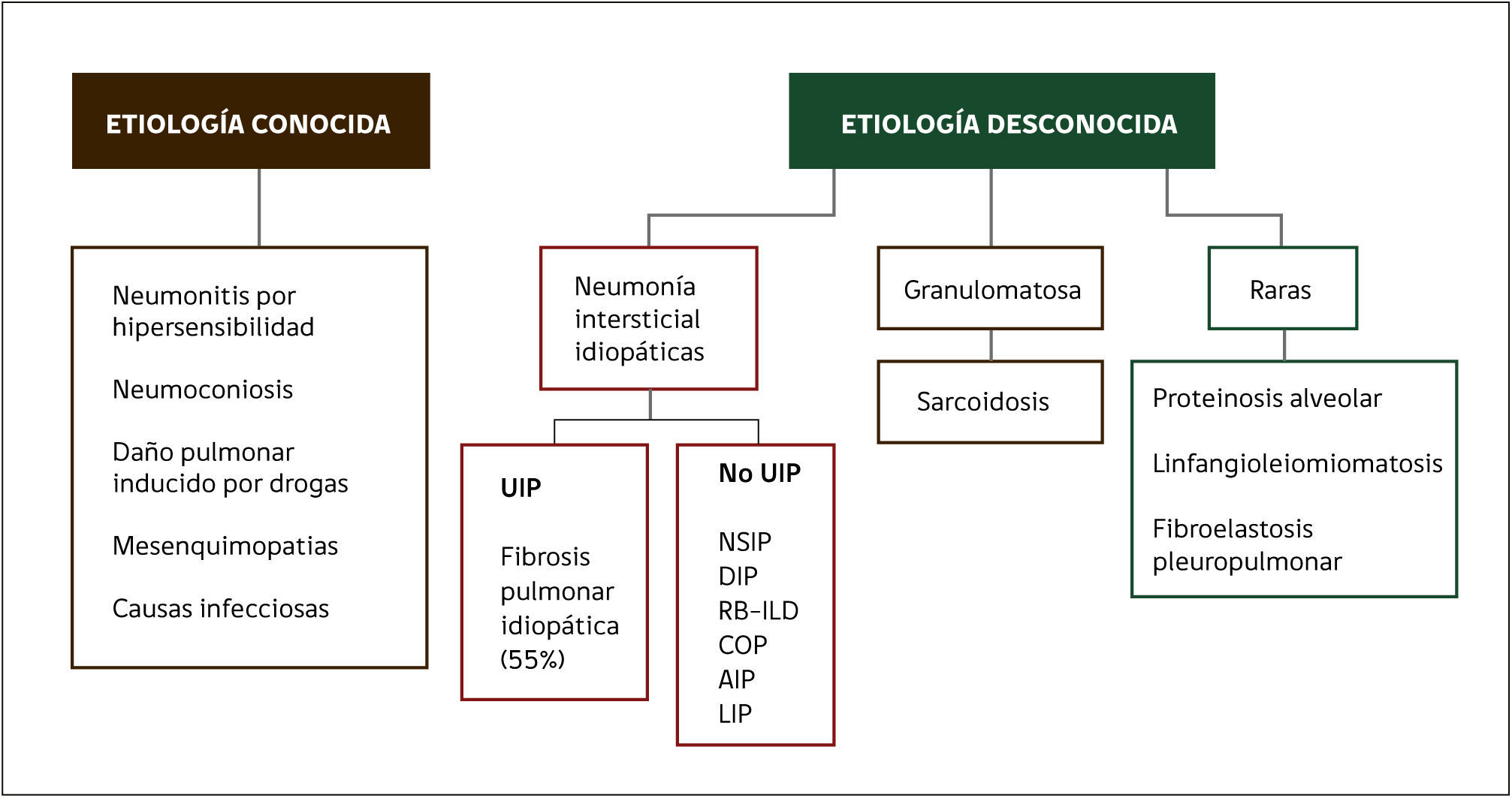
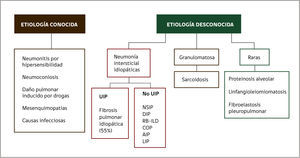
Podemos clasificar la EPD en aquellas de causa o etiología conocida y otras de causas desconocidas, incluyéndose en este último grupo todas las neumonías intersticiales idiopáticas que han sido agrupadas y estudiadas en varios consensos internaciones de la sociedad americana de tórax, sociedad europea respiratoria y la asociación latinoamericana de tórax. (Figura 1)4.
CLASIFICACIÓN DE LAS ENFERMEDADES PULMONARES DIFUSAS
UIP, Usual interstitial pneumonia, NSIP: Nonspecific interstitial pneumonia, DIP: Desquamative interstitial pneumonia, RB-ILD: Respiratory bronchiolitis and interstitial lung diseases, COP: Cryptogenic organizing pneumonia, AIP: Acute interstitial pneumonia, LIP: Limphocytic interstitial pneumonia. (Modificado de referencia 4).
Con respecto a las EPD que se clasifican de acuerdo a su tiempo de presentación clínica y evolución, se pueden considerar como enfermedades agudas, subagudas o crónicas. En este contexto la neumonía por Pneumocystis jiroveci se presentará como una EPD de presentación aguda mientras que la fibrosis pulmonar idiopática lo hará como una forma crónica. Esta forma de clasificación es bastante útil para acotar el espectro de diagnósticos etiológicos y por lo general se puede complementar paralelamente a la clasificación etiológica, antes arriba mencionada.
ESTUDIO DIAGNÓSTICOComo en todas las patologías, el apoyo del laboratorio es una herramienta de gran ayuda en el estudio de enfermedades pulmonares. El laboratorio debiera incluir, pruebas hematológicas como hemograma, velocidad de sedimentación, perfil bioquímico y pruebas reumatológicas como anticuerpos antinucleares, factor reumatoideo y otras específicas en caso de sospecha de mesenquimopatia. Ante la sospecha de una neumonitis por hipersensibilidad también es muy útil solicitar precipitinas específicas para aves como catas o paloma y cuando el antecedente lo amerite, pecipitinas para hongos, como Aspergilus.
Una vez establecida la sospecha de una EPD, el examen que no debe faltar para confirmar la enfermedad es la radiografía de tórax. La imagen radiológica dará la definición del compromiso difuso caracterizado por extensión de varios lóbulos, segmentos o pulmón completo ya sea en forma uni o bilateral. Al mismo tiempo podremos evaluar en forma indirecta tamaño de los pulmones, predominio espacial del compromiso, presencia de neumotórax o derrame pleural, así como también tamaño de la silueta cardiaca asociado a elementos radiológicos de congestión pulmonar. Sin embargo la interpretación más fina y precisa de una EPD debe ser complementada con la tomografía axial computada (TAC) de tórax con cortes de alta resolución.
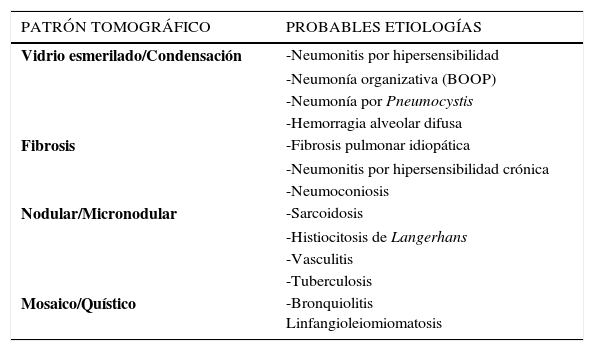
Tomografía axial computada de tórax de alta resoluciónTAC de tórax es el examen radiológico que definirá la presencia más detallada de alteraciones intersticiales, compromiso alveolar, vía aérea o alteraciones vasculares y también exploración del mediastino. Las imágenes tomográficas de pulmón pueden establecer patrones radiológicos que orientan a un determinado grupo de enfermedades que lo poseen. La técnica tomográfica está dada por imágenes de alta resolución (Tabla 1). La interpretación radiológica debiera incluir información previa para el radiólogo otorgada por el médico internista o especialista, con el fin de precisar mejor la alternativa diagnóstica6.
PATRONES RADIOLÓGICOS EN TAC DE TÓRAX
| PATRÓN TOMOGRÁFICO | PROBABLES ETIOLOGÍAS |
|---|---|
| Vidrio esmerilado/Condensación | -Neumonitis por hipersensibilidad |
| -Neumonía organizativa (BOOP) | |
| -Neumonía por Pneumocystis | |
| -Hemorragia alveolar difusa | |
| Fibrosis | -Fibrosis pulmonar idiopática |
| -Neumonitis por hipersensibilidad crónica | |
| -Neumoconiosis | |
| Nodular/Micronodular | -Sarcoidosis |
| -Histiocitosis de Langerhans | |
| -Vasculitis | |
| -Tuberculosis | |
| Mosaico/Quístico | -Bronquiolitis Linfangioleiomiomatosis |
(Modificado de referencia 7).
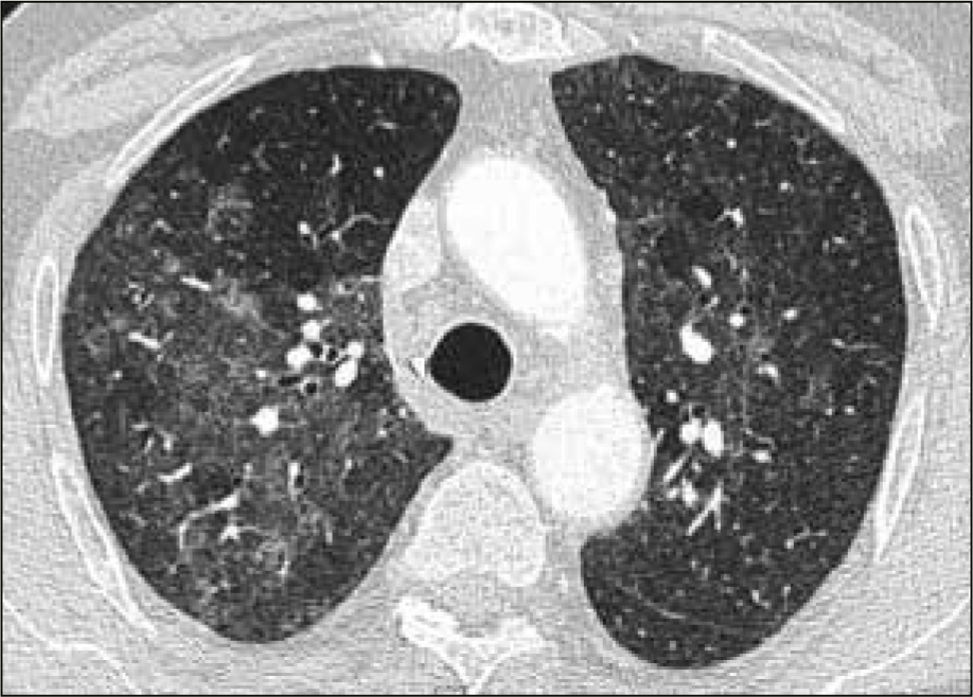
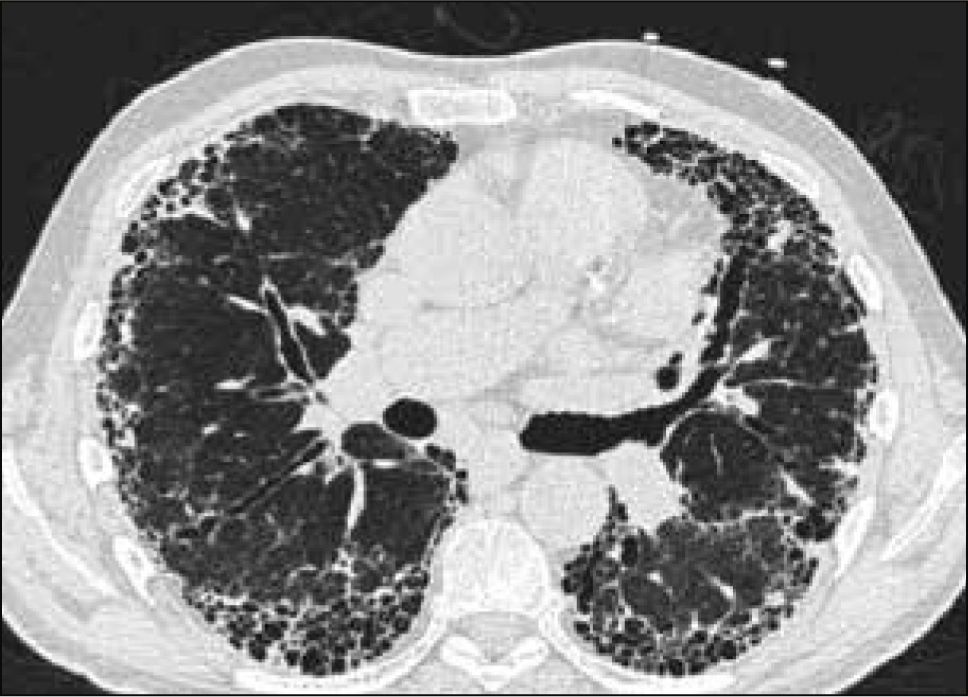
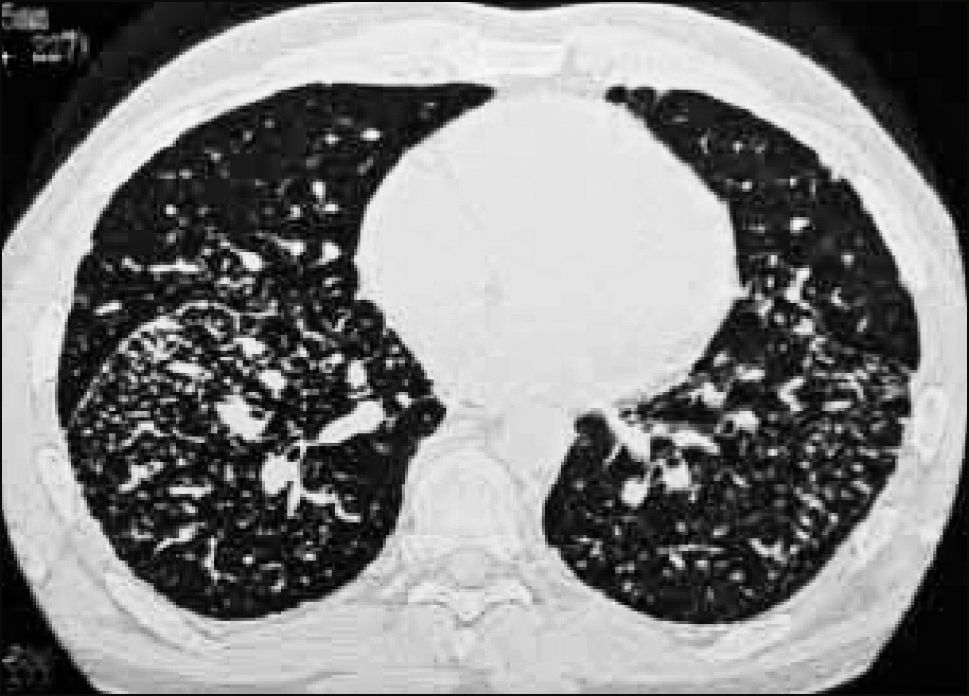
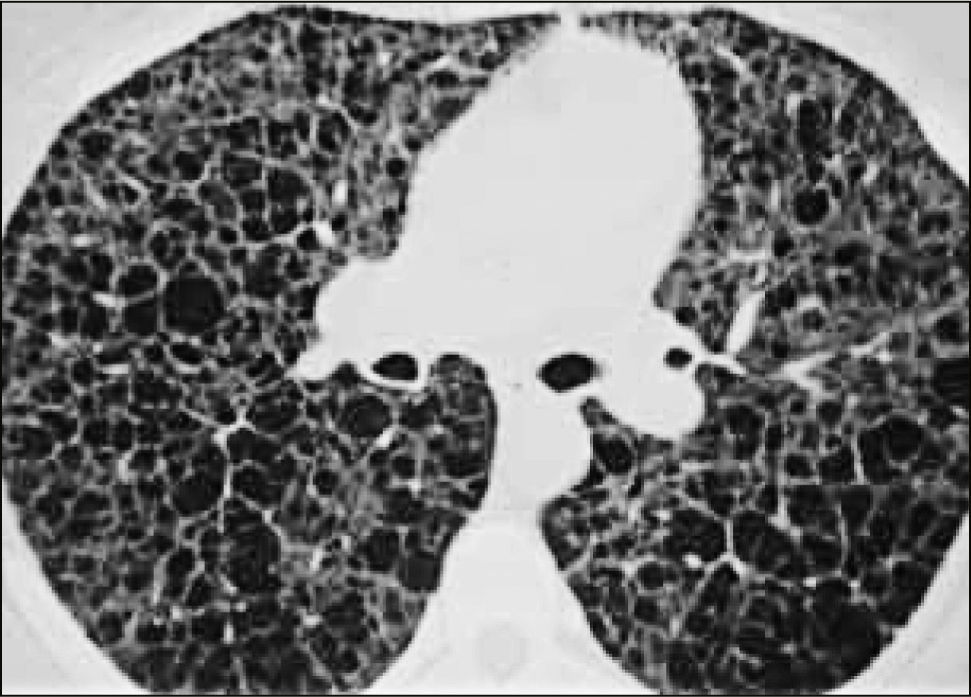
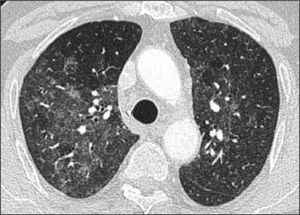
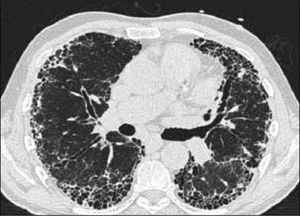
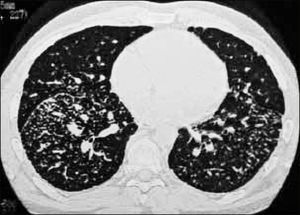
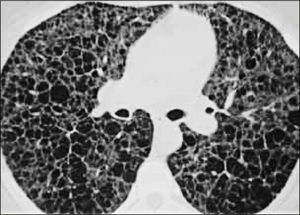
La neumonía intersticial usual (UIP) constituye un diagnóstico radiológico que deriva de los hallazgos de la anatomía patológica. Se trata de elementos de fibrosis caracterizados por opacidades reticulares de predominio basal, compromiso de ubicación subpleural, presencia de panal y bronquiectasias por tracción. La interpretación radiológica a cargo del radiólogo de tórax podrá acotar los diagnósticos de EPD según el patrón radiológico que predomine. En algunos casos, la presentación de un patrón fibrótico con elementos típicos de UIP podrá definir en el TAC de tórax diagnóstico definitivo de fibrosis pulmonar. (Figuras 2-5, imágenes tomadas previa autorización de pacientes).
ESTUDIO FUNCIONALLa presencia de una EPD, con frecuencia, presentará importante repercusión en la estructura del pulmón, que determinará alteraciones a nivel de su función. Por lo anterior, es que se debe realizar estudio funcional pulmonar para precisar el grado de compromiso y gravedad del cuadro respiratorio, así como también el seguimiento en el tiempo de las EPD. La espirometría basal y post broncodilatador como prueba básica, mostrará un patrón determinado según la etiología de la EPD. Es muy frecuente encontrar en las EPD asociadas a fibrosis, un patrón espirométrico restrictivo, pudiendo ser normal en estadios iniciales. En otros casos como la neumonitis por hipersensibilidad podremos encontrar un patrón espirométrico obstructivo inicial que según la evolución a cronicidad podría cambiar a restrictivo.
La otra prueba funcional de gran utilidad es la capacidad de difusión del monóxido de carbono (DLCO). Este examen mide en forma indirecta, cuan eficiente es la transferencia de O2 desde los alveolos a los capilares a través de la membrana alveolocapilar. La afección de la membrana en muchas EPD, hace que esta prueba muestre la disminución de la DLCO en forma puntual y también en el seguimiento.
Dado que la funcionalidad pulmonar involucra el ejercicio físico, una prueba que otorga excelente información es el test de caminata de seis minutos o test de marcha. Podremos investigar tolerancia al ejercicio expresado en escala de disnea, metros caminados durante la prueba y saturación de oxígeno inicial y durante la marcha. Este test de gran importancia en el estudio de las EPD también se debe solicitar como forma de evaluar la evolución de las enfermedades pulmonares6,7.
FIBROBRONCOSCOPÍA: LAVADO BRONQUIOALVEOLAR Y BIOPSIA TRANSBRONQUIALLa broncoscopia como método diagnóstico de la EPD es otra herramienta de utilidad en el estudio de la EPD. A través de ella podemos estudiar el parénquima pulmonar mediante el lavado bronquioalveolar o tomando muestras directas mediante la biopsia transbronquial.
El lavado bronquioalveolar consiste en el “baño” de una determinada zona de parénquima pulmonar afectada con solución salina al 0.9% generalmente en una cantidad de 100cc, rescatándose mediante una suave succión de la jeringa de instilación conectado al canal de trabajo del broncoscopio.
En múltiples estudios se concluyó que el rescate del 30% del volumen instilado es necesario para una adecuada interpretación de la muestra. Podremos estudiar el recuento celular, donde tendremos el valor de recuento celular total y el porcentaje diferencial de macrófagos, linfocitos, neutrófilos y eosinófilos. Se podrán hacer tinciones especiales según la sospecha diagnóstica como por ejemplo hemosiderófagos en el caso de hemorragia alveolar, tinción de Ziehl Neelsen para el estudio de tuberculosis, tinción de Grocott en neumonía por Pneumocystis jiroveci o tinción para estudio de células neoplásicas También el aspecto del lavado puede ayudar en el diagnóstico como lo vemos en la hemorragia alveolar y el líquido aspirado es progresivamente hemorrágico.
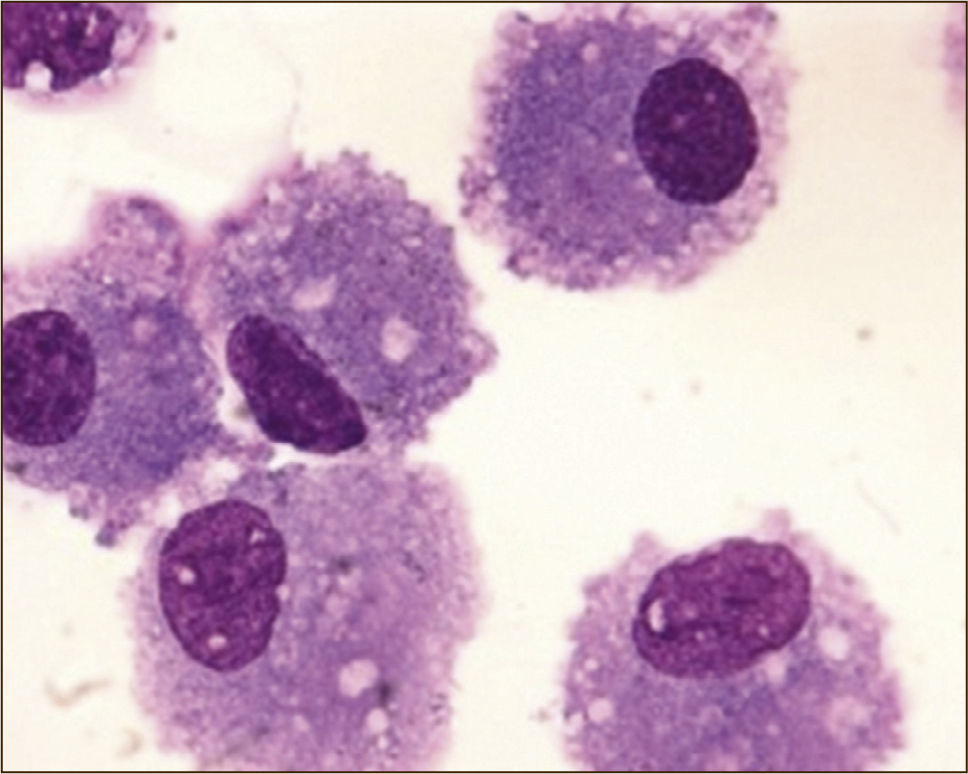
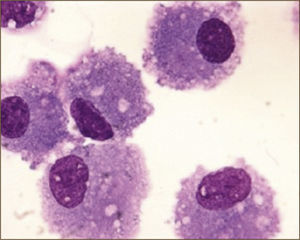
Respecto al recuento celular, a través de varios estudios se logró establecer un recuento absoluto y diferencial en personas sin patología pulmonar (Tabla 2). Sabiendo cuál es la fórmula de normalidad, a través del porcentaje de los grupos celulares, se puede orientar algún diagnóstico de EPD. Por ejemplo, la linfocitosis mayor al 30% es frecuente en la neumonitis por hipersensibilidad y la sarcoidosis. La presencia de eosinofília mayor al 25% hace el diagnóstico de neumonía eosinofílica. Y la neutrofilia mayor al 20% se puede ver en cuadros de infección pulmonar, exacerbaciones de fibrosis pulmonar o distres respiratorio (Figuras 6-8)8,9.
MACRÓFAGOS ALVEOLARES
(Tomado con autorización de www.wasog.org, BAL Atlas: © ild care foundation).
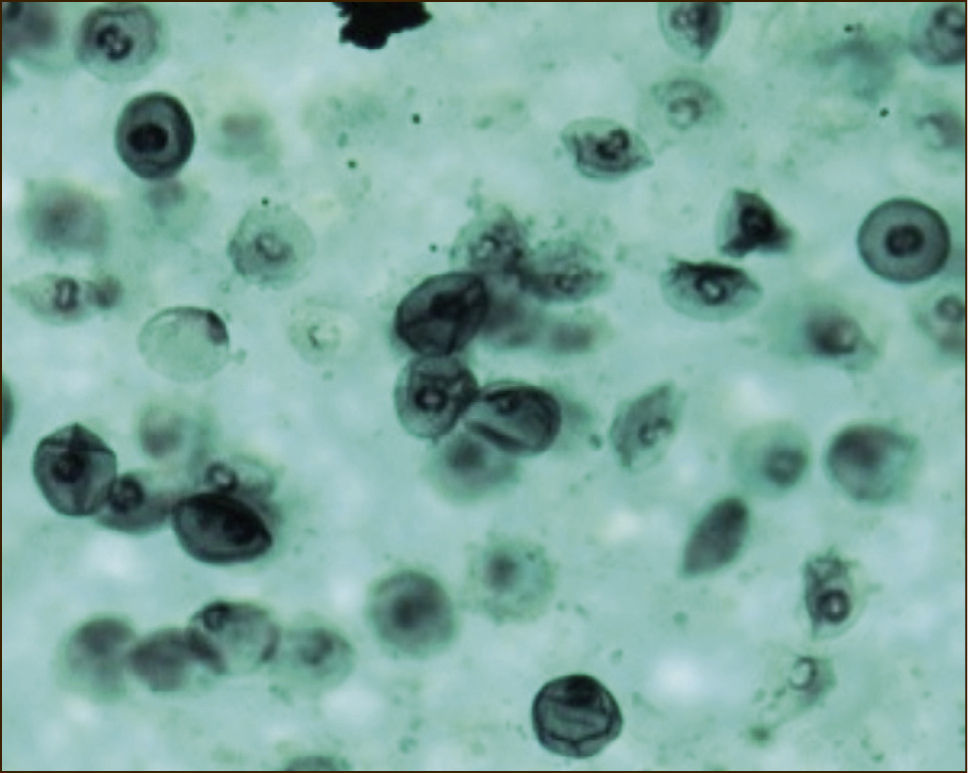
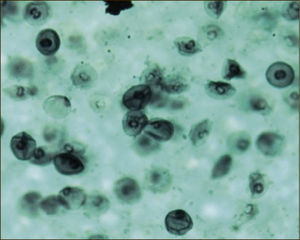
LAVADO BRONQUIOALVEOLAR: TINCIÓN DE GROCOTT PARA PNEUMOCYSTIS JIROVECI
(Tomada con autorización de www.wasog.org, BAL Atlas: © ild care foundation).
Otro método diagnóstico que se puede lograr a través de la broncoscopio es la biopsia transbronquial. Sin embargo la limitación del tamaño de tejido que se puede obtener mediante una pequeña pinza puede limitar el número de diagnósticos de EPD. Aquellas afecciones pulmonares como neumonía organizativa, sarcoidosis, neumonía eosinofílica, linfangitis carcinomatosa o infecciones pulmonares bacterianas o por hongos, pueden ser confirmadas por la biopsia transbronquial. En la actualidad también se pueden hacer diagnóstico de sarcoidosis mediante la punción de ganglios hiliomediastínicos guiada por ultrasonido endobronquial, técnica broncoscópica de última generación que visualiza vía ultrasonográfica, estructuras adyacentes a la vía aérea y permite punciones dirigida. Por otro lado, la biopsia quirúrgica por videotoracoscopía asistida es el método más invasivo para el estudio de la EPD. Sin embargo la experiencia de un patólogo experto es necesaria para la interpretación de la anatomía patológica, muchas veces de difícil diagnóstico, sobre todo en aquellas EPD avanzadas con componente fibrótico, pero que no cumplen criterios radiológicos de UIP10.
SÍNTESISLa aproximación diagnóstica de las EPD incluye un estudio sistemático donde la historia clínica completa es fundamental para la orientación etiológica y el plan de estudio a seguir, siendo fundamental la interacción multidisciplinaria que incluye imágenes pulmonares, estudio de funcionalidad, fibrobroncoscopía con lavado y/o biopsias transbronquiales, pudiéndose llegar a la necesidad de biopsia quirúrgica para aclarar el diagnóstico definitivo. El autor declara no tener conflictos de interés, en relación a este artículo.