Introducción
La enfermedad de Paget (EP) se origina por una resorción osteoclástica muy activa a la que se superpone una formación osteoblástica de igual intensidad, aunque desorganizada1. La importancia de esta alteración subyacente del remodelado aconseja utilizar como tratamiento de la enfermedad fármacos antirresortivos que disminuyan la velocidad de recambio óseo e inhiban la actividad de los osteoclastos2. En este grupo de fármacos destacan los bifosfonatos de segunda y tercera generación que, a diferencia de la supresión parcial y transitoria producida por la calcitonina3, pueden proporcionar una remisión completa y prolongada que se traduce en la normalización de las alteraciones bioquímicas e, incluso, en una mejoría de las lesiones radiológicas e histopatológicas de la enfermedad4,5. Un aspecto clave, sobre el que se dispone de escasa información, es el conocimiento de los factores que condicionan la respuesta al tratamiento, es decir, aquellas variables que determinan la intensidad y la duración de la remisión6. Ello permitiría definir a priori las condiciones de utilización de los bifosfonatos, así como las características biológicas de los pacientes y los rasgos de la EP que se asocian con una mejor respuesta.
El tiludronato (ácido 4-clorofenil tiometil bifosfónico) es un bifosfonato que ocasiona una marcada inhibición de la actividad de los osteoclastos maduros, al disminuir su capacidad para segregar protones al espacio de resorción y favorecer su separación de la matriz ósea7. Su eficacia en el tratamiento de la EP se ha comprobado en diversos estudios8-13. Presenta un excelente margen terapéutico, ya que la dosis que induce una inhibición eficaz de la resorción no ocasiona efectos apreciables sobre la mineralización14 ni disminuye la resistencia biomecánica del hueso15. Hace 10 años comunicamos los resultados de un estudio en el que analizábamos los factores que permiten predecir la respuesta al tiludronato16. Este estudio confirmó que el tiludronato proporciona, en la mayoría de los casos, una mejoría clínica y una remisión bioquímica rápida y completa, sin inducir efectos adversos importantes. Asimismo, nuestros datos indicaban que la concentración hística del fármaco, más que la absorción, es un factor importante en la respuesta. El objetivo del presente trabajo es investigar los factores que condicionan la duración de la respuesta al tiludronato en esta cohorte de pacientes a los que hemos seguido, de forma sistemática, hasta el momento actual.
Pacientes y métodos
Sujetos. Seguimiento
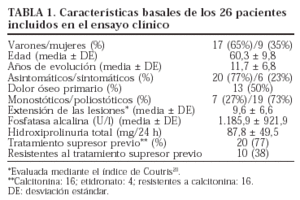
Se ha seguido a intervalos regulares hasta mayo de 2003 a todos los pacientes (n = 26) incluidos en el ensayo clínico sobre eficacia y bioequivalencia del tiludronato en la EP16,17. Este estudio inicial se llevó a cabo entre abril de 1993 y marzo de 1994, período en el que se atendió en una consulta monográfica sobre EP a 92 pacientes a quienes se había diagnosticado la enfermedad según los criterios radiológicos habituales18. De ellos se seleccionó de forma consecutiva a los 29 que tenían una concentración de fosfatasa alcalina (FA) superior al doble del valor de referencia y que no presentaban insuficiencia renal, alteraciones hematológicas relevantes, ulcus péptico o enfermedad hepática activa, cáncer de próstata, fractura en proceso de consolidación u otra enfermedad ósea distinta de la EP. Además, no debían haber recibido tratamiento supresor en los 3 (calcitonina), 6 (etidronato o tiludronato) o 24 (otros bifosfonatos) meses previos. Cada paciente tomó 400 mg/día de tiludronato por vía oral durante 90 ± 6 días, y se les indicó que debían ingerir las tabletas sólo con agua y guardar ayuno durante las 2 h previas y las 2 h siguientes a la toma, así como evitar cualquier otra medicación durante esas 4 h. Aparte del tiludronato no se administró ningún otro fármaco con efectos sobre el metabolismo óseo durante el período de estudio. El protocolo fue aprobado por el comité de ética e investigación clínica de nuestro hospital y todos los pacientes, tras ser informados sobre los objetivos y características del ensayo, dieron su consentimiento por escrito. Tres pacientes que reunían los requisitos para ser incluidos rehusaron participar. Los 26 pacientes completaron con exactitud los 3 meses de tratamiento y han seguido acudiendo a las visitas periódicas programadas desde entonces. La muestra está formada por 17 (65%) varones y 9 (35%) mujeres, cuya edad media ± DE era de 60,3 ± 9,8 años (rango: 38-76). En la tabla 1 se exponen las características fundamentales de los pacientes.
Métodos de evaluación
Los detalles sobre los procedimientos de evaluación de la respuesta en la fase de ensayo clínico se han publicado anteriormente16,17. Se estableció como criterio principal de eficacia la disminución en la concentración de FA sérica total, cuantificada mediante autoanalizador (valores normales: 90-280 U/l) y expresada como porcentaje de reducción respecto a la basal. Consideramos que existe remisión bioquímica cuando los valores de FA se sitúan dentro de los límites normales del método. Definimos la recaída como una vuelta a valores de FA superiores a 2 veces el valor de referencia (lo que implica la indicación de un nuevo ciclo de tiludronato). Consideramos que había resistencia al tratamiento si el porcentaje de reducción de FA era inferior al 50% respecto a los valores basales.
Análisis estadístico
Se investigó la evolución de la probabilidad de recaída bioquímica de FA mediante la prueba de Kaplan-Meier. Para determinar qué variables predecían mejor la duración de la respuesta, y en qué medida, se realizó un análisis de modelos de riesgo proporcional (regresión de Cox). Se consideró como "variable tiempo" el tiempo transcurrido (en meses) hasta que se producía la recaída bioquímica. En el modelo máximo se incluyeron como variables independientes las siguientes: a) demográficas: edad y sexo, b) "de respuesta": concentración basal de FA y porcentaje máximo de reducción de dicha enzima (a los 6 meses de finalizar el tratamiento), y c) parámetros farmacocinéticos del tiludronato (determinados al mes de iniciar el tratamiento): concentración mínima (o valle), concentración máxima y área bajo la curva de la concentración-tiempo. Estas variables se seleccionaron a partir de criterios clínicos y de los resultados obtenidos en el análisis previo16. Respecto a las variables que permanecen en el modelo final, la concentración de tiludronato se cuantificó en mg/dl, y la de la FA, en U/l. Como estrategia de modelización seguimos un procedimiento "por eliminación hacia atrás" (backward). Se usaron como criterios para eliminar una variable: a) la variación en la χ2 del modelo (> 10%), y b) el cambio en su significación estadística, al suprimir la variable que cada vez muestra un valor de p más alto. El procesamiento y análisis de los datos se realizó con el paquete PRESTA19.
Resultados
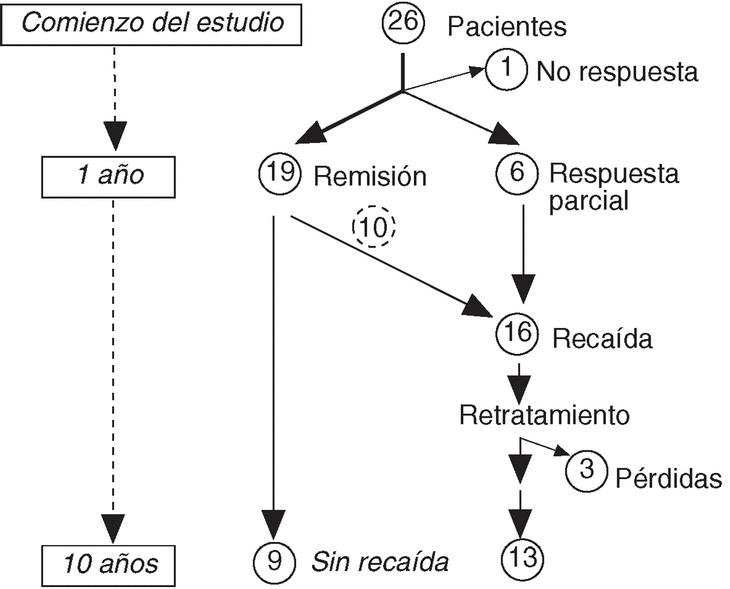
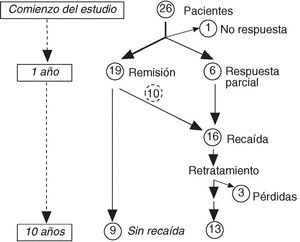
La evolución de las incidencias habidas en esta cohorte de pacientes, desde el tratamiento inicial (entre 1993 y 1994) hasta el final del período de observación (mayo de 2003), se muestra en la figura 1. Sólo uno de los 26 pacientes incluidos en el ensayo clínico presentó resistencia inicial al tratamiento con tiludronato. De los restantes, en 19 pacientes se normalizaron las cifras de FA y 6 tuvieron una respuesta superior al 50% de los valores basales, aunque no llegaron a alcanzar la remisión completa (respuesta parcial). Se han producido 3 pérdidas en el seguimiento, 2 por fallecimiento y una por cambio de domicilio. Nueve de los 19 pacientes en que se normalizaron las cifras de FA han permanecido durante los 10 años de seguimiento libres de recaída, por lo que no han precisado de nuevos ciclos de tratamiento. Los 16 restantes (10 del grupo que alcanzó la remisión inicial y los 6 con respuesta parcial) han presentado recaída, recibiendo uno o varios ciclos posteriores con una media ± DE de 1,43 ± 0,68 ciclos por paciente. De ellos, 11 pacientes recibieron 2 ciclos, 3 precisaron 3 ciclos, y 2 un total de 4 ciclos. Además, en 4 pacientes que mostraron resistencia tras varios ciclos de tiludronato, se realizó un cambio de tratamiento: pamidronato por vía intravenosa (90 mg) en un caso y risedronato (35 mg/día por vía oral, durante 2 meses) en los 3 restantes, y todos ellos alcanzaron remisión bioquímica con este fármaco. Tres pacientes han mantenido la remisión inicial a lo largo de los 10 años de seguimiento. No se observaron efectos secundarios clínicos importantes ni alteraciones analíticas relevantes que indicaran toxicidad en un total de 49 ciclos administrados. Ningún paciente tuvo que interrumpir o abandonar el tratamiento.
Figura 1. Evolución de la respuesta a lo largo del estudio.
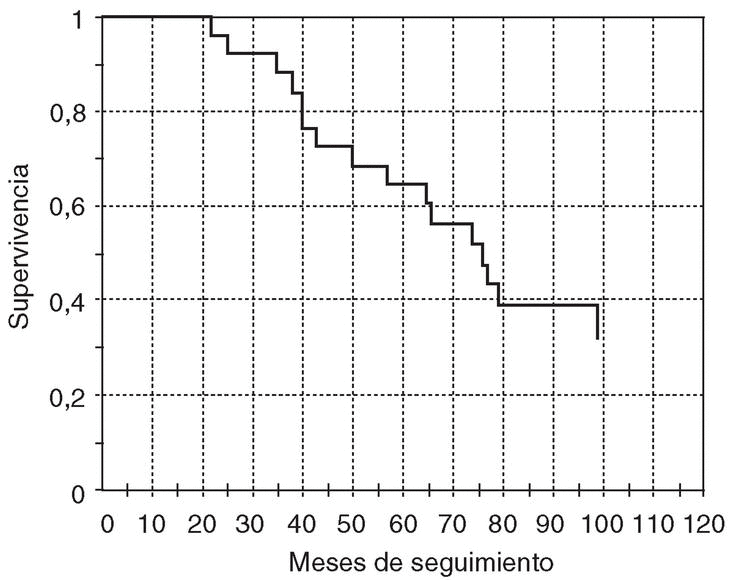
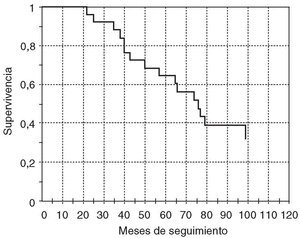
La evolución de la probabilidad de recaída bioquímica estimada mediante la prueba de Kaplan-Meier se muestra en la figura 2. El tiempo medio (mediana) hasta la primera recaída es de 53,5 meses, y de 36 meses hasta la segunda recaída (n = 13). El porcentaje máximo de reducción de FA (media ± DE) tras el segundo ciclo fue del 55,3 ± 12,9%. Ocho pacientes (50%) de los 16 que requirieron un segundo ciclo alcanzaron de nuevo la remisión.
Figura 2. Función de supervivencia. Probabilidad de permanecer sin recaída.
En la tabla 2 se comparan las variables demográficas, clínicas, farmacocinéticas y de evaluación de la respuesta al tratamiento, entre los 9 pacientes que no precisaron ningún nuevo ciclo y los 16 que mostraron recaída. Destaca la mayor extensión de las lesiones óseas (11,68 ± 7,4 frente a 5,33 ± 0,7; p = 0,003) y una concentración de FA más elevada (1.446 ± 810 frente a 849 ± 255; p = 0,01) en los pacientes con recaída. Igualmente, en los parámetros farmacocinéticos se aprecian diferencias importantes que indican una distribución más eficiente del fármaco en los pacientes sin recaída. Dichas diferencias alcanzan significación estadística (concentración mínima: 1,03 ± 0,40 frente a 0,67 ± 0,33; p = 0,02, y área bajo la curva: 61,98 ± 26,53 frente 39,40 ± 12,91; p = 0,03) o se encuentran cerca de ella (concentración máxima: 4,26 ± 2,21 frente a 2,66 ± 1,11; p = 0,06).
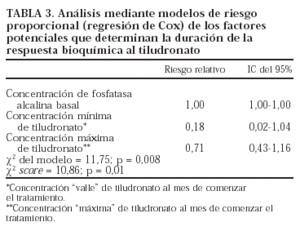
El modelo final de regresión de Cox se representa en la tabla 3. La concentración basal de FA y las concentraciones mínima y máxima de tiludronato, medidas al mes de iniciar el tratamiento, son las que predicen con mayor fiabilidad la duración de la respuesta bioquímica. La exclusión de las variables que, estando en el modelo máximo, no permanecen en el modelo final debe interpretarse en el sentido de que su efecto sobre la variable dependiente no es significativo cuando se tiene en cuenta la influencia de los demás factores21.
Discusión
En el presente estudio se analiza de forma prospectiva la duración del efecto del tiludronato en la EP y se investigan los factores que pueden influir en la respuesta a largo plazo. El estudio se basa en una cohorte de 26 pacientes seguidos de manera sistemática durante 10 años, tras un ensayo clínico en el que se administró el fármaco a la dosis de 400 mg/día por vía oral durante 3 meses. Los primeros resultados indicaban que el fármaco era eficaz en la supresión de los índices bioquímicos de recambio óseo, ya que a los 6 meses de finalizar el tratamiento, momento en que se alcanzaba la máxima intensidad en la respuesta, la disminución media en la concentración de FA respecto a los valores basales superaba el 75%, y el 65% de los pacientes presentaba una FA normal. El análisis multivariante demostró que la concentración mínima de tiludronato era el mejor predictor de la respuesta inicial.
El factor más importante para determinar la eficacia de un fármaco en la EP, junto con la intensidad de la respuesta inicial, es la duración de la remisión. Se ha sugerido que el tratamiento temprano con los nuevos bifosfonatos podría suprimir de forma continuada su actividad5,22. Esta sería una de sus características más interesantes y la principal ventaja respecto a otras terapias, como la calcitonina, ya que, al evitarse la deformidad y el agrandamiento óseos, disminuiría el riesgo de desarrollar fracturas y otras complicaciones evolutivas5. En el presente trabajo se ha observado que el efecto del tiludronato se mantiene de forma considerable a lo largo del tiempo. En este sentido, se ha observado que la mediana de tiempo hasta la primera recaída es de 53,5 meses, y que 9 de los 19 pacientes en que se normalizaron las cifras de fosfatasa alcalina tras el primer ciclo han permanecido libres de recaída. Además, 3 de ellos han mantenido la remisión durante los 10 años de seguimiento. El porcentaje máximo de reducción (media ± DE) tras el segundo ciclo fue del 55,3 ± 12,9% frente al 77,3 ± 8,8% (p = 0,001). Estas menores duración e intensidad de la respuesta tras el segundo ciclo indican un cierto grado de agotamiento en la acción del fármaco, algo ya observado con otros bifosfonatos23. Sin embargo, aun resultando inferiores a los observados tras el primer ciclo, estos parámetros continúan siendo elevados, por lo que la respuesta tras el segundo ciclo se puede considerar todavía aceptable. La tolerancia al tratamiento en los ciclos posteriores, al igual que en el ciclo inicial, es excelente y no se ha observado ningún efecto adverso grave.
A pesar de la amplia experiencia disponible en el empleo de los bifosfonatos, el conocimiento de las variables que pueden predecir la intensidad y la duración de la respuesta es escaso. En general, se acepta que cuanto más activa es la enfermedad menos intensa y prolongada es la respuesta6. Por ello resulta lógico que, como ocurre en nuestro estudio (tablas 2 y 3), los pacientes con una FA basal más baja tengan una mayor probabilidad de mantener la remisión. Por el contrario, como se observa en la comparación simple de variables (tabla 1) y en el análisis de regresión de Cox (tabla 3), la respuesta inicial no parece tener una influencia decisiva en la duración. En el análisis de regresión, además de las variables relacionadas con el recambio óseo (extensión y actividad bioquímica basal) y con la respuesta celular inicial (reducción de FA), se han considerado como posibles factores predictores las variables relativas a las propiedades farmacocinéticas del tiludronato (concentración mínima o valle, concentración máxima y área bajo la curva); el tiempo transcurrido desde el último tratamiento, y las características biológicas habituales. De todas las variables incluidas en el modelo final de Cox (tabla 3), la concentración mínima o valle de tiludronato al mes de comenzar el tratamiento es la que tiene una mayor influencia sobre la duración de la respuesta. Este mismo parámetro ya aparecía como el principal factor predictor de la respuesta inicial16. La concentración valle se puede considerar un indicador de la concentración hística del fármaco. Resulta lógico que cuanto más bifosfonato se acumule en el tejido diana, en este caso el hueso, mayor será la inhibición de la resorción osteoclástica y, por consiguiente, se obtendrá una supresión más acusada y duradera7. Este factor, junto a una hipotética variación interindividual en la sensibilidad de los osteoclastos a la acción de los bifosfonatos, se considera determinante en la intensidad y duración de la respuesta6. Por otra parte, en los estudios farmacológicos se demuestra que la respuesta bioquímica es relativamente constante a pesar de la gran variabilidad intra e interindividual en la absorción, y que ésta, una vez sobrepasado un mínimo crítico, no parece tener una influencia notoria sobre la respuesta bioquímica24. Por el contrario, en dichos estudios se señala que la acumulación en el tejido óseo resulta esencial en la magnitud de la respuesta terapéutica. De acuerdo con ello, la implicación práctica de nuestros resultados es que la concentración valle al mes de comenzar el tratamiento es el indicador más útil para evaluar la persistencia del efecto del tiludronato.
En conclusión, los resultados de nuestro estudio indican que el tiludronato proporciona una reducción de los marcadores bioquímicos de actividad de la EP profunda y duradera, sin inducir efectos adversos importantes. La concentración hística del fármaco resulta ser el factor clave tanto en la intensidad (respuesta a corto plazo) como en la duración de la respuesta.