El término polineuropatía (PNP) describe aquellas enfermedades que, bien por trauma externo, bien por agresión desde el medio interno, cursan con lesión de nervios periféricos. La prevalencia en ancianos ronda el 5-10%. La causa más habitual que se implica es la diabetes mellitus, aunque se relaciona con multiples etiologías. Un hecho característico en la PNP es la diversidad de síntomas que presentan, probablemente relacionada con la multifuncionalidad del nervio, lo que provoca un abanico de expresiones clínicas, desde simples déficits sensitivos o motores hasta inhabilidad para mantener el control motor, la postura o la marcha. El diagnóstico es difícil en ancianos y puede suponer un reto para el geriatra en pacientes con deterioro funcional; el estudio electrofisiológico es la principal herramienta diagnóstica. Se aporta una descripción de las PNP más habituales en el anciano basándose en la fisiopatología, así como una propuesta práctica de clasificación clínica.
The term polyneuropathy (PNP) is used to describe a group of entities affecting the peripheral nerves, due to external trauma or internal pathology. The prevalence of PNP in the elderly is between 5 and 10%. Despite the multiplicity of causes, the most common etiological factor is diabetes. PNP is characterized by a wide variety of symptoms, due to the multiple functions of nerves. Clinical manifestations range from sensory or motor deficit to inability to maintain gait and stability. Diagnosis is difficult in the elderly, and can be a challenge to the geriatrician in patients with functional impairment. The gold standard for diagnosis is electrophysiology testing. The present article describes the main PNP in the elderly based on the physiopathology of these diseases and provides a practical proposal for clinical classification.
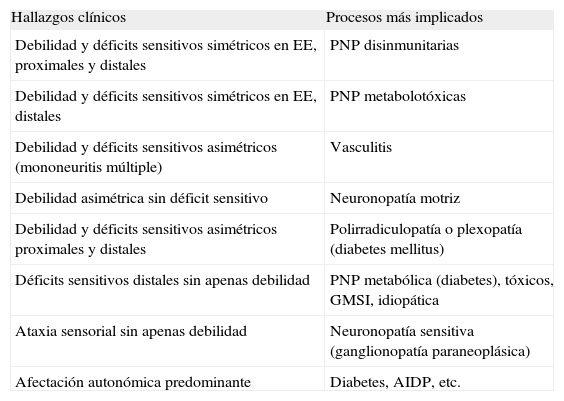
El término polineuropatía (PNP) describe las enfermedades que, bien por trauma externo, bien por agresión desde el medio interno, cursan con lesión de nervios periféricos. La amplia distribución en el organismo, su situación frecuentemente expuesta y el grado extremo de especialización funcional hacen que el nervio se convierta en una estructura muy vulnerable. La prevalencia en ancianos en países desarrollados ronda el 5-10%1, parecida a la del accidente cerebrovascular, lo que proporciona una alta repercusión en la morbimortalidad sociosanitaria. La causa más habitual que se implica es la diabetes mellitus2-4, aunque se relaciona con múltiples etiologías, incluso algunos autores refieren una nada despreciable proporción de causa idiopática5. Un hecho característico en la PNP es la diversidad de síntomas que presentan los pacientes, probablemente relacionada con la multifuncionalidad del nervio, lo que provoca un abanico de expresiones clínica, desde simples déficits sensitivos o motores hasta problemáticas de mayor complejidad (tabla 1) como inhabilidad para mantener el control motor, la postura o la marcha6.
Hallazgos clínicos en las polineuropatías del anciano
| Hallazgos clínicos | Procesos más implicados |
| Debilidad y déficits sensitivos simétricos en EE, proximales y distales | PNP disinmunitarias |
| Debilidad y déficits sensitivos simétricos en EE, distales | PNP metabolotóxicas |
| Debilidad y déficits sensitivos asimétricos (mononeuritis múltiple) | Vasculitis |
| Debilidad asimétrica sin déficit sensitivo | Neuronopatía motriz |
| Debilidad y déficits sensitivos asimétricos proximales y distales | Polirradiculopatía o plexopatía (diabetes mellitus) |
| Déficits sensitivos distales sin apenas debilidad | PNP metabólica (diabetes), tóxicos, GMSI, idiopática |
| Ataxia sensorial sin apenas debilidad | Neuronopatía sensitiva (ganglionopatía paraneoplásica) |
| Afectación autonómica predominante | Diabetes, AIDP, etc. |
AIDP: acute inflammatory demyelinating polyradiculoneuropathy; EE: extremidades; GMSI: gammapatía monoclonal de significado incierto; PNP: polineuropatía.
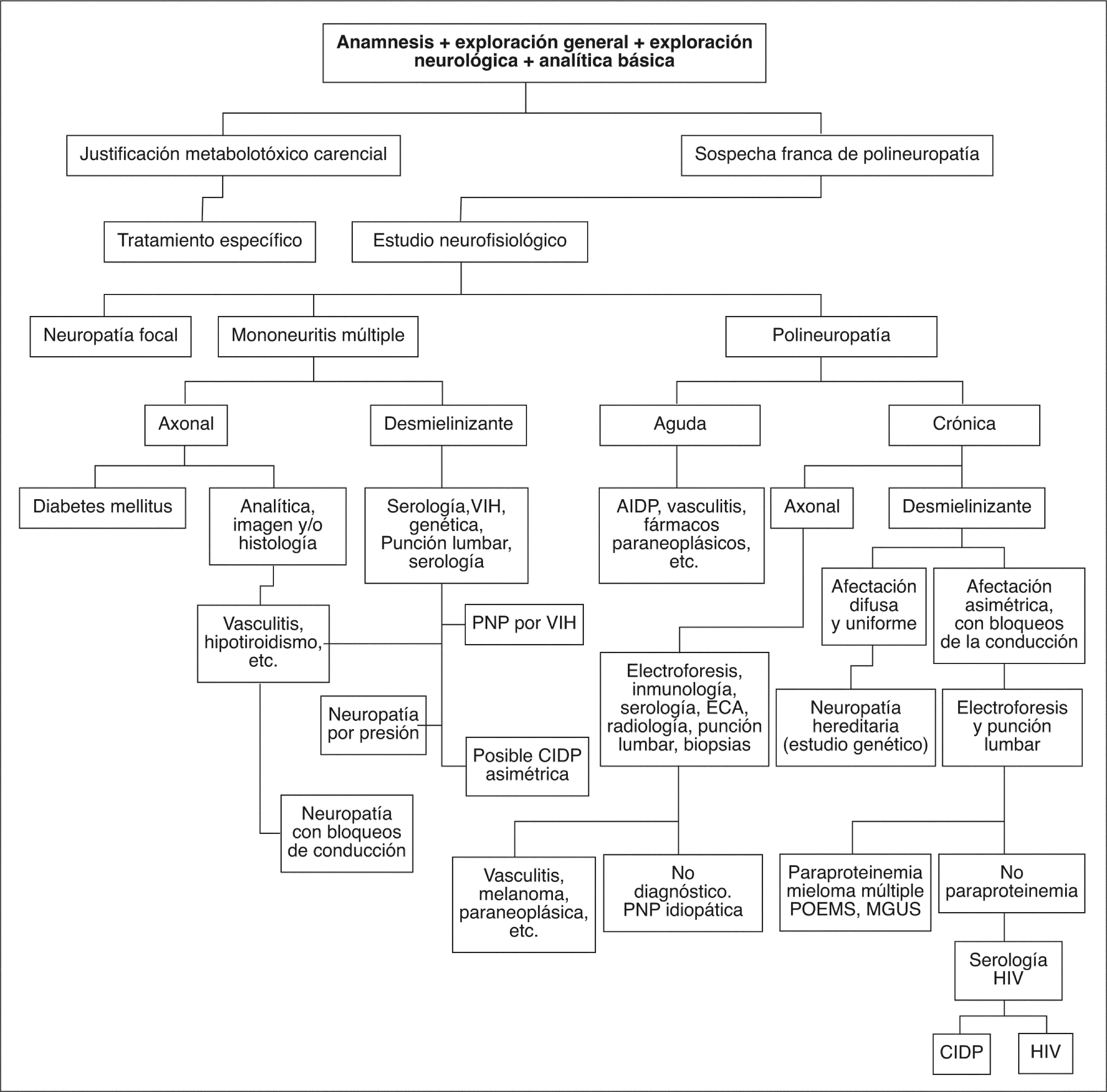
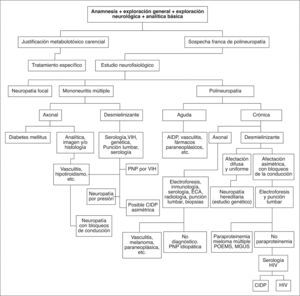
La implicación fisiopatológica es muy determinante en la evolución de estos procesos, de tal manera que la axonopatía en esta población es el mecanismo más involucrado, así como la mayor causa de secuelas funcionales. Las PNP axonales mayoritariamente comparten un tipo particular de agresión, la degeneración axonal retrógrada o dying back. Este fenómeno consiste en la destrucción axonal progresiva y centrípeta por causa de procesos no del todo bien conocidos, aunque aparentemente relacionados con el metabolismo neuronal, conflictos en el transporte axonal soma-axón distal y/o tóxicos, en cualquier caso causantes de desintegración axonal distal. Lógicamente, la lesión se localizará en las regiones más comprometidas para una adecuada nutrición y recambio de elementos estructurales, en concreto, por la mayor longitud, las distales de miembros inferiores. Se entiende, por tanto, que la enfermedad afecte de manera difusa, bilateral y simétrica, aunque con inicio y mayor expresividad en territorios distales de las piernas, a diferencia de la multineuritis o mononeuritis múltiple, en cuyo caso los déficits se circunscriben a los territorios inervados por los troncos nerviosos implicados, con frecuencia desencadenando cuadros asimétricos, bilaterales o no, y con frecuencia complejos en la distribución topográfica por implicar uno o varios troncos. Sobre la base de los datos clínicos y de laboratorio se puede proponer un algoritmo diagnóstico básico para estos procesos (fig. 1), en ocasiones de difícil evaluación por las características de la enfermedad y de la idiosincrasia del paciente.
Algoritmo diagnóstico de las polineuropatías en el anciano. AIDP: acute inflamarory demyelinating polyradiculoneumopathy; CIDP: chronic inflammatory demyelinating polyradiculoneuropathy; ECA: enzima conversora de la angiotensina; MGUS: gammapatías monoclonales de significado incierto; PNP: polineuropatía; VIH: virus de inmunodeficiencia humana; POEMS: polyneuropathy, organomegaly, endocrinopathy, or-protein plasma cell dyscrasia, skin lesions.
Aportamos una descripción de las PNP más habituales en el anciano sobre la base de la fisiopatología, así como una propuesta práctica de clasificación clínica.
Polineuropatías endocrinometabólicas y tóxicasEs una de las causas más habituales de consulta neurológica en geriatría. Son resultado de procesos metabólicos, como diabetes y uremia, o tóxicos, como el etilismo, medicamentos y quimioterápicos. Con mucho, la diabetes mellitus es el más frecuente, tanto más cuanto más tiempo se haya convivido con la enfermedad, lo que convierte a los ancianos en el grupo de afectados más numeroso de la población. La pérdida de axones sensitivos produce reducción o mala integración de las sensaciones. Se entiende que probablemente las parestesias espontáneas y las disestesias se produzcan por desmielinización, mientras que la debilidad sea consecuencia de mecanismos inespecíficos. Un hecho que se debe destacar es el protagonismo de la sintomatología sensitiva en estos pacientes; sin embargo, la realidad suele coexistir con daño motor en el 100% de los casos, aunque habitualmente subclínico. El sistema motor presenta mecanismos compensadores complejos muy eficientes (no tanto el sensitivo), que impiden la expresión clínica objetivable y que permiten mantener una fuerza suficiente. La aparición de debilidad objetiva se produce cuando existe ya una pérdida importante de axones, por encima del 30-50%, lo que coincide con frecuencia con períodos muy avanzados de la metabolopatía. Por tanto, en este grupo de PNP el daño axonal es por igual sensitivo y motor, aunque clínicamente de claro predominio sensitivo.
Este tipo de PNP se caracteriza por un inicio y progresión insidiosa, poco sintomática, en forma de parestesias distales en extremidades inferiores distribuidas en calcetín. La progresión es centrípeta y simétrica, y con el tiempo afecta a los miembros superiores, inicialmente distribuida en guante. Otro dato inicial muy significativo es la alteración e incluso la desaparición de los reflejos, especialmente los distales (aquíleos), aunque en ancianos puede ser engañoso por cuanto en un porcentaje alto están ausentes, sin que ello se relacione con neuropatía. Conforme progresa la neuropatía y claudican los mecanismos compensadores reinervativos/regenerativos, aparece debilidad progresiva de predominio distal y simétrica, que puede en casos graves ser generalizada y muy invalidante. Lo habitual en ancianos es que comprometa predominantemente la marcha, aunque no olvidemos que la clínica que domina el cuadro es siempre sensitiva.
Diabetes mellitusForma de afectación sensitivo-motriz distal. La prevalencia no es bien conocida aunque en casos de larga evolución, por encima de 5 años, la presentan clínicamente entre el 10 y el 60%7. Es más frecuente en la tipo 2 o de inicio tardío, y el factor pronóstico más relevante para que se desarrolle PNP es el tiempo de evolución desde el diagnóstico más que la edad del paciente8.
El proceso es el descrito previamente compartido por todas las PNP de origen metabolotóxico por causa de degeneración axonal retrógrada9. La sensibilidad inicialmente más comprometida es la vibratoria, aunque la progresión incluya todas con el tiempo, lo que no deja de ser llamativo por cuanto las fibras más afectadas suelen ser las pequeñas, con escasa o ninguna mielina. En algunos casos, sobre todo con la evolución, pueden asociar dolor en miembros inferiores de tipo profundo y lancinante. No es infrecuente la asociación con síndrome de piernas inquietas y en especial mononeuropatías por atrapamiento (síndrome del túnel carpiano, neuropatía cubital, meralgia parestésica, neuropatía peroneal, etc.).
Otras formas menos frecuentes de polineuropatía diabética- –
PNP diabética dolorosa aguda. Dolor intenso y agudo por afectación combinada de fibras de pequeño y gran diámetro asociando debilidad y trastorno de la marcha (atáxica).
- –
Amiotrofia diabética. Debilidad asimétrica, con o sin dolor, localizada en regiones proximales de miembros inferiores (plexorradiculitis) e hipoarreflexia.
- –
PNP autonómica. Suele asociarse a PNP sensitivo motriz, provocando arritmias cardíacas, hipotensión postural, disfunción de la termorregulación, anomalías gastrointestinales y disfunción genitourinaria.
- –
Neuropatía craneal. Puede expresarse como mononeuropatía, en especial como isquemia del III par (oculomotor), del VI o incluso del IV o del VII. También puede presentarse multineuritis craneal.
- –
Radiculopatías troncales. Especialmente dorsales, caracterizadas por dolor irradiado siguiendo un segmento costal, unilateral o bilateral, asociando déficit sensitivo en esa distribución metamérica. El origen es isquémico.
- –
Multineuritis (mononeuritis múltiple). Afectación, más o menos simultánea inicialmente dolorosa, en múltiples troncos nerviosos con distribuciones muy variadas. El origen igualmente es isquémico y el cuadro clínico dependerá, lógicamente, del nervio lesionado y de la intensidad de la agresión.
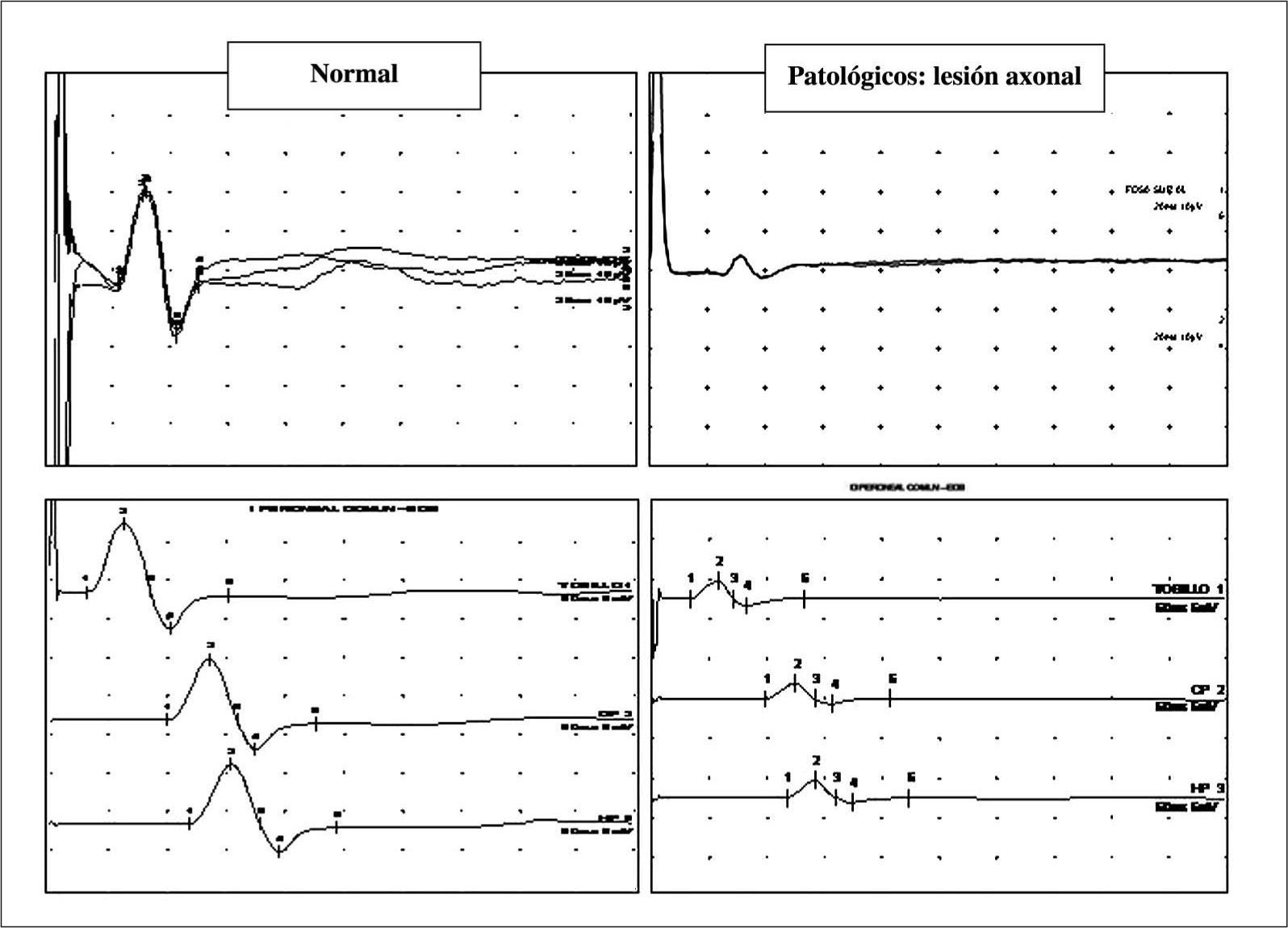
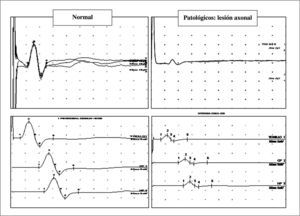
El diagnóstico complementario se realiza mediante neurofisiología (fig. 2), electroneurografía que demuestra un patrón de afectación mixta de claro predominio axonal distal y electromiografía que demuestra denervación crónica o subaguda/activa, dependiendo de la velocidad e intensidad de la agresión.
Superior: electroneurografía sensitiva antidrómica convencional de nervio sural. A la izquierda estudio normal; a la derecha patológico, definido por caída importante de amplitud, preservando latencia y velocidad de conducción (patrón axonal). Inferior: electroneurografía motora convencional de nervio peroneal. A la izquierda estudio normal: a la derecha patológico, definido por una caída importante de la amplitud, preservando latencia y velocidad de conducción en todos los segmentos (tobillo, pierna y rodilla/hueco poplíteo).
El tratamiento es principalmente etiopatogénico mediante un adecuado control metabólico. Es importante el control del dolor, que dependerá de la intensidad de la neuropatía. Son útiles los analgésicos, como el ácido acetilsalicílico o paracetamol, y los anticonvulsivantes como la amitriptilina, la carbamacepina, la gabapentina y la pregabalina10.
Polineuropatía urémicaLa causa parece ser tóxica, aunque los responsables no están aún claramente identificados, probablemente hormona paratiroidea y/o moléculas como mioinositol y otras de peso molecular medio. Un porcentaje muy alto de enfermos urémicos de larga evolución presentan lesión difusa de nervio, aunque la mayoría subclínica, demostrable en estudios neurofisiológicos. La afectación clínica suele existir en pacientes urémicos graves en situación de hemodiálisis crónica, sobre todo si además asocian diabetes mellitus o toman fármacos neurotóxicos como nitrofurantoína.
Los síntomas suelen ser mayoritariamente sensitivos, inicialmente déficit en la sensibilidad vibratoria en extremidades inferiores. Más tarde aparecen síntomas y signos semejantes a los descritos previamente. En casos evolucionados aparece también debilidad distal, trastorno de la marcha, así como síndrome de piernas inquietas y neuropatías por atrapamiento, tanto más frecuentes cuantos más factores de riesgo neuropático presente asociados (diabetes mellitus, etilismo, medicamentos, etc.).
Para el diagnóstico, se emplea la electroneurografía/ electromiograma (ENG/EMG) que demuestra una PNP axonal sensitivomotriz de predominio distal.
El tratamiento consiste en controlar el proceso de base (nefropatía) y el sintomático de la neuropatía (dolor, disestesias, etc.).
Polineuropatía en la hepatopatía crónicaEl mecanismo es poco conocido, probablemente más relacionado con tóxicos circulantes acumulados que lesionen el nervio. Se comporta como una polineuropatía axonal con síntomas de predominio sensitivo, asociando un moderado componente motor y autonómico. No es infrecuente la asociación de la hepatopatía con etilismo crónico, infección vírica o toma de fármacos, que pudieran también relacionarse con la neuropatía. La expresión clínica es indistinguible de la PNP de origen metabólico o tóxico, como la diabetes, uremia o etilismo.
Polineuropatía del hipotiroidismoLa neuropatía predominante es el atrapamiento del nervio mediano en el túnel carpiano, como resultado de los cambios tisulares producidos que comportan un mayor compromiso de espacio al paso del nervio. Puede aparecer una PNP axonal sensitivomotriz, predominando la sintomatología parestésica-disestésica en territorios distales de extremidades, con cierto componente de debilidad, en todo caso no dominante. El tratamiento de la endocrinopatía suele mejorar ambos procesos, en especial la PNP.
Polineuropatía por tóxicos- –
Alcohólica. Para que se produzca PNP es necesario consumir grandes cantidades de alcohol durante años y, del mismo modo, la abstinencia mejora paulatinamente la funcionalidad del nervio. Cabe pensar, por tanto, que el mecanismo tóxico, la mala dieta, los problemas de absorción pueden desempeñar un papel determinante11. Se produce pérdida de fibras, pequeñas y grandes, degeneración axonal y regeneración, y en menor medida desmielinización secundaria.
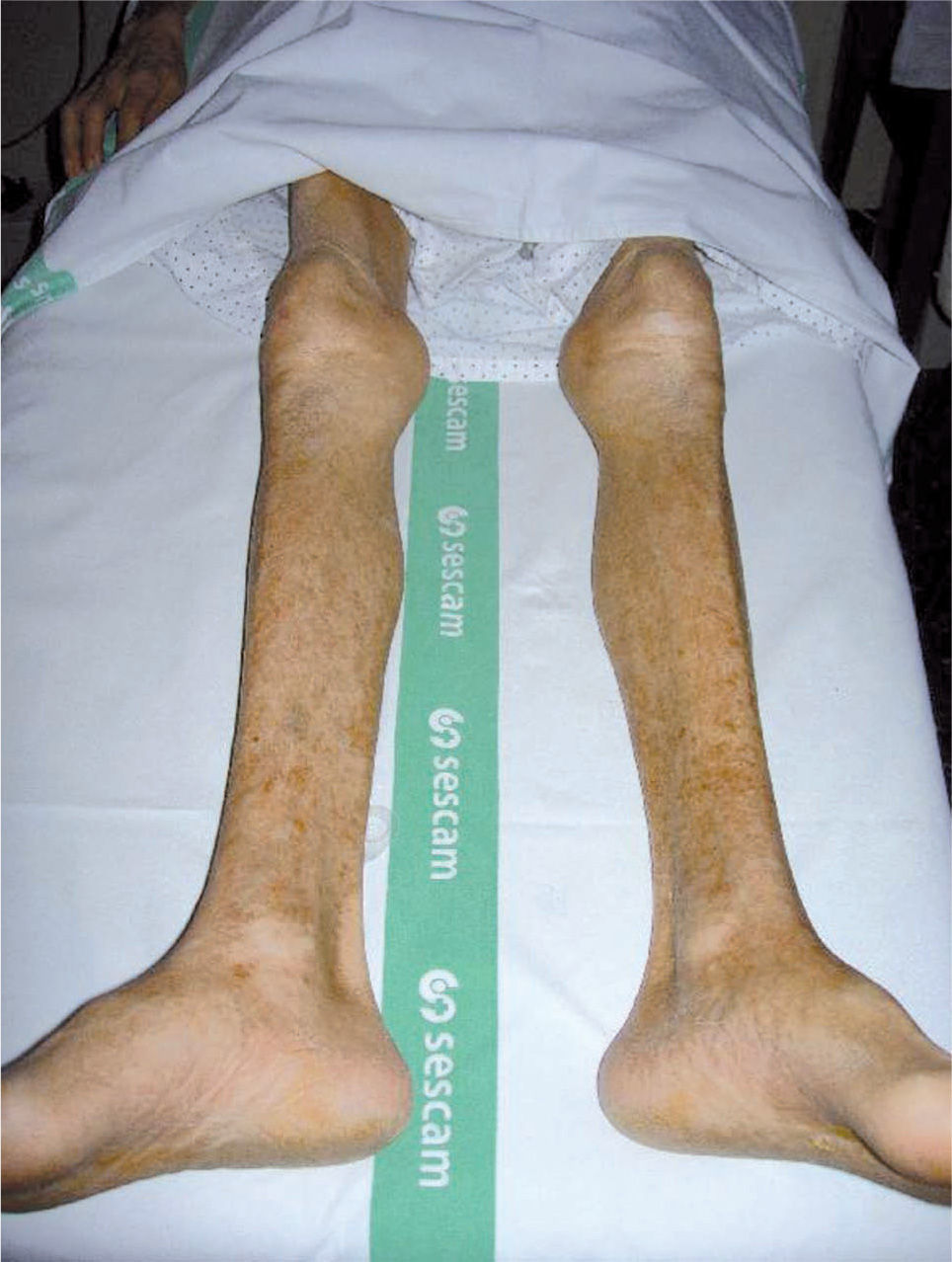
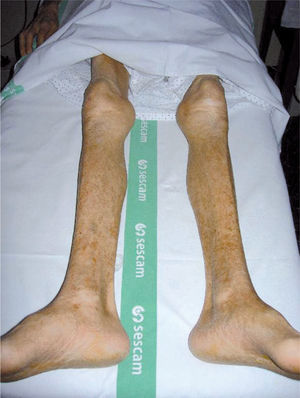
La sintomatología aparece de manera insidiosa, en meses-años, en forma de dolor, disestesias/parestesias distales y simétricas en MMII, al igual que en las anteriores PNP, asociando en casos graves debilidad y amiotrofia de predominio distal (fig. 3). Debemos diferenciar PNP de aquella debilidad originada por daño muscular directo (miopatías alcohólicas) sobre la base de la clínica, la neurofisiología y los hallazgos analíticos, y si es preciso a la anatomía patológica.
El diagnóstico es neurofisiológico y se encuentra una PNP axonal sensitivomotriz de predominio distal.
En el tratamiento, lo más importante es la suspensión del tóxico. La recuperación del nervio irá apareciendo en los siguientes meses, incluso con recuperación a veces completa de la función. Puede usarse vitamina B1, dirigida en especial a la sintomatología sensitiva (no modifica los trastornos tróficos o la debilidad). Es también obligado el tratamiento sintomático de las disestesias/parestesias.
- –
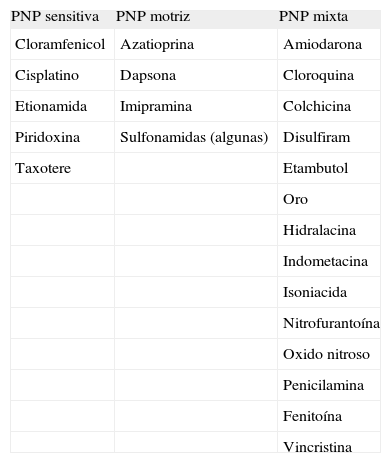
Fármacos. Múltiples fármacos se han relacionado con enfermedad de nervios (tabla 2). Los más conocidos son aquellas sustancias utilizadas en quimioterapia anticancerosa, pero muchos son los fármacos convencionales asociados a lesión de nervio. La estructura más implicada en la fisiopatología suele ser el axón, probablemente en el contexto de agresiones en las vías metabólicas celulares o del flujo axonal. Habitualmente, se producen neuropatías por el mecanismo de degeneración axonal retrógrada, lo que explicará toda la sintomatología clínica habitual sensitiva y motriz de inicio y predominio distal simétrico.
Tabla 2.Polineuropatía inducida por fármacos y sintomatología predominante
PNP sensitiva PNP motriz PNP mixta Cloramfenicol Azatioprina Amiodarona Cisplatino Dapsona Cloroquina Etionamida Imipramina Colchicina Piridoxina Sulfonamidas (algunas) Disulfiram Taxotere Etambutol Oro Hidralacina Indometacina Isoniacida Nitrofurantoína Oxido nitroso Penicilamina Fenitoína Vincristina PNP: polineuropatía.
Un capítulo especial lo constituye un fármaco de gran distribución en la población anciana, las estatinas. En los años noventa se produjo una serie casos de miopatía necrotizante grave, con resultado de muerte en unos cuantos, en relación con la lovastatina principalmente, clofibrato y gemfibrocilo, sobre todo cuando se combinaban. Desde entonces, con la retirada del preparado, apenas se han comunicado casos graves por este tipo de medicamentos, aunque en nuestra experiencia las nuevas estatinas todavía siguen provocando daño muscular, en la mayoría de los casos leve o subclínico, aunque con expresividad en el EMG y la analítica.
Polineuropatías nutricionalesSon un grupo de neuropatías de especial incidencia en la población anciana. Se relacionan con síndromes malabsortivos, como anemia perniciosa, disenterías, pelagra, dietas hipoproteicas o hipocalóricas, con la caquexia, con el etilismo y con síndromes paraneoplásicos. Todos estos procesos provocan que determinadas vitaminas como, la B12, fólico, E y B6, no presenten una aceptable disponibilidad.
Surgen de manera más o menos aguda, con dolor, parestesias, pérdida de sensibilidades y debilidad, en especial trastorno de la marcha, como siempre en un inicio más predominante en regiones distales del los miembros inferiores.
Un caso particular es la PNP por déficit de B12, que suele asociar mielopatía y a veces afectación del sistema nervioso central. Por tanto, son pacientes en los que se mezcla la sintomatología y semiología neuromuscular de PNP y la paraparesia espástica.
El estudio neurofisiológico mediante EMG/ENG muestra una PNP axonal sensitivomotriz distal. La presencia de mielopatía, con síndrome cordonal posterior±lesión motriz piramidal se evalúa mediante el estudio de potenciales evocados somatosensoriales y conducción motriz central (estimulación magnética transcraneal), respectivamente.
Mediante analíticas, se pueden evidenciar y cuantificar los déficits de vitaminas.
El tratamiento es el de la enfermedad de base, añadiendo complejos vitamínicos que detengan la progresión de la neuropatía, aunque los déficits residuales pueden persistir.
Polineuropatía del enfermo críticoEs un proceso que afecta a pacientes ingresados en unidad de cuidados intensivos con pronóstico muy grave o crítico. Inicialmente sólo se hablaba de PNP pero al poco se comprobó que también puede lesionarse el músculo o la placa12.
Todas las variedades se expresan como tetraparesia flácida hipoarrefléxica, con imposibilidad del«destete»de la intubación y preservación cognitiva completa, siempre que no exista daño encefálico. Precisar el tiempo evolutivo es, en muchos casos, imposible por cuanto estos pacientes suelen presentar disminución de conciencia o limitación de movimientos, con lo que la debilidad no puede detectarse y calibrarse bien en el inicio y, por tanto, se convierte en un síntoma de valoración dificultosa. La diferenciación clínica entre PNP y miopatía es imposible, tan sólo se realiza mediante neurofisiología. La importancia de realizar un adecuado diagnóstico diferencial del proceso radica en el pronóstico, muy bueno en miopatía (recuperación ad íntegrum en el 100%), y reservado, aunque habitualmente satisfactorio, en la PNP.
La PNP del paciente crítico aparece en pacientes con enfermedades muy graves, en los que se produce una reacción denominada respuesta inflamatoria de estrés, en algunos aspectos aún no bien conocida. Se ha relacionado desde el inicio sobre todo con la presencia de sepsis, además de la toma de relajantes musculares, corticoides (probablemente dependientes de la dosis) y, en algunos casos, con aminoglucósidos. Aparece degeneración axonal retrógrada y, por tanto, una PNP axonal simétrica de predominio distal. La mayoría se recupera satisfactoriamente en los meses siguientes, salvo algunos pacientes que presentarán déficits residuales.
Polineuropatías disinmunitarias adquiridasDe predominio desmielinizanteForma crónica o CIDP (chronic inflammatory demyelinating polyradiculoneuropathy). Es una enfermedad infrecuente, con una prevalencia de 1/100.000, con mayor afectación de varones (2:1), y con una edad predominante de inicio en el anciano en la sexta o séptima década13,14. Con frecuencia, se relaciona con inmunizaciones o infecciones previas.
El inicio es insidioso, evolucionando en semanas-meses, con la aparición en el 80% de pacientes de debilidad generalizada y pérdida sensorial en las extremidades, sin dolor. En general, el paciente al principio presenta debilidad de extremidades, proximal y distal, con progresión insidiosa durante semanas, persistiendo en el transcurso de meses o incluso años de varios modos, con mayor frecuencia mantenida aunque fluctuante, o bien recidivante con brotes imprevisibles entre los que persisten déficits. Suele asociar trastorno parestésico distal e hipoarreflexia universal, preservando tanto la función cognitiva como esfinteriana. El primer brote suele ser indistinguible de la forma aguda (acute inflammatory demyelinating polyradiculoneuropathy, AIDP) y tan sólo la evolución en las siguientes semanas podrá permitir el diagnóstico, bien por persistencia de déficit o por la aparición de uno nuevo en las semanas posteriores15.
La evolución es variable, dependiendo lógicamente de la intensidad, así como de la frecuencia de brotes. No es infrecuente encontrar a pacientes que a lo largo de años han desarrollado una gran limitación funcional, para la marcha y para la manipulación, amiotrofias difusas, déficits craneales motores y, en general, una gran dependencia para las tareas de la vida diaria.
La exploración neurológica muestra hipoarreflexia temprana (90%) y sobre todo debilidad y amiotrofias en las extremidades. En algunos pacientes puede objetivarse, con neuroimagen en la mitad de casos, hipertrofia nerviosa por remielinización aberrante en bulbos de cebolla (raíces o plexos). No es infrecuente encontrar fasciculaciones como expresión de mecanismos regenerativos/reinervativos.
El diagnóstico se realiza mediante neurofisiología. La ENG muestra desmielinización sensitiva y motriz difusa de múltiples nervios, sin un predominio definido. Suelen asociar atrapamientos o lesiones focales (mononeuropatías). La EMG muestra degeneración axonal secundaria. Encontraríamos denervación subaguda más llamativa en territorios distales, así como crónica en relación con el tiempo de evolución y la pérdida funcional. La punción lumbar muestra un líquido cefalorraquídeo con disociación albúmino/citológica. Son aconsejables otras pruebas complementarias para descartar otras afecciones, como el virus de la inmunodeficiencia humana, gammapatía monoclonal, lupus eritematoso sistémico, enfermedad de Hodgkin, sarcoidosis, neuroborreliosis, etc.
El tratamiento debe ser individualizado. La posibilidad de fracaso terapéutico no es infrecuente, aunque en la mayoría la inmunomodulación es efectiva. Con un adecuado tratamiento conseguiremos disminuir el tiempo del brote y la severidad de los déficits. Se emplean corticoides, inicialmente. Durante 4 semanas, se utiliza prednisona a altas dosis, al menos 1mg/kg/día de peso. Posteriormente, se pasa a días alternos durante semanas. En algunos casos se necesitarán dosis bajas de mantenimiento, 10–20mg/día, durante largos períodos. Una respuesta ineficaz es aquella que no consigue una respuesta satisfactoria durante al menos 3–6 meses de tratamiento corticoideo a dosis altas. También se utilizan inmunoglobulinas por vía intravenosa que son efectivas a dosis de 0,4g/kg de peso/día, durante 5 días, en el 70% de los pacientes. Son más respondedores aquellos con afectación predominantemente motriz en fase de actividad. Por otro lado, apenas presentan efectos adversos. La plasmaféresis se reserva para pacientes no respondedores a inmunoglobulinas.
Forma aguda o AIDP. La prevalencia se sitúa en 1-4/100.000 habitantes. Puede aparecer a cualquier edad y en cualquier lugar del mundo, precedida en un 70% por una infección poco relevante, 1–3 semanas antes. Parece relacionarse con mecanismos inmunológicos exagerados hacia componentes de la mielina. La permeabilidad y facilidad al paso de las células defensivas en la barrera hematonerviosa y la mayor vascularización a nivel de plexo y raíces convierten estos segmentos en el terreno de inicio y predominio en la progresión del proceso16. Por tanto, son desmielinizaciones de inicio y predominio proximal, aunque clínicamente se manifiesten con déficits sobre todo motores (más mielinizados), distales y proximales.
La mayoría de los pacientes presentan inicialmente parestesias distales en las extremidades, que en las primeras horas va ascendiendo desde las plantas hasta distribuirse en media y guante, dando paso en esas primeras horas al síntoma y signo predominante: la debilidad. Ésta es simétrica y aguda, rápidamente progresiva, desarrollada en pocas horas, con una variabilidad en su gravedad amplia, que va desde la tetraplejía con insuficiencia respiratoria grave a un mínimo trastorno de la marcha17. En los primeros días, es frecuente la irrupción de disautonomía, con taquiarritmias/bradiarritmias, hipotensión postural, hipertensión arterial y multitud de síntomas vasomotores. La presencia o aparición de insuficiencia respiratoria grave y/o disautonomía recomienda, si se disfruta de disponibilidad, la monitorización continua durante varios días en una unidad de cuidados intensivos.
En la exploración neurológica se puede encontrar debilidad muscular variable, proximal y distal, simétrica en las cuatro extremidades, que progresa rápidamente, deteniéndose al cabo de 3–4 semanas, y da paso en unas 2 semanas a una fase estable, de meseta, sin cambios llamativos, para terminar en una mejoría paulatina, la mayoría con recuperación funcional satisfactoria en las siguientes semanasmeses. Pueden aparecer atrapamientos nerviosos en regiones comprometidas: neuropatía cubital en codo, peroneal en rodilla, síndrome del túnel carpiano, paresia facial periférica, esta última en más del 50% de los afectados. También aparece arreflexia, más característicamente universal, aunque en algunas ocasiones, en especial en los primeros días del proceso, puede ser sólo distal. Existen casos raros con reflejos presentes. Por último, en la sensibilidad encontramos déficits poco significativos en regiones distales de extremidades, más en los momentos iniciales del proceso.
Neurofisiología clínicaENG. Deben existir patrones claramente desmielinizantes en al menos 2 nervios por extremidad, y al menos evidenciar estos datos en más de 2 extremidades. La sensibilidad es muy alta a partir del quinto día de evolución. Entre el primero y el sexto día la posibilidad de falsos negativos es muy alta.
Electromiografía. En el caso de degeneración axonal secundaria se observará denervación aguda a partir de la segunda semana de evolución. Hay que ser cautos en cuanto a la interpretación de estos datos por las consecuencias pronósticas que presentan (axonotmesis significa recuperación tardía y en ocasiones parcial), puesto que la desmielinización proximal intensa puede provocar fenómenos de«denervación funcional», que aporten datos engañosos. Se recomienda hacer seguimiento durante los 45–50 días de evolución, de tal modo que la persistencia de fenómenos denervativos EMG al cabo de mes y medio indica, ya de modo definitivo, la presencia de degeneración axonal.
De predominio axonalExisten formas de síndrome de Guillain-Barré axonales, indistinguibles clínicamente del AIDP, en los que la diana inmunológica son estructuras axonales. Actualmente se denominan neuropatía axonal motora aguda (AMAN), si la afectación es motora, o neuropatía axonal sensitivomotriz aguda (AMSAN), si la afectación es sensitiva y motriz. El diagnóstico es clínico, pero la diferenciación fisiopatológica y pronóstica se realiza por exploraciones neurofisiológicas. En estos procesos, el pronóstico es peor que en la forma desmielinizante.
En muy raras ocasiones aparecen enfermedades crónicas, habitualmente desarrolladas en brotes, con déficits neurológicos progresivos, sin afectación mielínica, que denominamos RAN (chronic relapsing axonal neuropathy)18.
Polineuropatía axonal idiopática o CIAP (chronic idiopatic axonal polineuropathy). Hasta un 30 % de las PNP axonales no presentan una causa conocida en la población general o no pueden encuadrarse en una forma etiopatogénica admitida. Mucho se ha discutido sobre este tipo de afecciones, y la mayor parte de investigadores apuntan la posibilidad de que se trate de PNP en las que el proceso diagnóstico protocolizado no se ha llevado de manera adecuada y, por tanto, se trate de una evaluación incompleta5,19,20.
Polineuropatía asociada a neoplasiasLa forma más frecuente de neuropatía en el contexto de una neoplasia es la agresión a la neurona sensitiva situada en el ganglio raquídeo, y que se conoce como neuronopatía sensitiva o ganglionopatía. El tumor más relacionado con este proceso es el cáncer de pulmón de células pequeñas, pero también puede aparecer con neoplasias linfomatosas y, de manera más infrecuente, con tumor de ovario, de esófago y hepatocarcinomas.
El mecanismo patogénico no está aclarado, aunque sobre la base de algunos hallazgos puede estar en relación con respuestas inmunitarias hacia una proteína tumoral que presente determinados epítopes antigénicos con esta población neuronal.
La clínica suele ser subaguda, caracterizada por la aparición de parestesias, disestesias y, en general, trastornos sensitivos inicialmente localizados en regiones distales de extremidades, más habitualmente superiores (60%), bastante simétricas en su distribución, aunque en algo más de una tercera parte pueden ser asimétrica. Progresan en sentido centrípeto durante semanas o meses, intensificándose los déficits, que pueden incluso ser la causa de un importante componente atáxico. Suele demostrarse arreflexia universal y, en muy raras ocasiones, asocian debilidad franca. No es infrecuente la asociación con otro proceso paraneoplásico frecuente, la encefalitis o la encefalomielitis.
Un dato de gran interés es la frecuente aparición de este proceso precediendo a la sintomatología tumoral durante meses y, a veces incluso años, lo que implica la necesidad de realizar un estudio amplio y profundo de búsqueda de la neoplasia original. En un porcentaje alto suelen aparecer títulos significativos de anticuerpos antinúcleo neuronal denominados anti-Hu, de gran especificidad. El pronóstico de esta enfermedad no suele ser bueno por cuanto el tratamiento de la neoplasia no suele modificar la evolución de la neuronopatía. El diagnóstico es clínico y electrofisiológico; en este último, se demuestra la presencia de una lesión axonal difusa y severa del componente sensitivo neuropático, con respeto casi absoluto del componente motor.
Polineuropatía sensitivo-motora paraneoplásicaParece relacionarse también con mecanismos inmunológicos no bien conocidos. Los tumores implicados más habituales son linfomas, tumores pulmonares de células pequeñas, adenocarcinoma pulmonar, cáncer prostático y renal. En este proceso se lesionan todos los componentes funcionales del nervio, produciéndose una agresión a todos los componentes histológicos pero predominantemente al axón. Se producen, por tanto, déficits difusos de predominio distal en extremidades y distribución simétrica. La progresión es centrípeta, provocando sintomatología sensitiva predominante pero en asociación con debilidad significativa. Igualmente se evidencia arreflexia universal.
Polineuropatía por paraproteinemiaLa presencia de proteína monoclonal de tipo inmunoglobulina (Ig) se relaciona con neuropatía frecuentemente. Las bandas monoclonales pueden ser IgM, IgG o IgA, desarrollando diferentes tipos de agresión, de tal modo que la IgM se relaciona con procesos desmielinizantes crónicos, mientras que el resto con desmielinización o axonotmesis. La paraproteinemia puede relacionarse con neoplasias (mielomas, etc.) o con bastante frecuencia no asociar enfermedad o hallazgos que pudieran permitir diagnósticos de otros procesos, por eso se ha venido denominando gammapatías monoclonales de significado incierto (MGUS, para los anglosajones). La patogenia de las formas IgM es inmunológica, pero no está tan clara en el resto de Ig.
Los procesos desmielinizantes son prácticamente indistinguibles de una CIDP, por eso es mandatorio en el cribado de una CIDP evaluar la posibilidad de paraproteinemia.
Un dato muy específico es la presencia de anticuerpos dirigidos contra glucoproteínas asociadas a la mielina (MAG), que aparecen en aproximadamente la mitad de los casos con IgM. Tienen gran importancia por la implicación pronóstica en el tratamiento, de tal manera que aquellas neuropatías MAG positivas responderán mejor a inmunoterapia. Asimismo la respuesta a tratamiento será más favorable en las formas de paraproteinemia IgG e IgA que las IgM.
El mieloma múltiple puede provocar neuropatía en el contexto de amiloidosis asociada con infiltración nerviosa directa, o por efectos metabólicos y tóxicos de la propia neoplasia. La neuropatía periférica aparece en el 10% de los casos, con mayor frecuencia como PNP axonal sensitivomotriz simétrica distal, con inicio y predominio de los déficits en las extremidades inferiores. Como en otros procesos, el tratamiento de la enfermedad tumoral no modifica el curso de la neuropatía. En algunos casos puede aparecer amiloidosis por depósito de trastirretina mutada, que provoca la aparición de polineuropatía grave en ancianos (enfermedad de Andrade o polineuropatía amiloidótica familiar), tratable mediante trasplante hepático de donante o trasplante«dominó».
El mieloma osteoesclerótico o síndrome de POEMS constituye menos de un 3% de todos los mielomas y se caracterizan por tener osteoesclerosis además de la asociación en la mitad de los casos con neuropatía periférica, junto a organomegalia, endocrinopatía, gammapatía monoclonal y afectación dermatológica. Algunos pacientes pueden presentar una única lesión lítica, o lesiones extramedulares, presentarse como enfermedad de Castleman o incluso no tener mieloma osteoesclerótico demostrable.
La neuropatía, como decimos, es muy frecuente y se comporta clínicamente como una CIDP. El tratamiento del tumor suele mejorar la evolución de la neuropatía, incluso la asociación con corticoterapia (tratamiento de la CIDP) y radioterapia local. En todo caso, la posibilidad de recidiva tumoral es alta.
Polineuropatía por vasculitisPueden ser entidades en las que el nervio sea una de las estructuras más afectadas. El ejemplo más característico, y además más frecuente, es la periarteritis nudosa (más del 60%). El nervio se afecta en forma de multineuritis o polineuropatía distal. El mecanismo habitual suele ser isquémico y, por tanto, la agresión será inespecífica a todas las estructuras del nervio; la disfunción se expresa como daño predominantemente axonal. La clínica suele ser aguda, dolorosa, con déficits neurológicos en el territorio subsidiario del nervio. Progresa durante horas para estabilizarse y el pronóstico dependerá de la intensidad de la agresión, aunque en términos generales suele considerarse bueno a medio plazo.