Uno de los errores más frecuentes para los no familiarizados con la Geriatría es creer que la edad es una enfermedad, y que hay enfermedades propias de la vejez, si bien los geriatras sabemos que esta creencia no tiene fundamento científico ni se ajusta a la realidad1,2. En el caso de la insuficiencia renal crónica (IRC) dependiendo de los criterios de valoración, afectaría al 7,2% de la población española a los 30 años, y entre el 23,45 y el 35,7% en los mayores de 64 años. Si aceptamos este criterio, en España habría aproximadamente 1.795.000 personas de más de 60 años clasificadas como insuficientes renales2, cifra absolutamente errónea.
En nuestra opinión, la causa de este error es tanto el desconocimiento de la fisiología del proceso de envejecimiento en general y del renal en particular, como los criterios utilizados para la definición de enfermedad.
Comenzando por la fisiología renal, se ha tomado el filtrado glomerular (FG) como única función valorable olvidando que el cometido asignado el riñón en el organismo es el de mantener el equilibrio del medio interno, para lo cual, además del FG son necesarias otras funciones (tabla 1).
Funciones renales
| Ajuste del balance de líquidos |
| Ajuste del balance de electrolitos |
| Mantener el equilibrio ácido-base |
| Mantener el metabolismo mineral calcio-fósforo |
| Modular síntesis de eritropoyetina |
| Catabolismo en los túbulos de algunas moléculas |
| Capacidad de reserva funcional |
| Eliminar productos provenientes del metabolismo |
| Filtrado glomerular |
Respecto al FG, sabemos que el FG acorde con la edad (FGAE) evoluciona a lo largo del ciclo vital desde 16-20ml/min/1,73m2 al nacimiento hasta 90-130ml/min/1,73m2 entre los 25-30 años, dependiendo de cada persona y desde esta edad en adelante, el FG se atenúa a razón de 0,8ml/min/1,73m2/año hasta los 70 años en que lo hace a razón de 1,05ml/min3–5. Por ello el FGAE puede calcularse según las formulas de la tabla 2.
Cálculo del filtrado glomerular acorde a la edad
| FGAE 25-70 años=FGO (óptimo a los 25-30 años)+20−0,8×edad años |
| FGAE>70 años=FGO (óptimo a los 25-30 años)+37,5−1,05×edad años |
FGAE: filtrado glomerular acorde a la edad; FGO: filtrado glomerular óptimo.
FGO=110ml/min/1,73m2 superficie corporal.
La segunda causa de error, y no menos importante, es el criterio utilizado para la definición de enfermedad. Hay 2 formas de definir la enfermedad, la primera está basada en el valor crítico, la segunda en el valor de referencia asociado a parámetros de salud.
El valor crítico es la cifra que marca estadísticamente mayor probabilidad de morbimortalidad del individuo sin tener en cuenta la edad. El valor de referencia asociado a parámetros clínicos de «buena salud»6 se obtiene de los datos de personas sanas, en nuestro caso sin enfermedad renal. En este último, el médico establece la ausencia de enfermedad siendo los datos de estas persona sanas las evaluadas.
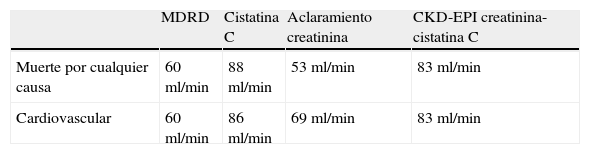
Respecto al valor crítico, se acepta universalmente que un FG estimado (FGe) menor de 60ml/min/1,73m2 clasifica a las personas como insuficientes renales sin tener en cuenta el FGAE ni la presencia de otros signos y síntomas presentes en el IRC como anemia, hiperfosfatemia, acidosis e hipocalcemia7. Como en muchas personas etiquetadas como portadores de IRC no aparecen ninguno de los signos y síntomas de IRC, se ha argumentado que FG<60ml/min/1,73m2 conllevan mayor morbilidad cardiovascular, aumento de la mortalidad o aparición de enfermedad renal terminal8, sin embargo, es interesante reseñar que, actualmente, no se conoce de qué manera o en qué grado un FG<60ml/min per se (en ausencia de hipertensión, diabetes u otras enfermedades asociadas) constituye o no un factor de riesgo independiente para llegar a desarrollar una IRC terminal, y lo que es mucho más significativo, si es o no reversible y prevenible en personas mayores de 70 años. Sin embargo un «valor crítico» eGFR<60ml/min/1,73m2 como factor de riesgo independiente para desarrollar en el futuro una insuficiencia renal crónica se encuentra en tela de juicio8–11, hasta tal punto que Shlipak et al. concluyen que el valor del FG a partir del cual aparecen complicaciones cardiovasculares y renales, depende del método utilizado para su estimación12 (tabla 3).
Filtrado glomerular estimado a partir de los cuales aumenta la morbimortalidad cardiovascular y renal según el método de obtención
| MDRD | Cistatina C | Aclaramiento creatinina | CKD-EPI creatinina-cistatina C | |
| Muerte por cualquier causa | 60ml/min | 88ml/min | 53ml/min | 83ml/min |
| Cardiovascular | 60ml/min | 86ml/min | 69ml/min | 83ml/min |
CKD-EPI: Chronic Kidney Disease Epidemiology Collaboration; MDRD: Modified Diet in Renal Disease.
La creatinina se filtra por el glomérulo reabsorbiéndose y secretándose en los túbulos, de manera que entre un 15 y un 30% de la creatinina presente en la orina proviene de la secreción tubular13,14. El manejo renal de creatinina difiere entre jóvenes y viejos sanos15. Por ello, cada vez más investigadores advierten que la creatinina no es un marcador fiable para determinar el FG en todos los casos.
Aclaramiento de creatinina en ancianosSalvo excepciones, la mayoría de los autores aceptan que el FG disminuye con la edad, aunque algunos estudios cuestionan que el descenso del FGe como aclaramiento de creatinina en orina de 24h sea universal. En el Baltimore Longitudinal Study, se observó que 92 de los 254 sujetos no sufrieron reducción en el aclaramiento de creatinina, e incluso algunos aumentaron sus valores16,17.
Fórmulas usadas para estimar el filtrado glomerularComo el estudio de aclaramientos renales en orina de 24h requiere la recogida y medida exacta de orina de 24h es muy tedioso y no siempre factible y fiable en ancianos por la presencia de síndromes geriátricos (incontinencia urinaria, deterioro cognitivo), se propusieron otros métodos para estimar el FG sin necesidad de recogida de orina, todos ellos basados en los valores de creatinina plasmática, que, naturalmente viene condicionada tanto por la síntesis endógena como por el manejo renal de creatinina que difiere según edad y estado de hidratación entre otros factores, como hemos comentado15. Entre las más conocidas se encuentran las de Kampmann et al.18, Rowe et al.19 Cockcroft y Gault20, Nicollet al.21, Keller22, Nankivell et al.23, Baracskay et al.24, Modified Diet in Renal Disease (MDRD)25 y Chronic Kidney Disease Epidemiology Collaboration (CKD-EPI)26. Es sorprendente que a pesar que las fórmulas del grupo MDRD no están validadas para personas sanas de cualquier edad, en mayores de 70 años con o sin IRC, embarazo y pacientes muy enfermos27, se ha impuesto como patrón para estimar el FG. Respecto a otras fórmulas para el cálculo del FGe (tabla 4) son válidas en general, aunque la variación individual en personas mayores puede ser considerable28.
Fórmulas utilizadas para estimar el filtrado glomerular
| Año | Autor | Fórmula de FG (ml/min/1,73m2) |
| 1973 | Jellife | FG=98−[0,8×(edad−20)/creat. sérica×(superf. corporal/1,73)×[0,9 si mujer] |
| 1974 | Kampmann | FG=creat. orina×peso×100/creat. sérica |
| 1976 | Rowe | FG=133−0,64×edad |
| 1976 | Cockcroft | FG=(140−edad)×peso (×0,85 si mujer)/(creat. sérica×72) |
| 1987 | Keller | FG=130−edad |
| 1993 | Walser | FG=7,57×(creat. sérica mmol/l)−1−0,103×edad+0,096×peso−6,66 |
| 1995 | Nankivell | FG=6,7/creat. sérica (mmol/l)+0,25×peso−0,5×urea−0,01×altura2+35(25 si mujer) |
| 1997 | Baracskay | FG=1/2[100/creat. sérica]+88−edad |
| 1999 | MDRD | FG=170×[creat. sérica]–,999×[edad]−0,175×[0,762 si mujer]×[1,180 afroamericano]×[BUN]−0,170×[Alb]+0,318 |
| 2004 | MDRD-4 | FG=186,3×[creat. sérica]−1,154×[edad]−0,203×[0,742 si mujer]×[1,142 si afroamericano] |
| 2005 | MDRD-IDMS | FG=175×(creatinina/88,4)−1,154×(edad)−0,203×(0,742 si mujer)×(1,210 si raza negra) |
| 2007 | MDRD-6 | FG estimado=170×(creatinina/88,4)−0,999×(edad)−0,176×(urea×2,8)−0,170×(albúmina/10)0,318×(0,762 si mujer)×(1,180 si raza negra) |
| 2009 | CKD-EPI | FG=141×min. (Scr/κ, 1)α×máx. (Scr/κ, 1)−1,209×0,993edad×1,018 (si mujer) Donde Scr es creatinina sérica, k es 0,7 para mujeres y 0,9 para varones, α es −0,329 para mujeres y −0,411 para varones |
| 2010 | DAF | FG=80/creat. sérica (70 si mujer) |
| 2014 | Gregori-Macías | FG=480,79/(creat. sérica)0,513×1,008 edad×1,003 urea×Peso0,2989 |
CKD-EPI: Chronic Kidney Disease Epidemiology Collaboration; creat.: creatinina; DAF:Fórmula de Damiandopoulos; FG: filtrado glomerular; MDRD: Modified Diet in Renal Disease; MDRD-IDMS: Modified Diet in Renal Disease-Isotope Dilution Mass Spectrometry.
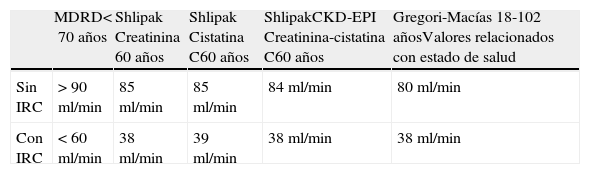
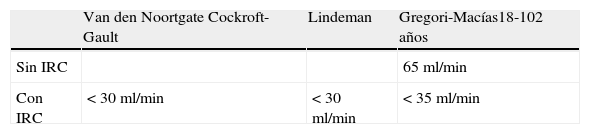
En la insuficiencia renal crónica, además de un FGe<60ml/min según recomendaciones de la National Kidney Foundation-Kidney Disease Outcomes Quality Initiative (NFK-KDOQI)29 tienen que alterarse otras funciones (tabla 1). Por ello, el diagnostico de IRC utilizando el FGe<60ml/min como único criterio ha sido diana de muchas críticas desde su publicación, siendo la más reciente la de Shlipak et al.12 que pone en evidencia la imprecisión de definir IRC basados en el valor crítico de FGe≤60ml en la población general y en los mayores de 70 años en particular (tablas 5 y 6).
Definición de IRC basados en valor crítico de filtrado glomerular estimado en la población general
| MDRD<70 años | Shlipak Creatinina 60 años | Shlipak Cistatina C60 años | ShlipakCKD-EPI Creatinina-cistatina C60 años | Gregori-Macías 18-102 añosValores relacionados con estado de salud | |
| Sin IRC | >90ml/min | 85ml/min | 85ml/min | 84ml/min | 80ml/min |
| Con IRC | <60ml/min | 38ml/min | 39ml/min | 38ml/min | 38ml/min |
IRC: insuficiencia renal crónica; MDRD: Modified Diet in Renal Disease.
Como acabamos de ver, existe una gran discrepancia según el método, fórmula y concepto usado para las estimaciones de FG y con ello un diagnóstico de IRC que puede resultar muy lejano a la realidad.
En el año 2012, fruto del trabajo de un grupo de investigación internacional multidisciplinar compuesto por geriatras, nefrólogos, cardiólogos, internistas y médicos de familia se obtuvo la fórmula HUGE30,31 para el rastreo poblacional de IRC, basada en datos referidos al «estado de salud» en vez de «valor crítico».
Esto no significa que las formulas MDRD o CKD-EPI no tengan utilidad ya que son, sin ninguna duda, válidas para la estadificación y el seguimiento de la progresión de IRC en los pacientes ya diagnosticados de insuficiencia renal crónica en adultos de menos de 70 años de edad. Sin embargo, el uso del FGe<60ml/min para el rastreo en pacientes sin diagnóstico conocido de IRC no solo es controvertido sino quizá desaconsejado32. Utilizando HUGE como método de cribado para IRC, en vez de MDRD, se evitaría que aproximadamente 1.800.000 personas mayores de 60 años en España (censo de población INE 2011)33 sean indebidamente clasificadas como IRC25,30 con la consiguiente repercusión sobre gestión de recursos sanitarios. Como sabemos, actualmente se recomienda remitir a todos los pacientes con FGe<60ml/min a una unidad de nefrología para confirmación diagnóstica, lo cual, teniendo en cuenta que solamente la primera consulta de nefrología con prueba de imagen y analítica tendría un coste medio aproximado de 151€34, supondría un gasto cercano a los 272 millones de euros, sin tener en cuenta el coste de la segunda consulta (91€) para confirmación o no de IRC, que añadiría otros 163 millones de euros (435 millones en total), los retrasos en listas de espera y los desplazamientos, a veces con un familiar que tiene que pedir permiso en el trabajo para acompañar al anciano a la consulta de Nefrología.
Si esto parece exagerado y lo analizamos por comunidades o incluso provincias, la estricta aplicación del MDRD en la población de Castilla y León supondría la consideración de 124.039 habitantes como portadores de ERC, el 17% de las 729.643 personas mayores de 60 años, mientras en Castilla-La Mancha la estimación nos llevaría a considerar a 79.589 personas portadoras de disfunción renal de un total de 468.171 mayores de 60 años y, en la provincia de Toledo, de un total de 148.890 habitantes, aproximadamente 25.300 personas serían clasificadas como insuficientes renales crónicos, lo que solo en esta provincia significaría un coste de 6 millones de euros en consulta especializada innecesaria.
Sin embargo, utilizando HUGE como método de cribado para IRC en vez de MDRD, se podría minimizar o contener la cifra aproximada de 1.800.000 personas mayores de 60 años en España (censo de población INE 2011)34 arbitrariamente clasificadas como IRC26,31.
ConclusionesCuatro son las conclusiones que podemos obtener del análisis de los datos expuestos:
- –
La primera, no confundir fórmulas de cribado con procedimientos diagnósticos.
- –
La segunda, no catalogar a un anciano con un FGe>60ml/min/1,73m2 como portador de IRC, en ausencia de confirmación por un médico. Ello lo excluiría de recibir tratamientos quirúrgicos o farmacológicos necesario para el paciente, pero contraindicado en insuficiencia renal.
- –
La tercera, no excluir de ensayos clínicos a personas mayores catalogadas de IRC con el criterio único de FGe>60ml/min/1,73m2. Ya que nos privaría de adquirir experiencia y evidencia terapéutica.
- –
La cuarta, no remitir a consultas especializadas de Nefrología a todas las personas añosas con un FGe>60ml/min/1,73m2 evitando así un dispendio considerable de recursos sanitarios y sociales.
Para prevenir los riesgos de asociar FGe disminuido con insuficiencia renal, sugerimos:
- 1.
Primero, utilizar para el rastreo de IRC herramientas distintas del FGe basado en la creatinina sérica, como por ejemplo la fórmula HUGE32.
- 2.
Segundo, que a toda persona con FGAE disminuido y/o HUGE sugestiva de padecer IRC, se le solicite calcemia, fosforemia y hemograma. Si además del FGAE bajo encontrásemos hipocalcemia, hiperfosfatemia y anemia deberíamos remitirla a la consulta de Nefrología para aquilatar el diagnóstico de IRC si las condiciones del paciente geriátrico así lo requieren.