El objetivo de este trabajo es reportar los resultados a corto plazo y las complicaciones de la artroplastia de superficie del húmero proximal (HemiCup®) en pacientes tratados por necrosis ósea avascular.
Material y métodosEntre 2010 y 2014 fueron evaluados 9 pacientes a los que se les realizó una artroplastia de superficie del húmero proximal. Todos los pacientes fueron tratados por necrosis ósea avascular. El seguimiento promedio fue de 44 meses (mínimo 24 meses). La edad promedio fue de 47 años (rango 32-57 años). Los pacientes fueron evaluados cínica y radiológicamente. Se reportaron las complicaciones.
ResultadosLos pacientes presentaron una mejoría significativa en los scores funcionales y la movilidad entre el preoperatorio y el último control en el seguimiento. El score de Constant mejoró de 35 a 79 puntos (p<0,001), el score de ASES mejoró de 31 a 76 puntos (p<0,001), la flexión anterior y la rotación externa mejoraron de 101 a 150° (p<0,001) y de 24 a 45° (p<0,001), respectivamente. Un paciente presentó desgaste sintomático en la glena durante el seguimiento, requiriendo una cirugía de revisión.
ConclusiónEn nuestra serie, la artroplastia parcial de superficie del húmero proximal (HemiCup®) demostró una mejoría significativa en los scores funcionales y la movilidad en pacientes tratados por necrosis ósea avascular, con un seguimiento promedio de 44 meses.
The aim of this study was to report the short-term results and complications of partial humeral head resurfacing (HemiCup®) in patients treated by avascular necrosis.
Material and methodsBetween 2010 and 2014, 9 patients who underwent partial resurfacing of humeral head were evaluated. All the patients were treated by avascular necrosis. The mean follow-up was 44 months (minimum 24 months). The average age was 47 years (range 32-57 years). The patients were evaluated clinically and radiologically. Complications were reported.
ResultsThe patients had a significant improvement in functional scores and mobility between the pre-operative and last follow-up control. The Constant score improved from 35 to 79 points (P<.001), ASES score improved from 31 to 76 points (P<.001), forward flexion and external rotation improved from 101 to 150° (P<.001), and from 24 to 45° (P<.001), respectively. One patient presented symptomatic glenoid wear during follow-up, requiring revision surgery.
ConclusionIn our patients treated by avascular necrosis, the partial resurfacing of humeral head (HemiCup®) demonstrated a significant improvement in functional scores and mobility with an average follow-up of 44 months.
La necrosis ósea avascular (NOA) del húmero proximal es una condición poco frecuente. Puede desarrollarse espontáneamente, sin una etiología aparente (primaria), o, como en la mayoría de los casos, en asociación con alguna condición específica o factor de riesgo (secundaria), siendo entre estas el uso de corticoides y la necrosis postraumática las causas más frecuentes1–4.
Los síntomas clásicos incluyen dolor, rigidez, pérdida de movilidad y disminución de la función. Los diferentes estadios de la NOA del húmero proximal son clasificados por Cruess2 (tabla 1) mediante la modificación de la clasificación de Ficat para NOA de fémur proximal5.
Estadios de Cruess. Necrosis ósea avascular del húmero proximal
| Estadio | Descripción |
|---|---|
| 1 | Húmero proximal con aspecto normal en Rx, solo evidente en RMN |
| 2 | Esclerosis subcondral del húmero proximal, sin cambios en la esfericidad de la cabeza |
| 3 | Alteración estructural del hueso y colapso del hueso subcondral, pérdida de la esfericidad |
| 4 | Colapso extenso del hueso subcondral, superficie glenoidea indemne |
| 5 | Compromiso de la cabeza humeral y la superficie glenoidea. Artrosis secundaria |
RMN: resonancia magnética nuclear; Rx: radiografía.
El tratamiento de la NOA del húmero proximal difiere según el estadio evolutivo de la enfermedad. Los pacientes en estadios iniciales, en los que no existe colapso subcondral (Cruess 1 y 2), son candidatos tanto a un tratamiento no quirúrgico como a una cirugía de descompresión del foco de necrosis mediante perforaciones, dependiendo de la evolución clínica6,7.
En estadios avanzados (Cruess 3-5), se requiere algún tipo de reemplazo protésico. Los pacientes con compromiso avanzado humeral, sin compromiso glenoideo (Cruess 3-4), son candidatos a una hemiartroplastia. Cuando existe afectación de la superficie glenoidea (Cruess 5) la indicación es una artroplastia total de hombro.
Los modelos protésicos tradicionales, con vástago endomedular, han sido ampliamente utilizados en este grupo de pacientes con buenos resultados8–10. Si bien actualmente permiten mayor versatilidad en el acoplamiento entre la cabeza humeral y el vástago, un condicionante teórico de este tipo de implantes es su capacidad limitada de reproducir con precisión la anatomía del húmero proximal11,12, teniendo en cuenta que es un sitio anatómico que presenta gran variabilidad en la inclinación, retroversión y centro de rotación, no solo entre diferentes pacientes, sino también entre ambos hombros del mismo paciente13.
La utilización de reemplazos de superficie, total o parcial, han ganado popularidad ya que permiten ahorrar capital óseo, con la ventaja de restaurar adecuadamente la anatomía normal del húmero proximal4,14–17.
El objetivo de este trabajo es reportar los resultados funcionales y las complicaciones de una serie de pacientes tratados por NOA con un reemplazo parcial de superficie del húmero proximal utilizando el sistema HemiCup®, con un seguimiento mínimo de 2 años.
Material y métodosEntre junio de 2010 y junio de 2014, 10 pacientes fueron tratados por NOA del húmero proximal con un reemplazo parcial de superficie utilizando el sistema HemiCup®, Arthrosurface®. Dos pacientes presentaban compromiso bilateral, aunque en el momento del análisis habían sido tratados solo de un hombro. Un paciente fue perdido durante el seguimiento, siendo incluidos en la serie 9 pacientes (9 prótesis). La edad promedio fue de 47 años (rango 32-57 años). Cinco procedimientos fueron realizados en mujeres y 4 en hombres. Siete prótesis fueron colocadas en el hombro derecho y 2 en el hombro izquierdo. El miembro dominante estuvo involucrado en 7 casos. El seguimiento mínimo fue de 24 meses. Los pacientes fueron clasificados mediante radiografías convencionales y resonancia magnética aplicando la clasificación de Cruess para la NOA de húmero proximal2. Siete pacientes fueron clasificados como Cruess grado 3 y 2 pacientes fueron clasificados como Cruess grado 4. Todos los pacientes presentaban una pérdida de capital óseo del húmero proximal menor del 40% medido mediante resonancia magnética18. La etiología de la NOA fue secundaria a corticoides en 7 casos e idiopática en 2 pacientes (tabla 2).
La indicación quirúrgica en todos los casos fue el dolor y la limitación funcional en el hombro afectado, que no respondía al tratamiento no quirúrgico (fisioterapia, medicación, modificación de la actividad) y que afectaba negativamente las actividades de los pacientes en la vida diaria.
Todos los procedimientos fueron realizados bajo anestesia combinada (bloqueo interescalénico y anestesia general) por el mismo cirujano experimentado (MR).
Técnica quirúrgicaLa posición en silla de playa se utilizó en todos los casos. A través de un abordaje deltopectoral se identificó el intervalo rotador, abordando la articulación mediante la desinserción del tendón del subescapular. Previa capsulotomía, se realizó la luxación controlada de la cabeza humeral. Una vez identificada la lesión, se realizó la medición en el plano anteroposterior y lateral, como también la profundidad de la misma mediante la utilización de guías específicas. Siguiendo la técnica quirúrgica se colocó el tornillo central. Una vez determinado el tamaño del implante, se realizó el fresado de la cabeza humeral. Finalmente, se colocó el componente definitivo impactándolo al tornillo central, mediante un sistema de cono Morse.
El subescapular fue reinsertado anatómicamente mediante puntos transóseos. En todos los pacientes se realizó tenodesis de la porción larga del bíceps. En un paciente se realizó reparación simultánea del supraespinoso.
En todos los casos se utilizaron prótesis de 40mm.
Los pacientes fueron inmovilizados con un cabestrillo durante 4 semanas, permitiendo movimientos de flexoextensión del codo y la muñeca, limitando la flexión anterior y la abducción del hombro. Después del primer mes todos los pacientes comenzaron un régimen de rehabilitación con una duración de 6-8 semanas. El regreso a las actividades se llevó a cabo progresivamente según lo tolerado.
Todos los pacientes fueron evaluados en el pre y postoperatorio por un examinador que no era el cirujano tratante. Se analizaron los scores funcionales (score de Constant y ASES)19,20, la escala analógica visual del dolor y la movilidad entre el preoperatorio y el último control en el seguimiento. Se realizaron radiografías en el plano anteroposterior, escapular en «Y» y axilar. Se evaluó la aparición de signos de aflojamiento o erosión glenoidea, aplicando los criterios descritos por Rispoli et al.21, como: ausente (sin signos de desgaste glenoideo), leve (horadación parcial o total de la placa subcondral), moderada (desgaste que se aproxima al proceso lateral de la coracoides), severa (desgaste medial al proceso lateral de la coracoides).
Las variables de resultado de Constant, ASES y movilidad (medida en grados) fueron consideradas como variables continuas y se presentan con medidas de tendencia central y dispersión. Las variables de nuestra muestra se ajustaban a una distribución normal, por lo tanto, los resultados se describen como media y desviación estándar.
La comparación entre los resultados pre y postoperatorios se realizó mediante la prueba t de Student, con un nivel de significación establecido en p<0,05. Se utilizó el software STATA versión 13.0 para el análisis estadístico.
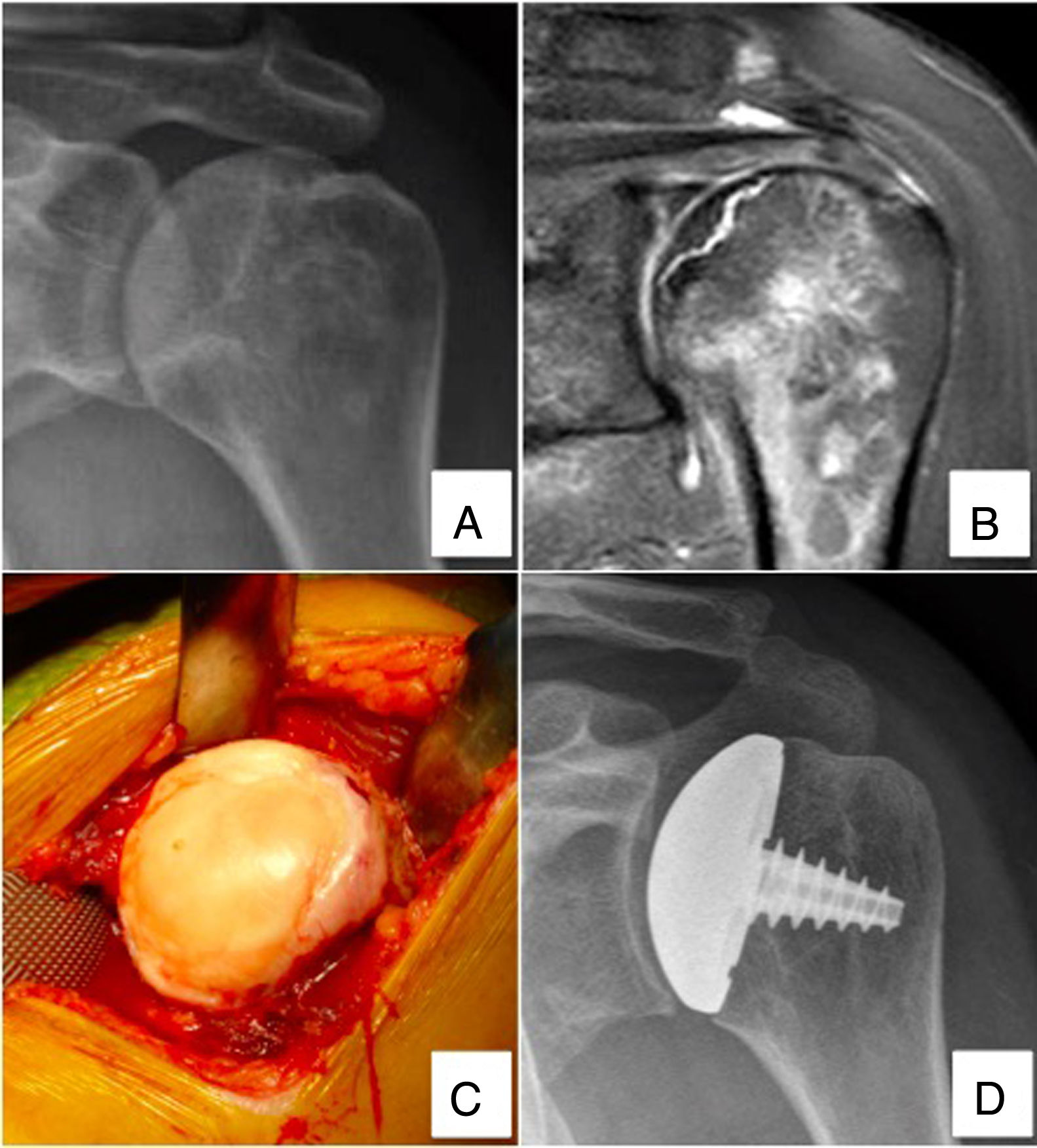
ResultadosNueve prótesis de superficie del húmero proximal fueron analizadas en pacientes tratados por NOA (fig. 1).
Paciente de 51 años con diagnóstico de NOA de húmero proximal tratado con artroplastia parcial de superficie (HemiCup®). A y B) Radiografía y resonancia magnética de hombro izquierdo donde se evidencian signos de colapso subcondral e indemnidad de la superficie glenoidea (Cruess 3). C) Imagen intraoperatoria donde se evidencia la pérdida de la esfericidad del húmero proximal. D) Radiografía de control a los 52 meses postoperatorios, que muestra una buena evolución.
El seguimiento promedio fue de 44 meses (rango 24-62 meses).
Según la clasificación de Rispoli et al.21, todos los pacientes se encontraban sin signos de desgaste glenoideo en el momento de la cirugía.
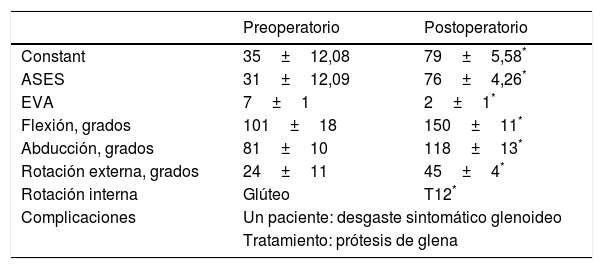
Los pacientes presentaron una mejoría significativa en los scores funcionales entre el preoperatorio y el último control en el seguimiento (tabla 3). El score de Constant mejoró de un valor de 35±12,08 en el preoperatorio a un valor de 79±5,58 (rango 70-88) en el postoperatorio (p<0,001). El score de ASES mejoró de un valor de 31±12,09 (rango 16-43) en el preoperatorio a un valor de 76±4,26 (rango 70-100) en el postoperatorio (p<0,001). En la escala visual analógica del dolor los valores mejoraron de 7,3±0,8 (rango 6-9) en el preoperatorio a 2,2±1 (rango 0-3) en el postoperatorio (p<0,001).
Resultados funcionales y complicaciones
| Preoperatorio | Postoperatorio | |
|---|---|---|
| Constant | 35±12,08 | 79±5,58* |
| ASES | 31±12,09 | 76±4,26* |
| EVA | 7±1 | 2±1* |
| Flexión, grados | 101±18 | 150±11* |
| Abducción, grados | 81±10 | 118±13* |
| Rotación externa, grados | 24±11 | 45±4* |
| Rotación interna | Glúteo | T12* |
| Complicaciones | Un paciente: desgaste sintomático glenoideo | |
| Tratamiento: prótesis de glena | ||
EVA: escala visual analógica del dolor.
Seguimiento promedio 44 meses (rango 24-62).
En el examen físico la movilidad mejoró significativamente. La flexión anterior aumentó desde un promedio de 101±18° a 150±11°. La abducción aumentó desde un promedio de 81±10° a 118±13°. La rotación externa mejoró desde un promedio de 24±11° a 45±4°. La rotación interna mejoró desde una movilidad promedio en el preoperatorio nivel «glúteo» hasta un promedio nivel «T12» en el postoperatorio (p<0,001).
En la evaluación radiológica, un paciente presentó signos leves de desgaste glenoideo21, asociado a reaparición del dolor y limitación funcional a los 38 meses de la artroplastia de superficie, y habiendo presentado más de 2 años de buena evolución en cuanto al dolor y la función. La reaparición de los síntomas fue interpretada como secundaria al desgaste glenoideo, realizándose una cirugía de revisión, con la colocación del componente protésico glenoideo. El paciente presentó una buena evolución luego del segundo procedimiento.
DiscusiónLos resultados del seguimiento a corto plazo de esta serie de pacientes con estadios avanzados de NOA (Cruess 3 y 4), sin compromiso glenoideo, tratados con reemplazo parcial de superficie de húmero proximal mediante el sistema HemiCup®, demuestran una mejoría significativa en los scores funcionales y la movilidad con un seguimiento promedio de 44 meses.
Si bien la NOA de húmero proximal es una afección poco frecuente, se relaciona con dolor, rigidez, pérdida de movilidad y disminución de la función del hombro afectado.
En los estadios iniciales (Cruess 1 y 2) la literatura sostiene que estos pacientes son candidatos a un tratamiento no quirúrgico (observación, antiinflamatorios, kinesiología, infiltraciones) o a un procedimiento descompresivo con perforaciones, dependiendo de la evolución clínica6,7.
A medida que ocurre el colapso del hueso subcondral y el compromiso articular, el reemplazo protésico se convierte en la opción de tratamiento adecuada.
La mayoría de los trabajos publicados en la literatura sobre tratamiento quirúrgico de NOA de húmero proximal22 coinciden en que los pacientes incluidos se encuentran en la quinta década de la vida, siendo en estos casos la conservación del capital óseo, el desgaste de la superficie articular de la glena y las probables cirugías de revisión en el futuro aspectos fundamentales a considerar a la hora de elegir el implante.
Clásicamente se han utilizado modelos protésicos convencionales endomedulares en pacientes con estadios avanzados NOA de húmero proximal con buenos resultados8,10.
Si bien estas series demuestran mejorías significativas en scores funcionales y en la movilidad, se relacionan con un porcentaje considerable de complicaciones, llegando en algunos casos hasta el 30%8, entre ellas las lesiones de manguito rotador, la inestabilidad, el desgaste glenoideo en las hemiartroplastias y el aflojamiento del componente glenoideo en las prótesis totales.
Al analizar los resultados de la hemiartroplastia utilizando prótesis con vástago en NOA, Smith et al. reportaron una serie de 32 pacientes con un seguimiento promedio de 12 años, todos tratados por NOA del húmero proximal relacionada con corticoides. Los autores describen que si bien este procedimiento se asocia a una mejoría significativa en los scores funcionales y en la movilidad, el 42% de los pacientes referían no estar satisfechos, un 38% con dolor moderado a severo, como consecuencia del desgaste glenoideo sintomático3.
Esta limitación asociada al desgaste glenoideo sintomático ha sido descrita por otros autores al analizar los resultados de la hemiartroplastia utilizando prótesis con vástago en NOA del húmero proximal9,23.
Como una alternativa de preservación del capital óseo, las artroplastias de superficie ganaron popularidad, alcanzando resultados similares a los modelos con vástago endomedular cementado24,25.
Levy et al.26, en una serie de 49 pacientes tratados con artroplastias de superficie con un seguimiento mínimo de 10 años, describieron un porcentaje de satisfacción del 82% entre sus pacientes, siendo 19 de estas prótesis indicadas por NOA, logrando este grupo los mejores resultados funcionales.
El reemplazo parcial de superficie de húmero proximal es otra alternativa protésica en este grupo de pacientes. Está diseñado para tratar las lesiones focales del húmero proximal, realizando un reemplazo parcial de la superficie articular.
Estudios biomecánicos describen que el reemplazo parcial de superficie restaura con mayor precisión el centro de rotación de la cabeza humeral en comparación con la hemiartroplastia, con menos sobrecarga excéntrica en la glena, disminuyendo su desgaste14.
El reemplazo parcial de superficie elimina la restricción ocasionada por el acoplamiento estático entre la cabeza humeral protésica y el vástago endomedular, y a su vez permite el posicionamiento y la medición del componente protésico tomando como referencia el cartílago articular remanente.
Existen escasos reportes publicados sobre los resultados de este tipo de modelo protésico en NOA de húmero proximal.
Recientemente, Franceschi et al.22 realizaron una revisión sistemática de la literatura sobre pacientes con NOA del húmero proximal, tratados quirúrgicamente. Fueron incluidos en el análisis 12 trabajos, 3 de los cuales analizan pacientes tratados con cirugía de descompresión, 8 analizan los resultados sobre pacientes tratados con hemiartroplastia o prótesis total de hombro y solo uno de ellos4 analiza pacientes tratados con prótesis de superficie. Los autores concluyen que los trabajos disponibles presentan un escaso seguimiento, resaltando este aspecto como una limitación significativa.
En 2009, Uribe y Botto-van Bemden4 reportaron los resultados de 11 pacientes con diagnóstico de NOA de húmero proximal tratados con reemplazo parcial de superficie (HemiCup®). Con un seguimiento promedio de 30 meses los pacientes alcanzaron buenos y excelentes resultados en los scores funcionales, con 142° de flexión anterior y 46° de rotación externa, resultados similares a los de nuestra serie. A diferencia de nuestro análisis, sus pacientes no presentaron complicaciones.
Sweet et al.27 analizaron a 19 pacientes tratados con el sistema HemiCup® (4 por NOA y 15 por artrosis primaria), concluyendo que la artroplastia parcial del húmero proximal es un procedimiento efectivo en cuanto al tratamiento del dolor y la función, con un alto índice de satisfacción por parte de los pacientes, reportando un 15% de complicaciones en 32 meses de seguimiento promedio, todas estas en pacientes tratados por artrosis primaria.
Mansat et al.28, en un análisis clínico y radiológico de 61 pacientes tratados con prótesis de superficie por diferentes diagnósticos, con un seguimiento promedio de 36 meses, concluyeron que si bien este tipo de prótesis reproduce la anatomía normal del húmero proximal, sus pacientes presentaron una tendencia al desgaste glenoideo, con reaparición del dolor en el 17% y requiriendo una cirugía de revisión a una prótesis total de hombro el 8% de los casos. Cabe destacar que esta tendencia al desgaste glenoideo probablemente se deba a la indicación quirúrgica, ya que todos los pacientes que presentaron complicaciones fueron operados por artrosis primaria, asociado a una tendencia a la colocación en varo del componente protésico humeral demostrada por los autores. Ninguno de los pacientes operados por NOA presentaron complicaciones.
Si bien un punto fundamental a analizar sería la comparación de los modelos protésicos con vástago y los modelos de reemplazo de superficie en cuanto al desgaste glenoideo, actualmente no existe evidencia suficiente en la literatura sobre series que analicen los resultados en pacientes tratados por NOA utilizando modelos protésicos con vástago actuales, los cuales permiten una mayor versatilidad en la colocación del componente cefálico, y por otro lado, las series que analizan prótesis de superficie son limitadas en cuanto al seguimiento y el número de pacientes. Otro punto fundamental al considerar el alto porcentaje de complicaciones publicadas en la serie de Smith et al.3, en relación con el desgaste glenoideo, es que este trabajo reporta los resultados de la hemiartroplastia en NOA a largo plazo (12 años de promedio). Al existir escasa evidencia sobre los resultados a largo plazo de otros modelos protésicos, realizar conclusiones sobre este punto sería precipitado.
Nuestro trabajo presenta la limitación de analizar un escaso número de pacientes, por un periodo de seguimiento acotado hasta el presente. Sin embargo, al ser la NOA una afección poco prevalente, esta serie se suma a los escasos reportes similares publicados previamente en la literatura, con lo cual, creemos que contribuye a la interpretación de los resultados de este tipo de modelo protésico en este grupo de pacientes. Si bien existe la necesidad teórica de realizar estudios prospectivos y aleatorizados, la baja frecuencia de esta dolencia fundamenta la falta de los mismos debido a sus dificultades metodológicas.
En nuestra serie, la artroplastia parcial de superficie del húmero proximal (HemiCup®) demostró una mejoría significativa en los scores funcionales y en la movilidad en pacientes tratados por NOA, con un seguimiento promedio de 44 meses.
Nivel de evidenciaNivel de evidencia iv.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.