Durante las últimas décadas se han sucedido pasos importantes en el diseño de los componentes de la artroplastia parcial de hombro. El mayor conocimiento de la anatomía mediante estudios que aplican las últimas tecnologías digitales ha permitido resaltar las principales características morfológicas y la variabilidad entre individuos de las estructuras sustituidas, permitiendo la fabricación de implantes más anatómicos. La posibilidad de seleccionar la orientación y tamaño de los componentes cefálicos, los métodos de fijación de los vástagos, los diseños que prescinden de estos últimos y las prótesis con filosofías diferentes a la imitación de la anatomía normal ponen a disposición del cirujano de hombro una gran variedad de opciones para las diferentes indicaciones de artroplastia parcial. Como en otros campos de nuestra especialidad, es necesario tener presentes los aspectos básicos del diseño y conocer los principales estudios clínicos que avalan las diferentes posibilidades que el mercado nos ofrece, teniendo siempre presente que la industria evoluciona más deprisa que el conocimiento científico-clínico.
En el presente trabajo se exponen conceptos fundamentales para la utilización de la prótesis parcial de hombro en diferentes indicaciones, discutiendo su utilización frente a otros tipos de implante, especialmente la prótesis total.
HISTORIA Y DISEÑO
Recuerdo histórico1
La primera prótesis parcial de hombro fue implantada en París por el cirujano francés Jules-Émiles Pean en 1893. Este implante estaba hecho de goma y platino. Tuvo que ser retirado dos años después de la cirugía tras la aparición de una infección crónica. El segundo intento fue hecho por F. Koenig en 1914. Su prótesis estaba fabricada de marfil. Posteriormente no hubo ningún nuevo intento hasta casi 40 años después.
Entre 1951 y 1952 se fabricaron prótesis de resina (Boron, Kevin, Judet) y de vitalio (Krueger). Al mismo tiempo, Charles S. Neer II desarrolló la prótesis moderna monobloque, teniendo como indicación la fractura de húmero proximal. En Europa (Scales y Lettin en 1969, Reeves y Jobbins en 1971, Zippel en 1972, Kölbel en 1972 y Kessel en 1973), al igual que en Estados Unidos (Neer y otros), se desarrollaron diferentes diseños para prótesis de hombro. En esos momentos no había mucho interés en este tipo de implante debido al alto índice de aflojamiento que se producía (mayor del 50%).
Hemiartroplastia: generaciones protésicas
Gracias al Dr. Neer la prótesis de hombro empezó a tener mayor difusión cuando comenzó a utilizar diseños no constreñidos. Neer creía que los resultados serían mejores imitando la anatomía normal del hueso, aunque su prótesis sólo disponía de un número limitado de tallas. Todavía hoy, en algunos sitios se usa el modelo Mark II, que el Dr. Neer desarrolló a principios de los setenta.
Los implantes de segunda generación aparecieron en el mercado a finales de los años ochenta (modelos Biomet, Cofield y Global). Tenían como característica principal la modularidad y su objetivo era intentar imitar los diferentes tamaños del canal humeral, pero se toparon con dos problemas importantes1. En primer lugar, la cabeza estaba mal posicionada tanto en el plano vertical como en el horizontal. Esto era consecuencia de la geometría fija del implante; la mayoría era sin cementar, press-fit, por lo que la posición del vástago condicionaba la posición final de la cabeza provocando el desplazamiento de su centro de rotación. En segundo lugar, con mucha frecuencia se sobredimensionaba el tamaño del módulo cefálico debido, por una parte, a la diferente relación entre la profundidad de inserción de la prótesis y el diámetro de la misma, y, por otra, al espacio que quedaba entre la osteotomía y la cabeza protésica.
A pesar de la modularidad, las prótesis de segunda generación seguían sin replicar la anatomía, llevando a problemas que incluso no se habían visto con el modelo de Neer1; en especial, la sobredimensión de la cabeza protésica llevaba a la erosión de la glenoides precozmente, y añadía exce-siva tensión a la articulación con riesgo de ruptura del manguito rotador y aparición de la inestabilidad anterior. Además, el desplazamiento del centro de rotación hacia arriba daba lugar al cambio de función de los músculos infraespinoso y subescapular, que se convertían en músculos aductores, sobrecargando el supraespinoso. Por otro lado, el exceso de retroversión daba lugar al desgaste de la región posterior de la glenoides, lo que ocasionaba dolor.
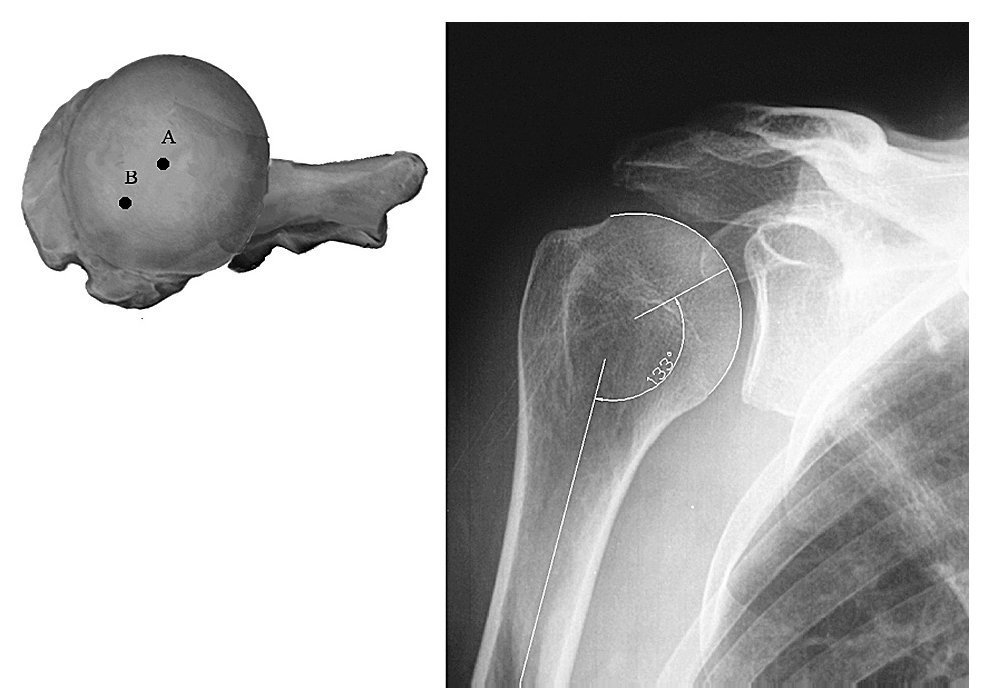
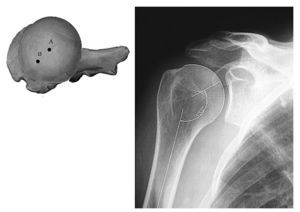
La primera prótesis de tercera generación fue diseñada por Boileau y Walch en Francia a principios de los noventa. Este tipo de prótesis se caracteriza por la réplica de las características y medidas tridimensionales del hueso, estudiadas por diferentes autores mediante el análisis de huesos de cadáveres con técnicas tridimensionales de identificación de superficies asistidas por ordenador2-4. Así se desarrolló el concepto de "reconstrucción anatómica del húmero proximal", que hace especial hincapié en las características anatómicas de cada paciente. Sus principales aportaciones son la posibilidad de adaptación de la prótesis a diferentes parámetros que reproducen las características anatómicas del hueso normal (fig. 1):
Figura 1.(A) Visión superior del húmero proximal, en la que el punto A representa el centro de la superficie articular y el punto B representa la proyección del eje de la diáfisis. Obsérvese que el centro de la superficie articular está situado posteriormente (offset posterior) y medialmente (offset medial) al eje de la diáfisis. Nótese la representación de la superficie articular dirigida hacia posterior con respecto al eje interepicondíleo (retroversión). (B) Radiografía anteroposterior en la que se representa el ángulo de inclinación céfalo-diafisario, en este caso de 133°.
1) Offset posterior: el centro de la superficie articular está desplazado hacia posterior con respecto al eje de la diáfisis.
2) Offset medial: el centro de la superficie articular está desplazado hacia medial con respecto al eje de la diáfisis
3) Variabilidad en la orientación de la superficie articular en el plano horizontal (retroversión entre 9 y 30°, con una media de 20) y el vertical (ángulo entre el eje de la diáfisis humeral y el eje de la orientación de la superficie articular, también llamado ángulo de inclinación, que oscila entre 123 y 135°, con 130° de media).
Hemiartroplastia: fijación del vástago
La mayoría de los diseños protésicos ofrece una versión cementada y otra no cementada. La fijación cementada se relaciona con una menor aparición de líneas radiolucentes entre el hueso y el cemento5,6, siendo todavía menor en las prótesis parciales que en las totales5. Sin embargo, la revisión del componente humeral cementado es técnicamente muy difícil, existiendo un riesgo considerable de fractura diafisaria durante la extracción debido al escaso grosor cortical en esta región anatómica.
Existen tres filosofías en la fijación de vástagos no cementados: la fijación press-fit diafisaria6, la fijación press-fit metafisaria7 y el uso de prótesis porosas para favorecer la incorporación y fijación del implante8. El desarrollo progresivo de líneas radiolucentes en vástagos no cementados no se ha demostrado hasta ahora que haya tenido una traducción clínica, aunque el seguimiento de las series es corto y la revisión de este tipo de componente es técnicamente más sencilla. Siguiendo los criterios desarrollados en la Clínica Mayo, se considera que existe riesgo de aflojamiento del vástago cuando se observa una línea radiolucente de 2 mm o más de ancho en 3 o más de 8 zonas, o se identifica un hundimiento o inclinación del vástago en series radiográficas consecutivas por al menos dos de tres observadores. Atendiendo a estos criterios, en la tabla 1 se muestra el análisis radiográfico de diferentes tipos de fijación de componentes5,6,8.
En cuanto a la fijación press-fit metafisaria, Matsen et al7 realizaron un estudio prospectivo con 127 pacientes seguidos una media de 3 años evaluando la aparición de líneas radiolucentes. Encontraron que 50 prótesis no tenían ningún signo de aflojamiento, 2 tenían líneas radiolucentes en la región metafisaria y 75 las tenían en la punta del implante. En sólo 11 casos había radiolucencias mayores de 1 mm de ancho. Este estudio incluía tanto prótesis parciales como totales, aunque no se encontraron diferencias entre ellas.
La tendencia actual es la de utilizar diseños porosos no cementados de fijación metafisaria, reservando la fijación con cemento para aquellos casos con mala calidad ósea.
Prótesis de resuperficialización
Este tipo de prótesis fue diseñado para el tratamiento de pacientes con necrosis avascular, artrosis y artritis reumatoide1, aunque también se ha usado para otras indicaciones9.
Sus ventajas son la preservación del stock o reserva ósea, la facilidad de la cirugía de revisión, la eliminación de elementos de concentración de fuerzas y la disminución del riesgo de fracturas periprotésicas. Además, este tipo de implante permite recrear de una manera precisa la anatomía con respecto al offset10, la retroversión y el ángulo de inclinación1. El implante con más años de seguimiento y con el que se tiene mayor experiencia es el diseñado por Copeland, que ya va por la tercera generación de prótesis. Se compone de una cúpula articular con un pequeño cilindro estabilizador. Los resultados clínicos esperables con este tipo de implante son similares a los de la artroplastia con vástago, con un riesgo de reintervención del 8% en la prótesis tipo Mark-29. Actualmente, el nuevo diseño Mark-3 incluye un revestimiento de hidroxiapatita en la superficie interna de la cúpula y en el cilindro estabilizador.
Prótesis bipolar
Las ventajas teóricas de este diseño son:
1) La disminución del desgaste por erosión de la glenoides al disponer de dos superficies de fricción en vez de una, aunque el mayor diámetro de la cabeza también favorecería el desgaste. Este punto no ha sido demostrado todavía en ningún estudio clínico comparativo.
2) La mejora mecánica de la función del hombro. El mayor tamaño de la cabeza también proporcionaría teóricamente un mayor brazo de palanca para el deltoides, al desplazar hacia lateral el centro de rotación del implante, aunque este punto podría ser discutible si atendemos a los teóricos efectos perjudiciales mencionados más arriba que supone la sobredimensión del segmento cefálico.
Hay dos estudios cuyo objetivo es averiguar si con el paso del tiempo sigue habiendo movimiento entre los dos componentes cefálicos. En uno de los estudios se evaluaron 11 prótesis con un mínimo de 2 años de seguimiento, y se concluyó que la mayoría del movimiento se produce a nivel de la articulación escápulo-torácica, comportándose la prótesis predominantemente como un implante monopolar11. El otro estudio evalúa 25 hombros de pacientes con artritis reumatoide operados mediante la sustitución con prótesis parcial bipolar. Inicialmente los autores encuentran que no hay diferencias entre la movilidad dentro y fuera del implante, pero en 12 pacientes que fueron evaluados después de tres años de la cirugía se observó que la movilidad dentro del implante era mucho menor, encontrando casos de movimiento paradójico e independiente de la movilidad entre la cabeza externa y la glenoides. En cuanto a los resultados clínicos, los autores refieren un mantenimiento de la movilidad 8 años después de la cirugía12.
INDICACIONES Y RESULTADOS
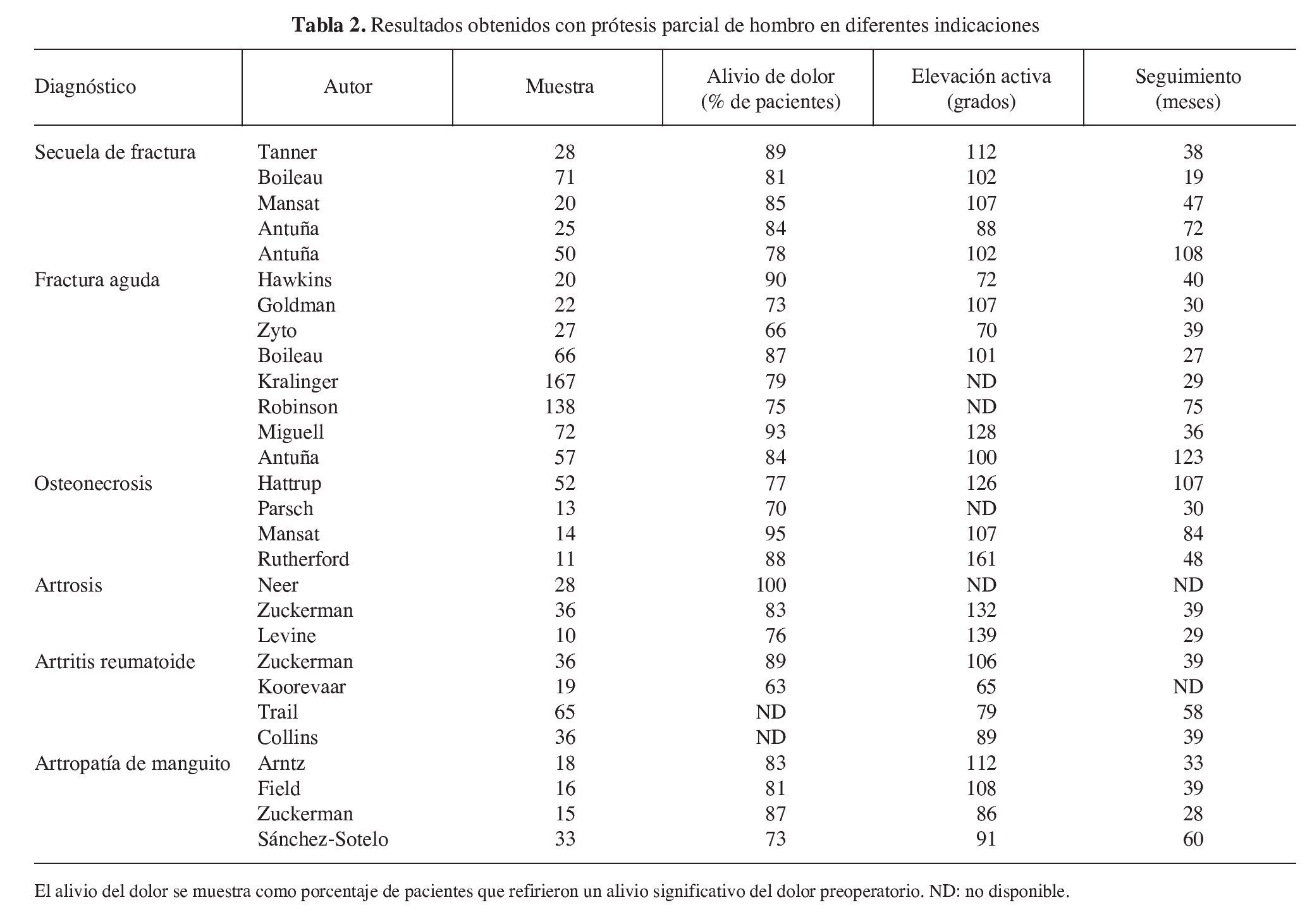
En la actualidad, la artroplastia parcial de hombro se usa como tratamiento de la necrosis avascular, la artrosis y la artritis reumatoide con resultados buenos y reproducibles1,13-16. Sin embargo, en el caso de la reconstrucción de fracturas de húmero proximal complejas y la artropatía de manguito, los resultados son más impredecibles1,17-19; aunque habitualmente se consigue un adecuado alivio del dolor, la mayoría de los pacientes tiene un rango de movilidad limitado, con dificultades para el desarrollo de las actividades de la vida diaria. Estos pobres resultados han estimulado el desarrollo de implantes específicos para estos problemas: prótesis específicas para las fracturas y una prótesis invertida semiconstreñida para la artropatía de manguito1. En la tabla 2 se muestra un resumen de los resultados obtenidos en diferentes indicaciones con la prótesis parcial no constreñida20,21.
Hemiartroplastia en la artrosis primaria glenohumeral
La artrosis primaria glenohumeral fue el diagnóstico más frecuente en los pacientes en los que se llevó a cabo una artroplastia del hombro en la Clínica Mayo durante la década de los noventa22.
Como en otras localizaciones, la indicación de realizar una artroplastia ante el diagnóstico de omartrosis se basa en la intensidad del dolor y la disminución de la función y la calidad de vida que supone la patología para el paciente, tras el fracaso de las medidas terapéuticas menos agresivas.
Las series clínicas en las que se obtienen resultados buenos y excelentes de manera reproducible son muy numerosas22, centrándose en la actualidad el debate en los factores de mal pronóstico preoperatorios y en la necesidad o no de realizar el recambio de la superficie glenoidea23.
Gartsman et al24 describen una puntuación en la escala de los American Shoulder and Elbow Surgeons (ASES)25 tras la hemiartroplastia de 62 puntos sobre 100, con una clara mejoría tanto en el dolor como en la función. Norris et al13 realizaron 43 hemiartroplastias para esta indicación, describieron cambios dramáticos en el dolor, la función y la satisfacción del paciente, y encontraron una incidencia de complicaciones intraoperatorias del 5,4% (la más frecuente fue la fractura) y posoperatorias del 7,8% (la más frecuente fue la subluxación del implante).
Los factores pronósticos preoperatorios han sido descritos por Iannotti et al23 tras la realización de un estudio multi-céntrico, que incluía 128 casos de hemiartroplastia y artroplastia total de hombro. Los pacientes con menos de 10º de rotación externa pasiva antes de la cirugía mejoraron muy poco este parámetro después de la artroplastia. La presencia de roturas reparables de espesor completo del manguito no influenciaron los resultados en la escala de los ASES25, en el descenso del dolor o la satisfacción del paciente, independientemente del tipo de sustitución protésica. Los pacientes que presentan una erosión glenoidea excéntrica obtuvieron mejores resultados con la artroplastia total que con la hemiartroplastia, con mejor elevación pasiva, mejor rotación externa activa, y una tendencia a obtener mejores valores de flexión del hombro. Los pacientes que presentaban una subluxación posterior inicial tuvieron una menor puntuación ASES, más dolor, y disminución de la rotación externa activa independientemente del tipo de intervención. Previamente se había estudiado la influencia de la rotura masiva irreparable del manguito en 33 hemiartroplastias con 5 años de media de seguimiento, y se encontraron resultados satisfactorios en el 67% de los casos, pasando la elevación media de 71º a 91º. Sin embargo, el 27% presentaba dolor moderado, y en un 20% de los casos se observó inestabilidad anterosuperior, relacionada significativamente con el antecedente de haber sido practicada previamente una acromioplastia26.
La mayoría de los trabajos actuales se centra en el debate de si se debe o no realizar una sustitución de la superficie articular glenoidea. Bryant et al27 han publicado recientemente una revisión sistemática de la literatura y meta-análisis al respecto que incluía 112 pacientes, y llegaron a la conclusión de que la artroplastia total obtenía mejores resultados a corto plazo que la hemiartroplastia en cuanto a las escalas de función y en la elevación, y una tendencia a mejor resultado también en términos de dolor. Es necesario ver si estos resultados se mantienen a lo largo del tiempo, teniendo en cuenta fenómenos de progresión de la erosión de la glenoides en la hemiartroplastia o aflojamiento del componente glenoideo en la artroplastia total. Edwards et al28 evaluaron 601 artroplastias totales y 89 hemiartroplastias en un estudio multicéntrico con un seguimiento mínimo de 2 años. Al final del seguimiento, la elevación media en las hemiartroplastias era de 130º, la rotación externa activa de 36º y el Constant ajustado por edad del 86%. Para las sustituciones totales los resultados fueron 145º, 42º y 96%, respectivamente, con diferencias significativas en todos los parámetros. El 56% de los componentes glenoideos tenía líneas radiolucentes al final del seguimiento.
Hemiartroplastia en artritis inflamatoria
La hemiartroplastia de hombro en la artritis inflamatoria es capaz de disminuir el dolor y mejorar los parámetros de función y movilidad de manera reproducible. El principal problema al que se enfrenta el cirujano en estos pacientes es la dificultad que presentan las características de las partes blandas y el déficit significativo de sustrato óseo29, por lo que la planificación preoperatoria se hace especial-mente importante en estos casos.
En cuanto al tipo de implante a utilizar, Collins et al16 presentaron un estudio multicéntrico prospectivo en el año 2004 en el que analizaban los resultados del tratamiento con 36 prótesis parciales y 25 totales. Con una media de seguimiento de 39 meses, encontraron que en ambos tipos de prótesis la cirugía mejoró las puntuaciones de las escalas analógicas visuales y del Simple Shoulder Test30 de manera significativa. Sin embargo, la movilidad activa fue significativamente mejor en las prótesis totales que en las parciales. La presencia de enfermedad de gravedad extrema no afectó a los resultados clínicos posquirúrgicos. La adaptación de la prótesis a la anatomía y el restablecimiento del alineamiento glenohumeral se relacionaron con los mejores resultados de movilidad, calidad de vida y uso del hombro para actividades laborales o de ocio. En 4 casos de hemiartroplastia hubo erosión glenoidea. En dos artroplastias totales se aflojó el componente glenoideo.
La fijación del vástago fue evaluada en un estudio pros-pectivo y aleatorizado31, y se comparó la fijación press-fit diafisaria con la fijación con cemento presurizado y sellado distal tras lavado del canal en 26 hombros afectados con artritis reumatoide. A dos años de seguimiento no hubo diferencias entre los dos tipos de fijación para esta indicación.
Hemiartroplastia en osteonecrosis
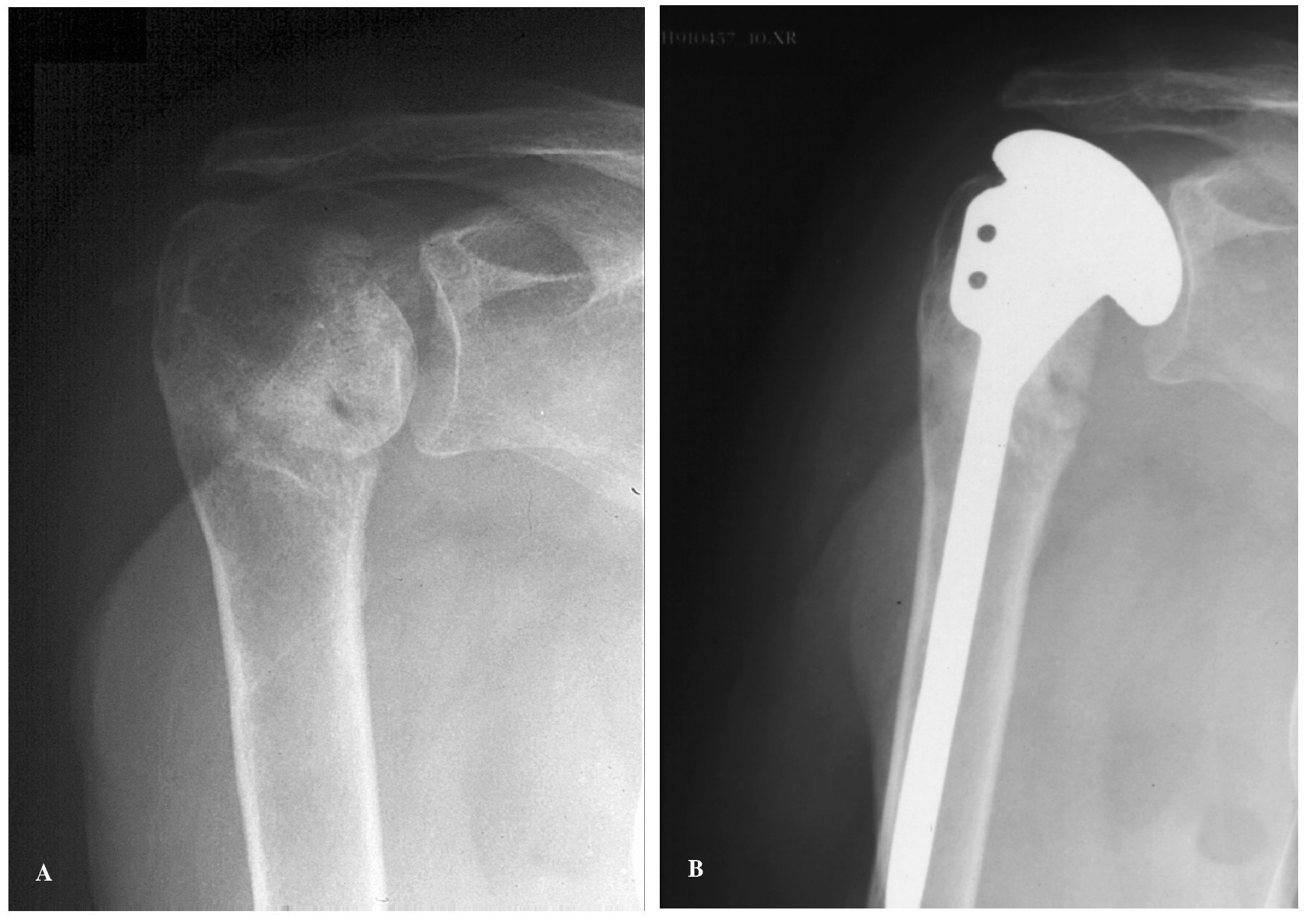
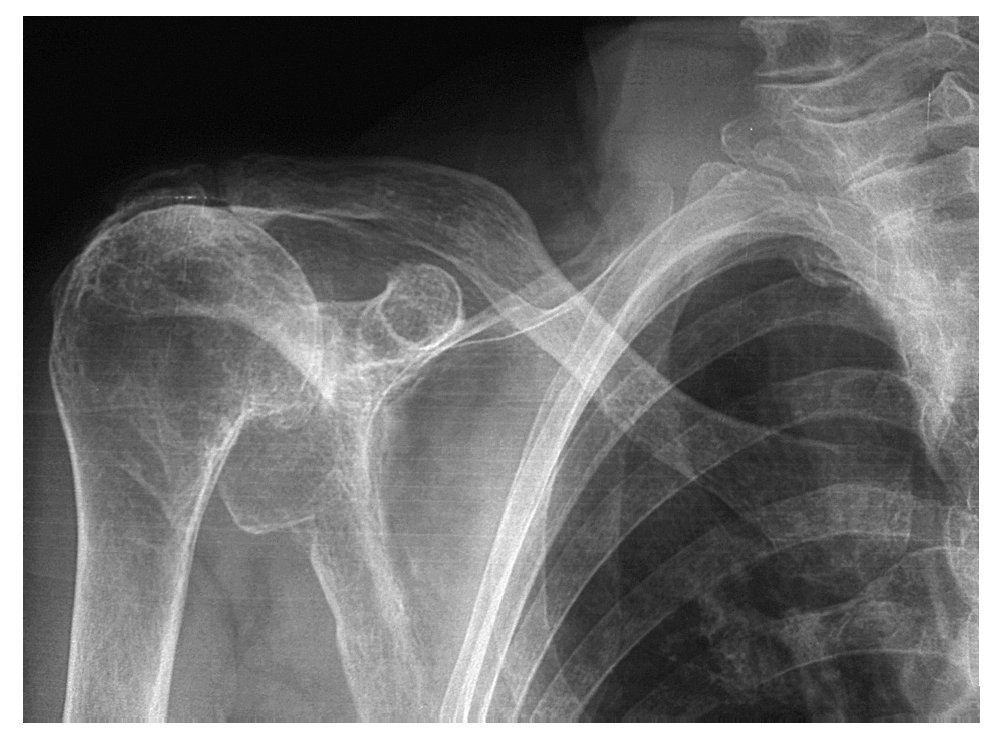
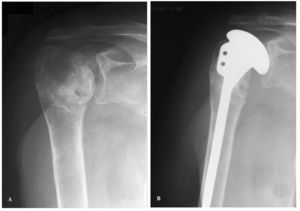
Las dos causas fundamentales de osteonecrosis de la cabeza del húmero son el uso de corticoides y como secuela posterior a una fractura por lesión vascular directa por la propia fractura o lesión iatrogénica durante la cirugía32. En otros casos son idiopáticas o debidas a enfermedades o condiciones menos frecuentes como la enfermedad de Gaucher, la anemia de células falciformes o la osteonecrosis inducida por radioterapia. La necesidad de realizar una artroplastia está condicionada por la extensión, el estadio del proceso y la etiología, siendo las necrosis traumáticas las que necesitan más frecuentemente una intervención quirúrgica33 (fig. 2).
Figura 2.(A) Necrosis avascular de la cabeza del húmero; obsérvese el aumento de densidad del segmento cefálico y el colapso de la superficie articular. (B) Resultado radiológico tras la implantación de una prótesis no constreñida sin cementar, con resultados clínicos satisfactorios.
En general, se obtienen mejores resultados en los estadios precoces en los que el dolor es moderado y el rango de movilidad está conservado14. Cuando la enfermedad no está muy avanzada, ésta se origina y se limita a la cabeza del húmero, no existiendo teóricamente afectación de la superficie glenoidea, por lo que podría suponerse que no es necesario realizar una artroplastia total en estos casos, siendo suficiente teóricamente el reemplazamiento de la cabeza humeral. Para responder a esta pregunta, Hattrup y Co-field34 realizaron un estudio en el que incluyeron 127 casos tratados con 71 hemiartroplastias y 56 prótesis totales, con una media de seguimiento de 9 años para los 88 casos que completaron el seguimiento. El 79% de los pacientes declaró una mejoría subjetiva y el 77% no presentaba dolor o lo sentía sólo de manera ocasional. La puntuación media del ASES fue de 63. No se encontraron diferencias entre la artroplastia parcial y la total en los parámetros evaluados. El factor pronóstico más importante fue la etiología postraumática de la osteonecrosis, que condicionaba peores resultados de movilidad y en la puntuación de ASES. La complicación postoperatoria más frecuente fue la rotura del manguito rotador, que se presentó en el 18% de los casos, circunstancia que era más frecuente cuando había antecedentes de alguna cirugía previa.
Hemiartroplastia en fracturas de húmero proximal
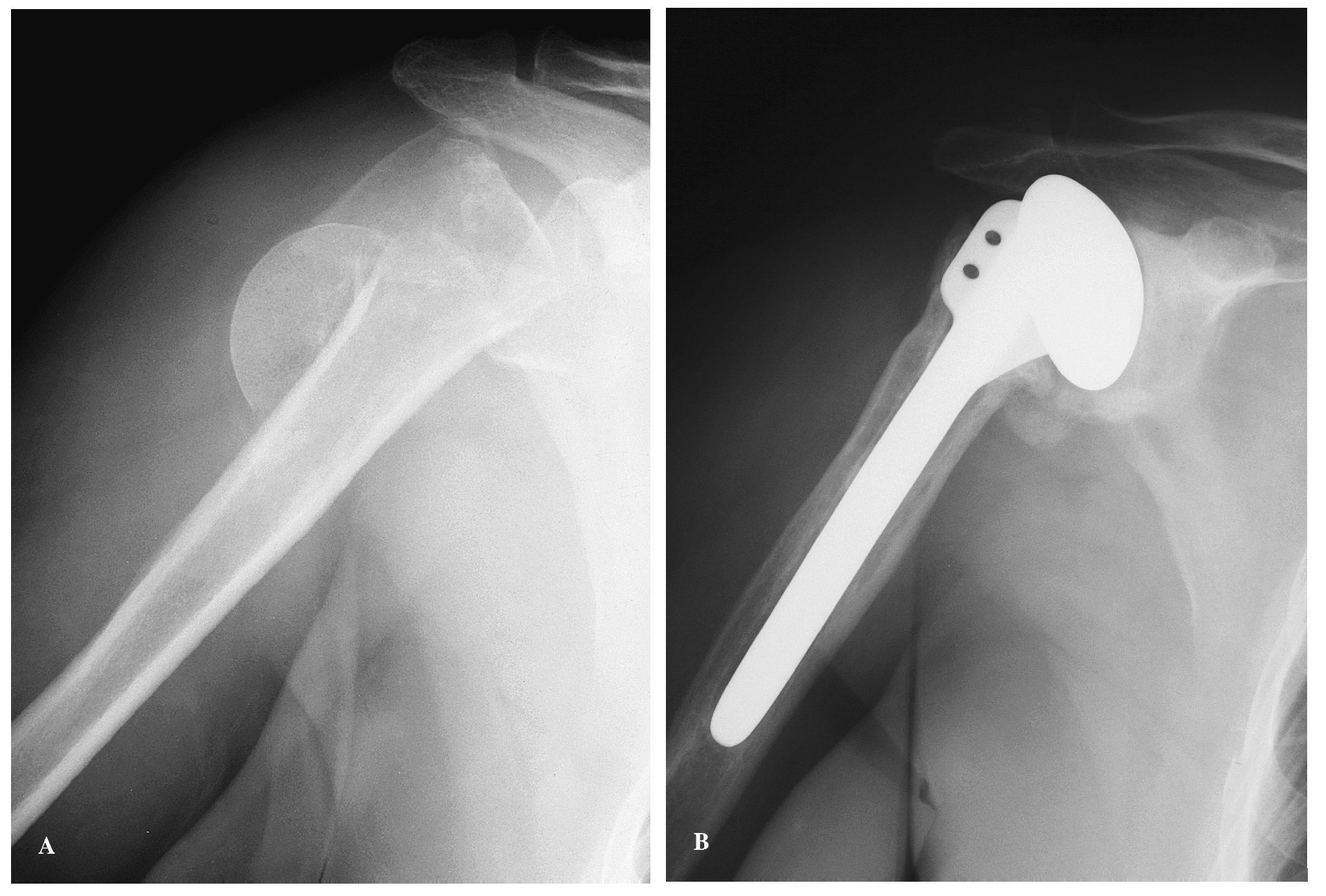
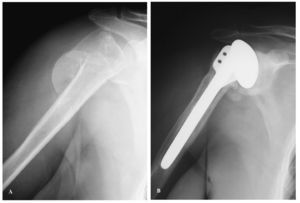
En las fracturas agudas, la sustitución protésica de la cabeza humeral se reserva para pacientes ancianos con mala calidad ósea y fracturas en las que sería muy difícil conservar la cabeza o intentar sintetizarlas, o en aquellos casos en los que exista un alto riesgo de necrosis (fig. 3). En general, en pacientes menores de 60 años debería intentar evitarse la artroplastia35.
Figura 3.(A) Fractura de húmero proximal en cuatro fragmentos con gran desplazamiento del segmento articular, que aparece volteado y situado lateralmente a la diáfisis. (B) Resolución del caso mediante artroplastia parcial de hombro no constreñida cementada. Imagen tomada en el quinto año de evolución, en la que se observa artrosis glenoidea con disminución del espacio articular y osteofitos en la región inferior.
Las principales indicaciones de sustitución protésica de hombro ante fracturas agudas son35,36:
1) Las fracturas en las que se estima un riesgo elevado de necrosis avascular de la cabeza humeral, es decir, las que dejan la superficie articular aislada de las tuberosidades y, por ende, de aporte vascular (por ejemplo, fracturas y fracturas luxaciones en 4 partes de Neer, fracturas del cuello anatómico). En este sentido, la integridad de la bisagra perióstica medial entre la cabeza y la diáfisis, y la mayor extensión del segmento metafisario posteromedial unido a la superficie articular se han propuesto como factores protectores frente a la isquemia del segmento cefálico37.
2) Las fracturas que afectan a la superficie articular, como aquellas denominadas división de la cabeza (head-splitting), o las fracturas por impresión de la superficie articular en las que se estima una destrucción mayor del 40%.
3) Aquellas fracturas desplazadas que, bien por su gran conminución, bien por la mala calidad ósea, son muy difíciles de sintetizar y el tratamiento conservador no parece adecuado.
En ausencia de compromiso de la superficie articular de la glenoides, el tipo de prótesis a emplear es una prótesis parcial, entre las que existen diferentes filosofías y tipos de diseño. En cuanto a la técnica quirúrgica, para conseguir un adecuado resultado funcional es fundamental la correcta reducción estable y duradera de la tuberosidad mayor18, siendo las alteraciones de la consolidación del troquíter la complicación más frecuente19. Los diferentes diseños plantean la posibilidad de aportar injerto en el lecho de la tuberosidad en la región metafisaria de la prótesis (por ejemplo, la prótesis diseñada por Pascal Boileau específica para fracturas), o el uso de un módulo metafisario de grandes dimensiones y superficie porosa para apoyar sobre él la tuberosidad y anclarla con suturas a través de la prótesis esperando la integración de la prótesis y la tuberosidad mayor (por ejemplo, el nuevo diseño de Popp Gerber). A este respecto, un estudio muy reciente38 comparó las prótesis de diseño anatómico con las de diseño específico para fracturas y, a pesar de encontrar un mayor porcentaje de curación completa de la tuberosidad mayor en las prótesis específicas para fractura, una mayor curación incompleta en las anatómicas y similar reabsorción de la tuberosidad mayor en ambos grupos (aproximadamente 45%), no hubo diferencias en cuanto a la escala de Constant y la satisfacción de los pacientes, poniendo en duda las ventajas clínicas supuestas para los diseños específicos para esta indicación.
En casos en los que no se puede llevar a cabo una adecuada reducción de las tuberosidades, se están empezando a utilizar los diseños invertidos para contrarrestar la ineficiencia del manguito rotador39.
Otros puntos importantes en cuanto a la elección del implante y su colocación son: la cabeza debe ser de igual o menor tamaño que la original, la retroversión debe ser de no más de 20º para disminuir la tensión sobre las suturas de la tuberosidad mayor, y se debe asegurar una correcta altura de la prótesis. Este último punto puede ser difícil de conseguir debido a la pérdida de referencias óseas producidas por la fractura. Una referencia útil es que en el 95% de los casos la punta de la tuberosidad mayor se encuentra a una distancia de 5,5 ± 0,5 cm del borde superior del tendón del pectoral mayor40.
Estudios de seguimiento a largo plazo demuestran una supervivencia general de las prótesis parciales en esta indicación de hasta el 94% a 10 años18. Los resultados en cuanto al alivio del dolor son bastante satisfactorios y reproducibles; sin embargo, esto no es así en el caso de la capacidad funcional, en el que los resultados son impredecibles18. Stableforth41 incluye en un estudio una serie retrospectiva histórica de tratamiento conservador de 32 fracturas en 4 partes, y una serie prospectiva de 49 pacientes, de los cuales 32 tenían fracturas desplazadas en 4 partes, tratadas la mitad con hemiartroplastia y la otra mitad de forma conservadora; encontró mejores resultados en cuanto a dolor y función en el grupo de hemiartroplastia. Bosch et al42 evalúan 39 fracturas en 3 y 4 partes tratadas con hemiartroplastia y ponen de manifiesto que esta cirugía obtiene mejores resultados cuando se realiza precozmente, poniendo el punto de corte en 4 semanas. Los mejores resultados se ven en los pacientes más jóvenes, sin problemas neurológicos preoperatorios, y con una radiografía satisfactoria a las 6 semanas de seguimiento.
Hemiartroplastia en secuelas de fracturas de húmero proximal
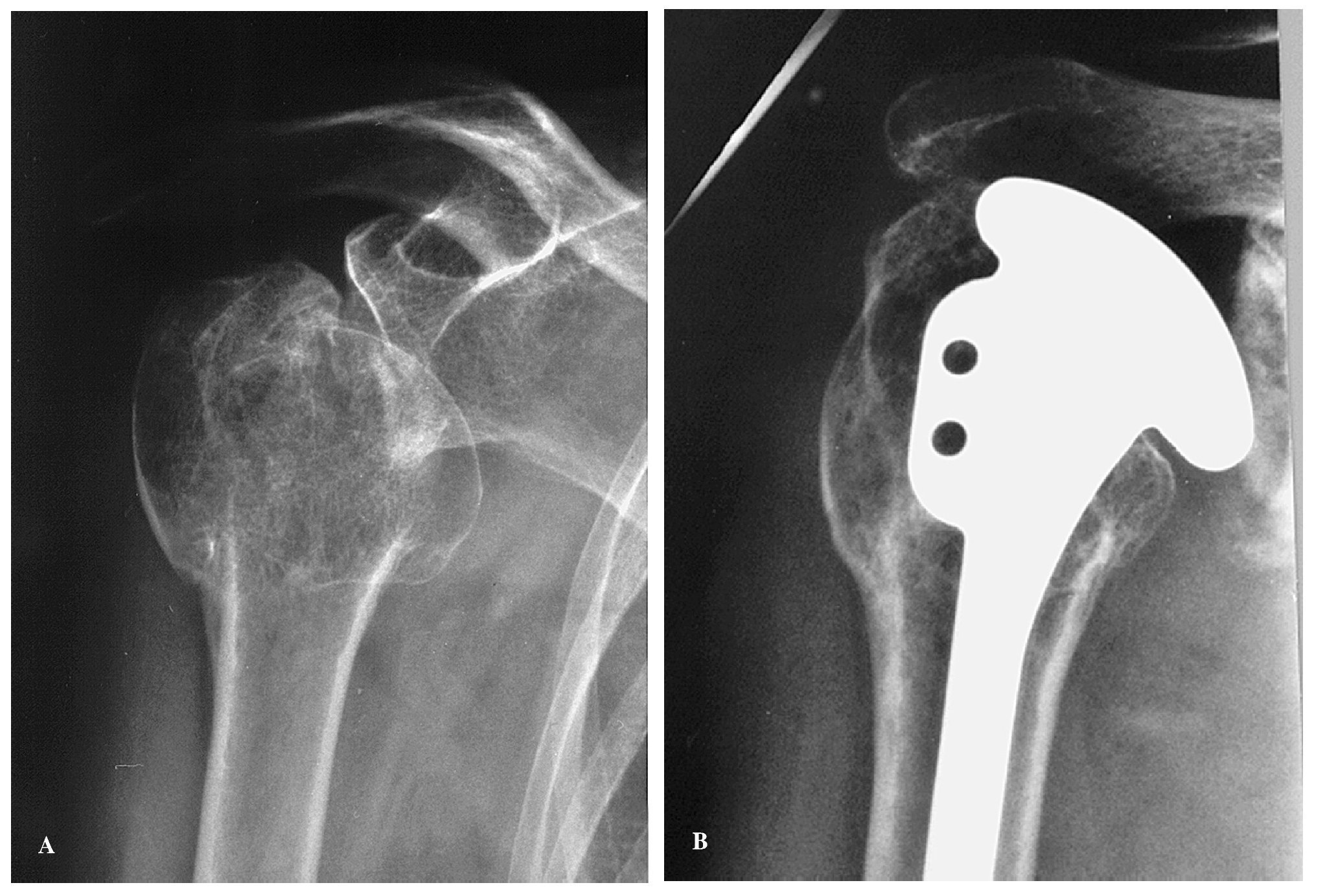
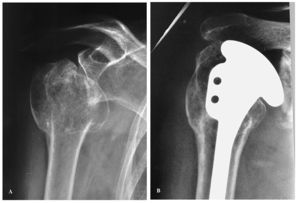
En cuanto al tratamiento de las secuelas de las fracturas de húmero proximal (fig. 4), Antuña et al43 obtuvieron resultados satisfactorios para el alivio del dolor, pero casi un 50% de malos resultados globales según la escala de Neer modificada por Cofield con la utilización de diferentes modelos de artroplastia parcial y total para el tratamiento de las pseudoartrosis, con una media de 9 años de evolución. Los mismos autores44 publicaron un estudio en el que se trataban 50 consolidaciones en mala posición con hemiatroplastia. Encontraron que los pacientes que sufrían más dolor al final del seguimiento (media de 9 años) eran aquellos que habían tenido cirugías previas, que asociaban osteonecrosis, o aquellos operados antes de los dos años tras producirse la fractura. En total, el 50% de los pacientes tuvo resultados no satisfactorios.
Figura 4.(A) Consolidación viciosa con superficie articular con deformidad en valgo y troquíter superpuesto. (B) Resolución del caso con hemiartroplastia no cementada. Nótese la conservación del troquíter en la radiografía de control.
Boileau et al45 publicaron en un artículo muy reciente la validación de su clasificación y propuesta de tratamiento de estas secuelas, mediante el análisis de los resultados en 203 pacientes tratados con prótesis no constreñidas modulares adaptables. Los autores clasifican las secuelas en 4 grupos:
1) Tipo 1 es aquella que presenta un colapso del segmento cefálico o necrosis avascular.
2) Las tipo 2 son aquellas en las que hay una luxación inveterada o una fractura-luxación.
3) La tipo 3 corresponde a las ausencias de consolidación del cuello quirúrgico, en las cuales los resultados son pobres con las prótesis no constreñidas, recomendándose bien la osteosíntesis con aporte de injerto como mejor opción de tratamiento con un segmento cefálico bien preservado, bien el uso de prótesis de bajo perfil que permita el aporte de injerto en la región metafisaria para facilitar la consolidación de las tuberosidades en los casos de artrosis glenohumeral o defectos cavitarios de la cabeza humeral.
4) La tipo 4 corresponde a las consolidaciones en mala posición de las tuberosidades, en las que los resultados con prótesis no constreñidas son reproduciblemente malos. En estos casos, el autor recomienda el uso de prótesis invertidas.
En las tipo 1 y 2 se consiguen resultados predecibles satisfactorios con el uso de una prótesis modular no constreñida, con mejores resultados con el uso de prótesis totales que parciales. El autor atribuye el éxito de estos implantes a que no es necesario realizar una osteotomía del troquíter.
En las tipo 3 y 4 se ha relacionado la necesidad de realizar una osteotomía del troquíter con los malos resultados de las prótesis modulares no constreñidas.
Hemiartroplastia en patología del manguito rotador
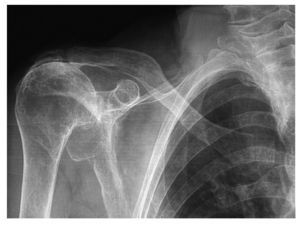
En este apartado se pueden considerar dos situaciones clínicas: la necesidad de realizar una artroplastia por diferentes motivos; por ejemplo, en una omartrosis o una artritis reumatoide en un paciente con una lesión de manguito irreparable, o el estadio final en la degeneración del manguito rotador, es decir, la artropatía de manguito46 (fig. 5). El tratamiento de elección usado para ambas condiciones ha sido hasta hace pocos años la hemiartroplastia con mantenimiento del arco coraco-acromial, lo cual produce beneficios significativos en cuanto al alivio del dolor, pero una mejoría muy modesta en cuanto a la movilidad17. Zuckerman et al47 publicaron un estudio retrospectivo con 15 pacientes diagnosticados de artropatía de manguito, con un seguimiento medio de 28 meses. La elevación media pasó de 69º a 86º, y la rotación externa de 15º a 29º. El 87% se mostró contento con los resultados, y el dolor mejoró significativamente en el 95% de los casos. También se observó un incremento de la fuerza en los 6 casos en los que este parámetro fue evaluado.
Figura 5.Artropatía de manguito en paciente anciano. Obsérvese el redondeamiento de la cabeza del húmero, que aparece subluxada hacia superior apoyándose en el acromion, formando una nueva "articulación" en esta localización.
En este campo, dados los pobres resultados funcionales obtenidos, se está empezando a utilizar otro diseño de implante: la prótesis invertida. Ésta parece mejorar los resultados en cuanto a la elevación, superando los 100º en diferentes estudios, pero no parece conseguirlo para las rotaciones externa e interna48. Por otro lado, las curvas de supervivencia de estos implantes, aunque mejores cuando la indicación es la artropatía del manguito, tienen dos importantes escalones: por aflojamiento temprano del implante a los 3 años y por deterioro de función a los 6 años, con Constant mayor de 30 del 58% a los 10 años49. Así, se recomienda su uso para pacientes mayores de 70 años con artrosis y rotura irreparable del manguito, con bajas demandas funcionales.
Como puede observarse, este problema continúa siendo un reto importante sin una solución claramente ventajosa.
COMPLICACIONES DE LA HEMIARTROPLASTIA DE HOMBRO
Las principales complicaciones que presentan las hemiartroplastias son:
1) El aflojamiento de la prótesis; ha sido discutido previamente en el apartado de opciones de fijación del vástago.
2) La migración de la prótesis; se produce principal-mente en aquellas situaciones en las que no existe el componente estabilizador que aportan las partes blandas, en especial el manguito rotador. Para intentar evitar este fenómeno se propone dejar intacto el arco coraco-acromial, para intentar que sirva de tope para la migración superior17.
3) Las fracturas periprotésicas50,51; tienen una incidencia de entre el 0,5 y el 3%. La mayoría se produce intraoperatoriamente implicando a la diáfisis y produciéndose fundamentalmente por fuerzas de torsión. Los factores de riesgo son el sexo femenino, la mala calidad ósea, la edad avanzada y el antecedente de artritis reumatoide. Los sistemas de clasificación existentes se basan en la relación anatómica entre la fractura y el vástago: las tipo A ocurren en la punta del vástago y se extienden proximalmente; las tipo B se limitan a la punta del vástago, y las tipo C aparecen distales al vástago. En las fracturas que ocurren postoperatoriamente, las decisiones terapéuticas deben tomarse según la estabilidad de la fractura y la estabilidad del implante, intentando conseguir una movilización precoz del hombro y preservar la función. Las fracturas consideradas estables pueden tratarse de manera conservadora. Las fracturas ines-tables con componentes aflojados requieren el recambio protésico utilizando vástagos largos que lleguen al menos de 2 a 3 veces la distancia entre corticales distalmente al extremo más inferior de la fractura. La fijación rígida con placas con tornillo bloqueados es una opción terapéutica en implantes estables. El tiempo medio para la consolidación de estas lesiones puede llegar a los 280 días.
4) Inestabilidad de la artroplastia52; las causas para la inestabilidad son la tensión capsular no adecuada, la disfunción o ausencia del manguito rotador y la posición inadecuada de los componentes. En la cirugía deben intentar resolverse estos problemas. En la serie publicada por Sánchez-Sotelo et al52, que incluyó 7 hemiartroplastias y 26 artroplastias totales, sólo en 9 casos se consiguió restaurar la estabilidad. Con una segunda cirugía, sólo se consiguieron estabilizar 5 casos más. La inestabilidad anterior se mostró más refractaria al tratamiento que la posterior. La clasificación de Neer modificada por Cofield mostró 4 resultados excelentes, 6 satisfactorios y 23 insatisfactorios (70%).
CONCLUSIONES
Existen diferentes diseños y generaciones protésicas de artroplastia parcial de hombro. Actualmente, los implantes diseñados imitando la anatomía normal, junto con una técnica adecuada y una correcta selección de componentes, ofrecen resultados satisfactorios y duraderos en indicaciones como la omartrosis, la artritis reumatoide y la necrosis avascular. En la patología de manguito y las fracturas de húmero proximal existen diseños específicos, aunque los resultados son menos reproducibles.
Declaración de conflicto de intereses
Los autores han declarado no tener ningún conflicto de intereses.
Correspondencia:
A.M. Foruria.
Hospital Universitario La Paz.
P.o de la Castellana, 261.
28046. Madrid. España.
Correo electrónico: antonio.foruria@uam.es
Recibido: febrero de 2007.
Aceptado: septiembre de 2007