El síndrome de glúteo profundo (SGP) es una enfermedad caracterizada por la compresión a nivel extra-pélvico del nervio ciático (NC) por cualquier estructura en el espacio glúteo profundo. El objetivo de este estudio fue evaluar los resultados clínicos en pacientes con SGP manejados con técnica endoscópica.
MétodosEstudio retrospectivo de pacientes con SGP intervenidos con técnica endoscópica entre 2012 al 2016 con seguimiento mínimo de 12 meses. Los pacientes fueron evaluados antes de la intervención y durante el primer año de seguimiento con las escalas WOMAC y VAIL.
ResultadosSe incluyeron 44 cirugías en 41 pacientes (36 mujeres y 5 varones) con un promedio de edad de 48,4±14,5 años. La causa más frecuente de atrapamiento fueron las bandas fibrovasculares, hubo 2 casos de variante anatómica en la salida del nervio, y en un caso aislado, el atrapamiento del NC fue atribuido a la aplicación de biopolímeros en la región glútea. Se encontró mejoría de la funcionalidad y dolor valorado con la escala WOMAC con una mediana de 63 a 26 puntos después de la intervención (p<0,05). Al final del seguimiento un paciente continuaba con dolor residual del nervio cutáneo femoral posterior. Cuatro casos requirieron de revisión a los 6 meses posteriores al procedimiento, por atrapamiento de tejido de cicatrización alrededor del NC.
ConclusiónLa liberación endoscópica del NC es una alternativa en el manejo del SGP al mejorar la función y disminuir el grado de dolor, cuando existe una adecuada selección de pacientes.
Deep gluteal syndrome (DGS) is characterized by compression, at extra-pelvic level, of the sciatic nerve within any structure of the deep gluteal space. The objective was to evaluate the clinical results in patients with DGS treated with endoscopic technique.
MethodsRetrospective study of patients with DGS treated with an endoscopic technique between 2012 and 2016 with a minimum follow-up of 12 months. The patients were evaluated before the procedure and during the first year of follow-up with the WOMAC and VAIL scale.
ResultsForty-four operations on 41 patients (36 women and 5 men) were included with an average age of 48.4±14.5. The most common cause of nerve compression was fibrovascular bands. There were two cases of anatomic variant at the exit of the nerve; compression of the sciatic nerve was associated with the use of biopolymers in the gluteal region in an isolated case. The results showed an improvement of functionality and pain measured with the WOMAC scale with a mean of 63 to 26 points after the procedure (P<.05). However, at the end of the follow-up one patient continued to manifest residual pain of the posterior cutaneous femoral nerve. Four cases required revision at 6 months following the procedure due to compression of the scarred tissue surrounding the sciatic nerve.
ConclusionEndoscopic release of the sciatic nerve offers an alternative in the management of DGS by improving functionality and reducing pain levels in appropriately selected patients.
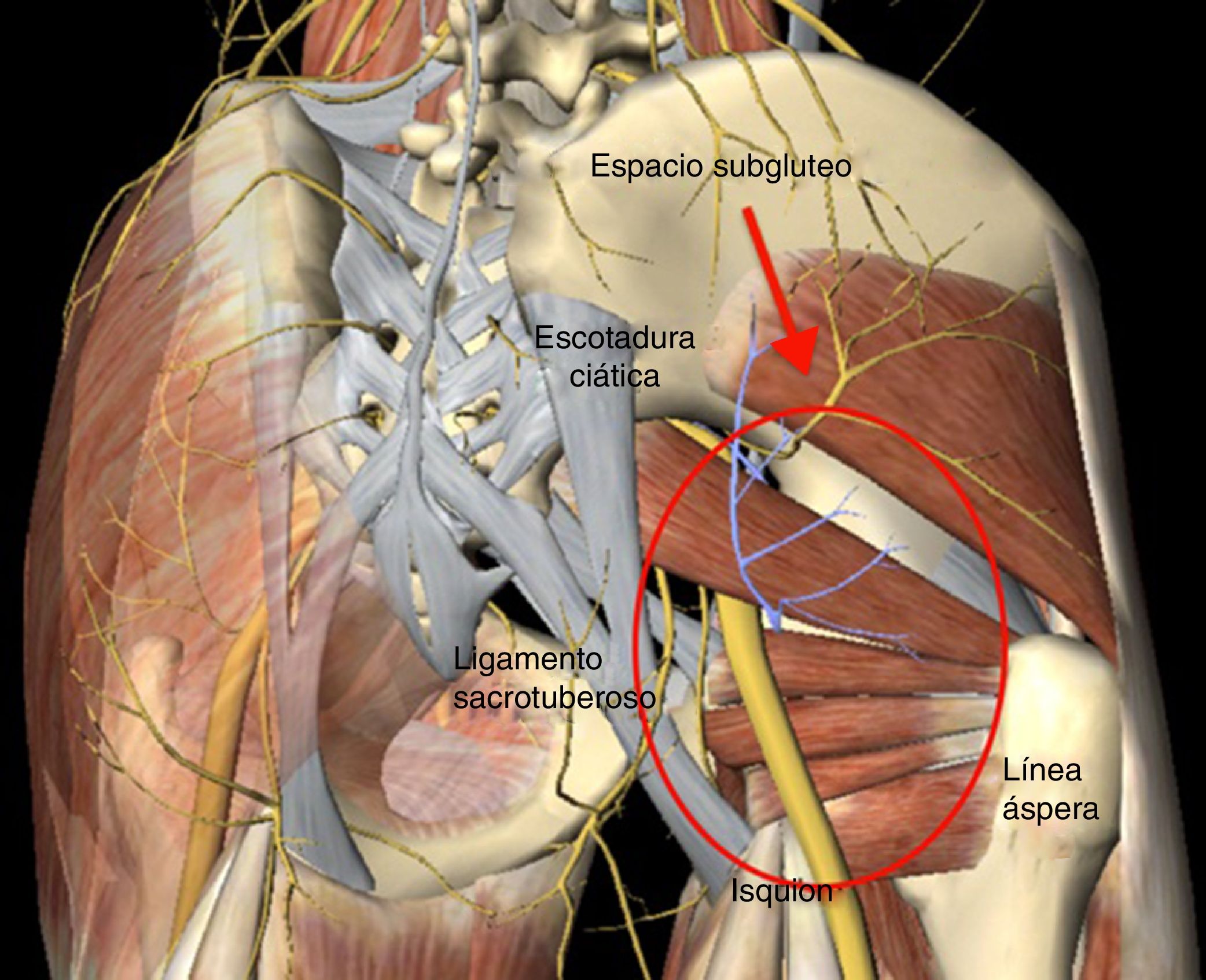
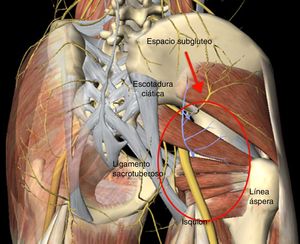
El síndrome del glúteo profundo (SGP) es una enfermedad caracterizada por la compresión a nivel extra-pélvico del nervio ciático (NC) por cualquier estructura en el espacio glúteo profundo1. El espacio subglúteo (ESG) está delimitado delante por el cuello femoral, detrás por el borde posterior del glúteo máximo, en la parte lateral por la línea áspera del fémur y en la parte medial por el ligamento sacrotuberoso y la fascia falciforme (fig. 1). El síntoma que predomina es la incapacidad para permanecer sentado durante periodos prolongados de tiempo, además de dolor irradiado en la pierna afectada. Existen diversos factores etiológicos para el desarrollo del SGP como son: trauma directo a nivel glúteo o pelvis, hipertrofia de los músculos en la región profunda del ESG, hematoma, variantes anatómicas en la salida del NC con respecto al músculo piriforme y bandas fibrovasculares1–5.
El SGP sigue siendo una enfermedad de difícil diagnóstico y tratamiento para el cirujano ortopédico, lo cual retrasa su identificación, afectando la calidad de vida del paciente. El diagnóstico del SGP se realiza por sospecha clínica de acuerdo a la historia y a la sintomatología manifiesta por el paciente durante el examen físico, en ausencia de enfermedad lumbar.
Existen algunas maniobras que pueden ayudar al médico a definir el diagnóstico como son: el test de estiramiento pasivo y activo del piriforme que sumados a la infiltración del ESG dan fuerza a la sospecha clínica6.
El tratamiento del SGP es inicialmente conservador con terapia física, la cual se enfoca en el estiramiento de todos los tejidos alrededor del ESG con el fin de movilizar las estructuras anatómicas de mayor riesgo de atrapamiento como son las bandas fibrovasculares6,7. Este manejo logra buenos resultados en más del 87% de los pacientes. Sin embargo, existe un porcentaje que no responde satisfactoriamente a este esquema de tratamiento1.
El abordaje quirúrgico es considerado en pacientes que fallan al manejo conservador después de un periodo mínimo de 3 meses, y se han descrito dentro de las opciones técnicas abiertas y endoscópicas. El abordaje endoscópico disminuye el riesgo de lesión a las estructuras cercanas por una visualización directa del nervio, además de disminuir los riesgos de infección y lesiones, ofreciendo buenos resultados con una mejoría en el grado de dolor y funcionalidad de los pacientes1,8–12. El objetivo de este trabajo fue describir los resultados clínicos en pacientes con SGP manejados con técnica endoscópica.
MétodosEstudio retrospectivo de pacientes diagnosticados con SGP, tratados con técnica endoscópica. Se incluyeron las cirugías realizadas entre los años 2012 y 2016 con un seguimiento mínimo de 12 meses. Durante el periodo de estudio, se intervinieron 47 pacientes y de estos 44 cumplieron los criterios de selección. Se excluyeron los sujetos menores de 18 años y con cirugías previas de pelvis o cadera. Todos los procedimientos fueron realizados por un mismo cirujano. Este estudio fue aprobado por el Comité de Ética en Investigación de la Institución.
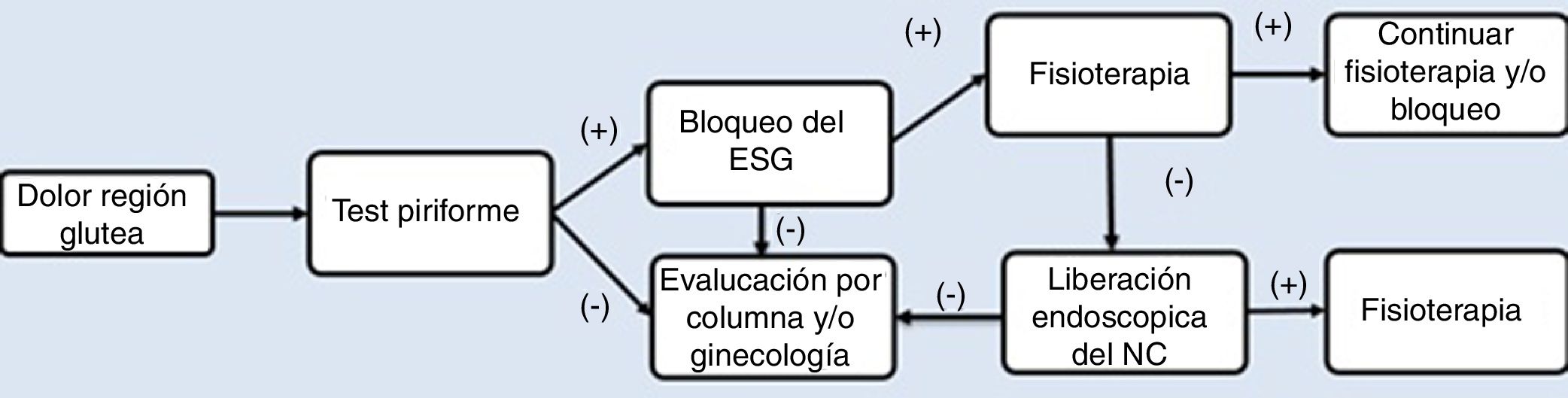
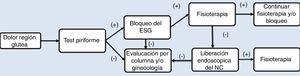
Como parte del protocolo de manejo, se realizó una historia clínica detallada, describiendo el inicio de los síntomas, antecedente de trauma y cirugías previas. El proceso diagnóstico se describe en la figura 2. Los estudios radiológicos incluyeron proyecciones anteroposterior (AP) de pelvis, Dunn de 45 y 90°, falso perfil de Lequesne, además de resonancia magnética (RM). La RM de columna lumbosacra fue indicada en pacientes con clínica sugestiva de radiculopatía lumbar para descartar como origen del dolor en la región posterior de la cadera. La RM de pelvis se indicó para identificar el trayecto del NC y descartar posibles compresiones intrapélvicas después de descartar puntos de comprensión lumbar en los casos con un resultado negativo en la prueba diagnóstica de bloqueo del NC.
El dolor a la palpación de la región glútea fue realizado durante el examen físico y se consideró como una señal diagnóstica, verificada posteriormente con pruebas específicas del ESG. Se realizó el test de estiramiento del piriforme pasivo con el paciente sentado en extensión de rodilla, mientras el examinador pasivamente movía la cadera flexionada en aducción con rotación interna y palpando a 1cm lateral al isquion (dedo medio) y proximalmente en la escotadura ciática (dedo índice)6. El test de piriforme activo se llevó acabo con el paciente en decúbito lateral con 40° de flexión de cadera y 40° de flexión de rodilla cuando el paciente hacía rotación externa contra resistencia. Estas pruebas fueron consideradas como positivas si el dolor aumentaba ante la maniobra. En aquellos sujetos con sospecha de SGP, se realizó la prueba diagnóstica de bloqueo del NC en el área de la escotadura ciática mayor, esta prueba bloquea por contigüidad el nervio. La sensación de mejoría del dolor se consideró una prueba positiva e indicó que el atrapamiento se encontraba en esa área6,13.
Antes de realizar el procedimiento endoscópico, todos los pacientes realizaron terapia física por un periodo de 3 a 6 meses de acuerdo al protocolo de manejo, sin mejoría o empeorando el cuadro de dolor (fig. 2).
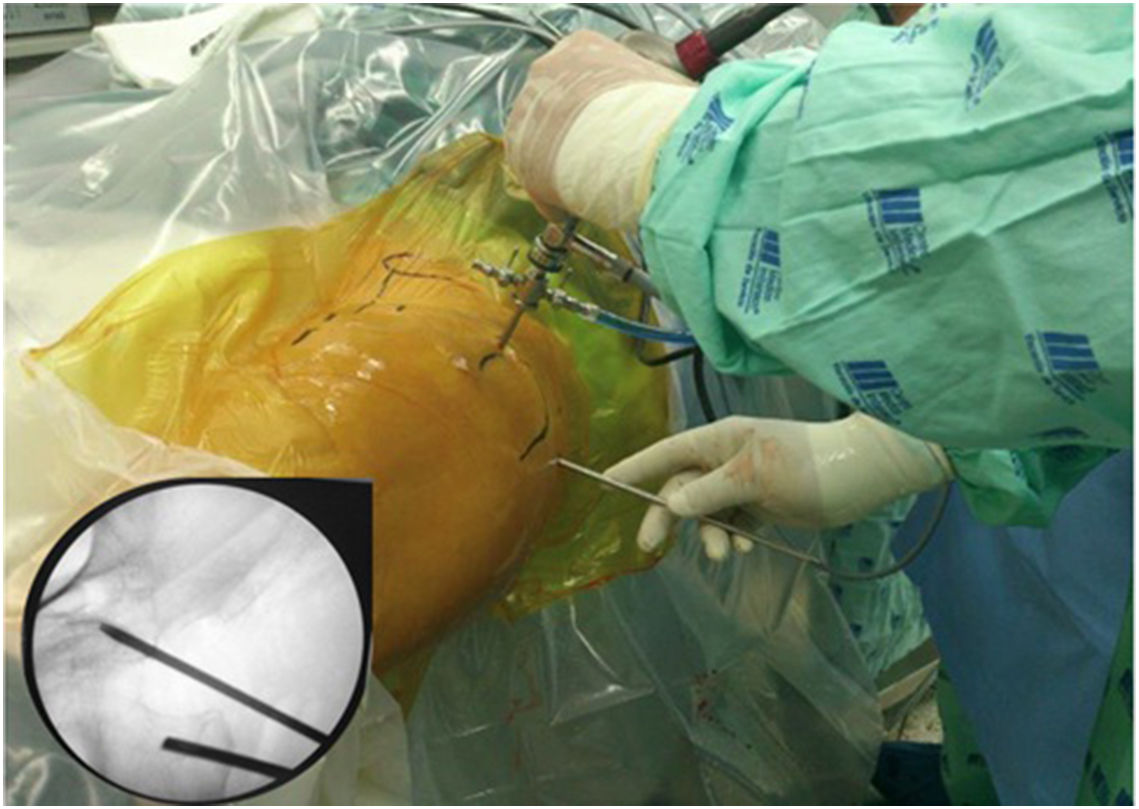
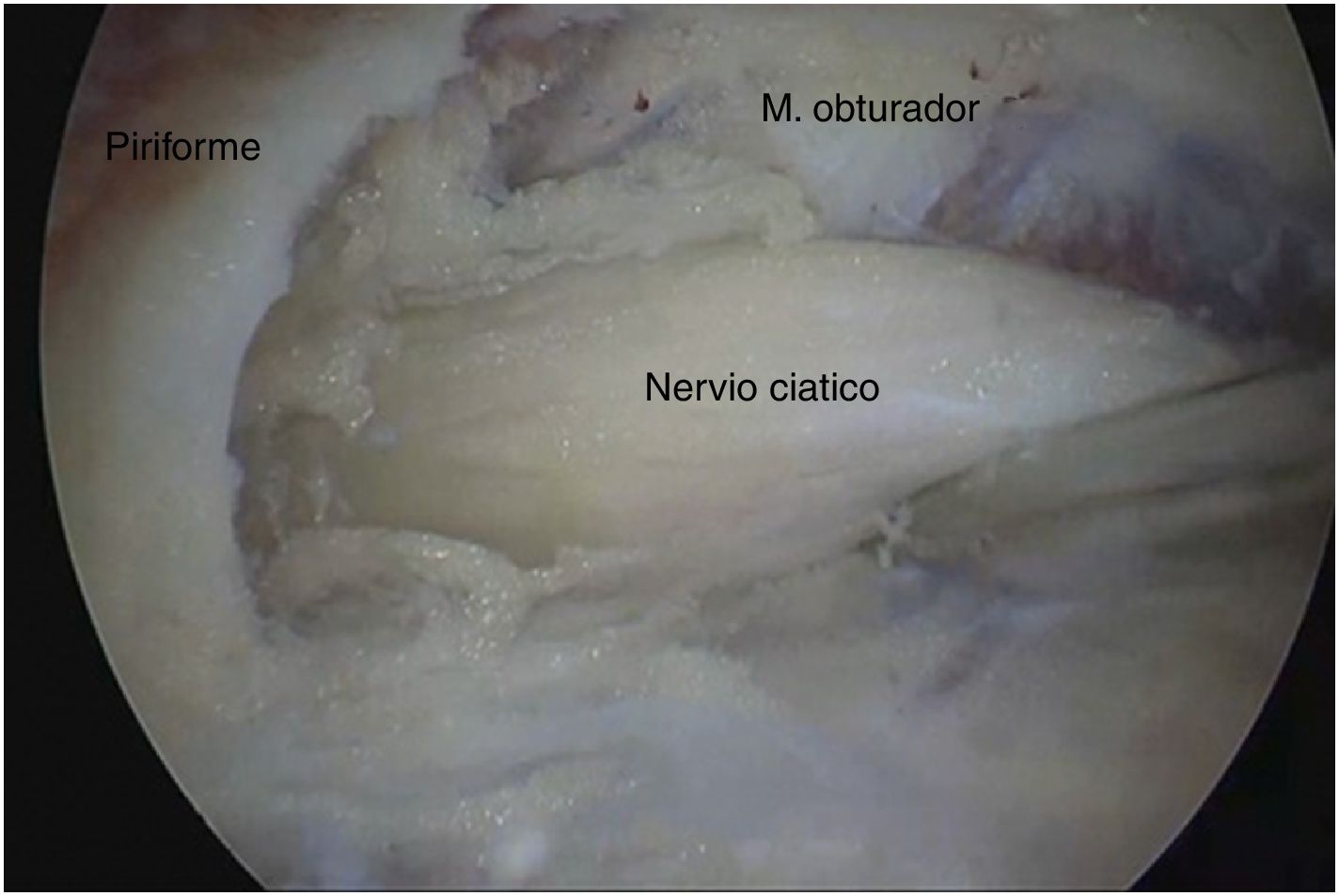
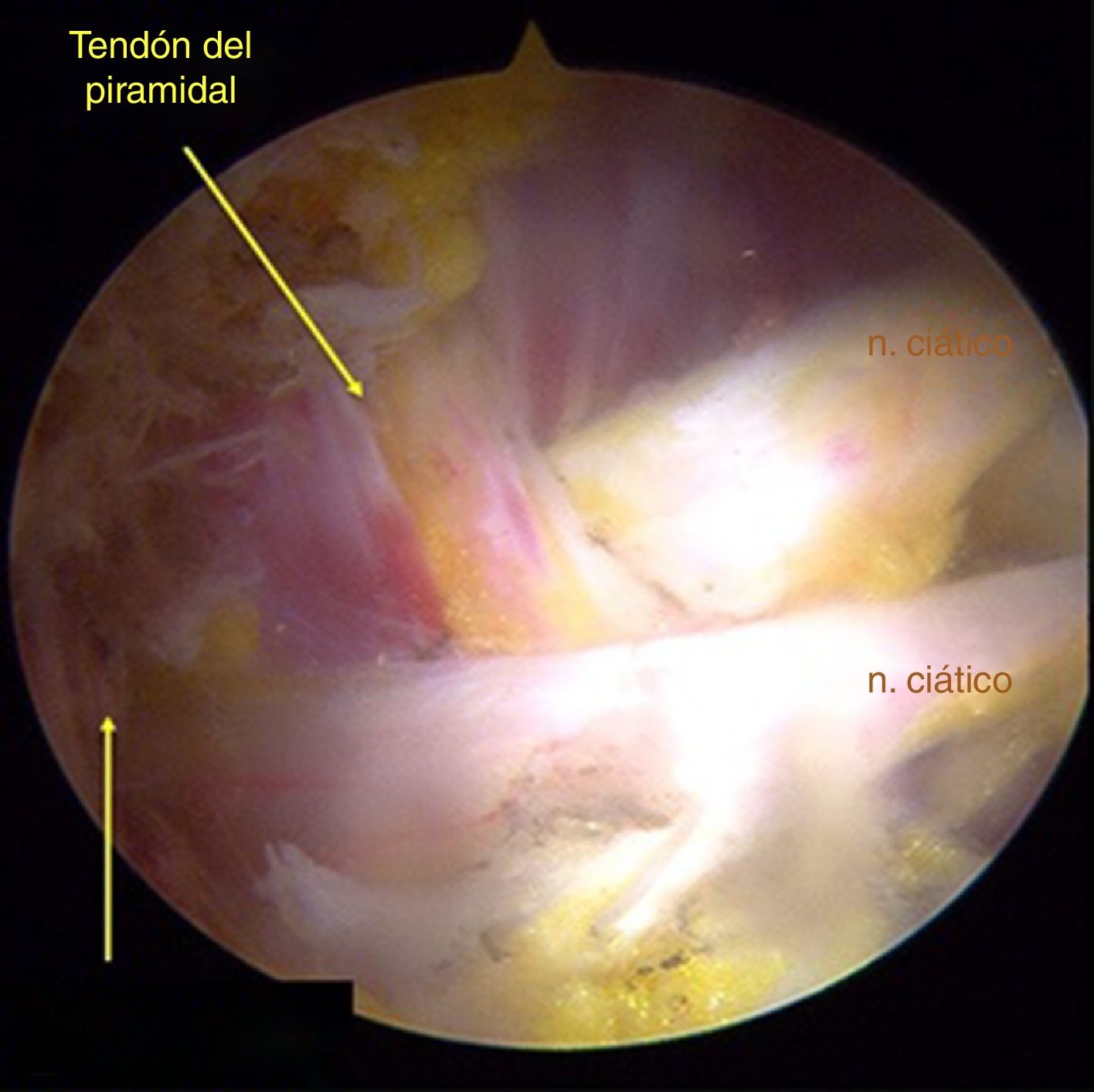
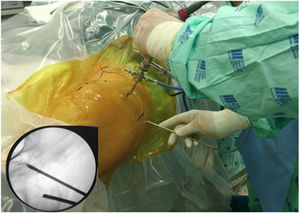
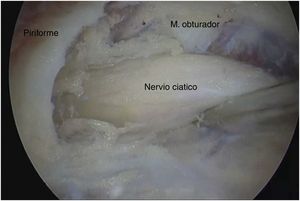
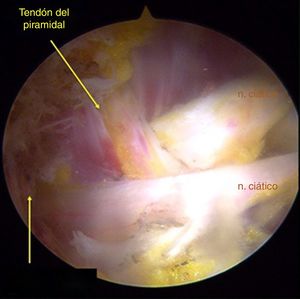
Técnica quirúrgicaPara acceder al ESG se realizaron los portales anterolateral, posterolateral y posterolateral accesorio superior con ayuda del fluoroscopio. Se ingresó el lente por el portal anterolateral, palpando la pared lateral del trocánter mayor y posteriormente deslizándose por su borde posterior para ingresar al ESG con lente de 30° (fig. 3). La inspección del ESG se inició proximal al músculo cuadrado femoral hasta la escotadura ciática mayor (fig. 4). Mediante disección roma se identificó el NC y la causa de atrapamiento para proceder a liberarlo y verificar su movilidad.
Se valoraron los hallazgos anatómicos del NC en cuanto al número de haces y relación de salida de la escotadura ciática mayor con el músculo piriforme con la clasificación descrita por Beaton y Anson7. Para la identificación de las posibles causas de atrapamiento se utilizó la clasificación patogénica de bandas fibrosas/fibrovasculares14. Se consideraron tipo I cuando existían bandas de compresión o de puente que limitaban el movimiento del NC de anterior a posterior; tipo II cuando las cintas adhesivas ejercían tracción lateral desde el trocánter mayor o medial desde el ligamento sacrotuberoso y las que presentaron una distribución indefinida fueron clasificadas como bandas tipo III. Se realizó tenotomía en los casos donde se evidenció compresión del NC por el músculo piriforme y/o obturador interno, la liberación se confirmó por medio de pruebas dinámicas para verificar la movilidad del nervio.
Análisis estadísticoLas variables fueron resumidas con media, mediana, desviación estándar y rango intercuartílico. Para la evaluación de la funcionalidad y el grado de dolor, antes y después de la intervención se realizó la prueba no paramétrica de Wilcoxon o la prueba t de Student para datos apareados, de acuerdo a criterios de normalidad. Se utilizó la prueba de Shapiro-Wilk para evaluar el ajuste a la distribución normal. Este análisis se realizó en Stata® v.13 (StataCorp, College Station, Texas, EE.UU.).
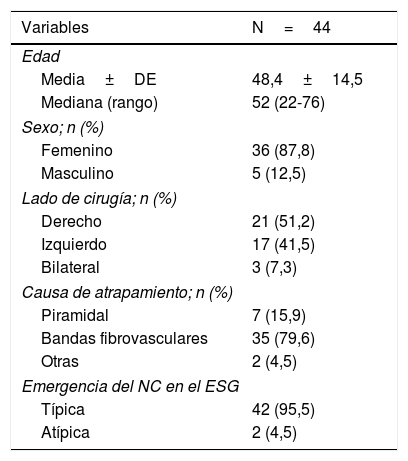
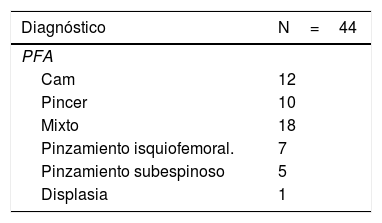
ResultadosSe incluyeron 44 caderas en 41 pacientes (36 mujeres y 5 varones) con un promedio de edad de 48,4±14,5 años. Las bandas fibrovasculares rígidas e hipertróficas fueron la causa más frecuente de atrapamiento del NC. La emergencia del NC de la pelvis tuvo un patrón de salida de un haz único por debajo del músculo piriforme en 42 caderas (95,4%). Dos (4,5%) pacientes presentaron salida con un patrón atípico de un haz a través del músculo piriforme y otro haz por debajo de este (fig. 5). En un caso aislado, el atrapamiento del NC fue atribuido a la aplicación de biopolímeros en la región glútea (tabla 1). Solo un caso fue intervenido por SGP sin presencia de otras enfermedades. En la tabla 2 se describen las enfermedades asociadas para todos los casos.
Características generales
| Variables | N=44 |
|---|---|
| Edad | |
| Media±DE | 48,4±14,5 |
| Mediana (rango) | 52 (22-76) |
| Sexo; n (%) | |
| Femenino | 36 (87,8) |
| Masculino | 5 (12,5) |
| Lado de cirugía; n (%) | |
| Derecho | 21 (51,2) |
| Izquierdo | 17 (41,5) |
| Bilateral | 3 (7,3) |
| Causa de atrapamiento; n (%) | |
| Piramidal | 7 (15,9) |
| Bandas fibrovasculares | 35 (79,6) |
| Otras | 2 (4,5) |
| Emergencia del NC en el ESG | |
| Típica | 42 (95,5) |
| Atípica | 2 (4,5) |
ESG: espacio subglúteo; NC: nervio ciático.
Se realizó tenotomía del músculo piriforme en 21 (47,7%) caderas y en 10 (22,7%) tenotomía del piriforme más obturador interno. En los hallazgos intraoperatorios se encontraron bandas fibrovasculares tipo I en 9 caderas (25,7%); tipo II en 19 caderas (54,3%) y tipo III en 13 caderas (37,1%).
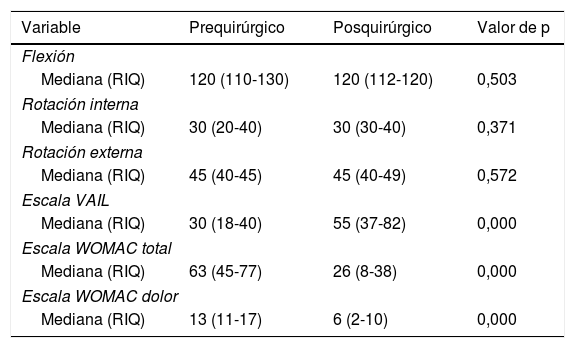
No se encontraron cambios estadísticamente significativos en los ángulos de rotación interna, externa y flexión, después de la intervención (p>0,05). El valor de la mediana del componente del dolor de la escala WOMAC prequirúrgico fue de 13 y en los controles postoperatorios se registró un valor de 6, representando una disminución del 54% con una mejoría estadísticamente significativa (p<0,05). La valoración de la escala de WOMAC total presentó una mediana de 63 puntos en el prequirúrgico con una disminución de 37 puntos al final del seguimiento, equivalente a una mejoría del 58%. La escala VAIL mostró un valor prequirúrgico de 30 puntos con un valor posquirúrgico de 55 puntos (p<0,05) (tabla 3).
Evaluación de arcos de movilidad, funcionalidad y dolor antes y después de la intervención
| Variable | Prequirúrgico | Posquirúrgico | Valor de p |
|---|---|---|---|
| Flexión | |||
| Mediana (RIQ) | 120 (110-130) | 120 (112-120) | 0,503 |
| Rotación interna | |||
| Mediana (RIQ) | 30 (20-40) | 30 (30-40) | 0,371 |
| Rotación externa | |||
| Mediana (RIQ) | 45 (40-45) | 45 (40-49) | 0,572 |
| Escala VAIL | |||
| Mediana (RIQ) | 30 (18-40) | 55 (37-82) | 0,000 |
| Escala WOMAC total | |||
| Mediana (RIQ) | 63 (45-77) | 26 (8-38) | 0,000 |
| Escala WOMAC dolor | |||
| Mediana (RIQ) | 13 (11-17) | 6 (2-10) | 0,000 |
RIQ: rango intercuartílico.
Se presentó una complicación con persistencia de dolor en el área sensitiva del nervio cutáneo femoral posterior a la cirugía. Se realizaron 4 revisiones a los 6 meses después de la intervención con resultados satisfactorios al final del seguimiento.
DiscusiónEl diagnóstico de atrapamiento del NC sigue siendo un desafío para el cirujano ortopédico. El SGP es de comportamiento dinámico, lo que hace difícil encontrar métodos de diagnóstico que permitan su adecuada identificación. Por lo anterior, la realización detallada de un examen físico sumado a la evaluación de imágenes que descarten posibles radiculopatías de origen intrapélvico, son necesarias como parte del estudio de esta enfermedad, requiriendo del uso de un esquema de manejo estandarizado (fig. 2). A pesar que la mayoría de los casos de atrapamiento del NC en el ESG responden bien al manejo conservador, la persistencia del cuadro clínico obliga a buscar otras formas de manejo que sean seguras y reproducibles en los pacientes.
Benson y Schutzer (1999) describieron el atrapamiento periférico del NC por el músculo piriforme de origen postraumático y recomendaron considerar el procedimiento quirúrgico en los casos de persistencia del cuadro de dolor después del manejo conservador8. Posteriormente en el año 2003, Dezawa et al. describen buenos resultados en una serie de 6 casos, en los cuales se realizó una liberación percutánea del músculo piriforme como causa única del atrapamiento del NC10. En el año 2011, Martin et al., realizaron la descripción del ESG, estableciendo limites anatómicos con los elementos que lo conforman (fig. 1) y reconocen que pueden existir otras causas de atrapamiento distintas al músculo piriforme como son las bandas fibrovasculares, músculos obturador interno y gemelos. Nuestros hallazgos concuerdan con lo reportado por Martin et al., debido a que la mayoría de los casos de atrapamiento fueron atribuidos a la presencia de bandas fibrovasculares como principal agente de compresión del NC, seguido de los casos que requirieron de tenotomía del músculo piriforme1. Pérez-Carro et al.15 publican en 2012 su experiencia preliminar en 6 casos con la técnica de Martin et al.1, con buenos resultados con una mejoría en la escala de Harris modificada de 56 a 84 puntos en el posquirúrgico a un seguimiento promedio de 6 meses.
En nuestra cohorte de pacientes se encontró un alivio en el grado de dolor posterior al procedimiento endoscópico. Las escalas de WOMAC y VAIL indicaron una mejoría de la función, similar a lo reportado en el estudio de Martin et al., en el cual se evaluó la funcionalidad con la escala de Harris Hip Score (mHHS), encontrando una puntuación de 78±14,1 puntos en un periodo de seguimiento de 6 a los 24 meses posquirúrgicos, representando un incremento del 43% en la puntuación media del mHHS con relación al prequirúrgico. Park et al., en un seguimiento a 24 meses, encontraron que después de la descomprensión endoscópica del NC, el 90% de sus pacientes mejoraron la sintomatología prequirúrgica específicamente en cuanto a la capacidad de mantener sentados por más de 30min seguidos y la presencia de parestesias12. Carro et al.7, en una revisión de 52 casos a un seguimiento medio de 17 meses, encontraron buenos a excelentes resultados en el 75% (39) de los casos con mejoría en el mHHS de 52 a 79 puntos después de la liberación endoscópica del NC. En los 13 casos restantes, se reportó mejoría de la sintomatología, sin embargo, en este grupo de pacientes se continuó con el uso de analgésicos.
En nuestra experiencia, el conocimiento detallado de la anatomía del ESG y las posibles causas de atrapamiento han sido factores esenciales para asegurar el éxito del procedimiento; debido a que el espacio donde se realiza la cirugía es virtual se prefiere realizar la liberación del nervio con un elemento romo y de forma cuidadosa con el fin de no afectar las estructuras vasculares de las bandas fibrosas y así evitar la presencia de sangrado que fácilmente puede ocasionar la suspensión de la cirugía por pérdida del campo visual. Es necesario identificar inicialmente el nervio cutáneo femoral posterior, el cual se encuentra siempre más hacia anterior y medial al NC para evitar lesionarlo.
Es importante no liberar más allá de lo necesario y realizar movilización temprana de la articulación para evitar nuevamente el atrapamiento del nervio por presencia de cicatrices como sucedió en nuestra cohorte en la cual los casos de revisión se debieron a un atrapamiento del NC por tejido de cicatrización. Estos pacientes presentaron recidiva del cuadro de dolor dentro de un periodo de 6 meses asociado en todos los casos a la falta de movilización temprana del NC por dolor en el postoperatorio.
Por otro lado, es importante vigilar el tiempo y la presión de la bomba de infusión durante el procedimiento quirúrgico, debido a que la escotadura ciática es un canal directo a la región intra-abdominal lo que podría incrementar el riesgo de producir extravasación de líquido al abdomen.
Se realizó la liberación del ESG como único procedimiento en un solo caso, el resto de pacientes requirieron procedimientos adicionales para enfermedades asociadas como pinzamiento femoroacetabular, pinzamiento isquiofemoral y displasia más osteotomía periacetabular. Aunque en todos los pacientes se obtuvo un resultado positivo en la prueba diagnóstica de bloqueo del NC en el ESG, no es posible aseverar si el dolor del paciente mejoró por el manejo de estas enfermedades o por la liberación del NC.
Entre las debilidades del presente estudio se encuentra el reducido número de pacientes incluidos. Sin embargo, esta casuística sirve de base para complementar el escaso conocimiento que se tiene del manejo del SGP. Otra debilidad está relacionada con el uso de las escalas WOMAC y VAIL para evaluar los resultados funcionales de los pacientes, lo que impide la comparación con otras series donde utilizaron la escala mHHs. Estas fueron implementadas porque tienen validación cultural al español y son utilizadas frecuentemente en nuestro medio, además en la actualidad no se cuenta con una escala específica para valorar la sintomatología asociada al SGP. Se hace imprescindible la realización de estudios prospectivos con seguimientos a largo plazo que permitan conocer objetivamente los resultados obtenidos con el manejo endoscópico incluyendo la valoración por medio de escalas de función y dolor con la finalidad de estandarizar algoritmos y/o protocolos en el manejo de la enfermedad compresiva periférica del NC.
Finalmente, se concluye que la liberación endoscópica del NC es una alternativa en el manejo del SGP al mejorar la función y disminuir el grado de dolor, cuando existe una adecuada selección de los pacientes.
Nivel de evidenciaNivel de evidencia IV.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Agradecemos al Instituto de Investigaciones del Centro Médico Imbanaco por su soporte durante la realización de este proyecto.