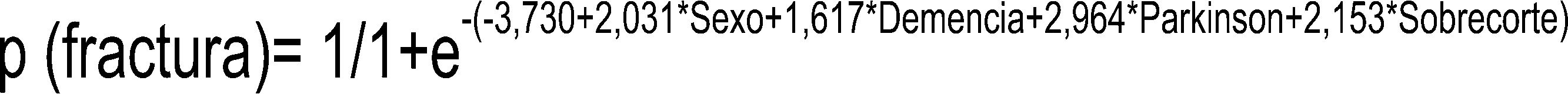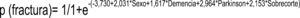Las fracturas periprotésicas tras artroplastia primaria de rodilla cobran gran importancia en nuestro medio debido tanto al aumento de su incidencia, como al reto que suponen para el cirujano. Múltiples factores se han asociado a su producción. El objetivo del estudio fue identificar los factores de riesgo que podían influir en la aparición de estas fracturas, cuáles de todos ellos son modificables y generar un modelo de predicción de probabilidad de las mismas en función de dichos factores.
Material y métodoEstudio analítico, observacional, retrospectivo, no pareado, de 38 casos de fracturas periprotésicas femorales de rodilla y 80 controles con prótesis de rodilla. En total, fueron incluidos en el estudio 118 pacientes, 83 mujeres y 35 hombres con una edad media de 72,49 años. Se recogieron datos sociodemográficos, antecedentes médicos y consumo de fármacos, así como los relativos a la cirugía. Se realizó un análisis uni- y bivariante de los factores determinantes de fractura, usando un modelo de regresión logística para evitar el sesgo de confusión.
ResultadosDe todos los factores estudiados según el modelo de regresión logística, se obtuvo que el sexo femenino (OR = 7,6), la demencia (OR = 5), la alteración motora/párkinson (OR = 19,3) y el sobrecorte femoral anterior (OR = 8,6) eran factores asociados al incremento de riesgo de este tipo de fracturas.
ConclusionesEste trabajo permite concluir que hay factores de riesgo, como son el sexo femenino, la demencia y el párkinson, que aumentan la probabilidad de fractura periprotésica, que son inherentes al paciente y no son modificables. Sin embargo, existe algún otro totalmente modificable que puede evitarse siendo exigente y exhaustivo en la técnica quirúrgica, como es el sobrecorte femoral anterior.
Periprosthetic fractures after primary knee arthroplasty has great importance in our environment due to the increase in their incidence and to the challenge they pose to the surgeon. Multiple factors have been associated with its production. The objective of the study was to identify the risk factors that could influence the appearance of these fractures, which of them are all modifiable and generate a probability prediction model based on these factors.
Material and methodsAnalytical, observational, retrospective, unpaired study of 38 cases of periprosthetic femoral knee fractures and 80 controls with knee prostheses. In total, 118 patients, 83 women and 35 men with a mean age of 72.49 years were included in the study. Sociodemographic data, medical history and drug consumption were collected, as well as those related to surgery. A univariate and bivariate analysis of the fracture determining factors was performed, using a logistic regression model to avoid confusion bias.
ResultsOf all the factors studied according to the logistic regression model, it was obtained that female sex (OR = 7.6), dementia (OR = 5), motor/parkinson's alteration (OR = 19.3) and femoral overcut Previous (OR = 8.6) were factors associated with the increased risk of this type of fractures.
ConclusionsThis work allows us to conclude that there are risk factors such as female sex, dementia and parkinson's that increase the probability of periprosthetic fracture that are inherent to the patient and are not modifiable. However, there is any other totally modifiable that can be avoided by being demanding and thorough in the surgical technique, such as the anterior femoral overcut.
Las fracturas periprotésicas de rodilla son aquellas que se producen en un paciente portador de una artroplastia total de rodilla (ATR), que ocurren a menos de 15cm de la interlínea articular o bien a 5cm del vástago si este existe1. Generalmente se producen en el contexto de traumatismo de baja energía hasta en el 94%2. El aumento de la esperanza y de la calidad de vida en los pacientes da lugar a un incremento de las indicaciones de ATR1,3. Una mayor supervivencia de la población puede dar lugar a una disminución de la calidad ósea periprotésica1,3 y aumentar la incidencia de fracturas periprotésicas, que en la actualidad varía entre 0,2 y 2,5%4 en la zona supracondílea. Estas fracturas cobran importancia en nuestro medio siendo actualmente un tema de cierta controversia, ya que en muchas ocasiones suponen un reto para el cirujano ortopédico, por presentarse en implantes movilizados que complican la técnica quirúrgica y siendo además unas fracturas que afectan principalmente a pacientes de edad avanzada con elevada mortalidad5 y morbilidad6,7 asociada.
Se han descrito una serie de factores que parecen estar asociados a su producción8-10. Los dependientes del paciente son la edad avanzada, sexo femenino8,9 y determinadas enfermedades como la artritis reumatoide, las enfermedades neurológicas, el tratamiento con corticoides y la osteoporosis10,11. En lo que respecta a los factores quirúrgicos se han estudiado el exceso de corte femoral anterior, la presencia de implantes posteroestabilizados y la osteólisis y/o aflojamiento1,4,10,11. Sin embargo, estos factores aparecen reseñados en series clínicas en los que se realiza exclusivamente un análisis univariante, lo que podría introducir un sesgo de confusión que daría lugar a la sobreexposición de diferentes factores.
Nuestro objetivo fue identificar los factores de riesgo que podían influir en la aparición de fracturas periprotésicas, valorando los modificables, y además generar un modelo de predicción de probabilidad de las mismas en función de dichos factores.
Material y métodoEstudio analítico, observacional, retrospectivo, no pareado de 38 casos (fracturas periprotésicas femorales de rodilla) y 80 controles (portadores de ATR sin fractura). El periodo de recogida de casos y controles fue desde enero de 2006 a octubre de 2016 con un tiempo medio de evolución desde la prótesis a la fractura de 9 años.
Definición de caso/paciente: pacientes que ingresaron con una fractura alrededor de componente femoral a menos de 15cm de la interlínea articular1 en ATR primaria, tras traumatismo de baja energía. Se excluyeron pacientes con fracturas tibiales o de rótula (3), cirugía de revisión (5) y fracturas interprotésicas o interimplante (7).
Definición de controles: pacientes intervenidos de ATR primaria sin fractura periprotésica. Una vez identificados los casos, se obtuvo un listado de todas las ATR intervenidas en el mismo periodo de estudio y se aplicó una aleatorización simple manual. Se ordenó dicha muestra por número de historia clínica seleccionando al azar un punto de inicio y a continuación la dirección de movimiento se mantuvo constante a lo largo de toda la tabla, en nuestro caso a la derecha. Por convenio, los últimos números pares (0, 2, 4, 6 y 8) se incluyeron en la muestra y los últimos números nones (1, 3, 5, 7 y 9) se excluyeron del estudio hasta completar el número necesario de controles.
Se recogieron datos sociodemográficos, edad y sexo, así como peso, talla e índice de masa corporal (IMC). Datos clínicos, como la toma de fármacos asociados a disminución de la masa ósea (corticoides), la toma de antidepresivos y/o benzodiacepinas, la presencia de demencia, ceguera, alcoholismo, osteoporosis u osteopenia (tomando como criterio de osteoporosis aquellos pacientes que cumplían criterios clínicos y radiológicos en relación con fracturas previas, con una densidad mineral ósea medida por T-score en la columna, cuello femoral o cadera < –1,0 y > –2,512) o enfermedades reumatológicas y neurológicas (dentro de las enfermedades neurológicas se recogieron aquellas que estaban relacionadas con alteraciones motoras y del equilibrio como la enfermedad de Parkinson [9], ataxia [1] o tetraparesia por ELA [1]).
Desde el punto de vista de la cirugía, se identificó la presencia o ausencia de corte femoral anterior excesivo, el tipo de implante, medición del grosor cortical y diámetro del canal femoral enmm a nivel diafisario medio. La medida se realizó con una regla digital que dispone el programa de visor de imágenes (RAIM Java 2009 _Visor DICOM Java_) tras remuestrear la imagen a partir de una marca radiológica (a escala). Se definió presencia sobre corte femoral en aquellos pacientes en los que se observó una penetración superior a 2mm del implante en la cortical anterior en la radiografía lateral estricta postoperatoria13. También se valoró la presencia de osteólisis o movilización del implante, definiendo implante movilizado como aquel que presentaba criterios radiológicos: osteólisis continua superior a dosmm con alteraciones significativas de la alineación (mayor de 3° en cualquier proyección) del implante o fractura del cemento asociada.
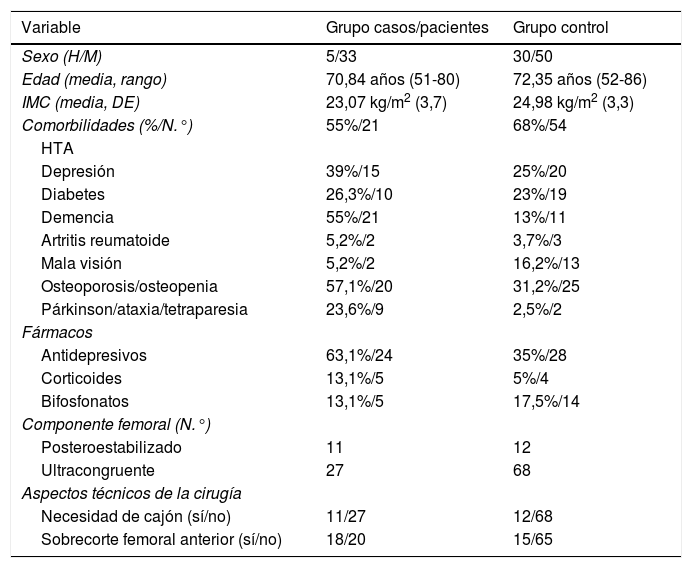
Todos los parámetros sociodemográficos, comorbilidades y aspectos quirúrgicos pueden observarse en la tabla 1.
Tabla comparativa grupo casos y grupo controles
| Variable | Grupo casos/pacientes | Grupo control |
|---|---|---|
| Sexo (H/M) | 5/33 | 30/50 |
| Edad (media, rango) | 70,84 años (51-80) | 72,35 años (52-86) |
| IMC (media, DE) | 23,07 kg/m2 (3,7) | 24,98 kg/m2 (3,3) |
| Comorbilidades (%/N.°) | 55%/21 | 68%/54 |
| HTA | ||
| Depresión | 39%/15 | 25%/20 |
| Diabetes | 26,3%/10 | 23%/19 |
| Demencia | 55%/21 | 13%/11 |
| Artritis reumatoide | 5,2%/2 | 3,7%/3 |
| Mala visión | 5,2%/2 | 16,2%/13 |
| Osteoporosis/osteopenia | 57,1%/20 | 31,2%/25 |
| Párkinson/ataxia/tetraparesia | 23,6%/9 | 2,5%/2 |
| Fármacos | ||
| Antidepresivos | 63,1%/24 | 35%/28 |
| Corticoides | 13,1%/5 | 5%/4 |
| Bifosfonatos | 13,1%/5 | 17,5%/14 |
| Componente femoral (N.°) | ||
| Posteroestabilizado | 11 | 12 |
| Ultracongruente | 27 | 68 |
| Aspectos técnicos de la cirugía | ||
| Necesidad de cajón (sí/no) | 11/27 | 12/68 |
| Sobrecorte femoral anterior (sí/no) | 18/20 | 15/65 |
Los modelos protésicos fueron Nex Gen® (Zimmer) en 5 de los controles y en 9 casos, Apex® (OMNIlife science) en 35 controles y en 6 casos, Natural Knee II® (Zimmer) en 35 controles y 21 casos y Persona® (Zimmer) en 5 controles y 2 casos. El tipo de implante se consideró en función del diseño de los implantes, dividiéndose en dos grupos, modelos posteroestabilizados con necesidad de cajetín femoral y modelos con conservación de cruzado posterior/ultracongruente.
Las fracturas se clasificaron atendiendo a los criterios de Lewis y Rorabeck14 y a los criterios de Su10. Según la clasificación de Rorabeck y Lewis el tipo más frecuente fue el tipo II (60,5%) seguido del tipo I (23,7%), la clasificación de Su más frecuente fue el tipo III (39,5%).
El intervalo medio entre la cirugía sustitutiva y la producción de la fractura fue de 108,3 meses considerándose un 94,7% fracturas tardías al haber transcurrido más de 6 meses desde la cirugía primaria.
El análisis estadístico se dividió en dos partes. Por un lado, la estadística descriptiva en la que se calcularon proporciones y medias con sus correspondientes intervalos de confianza al 95%. Y, por otro lado, en el contraste de hipótesis se utilizó el test de Chi-cuadrado de Pearson en el caso de variables cualitativas. De no cumplirse todos los requisitos para la aplicación de la prueba se aplicaron la corrección de Yates o el test exacto de Fisher. Para las variables cuantitativas se empleó la prueba de t de Student, si cumplían criterios de normalidad, aplicando la U de Man-Whitney en caso contrario. Así mismo se estableció un modelo de regresión logística binaria con el objetivo de evitar el probable sesgo de confusión por el análisis de factores que pueden actuar de forma conjunta. Se utilizó el programa SPSS v. 22.0 y un nivel general de significación p < 0,05.
El tamaño de muestra se estimó usando el programa G * Power versión 3.1.7 (Franz Faul; UniKiel, Düsseldorf, Alemania) software según criterios de evaluación de tamaño muestral mínimo, con un valor α = 0,05 y una β = 0,10 para los factores de estudio. Según estudios previos la frecuencia de exposición en los no enfermos para los parámetros principales modificables del estudio (sobrecorte femoral anterior) fue del 5%12, la frecuencia de exposición entre los enfermos del 30%13, para una odss ratio (OR) = 2,00, con dos controles para cada caso obtenemos una muestra mínima necesaria de 35 casos y 75 controles para obtener conclusiones con significación estadística.
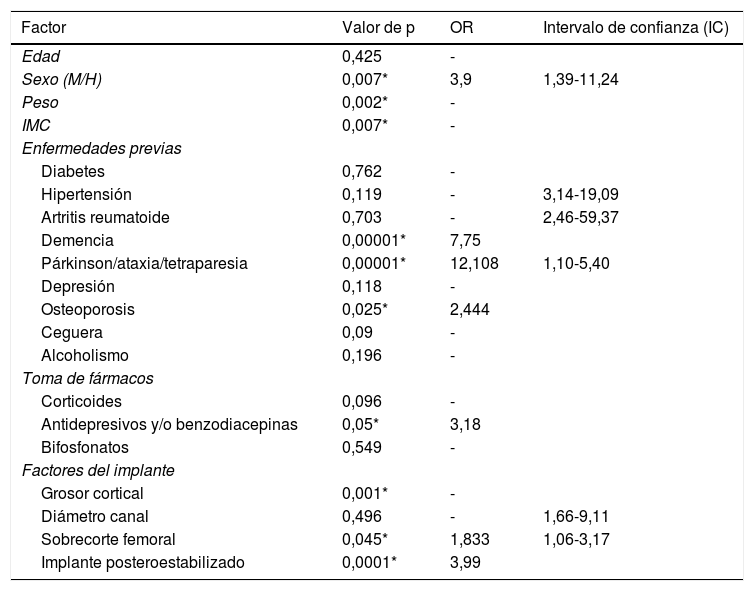
ResultadosEl resultado del análisis univariante se observa en la tabla 2. En cuanto a las características del paciente, el sexo femenino (p = 0,007), el menor peso (p = 0,002) y un menor IMC (p = 0,007) se identificaron como factores de riesgo. En la valoración de enfermedades previas observamos que la osteoporosis (p = 0,025), demencia (p = 0,0000) y alteración psicomotora previa (p = 0,00) parecían influir. Desde el punto de vista de aspectos quirúrgicos observamos que el grosor cortical fue significativamente menor en el grupo de las fracturas (p = 0,0001). También influyeron de forma significativa la presencia de sobrecorte femoral anterior (p = 0,001) y necesidad de cajón (p = 0,045).
Factores relacionados en estudio univariante
| Factor | Valor de p | OR | Intervalo de confianza (IC) |
|---|---|---|---|
| Edad | 0,425 | - | |
| Sexo (M/H) | 0,007* | 3,9 | 1,39-11,24 |
| Peso | 0,002* | - | |
| IMC | 0,007* | - | |
| Enfermedades previas | |||
| Diabetes | 0,762 | - | |
| Hipertensión | 0,119 | - | 3,14-19,09 |
| Artritis reumatoide | 0,703 | - | 2,46-59,37 |
| Demencia | 0,00001* | 7,75 | |
| Párkinson/ataxia/tetraparesia | 0,00001* | 12,108 | 1,10-5,40 |
| Depresión | 0,118 | - | |
| Osteoporosis | 0,025* | 2,444 | |
| Ceguera | 0,09 | - | |
| Alcoholismo | 0,196 | - | |
| Toma de fármacos | |||
| Corticoides | 0,096 | - | |
| Antidepresivos y/o benzodiacepinas | 0,05* | 3,18 | |
| Bifosfonatos | 0,549 | - | |
| Factores del implante | |||
| Grosor cortical | 0,001* | - | |
| Diámetro canal | 0,496 | - | 1,66-9,11 |
| Sobrecorte femoral | 0,045* | 1,833 | 1,06-3,17 |
| Implante posteroestabilizado | 0,0001* | 3,99 |
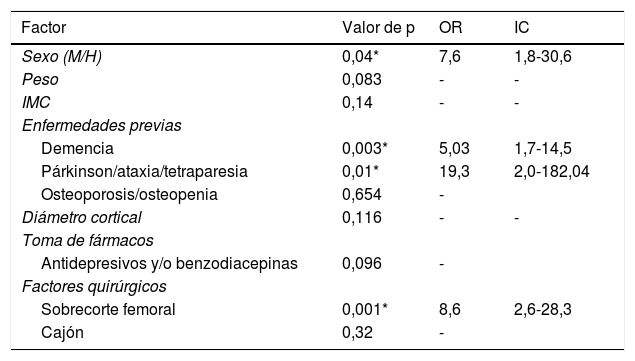
En cuanto al modelo de regresión logística, inicialmente empleamos un modelo de regresión hacia atrás de Wald que determinó que, el IMC bajo, la osteoporosis, los antidepresivos, el grosor cortical y los implantes posteroestabilizados podían considerarse como factores influidos por los demás. En un análisis por introducción se observó que, al eliminar los factores de confusión, el resto de factores alcanzaban valores más altos en cuanto al riesgo de sufrir una fractura periprotésica. Según el modelo de regresión logística son factores de riesgo de fractura periprotésica el sexo, la demencia, el párkinson y el sobrecorte femoral anterior. El factor con mayor asociación es el antecedente de párkinson según nuestra muestra (OR = 19,3; IC = 2,0-182,04; p = 0,01) seguido del sobrecorte femoral anterior (OR = 8,6; IC = 2,6-28,3; p = 0,001) y sexo femenino (OR = 7,6; IC = 1,8-30,6; p = 0,04) (tabla 3). El análisis del modelo de regresión logística podría explicar casi el 65% de la varianza (potencia intermedia). Clasificando correctamente el 78,8% de la muestra con una especificidad del 91,3%. Dicho modelo además genera la siguiente ecuación matemática que podría predecir la probabilidad de fractura (fig. 1).
Factores relacionados en estudio multivariante
| Factor | Valor de p | OR | IC |
|---|---|---|---|
| Sexo (M/H) | 0,04* | 7,6 | 1,8-30,6 |
| Peso | 0,083 | - | - |
| IMC | 0,14 | - | - |
| Enfermedades previas | |||
| Demencia | 0,003* | 5,03 | 1,7-14,5 |
| Párkinson/ataxia/tetraparesia | 0,01* | 19,3 | 2,0-182,04 |
| Osteoporosis/osteopenia | 0,654 | - | |
| Diámetro cortical | 0,116 | - | - |
| Toma de fármacos | |||
| Antidepresivos y/o benzodiacepinas | 0,096 | - | |
| Factores quirúrgicos | |||
| Sobrecorte femoral | 0,001* | 8,6 | 2,6-28,3 |
| Cajón | 0,32 | - |
El sexo femenino, las enfermedades neurológicas y el corte femoral anterior excesivo son los factores con mayor asociación en la aparición de fracturas periprotésicas femorales.
La pérdida del influjo estrogénico tras la menopausia, con la consecuente pérdida ósea, y una mayor esperanza de vida hacen al sexo femenino más susceptible15 de presentar fracturas periprotésicas configurándose como uno de los más factores más influyentes9,16. Un menor estímulo osteoblástico al producirse un descenso de solicitudes mecánicas sobre el fémur asociado a una menor producción de determinadas moléculas asociadas al panículo adiposo, como la estrona o la leptina, hacen que los pacientes con un menor contenido graso tengan una menor densidad mineral ósea incrementando significativamente el riesgo de fracturas15. Ello justificaría la asociación del peso bajo a la presencia de fracturas por fragilidad17,18. La obesidad, al igual que en la literatura, no ha sido relacionada como un factor de riesgo19.
En relación a las variables clínicas, el párkinson, otras enfermedades neurológicas/motoras y la demencia, pueden originar un aumento o mayor riesgo de caídas20–22. Además, se ha descrito que estos pacientes presentan un menor IMC frente a controles sin enfermedad, menor actividad física y fuerza muscular, asociada posiblemente a malnutrición, así como deficiencia de vitamina D20 disminuyen significativamente la densidad mineral ósea lo que podría favorecer la aparición de cualquier tipo de fractura21. La osteopenia se comporta como un factor de confusión debido a las características de la muestra ya que su incidencia aumenta con la edad y es más frecuente en el sexo femenino22–24. En la bibliografía25, encontramos cómo la artitis reumatoide y la toma de corticoides se han asociado a un mayor riesgo de fractura periprotésica, a diferencia de este estudio que no se ha observado asociación. Esto puede ser debido a la baja representación de estos factores en la muestra, menos del 5% en el caso de enfermedad reumática y un 8,6% la toma de corticoides.
En cuanto a los factores derivados de la cirugía, el corte femoral anterior excesivo es el segundo factor de riesgo para fracturas periprotésicas. Este aspecto, genera controversia en la literatura, dado que estudios teóricos indican que con cortes mayores de 3mm la resistencia a la torsión del hueso disminuye de un 29%26 a un 39%27 y la de flexión en un 18%27–29. En el estudio dirigido por Lesh et al.27 sobre 164 fracturas periprotésicas de fémur distal se observó que el corte anterior femoral excesivo estaba presente en el 30% de los casos. Sin embargo, en otros estudios, como el de Ritter et al.28 y el de Gujarathi et al.29, no se han encontrado diferencias. El grosor cortical fue significativamente menor en el grupo de fracturas comportándose como un factor de riesgo. Hay estudios realizados en fracturas interprotésicas, donde se ha observado que corticales más estrechas, con diámetros del canal más anchos, están asociados a fracturas interprotésicas30. Los implantes posteroestabilizados se han asociado tradicionalmente a fracturas periprotésicas por dos motivos31. En primer lugar, por la necesidad de crear un cajetín femoral y por otro lado por la transmisión de fuerzas creada por los implantes de polietileno posteroestabilizados que transfieren sobrecarga o aumento de la tensión en la zona supracondílea. A tenor de los resultados los implantes posteroestabilizados no incrementan por sí mismo el riesgo de fractura periprotésica ya que a pesar de que en el estudio univariante se vio que podía asociarse como un factor de riesgo, al realizar la regresión logística se percibió que estaba influenciado por el resto, comportándose como un factor de confusión.
Reconocemos algunas limitaciones del estudio. En primer lugar, se trata de un estudio retrospectivo de casos y controles muy susceptible a la introducción de sesgos. En segundo lugar, la baja incidencia de algunos factores asociados a las fracturas podría afectar al análisis univariante. Sin embargo, destacar con respecto a otros estudios, que se trata de un modelo matemático multivariante que nos permite un control estadístico de los factores de confusión presentando una sensibilidad global alta (78,8%) con una alta especificidad (91,3%) lo que permitiría una correcta identificación de pacientes susceptibles. Además, se ha seleccionado un tamaño muestral acorde con el objetivo del estudio en función de la potencia y significación estadística que se buscaba.
Con estos datos, podemos concluir que el sexo femenino, la demencia, la enfermedad de Parkinson, otras enfermedades neurológicas y el corte femoral anterior excesivo son los factores con mayor asociación a la aparición de fracturas periprotésicas femorales de rodilla. Los cuatro primeros no son factores modificables, pero su conocimiento y presencia en los pacientes debería poner en marcha un plan multidisciplinar para el control de estas enfermedades en el momento de la indicación de una cirugía primaria de rodilla y durante su seguimiento. El objetivo sería identificar estos pacientes mediante el modelo de predicción de probabilidad (fig. 1), para así controlar y tratar la enfermedad de base, optimizarlos y disminuir la incidencia de caídas, con el objetivo final de disminuir la incidencia de fracturas periprotésicas. Una revisión sistemática sobre la enfermedad de Parkinson proporciona evidencia para la intervención basada en el ejercicio como una opción de tratamiento rentable para la prevención de caídas, no solo desde el punto de vista clínico, sino también coste-efectivo32.
Además, por nuestra parte una cuidadosa técnica quirúrgica, que evite la presencia de sobrecorte femoral, también podría ayudar a disminuir la incidencia de estas fracturas.
Estudios prospectivos y más amplios serán necesarios para valorar si estos resultados se reproducen en pacientes con los factores de riesgo identificados.
Nivel de evidencia IV.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.