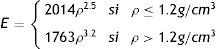No hay consenso en el tratamiento de elección de los recambios protésicos de rodilla con defectos óseos severos. Las opciones son variadas, cada una con sus ventajas e inconvenientes. Los trabajos clínicos publicados tienen sus limitaciones en cuanto al número de pacientes y el poco seguimiento clínico. Se presenta un trabajo biomecánico con elementos finitos comparativo de 5 diseños de implantes tibiales: vástago recto, con offset con/sin suplemento y vainas con/sin vástago, para poder analizar el comportamiento tanto del hueso tibial como del material a lo largo del tiempo. Dentro de las limitaciones que presenta un modelo matemático hemos podido ver que los implantes con vástago recto producen el mayor valor de reabsorción ósea alrededor del vástago, mientras que la menor reabsorción ósea tiene lugar en el hueso de la diáfisis proximal. Las vainas metafisarias tibiales sin vástago producen una menor reabsorción ósea que el resto en el canal medular.
The best management of severe bone defects following total knee replacement is still controversial. Metal augments, tantalum cones and porous tibial sleeves could help the surgeon to manage any type of bone loss, providing a stable and durable knee joint reconstruction. Five different types of prostheses have been analysed: one prosthesis with straight stem; two prostheses with offset stem, with and without supplement, and two prostheses with sleeves, with and without stem. The purpose of this study is to report a finite element study of revision knee tibial implants. The main objective was to analyse the tibial bone density changes and Von Misses tension changes following different tibial implant designs. In all cases, the bone density decreases in the proximal epiphysis and medullary channels, with a bone density increase also being predicted in the diaphysis and at the bone around the stems tips. The highest value of Von Misses stress has been obtained for the straight tibial stem, and the lowest for the stemless metaphyseal sleeves prosthesis.
Uno de los factores fundamentales en el recambio protésico de rodilla es el defecto óseo. Se puede hacer una evaluación preoperatoria mediante el estudio radiológico y TAC, pero va a ser durante el acto quirúrgico cuando vamos a poder definir el tipo de defecto1–3. Si el defecto no está contenido, es decir se trata de un tipo 2 o 3 de Anderson, se pueden utilizar los conos de metal trabecular o las vainas metafisarias4–9. Ambos favorecen un soporte mecánico al implante ayudando a la fijación biológica a largo plazo, disminuyendo la complejidad de la reconstrucción y evitando posibles problemas de transmisión de cargas relacionados con los injertos de banco1,10.
El efecto que tiene este tipo de recambio protésico de rodilla en la reabsorción ósea de la tibia no se conoce aún a largo plazo. Existen diversos estudios computacionales de remodelación ósea basados en el método de los elementos finitos para fijaciones en la componente femoral11,12 y también en la componente tibial pero solo en implantes primarios13–15.
En el presente trabajo, hemos realizado un estudio biomecánico basado en el método de los elementos finitos para analizar el efecto que tiene la incorporación de un implante tibial tras un recambio protésico de rodilla en el proceso de remodelación ósea. Para ello se comparan 5 tipos de diseños de implante tibial: vástago recto, vainas con vástago y sin vástago, vástago con offset, con y sin suplemento.
Las hipótesis de trabajo han sido las siguientes: a) que las vainas metafisarias presentan una mejor transmisión de cargas con un menor efecto punta; b) que el efecto punta es mayor en el caso del vástago recto, puesto que se trata de un vástago ajustado al canal diafisario; c) que el implante tibial con offset puede estar indicado en casos seleccionados de deformidad tibial. Los objetivos generales han sido: a) conocer mejor el comportamiento biomecánico del implante tibial según el diseño protésico; b) mejorar la indicación del tipo de implante para el tipo de tibia que debemos tratar en el recambio protésico. Los objetivos específicos han sido: a) analizar el estado tensional que soporta cada diseño protésico ante cargas fisiológicas para así poder predecir la evolución de la densidad ósea a largo plazo y b) comparar el comportamiento biomecánico de las vainas combinando un vástago corto y sin vástago.
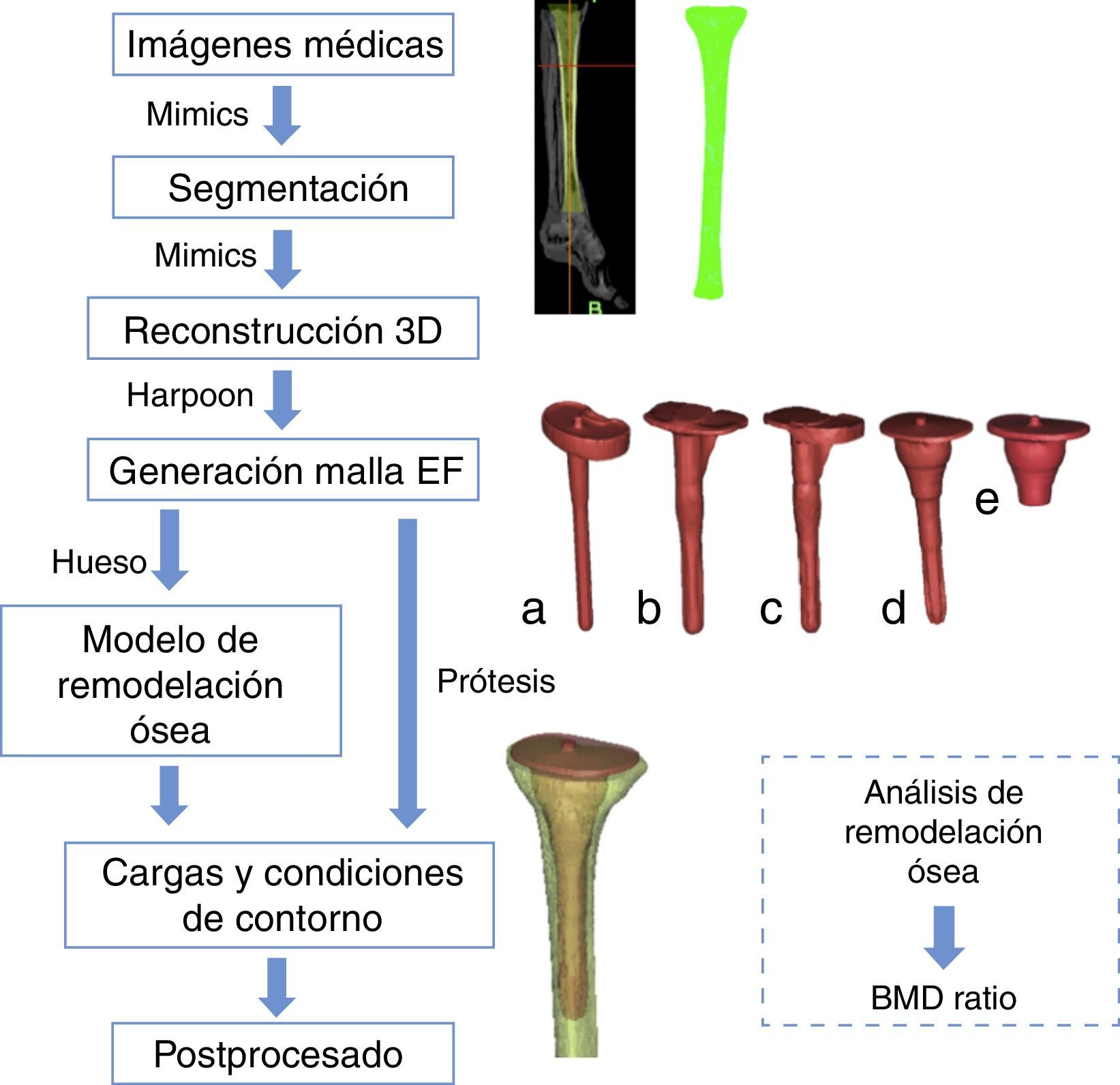
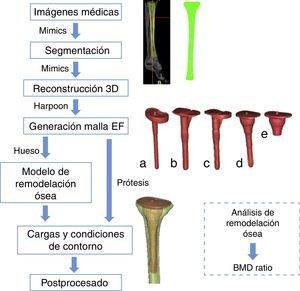
Material y métodosModelos de elementos finitosEl esquema que muestra todos los pasos seguidos para la completa reconstrucción del modelado de las prótesis hasta el análisis final de remodelación ósea ha sido representado en la figura 1. En primer lugar, se partió de las imágenes proporcionadas por una tomografía axial computerizada realizada a la tibia izquierda de un varón de 36 años. Las imágenes se adquirieron en un equipo Brilliance 64 (Philips Healthcare, The Netherlands) utilizando una corriente de 257mA y un voltaje de 120kV. La resolución espacial fue de 0,65×0,65mm, con una matriz de reconstrucción de 768×768. La distancia entre imágenes fue de 2mm. Se analizaron 5 tipos diferentes de modelos de prótesis de rodilla de revisión: vástago recto, vainas con vástago y sin vástago (modelo PFC SIGMA TC3, Depuy, Johnson & Johnson, Warsaw, EE. UU.) y vástago en offset, con y sin suplemento (modelo NextGen Legacy Constrained Condylar Knee-LCCK, Zimmer, Indiana, EE. UU.), (fig. 1 a-e). Los 5 modelos son de titanio y son vástagos no cementados con cementado en superficie.
Se utilizó el software Mimics v. 11 (Materialise, Lovaina, Bélgica) para segmentar y reconstruir los modelos geométricos. En este software se posicionaron los distintos vástagos tibiales en la orientación adecuada. Las mallas de elementos finitos fueron generadas automáticamente con el software Harpoon v. 2 (Harpoon Sharc Ltd, Manchester, UK, 2006), (fig. 1 a-e). Los elementos que componen los modelos eran tetraedros con el fin de reproducir la geometría compleja del hueso con suficiente precisión.
El tamaño de elemento usado (2mm) se encuentra dentro de la región asintótica de convergencia y representa una buena compensación entre precisión numérica y coste computacional.
A las prótesis se les asignaron propiedades de material correspondiente a titanio. El módulo de Young asignado fue de 80GPa y el coeficiente de Poisson fue establecido en 0,32.
La interfaz hueso-prótesis se ha simulado como completamente unida, es decir, como si estuviera perfectamente osteointegrada.
Modelo de remodelación óseaEl hueso es un tejido vivo cuyas propiedades mecánicas cambian según es el estímulo que recibe16. Existen en la literatura diversos modelos matemáticos que reproducen dicho comportamiento; a estos modelos se les conoce como «modelos de remodelación ósea»17–19. En este trabajo se utilizó el modelo de Doblaré y García20,21.
Este modelo de remodelación ósea, siguiendo el trabajo de Doblaré y García20,21 está basado en los principios de la mecánica del daño continuo, usando la teoría de daño como una herramienta matemática para formular la capacidad de remodelación del hueso. Las propiedades mecánicas del hueso dependen de la porosidad y del «fabric tensor», H. El «fabric tensor» H incluye la distribución de la masa de hueso y la direccionalidad de la estructura. Las direcciones principales de H son paralelas a la dirección de ortrotropía del tejido óseo y la influencia de la porosidad (o equivalentemente, la densidad aparente, ρ, o la fracción volumétrica del tejido óseo, vb) vienen dadas por:
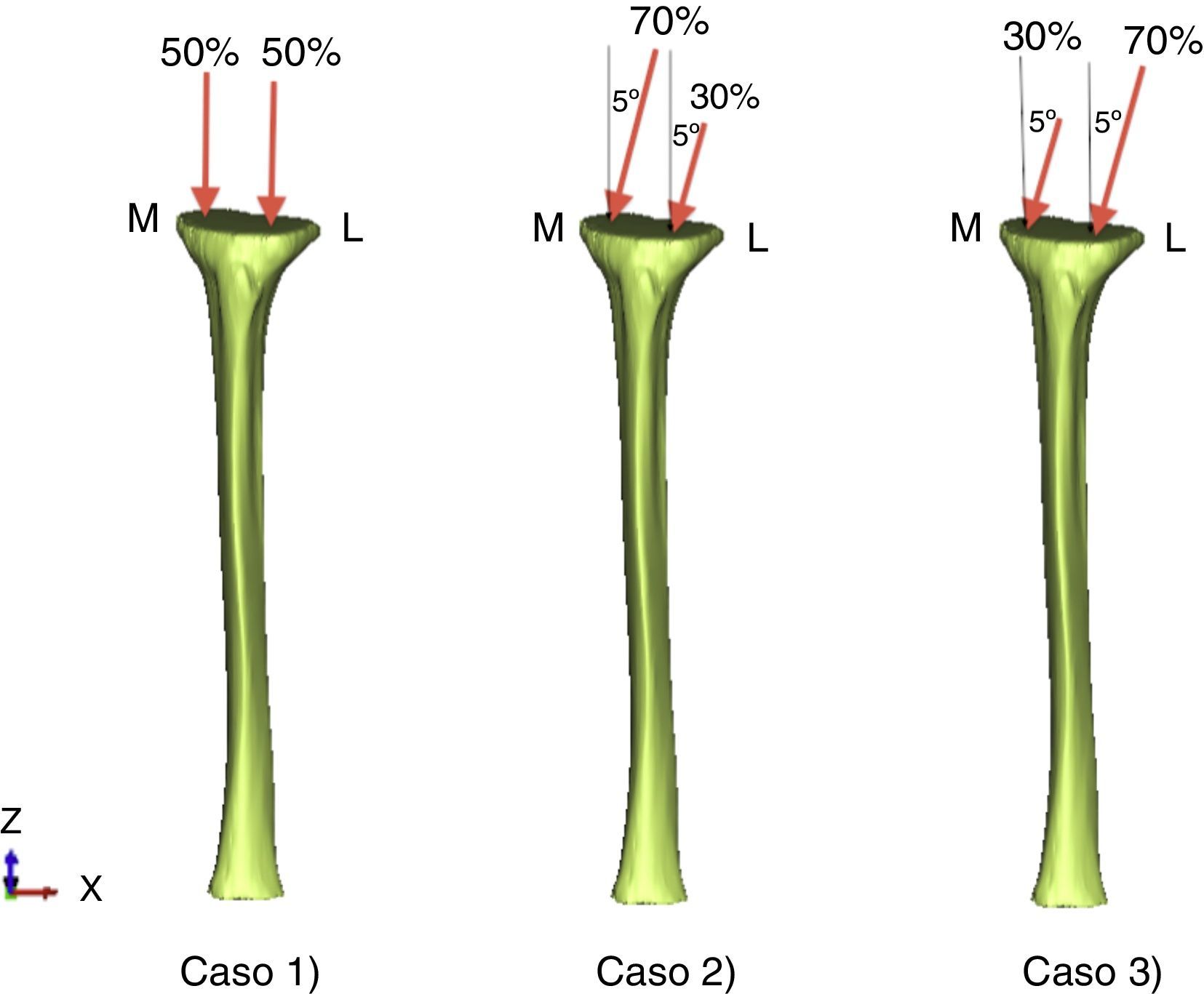
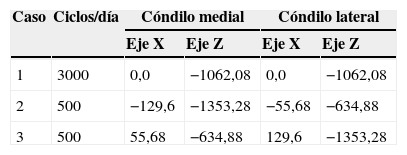
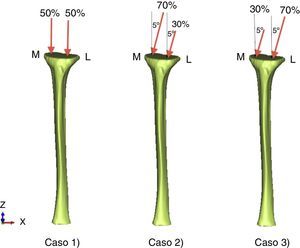
Cargas y condiciones de apoyoLa parte inferior de la diáfisis de la tibia fue restringida a lo largo de las direcciones vertical y horizontal (fig. 2). Las condiciones de carga fisiológicas que se corresponden con las tres etapas más representativas del proceso de caminar fueron consideradas en la simulación, incluyendo la fuerza de reacción en la superficie condilar22,23. Los tres casos de carga fueron (fig. 2): caso 1: la fuerza de reacción de la superficie condilar se distribuyó uniformemente a cada uno de los cóndilos en dirección perpendicular a dicha superficie; caso 2: la fuerza anterior se distribuyó en un 70 y un 30% en los cóndilos medial y lateral, respectivamente, inclinada la fuerza 5° con respecto a la vertical, de modo que la componente horizontal de la fuerza iba en dirección medial; y de manera similar el caso 3 se corresponde con el caso simétrico del caso 2. Los valores de carga considerados para la tibia han sido representados en la tabla 1.
Simulación numéricaEl análisis por elementos finitos (fig. 1) fue realizado usando Abaqus v6.11 (Dassault Systemes Simulia Corp., Providence, RI, EE. UU., 2006). El modelo matemático de remodelación ósea fue implementado en una subrutina de usuario y se simularon así las propiedades del hueso. En concreto, se parte de una situación inicial arbitraria (densidad uniforme ρ=0,5 g/cm3 y comportamiento isótropo del hueso), y se aplicaron las cargas correspondientes al proceso de caminar. Los cambios en la distribución de la densidad ósea fueron calculados durante 300 incrementos de análisis que se correspondían con 300 días de uso de la prótesis (fig. 1). Entre otros aspectos se ha evaluado la distribución de densidad obtenida por la simulación, así como el cambio en la evolución de la densidad mineral ósea que se ha denominado ratio de BMD.
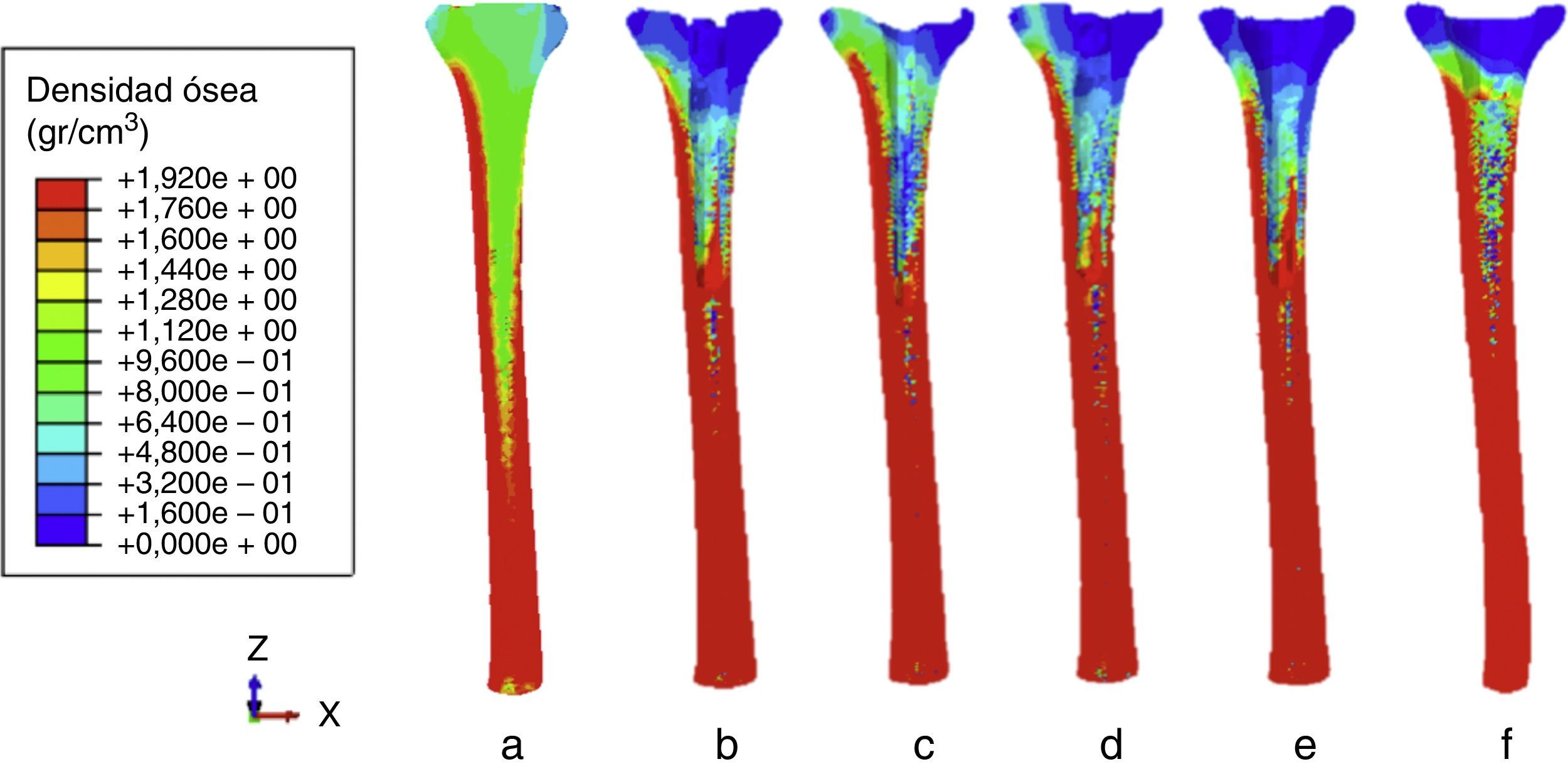
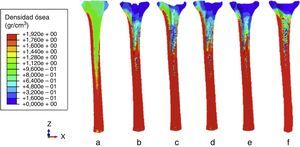
ResultadosLas distribuciones de densidad ósea predichas tras la inserción de la prótesis han sido representadas en la figura 3 (después de 300 días). En todos los casos, se redujo la densidad ósea en la epífisis proximal y en el canal medular, mientras que se incrementó en la diáfisis y en el hueso que rodeaba la punta de los vástagos.
Distribución de densidad ósea (g/cm3) 300 días después de la incorporación de la prótesis. a) Antes de la implantación. b) Vástago con offset sin suplemento. c) Vástago recto. d) Vástago en offset con suplemento. e) Vainas con vástago. f) Vainas sin vástago. (Véanse las diferentes prótesis en la figura 1).
La figura 3 muestra cómo la prótesis con vástago recto producía la mayor reabsorción ósea alrededor del vástago, mientras que la menor reabsorción ósea tenía lugar en el hueso de la diáfisis proximal. El mayor valor de reabsorción ósea en la diáfisis proximal se producía con la prótesis de vainas con vástago. Por otro lado, las vainas sin vástago producían menor reabsorción ósea que el resto de las prótesis, y cualitativamente las que mayor reabsorción ósea generaban eran las prótesis de vainas con vástago y las de offset sin suplemento.
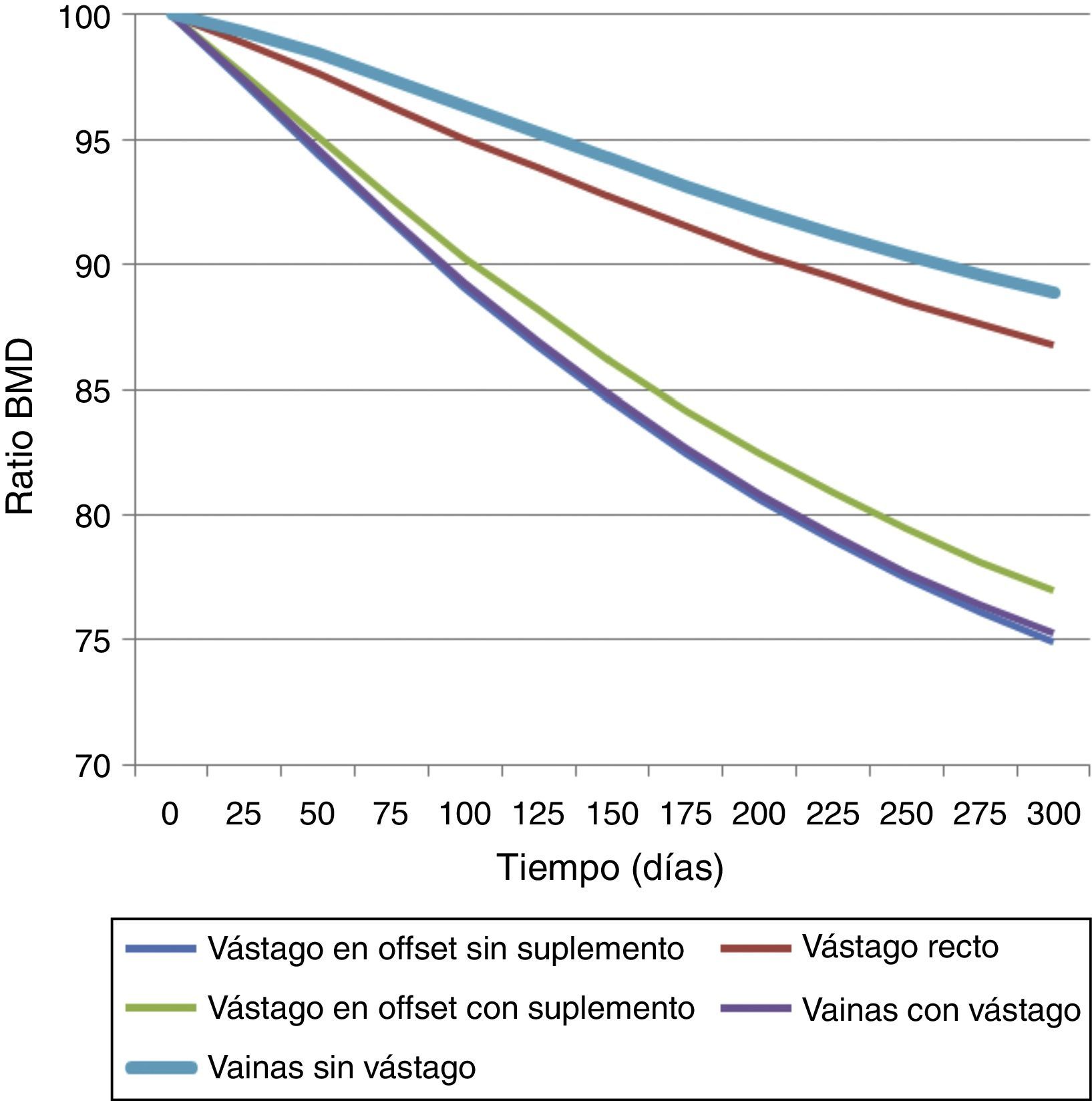
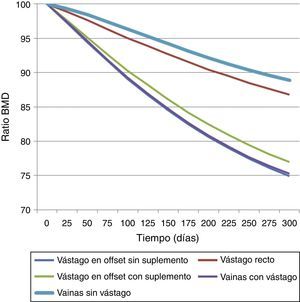
Cuantitativamente, en la figura 4 se muestra la variación del ratio de densidad mineral ósea (BMD) con el tiempo para las cinco prótesis. En las prótesis de vainas sin vástago se predijo la menor variación de densidad ósea, seguida de la de vástago recto. Por el contrario, las que más reabsorción ósea producían eran las de vainas con vástago y la de vástago en offset sin suplemento. Estos resultados respaldaban lo observado en la figura 3.
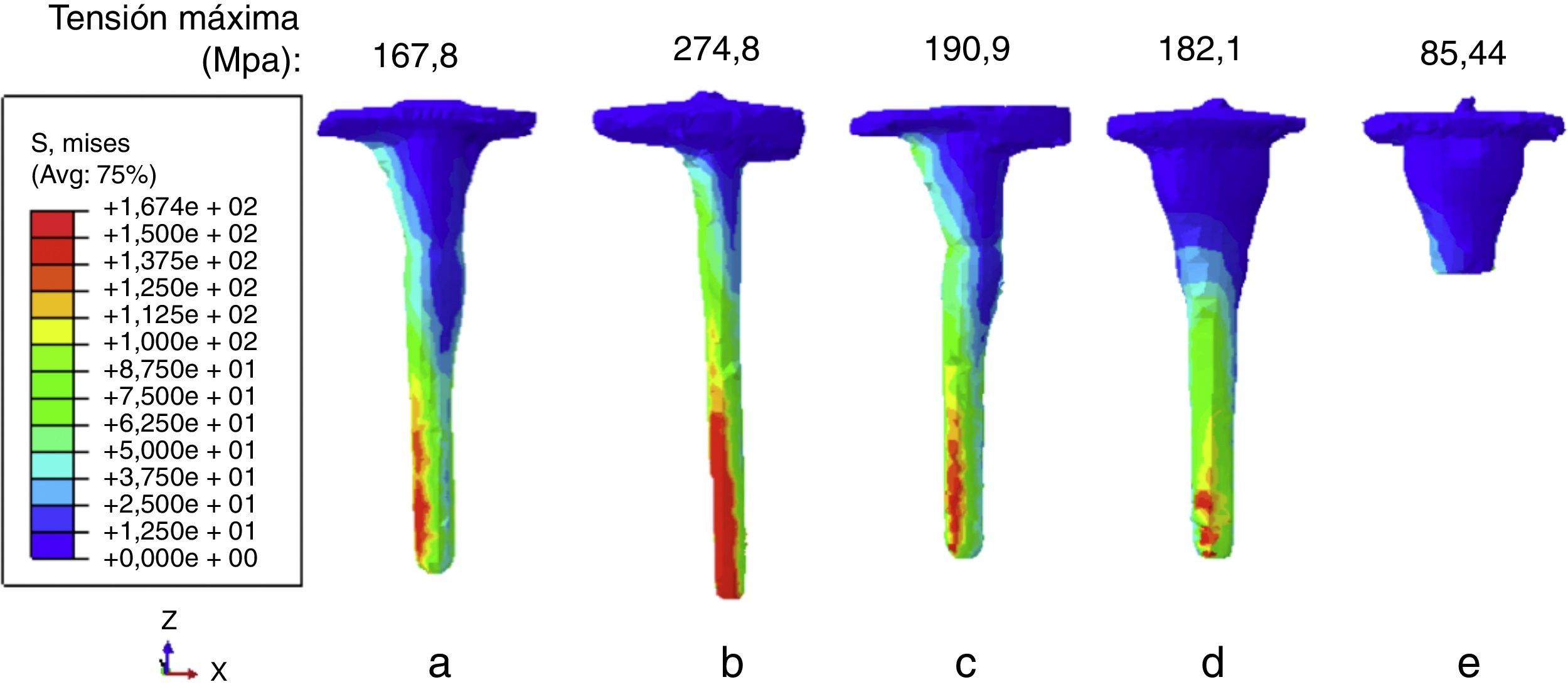
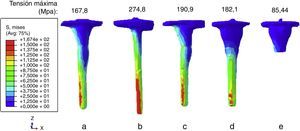
Se ha analizado también la tensión de Von Mises en las prótesis. Ninguna de las prótesis alcanzó su máximo valor de resistencia (450MPa). La distribución de la tensión de Von Mises ha sido representada en la figura 5. El mayor valor ha sido obtenido para la prótesis con vástago recto, y el menor para la prótesis de vainas sin vástago.
DiscusiónEl diseño de los implantes de revisión de rodilla va cambiando; lo mismo ocurre con el manejo de los defectos óseos24. Se calcula que el 82% de los pacientes van a necesitar un aumento femoral o tibial, y un 28% van a necesitar un injerto óseo24.
En los trabajos clínicos no hay consenso en el tratamiento de elección en los recambios protésicos de rodilla con defectos óseos severos. Dentro de los distintos métodos de fijación descritos, las vainas han supuesto una revolución en la filosofía de fijación de los implantes. Haidukewych25 afirma que los vástagos deberían utilizarse de rutina en los recambios puesto que descargan la zona epifisaria con mala fijación. Schmitz et al.10 destacan como ventajas biomecánicas de los conos de tantalio el bajo módulo de elasticidad (3MPa) y la alta porosidad (70-80%), lo que permite una transferencia de tensiones más uniforme en la tibia. Kindsfater et al.11 destacan las ventajas de las vainas sin vástagos: son sencillas de colocar con libertad en la rotación, sin sobresalir del platillo tibial e impactadas a presión sin necesidad de cemento, independientemente de cualquier deformidad diafisaria tibial; no es necesario un preparado del canal tibial con menos riesgo de fisuras intraoperatorias.
Para Agarwal et al.6 la diferencia entre conos y vainas es que los conos requieren cementado del implante, mientras que las vainas se impactan directamente sobre la metáfisis tibial. Las vainas proporcionan una plataforma estable y evitan la necesidad de una resección ósea excesiva. Otra ventaja importante es que con ellas se autoriza una carga completa inmediata.
Tras el análisis de todos los trabajos clínicos publicados, se plantean una serie de limitaciones en relación al tamaño muestral y al seguimiento a medio/corto plazo. Agarwal et al.6 presentan 103 pacientes intervenidos con vainas metafisarias tibiales con un seguimiento medio de 43 meses (30-65). El tamaño adecuado de la vaina debe rellenar el defecto metafisario, y no es necesario añadir un aumento metálico ni rellenar con injerto óseo. El objetivo del vástago estrecho y corto es ayudar al centraje del implante en el canal, mejor que soportar la carga. La osteointegración se estudió en radiología convencional, y se definió como buena aposición ósea en ausencia de radiolucencia entre la vaina y hueso esponjoso en tres interfases de las cuatro existentes, medida en el tercio proximal poroso de la vaina. En 102 casos, la osteointegración era buena. En 2 casos la revisión se realizó por un aflojamiento aséptico y en ambos casos las vainas no llevaban vástago. Alexander et al.7 realizaron un estudio retrospectivo de 28 recambios de rodilla utilizando el modelo de vainas metafisarias no cementadas (modelo Sigma TC3), en pacientes con defectos óseos intraoperatorios tipo 2B y 3, con un seguimiento a dos años. No encontraron ninguna complicación en cuanto a la vaina. Un 23% refería dolor en la punta del vástago, localizado en la diáfisis. En los casos de dolor crónico diafisario de más de dos años, el vástago era largo de más de 150mm de longitud y no era ranurado. Pero no había ninguna relación significativa con el tipo de vástago (ranurado o no ranurado) ni con la longitud del mismo. Tampoco encontraron diferencias con la cantidad de hueso que contactaba con el vástago. Sí que influía el diámetro del vástago. La muestra de este trabajo era pequeña, con una pérdida de 10 pacientes en el seguimiento. Barnett et al.12 estudian de manera retrospectiva 51 casos. En 11 pacientes se colocó vaina sin vástago tibial, para evitar el efecto punta descrito en el trabajo de Alexander7. En ambos trabajos, las series son pequeñas, con una pérdida de pacientes en el seguimiento, a pesar de lo cual, los autores afirman que las vainas es una opción de fijación biológica a largo plazo, que permite rellenar defectos tibiales severos, con buenos resultados clínicos y mínimas complicaciones, favoreciendo la osteointegración del implante sin la necesidad del cemento. Todos coinciden en la necesidad de trabajos clínicos a largo plazo para poder confirmar que este tipo de implante es una buena opción.
Jensen et al.26 estudian con DEXA los cambios de la densidad mineral ósea en un prospectivo randomizado de 40 casos intervenidos con recambios de rodilla modelo NexGen (Zimmer Warsaw, EE. UU.): 17 casos con cono trabecular y 19 sin cono. Los vástagos eran con y sin offset, tanto a nivel tibial como femoral. El patrón de remodelado óseo era muy similar en ambos grupos sin diferencias significativas. El aumento de la reabsorción ósea a lo largo del vástago tibial a los dos años del recambio es notable. En el estudio de elementos finitos no se han encontrado diferencias significativas comparando el vástago con offset y sin offset.
En cuanto a los trabajos biomecánicos, existen trabajos in vitro en modelos de composite de tibia con análisis tensional de la misma27, trabajos experimentales13,28 donde se analiza el reparto tensional en la cortical tibial tras la colocación de distintos tipos de prótesis de rodilla, y estudios matemáticos con elementos finitos para analizar el dolor en punta en los recambios protésicos de rodilla29.
Completo et al.13, valoran experimentalmente en tibias sintéticas mediante galgas en 3D, el reparto de tensiones en la cortical de la tibia proximal con tres tipos de prótesis de rodilla: platillo tibial cementado, vástago ajustado a presión, y solo bandeja tibial con vástago corto monobloque. Ellos observan un aumento del reparto de tensiones en la tibia próximo a la bandeja tibial en el vástago cementado. En el vástago ajustado a presión el reparto de tensiones es menor a nivel proximal, pero es mayor a lo largo del vástago. Esto puede generar reabsorción ósea como se ha observado en los casos analizados en el presente estudio. Existe una concentración de tensiones en la punta del vástago en ambos casos, debido a la reabsorción ósea fisiológica proximal.
Las vainas metafisarias no son un concepto nuevo en la cirugía de revisión, puesto que se utilizaban en implantes modulares en bisagra. Su empleo actualmente es posible en prótesis menos constreñidas, y son una buena opción para tratar defectos óseos metafisarios extensos tibiales. El trabajo aquí presentado coincide con lo observado en los trabajos de Kindsfater11, Agarwal6 y Alexander7 en la necesidad de asociar un vástago corto de pequeño diámetro ranurado, que favorezca el centraje del implante y la evolución a largo plazo.
En todos los diseños tibiales hemos podido observar un aumento de la reabsorción ósea a nivel tibial proximal con un aumento de la densidad ósea a nivel diafisario alrededor de la punta del vástago, similar a lo observado clínicamente (Jensen et al.26). Los implantes con vástago recto producen el mayor valor de reabsorción ósea alrededor del vástago, mientras que la menor reabsorción ósea tiene lugar en el hueso de la diáfisis proximal. A nivel global, las vainas sin vástago producen una menor reabsorción ósea que el resto de modelos, aspecto que se suma a las ventajas indicadas por Kindsfater et al.11.
Como limitaciones del estudio cabe destacar:
- -
Se trata de un modelo matemático con una restricción a nivel de la tibia distal.
- -
Se ha simulado únicamente el proceso de caminar despreciándose otras actividades menos frecuentes como subir escaleras, por ejemplo.
- -
La interfaz hueso-prótesis se ha simulado como completamente unida, es decir, considerando que la prótesis está perfectamente osteointegrada al hueso. Por lo tanto, se ha despreciado la situación inicial en la que dicha interfaz se encuentra suelta y no se ha simulado el proceso de osteointegración.
Como conclusiones podemos afirmar que:
- -
Los mayores valores de tensión se localizan en la punta del vástago.
- -
La prótesis que está sometida a más tensiones es la de vástago recto, lo que justifica el dolor en la punta diafisario.
- -
La prótesis con offset y las vainas con vástago son las que mayor reabsorción ósea producen.
- -
La prótesis que genera una menor reabsorción ósea a lo largo del tiempo es la de vainas sin vástago, por tanto es la que mejor comportamiento biomecánico presentaría a largo plazo.
Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Nivel de evidenciaNivel de evidencia II.
A la Fundación SECOT por el patrocinio de este estudio a través de la ayuda a Proyectos de Investigación del año 2012.