Determinar los efectos de la aplicación de la vancomicina en polvo dentro de la herida quirúrgica, sobre el riesgo de infecciones postoperatorias, pseudoartrosis y efectos adversos en pacientes sometidos a cirugías de columna.
Material y métodosSe realizó un metaanálisis incluyendo los estudios controlados que evaluaron el riesgo de infecciones postoperatorias y/o pseudoartrosis en pacientes sometidos a cirugía de columna a quienes les fue aplicada vancomicina en polvo en la herida quirúrgica.
Los resultados se presentaron como riesgos relativos combinados, con sus intervalos de confianza del 95%. Adicionalmente, se evaluó la frecuencia de complicaciones atribuibles al tratamiento.
ResultadosSe incluyeron 6estudios controlados (3.379sujetos). Los riesgos relativos combinados fueron: infección del sitio quirúrgico, 0,11 (IC95%: 0,05-0,25; p<0,00001), y pseudoartrosis, 0,87 (IC95%: 0,34-2,21; p=0,77). No se encontró heterogeneidad estadísticamente significativa en ninguno de los análisis. En 1.437pacientes tratados no se reportaron complicaciones asociadas al uso de la vancomicina.
ConclusiónLa aplicación de vancomicina en polvo dentro de la herida se asoció con una reducción significativa del riesgo de infecciones del sitio quirúrgico, sin incrementar el de pseudoartrosis o de efectos adversos. Sin embargo, se requieren estudios controlados y aleatorizados, con el fin de confirmar los presentes resultados y realizar recomendaciones más certeras.
To determine the effects of applying vancomycin powder within the surgical wound on the risk of surgical infections, pseudo-arthrosis and adverse events, in patients undergoing spinal surgery.
Material and methodsA meta-analysis was carried out, including controlled studies that evaluated the risk of postoperative infections and/or pseudo-arthrosis in patients undergoing spinal surgery in which vancomycin powder was applied within the surgical wound.
Resultswere presented as pooled relative risks, with its 95% confidence intervals. Additionally, the frequency of complications attributable to vancomycin was also assessed.
ResultsA total of six controlled studies (3,379subjects) were included. Pooled relative risks were: surgical site infection, 0.11 (95%CI: 0.05-0.25; P<.00001), and pseudo-arthrosis, 0.87 (95%CI; 0.34-2.21; P=.77). No statistically significant heterogeneity was found in both analyses. In 1,437patients treated with vancomycin, there were no recorded vancomycin-related adverse events.
ConclusionsApplication of vancomycin powder into the wound was associated with a significantly reduced risk of surgical site infections, without increasing pseudo-arthrosis or adverse events. However, randomized controlled trials are needed, in order to confirm the present results and make recommendations with more certainty.
Las infecciones de la herida quirúrgica (IHQ) son una de las complicaciones más frecuentes y devastadoras de las cirugías de columna vertebral. Su incidencia varía en función de múltiples factores, y se estima que entre el 2,8 y el 11,9% de los pacientes sometidos a cirugías de columna presentarán una IHQ, a pesar de las estrategias convencionales de prevención1,2.
Los pacientes afectados por estas infecciones presentan prolongación del tiempo de hospitalización e incapacidad laboral, menores índices de calidad de vida y, en general, desenlaces notablemente desfavorables, en comparación con aquellos cuyo postoperatorio transcurre sin estas complicaciones1. Adicionalmente, el tratamiento de las IHQ demanda una gran cantidad de recursos económicos, derivados de la prolongación del tiempo de hospitalización, de la utilización de ayudas diagnósticas, de reintervenciones y de antibioterapia intravenosa, entre otros2,3. Por estos motivos, se han investigado múltiples medidas enfocadas a reducir su incidencia al mínimo posible1,4.
La administración de antibióticos intravenosos es quizás la estrategia más utilizada para la profilaxis de las IHQ. Las guías clínicas más recientes del Grupo de Trabajo en Profilaxis Antibiótica de la Sociedad Norteamericana de Cirugía de Columna5 promulgan la administración de profilaxis intravenosa de forma sistemática; sin embargo, se ha demostrado que la magnitud de la reducción del riesgo de IHQ es relativamente baja, lo que ha motivado la búsqueda de otras alternativas6.
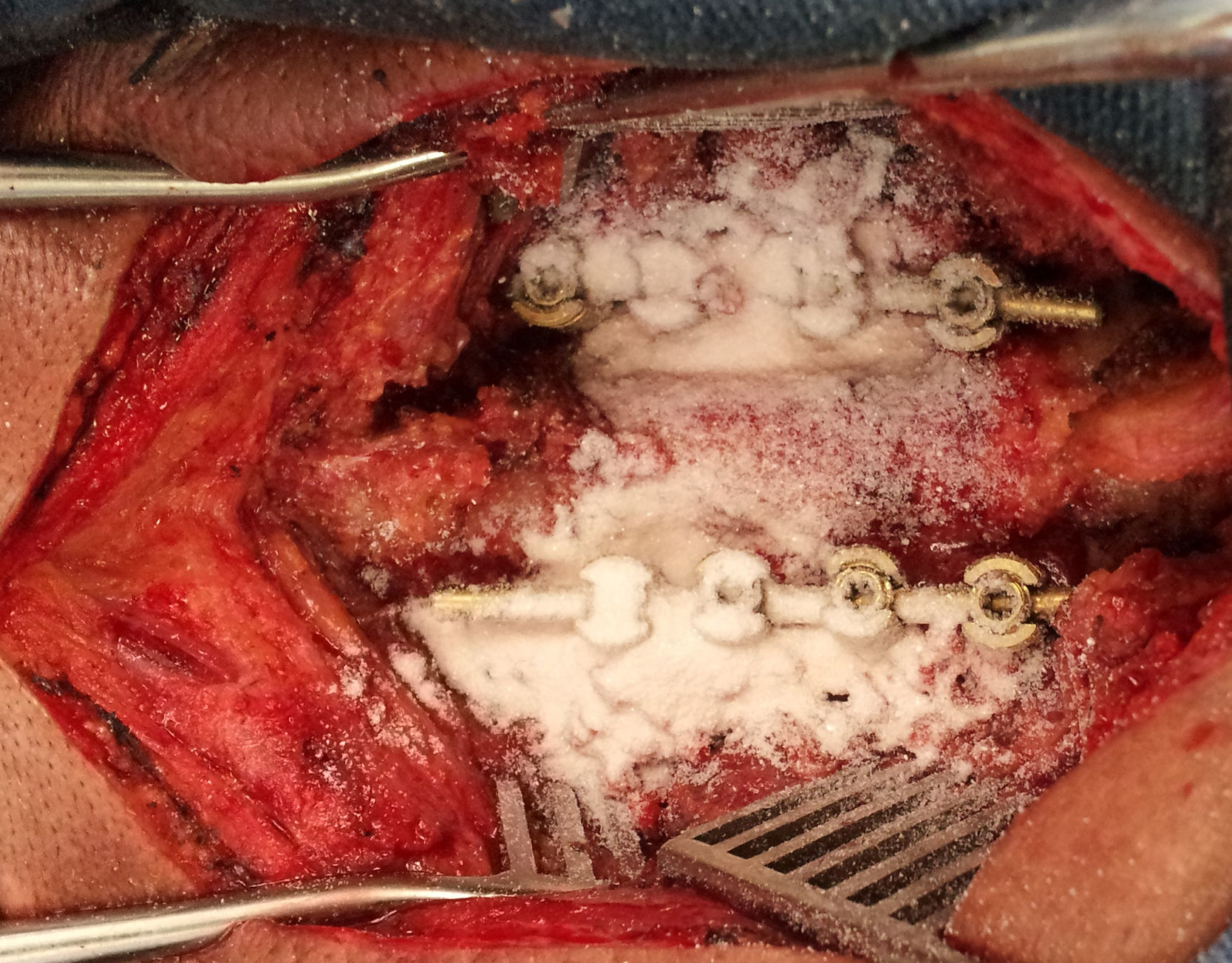
La aplicación de vancomicina dentro de la herida quirúrgica en forma de polvo sin reconstituir constituye una tendencia novedosa para la prevención de las IHQ, y va ganando creciente aceptación entre los cirujanos de columna debido a su bajo costo, a su amplia disponibilidad, a su fácil aplicación, a su buen perfil de seguridad y a la percepción de efectividad7-9. Sweet et al.10 determinaron que mediante la aplicación de vancomicina bajo la fascia muscular, las concentraciones dentro de la herida quirúrgica pueden superar hasta 1.000veces la concentración inhibitoria media necesaria para destruir Staphylococcus aureus resistente a la meticilina, uno de los gérmenes que con mayor frecuencia se aísla de las infecciones de cirugías espinales. Además, su espectro microbicida también cubre otros cocos grampositivos, como Staphylococcus epidermidis y Enterococcus spp., que también pueden causar infecciones espinales postoperatorias3,11.
A pesar de que las propiedades farmacocinéticas de la vancomicina aplicada dentro de la herida quirúrgica la convierten en un método de profilaxis muy atractivo, sus potenciales efectos adversos son una de las principales preocupaciones. La administración intravenosa se ha asociado con reacciones anafilácticas, hipotensión arterial, toxicidad renal, toxicidad otológica e inducción de resistencia antibiótica; sin embargo, aún no se conoce en detalle su perfil de seguridad cuando se aplica tópicamente12,13.
Adicionalmente, existen algunos estudios que describen mecanismos mediante los que la vancomicina podría interferir con la maduración y el funcionamiento de los osteoblastos, lo cual alteraría las vías biológicas implicadas en la fusión ósea. Por tal motivo, varios autores han planteado que las altas concentraciones locales de vancomicina dentro de la herida quirúrgica podrían asociarse a un mayor riesgo de pseudoartrosis14-16.
Debido a su creciente utilización en la práctica clínica, en la última década se han publicado varios estudios que han examinado los efectos de la aplicación de la vancomicina en polvo dentro de la herida quirúrgica durante cirugías de columna; sin embargo, dichos estudios no han sido previamente evaluados mediante un metaanálisis.
El objetivo del presente metaanálisis es determinar los efectos de la aplicación de vancomicina dentro de la herida quirúrgica sobre el riesgo de IHQ y pseudoartrosis en pacientes sometidos a cirugías de columna vertebral, así como los potenciales efectos adversos de esta práctica.
Material y métodosLa revisión sistemática de la literatura se realizó siguiendo el protocolo de la declaración Preferred Reporting Items for Systematic Reviews and Meta-Analyses (PRISMA)17, y para el metaanálisis se aplicaron las recomendaciones de la conferencia Quality of Reporting of Meta-analyses (QUORUM)18.
Búsqueda de la literaturaLa identificación y la clasificación de la literatura se realizaron por 2 revisores de forma independiente, utilizando los siguientes motores de búsqueda: Medline/Pubmed, EMBASE, Google Scholar, Cochrane Controlled Trials Registry y Google Académico. La selección de estudios se llevó a cabo en julio de 2013, sin restricciones de idioma o fecha de publicación.
Las combinaciones de términos utilizados fueron:
- •
«VANCOMYCIN» and «SPINAL SURGERY»
- •
«VANCOMYCIN» and «SPINE SURGERY»
- •
«VANCOMYCIN POWDER»
Tipo de estudios:
- •
Estudios controlados observacionales o ensayos clínicos aleatorizados.
- •
Recuperación de los datos prospectiva o retrospectivamente.
Tipo de participantes:
- •
Estudios que incluyan pacientes adultos o pediátricos.
- •
Estudios que incluyan únicamente pacientes operados mediante vías posteriores, incluyendo técnicas mínimamente invasivas para descompresión o fusión intervertebral.
- •
Estudios que incluyan cirugías de columna cervical, torácica, lumbar o lumbosacra.
Tipo de intervención:
- •
Aplicación local de polvo de vancomicina sin reconstituir dentro de la herida quirúrgica al final de la cirugía, justo antes del cierre.
- •
Dosis local mínima de 500mg.
Tipo de evaluación de desenlaces: Se incluyeron los estudios que reportaron explícitamente la frecuencia porcentual o los datos crudos alguno de las siguientes variables:
- •
IHQ.
- •
Pseudoartrosis.
- •
Efectos adversos y/o complicaciones asociadas al uso de la vancomicina.
- •
Estudios de series de casos y registros poblacionales.
- •
Estudios que incluyeran menos de 10pacientes en cada uno de los grupos.
- •
Estudios en pacientes intervenidos mediante abordajes anteriores.
- •
IHQ.
- •
Pseudoartrosis.
- •
Efectos adversos atribuibles a la aplicación de vancomicina dentro de la herida quirúrgica.
- •
IHQ. Se incluyeron infecciones superficiales (compromiso de piel y tejidos subcutáneos) y profundas a la fascia muscular (incluyendo material de instrumentación). Se excluyeron las infecciones de incisiones simultáneas (p.ej., para toma de injerto óseo autólogo o abordajes anteriores combinados).
- •
Pseudoartrosis. Documentación clínica y radiológica de fallas en la consolidación o fusión ósea, o necesidad de reintervención para una nueva fusión en el mismo nivel intervenido previamente.
- •
Efectos adversos atribuibles a la aplicación de vancomicina dentro de la herida quirúrgica. Incidentes y complicaciones que han sido descritas como potenciales efectos adversos de la administración intravenosa de vancomicina3.
Este proceso se realizó inicialmente mediante la revisión de los títulos de los artículos y sus respectivos resúmenes. Se examinó el texto completo de todos los artículos potencialmente relevantes. Tras la aplicación de los criterios de inclusión y exclusión previamente mencionados, se seleccionaron los artículos para la revisión cualitativa y cuantitativa. Las discrepancias en la selección se resolvieron mediante consenso entre los autores que revisaron la literatura.
Extracción de los datosDos revisores de forma independiente realizaron la extracción de los datos concernientes al diseño y a la metodología del estudio, población total, grupo de patología tratada (degenerativa, traumática, tumoral, inflamatoria o mixta), segmento espinal tratado (cervical o toracolumbar), dosis de vancomicina administrada, tiempo de seguimiento postoperatorio, frecuencia del desenlace primario y de los secundarios.
Evaluación de la calidad metodológicaLos estudios controlados y aleatorizados se evaluaron mediante la escala de Jadad19, la cual realiza la puntuación con base en 3 criterios, que incluyen: descripción de aleatorización (2puntos), cegamiento (2puntos) y explicación de las limitaciones (máximo 3estrellas), siendo 0 el puntaje mínimo y 5 el máximo19.
La escala Newcastle-Ottawa se utilizó para evaluar la calidad de los estudios observacionales. Este sistema de puntuación es el recomendado por el Grupo de Trabajo Cochrane para Metodología de Estudios no-Aleatorizados (Cochrane Non-Randomized Studies Methods Working Group)20. La clasificación se realiza con base en 3criterios: selección (máximo 4estrellas), comparabilidad (máximo 2estrellas) y desenlaces (máximo 3estrellas). Los estudios con puntuación entre 7 a 9 fueron considerados de calidad metodológica alta, entre 4 a 6, moderada, y menor de 4, baja20.
Análisis de los datosLos datos crudos fueron recolectados en una hoja de cálculo de Microsoft Office Excel 2010, desde donde se exportaron para su análisis combinado en el paquete estadístico de la Colaboración Cochrane RevMan 5,0 (Colaboración Cochrane, Oxford, Reino Unido).
Los efectos de la aplicación local de vancomicina sobre cada uno de los desenlaces dicotómicos se estimaron mediante el cálculo del riesgo relativo (RR) combinado, con su respectivo intervalo de confianza del 95%.
Para la selección del método de estimación de los RR combinados se calcularon previamente los índices de heterogeneidad estadística. Para ello, se aplicaron simultáneamente las pruebas de chicuadrado y la medición del estadístico I2. Cuando la prueba de chicuadrado arrojó un valor de p inferior a 0,1, o cuando el estadístico I2 fue mayor de 50%, se consideró que existía heterogeneidad estadísticamente significativa y se utilizó el modelo de efectos aleatorios para la estimación de los RR combinados. Por el contrario, cuando no fue estadísticamente significativa, se empleó el modelo de efectos fijos de Mantel-Haenszel. Los estimados derivados de estudios observacionales se obtuvieron con el modelo de efectos aleatorios20.
La detección de potenciales fuentes de heterogeneidad estadística se llevó a cabo mediante la inspección visual de los gráficos de bosque (forest plots) y el análisis de subgrupos de acuerdo con sitio anatómico de la cirugía (cervical versus toracolumbar) y la utilización de instrumentación. También se utilizaron los gráficos en embudo para detectar posibles sesgos de publicación.
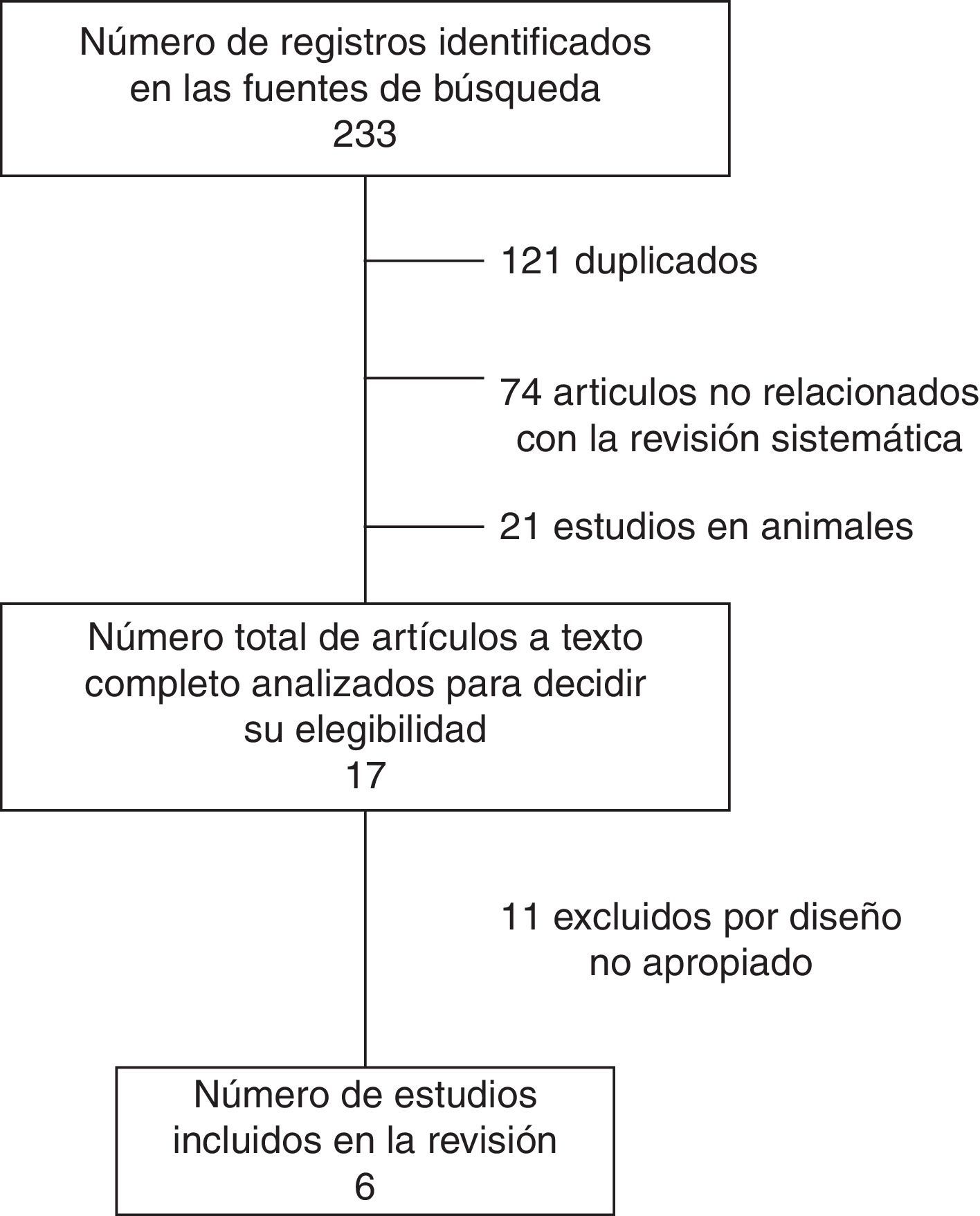
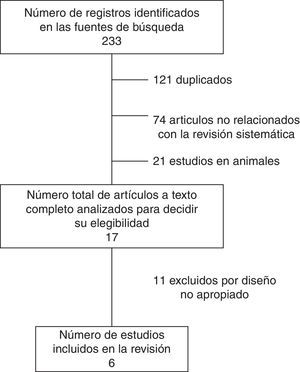
ResultadosResultados de la búsquedaSe identificaron un total de 233 artículos que coincidieron con los términos de búsqueda. Tras la evaluación del resumen, el texto completo y la aplicación de los criterios de inclusión y exclusión, fueron seleccionados 6estudios para la evaluación cualitativa y cuantitativa, los cuales incluyeron un total de 3.379sujetos2,10,21–24. Los resultados de la revisión de la literatura se presentan en la figura 1.
Todos los estudios incluidos fueron observacionales, con diseño de cohortes; uno prospectivo21 y 5 retrospectivos2,10,22-25. Todos fueron realizados en Estados Unidos y publicados posteriormente al año 20112,10,21-24. No se encontraron ensayos clínicos que evaluaran el desenlace primario de este metaanálisis (IHQ).
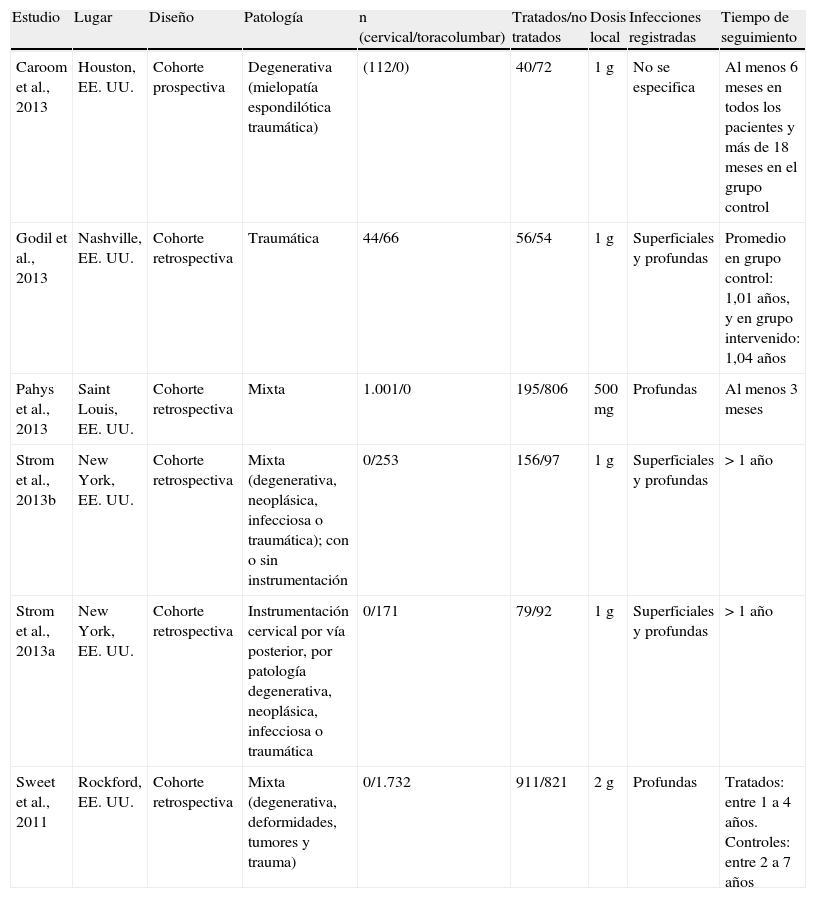
Cuatro estudios fueron realizados en población mixta, involucrando casos de patologías traumáticas, degenerativas, neoplásicas o infecciosas. En 2 estudios se involucraron pacientes con patología infecciosa preexistente (2casos en los 2estudios), pero en ninguno de estos casos se presentaron IHQ23,24. El estudio de Caroom et al.21 analizó de forma exclusiva pacientes operados por mielopatía espondiloartrósica cervical tratados mediante descompresión y fusión instrumentada. Los 6estudios incluidos hacían referencia a pacientes operados por abordajes posteriores y no se encontraron estudios referentes a cirugías por abordaje anterior. Cinco estudios evaluaron la incidencia de infecciones en pacientes que requirieron instrumentación2,10,21,22,24, y únicamente el estudio de Strom et al.23 analizó la tasa de infecciones en pacientes sometidos a cirugía descompresiva lumbar y fusión, con o sin instrumentación. Las características generales de cada uno de los estudios incluidos se presentan en la tabla 1.
Características generales de cada uno de los estudios incluidos
| Estudio | Lugar | Diseño | Patología | n (cervical/toracolumbar) | Tratados/no tratados | Dosis local | Infecciones registradas | Tiempo de seguimiento |
| Caroom et al., 2013 | Houston, EE.UU. | Cohorte prospectiva | Degenerativa (mielopatía espondilótica traumática) | (112/0) | 40/72 | 1 g | No se especifica | Al menos 6 meses en todos los pacientes y más de 18 meses en el grupo control |
| Godil et al., 2013 | Nashville, EE.UU. | Cohorte retrospectiva | Traumática | 44/66 | 56/54 | 1 g | Superficiales y profundas | Promedio en grupo control: 1,01 años, y en grupo intervenido: 1,04 años |
| Pahys et al., 2013 | Saint Louis, EE.UU. | Cohorte retrospectiva | Mixta | 1.001/0 | 195/806 | 500 mg | Profundas | Al menos 3 meses |
| Strom et al., 2013b | New York, EE.UU. | Cohorte retrospectiva | Mixta (degenerativa, neoplásica, infecciosa o traumática); con o sin instrumentación | 0/253 | 156/97 | 1 g | Superficiales y profundas | >1 año |
| Strom et al., 2013a | New York, EE.UU. | Cohorte retrospectiva | Instrumentación cervical por vía posterior, por patología degenerativa, neoplásica, infecciosa o traumática | 0/171 | 79/92 | 1 g | Superficiales y profundas | >1 año |
| Sweet et al., 2011 | Rockford, EE.UU. | Cohorte retrospectiva | Mixta (degenerativa, deformidades, tumores y trauma) | 0/1.732 | 911/821 | 2 g | Profundas | Tratados: entre 1 a 4 años. Controles: entre 2 a 7 años |
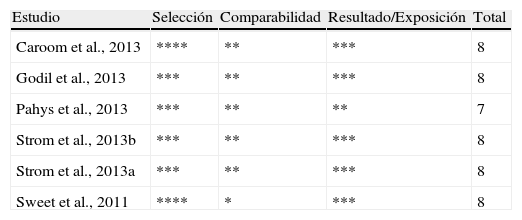
Todos los estudios fueron considerados de alta calidad metodológica, de acuerdo con la puntuación obtenida en la escala Newcastle-Ottawa para estudios de cohortes. Los resultados detallados de cada estudio se presentan en la tabla 2.
Evaluación de la calidad en los estudios incluidos mediante la escala Newcastle-Ottawa para estudios de cohortes
| Estudio | Selección | Comparabilidad | Resultado/Exposición | Total |
| Caroom et al., 2013 | **** | ** | *** | 8 |
| Godil et al., 2013 | *** | ** | *** | 8 |
| Pahys et al., 2013 | *** | ** | ** | 7 |
| Strom et al., 2013b | *** | ** | *** | 8 |
| Strom et al., 2013a | *** | ** | *** | 8 |
| Sweet et al., 2011 | **** | * | *** | 8 |
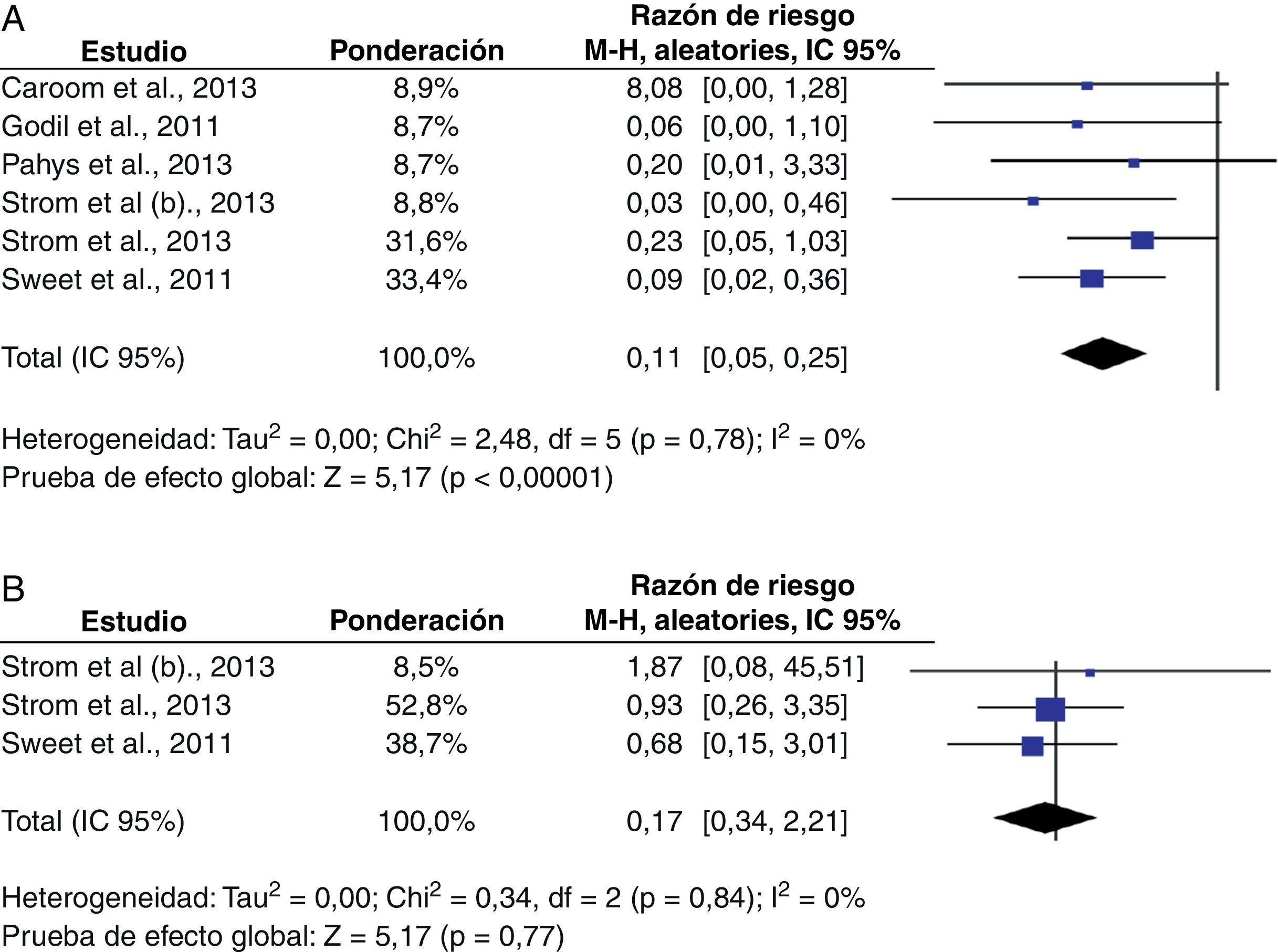
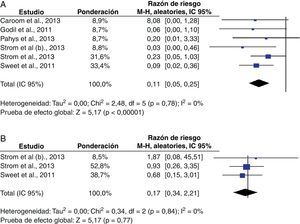
Seis estudios evaluaron el riesgo de IHQ, involucrando un total de 3.379individuos2,10,21-24. Al final del periodo de seguimiento, la incidencia en pacientes tratados fue del 0,28%, mientras que en el grupo control fue del 3,70%. El RR combinado entre los estudios que evaluaron este desenlace fue 0,11 (IC95%: 0,05-0,25), cumpliendo el criterio preestablecido de significación estadística (p<0,00001). Los índices I2 y el valor de p no demostraron heterogeneidad significativa (0% y 0,78, respectivamente) (fig. 2).
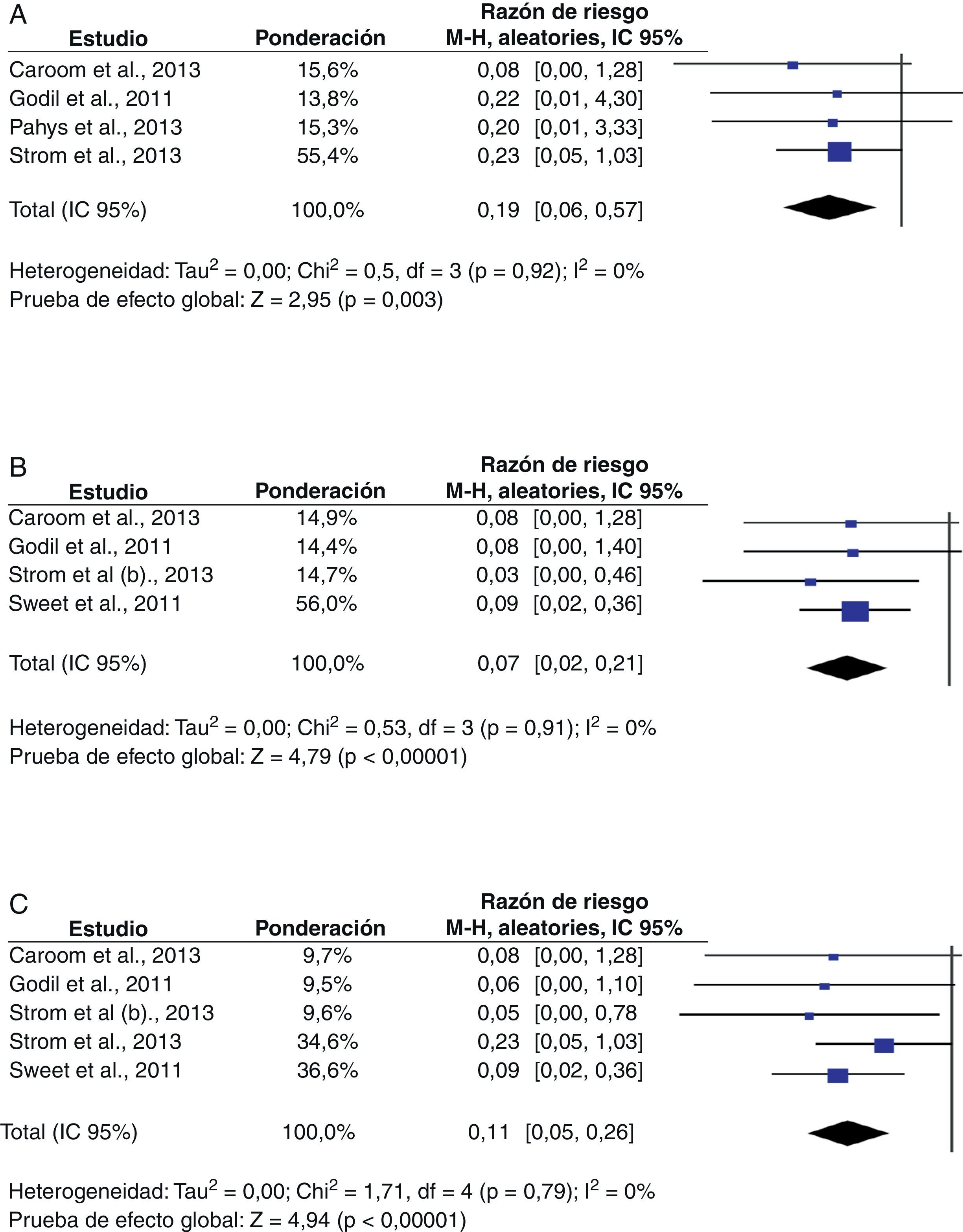
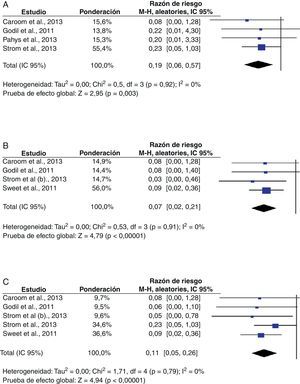
El efecto beneficioso del tratamiento también se observó en la mayoría de los subgrupos analizados, salvo en los pacientes cuyas cirugías no incluyeron instrumentación. El subgrupo de pacientes sometidos a cirugías de columna cervical estuvo constituido por 1.328sujetos, incluidos en 4estudios2,21,22,24. El RR combinado para IHQ fue 0,19 (IC95%: 0,06-0,57; p=0,003). El análisis del estadístico I2 demostró que la heterogeneidad no fue estadísticamente significativa (0%). El subgrupo de pacientes cuya cirugía se realizó en segmentos toracolumbares estuvo conformado por un total de 2.163individuos, involucrados en 4estudios2,10,21,23. La aplicación de la vancomicina en polvo también se asoció con menor riesgo de IHQ, dado que el RR combinado fue 0,07 (IC95%: 0,02-0,21; p<0,00001), y los índices no demostraron heterogeneidad estadísticamente significativa (I2=0%) (fig. 3).
En el subgrupo de las 2.290 cirugías instrumentadas, evaluadas en 5 estudios2,10,21,23,24, el riesgo de IHQ fue menor con la aplicación de vancomicina (RR=0,11; IC95%: 0,05-0,26; p<0,00001) (fig. 3). Los pacientes del subgrupo a quienes no se les implantó material de instrumentación provinieron exclusivamente del estudio realizado por Strom et al.23, por lo que no fue posible estimar el RR combinado.
PseudoartrosisEste desenlace fue evaluado por 3estudios, que incluyeron un total de 2.156sujetos10,23,24. La incidencia de pseudoartrosis fue del 0,7% en los pacientes tratados, y en el grupo control fue del 0,9%. El análisis mostró que el RR combinado de pseudoartrosis fue 0,87 (IC95%: 0,34-2,21), lo cual no fue estadísticamente significativo (p=0,77). Las pruebas de chicuadrado y el valor del estadístico I2 no demostraron heterogeneidad estadísticamente significativa entre los estudios (p=0,84 y 0%, respectivamente) (fig. 2).
Complicaciones atribuibles al uso de la vancomicina en polvoEn ninguno de los 1.437 individuos tratados con vancomicina incluidos en los 6estudios observacionales se registraron incidentes o complicaciones relacionados con la aplicación del fármaco dentro la herida quirúrgica2,21,23-25. Por tal motivo, no fue posible realizar los análisis comparativos.
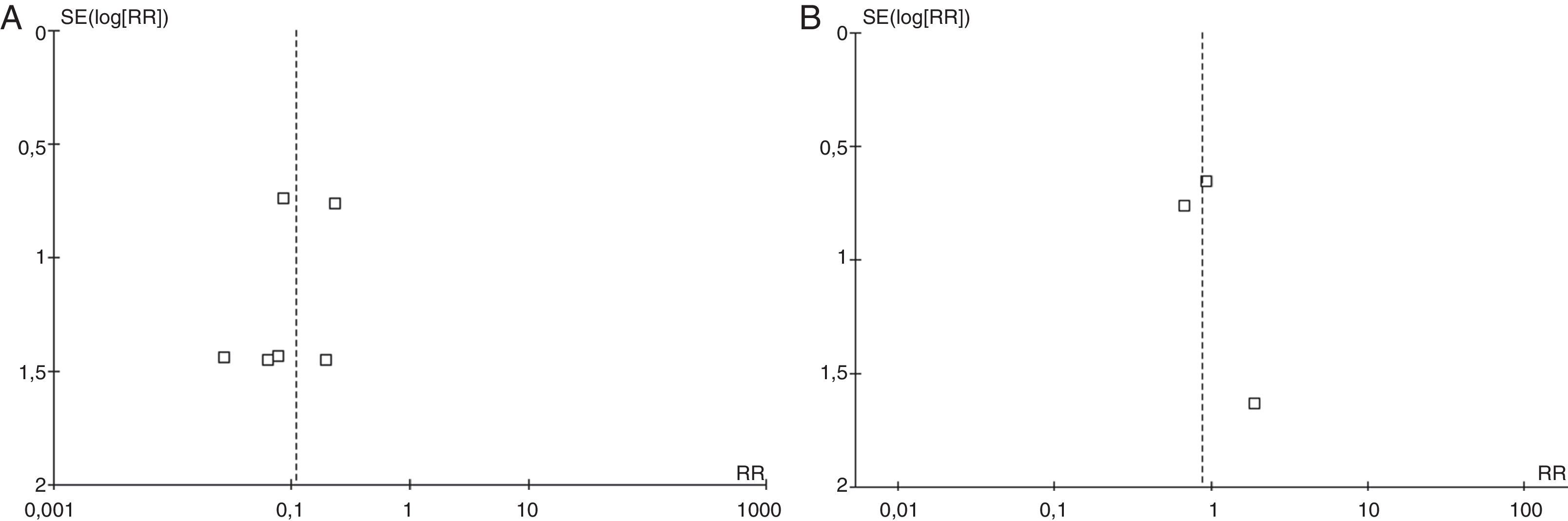
Riesgo de sesgos entre los estudiosLos estudios observacionales incluidos fueron considerados con bajo riesgo de sesgos, debido a su alta calidad metodológica. La detección de los riesgos de sesgos de publicación mediante los gráficos en embudo no demostró asimetrías en ninguno de los desenlaces (fig. 4).
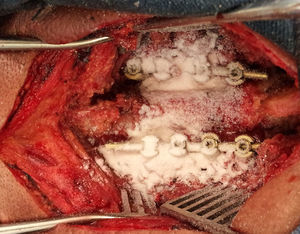
DiscusiónEl presente metaanálisis describe los efectos de la aplicación de vancomicina dentro de la herida quirúrgica en pacientes sometidos a cirugía de columna vertebral, demostrando una reducción estadísticamente significativa en el riesgo de IHQ. Estos hallazgos brindan sustento científico a esta práctica, la cual está ganando aceptación entre los cirujanos de columna a nivel mundial. De acuerdo con un estudio realizado por Glotzbecker et al.7 con 277cirujanos de columna adscritos a la Pediatric Orthopaedic Society of North America/Scoliosis Research Society, el 24% de los encuestados reportaron utilizar la vancomicina en polvo de forma rutinaria, administrada directamente dentro de la herida quirúrgica o mezclada con el injerto óseo utilizado durante las fusiones intervertebrales (fig. 5), y con base en la evidencia emergente, es posible que este porcentaje aumente.
La incidencia de IHQ varía en relación con la región anatómica de la columna vertebral que haya sido intervenida. Se ha demostrado que los procedimientos realizados en la columna cervical por vía posterior tienen mayor riesgo, en comparación con el de las cirugías toracolumbares23,24. Por tal motivo, se decidió realizar un análisis de estos 2 subgrupos, el cual mostró que los efectos son aplicables en ambos segmentos espinales.
Adicionalmente, también se consideró el mayor riesgo de infección que supone la utilización de instrumentación espinal. Sin embargo, los efectos preventivos también fueron observados en los pacientes que requirieron cirugía instrumentada, mientras que no fue posible determinarlos en las cirugías sin instrumentación, debido a que solo se obtuvieron datos procedentes de un subgrupo de 77pacientes estudiados por Strom et al.23.
A pesar de las teorías que señalan el potencial efecto tóxico que podrían tener las altas concentraciones de vancomicina dentro de la herida quirúrgica sobre los osteoblastos, el análisis del RR combinado indica que no existe diferencia estadísticamente significativa en el riesgo de pseudoartrosis, lo cual posiblemente esté relacionado con la rápida repoblación de estas células en el lecho de fusión, tan pronto las concentraciones de vancomicina disminuyen rápidamente dentro de la herida quirúrgica10.
Se planeó realizar el análisis de las complicaciones relacionadas con la aplicación de la vancomicina mediante la estimación del RR combinado, aunque ello no fue posible debido a que no se registraron efectos adversos en los 1.437pacientes tratados, lo cual resalta el perfil de seguridad de esta vía de aplicación. Dos series de casos también han descrito similares hallazgos10,11. En un estudio retrospectivo de 1.512pacientes operados durante 6años consecutivos, Molinari et al.11 no encontraron mayores tasas de complicaciones relacionadas con el uso de vancomicina en un centro de alto nivel de atención en trauma. En dicha serie, tan solo registró un paciente que presentó insuficiencia renal postoperatoria luego de una cirugía electiva (0,07% de todos los casos). No obstante, también cabe mencionar que la insuficiencia renal es una de las potenciales complicaciones en los pacientes sometidos a cirugías espinales, con una incidencia estimada del 1,6%26,27.
A pesar de que en el pasado se reconocía la nefrotoxicidad como una de las principales complicaciones del uso de la vancomicina intravenosa, la revisión de consenso publicada en 2010 por las Sociedades Americanas de Enfermedades Infecciosas, de Farmacólogos del Sistema de Salud y de Farmacólogos en Enfermedades Infecciosas reconoce que existe muy poca evidencia de esta asociación cuando se utiliza en monoterapia, pero se señala que puede potenciar la lesión renal inducida por otros fármacos como los aminoglucósidos28. También se han presentado casos de nefrotoxicidad cuando la dosis de vancomicina supera 4g al día, o las concentraciones plasmáticas sobrepasan los 28mg/l, las cuales superan en varias decenas de veces las concentraciones sanguíneas que se alcanzan con su aplicación local13,28.
En la serie de Molinari et al.11 también se presentaron 2casos (0,13%) de hipoacusia transitoria, la cual se recuperó durante el periodo postoperatorio temprano. La toxicidad otológica, así como la renal, no han sido bien establecidas en los pacientes que reciben vancomicina; sin embargo, se cree que también pueden estar relacionadas con concentraciones plasmáticas por encima de los rangos terapéuticos28. Otro potencial efecto adverso de la aplicación tópica de vancomicina es el colapso circulatorio, aunque la única evidencia de esta complicación proviene de un caso anecdótico informado recientemente por Mariappan et al.12 y no han sido documentadas complicaciones similares.
LimitacionesEn la interpretación de los hallazgos del presente metaanálisis deben reconocerse varias limitaciones propias de su metodología y de los estudios que fueron incluidos. Quizás la de mayor importancia involucra el diseño de los estudios analizados, ya que todos fueron observacionales2,10,21-24. Aunque los resultados fueron consistentes, tal como se evidenció en los bajos índices de heterogeneidad (I2=0% en todos los análisis), y la magnitud del efecto benéfico fue estadísticamente significativa, las recomendaciones de la Colaboración Cochrane enfatizan en que los metaanálisis de estudios controlados aleatorizados son los más idóneos para evaluar los efectos de una intervención en salud, debido a que permiten anular los potenciales sesgos de selección que pueden alterar los resultados de los estudios observacionales20. Es por ello que las recomendaciones acerca del uso de vancomicina deberán actualizarse tan pronto como los ensayos clínicos se encuentren disponibles.
Otra potencial limitación de este metaanálisis fue la evaluación de posibles riesgos de sesgos de publicación. Este procedimiento se realizó mediante la inspección visual de los gráficos en embudo, en la cual no se demostraron asimetrías. Sin embargo, debido al bajo número de estudios incluidos, la certeza de su interpretación puede alterarse28.
Adicionalmente cabe señalar que en el estudio de Pahys et al.22 el grupo control fue heterogéneo, ya que en algunos pacientes la asepsia prequirúrgica se realizó con preparaciones alcohólicas, lo cual se asoció con un menor riesgo de IHQ, y ello supondría un riesgo de sesgos de selección en el grupo control, disminuyendo la magnitud del efecto del tratamiento.
Otra de las consideraciones que deben valorarse referentes al uso sistemático de la vancomicina dentro de la herida quirúrgica es el desarrollo de resistencia bacteriana a los antimicrobianos, especialmente el surgimiento de Enterococcus spp. y Staphylococcus aureus resistentes a la vancomicina. Uno de los principales factores asociados al desarrollo de estas cepas es la subdosificación, ya que el microorganismo se mantiene expuesto por lapsos de tiempo relativamente prolongados a concentraciones que no lo erradican28. Un estudio prospectivo realizado por Gans et al.13 demostró que, en 87pacientes pediátricos, la aplicación de 500mg de vancomicina en polvo dentro de la herida quirúrgica no producía incrementos en la concentración sistémica, la cual se mantuvo indetectable (<2,0μg/ml) en 86 de los 87pacientes desde el primer día postoperatorio, lo cual sugiere que el riesgo de inducción de resistencia bacteriana podría ser bajo. Sin embargo, aún no se dispone de estudios enfocados específicamente a resolver esta incertidumbre.
ConclusiónLa aplicación de vancomicina en polvo dentro de la herida se asoció con una reducción estadísticamente significativa del riesgo de IHQ, sin incrementar el riesgo de pseudoartrosis o de los efectos adversos relacionados en la vancomicina. Sin embargo, se requieren estudios controlados aleatorizados, con el fin de confirmar los presentes resultados y realizar recomendaciones con mayor certeza.
Nivel de evidenciaNivel de evidencia II.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
FinanciaciónLa financiación del presente estudio provino de una beca del Grupo de Investigación en Ciencias de la Salud y Neurociencias (CISNEURO).
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.