En la cirugía mínimamente invasiva del cuello poco se ha evolucionado considerando que usualmente se acompaña de disecciones extensas, dolorosas y prolongadas en tiempo operatorio. Este tipo de cirugía que denominamos como: “cirugía en mínimos espacios del cuello”, es una línea de trabajo del grupo y a finales del 2015 se inició el programa de cirugía endoscópica de cuello. En junio del 2016 intervinimos una paciente joven con carcinoma papilar de tiroides, utilizando la Tiroidectomía Axilar Endoscópica Video Asistida (TAEVA) con equipo Endoeye Flex 3D. Se observaron claras ventajas al usarlo, como alta resolución visual, buena profundidad de campo y versatilidad derivada de la flexibilidad de la cámara que evitó el intercambio de lentes rígidos de 0°, 30° y 70°, lo que acortó el tiempo operatorio. Hasta donde se tiene conocimiento es el primer caso de TAEVA 3D publicado.
Little has evolved in minimally invasive neck surgery, considering that this is usually accompanied by extensive, painful, and prolonged operative time in dissections. This type of surgery is called “Minimum space surgery of the neck”, and is a line of work of our group. For this reason, an endoscopic neck surgery program was started in 2015. A young patient with papillary thyroid carcinoma was intervened in June 2016 using Endoscopic Axillary Video assisted thyroidectomy (TAEVA) with equipment EndoEYE Flex 3D. Clear advantages were observed including high visual resolution, good depth of field, versatility derived from the flexibility of the camera that avoided the exchange of inflexible 0°, 30°, and 70° lenses, and shortening the operating time. To our knowledge, it is the first case of 3D TAEVA published.
Desde el inicio de la cirugía laparoscópica abdominal se han diseñado múltiples abordajes endoscópicos en diferentes sitios del cuerpo. El área de cabeza y cuello no ha quedado excluida de esta tendencia mundial y en 1996 Gagner describió una paratiroidectomía subtotal endoscópica con insuflación de dióxido de carbono usando 4 trocares cervicales1. Seguidamente, Huscher et al. publicaron una técnica similar para la tiroidectomía endoscópica2.
Debido a la discriminación que sufrieron las mujeres jóvenes, con cicatrices visibles en el cuello luego de intervenciones quirúrgicas se impulsaron las tiroidectomías con incisiones no visibles en esta área del cuerpo3. Así surgieron múltiples descripciones de tiroidectomías mínimamente invasivas video asistidas (MIVAT, minimally invasive video-assisted thyroidectomy, por sus siglas en inglés) con accesos remotos cervicales y extracervicales, dentro de las cuales se cuentan el abordaje bilateral a través: del seno y axila (BABA, bilateral axillar breast approach, y ABBA por sus siglas en inglés); de la pared torácica anterior; de la axila, y a través de incisión retroauricular (facelift, por su nombre en inglés)3–8.
Para sostener el espacio operatorio estos procedimientos requieren de la insuflación de gas (dióxido de carbono) a baja presión o de retracción externa de los colgajos de piel con separadores complejos. Adicionalmente, se deben utilizar instrumentos, equipos endoscópicos o robóticos con dispositivos ópticos usualmente rígidos de 0, 30 y 70 grados de visión 2D o 3D9,10.
Recientemente el Grupo de Cabeza y Cuello del Instituto Nacional de Cancerología de Bogotá (INC) ha trabajado en el desarrollo de técnicas mínimamente invasivas denominadas como: “cirugía de mínimos espacios en el cuello”; dichas intervenciones se convirtieron en una línea de trabajo. Razón por la cual, a finales del 2015, iniciamos el programa de tiroidectomías endoscópicas. En junio del 2016, se realizó la primera tiroidectomía axilar endoscópica asistida con visión tridimensional (TAEVA 3D) usando un equipo EndoEYE Flex 3D (hasta donde tenemos conocimiento la primera reportada en la literatura médica), por lo que decidimos comunicar la experiencia y la descripción de la técnica.
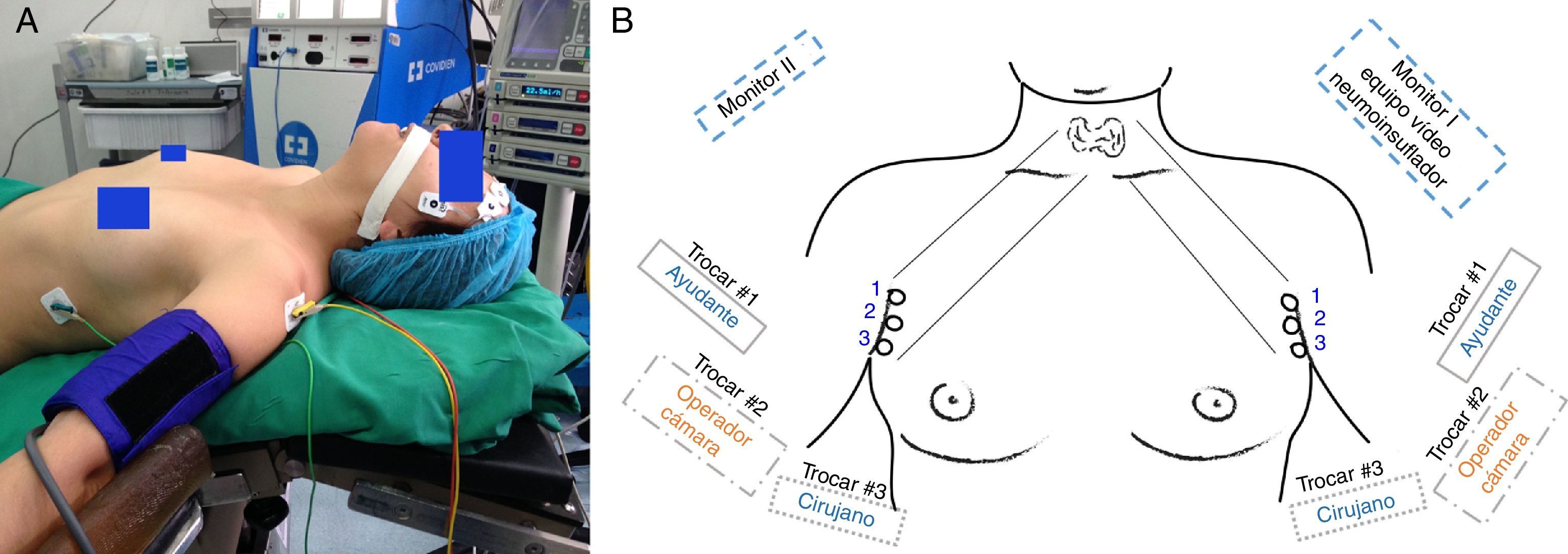
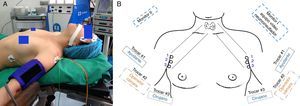
Caso clínicoEs el caso de una mujer de 35 años a quien se le realizó una ecografía de cuello por molestias inespecíficas, la cual reportó un lóbulo derecho de 36×15×10mm volumen 3 cc, un lóbulo izquierdo de 36×13×14mm volumen 3,8 cc, dependiente de este último en el polo inferior un nódulo sólido de 11×11×10mm, heterogéneo con calcificaciones en su interior, sombra lateral y flujo periférico a la exploración doppler color de aspecto sospechoso. El mencionado nódulo se analizó con ACAF (aspiración con aguja fina), que fue conclusivo para carcinoma papilar de tiroides (categoría VI) según la clasificación del consenso de Bethesda (clasificación utilizada de forma rutinaria en el INC)11,12. En consideración a que el nódulo era mayor de 11mm de diámetro y que la paciente tuvo la expectativa de una intervención quirúrgica sin cicatriz visible en el cuello, se tomó la decisión de realizarla con TAEVA, que para este caso y a manera de demostración se nos facilitó un equipo de la casa Olympus HD Endoeye Flex 3D, el cual consta de una cámara cuya parte distal es flexible y da la opción de rotación vertical y horizontal con ángulos de hasta de 100o. Dotado en su interior con un doble juego óptico, que permite visión tridimensional en monitores LCD 3D HD, que se conectan a un sistema de video EVIS Exera III, con la ayuda de gafas cinema 3D se puede obtener visualización tridimensional y buena profundidad de campo (fig. 1).
Indicaciones y contraindicacionesDebido a que las cirugías en cuello con incisiones remotas tienen un auge muy importante en los últimos años, las indicaciones y contraindicaciones se han venido redefiniendo. Pero en términos generales, los mejores candidatos para tiroidectomías mínimamente invasivas video asistidas (MIVAT) son aquellas mujeres jóvenes que no deseen cicatriz en el cuello, con antecedente de cicatrices hipertróficas o con queloide. Para este caso las hemos aplicado como una guía objetiva, por lo que las especificamos a renglón seguido.
Indicaciones para cirugías MIVAT3,10–12:
- -
Tiroides total con volumen menor a 30ml
- -
Tiroides con cáncer papilar T1
- -
Sin evidencia de metástasis locales o regionales
- -
Tiroides con nódulo menor a 3,5cm de diámetro mayor
Contraindicaciones relativas para cirugía MIVAT3,10,13,14:
- -
Antecedente de radiación en el cuello
- -
Antecedente de tiroiditis
- -
Volumen tiroideo total mayor a 30ml
- -
Antecedente de cirugía endoscópica de cuello
- -
Antecedente de cirugía abierta de cuello
- -
Enfermedad de Graves
- -
Disfunción cardiaca, respiratoria y de la coagulación
Debido a que la TAEVA 3D es una técnica modificada de la tiroidectomía endoscópica vía transaxilar, que utiliza la línea axilar anterior con disección subcutánea infraclavicular; se decidió emplear como referencia las indicaciones y contraindicaciones generales de las MIVAT.
Descripción de la técnicaUna vez verificado el consentimiento informado de la paciente para realizar el procedimiento, previa corroboración de su deseo a someterse a esta intervención tiroidectomía total axilar endoscópica video asistida en decúbito supino y con leve hiperextensión del cuello en posición de Trendelenburg invertida, se fijó el circuito de anestesia general y los elementos de monitorización en la línea media. Sobre los miembros superiores (MMSS) extendidos, en un ángulo de 70° en relación al eje del cuerpo, se demarcaron los puertos de entrada sobre la línea axilar anterior de forma bilateral en el borde externo del músculo pectoral mayor (fig. 2).
- -
Distribución de sala de operaciones y del equipo quirúrgico
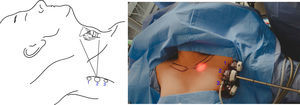
A. Posición quirúrgica para tiroidectomía axilar endoscópica video asistida (TAEVA): leve hiperextensión del cuello y posición de Trendelenburg invertida, brazos extendidos en ángulo 70 grados. B. Campos operatorios y posición del equipo: demarcación bilateral sobre línea axilar anterior de los puertos de entrada de los tres trocares: Trocar #1 de 5mm pinza Endo Clinch®II. Trocar #2 de 12mm cámara flexible. Trocar #3 de 5mm pinza LigaSure MaryLand de 5mm 37cm.
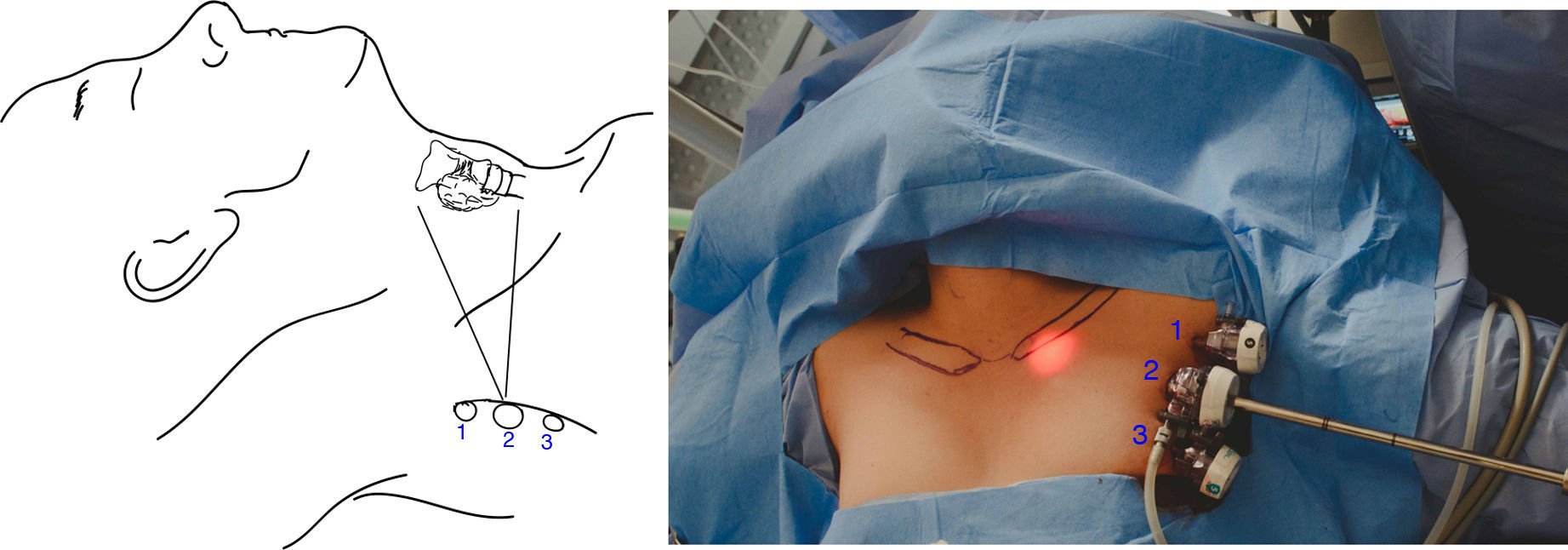
En la cabecera del paciente estaban el equipo de anestesia y dos monitores LCD 3D HD, derecha e izquierda. MMSS con ángulo de 70°. Los operadores se distribuyeron en disposición ipsilateral al tiroides que se iba a extirpar, el primer ayudante de pie y en posición cefálica al miembro superior, el operador de la cámara sentado en posición medial y el cirujano principal de pie caudal y proximal al cuerpo de la paciente (fig. 3).
- -
Instrumentos
Después de una curva de aprendizaje que conllevó la práctica en laboratorio de cirugía experimental con cerdos vivos, medicina legal con cadáveres frescos y posteriormente aplicación de la técnica con modificaciones propias, se procedió a realizar las primeras intervenciones en varios pacientes. Para este caso en particular, utilizamos diferentes implementos como son un trocar Versaport® Bladeless optical de Covidien de 10mm 12cm de longitud, dos trocares Versaport® Bladeless de Covidien 5mm 12cm de longitud, disector Ligasure Maryland® Covidien 5mm 37cm longitud, pinza Endo Clinch®II 5mm 37cm de longitud y Endocatch® Covidien de 10mm.
- -
Técnica quirúrgica TAEVA 3D
- -
Implantación de trocares e instrumental: incisión transversa de 10mm sobre el borde externo del músculo pectoral mayor en el punto medio de la línea axilar anterior lado izquierdo. Posteriormente, se insertó el trocar #2 de 12mm con dirección hacia el cartílago cricoides ruta subcutánea hasta la línea medio clavicular sobre el borde superior de la misma. En seguida se instaló la cámara de video y se procedió a insuflar gas CO2 con una presión de 6 a 8mm de Hg y un flujo de volumen de 10 a 12 L/min, con lo cual se logró disección subcutánea de la parte inferior del cuello. Entonces se procedió a la instalación del trocar #3 de 5mm con incisión transversa de 5mm sobre el borde anterior del músculo pectoral mayor en el punto inferior de la línea axilar anterior, igualmente ruta subcutánea con dirección hacia el cartílago cricoides hasta la línea clavicular interna sobre el borde superior de la misma, bajo visión directa de la cámara se deslizó el disector Ligasure Maryland® con el que se creó un colgajo subplatismal. En ese momento se insertó el trocar #1 con la misma técnica del anterior, pero con dirección hacia la línea clavicular externa, la cual se destinó para la pinza Endo Clinch®II (fig. 3).
- -
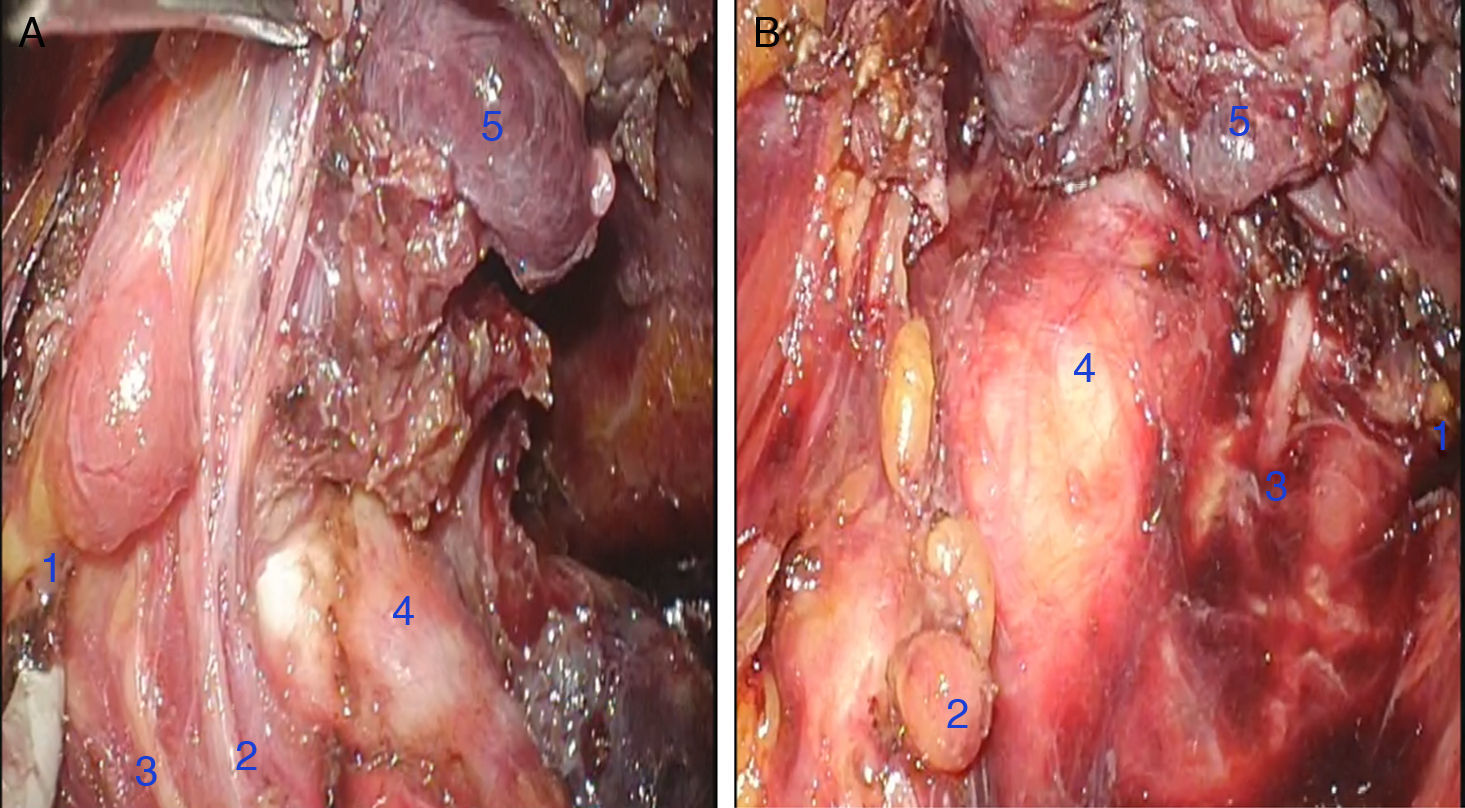
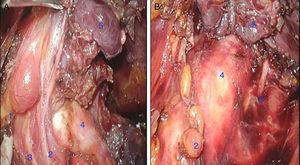
Disección de lóbulo tiroideo ipsilateral: a través del plano graso del borde anterior del músculo esternocleidomastoideo se alcanzó la celda tiroidea, se seccionó inferiormente de los músculos esternotiroideo y esternohiodeo. Con dicha maniobra se identificó y preservó la paratiroides inferior, y se seccionó el pedículo vascular inferior con ayuda del disector Ligasure Maryland®. Esto expuso el nervio laríngeo recurrente en el surco traqueo esofágico y el polo inferior de la tiroides y se procedió a disecar el nervio hasta su ingreso a la laringe, en la unión cricotiroidea, donde se lateralizó la paratiroides superior. Resultó en ese momento expuesto el pedículo vascular superior para su sección, se desinsertó el ligamento suspensorio de Berry y se desprendió el istmo tiroideo de la fascia pretraqueal con el uso del Ligasure Maryland® (fig. 4).
Figura 4.A. Vista endoscópica lado derecho: 1. Paratiroides superior derecha 2. Arteria tiroidea inferior derecha 3. Nervio laríngeo recurrente derecho 4. Tráquea 5. Lóbulo tiroideo izquierdo. B. Vista endoscópica lado izquierdo: 1. Paratiroides superior izquierda 2. Paratiroides inferior izquierda 3. Nervio laríngeo recurrente izquierdo 4. Tráquea 5. Hemitiroides izquierdo.
- -
Disección contralateral: se realizó primero el cierre de las incisiones axilares izquierdas 2 y 3 y se dejó el trocar #1 para facilitar la disección y extracción de la tiroides al final de la cirugía, esto evitó el escape del gas CO2 por estos orificios. Para proceder a la disección del hemitiroides derecho, se empleó la misma técnica del lado izquierdo. Extracción de la pieza quirúrgica: usualmente es la parte más dispendiosa de toda cirugía endoscópica, por esto se usó un Endocatch® Covidien de 10mm, que se instaló en el trocar #2 de 12mm y una cámara de 5mm que se introdujo en el trocar #3 derecho. De esta forma, con las 2 pinzas Endo Clinch®II y el disector de Ligasure Maryland® se depositó la glándula tiroides en la bolsa de Endocatch® de forma rápida y segura para su retiro sin contaminar el trayecto subcutáneo con la pieza quirúrgica. Se cerraron las incisiones con vicryl 3-0 y prolene 3-0 sin drenes. El tiempo operatorio de cada lado fue de 50 minutos, para un total de 100 minutos.
- -
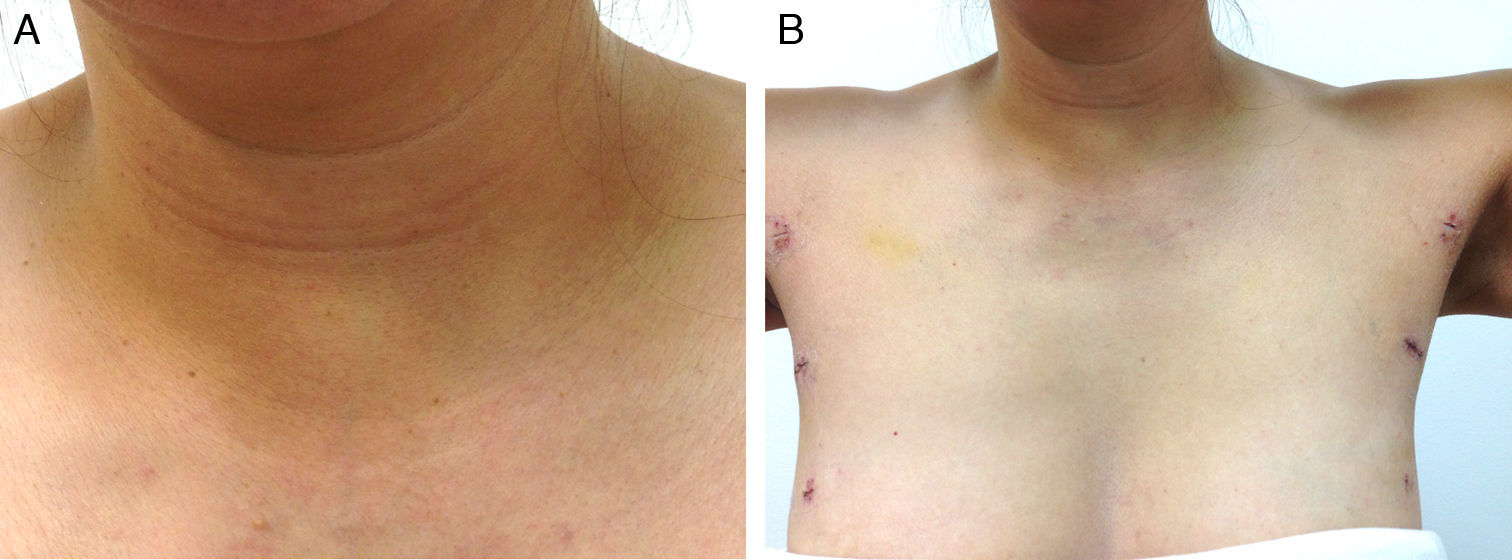
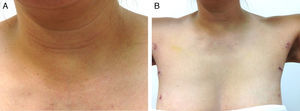
Evolución postoperatoria: vigilancia por 24 horas con buena evolución sin presentar disfonía, sin enfisema subcutáneo, ni complicaciones, el nivel de calcio postoperatorio a las 18 horas fue de 8,7mg/dl (8,6-10,0mg/dl). En el control por consulta externa al sexto día POP, se evaluó en una escala de 1 a 5: el grado de satisfacción 5/5, dolor postquirúrgico 1/5, cumplimiento con las expectativas de la cirugía según lo ofrecido con la técnica 5/5 (fig. 5).
Se realizó un estudio de nasolaringoscopia y se observó adecuada movilidad de los pliegues vocales así como competencia glótica adecuada, sin alteración en el tono de la voz, al igual la paciente no presentó síntomas de cansancio en su voz ni disfagia asociada con el procedimiento quirúrgico.
La patología definitiva demostró el producto de una tiroidectomía total con peso de 10 gramos, lóbulo derecho de 3,5×2,0×0,8cm, el istmo tiroideo de 1,0×1,0×0,5cm y el lóbulo izquierdo de 3,0×2,5×1,0cm, en este último se encontró un nódulo de 1,0×0,7×0,5cm. El diagnóstico definitivo fue carcinoma papilar clásico y variante folicular encapsulado, nódulo de 1cm del lóbulo izquierdo, sin invasión vascular y sin extensión extratiroidea (microtumor papilar tiroideo). Tiroiditis crónica asociada, sin paratiroides ni ganglios en la pieza quirúrgica.
DiscusiónEn las últimas décadas se ha observado un incremento muy importante en el número de casos de cáncer de tiroides en estadios tempranos, que se debe en gran medida a la mejor resolución de los equipos de imágenes diagnósticas que detectan nódulos pequeños sospechosos, con mayor frecuencia15. Las mujeres jóvenes son quienes usualmente deben ser intervenidas por esta patología, que tradicionalmente se ha manejado con incisiones en el cuello que dejan cicatrices muy visibles. Desde la década de los noventa se han publicado múltiples técnicas, con incisiones remotas al cuello para extraer la glándula tiroides parcial o totalmente. Pero probablemente la técnica más difundida ha sido la de Miccoli (descrita en 1999) que sustenta su ventaja cosmética en el desplazamiento de la cicatriz del cuello al área supraesternal donde puede ser menos visible, esto con la ayuda de endoscopios con diámetro de pocos milímetros8. Dicho procedimiento ha tenido diferentes modificaciones, como la anunciada en el 2013 por Shen et al., en donde mediante el uso de bisturí armónico se reduce la incisión a 2cm de longitud y en una localización 2cm por debajo de la horquilla esternal16. Sin embargo, las mujeres jóvenes generalmente no tienen pliegues dérmicos que permitan ocultar la cicatriz del cuello o de la zona esternal. De ahí que continúa la descripción de múltiples incisiones remotas al cuello para extirpar la glándula tiroides. Luego, Oghami et al. (año 2000) en un intento de dejar la cicatriz menos perceptible, diseñan el abordaje endoscópico a través de la incisión bilateral superior a la areola del seno de 5mm, acompañada de una paraesternal ipsilateral de 12mm, la cual continúa siendo evidente al usar un traje de baño17.
Otro sitio donde se puede disimular la cicatriz es la región axilar, por lo que Ikeda y Takami (año 2000) propusieron la tiroidectomía endoscópica por un abordaje axilar unilateral o bilateral con incisiones de 6cm para introducir 4 puertos de trabajo, pero reportan gran dificultad para disecar los pedículos vasculares de forma segura y para preservar las glándulas paratiroides, con un tiempo operatorio muy prolongado. Por esto pensamos que esta técnica no se popularizó y fue rápidamente abandonada5,6. Casi simultáneamente los mismos autores publican (año 2002) el abordaje endoscópico de la tiroides por medio de la pared anterior del tórax, con dos incisiones infraclaviculares ipsilaterales de 12 y 5mm, con otra de 5mm inferior a la horquilla esternal18.
Después, vinieron diferentes grupos con publicaciones de abordajes combinados de la axila (10mm) y el área del seno (5mm) bilateralmente (ABBA y BABA), con claras dificultades técnicas derivadas de la gran distancia entre los puertos de entrada y la celda tiroidea, que llevó al aumento del tiempo operatorio7,19–21.
Desde que se popularizó el uso del robot Da Vinci® en el 2009, se iniciaron los primeros ensayos para aprovechar las ventajas de esta tecnología, que ofrece verdadera visión tridimensional e instrumentos multiarticulados, con ángulos de rotación de 3600 y supresión del temblor fino de las manos. Instalando cuatro puertos de entrada: uno en la pared medial anterior del tórax (5mm) y a través de una incisión de 6cm en la axila otros tres puertos, que en el caso de tiroidectomía total aumenta el número de incisiones22. Paralelamente, se desarrollaron otros puntos de abordaje para posicionar los instrumentos robóticos usando la experiencia previa de la cirugía ABBA y BABA23,24. Finalmente, el abordaje a través de la axila con incisión de 7cm y con la ayuda de un retractor en C, que sostiene el colgajo de piel y con cuatro puertos de entrada25,26.
Conforme con la tendencia mundial nuestro grupo ha disminuido la extensión de la incisión de la tiroidectomía a 2,5cm (1 pulgada) en el cuello, esto con la ayuda de las nuevas energías como son el bisturí armónico y el ligasure. A pesar de esto, la cicatriz a nivel de la parte anterior del cuello en las mujeres jóvenes son notorias. El cambio de paradigma de que a mayor extensión de la incisión se garantiza mayor efectividad de la cirugía, ha sido parte de la línea de trabajo de los últimos años del Grupo de Cabeza y Cuello del INC. Para nosotros, las incisiones más pequeñas, funcionales y cosméticas, sin sacrificar seguridad oncológica, conforman una línea de investigación de la “cirugía en mínimos espacios del cuello”.
Por esta razón, decidimos explorar las opciones de tiroidectomía con accesos remotos al cuello como las previamente descritas. Estamos de acuerdo con la reflexión expresada por Tan CT et al. (año 2008) que se traduce: “La tiroidectomía endoscópica sin cicatriz en el cuello no es una técnica mínimamente invasiva sino una máximamente invasiva, que requiere tiempo operatorio prolongado y extensas disecciones con gran dolor postoperatorio”14.
Ikeda y Takami reportaron en el año 2000 el uso de un endoscopio flexible para cirugía endoscópica de cuello a través de un trocar de 12mm, 2 trocares de 5mm, realizando una incisión de 3cm en la axila y disección subcutánea de la pared anterior del tórax hasta las clavículas, y con insuflación de dióxido de carbono debajo del músculo platisma. Tuvieron gran trabajo para disecar el polo superior de la tiroides incluida la paratiroides, también refieren importante dificultad para encontrar la paratiroides inferior6. En contraste, en nuestra experiencia de casos previos y en especial de este último no tuvimos dicho inconveniente, por el contrario nos impresionó positivamente la facilidad en este paso de la cirugía. Es probable que esto sea debido al uso del lente flexible con visión 3D que proporcionó una excelente visión de campo operatorio. Esto sumado al uso del disector Ligasure Maryland® dotado de un sistema rotatorio de 360o y de punta recubierta, el cual disminuye el daño térmico. Razón de peso para no haber utilizado el monitor de nervio laríngeo recurrente, la paciente en el POP no presentó alteraciones de la voz.
La técnica de Ikeda se ha venido aplicando en varios centros alrededor del mundo, Chang en IOWA durante el 2005 al 2008 realizó 24 tiroidectomías totales endoscópicas, con un tiempo operatorio promedio de 114 minutos9. En contraste, en nuestra cirugía el tiempo quirúrgico total fue de 100 minutos. Cuando comparamos el equipo y el instrumental que empleamos, con el de Chang, vemos claras ventajas en el nuestro, dadas por la excelente magnificación, profundidad de campo y resolución HD 3D. Además de la facilidad logística de tener en un solo instrumento la visión de 00 a 1000, que deriva en ahorro de tiempo, ya que evita el intercambio de los lentes de 00, 300 y 700. Sumado a esto, la versatilidad del disector Ligasure Maryland® con rotación de 3600 que facilitó la disección de las estructuras sin necesidad de intercambiar pinzas.
Contrastando la TAEVA con los abordajes a través de la pared anterior del tórax, a través del seno o a través de la combinación de axila y seno, bien sea que se usen el endoscopio o el robot, se pueden observar claras ventajas de la primera técnica con respecto a las otras. Como son de menor tamaño de incisión, menor número de incisiones y menor distancia de estas incisiones a la celda tiroidea. Por lo que se disminuye la disección de tejidos, el trauma quirúrgico, el tiempo operatorio, el dolor postquirúrgico, facilitando la pronta recuperación, mejorando los resultados cosméticos y permitiendo el cierre sin sistema de drenaje27,28.
Lee et al. realizaron un estudio comparativo entre la tiroidectomía parcial más vaciamiento central vía axilar endoscópica y vía abierta convencional durante el 2002 y 2008 en pacientes con microcarcinomas papilares de tiroides. Ellos concluyen que las dos técnicas tienen resultados similares en complicaciones, pero en los resultados cosméticos la primera supera a la segunda y la consideran una alternativa efectiva en casos seleccionados de pacientes con microcarcinomas29. La patología definitiva (microtumor papilar tiroideo) de nuestro caso refuerza la acertada decisión de la TAEVA sin vaciamiento central, que se sustentó inicialmente en que se trataba de una mujer menor a 45 años, esperanzada en no quedar con cicatriz visible en el cuello, con un nódulo de 11mm (T1, N0, M0) y volumen tiroideo de 6,8 cc. La paciente no requirió manejo adyuvante con yodo-131 y no tuvo factores de riesgo de recaída en la pieza quirúrgica30,31.
Finalmente, un punto a considerar es el balance entre beneficio y costos del procedimiento, que para cada paciente puede ser diferente dependiendo de las expectativas cosméticas, funcionales y oncológicas. Sin embargo, no existe suficiente evidencia comparativa entre la TAEVA y la cirugía abierta en relación con los costos. Byrd et al., publican en el 2010 un estudio comparativo de la MIVAT y la cirugía abierta con análisis de costos, concluyen que estos son similares32.
Reflexiones y recomendacionesLa cirugía “mínimamente invasiva de cuello” es realmente una cirugía que se puede denominar como “máximamente invasiva de cuello”, esto debido a que se deben realizar extensas disecciones en los tejidos aledaños al cuello con más morbilidad, tiempo operatorio y dolor postoperatorio.
Las mejoras en la técnica de cirugía endoscópica en cabeza y cuello han sido posibles por el desarrollo de instrumental y equipos endoscópicos nuevos.
Después de un análisis cuidadoso y ajustado a la experiencia del grupo consideramos que la vía subcutánea de abordaje a través de la línea axilar anterior es la más conveniente para la cirugía endoscópica de cabeza y cuello en nuestro medio.
Recomendamos antes de iniciar un programa de cirugía endoscópica de cabeza y cuello desarrollar destreza en animales vivos, cadáver fresco y finalmente iniciar la aplicación de la técnica en cirugías parciales de tiroides. Igualmente, revisar y ajustar las indicaciones, contraindicaciones de este tipo de procedimiento de acuerdo al grupo operador y al medio donde se desarrollará.
Es importante practicar esta cirugía con el instrumental adecuado y recomendado, lo que optimizará el tiempo operatorio y asegurará una mayor tasa de éxito de esta novedosa intervención.
Por último, consideramos que el término “Cirugía mínimamente invasiva de cuello” debe cambiarse por el de “Cirugía en mínimos espacios del cuello”.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interésLos autores declaran no tener conflicto de intereses.