La seguridad de la dipirona ha sido objeto de numerosos debates, ya que pueden aparecer reacciones alérgicas graves cuya incidencia estimada es de 1 en 5.000 administraciones parenterales.
Hallazgos clínicosSe reporta un caso de una paciente que luego de una infusión con dipirona presenta tos, prurito faríngeo, disnea, cianosis generalizada y deterioro del estado de consciencia. Se hizo el diagnóstico de shock anafiláctico sin antecedentes previos de hipersensibilidad al medicamento que, a pesar del tratamiento con intubación orotraqueal, adrenalina, hidrocortisona, cloruro de sodio y bicarbonato de sodio, resultó fatal.
ConclusiónPueden presentarse casos de grave hipersensibilidad en pacientes sin antecedentes de esta, lo que hace importante reconocer este riesgo en nuestros pacientes.
The safety of dipyrone has been the subject of several debates; severe allergic reaction can occur; its incidence is 1 in 5.000 parenteral administrations.
Clinical findingsA case of a patient who following an infusion with dipyrone has a cough, pharyngeal pruritus, dyspnea, cyanosis and generalized impairment of consciousness. The diagnosis of anaphylactic shock by dipyrone in a patient without hypersensitivity precedent is reported, despite treatment with endotracheal intubation, adrenaline, hydrocortisone, sodium chloride and sodium bicarbonate, which proved fatal.
ConclusionSerious cases of hypersensitivity may occur in patients with no history of it; it is important recognized this risk in our patients.
La dipirona (metamizol), derivado de la pirazolona, es un analgésico no opioide utilizado para el tratamiento del dolor agudo y crónico. Actúa posiblemente a nivel espinal, supraespinal y en el tejido traumatizado. Se cree que inhibe especialmente la isoenzima ciclooxigenasa-3 en el sistema nervioso central. Tiene propiedades antiespasmódicas relajando el músculo liso y efectos antipiréticos a nivel del centro hipotalámico termorregulador1,2.
Sin embargo, su seguridad genera numerosos debates por su asociación con agranulocitosis y anafilaxia, por lo cual está prohibida en países como Estados Unidos, mientras en otros es de venta libre y ampliamente utilizado ya que es costo-efectivo y puede administrarse por diferentes vías1,2. Pueden aparecer, aunque en poca frecuencia, reacciones alérgicas tan graves y letales como shock anafiláctico y síndrome de Stevens-Johnson, incluso con desenlaces fatales1,3.
Descripción del casoInformación de paciente e historial médicoPaciente de 72 años de edad, de sexo femenino, mestiza, con cuadro clínico de 12 h de evolución caracterizado por malestar general, mialgias, artralgias principalmente en rodillas, poliuria y fiebre no cuantificada. Antecedente médico de hipertensión arterial tratada con 25mg de captopril cada día; quirúrgico de resección de lipoma y cirugía ocular no especificada; además exfumadora. Consultó a la misma clínica 4 meses antes con fiebre e infección de vías urinarias, tratada con 1g de dipirona por vía intravenosa (IV) en única dosis intrahospitalaria y dada de alta con acetaminofén y ciprofloxacina, sin ninguna reacción adversa medicamentosa.
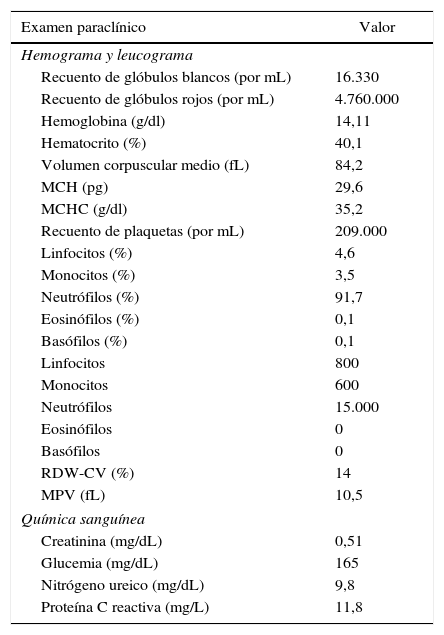
Hallazgos clínicosIngresó con 150/80mmHg de presión arterial, frecuencia cardiaca de 110 latidos por minuto, frecuencia respiratoria de 20 respiraciones por minuto, temperatura de 38,5°C, consciente, orientada, sin otros hallazgos en el examen físico. Solamente se hizo el diagnóstico de infección de vías urinarias y de síndrome febril. Los exámenes paraclínicos se describen en la tabla 1. No se alcanzó a realizar el uroanálisis.
Resultados de paraclínicos de ingreso de una paciente con shock anafiláctico por dipirona en una clínica de tercer nivel
| Examen paraclínico | Valor |
|---|---|
| Hemograma y leucograma | |
| Recuento de glóbulos blancos (por mL) | 16.330 |
| Recuento de glóbulos rojos (por mL) | 4.760.000 |
| Hemoglobina (g/dl) | 14,11 |
| Hematocrito (%) | 40,1 |
| Volumen corpuscular medio (fL) | 84,2 |
| MCH (pg) | 29,6 |
| MCHC (g/dl) | 35,2 |
| Recuento de plaquetas (por mL) | 209.000 |
| Linfocitos (%) | 4,6 |
| Monocitos (%) | 3,5 |
| Neutrófilos (%) | 91,7 |
| Eosinófilos (%) | 0,1 |
| Basófilos (%) | 0,1 |
| Linfocitos | 800 |
| Monocitos | 600 |
| Neutrófilos | 15.000 |
| Eosinófilos | 0 |
| Basófilos | 0 |
| RDW-CV (%) | 14 |
| MPV (fL) | 10,5 |
| Química sanguínea | |
| Creatinina (mg/dL) | 0,51 |
| Glucemia (mg/dL) | 165 |
| Nitrógeno ureico (mg/dL) | 9,8 |
| Proteína C reactiva (mg/L) | 11,8 |
Fuente: autores.
Se administró 1 g de dipirona en 250ml de cloruro de sodio 0,9% IV y al pasar menos de 20ml de la solución, durante los primeros 2 min de iniciada la infusión, la paciente refirió prurito en la extremidad donde se encontraba el acceso venoso; posteriormente presentó tos, prurito faríngeo seguido de disnea, cianosis generalizada y deterioro del estado de consciencia, con pupilas poco reactivas a la luz. Inmediatamente se suspendió la infusión pero la paciente entró en paro cardiorrespiratorio, por lo que se inició reanimación cardiopulmonar. Se realizó ventilación con dispositivo bolsa-válvula-máscara y posteriormente intubación orotraqueal.
Intervención farmacológicaSe administró adrenalina 1mg IV cada 5 min hasta totalizar 5 dosis, hidrocortisona 200mg y 500ml de cloruro de sodio 0,9% IV; adicionalmente se realizó cardioversión en 3 ocasiones y aplicación de 300mg IV de amiodarona por presencia de fibrilación ventricular fina; luego se decidió aplicar 50 mEq de bicarbonato de sodio considerando una acidosis, pero tras 40 min de reanimación no se logró retorno a ritmo de circulación espontánea; sin reflejos del tallo cerebral y con ritmo idioventricular en el monitor electrocardiográfico, se declaró fallecida.
Consentimiento informadoPara obtener la información se obtuvo el consentimiento informado de la familia de la paciente. El siguiente reporte se clasifica como investigación sin riesgo según la Resolución 8430 de 1993 del Ministerio de Salud y se respetan los principios de beneficencia y confidencialidad dados por la Declaración de Helsinki.
DiscusiónLa dipirona puede ser utilizada para dolores de diferente origen, su efecto espasmolítico es aprovechado en dolor tipo cólico y es un antipirético útil en adultos y niños2. La incidencia de reacciones anafilácticas se ha estimado en alrededor de 1:5.000 administraciones parenterales2; estas pueden desarrollarse inmediatamente u horas más tarde, sin depender de la dosis administrada, incluso se han dado raros casos sin antecedente de reacción adversa alguna2. Un estudio demostró un riesgo relativamente bajo de reacciones anafilácticas agudas intrahospitalarias asociadas con dipirona, similar al acetaminofén. No obstante, informes describen reacciones alérgicas graves, algunas con desenlace fatal, como el ocurrido en este caso3-5.
El mecanismo de generación de este grave trastorno por dipirona puede ser debido a una reacción anafiláctica mediada por anticuerpos tipo IgE o una reacción anafilactoide mediada por liberación de histamina de manera inespecífica2. La anafilaxia es una reacción alérgica de afectación multisistémica; los casos graves pueden resultar en obstrucción completa de la vía respiratoria y colapso cardiovascular por shock vasogénico6. La anafilaxia es responsable de una morbilidad considerable y mortalidad potencialmente evitable7. Los primeros síntomas a menudo son inespecíficos: taquicardia, eritema, urticaria, prurito difuso o localizado y sensación de muerte inminente. Hay compromiso de la vía respiratoria como rinitis y tos. A medida que el compromiso respiratorio es más severo, el edema de las vías aéreas superiores puede causar estridor y en las inferiores ocasionar sibilancias6,8.
El colapso cardiovascular es común en la anafilaxia grave, si no se corrige rápidamente; la vasodilatación y el aumento de la permeabilidad capilar causan disminución de la precarga e hipovolemia relativa, que puede conducir rápidamente a paro cardíaco. La isquemia miocárdica, el infarto agudo de miocardio (IAM), las arritmias y la depresión cardiovascular también pueden contribuir al deterioro hemodinámico rápido y al paro cardíaco. Además, la disfunción cardíaca puede ser el resultado de una enfermedad subyacente, donde cabe considerar la sepsis o el desarrollo de la isquemia miocárdica debido a la hipotensión o la aparición coincidente de un síndrome coronario agudo debido a vasoespasmo secundario a reacción alérgica (síndrome de Kounis)6,9, que como shock cardiogénico es extremadamente infrecuente, pues por lo general se presenta como una angina inestable10. Debido a la evidencia limitada, la gestión de un paro cardíaco secundario a la anafilaxia se debe tratar según la guía estándar de reanimación vigente acompañado del tratamiento de anafilaxia6. Es crítico iniciar inmediatamente la reanimación cardiopulmonar y no retrasar el manejo de vía aérea avanzada debido al rápido desarrollo de edema orofaríngeo o laríngeo6.
En caso de que exista una vía venosa permeable, es razonable considerar la ruta IV como una alternativa para la administración de epinefrina en el shock anafiláctico; la dosis recomendada, 0,2-0,5mg, puede repetirse cada 5 a 15 min en ausencia de mejoría clínica6. Además, la reposición de volumen es imprescindible, con un bolo de 20 a 30ml/kg de peso del paciente usando cristaloides isotónicos para mantener una presión arterial sistólica > 90mmHg6.
No existen estudios clínicos aleatorizados que evalúen el uso de otros agentes terapéuticos en el shock anafiláctico y en el paro cardíaco, pero el empleo adyuvante de forma simultánea de antihistamínicos, β2-agonistas y corticoides sistémicos por vía IV han resultado exitosos en el manejo de estos pacientes6. Los antihistamínicos son más lentos en el inicio de la acción y tienen poco efecto sobre la presión arterial. Se ha utilizado la difenhidramina (antagonista H1) a una dosis de 25-50mg intramuscular o por infusión IV lenta. Se ha informado de que el tratamiento con una combinación de antagonistas H1 y H2 puede ser más eficaz en la atenuación de las manifestaciones que el tratamiento con uno solo, y se puede considerar 1mg/kg de ranitidina parenteral6. Los glucocorticoides como metilprednisolona (1-2mg/kg) o hidrocortisona (200mg) no han demostrado ser eficaces para el tratamiento agudo de la anafilaxia, pero podrían, teóricamente, evitar la anafilaxia prolongada7. Los β2-agonistas inhalados se pueden dar a los pacientes con sibilancias, dificultad respiratoria o tos, especialmente cuando el broncoespasmo no responde a la adrenalina7.
LimitacionesDado el rápido desenlace que tuvo este caso, no fue posible evaluar si la paciente tenía evidencia de una sepsis mediante hemocultivos o de infarto agudo de miocardio mediante marcadores enzimáticos.
ConclusiónDebe considerarse el diagnóstico diferencial con el síndrome de Kounis y con el agravamiento de una sepsis a consecuencia de la hipotensión asociada al uso de dipirona. Sin embargo, se han reportado algunos pocos casos de anafilaxia grave en pacientes que no tenían previamente un antecedente de hipersensibilidad, por lo que se consideró que el cuadro correspondió a un evento asociado a la dipirona, que por ser un analgésico de tan amplio uso en nuestro país amerita ser reportado para que el personal sanitario reconozca este riesgo en sus pacientes, esté alerta ante cualquier señal de respuesta alérgica al medicamento y emprenda oportunamente el manejo adecuado.
Lecciones principalesEs posible que se presenten casos de shock anafiláctico secundario a la aplicación de dipirona en pacientes sin antecedente previo de hipersensibilidad, lo cual es una condición poco frecuente, pero muy relevante clínicamente debido a la severidad que puede tener.
Declaración bioéticaEl reporte de caso se hizo bajo consentimiento informado de la familia, según la resolución N.° 8430 de 1993 del Ministerio de Salud de Colombia, garantizando la confidencialidad de los datos de la paciente según los principios de la Declaración de Helsinki.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
FinanciamientoEl trabajo fue financiado por Universidad Tecnológica de Pereira y Audifarma S.A.
Conflicto de interesesLos autores declaran que no tienen conflicto de intereses.