La intoxicación sistémica por anestésicos locales es una de las complicaciones más temidas en la anestesia regional por su potencial tóxico cardiaco, neurológico y principalmente por el riesgo de desencadenar paro cardiorrespiratorio de difícil manejo, aun en pacientes sanos. La prevención como la primera meta, seguida de un rápido reconocimiento y tratamiento oportuno basado en diversas medidas generales y luego del tratamiento específico con las emulsiones lipídicas al 20%, permiten mejorar drásticamente el pronóstico de estos pacientes. Su disponibilidad inmediata en las salas de cirugía o en las áreas destinadas para la realización de la anestesia regional, como sala de bloqueos y servicios de urgencias, entre otros, puede significar la diferencia entre un pronóstico favorable o adverso en situaciones de toxicidad sistémica grave por anestésicos locales.
El objetivo de este artículo es sensibilizar al lector para prevenir los eventos de toxicidad por anestésicos locales y, en caso de presentarse, conocer el protocolo de manejo y reconocer la importancia de disponer en su práctica diaria de un kit de toxicidad por anestésicos locales, siguiendo unos lineamientos básicos de manejo pero adaptados a las necesidades de cada institución, pues si bien esta complicación es rara, es potencialmente devastadora.
Systemic toxicity due to local anesthetics is one of the most feared complications in regional anesthesia due to the risk for the heart, the central nervous system and, in particular, the risk of triggering cardiorespiratory arrest, which is difficult to manage, even in healthy patients.
Prevention as the main goal, together with prompt recognition and early treatment using several general measures followed by specific treatment with 20% lipid emulsions, improve prognosis dramatically for these patients. Their immediate availability in the operating theater or in areas where regional anesthesia is provided such as the emergency services and rooms where blocks are performed, may make the difference between a favorable or adverse prognosis in situations of severe systemic toxicity from local anesthetics.
The objective of this article is to create awareness on the prevention of toxicity events due to local anesthetics and provide knowledge about the management protocols in case such events should happen, recognizing the importance of having a toxicity kit available during daily practice and of following basic management guidelines adapted to the needs of each institution because, although this is a rare occurrence, it may be devastating.
La intoxicación sistémica por anestésicos locales (ISAL) es una complicación rara pero potencialmente fatal que puede ocurrir por concentraciones plasmáticas elevadas por dosis altas o por la administración intravenosa inadvertida1-3. Barrington et al. refieren una incidencia de ISAL de 0,98 por cada 1.000 bloqueos4,5, que constituye una de las causas de paro cardiorrespiratorio de origen anestésico más frecuente2.
MetodologíaSe realizó una revisión narrativa acerca de la toxicidad sistémica por anestésicos locales, se hizo una búsqueda en PubMed y LILACS, sin restricción de idioma, fecha de publicación o lenguaje, empleando los términos MeSH: local anesthetics, toxicity y lipids.
Presentación clínicaToxicidad neurológicaEn el 89% de los casos se reporta toxicidad neurológica, sin signos de cardiotoxicidad en el 45% de los casos6. Los signos más comunes son convulsiones, agitación y pérdida del estado de consciencia1,6. Los pródromos como disartria, entumecimiento perioral, sabor metálico, tinnitus, disforia, confusión y mareo solo se presentan en el 18% de los pacientes6.
Toxicidad cardiacaSe presenta en el 55% de los casos como bradiarritmias, hipotensión, taquiarritmias, defectos de conducción, QRS ancho, cambios en el ST con disnea e hipertensión y pueden progresar a taquicardia ventricular sin pulso, fibrilación ventricular o asistolia1,6.
Presentaciones de toxicidad atípicasExisten presentaciones atípicas de la ISAL como el inicio de los síntomas luego de 5 minutos de la inyección del anestésico local, la cual se asocia a la administración de sedación profunda o de anestesia general1,6. La otra forma de presentación atípica es la presencia de cardiotoxicidad en ausencia de neurotoxicidad6. Es importante reconocer la clínica y el manejo de esta complicación por ser potencialmente fatal7-9.
Prevención y detección precozEl riesgo de la aparición de un cuadro de toxicidad sistémica grave por anestésicos locales se ve incrementado en el caso de los bloqueos de nervio periférico, ya que varios abordajes hacia las estructuras nerviosas se realizan próximos a vasos sanguíneos y, a veces, es necesario más de una inyección de anestésico local para lograr un bloqueo regional anestésico adecuado10-12. La prevención, como primera medida, es la base para reducir el riesgo de toxicidad por anestésicos locales13. Las normas de práctica para la prevención de toxicidad sistémica por anestésicos locales en anestesia regional incluyen14-16:
- –
Limite la dosis total de anestésico local administrado: restringir las dosis de anestésico local administrado usando el volumen más pequeño y la concentración mínima necesaria para conseguir el bloqueo, según las dosis máximas recomendadas para cada uno de los anestésicos locales17, teniendo presente que puede haber variabilidad individual y presentar toxicidad a dosis menores de las recomendadas. Es importante proceder con más cautela en aquellos pacientes que se consideran de mayor riesgo porque los pacientes con alteraciones de la conducción, bajo gasto cardiaco o isquemia, enfermedades metabólicas, enfermedades hepáticas o pacientes con concentraciones de proteínas plasmáticas bajas tienen un aumento de la fracción libre de anestésicos locales y es probable que tengan menos resistencia a la toxicidad13.
- –
Inyección incremental: es aconsejable inyectar lentamente y en dosis fraccionadas anestésico local, aspirando periódicamente en búsqueda de retorno sanguíneo, cada 3-5mL de inyectado y esperando un tiempo prudencial (30-45 s) antes de un nuevo inyectado, durante el tiempo que dure la administración del anestésico local14. Hay que recordar que la aspiración intermitente puede tener un índice de falso negativo de 0,6-2,3%18.
- –
Utilice anestésicos con menor toxicidad: los anestésicos locales de corta duración (lidocaína) presentan un perfil de toxicidad menor que los de acción prolongada (bupivacaína o L-bupivacaína)19, estos últimos, con una potencia y duración mayores a los de corta duración20,21. El uso de L-enantiómeros presenta un mejor perfil de seguridad en sistema nervioso central y cardiovascular con respecto a los compuestos racémicos (bupivacaína)21,22.
El uso de los L-enantiómeros no elimina la necesidad de seguir otras recomendaciones de seguridad3,21.
- –
Marcadores de inyección intravascular: el factor etiológico más importante capaz de desarrollar un cuadro de intoxicación sistémica sigue siendo la inyección intravascular inadvertida de anestésico local16. Para detectarla, la utilización de epinefrina (2,5-5 μg/mL) es de suma utilidad como marcador de inyección vascular20,23. Un aumento sin explicación de la frecuencia cardiaca (10 latidos por minuto) y/o presión arterial (15mmHg), así como cambios en el estado del paciente (obnubilación, inquietud, mareos, convulsiones, etc.), pueden corresponder a una inyección intravascular aunque la aspiración fuera negativa1,10,11,13,23. En caso de sedación del paciente, los síntomas descritos por el paciente pueden estar ausentes24. El paciente anciano bajo anestesia general o con uso de betabloqueadores puede tener limitada la respuesta a la inyección intravascular de epinefrina14,25. El uso de ultrasonido se ha asociado a una incidencia menor de punción intravascular inadvertida4,26 y podría asociarse a un riesgo menor de toxicidad por anestésicos locales27. En caso de utilizarse, debe visualizarse siempre la distensión de los tejidos con el inyectado de anestésico local; en caso contrario, sospeche inyección intravascular, incluso si el doppler color descarta la presencia de vasos sanguíneos en la vecindad del área a bloquear28,29.
- –
Monitorización básica: antes, durante y como mínimo luego de 30 min de realizado el bloqueo nervioso y con equipo de reanimación cardiovascular disponible inmediatamente15,30-32.
- –
Deben conocerse las presentaciones atípicas de la ISAL para su diagnóstico y tratamiento oportuno18 y reconocer que la sintomatología puede recurrir18.
En caso de detectar inyección intravascular, se debe suspender la inyección del anestésico local, pedir ayuda33 y cancelar el procedimiento quirúrgico. Es primordial una adecuada oxigenación, suprimir las convulsiones con midazolam y, en caso de persistir, considerar el uso de succinilcolina para evitar la acidosis de la actividad muscular15,33. Se debe evitar los medicamentos cardiodepresores15,33. En caso de paro cardiorrespiratorio, se debe seguir las guías de soporte vital básico y avanzado con las modificaciones de usar epinefrina en dosis menores de 1 μg/kg, evitar el uso de vasopresina, evitar el uso de lidocaína como antiarrítmico15,33 y recordar que puede ser una reanimación prolongada, incluso mayor de una hora34. Un ayudante debería consultar la lista de chequeo de manejo de la ISAL35. Trasladar a la Unidad de Cuidados Intensivos (UCI) o a la Unidad de Cuidados Especiales (UCE) por un mínimo 12-24 h, ya que pueden presentarse nuevamente los síntomas. Descartar en los 2 primeros días la aparición de pancreatitis con mediciones de amilasa y lipasa34.
Se debe reportar el evento y el uso de lípidos en las páginas registradas www.lipidrescue.org y www.lipidregistry.org15,33.
LípidosLa base del tratamiento para la ISAL son las medidas básicas ya descritas, las cuales pueden solucionar la mayoría de los casos leves-moderados, e incluso algunos casos graves. La emulsión lipídica al 20% es el único tratamiento específico con éxito para la ISAL1 basados en reportes de casos y estudios en animales36-41. La teoría más aceptada para el mecanismo de acción de la terapia emulsión de lípidos es la del «sumidero lipídico», la cual postula que la infusión de los lípidos crea un compartimento de lípidos dentro del plasma que permanece separado de la fase acuosa del plasma42. Los anestésicos locales lipofílicos son recogidos en este sumidero de lípidos, reduciendo así la concentración de anestésico local en la fase acuosa del plasma42,43.
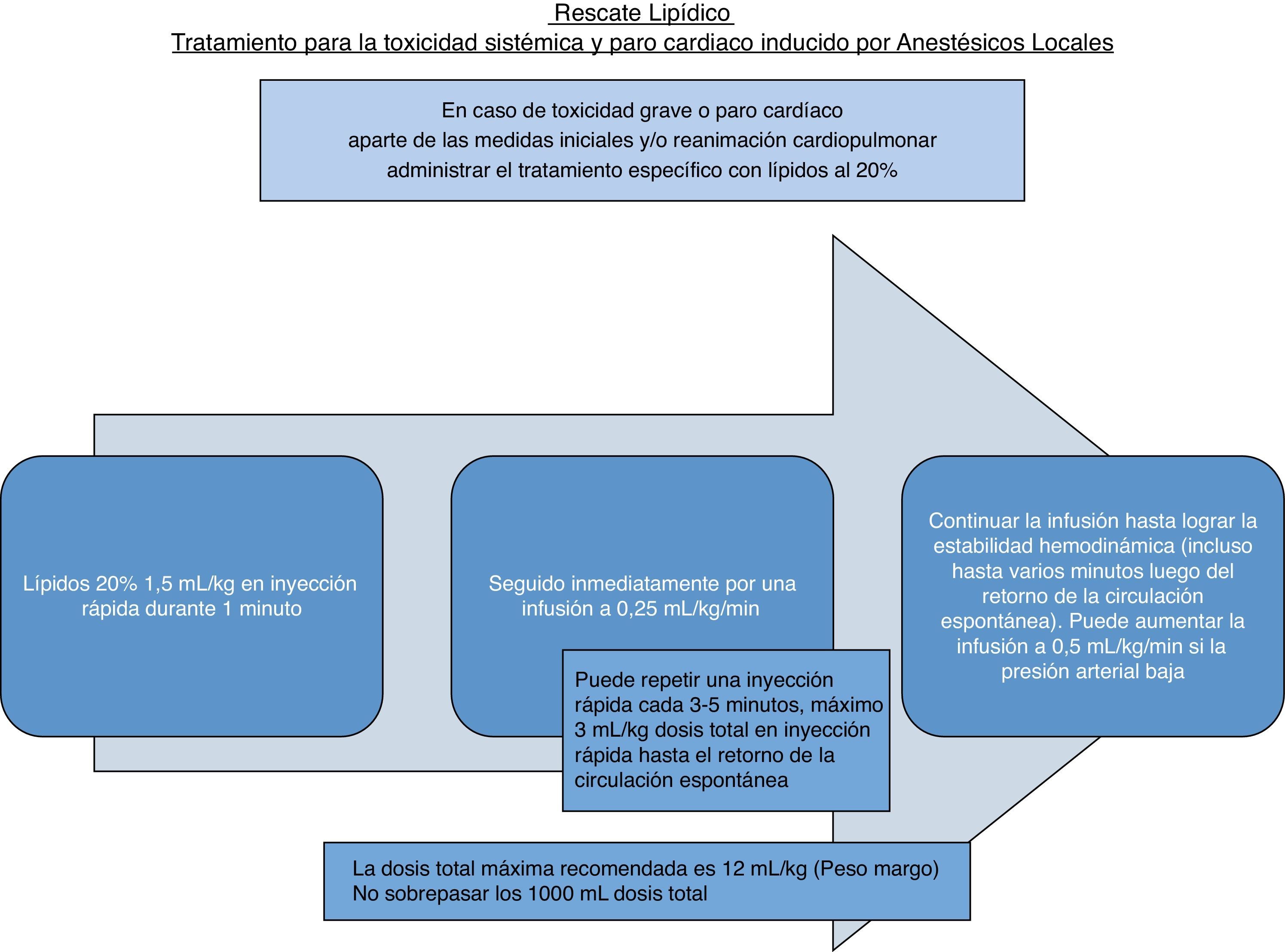
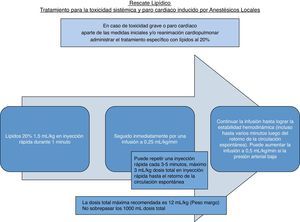
Se emplea un bolo de 1,5mL/kg IV en un minuto, seguido de 0,25mL/kg/min IV, repitiendo el bolo a los 3-5 min si no hay retorno de la circulación espontánea y seguido de 0,5mL/kg/min18, con un máximo de 10-12mL/kg33 como lo muestra la figura 1.
Es importante reconocer que los lípidos no solo se emplean en caso de paro cardiorrespiratorio, sino que deben usarse tempranamente en la toxicidad sistémica grave cardiaca y/o neurológica. El uso de propofol no está recomendado como sustituto de los lípidos en la ISAL18, ya que tiene una matriz lipídica solo del 10% y es cardiodepresor19.
Entre los efectos adversos asociados a la terapia lipídica, aunque no reportados en pacientes sometidos a tratamiento de ISAL, pueden presentarse reacciones de hipersensibilidad en pacientes alérgicos a la proteína de soja o alérgicos al huevo36. Asimismo, pacientes con metabolismo alterado de los lípidos (tales como alteración hepática, pancreática o renal) pueden exacerbar su condición de base36.
La terapia lipídica es de corta duración, por lo que los riesgos son menores que los posibles durante la nutricional parenteral prolongada44, tales como aumento del riesgo de infección45, tromboflebitis46 o embolia grasa47.
El empleo de lípidos no está soportado en estudios aleatorizados, controlados con placebo y doble ciego realizados en humanos por obvias razones éticas44, por lo que los datos provienen de los estudios experimentales en animales y reporte de casos en humanos y son limitados, pero sugieren que la emulsión lipídica puede ser útil para cardiotoxicidad o paro cardiaco potencialmente letal atribuible a otros medicamentos, como antidepresivos, verapamilo, betabloqueadores, bupropión y quetiapina, entre otros48,49.
A pesar de que en la mayoría de los artículos se describe el rescate lipídico con una marca registrada determinada, diferentes marcas y preparaciones de lípidos se han usado con éxito para el rescate de la ISAL50, lo que implica que la formulación exacta de la emulsión puede no ser importante36.
RecomendacionesEn Hospital Pablo Tobón Uribe tenemos 2 kits cada uno con su ficha del protocolo de las dosis de los lípidos y el manejo del paciente con IASL. La socialización del protocolo y los kits en nuestra unidad se hizo a los anestesiólogos a través de la entrega masiva de guías de bolsillo, así como el envío por correo electrónico de la información y bibliografía allí descrita. Asimismo, se realizaron presentaciones del protocolo en reuniones académicas para su conocimiento. Al personal paramédico del área de cirugía, una enfermera del área quirúrgica se encargó de mostrar e instruir acerca del kit, su ubicación e indicación para todo el personal, para ser llevado inmediatamente en caso de ser solicitado por el anestesiólogo. Debido a lo raro pero con consecuencias potencialmente fatales de la intoxicación, se cuenta con 2 kits: uno en el área de bloqueos regionales y el otro en el almacén de cirugía, sitio estratégico por su ubicación en caso de solicitarse en un quirófano. La revisión periódica del kit es semanal y está cargo del personal no paramédico de las salas de cirugía y su comprobación posterior por el personal de enfermería.
Tener este protocolo a la mano es importante, ya que este es un evento crítico de anestesia de rara ocurrencia que requiere un manejo óptimo para evitar desenlaces fatales. Incluso se recomienda que este protocolo de manejo debe ser conocido por el personal de la UCI y la UCE, quienes son los que continúan con el manejo posterior del paciente.
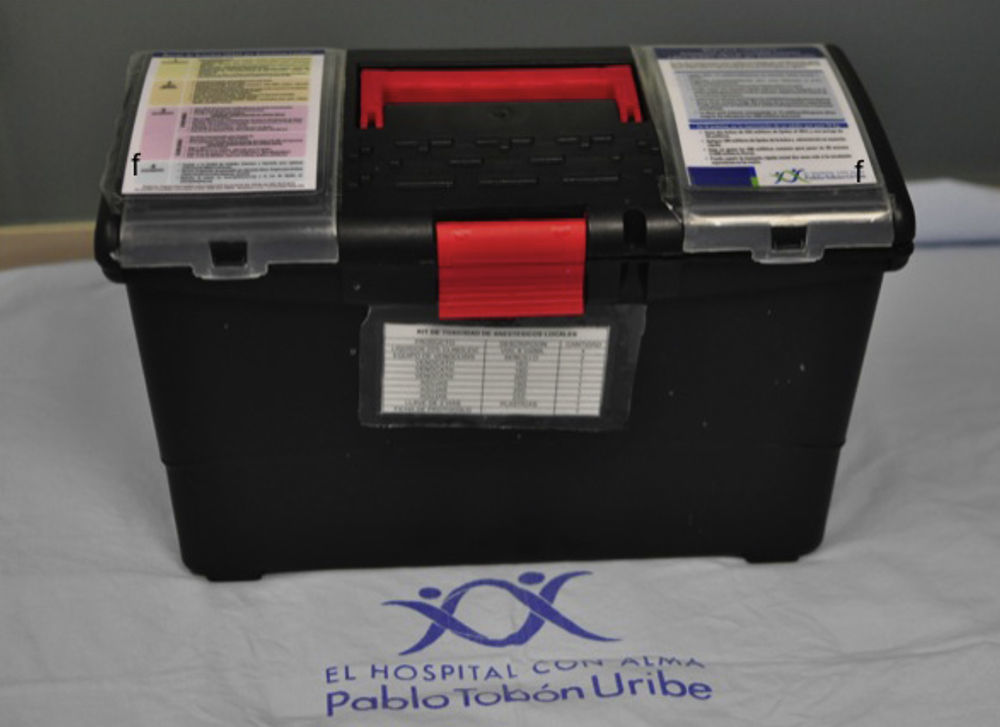
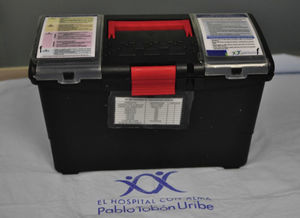
El kit (fig. 2) cuenta con emulsión lipídica al 20% (250mL) en 4 bolsas, basados en la sugerencia de Marwick et al.51 de disponer de una dosis total de 1.000mL en el momento de su empleo, ante la posibilidad de recurrencia de la inestabilidad cardiovascular luego de haber logrado revertir el cuadro inicial. El kit tiene también una llave de 3 vías, 2 jeringas luer-lock de 50mL, equipos de venoclisis y de canalización de acceso intravenoso y la ficha de protocolo. El kit tiene un costo aproximado de 400.000 pesos. Disponemos de una emulsión lipídica que contiene por cada 100mL aceite de oliva refinado 80% y aceite de soja refinado al 20% (fig. 3). Esta emulsión debe estar protegida de la luz, almacenarse a temperaturas menores a 30°C, no refrigerarse y agitarse antes de usar.
Kit de toxicidad por anestésicos locales del Hospital Pablo Tobón Uribe. Nótese la facilidad de transporte, así como la inclusión de la ficha técnica (f) y el protocolo de toxicidad por anestésicos en la parte superior, para facilidad de consulta en situaciones de urgencia.
Fuente: autores.
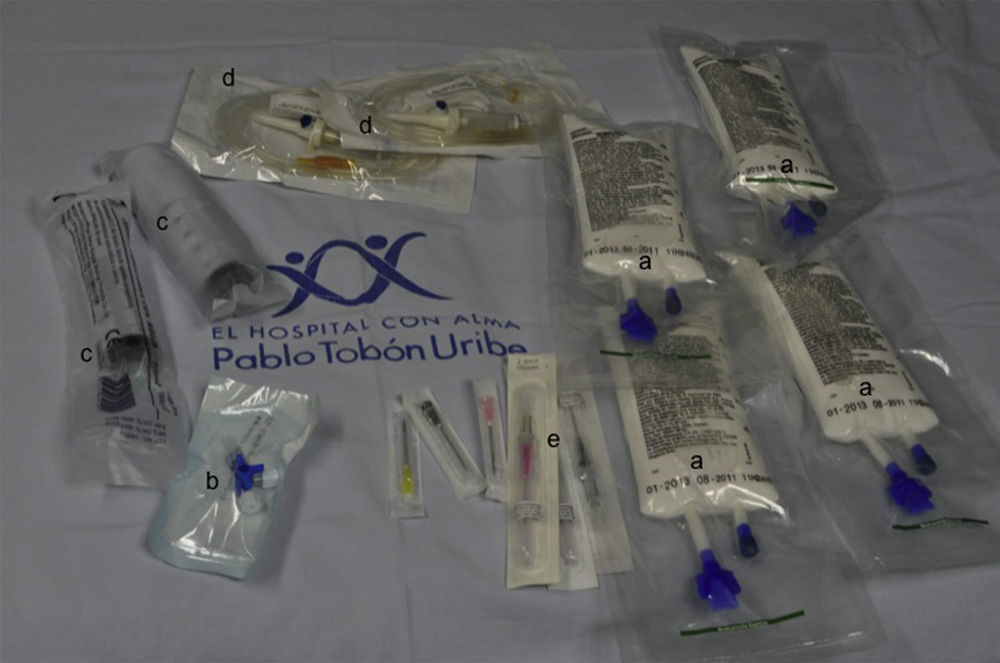
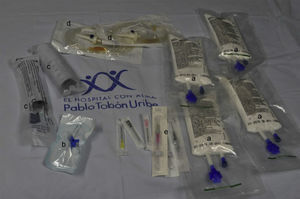
Kit de toxicidad por anestésicos locales del Hospital Pablo Tobón Uribe. Detalle del contenido interior. a) Emulsión de lípidos al 20% (4 bolsas por 250mL). b) Llave de 3 vías. c) Jeringas luer-lock de 50mL para infusión rápida de la emulsión de lípidos. d) Equipos de venoclisis para infusión. e) Dispositivos para canalización venosa, diferentes diámetros.
Fuente: autores.
El auge de los bloqueos nerviosos periféricos puede hacer que la ISAL sea un poco más frecuente de lo que se menciona antes, ya que incluso el uso de la ecografía no ha mostrado disminuir este riesgo. Por esto y por sus consecuencias potencialmente fatales, debemos estar familiarizados con el manejo de esta complicación y tener kits inmediatamente disponibles en los sitios de trabajo donde se emplee la anestesia regional, incluidos los servicios obstétricos, para ofrecer un tratamiento oportuno.
Fuentes de financiaciónRecursos propios de los autores.
Conflicto de interesesNinguno.