La preparación del paciente para el acto quirúrgico y el traslado del paciente al quirófano son 2 procesos prioritarios definidos dentro de los procedimientos y condiciones de habilitación de servicios de salud por parte del Ministerio de Salud y la Protección Social en Colombia.
ObjetivosEl objetivo de esta iniciativa fue desarrollar un manual de manejo clínico basado en la evidencia sobre la preparación del paciente para el acto quirúrgico y traslado al quirófano.
Materiales y métodosSe realizó un proceso dividido en 4 fases (conformación del grupo elaborador, revisión sistemática de literatura secundaria, método participativo de consenso, y preparación y escritura del documento final). Cada una de ellas usó técnicas y procedimientos estandarizados para el desarrollo de manuales basados en la evidencia.
ResultadosSe realizaron recomendaciones basadas en la evidencia sobre valoración preanestésica, manejo preoperatorio de condiciones médicas, educación y comunicación con los pacientes, consentimiento informado, traslado del paciente al área quirúrgica, marcación del sitio quirúrgico, estrategias para la prevención de infecciones, y lista de chequeo preoperatorio.
ConclusionesSe espera que con el uso de este manual se minimice la incidencia de eventos que produzcan morbimortalidad en pacientes sometidos a procedimientos quirúrgicos.
Patient preparation for surgery and transfer to the operating room are two priority processes defined within the procedures and conditions for authorization of health care services by the Ministry of Social Protection in Colombia.
ObjectivesThe aim of this initiative was to develop a manual of clinical management based on the evidence on patient preparation for surgery and transfer to the operating room.
Materials and methodsA process divided into four phases (conformation of the development group, systematic review of secondary literature, participatory consensus method, and preparation and writing of the final document) was performed. Each standardized techniques and procedures used to develop evidence-based manuals.
ResultsEvidence-based recommendations on pre-anesthetic assessment, preoperative management of medical conditions, education and patient communication, informed consent, patient transfer to the surgical area, surgical site marking, strategies for infection prevention and checklist were performed.
ConclusionIt is expected that with the use of this manual the incidence of events that produce morbidity and mortality in patients undergoing surgical procedures will be minimized.
Los protocolos tienen un papel fundamental en la práctica clínica, particularmente para garantizar la seguridad en la atención de los pacientes. Esto se debe a que su adopción minimiza la variabilidad de procedimientos, registros, tratamientos y tareas realizados rutinariamente. Los protocolos facilitan la estandarización e incrementan la confiabilidad en el cuidado de la salud del paciente, reduciendo el error humano en la ejecución de procesos complejos1. La posibilidad de seguir protocolos expande la generación de datos cada vez más robustos, permite medir desenlaces e indicadores y retroalimenta los procesos. El reconocimiento de la existencia de procesos que son críticos dentro de la atención del paciente quirúrgico ha llevado a implementar códigos y técnicas efectivas de comunicación, y a disminuir las distracciones y variaciones durante la realización de los mismos. Lo anterior da soporte a cumplir, cambiar y mejorar las acciones emprendidas para disminuir los riesgos que amenazan la vida y el bienestar de los pacientes dentro del ambiente quirúrgico. Actualmente, en todos los países la seguridad del paciente es un campo de estudio e investigación del cual se han derivado conocimientos y prácticas de indudable beneficio, como la conocida WHO Surgical Safety Checklist2. Los eventos de los que más evidencia se dispone incluyen los llamados «eventos que nunca deben ocurrir» (en inglés, never events):
- •
La realización de un procedimiento quirúrgico al paciente equivocado.
- •
La realización de un procedimiento equivocado al paciente.
- •
La realización de un procedimiento quirúrgico en el sitio equivocado.
- •
La permanencia de cuerpo extraño olvidado después de la cirugía3.
También se cuentan otros, como la infección del sitio operatorio y la hipotermia.
En Colombia, el Ministerio de Salud y Protección Social ha establecido los procedimientos y condiciones de habilitación de servicios de salud y ha definido los procesos prioritarios dentro de las condiciones de habilitación de los servicios quirúrgicos. Dos de estos procesos son la preparación del paciente para el acto quirúrgico y el traslado del paciente al quirófano. Este protocolo establece los pasos ineludibles de aplicación constante y sistemática por parte de un equipo interdisciplinario informado y comprometido con el cuidado y bienestar del paciente quirúrgico.
Si bien será aplicado antes del procedimiento quirúrgico (periodo preoperatorio), su ejecución obliga al equipo a anticipar medidas diagnósticas o terapéuticas durante la cirugía (período intraoperatorio) o después de la cirugía (período postoperatorio). Por todo esto, en ciertos apartados el protocolo hace referencia al perioperatorio (pre, intra y postoperatorio).
El fin del uso de este manual es minimizar la incidencia de eventos que produzcan morbimortalidad en pacientes sometidos a procedimientos anestésicos.
JustificaciónLa elaboración de este manual está justificada en el cumplimiento de los requisitos de la resolución 2003 de 2014 del Ministerio de Salud, por la cual se definen los procedimientos y condiciones de inscripción de los Prestadores de Servicios de Salud y de habilitación de servicios de salud. En dicha resolución se estableció como un proceso prioritario estándar que las instituciones que prestan servicios quirúrgicos en todos los niveles de complejidad deben contar con un protocolo, manual o procedimiento para la preparación del paciente para el acto quirúrgico y traslado del paciente al quirófano, entre otros.
El objetivo de esta iniciativa fue desarrollar un manual de manejo clínico basado en la evidencia sobre la preparación del paciente para el acto quirúrgico, incluyendo el manejo de complicaciones posquirúrgicas y los controles posquirúrgicos.
MetodologíaSe realizó un proceso dividido en 4 fases. Cada una de ellas usó técnicas y procedimientos estandarizados para el desarrollo de guías y protocolos basados en la evidencia:
- •
Conformación del grupo elaborador.
- •
Revisión sistemática de literatura secundaria.
- •
Método participativo.
- •
Preparación y escritura del documento final.
Se conformó un grupo de expertos en anestesiología y en epidemiología, quienes establecieron las directrices metodológicas y técnicas en el marco del desarrollo del protocolo. El grupo fue conformado por 2 coordinadores metodológicos con experiencia en el desarrollo de guías de práctica clínica y protocolos de manejo basados en la evidencia, quienes realizaron la coordinación metodológica del proceso. Además se conformaron 3 grupos, cada uno compuesto por un médico especialista en anestesiología y un epidemiólogo con experiencia en análisis crítico de evidencia científica. Todos los miembros del grupo elaborador aceptaron la participación en el proceso y diligenciaron y firmaron el formato de conflicto de intereses, el cual cumple con la normatividad vigente dentro del desarrollo de guías y protocolos basados en la evidencia.
Revisión sistemática de literatura secundariaSe realizó una revisión sistemática con el propósito de identificar los protocolos clínicos y guías de práctica clínica que abordarán el tema del protocolo. La unidad de análisis de dicha revisión fueron los artículos publicados en revistas científicas o documentos técnicos encontrados como literatura gris:
- •
Protocolos de manejo (o eventualmente guías de práctica clínica) basados en la evidencia que presentaran indicaciones o recomendaciones con relación al manejo clínico por parte del grupo de anestesiología, en el tema del protocolo.
- •
Publicados desde el año 2011 hasta la actualidad.
- •
Publicados en inglés o en español.
Las búsquedas de la literatura fueron diseñadas por el coordinador de búsquedas del grupo Cochrane de Infecciones de Transmisión Sexual. Se diseñó una estrategia de búsqueda digital sensible (anexo 1) con el fin de encontrar los documentos que cumplieran con los criterios antes descritos. La búsqueda se extendió hasta el 24 de agosto de 2014.
Las fuentes de información fueron las bases de datos de literatura científica biomédica Medline, Embase, Lilacs y fuentes de literatura gris: Google Scholar.
Selección de evidenciaA partir de los resultados de las estrategias de búsquedas diseñadas se conformó una base de datos de posibles documentos que cumplieran con los criterios antes mencionados. Esta base fue entregada a 2 revisores, que de forma independiente, a través de la lectura de títulos y resumen, realizaron la identificación de los documentos que cumplieran con los requisitos. En el caso de que hubiera desacuerdo, los 2 revisores lo dirimieron a través de comunicaciones. Los documentos seleccionados fueron descargados en texto completo y luego se les realizó una tamización final.
Evaluación de la calidadSe utilizó el instrumento AGREEII como herramienta para la evaluación de la calidad de la evidencia encontrada en el paso anterior (anexo 2). Este análisis de la calidad se realizó de forma pareada4.
Finalmente se identificó un protocolo que cumplió con los requisitos de elegibilidad y que sirvió de documento fuente para la adaptación del protocolo de manejo clínico en el contexto mencionado. La identificación final del documento fuente se realizó con base en el criterio clínico de los expertos, actualidad (vigencia), exhaustividad en las indicaciones (recomendaciones) y calidad del documento.
Calificación de la calidad de la evidencia y fuerza de la recomendaciónSe usó la estrategia Grade para informar la calidad de la evidencia de la fuente y la fuerza de la recomendación5,6 (tablas 1 y 2).
Definiciones de la calidad de la evidencia
| Nivel de calidad | Definición |
|---|---|
| A. Alto | Existe mucha seguridad de que el verdadero efecto se encuentra cerca de la de la estimación del efecto |
| B. Moderado | Existe una confianza moderada en la estimación del efecto. Es probable que el efecto real sea cercano a su estimación, pero existe la posibilidad de que sea sustancialmente diferente |
| C. Bajo | La confianza en la estimación del efecto es limitada. El verdadero efecto puede ser diferente a la estimación del efecto |
| D. Muy bajo | Existe muy poca confianza en la estimación del efecto. Es probable que el efecto real sea sustancialmente diferente de la estimación del efecto |
Fuente: definiciones tomadas de Balshem et al.6.
Definiciones de la fuerza de la recomendación
| Fuerza de la recomendación | Definición |
|---|---|
| 1. Fuerte | Los efectos deseables de seguir la recomendación sobrepasan a los efectos indeseables. Aplica para la mayoría de los pacientes |
| 2. Débil | Los efectos deseables de seguir la recomendación pueden ser mayores a los efectos indeseables. Este balance puede depender de las circunstancias locales, los valores y preferencias de los pacientes y los anestesiólogos |
Fuente: definiciones tomadas de Card et al.7.
Se utilizó una modificación del método Delphi. El grupo elaborador escogió a los expertos que participaron en el Delphi. La reunión fue realizada el jueves 18 de septiembre en las instalaciones de la SCARE y contó con la participación de 28 expertos en anestesiología y epidemiología.
La reunión tuvo la siguiente agenda:
- i.
Presentación de proyecto.
- ii.
Metodología de la reunión.
- iii.
Resultados de la evidencia.
- iv.
Contenido clínico del manual.
- v.
Votación.
Después de la presentación del contenido clínico del manual y de la discusión por parte de los expertos, se realizó una evaluación del acuerdo que tenían los expertos con relación a si el protocolo cumplía con las siguientes características:
- •
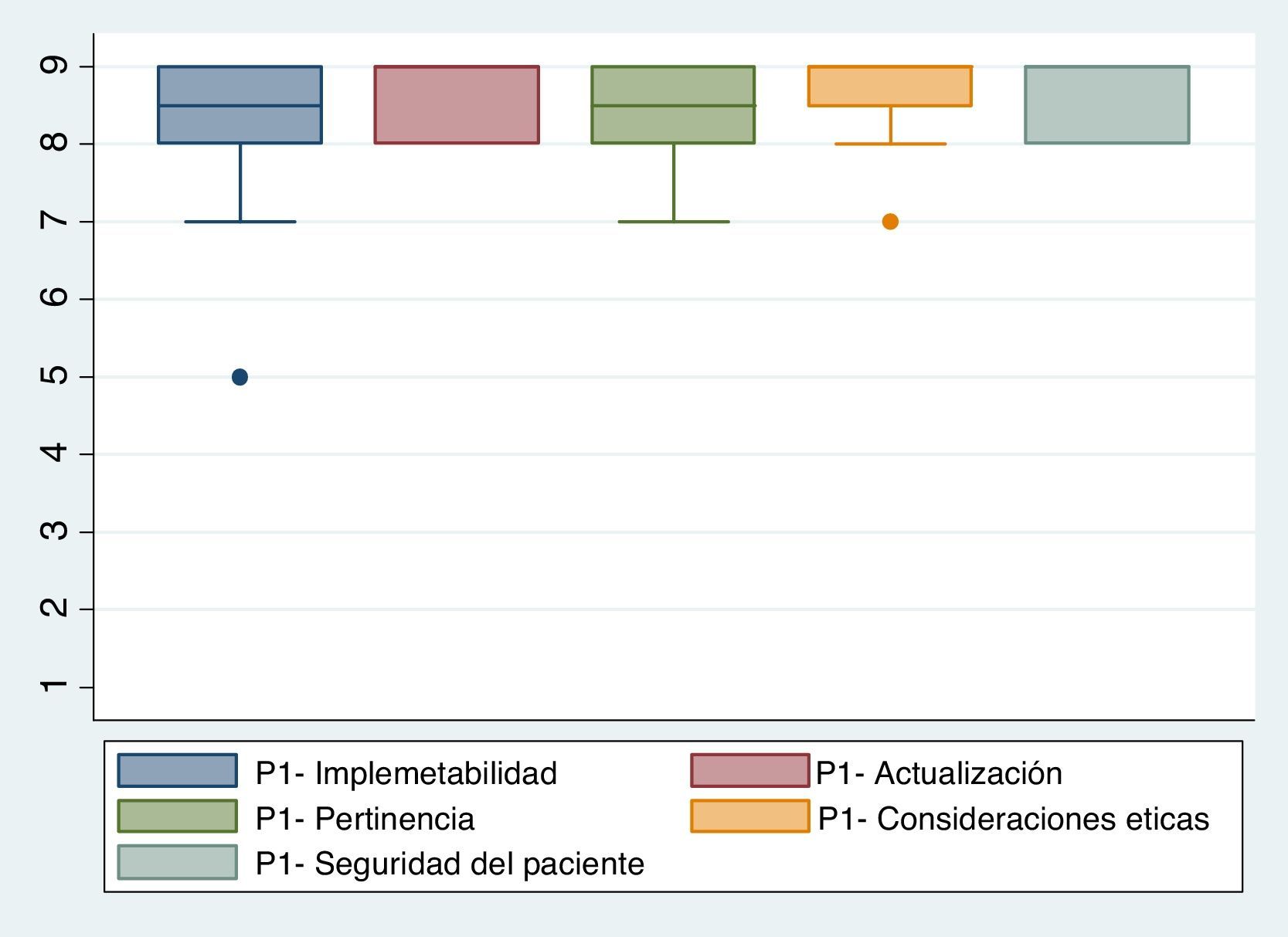
Implementabilidad: evalúa la posibilidad de que el manual sea fácilmente utilizado en las diferentes instituciones.
- •
Actualización: evalúa si las indicaciones están actualizadas con relación a la evidencia actual.
- •
Pertinencia: evalúa si las indicaciones son pertinentes para el contexto de la mayoría de las áreas quirúrgicas.
- •
Consideraciones éticas: evalúa si es ético utilizar este manual.
- •
Seguridad del paciente: evalúa si existe un riesgo elevado en la utilización de este protocolo para los pacientes.
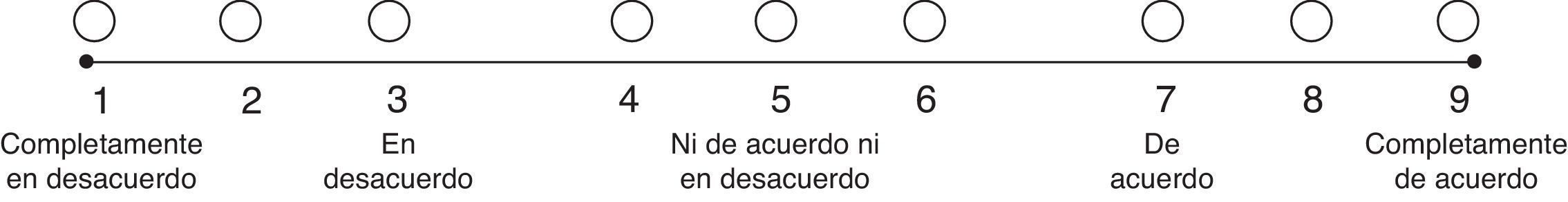
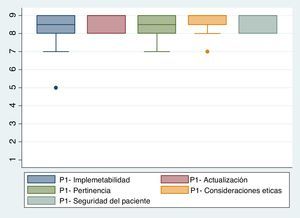
Se utilizó una escala ordinal de 9 categorías para calificar el acuerdo con cada una de las características antes mencionadas (fig. 1). Teniendo en cuenta esto, cada una de las indicaciones propuestas se calificó como recomendada (apropiada), contraindicada (inapropiada) o dentro de un nivel de incertidumbre. Esta calificación se basó en el método Rand (2004), que es citado por Sánchez Pedraza y Jaramillo González8. La figura 2 muestra los resultados del acuerdo por parte de los participantes del consenso.
Escala para calificación en un consenso formal (Delphi en tiempo real).
Fuente: tomado Sánchez Pedraza y Jaramillo González8.
Finalmente se estructuró el modelo del documento de protocolo final que incluyera justificación de la realización del documento, metodología utilizada y adaptación del protocolo propuesto y que acogiera las recomendaciones de los expertos sobre el método participativo. El documento final fue desarrollado por el equipo elaborador del protocolo.
La figura 2 muestra los resultados del acuerdo por parte de los participantes del consenso.
Conflicto de interesesTodos los participantes del grupo elaborador y del consenso de expertos diligenciaron y firmaron el formato de conflicto de intereses de acuerdo con el formato y la recomendación del grupo Cochrane.
Derechos de autorSe solicitaron los permisos necesarios para la utilización y traducción del contenido de las guías contenidas en esta serie de manuales. La traducción y reproducción parcial se realizó con permiso de Lippincott Williams and Wilkins/Wolters Kluwer Health, Association of Anaesthetists of Great Britain & Ireland & the AAGBI Foundation, Institute of Clinical Systems Improvement.
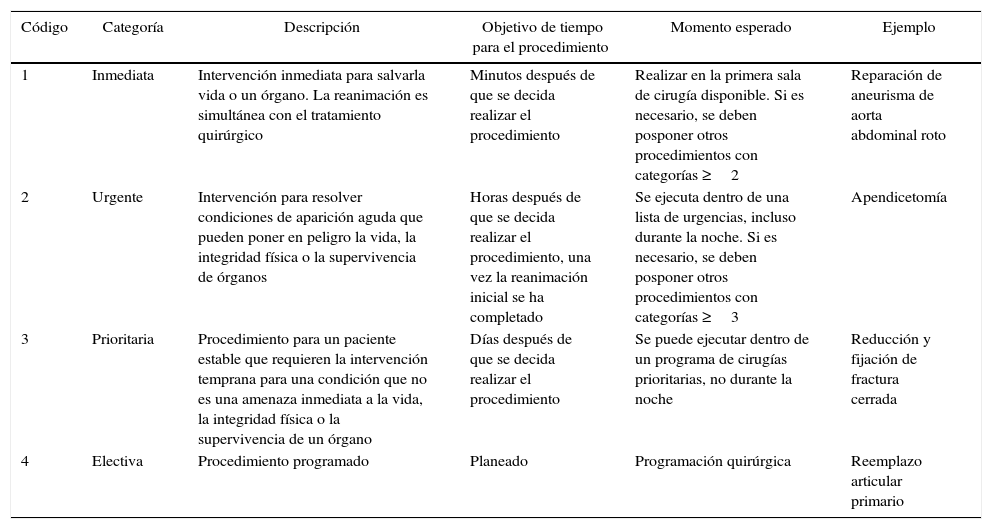
Contenido clínicoPreparar al paciente para un procedimiento quirúrgico es el resultado de varios subprocesos que habitualmente son ejecutados en serie. Estos subprocesos deben ejecutarse de manera secuencial, pues es un prerrequisito para la ejecución del siguiente subproceso. Sin embargo, se debe ajustar al contexto de cada paciente la aplicación completa y el intervalo de tiempo requerido para cada una de las etapas, especialmente en la categoría de la intervención. En este protocolo se adoptará la clasificación National Confidential Enquiry into Patient Outcome and Death (NCEPOD)9 (tabla 3).
Clasificación de la intervención NCEPOD
| Código | Categoría | Descripción | Objetivo de tiempo para el procedimiento | Momento esperado | Ejemplo |
|---|---|---|---|---|---|
| 1 | Inmediata | Intervención inmediata para salvarla vida o un órgano. La reanimación es simultánea con el tratamiento quirúrgico | Minutos después de que se decida realizar el procedimiento | Realizar en la primera sala de cirugía disponible. Si es necesario, se deben posponer otros procedimientos con categorías ≥2 | Reparación de aneurisma de aorta abdominal roto |
| 2 | Urgente | Intervención para resolver condiciones de aparición aguda que pueden poner en peligro la vida, la integridad física o la supervivencia de órganos | Horas después de que se decida realizar el procedimiento, una vez la reanimación inicial se ha completado | Se ejecuta dentro de una lista de urgencias, incluso durante la noche. Si es necesario, se deben posponer otros procedimientos con categorías ≥3 | Apendicetomía |
| 3 | Prioritaria | Procedimiento para un paciente estable que requieren la intervención temprana para una condición que no es una amenaza inmediata a la vida, la integridad física o la supervivencia de un órgano | Días después de que se decida realizar el procedimiento | Se puede ejecutar dentro de un programa de cirugías prioritarias, no durante la noche | Reducción y fijación de fractura cerrada |
| 4 | Electiva | Procedimiento programado | Planeado | Programación quirúrgica | Reemplazo articular primario |
Fuente: tomada de www.ncepod.org.uk9
La historia médica y el examen físico son la mejor estrategia para identificar problemas preoperatorios. El tiempo asignado a la consulta de la valoración preanestésica se puede optimizar mediante el uso de cuestionarios (tabla 4) que no sustituyen la valoración del anestesiólogo sino que facilitan la identificación de puntos importantes y que documentan las respuestas de los pacientes10.
Cuestionario recomendado para pacientes
| ¿Ha sido operado antes? | No □ Sí □ |
| ¿Ha sufrido alguna reacción a la anestesia? | No □ ¿Cuál? _______________ |
| ¿Es alérgico a algún medicamento? | No □ ¿Cuál? _______________ |
| ¿Tiene alguna otra alergia (esparadrapo, yodo, alimentos, etc.)? | No □ ¿Cuál? _______________ |
| ¿Consume alguna droga (cannabis, cocaína, opiáceos u otras)? | No □ ¿Cuál? _______________ |
| ¿Toma bebidas alcohólicas habitualmente? | No □ Sí □ |
| ¿Tiene o ha tenido la presión arterial alta? | No □ Sí □ |
| ¿Tiene algún problema del corazón? | No □ ¿Cuál? _______________ |
| (arritmia, angina, lleva marcapasos o desfibrilador) | No □ Sí □ |
| ¿Ha tenido trombosis / flebitis / tromboflebitis? | No □ Sí □ |
| ¿Necesita más de una almohada para dormir? | No □ Sí □ |
| ¿Se ahoga o tiene dolor en el pecho al subir escaleras? | No □ Sí □ |
| ¿Ha fumado durante el último año? | No □ Sí □ |
| ¿Tiene alguna enfermedad pulmonar? | No □ ¿Cuál? _______________ |
| ¿Tiene apneas del sueño? | No □ Sí □ |
| ¿Utiliza CPAP? | No □ Sí □ |
| ¿Ha tenido alguna enfermedad de riñón? | No □ Sí □ |
| ¿Ha tenido alguna enfermedad en el hígado o una hepatitis? | No □ Sí □ |
| ¿Le han diagnosticado hepatitis B, C o HIV? | No □ Sí □ |
| ¿Tiene diabetes? | No □ Sí □ |
| ¿Usa insulina? | No □ Sí □ |
| ¿Ha tenido convulsiones, desmayos, embolismo o derrame cerebral? | No □ Sí □ |
| ¿Sangra fácilmente por las encías, nariz o heridas? | No □ Sí □ |
| ¿Ha tenido anemia? | No □ Sí □ |
| ¿Tiene alguna objeción a la transfusión de sangre? | No □ Sí □ |
| ¿Toma aspirinas o algún otro medicamento anticoagulante? | No □ Sí □ |
| ¿Ha estado hospitalizado antes? | No □ Sí □ |
| ¿Tiene algún diente flojo? | No □ Sí □ |
| ¿Tiene prótesis dental? | No □ Sí □ |
| ¿Usa lentes de contacto? | No □ Sí □ |
| ¿Tiene piercings? | No □ Sí □ |
| ¿Usa extensiones de cabello? | No □ Sí □ |
| ¿Tiene otros problemas médicos? | No □ ¿Cuáles? _____________ |
Fuente: adaptado de Card et al.7.
Idealmente, la valoración preanestésica se debe realizar por lo menos una semana antes de un procedimiento quirúrgico programado con el fin de hacer una adecuada educación del paciente. Es importante señalar que este intervalo de tiempo se puede adaptar a las características específicas de cada paciente y al tipo de procedimiento quirúrgico a realizar7.
Los pacientes, familiares o cuidadores deben ser advertidos de que la valoración preanestésica no es un sustituto de los programas de promoción y prevención o detección temprana de enfermedades.
- •
La valoración preanestésica se debe realizar a todos los pacientes que se someten a procedimientos diagnósticos o terapéuticos, exceptuando pacientes sin enfermedades sistémicas severas que requieran anestesia tópica o local [GRADE C1].
La valoración preanestésica debe incluir como mínimo:
- •
Procedimiento programado.
- –
Motivo del procedimiento quirúrgico.
- –
Riesgo quirúrgico estimado (tabla 5)11.
Tabla 5.Estimación del riesgo quirúrgico de acuerdo con el tipo de cirugía o intervención
Riesgo bajo (< 1%) Riesgo intermedio (1-5%) Riesgo alto (> 5%) Cirugía superficial Intraperitoneal (esplenectomía, reparación de hernia hiatal, colecistectomía) Cirugías aórtica y vascular mayor Cirugía de seno Carotídea (en pacientes sintomáticos) Cirugía pancreática-duodenal Odontología Angioplastia arterial periférica Revascularización abierta de miembros inferiores Tiroides Reparación endovascular de aneurisma Resección hepática o cirugía de la vía biliar Ojo Cirugía de cabeza y cuello Esofagectomía Reconstructiva Neurocirugía Reparación de perforación intestinal Carotídea (en pacientes asintomáticos) Ortopédica mayor (cadera, columna) Resección adrenal Ginecológica menor Urológica o ginecológica mayor Cistectomía total Ortopédica menor Trasplante renal Neumonectomía Urológica menor Intratorácica (no mayor) Trasplante hepático Trasplante pulmonar Fuente: la estimación del riesgo quirúrgico es una aproximación de riesgo de muerte cardiovascular e infarto cardiaco a 30 días que toma en cuenta solamente la intervención quirúrgica específica y resta importancia a las comorbilidades del paciente11.
- –
- •
Historia médica.
- –
Antecedentes y complicaciones quirúrgicas.
- –
Antecedentes y complicaciones anestésicas.
- –
Alergias e intolerancias a medicamentos y otras sustancias (especificando el tipo de reacción).
- –
Uso de medicamentos (prescritos, de venta libre, herbales, nutricionales, etc.).
- –
Antecedentes patológicos.
- –
Estado nutricional.
- –
Estado cardiovascular (tabla 6)12,13.
Tabla 6.Factores usados en la estratificación del riesgo cardiovascular
Modelo NSQIP13 Índice de riesgo de Lee12 Dependencia funcional total Cirugía de alto riesgo Estado físico ASA Cardiopatía isquémica Creatinina sérica > 1,5 mg/dl Antecedente de falla cardiaca congestiva Edad Antecedente de enfermedad cerebrovascular Tipo de cirugía Uso de insulina Creatinina sérica > 2,0 mg/dl Fuente: tomado de National Surgical Quality Improvement Program (NSQIP)7.
- –
Estado pulmonar.
- –
Clase funcional14-16.
- –
Estado hemostático (historia personal y familiar de sangrado anormal).
- –
Posibilidad de anemia sintomática.
- –
Posibilidad de embarazo (mujeres en edad fértil).
- –
Historia personal y familiar de complicaciones anestésicas.
- –
Tabaquismo, consumo de alcohol y otras sustancias.
- –
Identificación de factores de riesgo para infección del sitio quirúrgico (tabaquismo, diabetes, obesidad, desnutrición, enfermedades crónicas de la piel).
- –
- •
Examen físico.
- –
Peso, talla e índice de masa corporal.
- –
Signos vitales: presión arterial, pulso (frecuencia y regularidad), frecuencia respiratoria.
- –
Cardiaco.
- –
Pulmonar.
- –
Probabilidad de vía aérea difícil.
- –
Los modelos de riesgo no deben determinar las decisiones de manejo, pero deben ser considerados como una pieza del rompecabezas y deben ser evaluados en conjunto con la información tradicional con la que cuenta el médico17.
Paraclínicos preoperatorios. El paradigma sobre la solicitud de exámenes paraclínicos ha cambiado en las últimas décadas en todo el mundo18. Los exámenes paraclínicos que no se sustenten en hallazgos de la historia médica o del examen físico no son costo-efectivos, no confieren protección médico-legal y pueden llegar a ser peligrosos para los pacientes19-21. Abarcar las indicaciones respecto a la solicitud de la extensa lista de exámenes paraclínicos disponible en el ejercicio clínico se sale del objetivo de este protocolo.
Para pacientes sometidos a cirugía no cardiaca se recomienda ajustar la solicitud de paraclínicos de evaluación cardiovascular a alguna de las guías actuales de uso internacional17,22.
Electrocardiograma- •
Se puede considerar obtener un electrocardiograma preoperatorio a pacientes con 65 años o más dentro del año previo al procedimiento quirúrgico [GRADE C2].
- •
El electrocardiograma preoperatorio no se recomienda en pacientes que serán sometidos a otros procedimientos de bajo riesgo, a menos de que en la historia médica o el examen físico se indique que se trata de un paciente de alto riesgo [GRADE A1].
- •
El electrocardiograma no está indicado —sin importar la edad— en pacientes que serán sometidos a cirugía de cataratas. [GRADE A1].
- •
La obtención de un hemograma preoperatorio se debe hacer con base en los hallazgos de la historia médica y del examen físico de los pacientes y de la pérdida sanguínea potencial del procedimiento programado [GRADE C1].
- •
Se recomienda obtener de pacientes con consumo crónico de digoxina, diuréticos, inhibidores de la enzima convertidora de angiotensina (IECA) o antagonistas del receptor de angiotensina (ARA) [GRADE D2].
- •
Se debe obtener una radiografía de tórax (en proyecciones anteroposterior y lateral) en pacientes con signos o síntomas sugestivos de enfermedad cardiopulmonar no diagnosticada o crónica inestable [GRADE D2].
- •
Se debe obtener en mujeres en edad fértil y que tengan la posibilidad de estar en embarazo dado por un retraso menstrual, por una sospecha explícita de embarazo por parte de la paciente o por una posibilidad incierta de embarazo (por ejemplo, menstruación irregular) [GRADE C1].
- •
En todos los pacientes se debe evaluar la presencia de factores de riesgo para complicaciones cardiovasculares perioperatorias17 [GRADE A1].
- •
La terapia con betabloqueadores se debe continuar en el perioperatorio en paciente que cuente con una historia de uso permanente de este tipo de medicamentos [GRADE A1].
- •
Se debe considerar el inicio de la terapia con betabloqueadores en pacientes con alto riesgo de complicaciones cardiacas (tabla 5) que sean sometidos a cirugía vascular [GRADE C2].
- •
Se debe considerar el inicio de la terapia con betabloqueadores en pacientes con enfermedad coronaria o riesgo cardiaco alto (2 o más factores de riesgo) que sean sometidos a cirugía de riesgo cardiovascular intermedio (tablas 5 y 6) [GRADE C2].
- •
La terapia con betabloqueadores se debe iniciar entre una y 2 semanas antes de la cirugía, y la dosis se debe titular para obtener una frecuencia cardiaca entre 60 y 80 latidos por minuto [GRADE A1].
- •
Los pacientes con uso permanente de estatinas deben continuar con su uso durante el perioperatorio [GRADE 1].
- •
Se debe considerar el inicio de la terapia perioperatoria con estatinas en pacientes sometidos a cirugía vascular o de riesgo intermedio [GRADE C2].
- •
Si la historia médica sugiere la posibilidad potencial de problemas de coagulación, se deben obtener pruebas de coagulación [GRADE C1].
- •
La cirugía debe ser evitada por lo menos 6 semanas después de la implantación de un stent metálico [GRADE C1].
- •
La cirugía debe posponerse por lo menos un año después de la implantación de un stent medicado [GRADE C1].
- •
Si la cirugía no puede ser pospuesta durante los periodos de tiempo recomendados, la antiagregación plaquetaria dual debe continuarse en el perioperatorio a menos de que esté contraindicado (cirugía con alto riesgo de sangrado, cirugía intracraneal, etc.) [GRADE C1].
- •
Si se considera necesario suspender clopidogrel / prasugrel / ticlopidina antes de la operación, la aspirina debe continuarse —si es posible— en el periodo perioperatorio para reducir el riesgo cardiaco [GRADE C1].
- •
En los pacientes se debe evaluar la posibilidad de apnea del sueño (tabla 7) y comunicar los resultados de la evaluación al equipo quirúrgico [GRADE C1].
Tabla 7.Detección preoperatoria de pacientes con apnea del sueño
STOP-BANG Ítem S (del inglés Snoring) ¿Ronca tan alto que incluso puede escucharse desde otra habitación? T (del inglés Tired) ¿Con frecuencia se encuentra fatigado o somnoliento durante el día? O (del inglés Observed) ¿Le han observado hacer pausas al respirar mientras duerme? P (del inglés Pressure) ¿Ha sido o es tratado de hipertensión arterial? B (del inglés Body mass index) Índice de masa corporal mayor de 35 kg/m2 A (del inglés Age) Edad mayor de 50 años N (del inglés Neck size) Circunferencia cervical mayor a 40 cm G (del inglés Gender) Sexo masculino - •
Los pacientes con diagnóstico de apnea del sueño que reciban tratamiento con presión positiva continua en la vía aérea (CPAP) deben llevar con ellos el dispositivo para su uso en el postoperatorio inmediato [GRADE B2].
- •
El control de la glucemia se debe dirigir para lograr concentraciones de glucemia entre 140 y 180mg/dl y no a rangos más estrictos (por ejemplo, entre 80 y 110mg/dl) [GRADE A1].
- •
Se debe hacer una evaluación individualizada para generar instrucciones que eviten los cambios extremos de la glucemia [GRADE C1].
- •
La dosis de insulina de acción prolongada (glargina, NPH, etc) se debe disminuir hasta el 50% en el preoperatorio [GRADE C1].
- •
Agentes diabéticos orales e insulinas de acción corta no deben tomarse antes de la operación [GRADE C1].
- •
Los esquemas móviles de insulina durante el perioperatorio se deben usar para tratar la hiperglucemia en pacientes con diabetes mellitus de difícil manejo [GRADE C1].
- •
Los agonistas GLP-1 (exenatide, liraglutide, pramlintide) se deben suspender en el perioperatorio [GRADE C1].
- •
Los inhibidores DPP-4 (sitagliptin) se puede seguir usando en el perioperatorio [GRADE C2].
- •
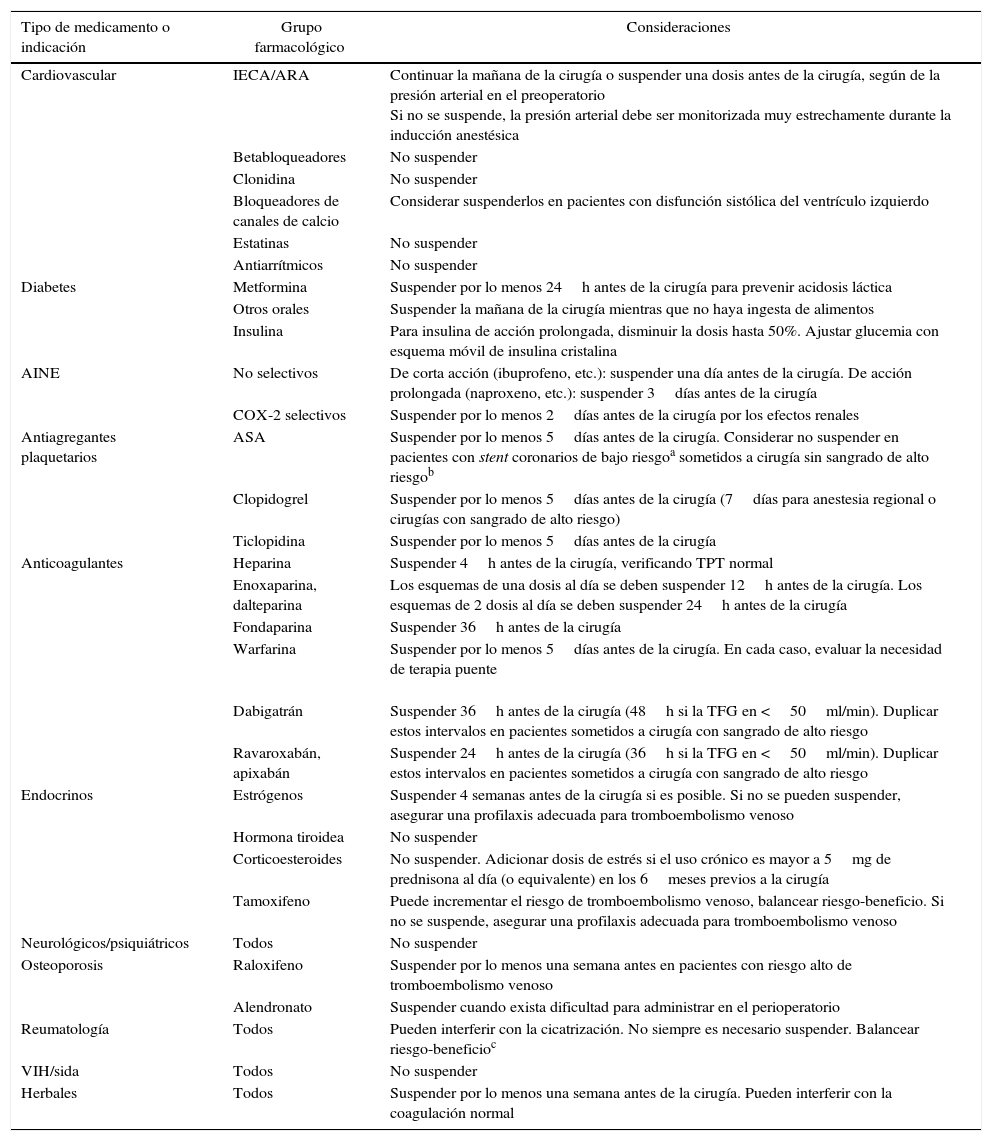
Se debe realizar una revisión a fondo de los medicamentos usados por el paciente (medicamentos formulados, no formulados, herbales y suplementos nutricionales) por lo menos una semana antes de una cirugía programada [GRADE C1].
Tabla 8.Manejo preoperatorio de medicamentos de uso crónico
Tipo de medicamento o indicación Grupo farmacológico Consideraciones Cardiovascular IECA/ARA Continuar la mañana de la cirugía o suspender una dosis antes de la cirugía, según de la presión arterial en el preoperatorio
Si no se suspende, la presión arterial debe ser monitorizada muy estrechamente durante la inducción anestésicaBetabloqueadores No suspender Clonidina No suspender Bloqueadores de canales de calcio Considerar suspenderlos en pacientes con disfunción sistólica del ventrículo izquierdo Estatinas No suspender Antiarrítmicos No suspender Diabetes Metformina Suspender por lo menos 24h antes de la cirugía para prevenir acidosis láctica Otros orales Suspender la mañana de la cirugía mientras que no haya ingesta de alimentos Insulina Para insulina de acción prolongada, disminuir la dosis hasta 50%. Ajustar glucemia con esquema móvil de insulina cristalina AINE No selectivos De corta acción (ibuprofeno, etc.): suspender una día antes de la cirugía. De acción prolongada (naproxeno, etc.): suspender 3días antes de la cirugía COX-2 selectivos Suspender por lo menos 2días antes de la cirugía por los efectos renales Antiagregantes plaquetarios ASA Suspender por lo menos 5días antes de la cirugía. Considerar no suspender en pacientes con stent coronarios de bajo riesgoa sometidos a cirugía sin sangrado de alto riesgob Clopidogrel Suspender por lo menos 5días antes de la cirugía (7días para anestesia regional o cirugías con sangrado de alto riesgo) Ticlopidina Suspender por lo menos 5días antes de la cirugía Anticoagulantes Heparina Suspender 4h antes de la cirugía, verificando TPT normal Enoxaparina, dalteparina Los esquemas de una dosis al día se deben suspender 12h antes de la cirugía. Los esquemas de 2 dosis al día se deben suspender 24h antes de la cirugía Fondaparina Suspender 36h antes de la cirugía Warfarina Suspender por lo menos 5días antes de la cirugía. En cada caso, evaluar la necesidad de terapia puente
Dabigatrán Suspender 36h antes de la cirugía (48h si la TFG en <50ml/min). Duplicar estos intervalos en pacientes sometidos a cirugía con sangrado de alto riesgo Ravaroxabán, apixabán Suspender 24h antes de la cirugía (36h si la TFG en <50ml/min). Duplicar estos intervalos en pacientes sometidos a cirugía con sangrado de alto riesgo Endocrinos Estrógenos Suspender 4 semanas antes de la cirugía si es posible. Si no se pueden suspender, asegurar una profilaxis adecuada para tromboembolismo venoso Hormona tiroidea No suspender Corticoesteroides No suspender. Adicionar dosis de estrés si el uso crónico es mayor a 5mg de prednisona al día (o equivalente) en los 6meses previos a la cirugía Tamoxifeno Puede incrementar el riesgo de tromboembolismo venoso, balancear riesgo-beneficio. Si no se suspende, asegurar una profilaxis adecuada para tromboembolismo venoso Neurológicos/psiquiátricos Todos No suspender Osteoporosis Raloxifeno Suspender por lo menos una semana antes en pacientes con riesgo alto de tromboembolismo venoso Alendronato Suspender cuando exista dificultad para administrar en el perioperatorio Reumatología Todos Pueden interferir con la cicatrización. No siempre es necesario suspender. Balancear riesgo-beneficioc VIH/sida Todos No suspender Herbales Todos Suspender por lo menos una semana antes de la cirugía. Pueden interferir con la coagulación normal aStent de alto riesgo: stent metálicos con menos de 6 semanas de implantados o stent medicados con menos de un año de implantados.
bSangrado de alto riesgo: sangrado mayor a 15ml/kg o que compromete cerebro, retina, cordón espinal o troncos nerviosos; la anestesia neuraxial se debe considerar dentro de este grupo25.
cSi se decide suspender, hacer un intervalo preoperatorio equivalente de 4 a 5 vidas medias del respectivo medicamento; por ejemplo: hidroxicloroquina (4 meses), etanercept (2 semanas), infliximab/adalimumab (4 semanas), rituximab (6 meses); abatacept (2 meses), tocilizumab (4 semanas)26,27.
- •
En general, los medicamentos que contribuyan a mantener la homeostasis se deben continuar durante el perioperatorio, excepto los medicamentos que puedan aumentar la probabilidad de eventos adversos (AINE, IECA/ARA, insulina e hipoglucemiantes, anticoagulantes, productos biológicos, medicamentos para la osteoporosis, terapia hormonal, etc.) [GRADE C1].
En general, se deben suspender todos los medicamentos que no contribuyan a mantener la homeostasis de los pacientes (medicamentos no prescritos, herbales o naturistas, suplementos nutricionales, etc.) [GRADE C1].
Suspensión del tabaquismo- •
Se debe fomentar en los pacientes suspender el tabaquismo [GRADE C1].
- •
Esta se debe obtener en todos los pacientes con una cuantificación del riesgo perioperatorio de tromboembolismo venoso, y dicha cuantificación se debe consignar en la historia clínica. Se recomienda discutir las medidas apropiadas para la prevención de estas complicaciones tromboembólicas con otros miembros del equipo quirúrgico28.
Tabla 9.Estimación preoperatoria de riesgo para tromboembolismo venoso
Factor de riesgo Puntos Edad ≥ 60 años 1 Índice de masa corporal ≥ 40 kg/m2 1 Sexo masculino 2 SIRS/sepsis/choque séptico 3 Historia personal de tromboembolismo venoso 3 Historia familiar de tromboembolismo venoso 4 Cáncer en curso 5 Riesgo mínimo: 0 puntos; riesgo bajo: 1 a 2 puntos; riesgo moderado: 3 a 5 puntos; riesgo alto: (≥ 6 puntos).
Fuente: tomada de Pannucci et al.28.
Las recomendaciones sobre ayuno preoperatorio (nada por vía oral) han sido revisados y simplificados considerablemente en la última década. Se han publicado guías de manejo que establecen la regla «2, 4, 6, 8horas», y se aplica a pacientes de todas las edades29,30.
Los pacientes deben ser educados e informados de los requisitos de ayuno con suficiente antelación.
- •
Se recomienda que el período de ayuno para líquidos claros, como agua, jugos de fruta sin pulpa, bebidas carbonatadas, té claro y café sea de 2h o más antes de la cirugía [GRADE B1].
- •
Se recomienda que el período de ayuno para leche materna debe ser de 4h o más antes de la cirugía [GRADE B1].
- •
Se recomienda que el período de ayuno para leche de fórmula, leche no humana y comidas ligeras (como pan tostado) debe ser de 6h o más antes de la cirugía [GRADE B1].
- •
El período de ayuno para los alimentos fritos y grasos o carne debe ser de 8h o más, ya que estos alimentos pueden prolongar el tiempo de vaciamiento gástrico [GRADE B1].
Para el propósito de prevenir infecciones, los pacientes deben ser alentados a bañarse el día del procedimiento quirúrgico. Ellos deben ser alertados de no afeitarse ni eliminar cualquier pelo en o cerca del sitio quirúrgico. Cada centro debe establecer directrices específicas para su población de pacientes y los procedimientos específicos que se realizan (ver Preparación de la piel).
Comunicación con pacientes y cuidadoresSe debe establecer un mecanismo fiable para comunicar el resultado de la valoración preanestésica, incluidos los resultados de las pruebas paraclínicas y las instrucciones para la marcación del sitio quirúrgico, además de la identificación del paciente antes del procedimiento (tabla 10)7.
- •
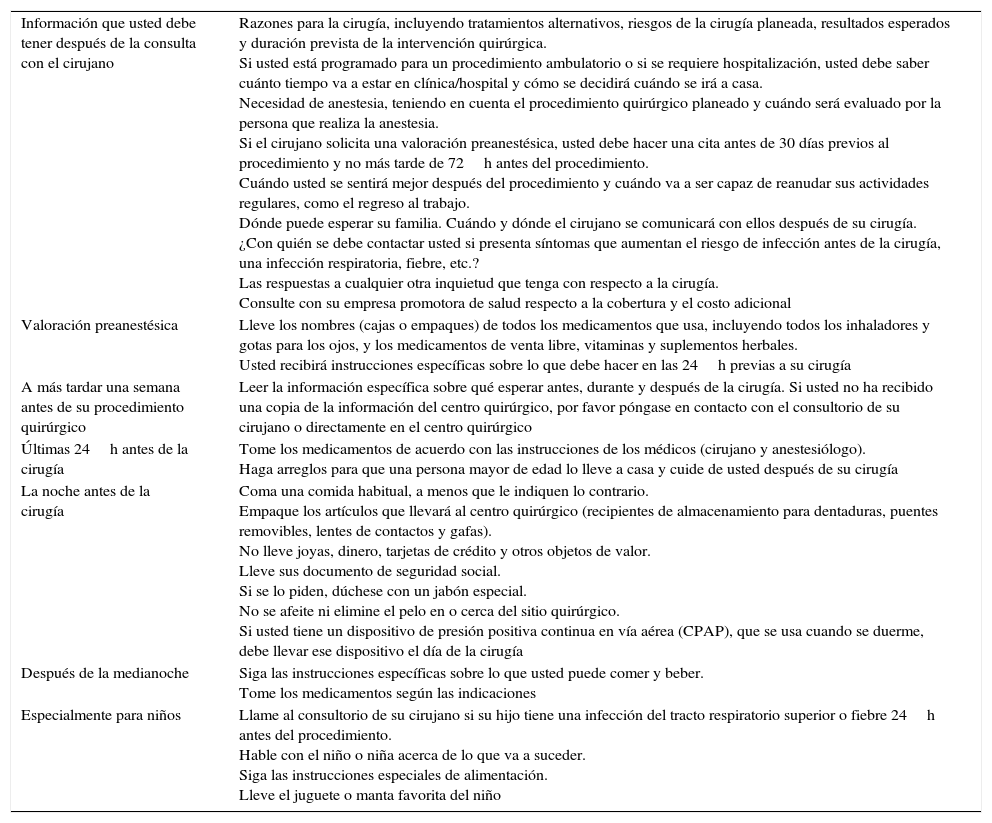
En el caso de procedimientos electivos se recomienda entregar a los pacientes o cuidadores material impreso en el que estén las indicaciones más importantes respecto al proceso de preparación para el procedimiento quirúrgico [GRADE D2].
Guía del preoperatorio para pacientes y cuidadores
| Información que usted debe tener después de la consulta con el cirujano | Razones para la cirugía, incluyendo tratamientos alternativos, riesgos de la cirugía planeada, resultados esperados y duración prevista de la intervención quirúrgica. Si usted está programado para un procedimiento ambulatorio o si se requiere hospitalización, usted debe saber cuánto tiempo va a estar en clínica/hospital y cómo se decidirá cuándo se irá a casa. Necesidad de anestesia, teniendo en cuenta el procedimiento quirúrgico planeado y cuándo será evaluado por la persona que realiza la anestesia. Si el cirujano solicita una valoración preanestésica, usted debe hacer una cita antes de 30 días previos al procedimiento y no más tarde de 72h antes del procedimiento. Cuándo usted se sentirá mejor después del procedimiento y cuándo va a ser capaz de reanudar sus actividades regulares, como el regreso al trabajo. Dónde puede esperar su familia. Cuándo y dónde el cirujano se comunicará con ellos después de su cirugía. ¿Con quién se debe contactar usted si presenta síntomas que aumentan el riesgo de infección antes de la cirugía, una infección respiratoria, fiebre, etc.? Las respuestas a cualquier otra inquietud que tenga con respecto a la cirugía. Consulte con su empresa promotora de salud respecto a la cobertura y el costo adicional |
| Valoración preanestésica | Lleve los nombres (cajas o empaques) de todos los medicamentos que usa, incluyendo todos los inhaladores y gotas para los ojos, y los medicamentos de venta libre, vitaminas y suplementos herbales. Usted recibirá instrucciones específicas sobre lo que debe hacer en las 24h previas a su cirugía |
| A más tardar una semana antes de su procedimiento quirúrgico | Leer la información específica sobre qué esperar antes, durante y después de la cirugía. Si usted no ha recibido una copia de la información del centro quirúrgico, por favor póngase en contacto con el consultorio de su cirujano o directamente en el centro quirúrgico |
| Últimas 24h antes de la cirugía | Tome los medicamentos de acuerdo con las instrucciones de los médicos (cirujano y anestesiólogo). Haga arreglos para que una persona mayor de edad lo lleve a casa y cuide de usted después de su cirugía |
| La noche antes de la cirugía | Coma una comida habitual, a menos que le indiquen lo contrario. Empaque los artículos que llevará al centro quirúrgico (recipientes de almacenamiento para dentaduras, puentes removibles, lentes de contactos y gafas). No lleve joyas, dinero, tarjetas de crédito y otros objetos de valor. Lleve sus documento de seguridad social. Si se lo piden, dúchese con un jabón especial. No se afeite ni elimine el pelo en o cerca del sitio quirúrgico. Si usted tiene un dispositivo de presión positiva continua en vía aérea (CPAP), que se usa cuando se duerme, debe llevar ese dispositivo el día de la cirugía |
| Después de la medianoche | Siga las instrucciones específicas sobre lo que usted puede comer y beber. Tome los medicamentos según las indicaciones |
| Especialmente para niños | Llame al consultorio de su cirujano si su hijo tiene una infección del tracto respiratorio superior o fiebre 24h antes del procedimiento. Hable con el niño o niña acerca de lo que va a suceder. Siga las instrucciones especiales de alimentación. Lleve el juguete o manta favorita del niño |
Fuente: modificado de Card et al.7.
A pesar de los retos únicos que implican obtener el consentimiento informado para procedimientos anestésicos, a los pacientes, padres o cuidadores se les debe proporcionar información respecto a los riesgos anestésicos generales y específicos previstos, y sobre el cuidado anestésico. Se deben adoptar estrategias que permitan mejorar la comprensión de la información con el fin de asegurar que los encargados de tomar las decisiones están adecuadamente informados31,32.
- •
Se debe obtener consentimiento informado anestésico para todos los pacientes (firmado por ellos mismos, por los padres o cuidadores) que sean sometidos a procedimientos diagnósticos o terapéuticos [GRADE A1].
Los pacientes deben ser trasladados al quirófano de acuerdo con su estado clínico. Este traslado implica necesariamente que los pacientes sean cuidados en diferentes áreas de una institución prestadora de servicios de salud y, por tanto, existen procesos de entrega y recepción de pacientes. En la actualidad existe un consenso generalizado de que los procesos de entrega robustos y estructurados son críticos para una atención segura al paciente. Las listas de verificación y herramientas de software para facilitar el proceso de traslado pueden mejorar la fiabilidad y aliviar la presión sobre el personal de salud. Los procesos de traslado y entrega de pacientes se deben adaptar a cada ambiente clínico específico33.
Teniendo en cuenta lo anterior, se pueden definir 2 grupos de pacientes a los que se les debe tener algunas consideraciones específicas:
- •
En pacientes ambulatorios y hospitalizados no críticos:
- –
Con la finalidad de prevenir lesiones por caídas, los pacientes no se pueden trasladar mediante deambulación. Deben trasladarse en silla de ruedas o en camilla.
- –
Según las necesidades específicas de cada paciente, se debe disponer de los dispositivos para asegurar un transporte seguro (por ejemplo, oxígeno de transporte, bombas de infusión, etc.).
- –
Debe participar por lo menos un paramédico en el transporte.
- –
- •
En pacientes críticamente enfermos, además de lo anterior:
- –
Transportar monitorizado, por lo menos con presión arterial no invasiva, electrocardiografía continua y oximetría de pulso.
- –
De acuerdo con las indicaciones clínicas, se debe contar con dispositivos para soporte ventilatorio invasivo con la posibilidad de administrar presión positiva al final de la espiración (PEEP).
- –
El grupo de traslado debe ser liderado por al menos un médico, con la asistencia de personal paramédico.
- –
- •
El traslado de los pacientes al quirófano se debe adaptar al estado clínico del paciente (crítico o no crítico). El proceso de entrega y recepción se debe registrar en la historia clínica [GRADE C1].
Una cirugía incorrecta se puede dar como resultado de desinformación del equipo quirúrgico o mala percepción de la orientación del paciente. La clave para la prevención de este evento es tener múltiples controles independientes de información. Las discrepancias entre la valoración preanestésica, el consentimiento informado y el registro del cirujano de la historia y examen físico deben ser resueltas, idealmente, antes de iniciar cualquier tipo de proceso prequirúrgico34. Antes de marcar el lugar de la cirugía se debe verificar la identidad del paciente y el sitio correcto del procedimiento quirúrgico mediante:
- –
La información del consentimiento informado.
- –
La información contenida en la historia clínica.
- –
Los estudios diagnósticos.
- –
El interrogatorio al paciente, padre o cuidador [GRADE A1].
La infección posoperatoria es una complicación grave. Es la fuente más frecuente de morbilidad hospitalaria para los pacientes sometidos a procedimientos quirúrgicos y está asociada a un aumento de la estancia hospitalaria, mayor riesgo de mortalidad y disminución de la calidad de vida35,36.
Esta puede ocurrir por el procedimiento quirúrgico, y también por los procedimientos anestésicos. Se han descrito varias estrategias que, desde el punto de vista del anestesiólogo, disminuyen el riesgo de infección posoperatoria. Estas incluyen:
- •
Profilaxis antibiótica.
- •
Normotermia perioperatoria.
- •
Preparación adecuada de la piel, entre otras37-39.
El uso de antibióticos profilácticos preoperatorios ha demostrado disminuir el riesgo de infección postoperatoria del sitio quirúrgico. Se han publicado recomendaciones respecto al tipo de antibióticos (tabla 11) y a las dosis (tabla 12) que se deben usar como profilaxis preoperatoria de acuerdo con el tipo de procedimiento quirúrgico40. Los antibióticos preoperatorios se deben administrar con el fin de obtener concentraciones bactericidas en los tejidos al momento de la incisión. Para la mayoría de antibióticos esta concentración se logra 30min después de la administración. La vancomicina y las fluoroquinolonas se deben iniciar dentro de los 120min previos a la cirugía porque requieren un tiempo de infusión más prolongado40. En los casos en los que no se pueda administrar el antibiótico dentro de los intervalos recomendados (por ejemplo, en niño sin acceso vascular), este se debe aplicar tan pronto se resuelva el impedimento. La administración tardía de la profilaxis antibiótica no disminuye su efectividad41.
- •
Todos los pacientes deben ser evaluados respecto a alergias conocidas a medicamentos [GRADE C1].
- •
Se debe administrar un adecuado antibiótico profiláctico, según la cirugía, entre 30min y 2h antes. Este tiempo depende del antibiótico usado [GRADE C1].
- •
Los antibióticos profilácticos, en cirugía no cardiaca, se deben suspender antes de que pasen 24h de finalizado el procedimiento [GRADE C1].
- •
Los antibióticos profilácticos, en cirugía cardiaca, se deben suspender antes de que pasen 48h de finalizado el procedimiento [GRADE C1].
Recomendaciones para profilaxis antibiótica preoperatoria
| Tipo de procedimiento/Sitio quirúrgico | Patógenos comunes | Antibiótico de eleccióna | Alternativa en pacientes alérgicos |
|---|---|---|---|
| Cardiovascular | S. epidermidis, S. aureus | Cefazolina o cefuroxima (mupirocina intranasal la noche previa, el día de la cirugía y cada 12h por 5 días si el cultivo nasal es positivo para MRSA) | Vancomicina o clindamicina |
| Gastroduodenalb | Bacilos entéricos gramnegativos, cocos grampositivos | Cefazolina o cefotetan o cefoxitina o ceftizoxima o cefuroxima | Clindamicina + (ciprofloxacina o levofloxacina o gentamicina o aztreonam) |
| Vía biliarc | Bacilos entéricos gramnegativos, cocos grampositivos | Cefazolina o ceftizoxima | Clindamicina + (ciprofloxacina o levofloxacina o gentamicin o aztreonam) |
| Colangiopancreatografia retrograda endoscópica (CPRE) (solo si hay obstrucción) | Bacilos gramnegativos entéricos, enterococo, clostridia | Ciprofloxacina o ceftizoxima o piperacillina/tazobactam | Clindamicina + (ciprofloxacina o levofloxacina o gentamicina o aztreonam) |
| Colorrectal, incluye apendicectomíad | Bacilos entéricos gramnegativos, anaerobios, enterococos | Cefazolina + metronidazol o cefoxitina o cefotetan o ampicillina-sulbactam | Clindamicina + (ciprofloxacina o levofloxacina o gentamicina o aztreonam) o metronidazol + aztreonam + (ciprofloxacina o levofloxacina o gentamicina) |
| Cabeza y cuello (los antibióticos parecen ser eficaces solo en procedimientos que involucran la mucosa oral de la faringe. Cirugías no contaminadas de cabeza y cuello no requieren profilaxis) | Anaerobios, bacilos gramnegativos, S. aureus | Clindamicina o cefazolina + metronidazol | Gentamicina + clindamicina |
| Neurocirugía | S. aureus, S. epidermidis | Cefazolina | Vancomicina o clindamicina |
| Ortopediae | S. aureus, S. epidermidis | Cefazolina o cefuroxima o ceftriaxone | Clindamicina o vancomicina |
| Urología (antibióticos solo si hay bacteriuria preoperatoria [cultivo positivo no disponible] o sonda o catéter desde el preoperatorio) | Bacilos entéricos gramnegativos, enterocos | Bacteriuria preoperatoria: cefazolina cada 8h, entre una y 3 dosis postoperatorias seguidas de antibiótico oral (nitrofurantoína o TMP-SMX hasta el retiro de la sonda o hasta completar 10días). Biopsia transrectal de próstata: ciprofloxacina ora 500mg 2h antes de la biopsia y repetir 12h después | |
| Obstetricia/ginecología | Bacilos entéricos gramnegativos, anaerobios, estreptococo grupo B, enterococos | Histerectomía laparoscópica, vaginal o abdominal: cefazolina o cefoxitin o cefotetan o cefuroxima o ampicillina-sulbactam Cesárea: cefazolina | Clindamicina + (ciprofloxacina o levofloxacina o gentamicina o aztreonam) |
| Oftalmología | S. epidermidis, S. aureus, streptococcos, bacilos entéricos gramnegativos, Pseudomonas spp. | Gotas tópicas entre 2 y 24h: gentamicina o tobramicina o ciprofloxacina o gatifloxacina o levofloxacina o moxifloxacina o ofloxacina o neomomycina-gramicidina-polimixina B, cefazolina, yodo-providona | |
| Tórax (no cardiaco) | S. aureus, S. epidermidis, estreptococos, bacilos entéricos gramnegativos | Cefazolina o cefuroxima | Vancomicina |
| Vascularf | S. aureus, S. epidermidis, bacilos entéricos gramnegativos, clostridia | Cefazolina | Vancomicina |
La administración de dosis repetidas de antibiótico para la prevención de infección del sitio quirúrgico depende del antibiótico seleccionado y de la duración del procedimiento quirúrgico. Solo se recomiendan dosis únicas de antibiótico para procedimiento con una duración menor a 4h. En procedimientos de más de 4h o cuando haya una pérdida sanguínea mayor a 70ml/kg la nueva dosis se puede aplicar cada una o 2 vidas medias (en pacientes con función renal normal) para mantener concentraciones bactericidas en los tejidos mientras estos se mantengan expuestos42-44.
Solo para pacientes con alto riesgo para infección: obstrucción esofágica, obesidad mórbida, reducción de la acidez gástrica o de la motilidad gástrica (debido a la obstrucción, hemorragia, úlcera gástrica, cáncer o tratamiento con inhibidores de la bomba de protones). No indicado para la endoscopia gastroesofágica de rutina
Solo para pacientes con alto riesgo para infección: mayores de 70años, colecistitis aguda, vesícula biliar no funcional, ictericia obstructiva. La colangitis se debe tratar como una infección y no como profilaxis.
El uso de preparación intestinal con antibiótico por vía oral un día previo a la cirugía es controversial y se debe usar a discreción del cirujano45-47.
Si se usa un torniquete en el procedimiento, la totalidad de la dosis de antibiótico debe ser administrada antes de ser inflado.
Dosis única de amoxicilina/clavulanato reduce las infecciones del sitio quirúrgico en la ingle después de la cirugía para varices, por eso debe ser considerada para este procedimiento48.
Dosis recomendadas de antibióticos profilácticos
| Antibiótico | Dosis para adultos | Dosis pediátrica | Re-dosificación |
|---|---|---|---|
| Ampicilina-sulbactam | 3 g | 50 mg/kg (calculado con ampicilina) | 2 h |
| Cefazolina | Peso < 60 kg=1 g Peso entre 60 y 120 kg=2 g Peso > 120 kg=3 g | 30 mg/kg | 4 h |
| Cefoxitina | 2 g | 40 mg/kg | 2 h |
| Ciprofloxacina | 400 mg | 10 mg/kg | No |
| Clindamicina | 900 mg | 10 mg/kg | 6 h |
| Metronidazol | 500 mg | 15 mg/kg | No |
| Vancomicina | 15 mg/kg | 15 mg/kg | No |
Fuente: adaptado de Bratzler et al.40.
- •
Pacientes con diagnóstico de patologías valvulares cardiacas que se sometan a procedimientos quirúrgicos deben recibir profilaxis antibiótica adecuada [GRADE C1].
- •
Pacientes con prótesis articulares no deben recibir profilaxis antibiótica para prevenir infección en la prótesis [GRADE C1].
- •
No se recomienda el uso de preparación intestinal mecánica para disminuir el riesgo postoperatorio de infección del sitio quirúrgico [GRADE A1].
- •
Al momento de la cirugía todos los pacientes deben recibir una dosis profiláctica de antibióticos efectivos contra la flora del colon y la piel [GRADE A1].
La temperatura se debe monitorizar en todos los pacientes que reciben anestesia y que se espera sufran cambios significativos de la temperatura central49,50 SMD. Existen muchos medios y sitios para medir la temperatura central con diferentes niveles de precisión, exactitud y facilidad de uso (oral, timpánico, esofágico, axilar, cutáneo, vesical, rectal, traqueal, nasofaríngeo y mediante un catéter de arteria pulmonar). La elección del sitio depende del acceso y del tipo de cirugía51.
- •
Se deben establecer estrategias para disminuir el riesgo de hipotermia intraoperatoria con el fin de disminuir complicaciones asociadas (infección del sitio quirúrgico, complicaciones cardiacas, aumento del sangrado, etc.) [GRADE A1].
La mayoría de las infecciones del sitio quirúrgico se producen por la flora normal de la piel. El sitio quirúrgico debe ser evaluado antes de la preparación de la piel.
La piel debe ser evaluada por la presencia de:
- •
Lunares.
- •
Verrugas.
- •
Erupciones.
- •
Otras condiciones de la piel.
La eliminación inadvertida de lesiones puede proporcionar una oportunidad para la colonización de la herida52. Las recomendaciones respecto a la preparación de la piel también se deben aplicar tanto para procedimientos anestésicos como para la inserción de accesos vasculares centrales53.
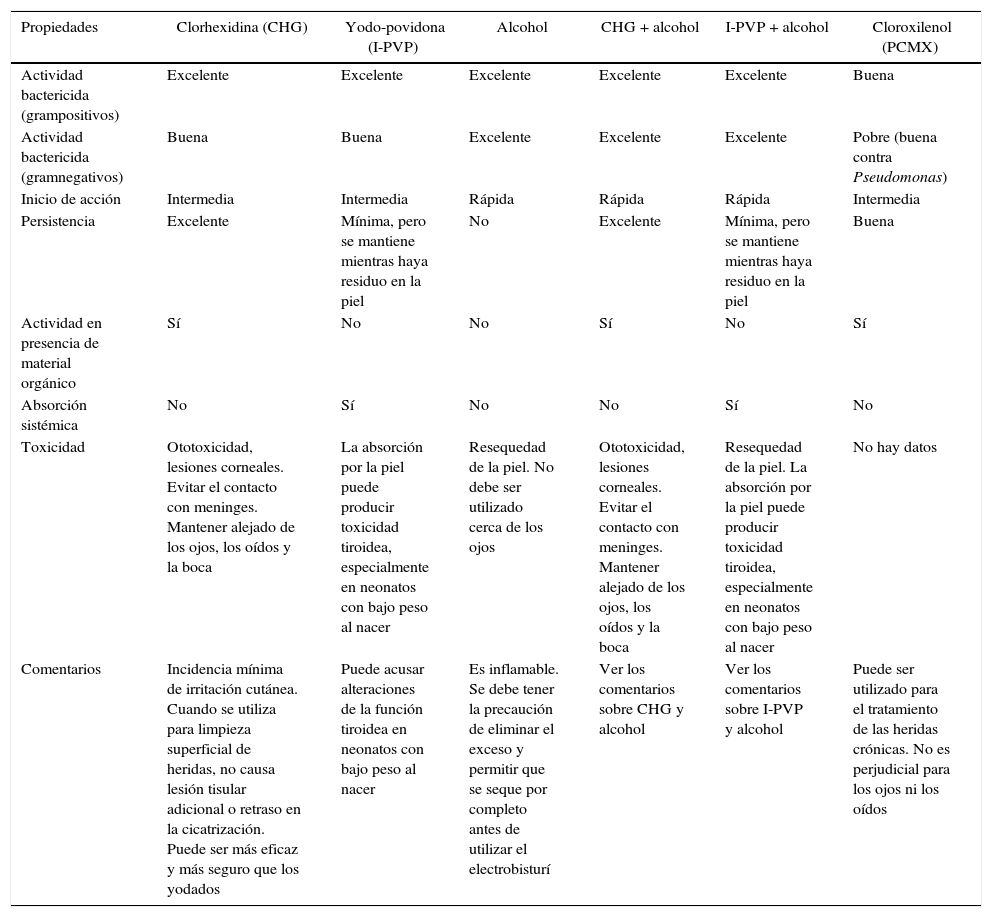
Aplicación de soluciones antisépticasVarios agentes antisépticos están disponibles para la preparación preoperatoria de la piel en el sitio de la incisión (tabla 13). Existe evidencia limitada para recomendar el uso de alguna sustancia antiséptica sobre otra para la preparación de la piel54. Se debe hacer una consideración cuidadosa con el fin de elegir la sustancia ideal de acuerdo con cada grupo de pacientes. Algunos agentes antisépticos pueden lesionar las mucosas, y otros son altamente inflamables.
Comparación de algunas soluciones antisépticas de uso clínico
| Propiedades | Clorhexidina (CHG) | Yodo-povidona (I-PVP) | Alcohol | CHG + alcohol | I-PVP + alcohol | Cloroxilenol (PCMX) |
|---|---|---|---|---|---|---|
| Actividad bactericida (grampositivos) | Excelente | Excelente | Excelente | Excelente | Excelente | Buena |
| Actividad bactericida (gramnegativos) | Buena | Buena | Excelente | Excelente | Excelente | Pobre (buena contra Pseudomonas) |
| Inicio de acción | Intermedia | Intermedia | Rápida | Rápida | Rápida | Intermedia |
| Persistencia | Excelente | Mínima, pero se mantiene mientras haya residuo en la piel | No | Excelente | Mínima, pero se mantiene mientras haya residuo en la piel | Buena |
| Actividad en presencia de material orgánico | Sí | No | No | Sí | No | Sí |
| Absorción sistémica | No | Sí | No | No | Sí | No |
| Toxicidad | Ototoxicidad, lesiones corneales. Evitar el contacto con meninges. Mantener alejado de los ojos, los oídos y la boca | La absorción por la piel puede producir toxicidad tiroidea, especialmente en neonatos con bajo peso al nacer | Resequedad de la piel. No debe ser utilizado cerca de los ojos | Ototoxicidad, lesiones corneales. Evitar el contacto con meninges. Mantener alejado de los ojos, los oídos y la boca | Resequedad de la piel. La absorción por la piel puede producir toxicidad tiroidea, especialmente en neonatos con bajo peso al nacer | No hay datos |
| Comentarios | Incidencia mínima de irritación cutánea. Cuando se utiliza para limpieza superficial de heridas, no causa lesión tisular adicional o retraso en la cicatrización. Puede ser más eficaz y más seguro que los yodados | Puede acusar alteraciones de la función tiroidea en neonatos con bajo peso al nacer | Es inflamable. Se debe tener la precaución de eliminar el exceso y permitir que se seque por completo antes de utilizar el electrobisturí | Ver los comentarios sobre CHG y alcohol | Ver los comentarios sobre I-PVP y alcohol | Puede ser utilizado para el tratamiento de las heridas crónicas. No es perjudicial para los ojos ni los oídos |
Fuente: adaptado de Card et al.7.
El área preparada debe ser lo suficientemente grande como para permitir la extensión de la incisión o la inserción de drenes. El personal debe tener conocimiento de las técnicas de preparación de la piel, incluyendo el mantenimiento de la integridad de la piel y prevenir la lesión en la piel52. El proceso de preparación debe contar con algunas consideraciones especiales:
- •
Las áreas con un alto conteo microbiano se deben preparar a lo último.
- •
Aislar las colostomías mediante una gasa impregnada en antiséptico para prepararlas al final del proceso.
- •
Se recomienda el uso de solución salina normal para preparar áreas de piel quemadas o traumatizadas.
- •
Se debe evitar el uso de productos con base en clorhexidina y alcohol en las mucosas.
- •
Permitir suficiente tiempo de contacto para los antisépticos antes de aplicar los campos estériles.
- •
Permitir el tiempo suficiente para la evaporación completa de agentes inflamables.
- •
Prevenir que los antisépticos se acumulen debajo del paciente o los equipos.
La preparación de la piel se debe documentar en la historia clínica del paciente. Las políticas y procedimientos de preparación de la piel deben ser revisados periódicamente para evaluar nueva evidencia.
- •
Se debe preparar la piel de las áreas que se someterán a procedimientos terapéuticos (cirugía), anestésicos (anestesia regional) y diagnósticos (inserción de catéteres) con una solución antiséptica con el fin de reducir el riesgo de infección [GRADE A1].
El afeitado con una rasuradora puede producir cortes y abrasiones en la piel, y por tanto no debe ser utilizado. El método de recorte utiliza máquinas de cortar con los dientes finos para cortar el pelo cerca de la piel del paciente. Deja el pelo normalmente de un milímetro de longitud. Una recortadora (clipper) normalmente tiene una cabeza desechable o cabezas reutilizables que se desinfectan entre pacientes. Estas máquinas cortadoras no entran en contacto con la piel del paciente, disminuyendo así los cortes y abrasiones. El uso de cremas depilatorias es un método en el que los productos químicos disuelven el pelo. Este es un proceso más lento que dura entre 5 y 20min. Los depilatorios químicos pueden irritar la piel o provocar reacciones alérgicas. El proceso de eliminación del pelo debe contar con algunas consideraciones especiales:
- •
Se debe evitar la eliminación del pelo a menos de que este pueda interferir con el procedimiento55.
- •
La eliminación del pelo debe ser la excepción, no la regla.
- •
La eliminación del pelo, cuando sea necesario, debe realizarse lo más cerca posible de la hora del procedimiento quirúrgico. No hay evidencia que indique un tiempo específico cuando se abstengan de eliminación del pelo en o cerca del sitio quirúrgico. Afeitar más de 24h antes del procedimiento aumenta el riesgo de infección56.
- •
La eliminación del pelo en el campo estéril podría contaminar el sitio quirúrgico y los campos estériles debido a los pelos sueltos.
- •
Para algunos procedimientos quirúrgicos, la depilación puede no ser necesaria. Los pacientes que requieren procedimientos inmediatos pueden no tener tiempo para la depilación.
- •
El personal encargado de efectuar la depilación al paciente debe ser instruido para usar la técnica adecuada.
- •
Las políticas y procedimientos deben indicar cuándo y cómo quitar el pelo en el lugar de la incisión. La eliminación del pelo debe ocurrir bajo las órdenes del médico o siguiendo el protocolo de determinados procedimientos quirúrgicos.
- •
Si se realiza la eliminación del pelo, se debe documentar en la historia clínica. La documentación debe incluir la condición de la piel en el sitio quirúrgico, quién ha realizado la eliminación, el método de eliminación, la zona de depilación y el momento en el que se hizo.
Las listas de chequeo se han convertido en un lugar común en la práctica de la salud, como una estrategia para mejorar la seguridad del paciente. La Organización Mundial de la Salud (OMS) ha implantado una propuesta de lista de chequeo en más de 120 países (fig. 3). Se hace énfasis en el uso de estas listas en los procesos más importantes para la seguridad del paciente:
- •
Anestesia segura y riesgo de vía aérea difícil.
- •
Sitio quirúrgico correcto.
- •
Prevención de infecciones.
- •
Trabajo en equipo.
Lista de chequeo quirúrgico, adaptada por la Sociedad Colombiana de Anestesiología y Reanimación
Fuente: tomado de Ibarra et al.32.
La intención de una lista de chequeo como una herramienta de seguridad es estandarizar y hacer más predecible el rendimiento del equipo quirúrgico a través de una diversa gama de personas, situaciones y entornos clínicos57. Así, las listas de comprobación se han convertido en sinónimo de la mejor práctica en áreas de alto riesgo, como en anestesiología, y se han adoptado en Colombia como una norma mínima de seguridad en anestesiología32,58.
- •
En todos los pacientes sometidos a procedimientos quirúrgicos, una vez dentro del quirófano, se debe verificar el cumplimiento de los procesos prequirúrgicos y la disponibilidad del personal y de los dispositivos requeridos mediante la lista de chequeo de la OMS [GRADE A1].
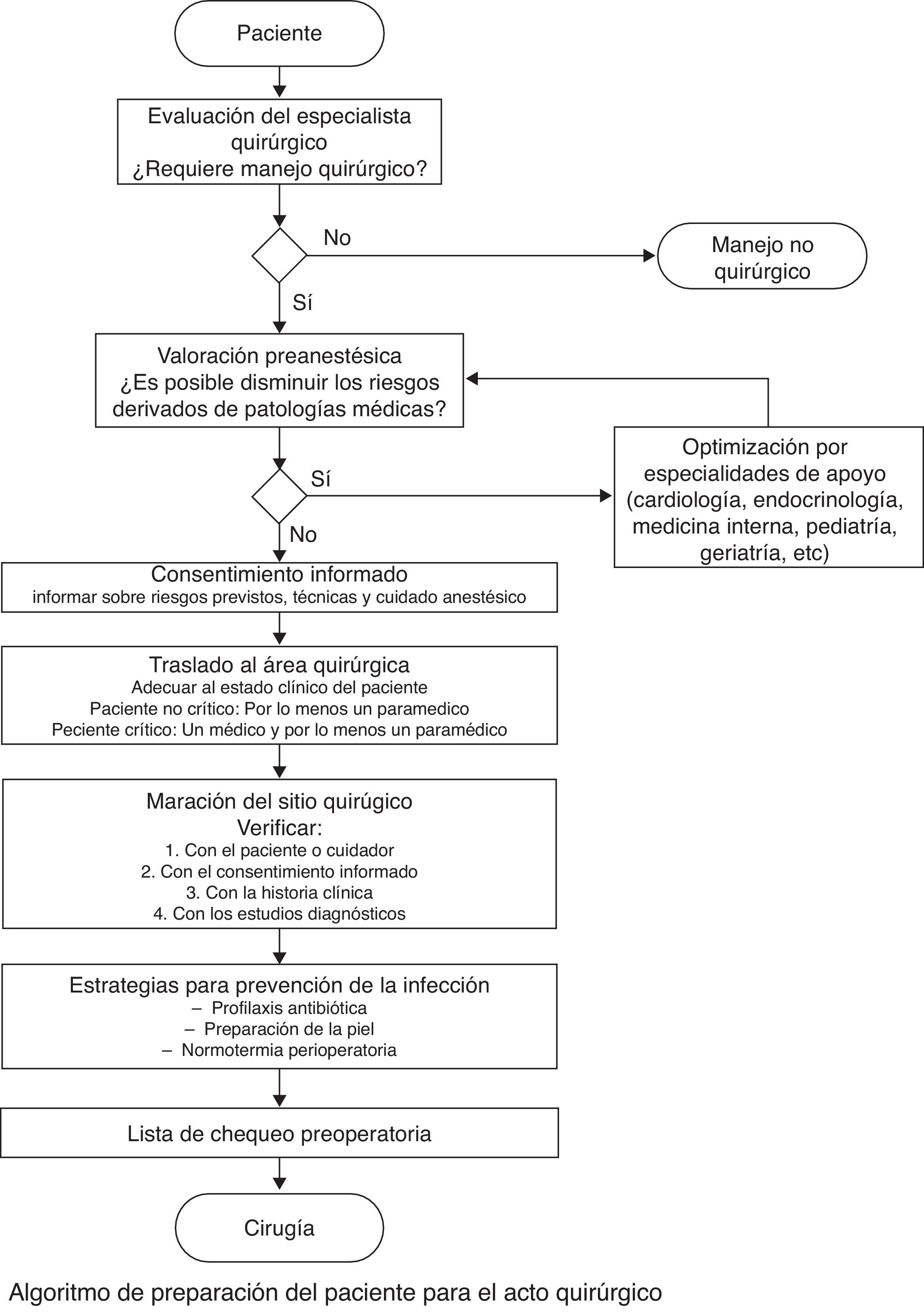
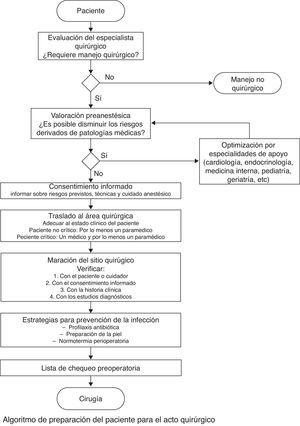
El diagrama de flujo del protocolo de preparación del paciente para el acto quirúrgico muestra varios subprocesos dispuestos en serie, en los que cada uno se constituye en un prerrequisito para el siguiente subproceso (fig. 4).
Diagrama de flujo. Algoritmo de preparación del paciente para el acto quirúrgico.
Fuente: tomado de Ibarra et al.32.
Los autores declaran no tener ningún conflicto de intereses.