La anestesia regional brinda una excelente anestesia y analgesia en pacientes obstétricas, pero existe el potencial de complicaciones tales como la cefalea pospunción dural y lesión neurológica permanente o transitoria. El presente estudio pretende describir la incidencia de la cefalea pospunción dural y daño neurológico en la población obstétrica de un hospital universitario que fue tratada con bloqueo neuroaxial, en comparación con la literatura mundial e identificar los factores de riesgo.
Material y métodosSe hizo una cohorte retrospectiva incluyendo los datos recolectados a partir de los registros de consultas posanestesia durante el año 2010. El análisis central se hizo en función de las quejas de déficit neurológico periférico y cefaleas reportadas por los pacientes, el tipo de anestesia y el procedimiento quirúrgico realizado. Se aplicó un análisis de regresión múltiple para investigar la relación entre el inicio de parestesias de las extremidades inferiores y el tiempo en que permanecieron estas pacientes en posición ginecológica y otras variables.
ResultadosSe evaluaron en total 2399 pacientes embarazadas tratadas con bloqueo neuroaxial. Las complicaciones neurológicas que se presentaron en estas pacientes se dividieron en parestesias de las extremidades inferiores (0,3%), irritación radicular transitoria (0,1%) y cefalea pospunción dural (3%). Las pacientes que permanecieron más de 60min en posición ginecológica mostraron un índice de probabilidades (odds ratio) de evolución con parestesia de las extremidades inferiores de 1,75, y las pacientes que estuvieron más de 120min mostraron un índice de probabilidades de 2,1, pero sin significación estadística.
ConclusionesLas pacientes que se sometieron a bloqueo neuroaxial y se colocaron en posición ginecológica tenían mayores probabilidades de evolucionar con parestesias de las extremidades inferiores por el tiempo que permanecieron en esta posición.
Regional anesthesia provides excellent anesthesia and analgesia in obstetric patients, but has potential for complications such as post-dural puncture headache and permanent or transient nerve damage. This study aimed to describe the incidence of post-dural puncture headache and nerve damage in the obstetric population of auniversity hospital that was submitted to neuraxial blockades, comparing with the world literature, and identify risk factors.
Materials and methodsA retrospective cohort was performed including data collected in the records of post-anesthetic consults conducted during the year 2010. The main analysis was performed on the complaints of peripheral neurological deficits and headaches reported by patients, type of anesthesia and performed surgical procedures. A multiple regression analysis was performed to investigate the association between the onset of lower limb paresthesias and the length of stay of these patients in the gynecological position and other variables.
ResultsA total of 2399 pregnant patients who had undergone neuraxial blockade were evaluated. Neurologic complications that occurred in these patients were divided into lower limb paresthesias (0.3%), transient radicular irritation (0.1%), and post-dural puncture headache (3%). The patients who stayed more than 60 min in gynecological position showed an odds ratio of evolution with lower limb paresthesias of 1.75 and patients who stayed more than 120 min showed an odds ratio of 2.1, but without statistical significance.
ConclusionsPatients submitted to neuraxial blockades and placed in gynecological position were more likely to evolve with lower limb paresthesias related to duration of this position.
Los bloqueos neuroaxiales (anestesia raquídea, epidural y combinada raquídea-epidural [ARE]) se asocian a una menor morbilidad en comparación con la anestesia general1–5. Estas ventajas son más pertinentes cuando se incluyen pacientes obstétricas. Los cambios en la fisiología materna durante el embarazo hacen que los bloqueos neuroaxiales sean una técnica más efectiva que la anestesia general6–10. Sin embargo, algunas complicaciones, incluyendo lesiones neurológicas, pueden ser muy angustiosas para pacientes y familias11,12. Las principales complicaciones neurológicas asociadas a los bloqueos neuroaxiales, especialmente la anestesia raquídea, epidural o ARE, son: cefalea pospunción dural (CPPD), daño neurológico y complicaciones cardiovasculares tales como hipotensión, bradicardia o paro cardiaco13–40. La incidencia de complicaciones neurológicas ocasionadas por bloqueos neuroaxiales no se conoce. Esta información es esencial para adaptar las técnicas anestésicas a nuestros pacientes, mejorando así la calidad de la anestesia administrada y prevenir posibles complicaciones.
El presente estudio está diseñado para describir la incidencia de CPPD y otras complicaciones neurológicas en pacientes obstétricas en un hospital universitario, quienes recibieron anestesia regional, y compararla con la incidencia reportada en la literatura mundial1,6,13,15,17, así como observar las relaciones entre complicaciones neurológicas y factores de riesgo identificables.
Material y métodosLuego de la aprobación por parte del Comité de Ética de Investigación en nuestro hospital, que obvió el consentimiento informado, se hizo una cohorte retrospectiva con los registros de los datos de las consultas posanestesia que habían tenido lugar durante el año 2010. Estos datos se refieren a todos los síntomas reportados por las pacientes obstétricas sometidas a bloqueo neuroaxial el primer día después de la anestesia y su posterior evolución y tratamiento. Estas pacientes se sometieron a cesárea, uso de fórceps o tuvieron parto vaginal. Las pacientes que recibieron anestesia local o general se excluyeron de este análisis. El análisis central se hizo sobre las quejas de déficit neurológico periférico o cefaleas reportadas por las pacientes, el tipo de anestesia y el procedimiento quirúrgico realizado. Se calculó la incidencia de estas complicaciones y se comparó con la incidencia descrita en la literatura, así como los tratamientos descritos en nuestro servicio y su eficiencia. La asociación de déficit neurológico periférico y el tiempo transcurrido en posición ginecológica de estas pacientes u otras variables se investigaron mediante un análisis de regresión múltiple.
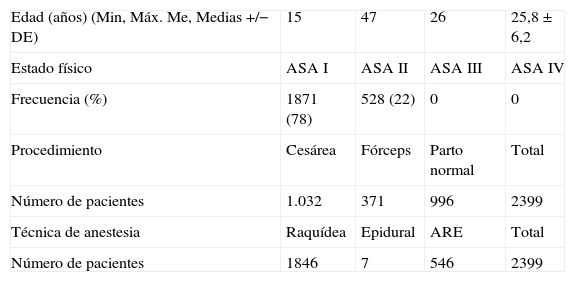
ResultadosEvaluamos 2399 pacientes embarazadas que recibieron bloqueo neuroaxial, el primer día del posoperatorio. En la tabla 1 se describe la edad promedio y la condición física de las pacientes. Las pacientes analizadas se sometieron a anestesia epidural, anestesia raquídea y ARE. Los procedimientos se dividieron en cesárea, parto vaginal y uso de fórceps (tabla 1).
Edad, condición física (ASA), tipo de procedimiento quirúrgico y técnica anestésica
| Edad (años) (Min, Máx. Me, Medias +/− DE) | 15 | 47 | 26 | 25,8 ± 6,2 |
| Estado físico | ASA I | ASA II | ASA III | ASA IV |
| Frecuencia (%) | 1871 (78) | 528 (22) | 0 | 0 |
| Procedimiento | Cesárea | Fórceps | Parto normal | Total |
| Número de pacientes | 1.032 | 371 | 996 | 2399 |
| Técnica de anestesia | Raquídea | Epidural | ARE | Total |
| Número de pacientes | 1846 | 7 | 546 | 2399 |
ARE: anestesia combinada raquídea-epidural.
Fuente: autores.
Las complicaciones neurológicas en estas pacientes se dividieron en parestesias de las extremidades inferiores, irritación radicular transitoria, cefaleas (CPPD y otras causas), y se describen en la tabla 2.
Complicaciones neurológicas observadas y su frecuencia en la población estudiada
| Complicaciones neurológicas | Parestesia de las extremidades inferiores | IRT | CPPDAR | CPPDARE |
| Número de pacientes (frecuencia) | 7 (0,3%) | 2 (0,1%) | 22 (1,2%) | 10 (1,8%) |
CPPD: cefalea pospunción dural; CPPDAR: CPPD después de anestesia raquídea; CPPDEPI: CPPD después de anestesia raquídea o anestesia combinada raquídea-epidural; IRT: irritación radicular transitoria.
Fuente: autores.
La frecuencia de CPPD se calculó tomando en consideración la totalidad de anestesias raquídeas (CPPDAR) y también se calculó la frecuencia de CPPD después de ARE y de anestesia epidural (CPPDEPI).
En el período posoperatorio evaluamos a 38 pacientes con molestias de dolor de cabeza. De estas, 6 pacientes presentaban otras causas de cefalea, como migraña13, 2 pacientes con anemia y una paciente con sinusitis.
También se investigó la relación entre el inicio de la parestesia en las extremidades inferiores y el tiempo de permanencia en posición ginecológica. Entre las pacientes que permanecieron más de 60min en posición ginecológica, cuando se compararon contra las pacientes que permanecieron un menor tiempo en esa posición, encontramos una relación de probabilidad (odds ratio) de la evolución con parestesias de las extremidades inferiores de 1,75 (OR: 1,75; IC95%: 0,34 a 9,04). Entre las pacientes que se quedaron más de 120min en posición ginecológica, cuando se compararon con las que permanecieron menos de 120min, encontramos una relación de probabilidad de evolución a parestesias de las extremidades inferiores de 2,1 (OR: 2,1; IC95%: 0,21 a 21,26). Otras variables, tales como la edad, el estado físico, el tipo de anestesia (raquídea, epidural o ARE) y el tipo de parto (fórceps, parto normal), no se relacionaron con parestesias de las extremidades inferiores.
DiscusiónLa incidencia de CPPD luego de anestesia raquídea (CPPDAR) en nuestro estudio fue de 1,2% (22pacientes), de las cuales 19 (86%) se trataron con analgésicos y solo 3pacientes (14%) desarrollaron cefalea refractaria a tratamiento clínico, luego de lo cual se sometieron a terapia de parche hemático. Esta frecuencia es más alta que la incidencia reportada de 0,4% en la literatura mundial39. La incidencia de CPPD luego de anestesia epidural o anestesia combinada raquídea-epidural (CPPDEPI) fue de 1,8% (10pacientes). De estas, 7pacientes (70%) respondieron a tratamiento médico con analgésicos y esteroides, y 3pacientes (30%) recibieron terapia de parche hemático. La incidencia de CPPDEPI en la literatura se estima alrededor de 0,35%41, reportando una eficacia del 96 al 98% del parche hemático41–45. Todas nuestras pacientes que se sometieron a parche hemático tuvieron resolución de sus síntomas.
La población de pacientes estudiadas mostró una incidencia de complicaciones neurológicas de 0,4% (2pacientes con irritación radicular transitoria y 7pacientes con parestesias de las extremidades inferiores). En la literatura revisada encontramos una incidencia de complicaciones neurológicas del 0,7%19 al 0,01%1. Los datos más recientes, publicados por Navarro Vargas et al.26, describieron una incidencia de complicaciones neurológicas luego de anestesia raquídea que varió del 0,005 al 0,13%. Por lo tanto, observamos una incidencia de complicaciones neurológicas en nuestro estudio, en comparación con otros estudios, pero con una tendencia hacia una mayor incidencia. Es necesario tomar en consideración que estas incidencias pueden variar de acuerdo con las distintas complicaciones neurológicas: parestesias, déficit motor. En nuestro análisis incluimos 3tipos de bloqueos (raquídeo, epidural y combinado). Los estudios revisados hasta el momento han incluido complicaciones neurológicas de la anestesia raquídea o epidural, pero no combinada (ARE)1. Este hecho se debe a que estos estudios se hicieron entre 1995 y 1998, época en la cual no era una práctica el uso de ARE en pacientes obstétricas46–49. Adicionalmente, nuestro servicio tiene residentes de primer año de anestesiología que son quienes realizan la mayoría de estos bloqueos (bajo la supervisión de los médicos tratantes), y los datos de los estudios no se analizaron para evaluar la presencia o ausencia de experticia médica en tales servicios50. Los médicos residentes tienen mayores dificultades para realizar los bloqueos neuroaxiales, y se hace una búsqueda activa para identificar complicaciones en la consulta posanestesia; en consecuencia, es muy raro que una paciente con complicaciones neurológicas posanestesia no sea diagnosticada en nuestro servicio50.
Entre las 2399 pacientes analizadas, 7 desarrollaron parestesias, una paciente dolor del nervio ciático y 6 pacientes neuropatía femoral (todas con remisión espontánea después de tratamiento farmacológico). Todas las pacientes que desarrollaron parestesia de las extremidades inferiores se sometieron a bloqueos neuroaxiales y luego se colocaron en posición ginecológica. Este hecho nos hizo asociar la aparición de parestesia con la posición de estas pacientes y no con el bloqueo neuroaxial realizado En nuestro análisis encontramos que el riesgo de parestesia es mayor cuanto más largo es el tiempo en posición ginecológica, pero sin significación estadística. Dicha falta de significación podría deberse a la baja prevalencia de parestesias, lo cual hizo necesario analizar a un mayor número de pacientes.
Nuestro estudio tuvo otra limitación: dado que el período de seguimiento de los pacientes fue un día después del procedimiento anestésico, no se detectaron las complicaciones neurológicas o la CPPD que se presentaron después del segundo día.
Las pacientes obstétricas sometidas a bloqueos neuroaxiales y colocadas en posición ginecológica tienen mayores probabilidades de evolucionar hacia parestesias de las extremidades inferiores relacionadas con el tiempo en que permanecieron en dicha posición.
FinanciaciónNinguna.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Nuestros agradecimiento a la dra. Nora Elizabeth Rojas Álvarez y el dr. German Collazos, quienes nos ayudaron con la traducción al español.