Las intervenciones de microcirugía sobre la mano son procedimientos realizados por cirujanos reconstructores que requiere un abordaje complejo y altamente individualizado. El manejo anestésico en pacientes con cirrosis puede ser difícil. La disfunción hepática puede condicionar una duración prolongada de los fármacos anestésicos por un metabolismo e índice de aclaramiento alterados.
Describimos el manejo anestésico de un paciente con cirrosis, empleando una técnica anestésica combinada con bloqueo axilar continuo del plexo braquial para prevenir el dolor postoperatorio y mantener una vasodilatación prolongada. El bloqueo continuo del plexo braquial con anestésicos locales ha mostrado mejorar la perfusión tisular tras la cirugía de reimplante de miembros. Esta técnica es especialmente beneficiosa para prevenir el vasoespasmo en el tejido reconstruido en el periodo postoperatorio. En los pacientes cirróticos, esta técnica ofrece un adecuado control del dolor postoperatorio.
Hand microsurgeries are procedures performed by reconstructive surgeons and require a complex and highly individualized approach. The management of anesthesia in patients with cirrhosis may be challenging. Liver dysfunction may condition the extended use of anesthetic agents as a result of a disrupted metabolism and clearance.
This case describes the anesthetic management of a patient with cirrhosis, using a combined anesthetic technique with continuous axillary block of the brachial plexus to prevent postoperative pain and maintain extended vasodilatation. The continuous brachial plexus block under local anesthesia has shown improved tissue perfusion following limb replantation surgery. This technique is particularly helpful to prevent vasospasm in the reconstructed tissue during the postoperative period. In patients with cirrhosis, this technique provides adequate postoperative pain control.
El bloqueo continuo del plexo braquial (BCPB) en la cirugía de reimplante digital proporciona numerosas ventajas en relación a la mejor perfusión del injerto1–3. Los pacientes con enfermedad hepática presentan un alto riesgo de morbimortalidad perioperatoria como consecuencia de los efectos de la cirugía y de los fármacos empleados, que podrían agravar el estado basal hacia una descompensación hepática4. El metabolismo de la mayoría de los fármacos opioides se encuentra enlentecido5, con una vida media prolongada y condicionando un mayor riesgo de depresión respiratoria.
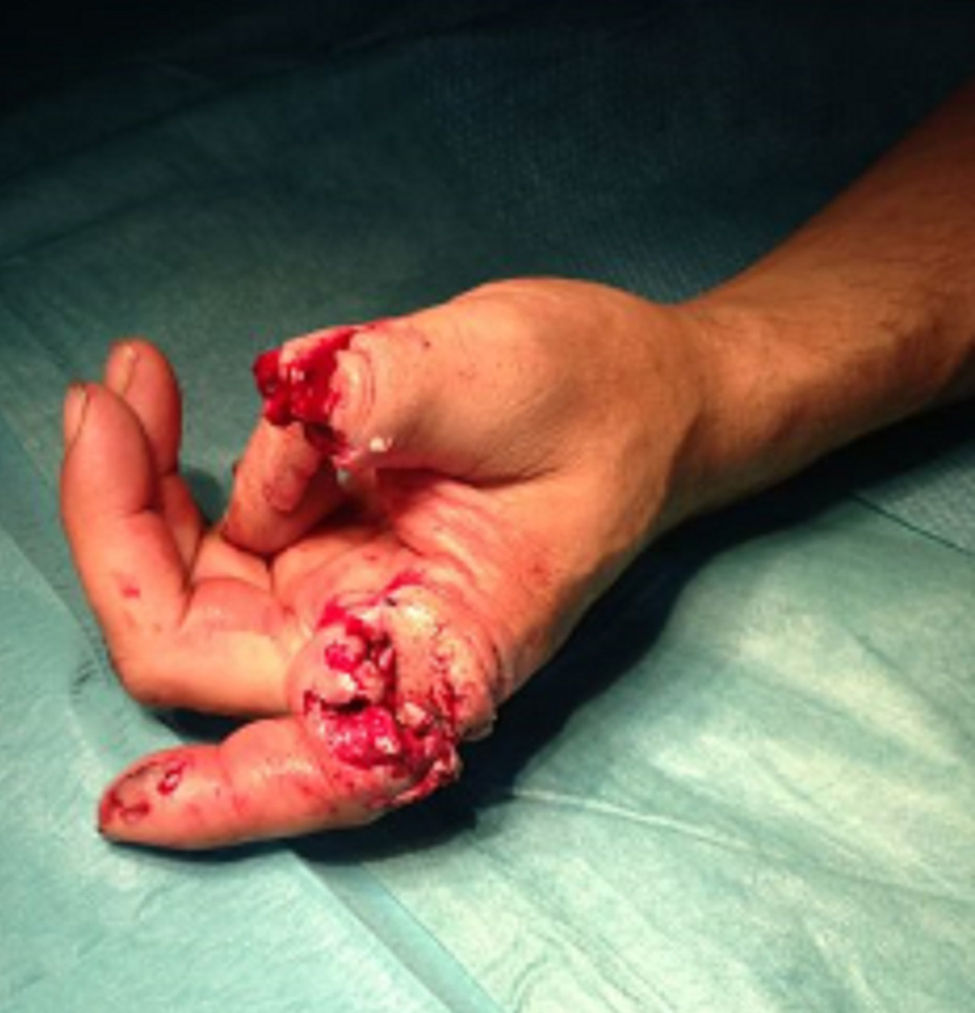
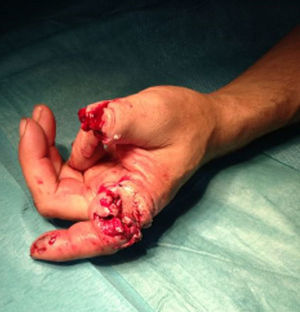
Caso clínicoPresentamos el caso de un paciente de 46 años con amputación traumática de la falange proximal del primer y segundo dedo (fig. 1). Como antecedentes personales destaca: cirrosis hepática por virus de la hepatitis B estadio A en la clasificación de Child-Turcotte-Pugh y resección quirúrgica de hepatocarcinoma. Tras la valoración del caso por un equipo multidisciplinar constituido por cirujanos plásticos, traumatólogos y anestesiólogos, se decidió la realización de un reimplante digital. Como pruebas complementarias se obtuvo hemograma, bioquímica y estudio de coagulación, sin alteraciones.
Tras monitorización habitual no invasiva mediante presión arterial, electrocardiograma, pulsioximetría (SpO2), bloqueo neuromuscular mediante monitor TOF watch SX y colocación de manta térmica, se administraron 3mg de midazolam para disminuir la ansiedad. Se colocó al paciente en decúbito supino con el brazo en abducción 90° respecto al tronco, localizándose la arteria axilar mediante ecografía. Se objetivaron los nervios mediano, cubital, musculocutáneo y radial, realizándose un abordaje en plano del plexo con la aguja. Se introdujo el catéter en el compartimento fascial perivascular del plexo braquial para mantener una analgesia continua administrándose inicialmente una dosis de ropivacaína 0,2% de 20ml a través del catéter. Posteriormente se realizó una inducción anestésica con propofol 150mg, fentanilo 150μg y cisatracurio 18mg siendo intubado y conectado a ventilación mecánica. Para el mantenimiento anestésico se emplearon sevoflurano a 1 CAM y perfusión continua de ropivacaína 0,2% a 6ml/h a través de catéter nervioso. El paciente se mantuvo estable hemodinámicamente durante el periodo intraoperatorio de 5 horas. Se realizó una remodelación del primer dedo y anastomosis de los pedículos vasculares manteniendo un adecuado nivel analgésico. Tras la finalización del procedimiento y extubación, fue trasladado a la unidad de reanimación postoperatoria. Durante el periodo postoperatorio evolucionó de forma favorable objetivándose una buena perfusión distal mediante ecografía doppler y colocación del pulsioxímetro en el dedo reimplantado. Se mantuvo el catéter axilar y una perfusión continua con ropivacaína 0,2% a 6ml/h durante 72 horas con un adecuado nivel analgésico y valor en escala visual análoga menor de 3 sin precisar analgesia coadyuvante, sin objetivarse lesión neural ni complicaciones.
DiscusiónEl BCPB mediante abordaje axilar con anestésicos locales es una técnica ampliamente utilizada por los anestesiólogos6, dada su alta eficacia analgésica y bajo riesgo de complicaciones. Ha demostrado mejorar la perfusión tisular digital tras la cirugía microvascular de reimplante como consecuencia del bloqueo simpático y la vasodilatación asociada al mismo7–10, disminuyendo el riesgo de vasoespasmo postoperatorio1,2 en áreas donde la circulación periférica pueda hallarse comprometida1 con el consiguiente aumento de la temperatura del mismo1.
El BCPB ofrece un inmejorable nivel de analgesia durante el periodo postoperatorio siendo esta la principal indicación del mismo2,10, tratándose de una técnica analgésica ideal para la cirugía de reimplante de miembro9. Dados los escasos centros que realizan esta cirugía, existen pocos casos descritos. El BCPB presenta otras indicaciones: la insuficiencia vascular causada por el tratamiento con fármacos vasoactivos, lesiones traumáticas de la mano, amputaciones digitales, cirugía prolongada del miembro superior y tratamiento en el síndrome de dolor regional complejo1. La anestesia regional mantiene de forma prolongada y continua la vasodilatación de la extremidad intervenida1,2,9,10. Se han descrito complicaciones2,11 en relación al bloqueo del plexo braquial como infecciones, hematomas12, retención de fragmentos del catéter, parestesias y toxicidad farmacológica2,11. El avance en el manejo de la ecografía ha permitido reducir la incidencia de lesiones neurovasculares13 por la visualización directa de los nervios, la aguja, las estructuras adyacentes y principalmente el control de la distribución del anestésico local6.
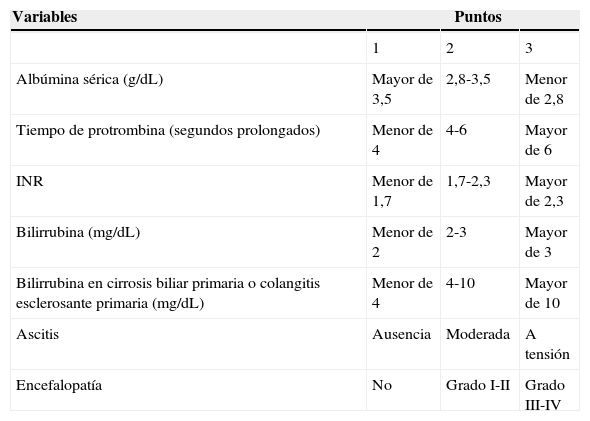
Los hepatópatas presentan un alto riesgo de morbimortalidad perioperatoria14 debido a los efectos de la cirugía y la anestesia sobre el hígado. Se han empleado diferentes escalas de evaluación pronóstica como la clasificación de Child-Pugh-Turcotte (tabla 1) o el modelo matemático de predicción de supervivencia en pacientes con enfermedad en estadio terminal (MELD –Model for End-stage Liver Disease–), que evalúa las variables: niveles de creatinina, de bilirrubinas, el International Normalized Ratio, el tiempo de protrombina y la etiología de la hepatopatía.
Clasificación modificada de Child-Turcotte-Pugh. Clases A: 5-6; B: 7-9; C: 10-15
| Variables | Puntos | ||
|---|---|---|---|
| 1 | 2 | 3 | |
| Albúmina sérica (g/dL) | Mayor de 3,5 | 2,8-3,5 | Menor de 2,8 |
| Tiempo de protrombina (segundos prolongados) | Menor de 4 | 4-6 | Mayor de 6 |
| INR | Menor de 1,7 | 1,7-2,3 | Mayor de 2,3 |
| Bilirrubina (mg/dL) | Menor de 2 | 2-3 | Mayor de 3 |
| Bilirrubina en cirrosis biliar primaria o colangitis esclerosante primaria (mg/dL) | Menor de 4 | 4-10 | Mayor de 10 |
| Ascitis | Ausencia | Moderada | A tensión |
| Encefalopatía | No | Grado I-II | Grado III-IV |
Fuente: elaboración propia.
Algunos autores sugieren que un paciente con un MELD menor de 10 puede ser sometido a procedimientos electivos; entre 10 y 15 la cirugía electiva puede realizarse ante la posibilidad de efectos adversos en función del procedimiento quirúrgico; mayor de 15 la cirugía electiva debe ser evitada y generalmente el paciente se considera candidato a trasplante hepático15. Al caso expuesto, con clasificación Child A y MELD menor de 10, se asocia un riesgo anestésico moderado.
En la cirrosis hepática existe un riesgo aumentado de coagulopatía4,14. La corrección de la coagulopatía es controvertida, ya que la expansión de volumen puede ser un factor de sangrado al incrementar la presión portal y producir un desequilibrio entre los factores pro- y anticoagulantes4. Debe reservarse a las situaciones de sangrado activo y evidencia de un déficit de factores de coagulación4.
Se recomienda una monitorización mediante el catéter de fracción de eyección del ventrículo derecho y ecocardiografía transesofágica4 sobre todo en cirugía intraabdominal y MELD mayor de 10, considerado un procedimiento de alto riesgo.
El hígado es el principal órgano encargado del metabolismo y eliminación de fármacos5. En la insuficiencia hepática, muchos fármacos pueden presentar una duración de acción prolongada por retraso en el metabolismo y disminución del índice de aclaramiento5,15,16. Se deben dosificar cuidadosamente las benzodiacepinas, porque el aumento de los receptores GABA condiciona una mayor sensibilidad a las mismas15. La ansiedad2 desencadenada por el dolor en el periodo postoperatorio inmediato condiciona la liberación de catecolaminas y vasoconstricción del tejido reimplantado2, por lo que su control es primordial.
Podemos clasificar en tres categorías15 los fármacos anestésicos según el comportamiento farmacocinético4, incluyéndose los hipnóticos propofol, etomidato, ketamina, morfina o fentanil4 en el grupo de baja unión proteica y alta tasa de extracción hepática, con un buen perfil de seguridad en la insuficiencia hepática e influenciados por el flujo hepático. Los otros dos grupos incluyen aquellos con una baja tasa de extracción hepática que se acumulan en la cirrosis (tiopental diazepam y metadona)4, y los dependientes parcialmente del flujo sanguíneo hepático con una actividad relacionada directamente con la concentración plasmática (midazolam, bloqueantes neuromusculares)4. Para el mantenimiento anestésico tanto el desflurano como el sevoflurano pueden emplearse de forma segura, asociándose el sevoflurano a una menor elevación de las transaminasas en el periodo postoperatorio15,16.
El cisatracurio plantea la mejor alternativa como bloqueante neuromuscular ya que se metaboliza por la vía de Hoffman, independiente de la afectación hepática.
El BCPB, reduce el empleo de opioides ofreciendo el fentanilo un buen perfil de seguridad4,15. El remifentanilo, con un metabolismo independiente del hígado por estearasas plasmáticas, resulta el fármaco opioide de elección durante el periodo intraoperatorio15. El empleo de AINES15 presenta ciertas limitaciones en la insuficiencia hepática, ya que la inhibición de la síntesis de prostaglandinas podría exacerbar el estado de vasoconstricción de las arterias renales causada por la presencia de sustancias vasoconstrictoras15 (como la angiotensina II o la noradrenalina).
En resumen en la cirugía de reimplante digital una técnica anestésica combinada se considera la mejor estrategia anestésica, permitiendo el BCPB optimizar la perfusión distal y aumentar la supervivencia del injerto previniendo el desarrollo de vasoespasmo en las arterias digitales del miembro reimplantado17,18. En el manejo anestésico de la disfunción hepática están implicados el metabolismo de los fármacos, la circulación hiperdinámica, la hipoxemia perioperatoria y el riesgo hemorrágico14.
Responsabilidades éticasDerecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Protección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
FinanciamientoLos autores no recibieron patrocinio para llevar a cabo este artículo.
Conflicto de interesesLos autores declaran no tener conflicto de intereses.