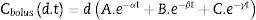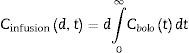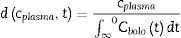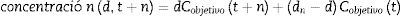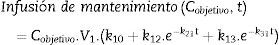La administración de remifentanil y propofol con el uso de perfusores TCI ha mostrado beneficios en la práctica anestésica, sin embargo, su disponibilidad es limitada.
ObjetivoBasados en modelos farmacocinéticos, diseñar un algoritmo capaz de calcular esquemas de infusión manual para alcanzar concentraciones en plasma y sitio efecto que puedan ser utilizados en bombas de infusión volumétricas. Adicionalmente, comparar la diferencia entre concentraciones deseadas y predichas mediante simulación farmacocinética.
MétodosSiguiendo modelos de Minto y Schnider para remifentanil y propofol, respectivamente, el algoritmo se implementó en una aplicación llamada interactive TIVA (iTIVA) para los sistemas operativos iOS y Android. El desempeño del algoritmo se evaluó calculando esquemas de infusión para obtener distintas concentraciones en sitio efecto en la inducción y mantenimiento en 34 pacientes teóricos durante 240 min.
ResultadosLos esquemas de infusión obtenidos para remifentanil y propofol presentaron una desviación sistemática promedio menor al 5% respecto a las concentraciones en sitio efecto objetivo en la inducción y mantenimiento. En la inducción una única infusión fue requerida para el remifentanil y propofol. Durante el mantenimiento, una única tasa de infusión fue requerida para el remifentanil y entre 2 y 5 cambios de tasa de infusión para el propofol para mantener una concentración estable. El algoritmo implementado en iTIVA calcula concentraciones similares que el software TivaTrainer®.
ConclusionesEl desempeño del algoritmo para alcanzar concentraciones en sitio efecto durante la inducción y mantenimiento para remifentanil y propofol fue excelente con una desviación sistemática baja con respecto a las concentraciones objetivo deseadas.
Remifentanil and propofol infusion using TCI pumps has proven to be beneficial for the practice of anesthesia but the availability of these systems is limited.
ObjectiveDesigning a pharmacokinetic model-based algorithm for calculating manual infusion regimens to achieve plasma and effect-site concentrations that may be used in volume infusion pumps, and to compare the difference between the desired and the forecasted concentrations via pharmacokinetic simulation.
MethodsUsing the Minto & Schnider models for remifentanil and propofol respectively, the algorithm was implemented on an iTIVA application (interactive TIVA) for iOS and Android operating systems. The performance of the algorithm was evaluated estimating the infusion regimens for achieving different effect-site concentrations for induction and maintenance in 34 theoretical patients for 240minutes.
ResultsThe infusion regimens obtained for remifentanil and propofol resulted in less than 5% average systemic deviation versus the target effect-site concentrations during induction and maintenance. Only one induction infusion was required for remifentanil and propofol. Just one infusion rate was required for remifentanil during maintenance, and between 2 to 5 infusion rate changes for propofol to maintain a stable concentration. The iTIVA-based algorithm estimates concentrations similar to the TivaTrainer® software.
ConclusionsThe performance of the algorithm to achieve effect-site concentrations during induction and maintenance for remifentanil and propofol was excellent, with a low systemic deviation versus the desired target concentrations.
En la práctica actual de la anestesiología, los fármacos intravenosos son administrados utilizando dosificaciones estándar que se ajustan de manera empírica. Esta aproximación ignora la variabilidad interindividual de la cinética de los fármacos, la relación variable entre la dosis y la concentración en plasma y conlleva en algunas ocasiones a efectos adversos1.
En las últimas 2 décadas se han desarrollado modelos matemáticos —producto del estudio de las concentraciones plasmáticas de distintos fármacos— que describen el proceso de distribución y eliminación de los mismos. Estos han permitido predecir el efecto de administrar múltiples bolos, infusiones intravenosas o la combinación de ambos. El uso de estos modelos facilita la enseñanza y el aprendizaje de la farmacocinética aplicada a la anestesiología2,3.
La tecnología computacional ha facilitado la incorporación de los modelos teóricos para la simulación farmacocinética de fármacos como propofol (modelo de Schnider)4 y remifentanil (modelo de Minto)5. Estos sistemas permiten controlar las infusiones ajustándolas a determinadas concentraciones objetivo del fármaco deseado6-9. Esta tecnología se conoce en la actualidad como target control infusión (infusión controlada por objetivo, por sus siglas en inglés como TCI) y ha facilitado la administración de fármacos intravenosos como el remifentanil y propofol, permitiendo una rápida titulación para alcanzar distintos objetivos terapéuticos con mayor estabilidad hemodinámica3,10.
La disponibilidad de perfusores TCI en nuestra práctica diaria es limitada y pocos centros hospitalarios cuentan con estos, lo cual ha limitado la utilización de anestesia total intravenosa. Sin embargo, aun en países con libre acceso a la tecnología TCI, solo un 15-40% administran TIVA con esta tecnología11-13 y restricciones de acceso en Estados Unidos de América o restricciones económicas, como en muchos países en desarrollo14,15, limitan su amplia difusión y uso. Por lo tanto, la administración manual de fármacos anestésicos con bombas de infusión volumétricas (BIV) es una práctica vigente.
En la actualidad, se han desarrollado sistemas de TCI pasivos que muestran la simulación farmacocinética en tiempo real de los fármacos administrados, los cuales han demostrado facilitar conseguir concentraciones estables en plasma y sitio efecto, con disminución en la carga mental para el anestesiólogo16-18. Estos sistemas solo se encuentran disponibles en ciertas máquinas de anestesia (p. ej., Navigator Applications Suite-GE Healthcare y SmartPilot View-Drager Medical), exigen una titulación cuidadosa pero no sugieren al profesional una tasa de infusión para alcanzar una concentración deseada19.
A diferencia de los sistemas de TCI pasivos, los perfusores TCI alcanzan concentraciones en plasma y sitio efecto de una manera rápida y precisa con el uso de complejos esquemas de infusión que varían cada 10 s controlados por un microprocesador según un modelo farmacocinético, manteniendo concentraciones estables en el tiempo20. Hasta el momento, no es posible emular el desempeño de los perfusores TCI con un método manual, dadas la alta complejidad matemática y la variación estrecha de las tasas de infusión.
Utilizando los modelos descrito por Minto et al.5 y Schnider et al.4 —para remifentanil y propofol, respectivamente— es posible alcanzar y mantener concentraciones en plasma y sitio efecto utilizando un algoritmo matemático que permita una pequeña —y tolerable— variación en dichas concentraciones. Basados en esta hipótesis, el objetivo de este estudio fue diseñar un algoritmo capaz de calcular esquemas de infusión manual para alcanzar concentraciones en plasma y sitio efecto, y comparar la diferencia entre las concentraciones deseadas y las predichas mediante simulación farmacocinética.
MetodologíaEste estudio fue desarrollado en 2 fases: primero se obtuvo la información teórica sobre el comportamiento farmacocinético de los fármacos anestésicos intravenosos, con lo cual se desarrolló un algoritmo para simular concentraciones en plasma y sitio efecto, y calcular esquemas de infusión para alcanzar una concentración en plasma y sitio efecto específicas. Este algoritmo se implementó en una aplicación móvil llamada «iTIVA» (del inglés, interactive TIVA, TIVA interactiva), para los sistemas operativos iOS y Android.
En la segunda fase se usó la simulación de los esquemas de infusión calculados a partir del algoritmo desarrollado como método para evaluación, como ha sido descrito en trabajos previos21.
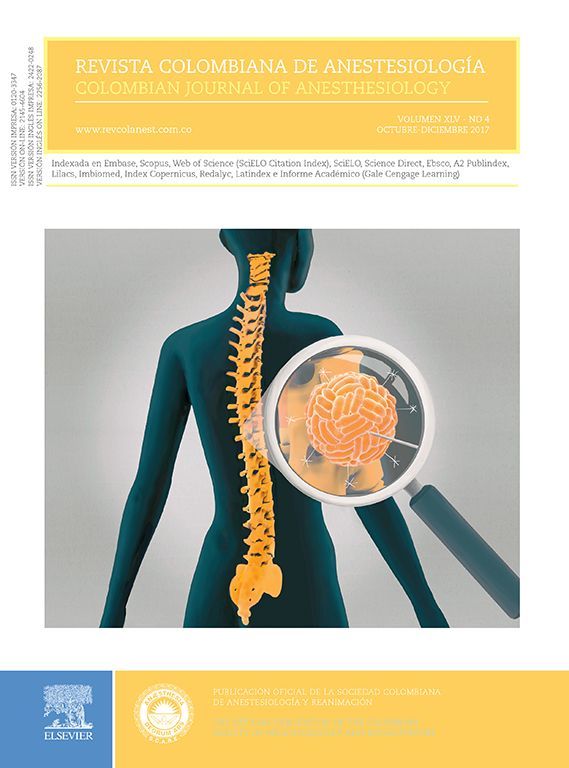
Desarrollo del algoritmoLa mayoría de los modelos de los anestésicos intravenosos como el remifentanil y propofol están basados en modelos tricompartimentales2,3, que son descritos por la ecuación 1, que predice la concentración en plasma luego de un bolo «d» en un tiempo «t»21:
La concentración plasmática de una infusión continua a una dosis «d» es igual a la repetición infinitesimal de bolos «di» equivalentes a «d» en un tiempo «t», lo cual es descrito por la integral de la ecuación 1:
Al despegar «d» de la ecuación 2, se obtiene la dosis de infusión «d» para alcanzar una concentración plasmática en un tiempo «t».
Cuando se varían las infusiones en el tiempo, la diferencia entre la nueva infusión «dn» en un tiempo «t+n» se adiciona a la primera infusión, como se describe en la ecuación 4:
Las concentraciones en sitio efecto se obtienen a partir de las concentraciones plasmáticas a través de una solución no analítica explicado en la sección de códigos en el sitio web http://www.opentci.org/
Con la ecuación 3 se obtiene una velocidad de infusión «d» para alcanzar concentraciones en plasma «Cp» en un tiempo «t», a partir de esa velocidad de infusión «d», se aumenta «d» iterativamente en 0,1, hasta obtener la dosis «d» para alcanzar la concentración en sitio efecto objetivo.
Posteriormente, debemos calcular una infusión de mantenimiento que compense las pérdidas por distribución y eliminación, para mantener un estado seudoestable para una concentración deseada. Para lo cual la ecuación 5 permite calcular una tasa de infusión «d» en un tiempo «t», la cual compensa en ese momento las pérdidas por distribución y eliminación, la cual se mantiene por un tiempo «t+n», hasta que la concentración en plasma simulada supere la concentración objetivo «C»+0,1, en ese momento se recalcula una nueva infusión de mantenimiento en un tiempo «t+n», con la ecuación 5, y así sucesivamente durante el tiempo que deseemos mantener la concentración.
Durante el mantenimiento no hay diferencia cuando el objetivo es plasma o sitio efecto, dado que ambos compartimientos tienden a equilibrarse rápidamente durante esta etapa.
Desempeño del algoritmoPara evaluar el desempeño de iTIVA en obtener concentraciones en sitio efecto a partir de un esquema de infusión manual, se usaron datos de 34 pacientes teóricos. A partir de estos, se calcularon esquemas de infusión para un tiempo de 240 min, para obtener diferentes concentraciones en sitio efecto, asignadas de manera aleatoria para remifentanil y propofol. Los datos utilizados se muestran en la tabla 1.
Datos antropométricos de los pacientes simulados (n=34)
| Remia | Propoa | |||||||
|---|---|---|---|---|---|---|---|---|
| Sexo | Edad (años) | Peso (kg) | Altura (cm) | IMC (kg/m2) | (ng/ml) | (μg/ml) | ||
| I | M | I | M | |||||
| F | 77 | 88 | 166 | 31,9 | 7,0 | 5,0 | 3,0 | 2,5 |
| F | 70 | 84 | 174 | 27,7 | 5,0 | 4,0 | 3,0 | 2,0 |
| F | 46 | 91 | 166 | 33,0 | 7,0 | 5,0 | 3,0 | 2,0 |
| F | 72 | 76 | 155 | 31,6 | 5,0 | 4,0 | 3,0 | 2,5 |
| F | 55 | 68 | 170 | 23,5 | 7,0 | 5,0 | 3,0 | 2,0 |
| F | 51 | 58 | 161 | 22,4 | 7,0 | 5,0 | 3,5 | 3,0 |
| F | 21 | 56 | 160 | 21,9 | 7,0 | 5,0 | 3,0 | 2,5 |
| F | 33 | 62 | 156 | 25,5 | 7,0 | 5,0 | 3,5 | 3,0 |
| F | 36 | 54 | 158 | 21,6 | 5,0 | 4,0 | 3,0 | 2,0 |
| F | 28 | 68 | 156 | 27,9 | 5,0 | 4,0 | 3,0 | 2,5 |
| F | 61 | 71 | 174 | 23,5 | 7,0 | 5,0 | 3,5 | 3,0 |
| F | 31 | 88 | 180 | 27,2 | 7,0 | 5,0 | 3,5 | 3,0 |
| F | 65 | 90 | 182 | 27,2 | 5,0 | 4,0 | 3,0 | 2,0 |
| M | 30 | 81 | 186 | 23,4 | 7,0 | 5,0 | 3,0 | 2,5 |
| M | 27 | 79 | 171 | 27,0 | 7,0 | 5,0 | 3,5 | 3,0 |
| M | 41 | 102 | 188 | 28,9 | 7,0 | 5,0 | 3,5 | 3,0 |
| M | 75 | 61 | 158 | 24,4 | 5,0 | 4,0 | 3,0 | 2,0 |
| M | 26 | 110 | 173 | 36,8 | 7,0 | 5,0 | 3,0 | 2,5 |
| M | 72 | 79 | 167 | 28,3 | 5,0 | 4,0 | 3,0 | 2,0 |
| M | 31 | 64 | 177 | 20,4 | 7,0 | 5,0 | 3,5 | 3,0 |
| M | 25 | 88 | 178 | 27,8 | 5,0 | 4,0 | 3,0 | 2,0 |
| M | 62 | 70 | 170 | 24,2 | 5,0 | 4,0 | 3,0 | 2,5 |
| M | 22 | 70 | 168 | 24,8 | 7,0 | 5,0 | 3,5 | 3,0 |
| M | 44 | 72 | 162 | 27,4 | 7,0 | 5,0 | 3,5 | 3,0 |
| M | 53 | 86 | 150 | 38,2 | 5,0 | 4,0 | 3,0 | 2,0 |
| M | 66 | 72 | 164 | 26,8 | 5,0 | 4,0 | 3,0 | 2,5 |
| M | 27 | 62 | 154 | 26,1 | 7,0 | 5,0 | 3,0 | 2,5 |
F: femenino; M: masculino.
Los datos fueron tabulados en Microsoft Excel 2011 (Redmond, EE. UU.) y exportados al paquete estadístico R para su análisis y manejo gráfico22. Las medias ± desviaciones estándar de las concentraciones simuladas fueron calculadas para cada minuto y los datos se agruparon de acuerdo con las concentraciones objetivo en sitio efecto.
Para evaluar la precisión de las concentraciones predichas por iTIVA se calcularon el error predictivo, la tasa de error predictivo y la desviación sistemática (o sesgo) con respecto a la concentración deseada (tabla 2). Esta metodología fue previamente descrita por Lerou y Booij23. Estos resultados se presentan de forma gráfica mediante estadísticos de resumen y de dispersión. El desempeño del algoritmo se analizó de manera independiente para obtener concentraciones objetivo durante la inducción y mantenimiento. Por definición, se consideró la inducción como el periodo comprendido entre el quinto y sexto minutos, y el mantenimiento como el periodo entre el minuto 7 hasta la finalización de la simulación (minuto 240).
Definición de las variables para estimación del desempeño
| Variable | Unidad | Definición matemática | Definición |
|---|---|---|---|
| Error predicho (ep) | No aplica | ep=Cp−Cd | Diferencia entre las concentraciones predichas y deseadas |
| Porcentaje de error predicho (%ep) | % | %ep=Cp−CdCd×100 | Porcentaje de error entre las concentraciones predichas y deseadas |
| Desviación sistemática (DS) | % | DS=1n∑i=1n%ep | Desviación sistemática del error total, con dirección (signo) y magnitud |
Cd: concentración deseada; Cp: concentración predicha.
Fuente: adaptada de Lerou et al.23.
Finalmente, las concentraciones obtenidas en plasma y sitio efecto mediante iTIVA se compararon con las concentraciones calculadas con el software TivaTrainer® (versión 8; European Society for Intravenous Anaesthesia, Glasgow, Reino Unido) (tabla 3). Dados los resultados post hoc, no se realizaron contrastes de hipótesis en esta comparación.
Concentraciones en plasma y sitio efecto para propofol y remifentanil al simular distintos esquemas de infusión con iTIVA vs. TivaTrainer®
| iTIVA | TivaTrainer® | |||
|---|---|---|---|---|
| Tiempo (min) | Plasma | Sitio efecto | Plasma | Sitio efecto |
| Propofol | ||||
| Minuto 5 | 3,0±0,7 | 2,4±0,5 | 3,0±0,7 | 2,4±0,5 |
| Minuto 10 | 2,2±0,6 | 2,2±0,6 | 2,2±0,6 | 2,2±0,6 |
| Minuto 30 | 2,3±0,5 | 2,4±0,5 | 2,3±0,5 | 2,4±0,5 |
| Minuto 60 | 2,4±0,5 | 2,4±0,5 | 2,4±0,5 | 2,4±0,5 |
| Minuto 120 | 2,3±0,5 | 2,4±0,5 | 2,3±0,5 | 2,4±0,5 |
| Minuto 180 | 2,4±0,5 | 2,4±0,5 | 2,4±0,5 | 2,4±0,5 |
| Minuto 240 | 2,3±0,5 | 2,4±0,5 | 2,3±0,5 | 2,4±0,5 |
| Remifentanil | ||||
| Minuto 5 | 6,5±2,9 | 5,2±2,3 | 6,5±2,9 | 5,2±2,3 |
| Minuto 10 | 4,0±1,7 | 4,3±1,8 | 4,0±1,7 | 4,3±1,8 |
| Minuto 30 | 4,1±1,8 | 4,1±1,7 | 4,1±1,8 | 4,1±1,7 |
| Minuto 60 | 4,1±1,8 | 4,1±1,8 | 4,1±1,8 | 4,1±1,8 |
| Minuto 120 | 4,2±1,8 | 4,2±1,8 | 4,2±1,8 | 4,2±1,8 |
| Minuto 180 | 4,2±1,8 | 4,2±1,8 | 4,2±1,8 | 4,2±1,8 |
| Minuto 240 | 4,2±1,8 | 4,2±1,8 | 4,2±1,8 | 4,2±1,8 |
Los datos se presentan como media±desviación estándar (DE).
Fuente: autores.
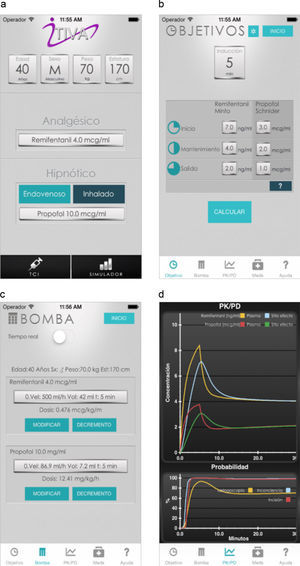
El algoritmo se implementó exitosamente en una aplicación para iOS y Android, la cual se encuentran disponible de manera gratuita en AppStore y Google Play. La figura 1 muestra diferentes pantallas de la aplicación para iPhone, entre ellas, ingreso de datos antropométricos, las concentraciones objetivo, el esquema de infusión calculado y la visualización gráfica del comportamiento farmacocinético y farmacodinámico24 en el tiempo.
Para poder mantener una concentración estable durante la inducción, se requirió una única velocidad de infusión para remifentanil y propofol. Para mantener una concentración estable durante los 235 min del mantenimiento, se necesitó una única velocidad de infusión para remifentanil y entre 2 y 5 variaciones de la velocidad de infusión para propofol (moda=4).
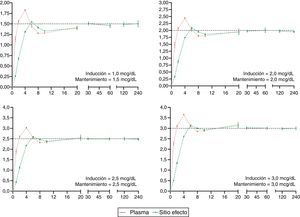
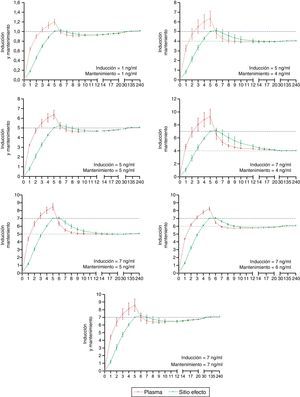
Las concentraciones deseadas y predichas para plasma y sitio efecto resultado de la simulación y organizadas por objetivos deseados para propofol y remifentanil se presentan en las figuras 2 y 3 respectivamente. Los ejes de tiempo (eje X) presentan un énfasis en los minutos iniciales correspondientes a la inducción anestésica.
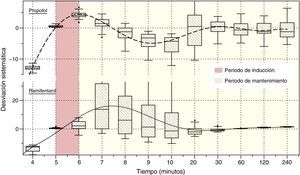
La figura 4 presenta la desviación sistemática versus el tiempo de las concentraciones predichas para propofol y remifentanil por el algoritmo en comparación con las deseadas por el operador.
Las concentraciones en plasma y sitio efecto, así como su variabilidad al simular distintos esquemas de infusiones con el algoritmo implementado en iTIVA versus las calculadas con el software TivaTrainer®, fueron similares para diferentes tiempos de evaluación (tabla 3).
DiscusiónLos principales resultados de este estudio son: 1) se desarrolló e implementó el algoritmo descrito de forma exitosa; 2) el desempeño del algoritmo propuesto para alcanzar concentraciones en sitio efecto durante la inducción y mantenimiento para remifentanil y propofol fue excelente; 3) el algoritmo presenta una variabilidad tolerable con respecto a las concentraciones deseadas la cual se reduce en el periodo de mantenimiento, y 4) el algoritmo implementado en iTIVA para simular concentraciones en plasma y sitio efecto según un esquema de infusión se comporta de forma similar que el software TivaTrainer®.
Desarrollo e implementación del algoritmoLa implementación del algoritmo desarrollado se hizo sin mayores dificultades con la ayuda de herramientas de desarrollo de las compañías Apple y Google para sus sistemas iOS (Xcode) y Android (Eclipse), respectivamente. Inicialmente, el algoritmo se implementó para Android dado que ofrece menores restricciones para la publicación en su tienda de aplicaciones (este hecho facilitó la depuración del código de programación). Posteriormente, se adaptó al sistema operativo iOS aprovechando las similitudes en la sintaxis entre los lenguajes de programación (Java y C++).
Para el óptimo desempeño de este algoritmo (durante 240 min de simulación), se requieren entre 200.000 y 250.000 cálculos matemáticos. En la actualidad, esto no representa mayores limitaciones para los microprocesadores disponibles aún en dispositivos móviles básicos.
Desempeño del algoritmo y variabilidadDurante el periodo de inducción anestésica (minuto 5 y 6) la desviación sistemática de las concentraciones deseadas de los 2 medicamentos fue inferior al 5%. Esta baja variabilidad se traduce como una proximidad alta entre la concentración deseada y la alcanzada por el algoritmo.
Durante el mantenimiento (minuto 7 a 240), los esquemas de infusión mostraron cambios en la desviación sistemática, que en general fue inferior al 5% para propofol y el 15% para remifentanil. Esta variabilidad se reduce a significativamente en el minuto 20 para remifentanil y en el 30 para propofol. La divergencia observada en los primeros minutos se puede relacionar al cambio de una concentración objetivo mayor a una menor. Durante este periodo —y para mantener una concentración estable con variación inferior al 5%— se requirió una única tasa de infusión para remifentanil y entre 2 y 5 cambios progresivos en la tasa de infusión de propofol. Esta diferencia puede explicarse por las propiedades farmacocinéticas del primero que lo hacen insensible al contexto25.
A diferencia de los esquemas de infusión usados por perfusores TCI que requieren aproximadamente 1.400 cambios de la tasa de infusión durante 240 minutos, este algoritmo permite obtener esquemas sencillos que son de fácil implementación con BIV. Entrega datos con alta precisión para alcanzar y mantener concentraciones deseadas en sitio efecto, proporcionando una ventaja con respecto a la administración farmacológica de acuerdo con dosis estándar. Dichas concentraciones (según objetivos terapéuticos) han sido reportadas por diversos autores26-31.
Hay que resaltar que la mayoría de los procesos de simulación farmacológica están limitados por la variación interindividual y el gran número de variables que alteran la farmacocinética y la farmacodinamia de los medicamentos. Este hecho reduce la precisión de los modelos farmacocinéticos y el desempeño de este y otros algoritmos. Por lo tanto, es imprescindible la evaluación de los efectos individuales. Diversos sistemas de medición de la profundidad anestésica están disponibles en la actualidad y su uso contextualizado puede mejorar ciertos desenlaces para el paciente y reducir el riesgo de eventos indeseables como el recordar intraoperatorio32.
Esta investigación no presenta una validación de una predicción farmacológica versus una concentración real (medida en sangre). Recurrimos a la estrategia usada por Lerou et al.23, ya utilizada por otros autores, que permitió de forma sencilla comparar nuestra predicción matemática (dada por el algoritmo) versus una deseada por el operador. Es de gran interés realizar en el futuro una medición directa de las concentraciones en sangre y compararlas con lo predicho por el modelo propuesto.
Simulación de concentraciones: iTIVA versus TivaTrainer®El algoritmo iTIVA permite obtener en tiempo real las concentraciones en plasma y sitio efecto de los esquemas calculados (de acuerdo con las ecuaciones 1 y 2). Las concentraciones obtenidas con iTIVA son iguales a las de TivaTrainer®; este último software es utilizado ampliamente en investigación y simulación farmacológica2. Este hallazgo, que era esperado puesto que ambas aplicaciones están basadas en el mismo algoritmo matemático, confirma la adecuada implementación del mismo en iTIVA.
ConclusiónMediante el uso de modelos farmacocinéticos, la aplicación iTIVA cuantifica las velocidades de infusión necesarias para alcanzar concentraciones en sitio efecto de manera manual para remifentanil y propofol y esto facilita su uso en BIV. Hasta el momento, esta aplicación solo está diseñada para ser una guía durante la administración de infusiones manuales. Su uso no está aprobado como estrategia única de manejo de pacientes y su utilización debe estar orientada y bajo la responsabilidad del anestesiólogo. Este artículo presenta una aproximación teórica basado en un proceso de simulación y su generalización a la práctica clínica requiere de un proceso de validación y comparación frente a otros esquemas de infusión33.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciamientoEste trabajo contó con el apoyo de la Sociedad Colombiana de Anestesiología y Reanimación SCARE.
Conflicto de interesesNinguno declarado.