Las náuseas y vómitos postoperatorios (NVPO) son un problema frecuente en los pacientes quirúrgicos. Cuando no son prevenidos adecuadamente pueden provocar mayor morbilidad, estadía prolongada en la unidad de recuperación postoperatoria y hospitalización no planificada. El objetivo del equipo quirúrgico debe ser la profilaxis de las NVPO más que su tratamiento, con el fin de disminuir significativamente su incidencia y complicaciones asociadas.
Los principales factores de riesgo para NVPO son: sexo femenino, historia de NVPO en cirugías previas y/o cinetosis, no fumar, uso de opioides sistémicos en el postoperatorio, someterse a ciertos tipos de cirugía (como colecistectomía, cirugía laparoscópica y cirugía ginecológica), utilizar anestésicos volátiles y/u óxido nitroso intraoperatorios, y duración de la cirugía. Sugerimos objetivar el riesgo de NVPO utilizando las escalas de riesgo de NVPO de Apfel o Koivuranta. Los principales fármacos antieméticos usados como profilaxis y tratamiento en el período perioperatorio son dexametasona, ondansetrón y droperidol.
Existen estrategias generales que se pueden utilizar para reducir el riesgo quirúrgico basal de NVPO como evitar la anestesia general, privilegiando la anestesia regional, utilizar propofol para la inducción y mantención de la anestesia, evitar el uso de óxido nitroso y/o anestésicos inhalatorios, minimizar el uso postoperatorio de opioides sistémicos y recibir una hidratación intravenosa abundante durante la cirugía.
La etiología de las NVPO es multifactorial, por lo que la prevención y tratamiento deben incluir diferentes clases de antieméticos, que actúen sobre los diferentes receptores de náuseas y/o vómitos hasta el momento conocidos, junto con las estrategias generales antes mencionadas.
Postoperative nausea and vomiting (PONV) are a common problem in surgical patients. When not properly prevented, they can lead to increased morbidity, prolonged stay in the postoperative recovery unit and unplanned hospitalization. The objective of the surgical team should be the prophylaxis of PONV rather than its treatment, in order to significantly reduce its incidence and associated complications.
The main risk factors for PONV are: female sex, history of PONV in prior surgeries and/or motion sickness, non-smoking, use of systemic opioids postoperatively, undergo certain types of surgery (such as cholecystectomy, laparoscopic surgery and gynecological surgery), use volatile anesthetics and/or intraoperative nitrous oxide, and duration of surgery. We suggest to objectify the risk of PONV using the Apfel or Koivuranta PONV risk scales. The main anti-emetic drugs used as prophylaxis and treatment in the perioperative period are dexamethasone, ondansetron and droperidol.
There are general strategies that can be used to reduce the baseline surgical risk of PONV such as avoiding general anesthesia, favoring regional anesthesia, using propofol for induction and maintenance of general anesthesia, avoiding the use of nitrous oxide and/or inhalational anesthetics, minimizing the postoperative use of systemic opioids and to receive an abundant intravenous hydration during surgery.
The etiology of PONV is multifactorial, so prevention and treatment should include different classes of antiemetics, acting on the different receptors of nausea and/or vomiting so far known, together with the general strategies mentioned above.
Las náuseas y vómitos postoperatorios (NVPO) son un problema frecuente en los pacientes quirúrgicos, con una incidencia del 50% y del 30% respectivamente1. En pacientes con alto riesgo de presentar esta complicación pueden llegar a una incidencia de hasta el 80%2. Las NVPO pueden prolongar significativamente el tiempo de estadía en la unidad de recuperación postoperatoria (URP) y aumentar de forma relevante los costos de la cirugía3. Cada episodio de vómitos aumenta en 20min la estadía en una URP1. Además, las NVPO son la principal causa de hospitalización no programada en cirugía ambulatoria4.
Nuestro objetivo debe ser la profilaxis de las NVPO más que su tratamiento, con el fin de disminuir significativamente su incidencia, molestias secundarias del paciente y las varias complicaciones asociadas, como alteraciones hidroelectrolíticas, dehiscencia de suturas, aspiración pulmonar de contenido gástrico, aumento de la presión intracraneana, entre otras1.
El objetivo de la presente revisión es reconocer los factores de riesgo para presentar NVPO, su estratificación para realizar una profilaxis adecuada según el nivel de riesgo de manifestar esta complicación y un tratamiento basado en la mejor evidencia científica disponible en caso de presentar NVPO.
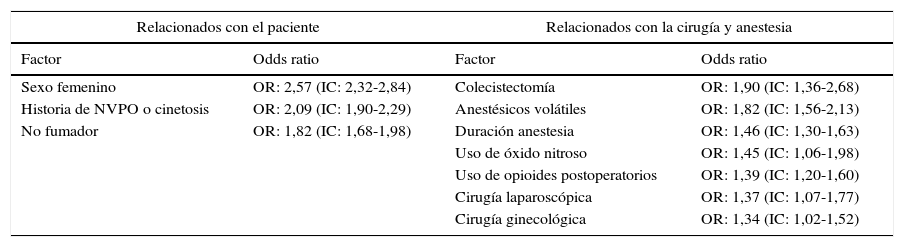
Factores de riesgo para náuseas y vómitos postoperatoriosApfel et al.5 realizaron en 2012 una revisión sistemática de 22 estudios prospectivos, con más de 500 pacientes cada uno, para identificar factores predictores independientes de NVPO. Los resultados demostraron que, de los factores de riesgo relacionados con el paciente, el sexo femenino fue el factor predictor más importante, seguido de historia de NVPO en cirugías previas y/o cinetosis, y no fumar. A mayor edad, disminuye significativamente el riesgo de NVPO, especialmente sobre los 50 años. De los factores de riesgo relacionados con la cirugía-anestesia, el uso de anestésicos inhalatorios fue el predictor más importante, seguido de duración de la anestesia, utilización de opioides postoperatorios y uso de óxido nitroso. La evidencia encontrada para el tipo de cirugía como factor de riesgo independiente de NVPO resultó controversial. Sin embargo, sí se identificaron 3 tipos de cirugías como factores predictores importantes para NVPO: colecistectomía, cirugía laparoscópica y cirugía ginecológica. Los principales factores predictores de NVPO se muestran en la tabla 15,6.
Principales factores de riesgo para NVPO relacionados con el paciente, la cirugía y la anestesia, ordenados de mayor a menor
| Relacionados con el paciente | Relacionados con la cirugía y anestesia | ||
|---|---|---|---|
| Factor | Odds ratio | Factor | Odds ratio |
| Sexo femenino | OR: 2,57 (IC: 2,32-2,84) | Colecistectomía | OR: 1,90 (IC: 1,36-2,68) |
| Historia de NVPO o cinetosis | OR: 2,09 (IC: 1,90-2,29) | Anestésicos volátiles | OR: 1,82 (IC: 1,56-2,13) |
| No fumador | OR: 1,82 (IC: 1,68-1,98) | Duración anestesia | OR: 1,46 (IC: 1,30-1,63) |
| Uso de óxido nitroso | OR: 1,45 (IC: 1,06-1,98) | ||
| Uso de opioides postoperatorios | OR: 1,39 (IC: 1,20-1,60) | ||
| Cirugía laparoscópica | OR: 1,37 (IC: 1,07-1,77) | ||
| Cirugía ginecológica | OR: 1,34 (IC: 1,02-1,52) | ||
Fuente: Apfel et al.5,6.
Apfel et al.6 en 2007 y en 2008 condujeron un estudio prospectivo, multicéntrico, de 2.170 pacientes adultos sometidos a anestesia general en cirugías ambulatorias en EE. UU. La incidencia de náuseas y vómitos posteriores al alta de una cirugía ambulatoria (NVPO CA), entre el día del alta y el segundo día postoperatorio, fue de un 37%. El análisis identificó 5 predictores independientes estadísticamente significativos para NVPO CA: náuseas en URP, edad menor de 50 años, administración de opioides postoperatorios, género femenino e historia de NVPO en anestesias previas. Los principales factores predictores para NVPO CA se muestran en la tabla 26. El puntaje en la escala de Apfel simplificada y su respectivo riesgo de presentar NVPO CA se muestran en la tabla 36.
Principales factores de riesgo para NVPO postalta de cirugía ambulatoria, ordenados de mayor a menor, con su respectivo puntaje de la escala de Apfel simplificada
| Factores de riesgo | Odds ratio | Puntaje |
|---|---|---|
| Sexo femenino | OR: 1,54 (IC: 1,22-1,94) | 1 |
| Historia de NVPO | OR: 1,50 (IC: 1,19-1,88) | 1 |
| Uso de opioides postoperatorios | OR: 1,93 (IC: 1,53-2,43) | 1 |
| Edad<50 años | OR: 2,17 (IC: 1,75-2,69) | 1 |
| Náuseas en unidad de recuperación postoperatoria | OR: 3,14 (IC: 2,44-4,04) | 1 |
| Total | 5 |
Fuente: Apfel et al.6.
Puntaje en la escala de Apfel simplificada y su respectivo riesgo de presentar NVPO postalta de cirugía ambulatoria
| Puntaje | Porcentaje de riesgo de presentar NVPO CA | Tipo de riesgo |
|---|---|---|
| 0 | 7 | Bajo |
| 1 | 20 | Bajo |
| 2 | 28 | Moderado |
| 3 | 53 | Moderado |
| 4 | 60 | Alto |
| 5 | 89 | Alto |
Fuente: Apfel et al.6.
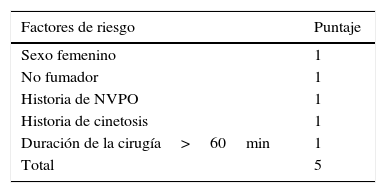
Como todos los fármacos, los antieméticos conllevan ciertos efectos adversos potenciales, por lo que el riesgo de NVPO de un paciente debiera objetivarse usando una escala de riesgo validada por la literatura médica, para elegir de la mejor manera el tipo y número de antieméticos a utilizar1. Ninguno de los factores mencionados por sí solo es suficiente para evaluar el riesgo de NVPO o para tomar decisiones sobre qué antieméticos profilácticos utilizar. El uso de escalas de riesgo y las respectivas profilaxis para NVPO han demostrado disminuir significativamente la tasa de esta complicación. Las 2 escalas más utilizadas son las de Koivuranta7 (tabla 4) y Apfel2 (tabla 5). El puntaje en la escala de Apfel y su respectivo riesgo de presentar NVPO se muestran en la tabla 62.
Puntaje de Apfel para predecir riesgo perioperatorio de NVPO
| Factores de riesgo | Puntaje |
|---|---|
| Sexo femenino | 1 |
| No fumador | 1 |
| Historia de NVPO o cinetosis | 1 |
| Uso de opioides en el postoperatorio | 1 |
| Total | 4 |
Fuente: Apfel et al.2.
Puntaje en la escala de Apfel y su respectivo riesgo perioperatorio de presentar NVPO
| Puntaje | Porcentaje de riesgo de presentar NVPO | Tipo de riesgo |
|---|---|---|
| 0 | 10 | Bajo |
| 1 | 20 | Bajo |
| 2 | 40 | Moderado |
| 3 | 60 | Moderado |
| 4 | 80 | Alto |
Fuente: Apfel et al.2.
Aunque son una aproximación objetiva para evaluar el riesgo de un paciente de presentar NVPO, ya sea en pacientes hospitalizados o cirugía ambulatoria, tienen una sensibilidad y especificidad entre 65% y el 70%1. Otro aspecto clínico que el equipo quirúrgico debe tener en consideración es si las eventuales NVPO son un riesgo médico importante para el paciente, como pacientes neuroquirúrgicos con presión intracraneana elevada o pacientes recién operados de cirugía esofágica y gástrica, ante eventuales dehiscencias de suturas.
En el año 2000, Eberhart et al.8 realizaron una comparación de las 3 escalas predictoras de NVPO disponibles a esa fecha: Apfel, Koivuranta y Palazzo. Para ello, 1.444 pacientes sometidos a diversas cirugías no recibieron profilaxis perioperatoria para NVPO y fueron observados en la URP. Las 3 escalas muestran una moderada precisión para predecir NVPO. Las escalas de Apfel y Koivuranta predicen NVPO significativamente mejor que la escala de Palazzo. Las escalas de Apfel y Koivuranta no presentan diferencias estadísticamente significativas entre ellas. Por lo tanto, nuestra recomendación es utilizar indistintamente las escalas de Apfel o Koivuranta durante la evaluación preoperatoria para estratificar el riesgo de presentar NVPO, pero siempre teniendo en cuenta la evaluación clínica de cada paciente en particular.
La estratificación del riesgo de NVPO nos permite clasificar a los pacientes en:
- a)
riesgo bajo: 0-1 factores de riesgo presentes
- b)
riesgo intermedio: 2-3 factores de riesgo
- c)
riesgo alto: 4-5 factores de riesgo, dependiendo de la escala utilizada
Las estrategias generales que se pueden utilizar para reducir el riesgo basal de NVPO son1:
- •
Evitar la anestesia general, prefiriendo la anestesia regional (evidencia tipo 1A).
- •
Utilizar propofol intravenoso (iv) para la inducción y mantención de la anestesia general (1A).
- •
Evitar el uso de óxido nitroso (1A).
- •
Evitar el uso de anestésicos inhalatorios (2A).
- •
Minimizar el uso intraoperatorio (2A) y postoperatorio de opioides (1A).
- •
Hidratación iv abundante (1A)1,9.
Los pacientes con riesgo bajo deben recibir solo un fármaco como profilaxis de NVPO, siendo de elección la dexametasona 4mg iv al inicio de la cirugía, principalmente por su bajo costo y alta efectividad antiemética. Los pacientes con riesgo intermedio deben recibir 2 fármacos antieméticos profilácticos, siendo de preferencia el uso de dexametasona antes descrito, junto a ondansetrón 4mg iv o droperidol 0,625mg iv al final del procedimiento quirúrgico. Los pacientes con riesgo alto deberían recibir 2-3 fármacos antieméticos, como los ya mencionados, además de todas las estrategias generales anteriormente descritas.
Apfel et al.10 realizaron en 2004 un estudio aleatorizado, ciego, de 5.199 pacientes con alto riesgo de NVPO, quienes recibieron en el período perioperatorio hasta 3 fármacos antieméticos diferentes. Ondansetrón, dexametasona y droperidol fueron igualmente efectivos como profilaxis, reduciendo cada uno el riesgo de NVPO en aproximadamente un 25%. El propofol intraoperatorio redujo este riesgo en un 19%. Un 34% del total de los pacientes presentaron NVPO, mientras que un 31% mostró solo náuseas y un 14% únicamente vómitos. Las tasas de efectos adversos fueron similares con cualquier antiemético. El hecho de aumentar el número de antieméticos administrados redujo la incidencia de NVPO desde un 52% sin antieméticos a un 37, 28 y 22%, con el uso de uno, 2 o 3 de estos fármacos respectivamente. Al administrar 2 antieméticos, combinando dexametasona, ondansetrón y/o droperidol, no hubo diferencias estadísticamente significativas de una pareja de fármacos sobre otra para prevenir el riesgo de NVPO10.
Fármacos utilizados para la profilaxis y tratamiento de las náuseas y vómitos postoperatoriosAntagonistas del receptor de 5-hidroxitriptaminaActualmente, ondansetrón es el estándar de oro para la prevención de las NVPO, teniendo un mayor efecto en la prevención de vómitos que náuseas. Tiene una dosis recomendada de 4mg iv y 8mg vía oral (vo)11. Es tan efectivo como otros antagonistas del receptor de 5-hidroxitriptamina (5-HT3), incluyendo granisetrón 1-3mg. También es tan eficaz como la dexametasona 4mg y haloperidol 1mg iv12. Los antagonistas 5-HT3 son más efectivos en la profilaxis de NVPO cuando son administrados al final del procedimiento quirúrgico, aunque el palonosetrón se indica típicamente al comienzo de la cirugía. Los antagonistas 5-HT3 tienen un buen perfil de seguridad, sin embargo, todos salvo el palonosetrón prolongan el intervalo QT del electrocardiograma en dosis superiores a 16mg iv. Otros efectos adversos descritos son cefalea, elevación de enzimas hepáticas y estreñimiento, aunque poco frecuentes1.
CorticoidesLa dexametasona puede ser administrada como profilaxis o tratamiento para las NVPO13,14. Una dosis profiláctica de 4-5mg iv es recomendada después de la inducción anestésica en pacientes con riesgo de presentar esta complicación. Su eficacia en la profilaxis es similar a la del ondansetrón 4mg iv y droperidol 1,25mg iv. Estudios recientes prefieren una dosis de 8mg iv, en vez de la dosis mínima de 4-5mg15,16, ya que esta dosis mejora la calidad de la recuperación postoperatoria global, además de reducir significativamente las náuseas, el dolor y la fatiga. Por otro lado, la dexametasona tendría un efecto analgésico leve a moderado, disminuyendo el uso de opioides postoperatorios17. Dentro de sus efectos adversos, la evidencia es contradictoria en relación si aumenta o no el riesgo de infección postoperatoria1, por lo que no podemos concluir nada categórico al respecto. Al recibir 8mg iv, la dexametasona sí produce aumento significativo de la glucemia intra- y postoperatoria inmediata, en pacientes con intolerancia a la glucosa, diabéticos tipo 2 y sometidos a cirugía bariátrica18,19. Recomendamos utilizar solo 4mg iv del fármaco en este tipo de pacientes para evitar una hiperglucemia postoperatoria significativa. La metilprednisolona 40mg iv también es efectiva como profilaxis, con efectos adversos similares a la dexametasona1, pero con mayor costo.
ButirofenonasLa dosis profiláctica de droperidol está entre 0,625 y 1,25mg iv, siendo efectiva para prevenir NVPO20, similar al ondansetrón y la dexametasona. Es más eficaz cuando se administra al final del procedimiento quirúrgico21. Muchos estudios han documentado un efecto similar en la prolongación del intervalo QT del electrocardiograma entre droperidol y ondansetrón22,23. El utilizar ambos fármacos combinados es más efectivo sobre la prevención de NVPO que administrar cada fármaco por separado, no así la prolongación del intervalo QT, en donde la combinación de ambos fármacos no potencia este efecto24. Por otro lado, el haloperidol también tiene propiedades antieméticas al utilizarse en dosis más bajas que las usadas para tratar enfermedades psiquiátricas y se ha investigado como una alternativa al droperidol25. Dosis de 0,5-2mg intramuscular o iv son efectivas en reducir el riesgo de NVPO, de forma similar al droperidol26, no ocurriendo sedación ni arritmias cardiacas significativas. Sin embargo, conlleva un riesgo mayor de prolongación del intervalo QT del electrocardiograma, no siendo recomendable como primera línea profiláctica o terapéutica1. En un estudio de Buttner et al.26 solo un 0,1% de los pacientes tratados con 4mg de haloperidol iv presentaron síntomas extrapiramidales. Meyer-Massetti et al.27 recomiendan dosis profilácticas de haloperidol menores a 2mg iv, las cuales tienen un significativo menor riesgo de prolongación del intervalo QT. La administración iv de haloperidol como antiemético no ha sido aprobada por la Food and Drug Administration.
MidazolamEn 2016, Grant et al.28 publicaron un metaanálisis de 12 estudios, el cual concluyó que la administración de midazolam iv, entre 2 y 5mg, en el período pre- o intraoperatorio, reducía significativamente las NVPO, náuseas o vómitos por sí solos, y el uso de antieméticos de rescate durante las primeras 24h postoperatorias. Además, no hubo diferencias significativas en la aparición de efectos adversos de midazolam, como sedación y depresión respiratoria. Ahn et al.29 publicaron en 2016 una revisión sistemática y metaanálisis de 16 estudios, en los cuales se administró midazolam iv profiláctico en el pre- o postoperatorio, encontrándose una incidencia significativamente menor de náuseas exclusivas, vómitos exclusivos y NVPO, comparado con placebo. Asimismo, Lee et al.30 publicaron que administrar 2mg iv del fármaco 30min antes de la cirugía resultó igual de efectivo en la prevención de NVPO que 4mg de ondansetrón. El administrar midazolam con dexametasona resultó más efectivo en la profilaxis de NVPO que utilizar cada uno por separado1, demostrando un efecto sinérgico.
PropofolNumerosos estudios han demostrado sus propiedades antieméticas1. Utilizarlo como parte de una anestesia total intravenosa es altamente recomendado para reducir el riesgo basal de NVPO, disminuyendo su incidencia hasta en un 25%1,10. El uso de propofol para la inducción y mantención de la anestesia disminuye significativamente la incidencia de NVPO dentro de las primeras 6h postoperatorias31. Una revisión sistemática demostró que utilizar propofol iv en comparación con usar anestesia inhalatoria también disminuye significativamente el riesgo de NVPO CA32. Este fármaco se puede utilizar como terapia de rescate en caso de NVPO persistentes en la URP, usando pequeñas dosis de entre 10 y 20mg iv, siendo tan efectivo como el ondansetrón33. Sin embargo, tiene el inconveniente de tener un efecto antiemético breve y complicaciones asociadas, como hipotensión arterial, apnea/hipopnea y sedación33.
Otros antieméticosMeclizina administrado en dosis de 50mg vo y asociado a ondansetrón 4mg iv sería más efectivo en la profilaxis de NVPO que utilizar cualquiera de los 2 medicamentos por sí solo1. Actualmente, los antihistamínicos son un fármaco de segunda o tercera línea para la profilaxis y tratamiento de NVPO.
La escopolamina transdérmica es un anticolinérgico que sería útil para prevenir las NVPO como coadyuvante de otras terapias antieméticas34,35, administrada el día previo a la cirugía o 2h previas al inicio de la anestesia.
Dentro de las fenotiazinas, la perfenazina reduciría el riesgo de NVPO en un 5%, con una dosis recomendada de 5mg iv, sin producir sedación ni mareos36. La metoclopramida es considerada un antiemético débil. Una dosis de 10mg iv no es efectiva para reducir significativamente las NVPO1,36.
Los alfa-2 agonistas, como clonidina y dexmedetomidina, mostraron solo en un metaanálisis un significativo efecto contra la aparición de náuseas postoperatorias37, no así contra los vómitos.
La mirtazapina es un antidepresivo noradrenérgico y serotoninérgico, que sería útil como un coadyuvante de otras terapias antieméticas, como 30mg vo asociado a dexametasona 8mg iv38.
La gabapentina en dosis de 600 y 800mg vo, administrada 1h previa a la cirugía, disminuiría eficazmente las NVPO, similar a dexametasona. La combinación de gabapentina y dexametasona es mejor que administrar cada una por sí sola1.
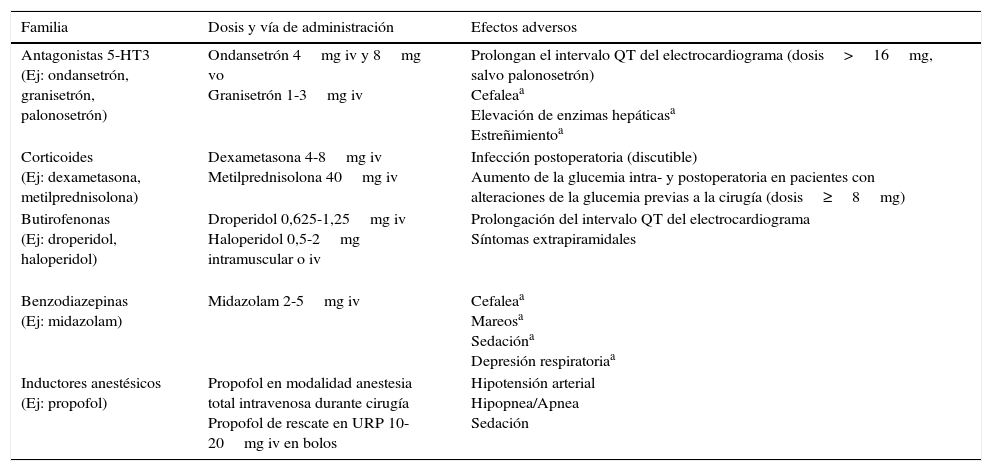
Las dosis y efectos adversos de los fármacos más utilizados como profilaxis y tratamiento de NVPO se resumen en la tabla 7.
Dosis y efectos adversos de los fármacos más utilizados como profilaxis y tratamiento de NVPO
| Familia | Dosis y vía de administración | Efectos adversos |
|---|---|---|
| Antagonistas 5-HT3 (Ej: ondansetrón, granisetrón, palonosetrón) | Ondansetrón 4mg iv y 8mg vo Granisetrón 1-3mg iv | Prolongan el intervalo QT del electrocardiograma (dosis>16mg, salvo palonosetrón) Cefaleaa Elevación de enzimas hepáticasa Estreñimientoa |
| Corticoides (Ej: dexametasona, metilprednisolona) | Dexametasona 4-8mg iv Metilprednisolona 40mg iv | Infección postoperatoria (discutible) Aumento de la glucemia intra- y postoperatoria en pacientes con alteraciones de la glucemia previas a la cirugía (dosis≥8mg) |
| Butirofenonas (Ej: droperidol, haloperidol) | Droperidol 0,625-1,25mg iv Haloperidol 0,5-2mg intramuscular o iv | Prolongación del intervalo QT del electrocardiograma Síntomas extrapiramidales |
| Benzodiazepinas (Ej: midazolam) | Midazolam 2-5mg iv | Cefaleaa Mareosa Sedacióna Depresión respiratoriaa |
| Inductores anestésicos (Ej: propofol) | Propofol en modalidad anestesia total intravenosa durante cirugía Propofol de rescate en URP 10-20mg iv en bolos | Hipotensión arterial Hipopnea/Apnea Sedación |
Si se ha utilizado profilaxis de NVPO durante la cirugía, el tratamiento postoperatorio debe ser con un antiemético de una familia diferente al fármaco inicialmente administrado como profilaxis. Por ejemplo, si usamos dexametasona el tratamiento debe ser con algún antagonista 5-HT3 o butirofenona como primera elección. Por el contrario, si no se administró profilaxis, se recomienda utilizar como tratamiento de primera línea dosis bajas de algún antagonista 5-HT3, como el ondansetrón. Las dosis iv de estos fármacos para el tratamiento de las NVPO deben ser inferiores a las utilizadas como profilaxis: ondansetrón 1mg y granisetrón 0,1mg. Todos los antagonistas 5-HT3, excepto el palonosetrón (que no ha sido estudiado), son igualmente efectivos para el tratamiento de las NVPO39. Tratamientos alternativos incluyen dexametasona 2-4mg iv, droperidol 0,625 iv o propofol en bolos de 20mg iv según sea necesario. Este último puede considerarse una terapia de rescate en pacientes durante su estadía en la URP, siendo tan efectivo como el ondansetrón, pero teniendo un efecto mucho más breve. En 1999, Kovac et al.40 publicaron un estudio que demostró que repetir la administración de ondansetrón en aquellos pacientes que habían recibido previamente profilaxis de NVPO con este fármaco, no tuvo diferencias significativas en comparación con el tratamiento con placebo. Esto último podría explicarse por pacientes que inherentemente son refractarios al tratamiento con antagonistas 5-HT3 o por saturación de los receptores antieméticos. Por lo tanto, como la etiología de las NVPO es multifactorial, la aproximación a la prevención y tratamiento debe incluir diferentes clases de antieméticos, que actúen sobre los diferentes receptores de náuseas y/o vómitos conocidos1.
ConclusionesLas NVPO son un problema frecuente en los pacientes quirúrgicos. Cuando esta complicación no es prevenida o tratada adecuadamente, puede provocar mayor morbilidad, estadía prolongada en la URP, hospitalización no planificada y aumento significativo de los costos de la hospitalización3. Las NVPO son la principal causa de hospitalización no programada en cirugía ambulatoria4. El objetivo del equipo quirúrgico debe ser la profilaxis de las NVPO más que su tratamiento, con el fin de disminuir significativamente su incidencia y complicaciones asociadas, la angustia de los pacientes y los costos de la atención de salud1.
Los principales factores de riesgo para NVPO son: sexo femenino, historia de NVPO en cirugías previas o cinetosis, no fumar, uso de opioides en el postoperatorio, someterse a ciertos tipos de cirugía, utilizar anestésicos volátiles y/u óxido nitroso y duración de la cirugía. El riesgo de NVPO de un paciente quirúrgico debe objetivarse usando una escala de riesgo validada por la literatura científica, para elegir de la mejor forma la profilaxis a utilizar. Sugerimos usar las escalas de riesgo de Apfel o Koivuranta para decidir el tipo y número de antieméticos profilácticos a administrar según el puntaje obtenido en cada escala. Los principales fármacos antieméticos usados en el período perioperatorio son dexametasona, ondansetrón y droperidol. Otros fármacos antieméticos, como el midazolam, también han demostrado ser efectivos en la profilaxis de NVPO, pero actualmente se administran como coadyuvantes de la terapia antiemética, y requieren mayor evidencia y/o experiencia clínica para reemplazar a los fármacos actualmente utilizados.
Existen estrategias generales que se pueden utilizar para reducir el riesgo basal de NVPO, como evitar la anestesia general, privilegiando la anestesia regional, utilizar propofol para la inducción y mantención de la anestesia, evitar el uso de óxido nitroso y/o anestésicos inhalatorios, minimizar el uso postoperatorio de opioides y recibir una hidratación iv abundante durante la cirugía.
Finalmente, recomendamos considerar el uso de antieméticos para el tratamiento o «rescate» de pacientes con NVPO durante su postoperatorio inmediato. Los fármacos más utilizados son ondansetrón, droperidol y propofol en bolos. Cabe destacar que el propofol solo se administra durante la estadía en la URP y bajo la estricta vigilancia de un especialista, dados sus complejos efectos secundarios.
La etiología de las NVPO es multifactorial, por lo que la prevención y tratamiento deben incluir diferentes clases de antieméticos, que actúen sobre los diferentes receptores de náuseas y/o vómitos hasta el momento conocidos, junto con las estrategias generales antes mencionadas.
Conflicto de interesesLos autores no refieren conflictos de intereses.