Evaluar la relación entre el número de folículos antrales en condiciones basales y la cantidad de ovocitos recuperados luego del tratamiento de estimulación ovárica, y establecer el rol del recuento de folículos antrales mediante ecografía como predictor de la respuesta ovárica. Como propósito secundario, se examinó la correlación del recuento de folículos antrales con la edad de las pacientes y el éxito del tratamiento.
Materiales y métodosEntre enero y marzo de 2015 se estudió retrospectivamente a 40 candidatas a punción aspiración folicular, que se habían realizado una ecografía transvaginal con recuento de folículos antrales antes de la estimulación. Se tomaron en cuenta solo los folículos que medían entre 3 y 8mm. Todas las pacientes recibieron estimulación hormonal y monitoreo ecográfico y hormonal en sangre hasta la punción aspiración de folículos.
ResultadosSe observó una importante correlación inversa entre la edad de las pacientes y el recuento de los folículos antrales y una correlación inversa muy marcada entre la edad y la recuperación de ovocitos. También se constató una muy importante correlación positiva entre el recuento de folículos antrales y la cantidad de ovocitos recuperados en la aspiración transvaginal. El número reducido de pacientes limitó el análisis del éxito del tratamiento.
ConclusiónEl recuento de folículos antrales permite predecir la respuesta ovárica y la cantidad de ovocitos recuperados mediante punción folicular. Debido a su bajo costo, alto rendimiento diagnóstico y fácil acceso y realización, el recuento ovárico folicular mediante ecografía debería ser considerado la prueba de reserva ovárica de primera elección
To evaluate the relationship between the number of antral follicles under basal conditions and the number of oocytes retrieved after ovarian stimulation treatment, to establish the role of antral count follicles by ultrasonography as a predictor of ovarian response. Secondary objective: to assess the correlation of antral follicle count with the age of patients and the success of treatment.
Materials and methodsThis is a retrospective cohort study, between January and March 2015, assessing 40 women undergoing transvaginal ultrasonography guided follicular aspiration. Transvaginal ultrasonography follicle count was performed prior to antral follicles stimulation, (follicles measuring between 3 and 8mm were taken into account), they also received hormonal stimulation, ultrasonography and hormonal monitoring blood until the follicle aspiration.
ResultsA strong inverse correlation between patient age and antral follicle count and a very strong inverse correlation between age and oocyte retrieval was observed. A very strong positive correlation between the antral follicle count and the number of oocytes retrieved in the transvaginal aspiration was also observed. The small number of patients limited the analysis linked to the success of treatment.
ConclusionThe antral follicle count had significant associations with ovarian response and the number of oocytes retrieved. The antral follicles count by ultrasonography should be considered the first choice of test of ovarian reserve because of its low cost, good performance and accessibility.
El éxito de la fertilización in vitro (FIV) y la transferencia embrionaria depende, entre otros factores, del número de ovocitos recuperados luego de la estimulación ovárica mediante distintas drogas (gonadotrofinas exógenas, hormona liberadora de gonadotrofinas, citrato de clomifeno, etc.)1. A su vez, la cantidad de ovocitos recuperados luego de la estimulación ovárica está relacionada con el número de ovocitos disponibles para ovularse en el ovario y con la edad cronológica de la paciente2,3.
La mujer nace con un número finito de óvulos. Estos se utilizan a lo largo de la vida reproductiva y van reduciéndose en cantidad y calidad conforme la edad de la mujer avanza. La posibilidad de identificar el número de folículos disponibles y de medir la función ovárica permitiría valorar el potencial reproductivo de la paciente.
Al respecto, la verdadera reserva ovárica está representada por el número de folículos primordiales o en reposo presentes en ambos ovarios. Estos solo podrían ser examinados histológicamente debido a su pequeño tamaño4.
Los folículos primordiales son los que inician la foliculogénesis en el ovario, evolucionando a folículos primarios, secundarios o preantrales, no identificables por ecografía. Una proporción de folículos progresa a folículos antrales, es sensible a la hormona foliculoestimulante (FSH) e identificable por ecografía, y progresivamente alcanza el estadio preovulatorio. Ese capital folicular puede cuantificarse a través de la determinación de gonadotrofinas (FSH, estradiol basal, hormona luteinizante), especialmente por la hormona antimulleriana (AMH), junto con la definición del número de folículos con antro en desarrollo en el ovario por ecografía.
La AMH es producida en el ovario adulto por las células de la granulosa de los folículos pequeños (primordiales, primarios y secundarios) hasta el estadio preantral. Posee un efecto inhibitorio y protector en la foliculogénesis, pero sobre todo refleja en forma fidedigna la masa folicular latente. Es considerada el marcador por excelencia del capital folicular.
Varios autores coinciden en que el recuento de folículos antrales (RFA) por ecografía transvaginal, antes de la estimulación ovárica, es el mejor predictor de la respuesta a los ciclos de reproducción asistida3–9. Así, el RFA en el inicio del ciclo ovárico puede informar sobre la reserva, pero también sobre el tipo de respuesta frente a la estimulación ovárica. Se considera una reserva ovárica adecuada cuando el recuento de folículos con antro (entre 3-8mm), identificados en cada ovario, es mayor o igual a 5.
El riesgo de hiperrespuesta se asocia a más de 10 folículos antrales en cada ovario, mientras que una baja respuesta se basa en un conteo de folículos con antro menor de 10 en total (baja reserva ovárica). Otro parámetro ecográfico es la medición de volumen ovárico, aun con controversias sobre su utilidad. Se la incluye en la evaluación inicial de la paciente, considerándose que un volumen ovárico menor de 3 cm3 tiene alta probabilidad de falla en la respuesta al tratamiento4.
La identificación de las mujeres con mayor riesgo de baja respuesta ovárica antes del tratamiento es útil para elegir una conducta terapéutica adecuada, ajustar la dosis de la medicación y, así, optimizar la respuesta ovárica. Una vez iniciado el tratamiento se realiza un monitoreo ecográfico para valorar el grado de respuesta del ovario ante la estimulación gonadotrófica. Este seguimiento se complementa funcionalmente durante el estímulo con valores de estradiol sérico, permitiendo identificar el tipo de respuesta (baja o alta) y el riesgo asociado de complicaciones clínicas1,5.
El objetivo de este trabajo fue evaluar la relación entre el número de folículos antrales en condiciones basales y la cantidad de ovocitos recuperados luego del tratamiento, y poder establecer el rol del RFA como predictor de la respuesta ovárica. Asimismo, se buscó establecer si existe una correlación entre el RFA y la edad de las pacientes y el éxito del tratamiento.
Materiales y métodosConsideraciones éticasTodos los procedimientos del estudio formaron parte de la práctica habitual, así como todos los datos del estudio fueron tratados con máxima confidencialidad y de manera anónima, con acceso restringido solo al personal autorizado a los fines del estudio de acuerdo con la normativa vigente en la Ley Nacional de Protección de Datos Personales 25.326/00 y la Ley 26. 529/09. El manuscrito final fue revisado y aprobado por el Comité de Bioética de la institución.
Población de estudio y equipamientoEn este estudio de corte transversal y período retrospectivo, hecho en nuestra institución, se revisó a las pacientes candidatas a punción aspiración folicular, que se habían realizado una ecografía transvaginal para el recuento basal de folículos antrales, antes de la estimulación, durante un período comprendido entre enero y marzo de 2015. La edad y el motivo de la estimulación ovárica fueron registrados de manera tabular.
Protocolo de estudioLas ecografías transvaginales de las pacientes incluidas en este estudio fueron realizadas por cuatro médicos especialistas en Diagnóstico por imágenes entrenados en ecografías ginecológicas con equipos Toshiba Xario 200 utilizando un transductor TV de 7MHz. Los folículos antrales fueron medidos durante la fase folicular temprana (es decir, entre el día 2 y 4 del ciclo menstrual) para evitar falsos positivos, como quistes ováricos coexistentes o el cuerpo lúteo.
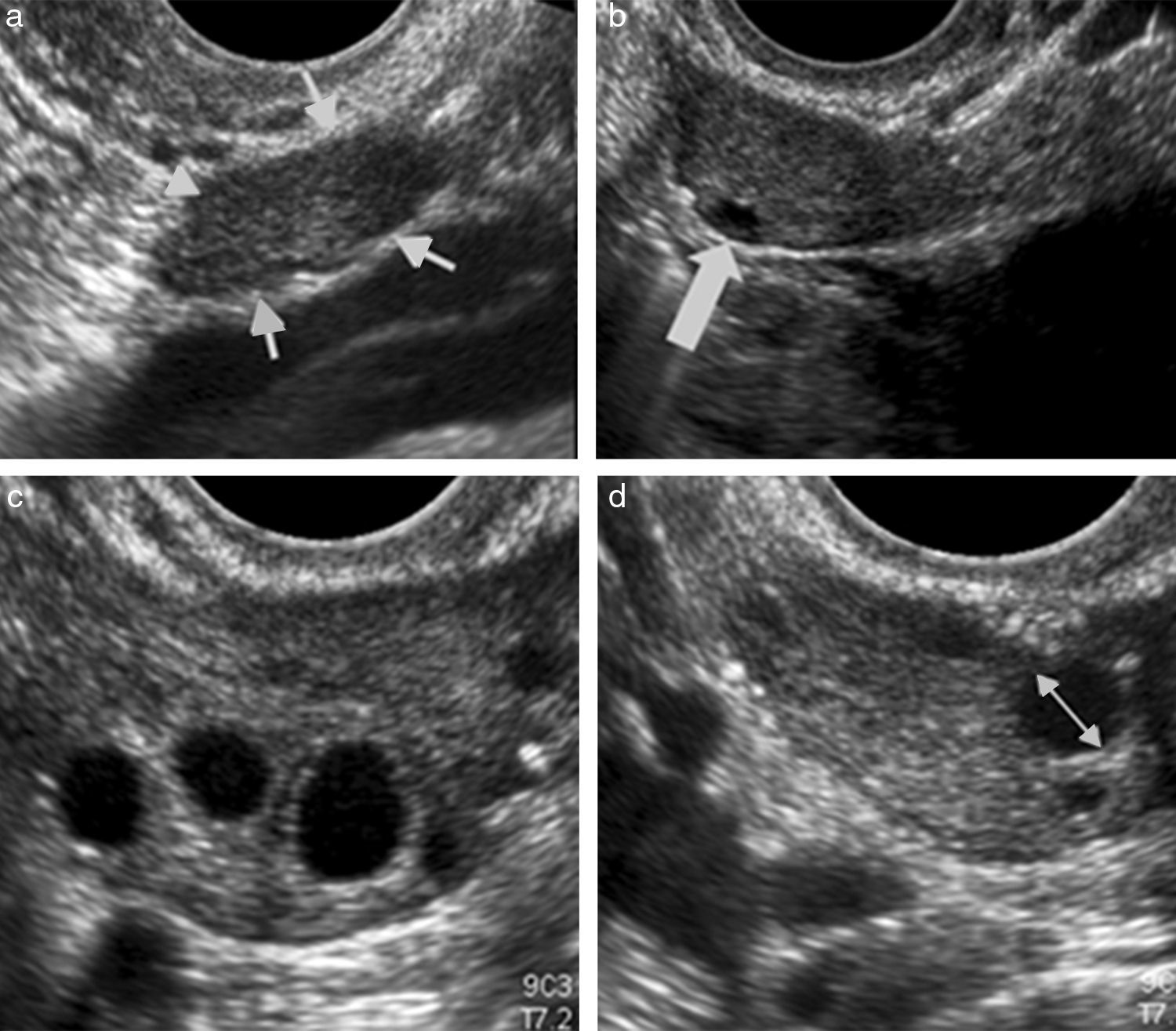
Se tomaron en cuenta solo los folículos que medían entre 3 y 8mm. El tamaño fue calculado usando el diámetro interno del área anecogénica (fig. 1), mientras que para el recuento se utilizó la sistematización recomendada por Broekmans et al.4:
- 1.
Identificar el ovario.
- 2.
Explorar en dos planos.
- 3.
Examinar detenidamente todo el ovario en sentido anteroposterior y sagital-parasagital, con el fin de contar todos los folículos antrales visibles.
Ecografías transvaginales para recuento de folículos antrales: (a) ovario (flechas) sin ningún folículo antral; (b) ovario con un solo folículo antral (flecha); (c) imágenes anecogénicas redondeadas que representan folículos antrales; y (d) medición el diámetro interno del folículo (flecha).
El número de folículos fue registrado de manera cuantitativa de forma tabular, a la vez que las pacientes fueron divididas en cuatro grupos según su recuento de folículos antrales (FA), de modo similar al reportado por Huang et al.10: grupo A, menos de 5 FA; grupo B, entre 6 y 10 FA; grupo C, entre 11 y 15 FA; y grupo D, más de 16 FA.
Control y seguimientoLuego del recuento basal de FA, se estimuló a las pacientes con el esquema de antagonistas móvil. Estas recibieron en fase folicular temprana, desde su segundo día del ciclo, la hormona folículo estimulante recombinante (FSHr; Puregon, Laboratorio Organon) en dosis ajustadas de acuerdo a cada una.
Se realizó un seguimiento ecográfico y la determinación del estradiol correspondiente durante el estímulo, con folículos mayores de 14mm (diámetro promedio) por ecografía y una correlación complementaria con niveles de estradiol plasmático, se iniciaron antagonistas de hormona liberadora de gonadotropina (GnRH; cetrorrelix 0,25mg/ml, Orgalutran, Organon) en forma diaria, junto con 75 UI/día de gonadotrofina menopáusica humana (HMG; Menopur, Ferring).
Con folículos mayores de 17mm de diámetro promedio, medidos por ecografía, se programó la descarga ovulatoria con gonadotropina coriónica humana (hCG: de 5.000 a 10.000 UI) o con agonistas de GnRH (triptorrelina acetato, Ferring), con el fin de lograr los cambios ovulatorios necesarios.
La punción aspiración folicular se planificó entre 34 y 36h después de la descarga. Se analizó la cantidad de ovocitos recuperados en cada paciente, lo cual se registró tabularmente. Se consignó la presencia de embarazo luego de la transferencia.
Análisis estadísticoLas variables categóricas fueron reportadas mediante proporciones con intervalos de confianza (IC), mientras que las continuas se describieron como media y desvío estándar o mediana y rango intercuartil, dependiendo de su distribución.
Para la correlación entre las variables cuantitativas se utilizó la prueba Spearman para aquellas de distribución no normal y la de Pearson para las de distribución normal. Los coeficientes de correlación se reportaron con sus IC de 95%.
Para la comparación múltiple entre grupos se utilizó el examen Kruskal-Wallis, dada la distribución no normal observada en grupos pequeños. La diferencia entre variables continuas entre dos grupos se realizó con la prueba Mann-Whitney o la T de Student para muestras independientes, según su distribución.
Todos los exámenes fueron realizados con el programa Medcalc 12.7, considerándose como resultado estadísticamente significativo aquel con una p inferior a 0,05.
ResultadosDurante el período estudiado, 40 pacientes se realizaron el recuento de folículos antrales para la aspiración folicular. Algunas de ellas eran candidatas a FIV (n=26) y otras (n=14) a ovodonación (como donantes de ovocitos) o preservación ovárica. La mediana de edad fue de 38 años (rango intercuantil entre 31 y 41 años).
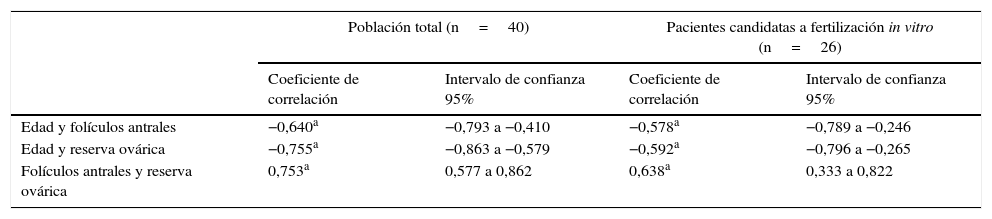
En la población total (n=40) se observó una importante correlación inversa entre la edad de las pacientes y el conteo de los folículos antrales, a la vez que se constató una correlación inversa muy pronunciada entre la edad y la recuperación de ovocitos. También se registró la existencia de una muy importante correlación positiva entre la cantidad de folículos antrales y de ovocitos recuperados de la aspiración transvaginal (tabla 1).
Correlación entre la cantidad de folículos antrales y ovocitos recuperados
| Población total (n=40) | Pacientes candidatas a fertilización in vitro (n=26) | |||
|---|---|---|---|---|
| Coeficiente de correlación | Intervalo de confianza 95% | Coeficiente de correlación | Intervalo de confianza 95% | |
| Edad y folículos antrales | −0,640a | −0,793 a −0,410 | −0,578a | −0,789 a −0,246 |
| Edad y reserva ovárica | −0,755a | −0,863 a −0,579 | −0,592a | −0,796 a −0,265 |
| Folículos antrales y reserva ovárica | 0,753a | 0,577 a 0,862 | 0,638a | 0,333 a 0,822 |
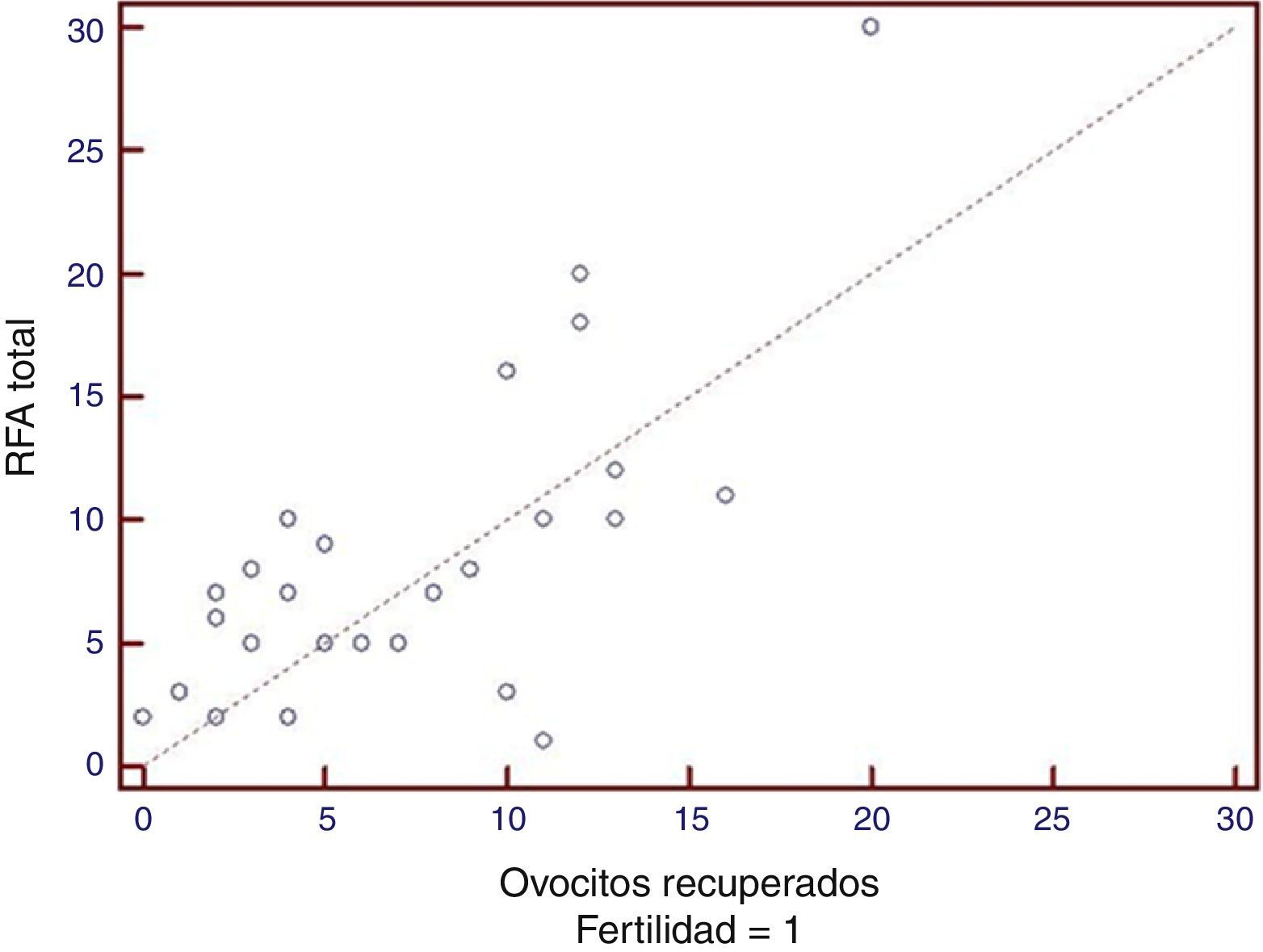
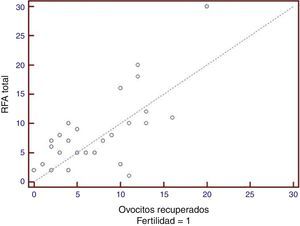
Si de esta población total se analizara el subgrupo de pacientes con trastornos de la fertilidad que realizaron transferencia embrionaria (n=26), persistirían estas asociaciones, aunque con menor fuerza (tabla 1; fig. 2).
De acuerdo con la comparación entre los diferentes grupos (A, B, C y D), se evidenció que las edades de las pacientes del grupo A y B eran significativamente diferentes a las del D (p<0,05). Luego, se juntó al grupo A con el B y al C con el D, observándose una diferencia significativa (p<0,05) entre las edades de ambas muestras. La mediana del grupo A-B fue de 40 años y la del C-D de 33 años.
Cuando el cotejo fue aplicado solo a la serie de pacientes con trastornos de fertilidad (n=26), es decir, a aquellas con embriotransferencia, la diferencia de edad no fue significativa entre los grupos (p=0,145), aunque sí hubo una tendencia en el agrupamiento. Las pacientes del C y D formaban un grupo más joven que las del A y B (p=0,081). Si la muestra hubiese sido mayor, probablemente se habría podido confirmar esta tendencia.
Además, se observó una diferencia significativa entre la cantidad de ovocitos recuperados por aspiración en el grupo A y B en comparación con el C y D (p<0,05), así como también fue significativa esta diferencia en la población con trastornos de la fertilidad (p<0,05). Luego se analizaron los datos reuniendo a aquellas pacientes que se realizaron transferencia embrionaria del grupo A-B y las del C-D, para evaluar el éxito de la FIV.
La tasa de embarazo en las pacientes del grupo A-B fue de un 20% y del C-D de un 50%; sin embargo, estos resultados fueron no significativos (p=0,29). En nuestra muestra tampoco hubo asociación entre la cantidad de embriones transferidos y el éxito terapéutico (p=1), ni diferencia de edad entre las pacientes que se embarazaron y las que no (p=0,97). Además, tampoco se registraron diferencias en el conteo total de folículos antrales entre pacientes con éxito terapéutico y sin éxito (p=1), ni de ovocitos recuperados entre embarazos y no embarazos (p=0,67).
DiscusiónEn este estudio, en el que se midieron los folículos antrales de 3 a 8mm de diámetro mediante ecografía transvaginal durante la fase folicular temprana, se observó una significativa correlación entre el número de folículos antrales y los ovocitos recuperados luego del tratamiento (registrando más en los grupos C y D). En coincidencia con otros autores, podemos afirmar que a mayor conteo folicular, mayor recuperación de ovocitos9–11.
También se observó una correlación con la edad de las pacientes, siendo más jóvenes las pertenecientes a los grupos C y D con una mediana de edad de 33 años. En ellas se recuperaron mayor cantidad de ovocitos. Así, se puede concluir que a mayor edad, menor es el recuento de folículos antrales y menor la cantidad de ovocitos recuperados. Esto coincide con lo dicho anteriormente y con la literatura, esto es, que la reserva ovárica cuantitativa se encuentra en relación con la edad cronológica de la mujer2,3.
En aquellas pacientes con trastornos de la fertilidad, esta correlación de la edad con el conteo folicular decae (posiblemente por factores no evaluados o desconocidos). Esto coincide con lo expuesto por Scheffer et al.3, que afirman que la edad cronológica puede predecirse según el número de folículos antrales en mujeres sin desórdenes, pero que esto no es posible en aquellas con trastornos de la fertilidad.
Es importante realizar una predicción de la reserva ovárica y un adecuado monitoreo de la ovulación para evitar el uso innecesario de drogas que puedan llegar a ocasionar una hiperestimulación ovárica. Es posible que esto suceda porque que en un ciclo menstrual espontáneo usualmente solo se selecciona un folículo antral, que llega a ser dominante, mientras que durante los tratamientos de estimulación ovárica los folículos antrales que progresan son múltiples, conformando folículos dominantes (mayores de 20mm de diámetro)4,5. Por este motivo, si el protocolo de inducción no es modificado en cada paciente, se pueden producir múltiples quistes ováricos y generar complicaciones, conformando un síndrome de hiperestimulación.
Diversos estudios ya han concluido que el RFA es un buen predictor de la reserva ovárica. En coincidencia con la mayoría de ellos, creemos que un recuento bajo de folículos antrales es predictor de una mala respuesta y que un recuento alto anticipa una adecuada respuesta a la estimulación ovárica3,5,10,12.
Si bien algunos reportes indican que con un RFA ≥ 10 se observan mayor cantidad de embarazos y nacimientos en comparación a un RFA ≤ 10, en nuestro estudio esto no fue significativamente diferente7,9,10,12–14. Es probable que nuestro resultado entre las pacientes con trastornos de fertilidad no haya sido significativo por el número reducido de la muestra, o bien porque existen otras variables, más allá de la cantidad de folículos antrales, que influyen en el éxito de la FIV, como las condiciones uterinas u hormonales o el factor masculino.
Existen diversas limitaciones en nuestro trabajo. La primera y principal es la pequeña cantidad de pacientes que imposibilitó detectar diferencias significativas en el éxito de los tratamientos en mujeres infértiles, ni permitió obtener intervalos de confianza de 95% más angostos. La segunda es el trabajo con una base de datos secundaria, ya que esta predispone a un posible sesgo de información, con pérdida de cierta información e imposibilidad de registrar otra, como el dosaje de la hormona antimulleriana que no fue registrado en la historia clínica electrónica.
ConclusiónEl recuento de folículos antrales permite predecir la respuesta ovárica y la cantidad de ovocitos que se recuperarán, siendo útil para elegir el tratamiento adecuado para la paciente. Debido a su bajo costo, alto rendimiento diagnóstico y fácil acceso y realización, el recuento ovárico folicular mediante ecografía debe ser considerado el examen de reserva ovárica de primera elección.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
ComentarioAl momento de la realización del estudio la Dra. Lonegro se encontraba cursando la residencia en el Servicio de Diagnóstico por Imágenes del Hospital Italiano de Buenos Aires.