Introducción
Se conoce como reacción adversa a medicamentos a todo efecto indeseable, nocivo y no intencionado que difiere de los efectos terapéuticos esperados y que ocurre durante el uso clínico de un medicamento o combinación de medicamentos, en las dosis y vías recomendadas y con propósito diagnóstico, terapéutico o profiláctico.1-4 Las RAM se pueden manifestar como un efecto conocido o presentarse por primera vez. En este tópico se excluyen las sobredosis absolutas o relativas, intentos de suicidios, etc.4
Las RAM se han clasificado de acuerdo a características químicas, farmacológicas y clínicas. Las reacciones tipo A son predecibles y representan 80% de las RAM, tienen una relación dosisrespuesta, pueden evitarse con la suspensión o reducción de la dosis y rara vez ponen en peligro la vida. Las reacciones tipo B son impredecibles y son de mayor riesgo para la vida. Este tipo de reacciones son independientes de la dosis y se relacionan a la respuesta individual del huésped. En este grupo se encuentran las reacciones por intolerancia, idiosincráticas, alérgicas y pseudoalérgicas. Las reacciones de tipo C, también llamadas químicas, se relacionan a la estructura química de la droga o sus metabolitos. Las reacciones tipo D se definen como reacciones tardías por presentarse a largo plazo y se detectan durante el desarrollo de nuevos medicamentos. Finalmente las reacciones de tipo E, se describen como aquellas que se desarrollan tiempo después de finalizado el tratamiento.5-7 Hace pocos años se ha propuesto otra clasificación de RAM, basada en criterios de dosis-respuesta, tiempo de evolución y susceptibilidad, pero resulta compleja en su aplicación clínica.8
Otra forma de clasificar a las RAM se basa en el mecanismo de daño inmunológico involucrado en las reacciones de hipersensibilidad, de acuerdo a Gell y Coombs. Las reacciones de tipo I son mediadas por IgE y ocurren tras la administración de fármacos o biológicos, y los desencadenantes más frecuentes son los antibióticos. Se presentan inmediatamente tras la administración de un medicamento y pueden ocasionar anafilaxia y la muerte. Las reacciones de tipo II son citotóxicas, relacionadas a cuadros clínicos graves y potencialmente fatales. Las reacciones tipo II están mediadas por anticuerpos IgG e IgM citotóxicos, que se forman en respuesta a la exposición de las membranas celulares con fármacos. Las reacciones de tipo III se presentan por la formación de complejos inmunes, las características principales son fiebre, exantema, urticaria, linfadenopatía y artralgias una a tres semanas posteriores a la administración del fármaco. Las reacciones de tipo IV, mediadas por linfocitos T, se desarrollan por el uso tópico o sistémico de medicamentos.9 Hay otras cuatro subcategorías de reacciones de tipo IV, según el tipo de células predominantes involucradas.10
Debido a que la mayoría de fármacos se administran por la vía oral, frecuentemente ocasionan síntomas gastrointestinales como pérdida del apetito, náuseas, distensión abdominal, estreñimiento y diarrea. Las manifestaciones clínicas más frecuentes pueden ser sistémicas o localizadas a un órgano como la piel, médula ósea, corazón, riñón, pulmón, hígado, entre otros.11
De acuerdo con el Programa Internacional de Vigilancia de Medicamentos de la Organización Mundial de la Salud (OMS) iniciado en 1960, se ha estimado una prevalencia de RAM en la población que varía de 0.7% a 35%.12 Las RAM son causa de hospitalización de hasta 8% de los pacientes.13 Estudios en otros países han descrito que las RAM se presentan en 15% de los pacientes hospitalizados.14,15 Los antibióticos, antineoplásicos y antiinflamatorios son los medicamentos con mayor frecuencia asociados a RAM.16,17
Objetivo
Determinar, mediante una encuesta, la prevalencia de RAM en pacientes internados en un hospital de tercer nivel de atención, así como algunas características clínicas de este tipo de reacciones.
Métodos
Se desarrolló un estudio descriptivo, transversal, mediante la aplicación de una historia clínica alergológica a pacientes hospitalizados en el Hospital de Especialidades Dr. Antonio Fraga Mouret del Centro Médico Nacional La Raza del Instituto Mexicano del Seguro Social, en la ciudad de México, el mes de julio de 2004. El hospital cuenta con 500 camas distribuidas entre 18 departamentos clínicos. Se incluyeron todos los pacientes hospitalizados cuyas condiciones de salud permitieran hacerles una historia clínica, enfocada en antecedentes atópicos y de RAM, con una descripción de las manifestaciones clínicas presentadas. Además se registraron las variables demográficas de cada paciente. No se incluyó a los pacientes que por la gravedad de su estado clínico, fueran incapaces de participar en el estudio. El protocolo fue aprobado por el Comité local de Ética e Investigación y cada paciente aceptó su participación mediante el consentimiento bajo información.
Resultados
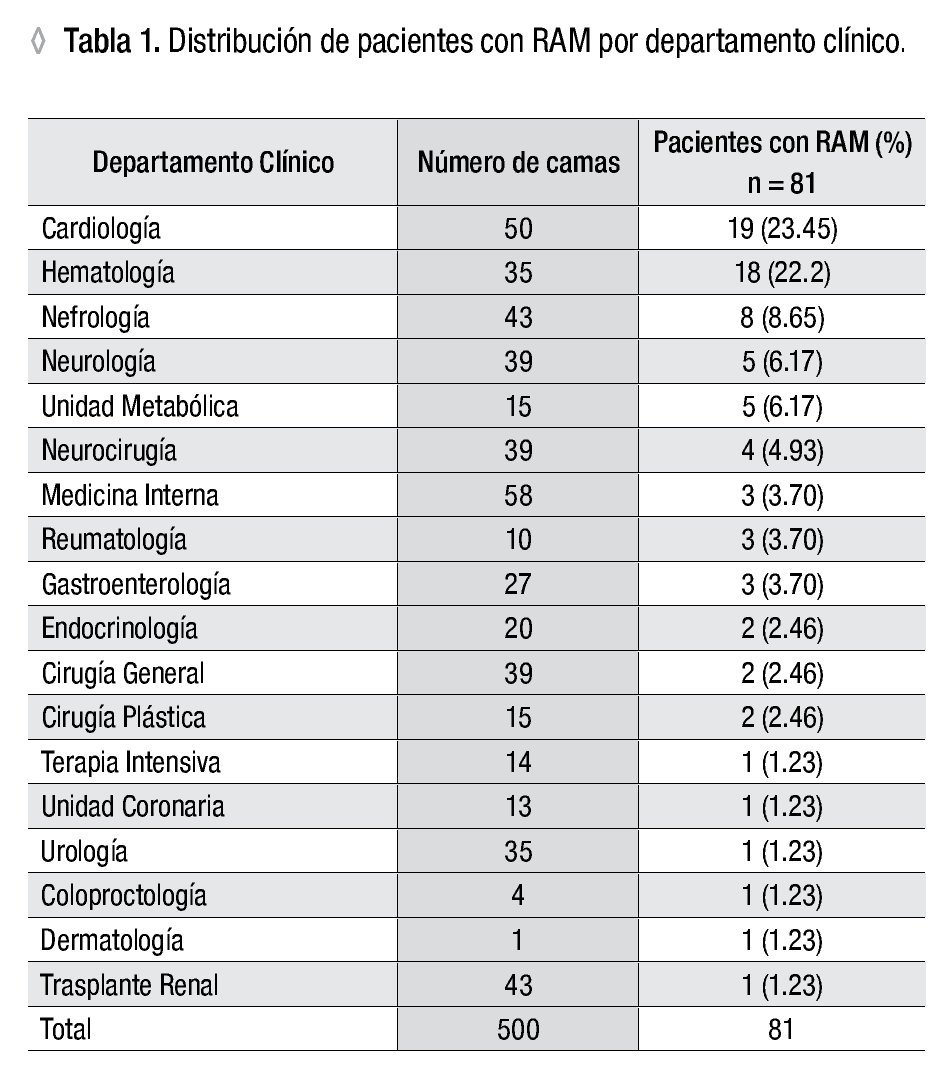
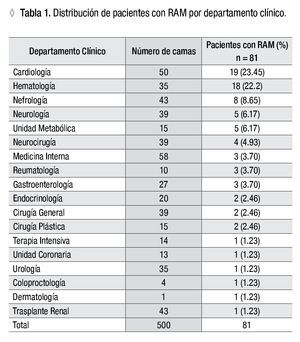
En el momento de la encuesta había 377 pacientes hospitalizados en los diferentes Departamentos, de los cuales se incluyeron 328 (87%). El promedio de medicamentos por cada paciente encuestado fue de 2.4. Casi una cuarta parte de los pacientes refirió antecedentes de una o más reacciones adversas a medicamentos. En este grupo con RAM, con una edad promedio de 48.2 años (21 a 89), hubo 50 mujeres y 31 hombres. Casi 80% de los pacientes con RAM tenía antecedentes familiares atópicos. Cuarenta y dos pacientes (51.83%) refirieron RAM a un medicamento y los 39 restantes tuvieron reacciones a dos medicamentos o más. En el Departamento de Cardiología encontramos el mayor número pacientes con RAM, 19 (23.45%); en Hematología encontramos casi el mismo número, 18 (22.2%). En los pacientes de Nefrología, Neurología y Unidad Metabólica se encontró un menor número de casos de RAM. Entre los dos primeros Departamentos suman casi la mitad de pacientes con RAM (Tabla 1).
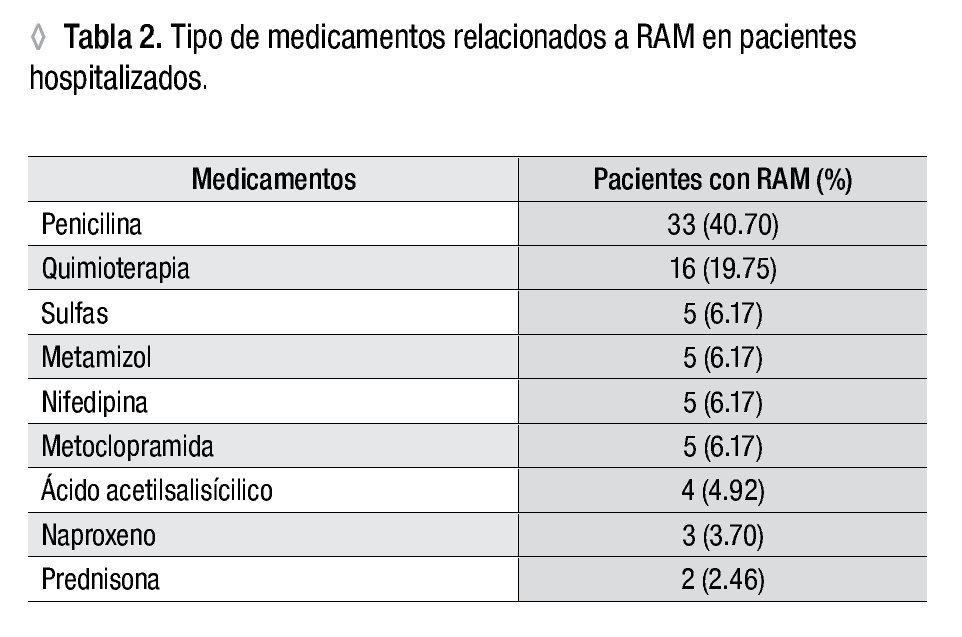
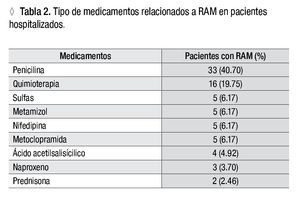
La penicilina fue responsable de 40% de las RAM. Los medicamentos utilizados para quimioterapia se asociaron a cerca de 20% de las reacciones adversas. Las sulfas y los AINE se relacionaron a un número menor de RAM (Tabla 2). Entre los pacientes con reacciones adversas a la penicilina, 66% tenían antecedentes familiares atópicos.
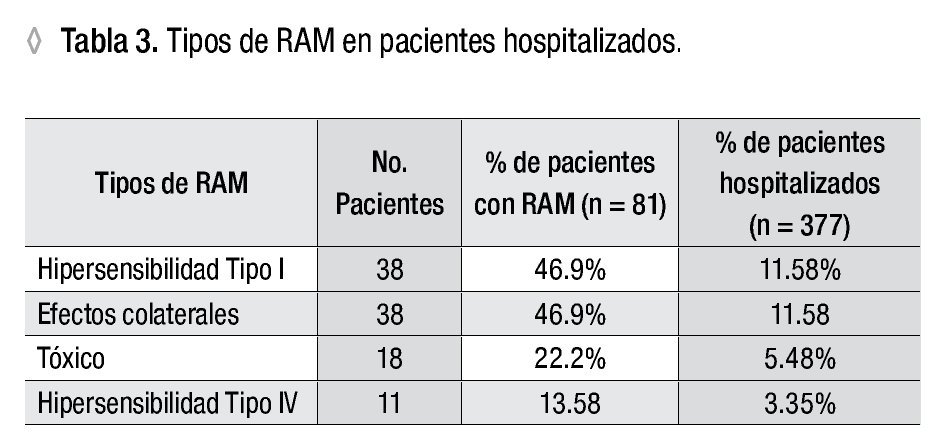
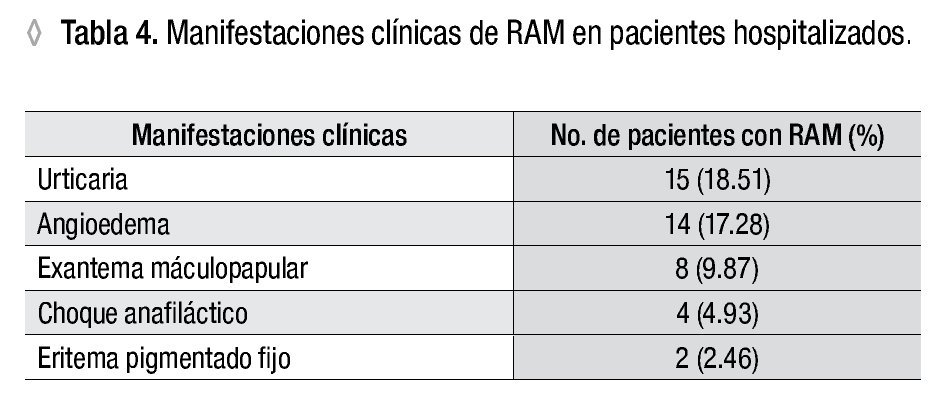
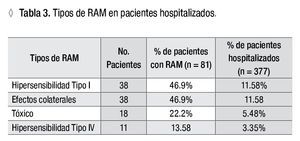
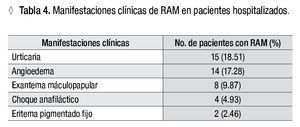
De acuerdo con las manifestaciones clínicas referidas, observamos que las reacciones de hipersensibilidad de tipo I y los efectos colaterales fueron las RAM más frecuentes, 46.9% cada una, y se presentaron en casi 12% del total de pacientes hospitalizados (Tablas 3 y 4). Las manifestaciones clínicas más frecuentes asociadas a las RAM fueron urticaria y angioedema y en 5% de los casos, choque anafiláctico. No se refirieron RAM con afectación pulmonar, gastrointestinal, renal, de médula ósea ni del sistema nervioso.
Encontramos que 24% de los casos con antecedente de hipersensibilidad a medicamentos no estaban registrados en el expediente clínico.
Discusión
Las reacciones adversas a fármacos son frecuentes en el ambiente hospitalario y ambulatorio.16 Las RAM predecibles son las más frecuentes. Las reacciones a fármacos mediadas por mecanismos de hipersensibilidad, representan casi 10% de las RAM. Diferentes estudios han reportado RAM hasta en 15% de los pacientes hospitalizados.15,16 En nuestra encuesta encontramos una prevalencia de RAM en pacientes hospitalizados de 24.69%, lo que podría atribuirse a haber incluido los antecedentes de reacciones previas a su internamiento.
Se ha descrito que las mujeres hospitalizadas presentan más RAM que los hombres, tal como observamos en nuestro estudio, con una relación mujeres/hombres de 5/3.18,19 La razón del predominio de RAM en mujeres no es clara todavía y es probable que la actividad hormonal relacionada al ciclo menstrual, embarazo y menopausia afecte el metabolismo y la respuesta a medicamentos en mujeres.20
Los antecedentes atópicos como factores de riesgo para presentar RAM son un punto de discusión, pero en pacientes con hipersensibilidad a AINE está demostrada esta asociación.21 En el aspecto étnico se ha observado mayor susceptibilidad de RAM con anti-retrovirales en caucásicos y con la enzima convertidora de angiotensina en afroamericanos.22,23 Nosotros encontramos que 80% de los casos con RAM tenían antecedentes familiares atópicos, en particular en pacientes con hipersensibilidad a β-lactámicos.
Al igual que en otros estudios, nosotros observamos que los antibióticos β-lactámicos y los fármacos quimioterápicos son los más frecuentemente involucrados en las reacciones adversas a fármacos.24,25 En los pacientes con hipersensibilidad a penicilinas y sulfas, observamos una asociación elevada con antecedentes familiares de atopia.
Las lesiones cutáneas son la manifestación clínica más frecuente en reacciones por hipersensibilidad a medicamentos, ocurren hasta en 95% de los casos.19 En nuestra muestra de pacientes las manifestaciones más frecuentes fueron urticaria, angioedema, exantema maculopapular y eritema pigmentado fijo y ocurrieron en la mitad de los casos de RAM.
Los departamentos clínicos donde encontramos más casos de RAM fueron Cardiología, Hematología y Nefrología, tal vez por el mayor número de camas asignadas y por la polifarmacia y tipo de medicamentos utilizados. Las RAM asociadas a la quimioterapia utilizada en Hematología se han documentado como las causas más frecuentes en otros estudios.17
El uso más frecuente de la terapia biológica con anticuerpos monoclonales, contra receptores TNF-α y factor 2 de crecimiento epidérmico humano entre otros, se ha relacionado a reacciones adversas. Lo mismo ocurre con los medicamentos usados en quimioterapia contra diversos tipos de cáncer, los cuales después de varios cursos pueden causar hipersensibilidad hasta en uno de cada cuatro pacientes.26-28
No obstante que el estándar de oro diagnóstico en hipersensibilidad a medicamentos es la prueba de reto, su uso está restringido en pacientes con reacciones graves, en estos casos las pruebas cutáneas y algunas pruebas in vitro de hipersensibilidad inmediata y tardía son auxiliares diagnósticos confiables.29
Los análisis de RAM hospitalarias en periodos de varios años permiten ver las tendencias e identificar los efectos de los medicamentos como responsables de daño orgánico.17 Nuestro estudio transversal, tiene la limitante de no explorar los efectos farmacológicos de manera prospectiva. Algunas debilidades de nuestro trabajo son la muestra pequeña de pacientes adultos incluidos y, al tratarse de una encuesta, no haber confirmado mediante pruebas diagnósticas los casos probables de hipersensibilidad a medicamentos.
Es importante contar con programas efectivos de farmacovigilancia, que registren todos o la mayoría de los casos de RAM, principalmente aquellos graves y de hipersensibilidad, por su utilidad en la identificación de factores de riesgo y la prevención de futuros eventos a corto y largo plazo. En este aspecto es preocupante el elevado sub-reporte de RAM, cercano a 90% en estudios británicos.30 En nuestro trabajo 24% de los pacientes con RAM por hipersensibilidad no se informaron al Comité local de Farmacovigilancia ni fueron registrados en el expediente clínico, lo cual es un riesgo para desarrollar reacciones anafilácticas. En nuestro Departamento de Alergia otorgamos anualmente cerca de 450 interconsultas a pacientes hospitalizados, de las cuales una cuarta parte corresponden a RAM y casi todas no son notificadas al Comité local de Farmacovigilancia por los departamentos donde suceden.
En México existe un programa permanente de farmacovigilancia y los médicos de instituciones públicas o privadas deben notificar en formatos específicos las RAM que ocurren, pero el reporte de RAM es muy bajo. Otra estrategia oficial de farmacovigilancia son los reportes periódicos de seguridad que deben hacer los propietarios del registro de medicamentos, cada seis meses los primeros dos años, cada año durante los siguientes tres años y luego cada cinco años, pero esa información no se difunde adecuadamente entre la comunidad médica.
Conclusiones
En nuestra muestra de 377 pacientes adultos hospitalizados, evidenciamos que uno de cada cuatro manifestó RAM durante o antes de su hospitalización. Las mujeres presentaron mayor frecuencia de RAM que los hombres. La mayoría de los pacientes con RAM refirió antecedentes atópicos. Los antibióticos β-lactámicos fueron la primera causa de RAM. En los departamentos de Cardiología y Hematología se presentó el mayor número de casos de RAM. Una cuarta parte de los casos de RAM por hipersensibilidad no se registra en el expediente clínico, lo que representa un riesgo para el desarrollo de anafilaxia por medicamentos.
Correspondencia: Dr. Martín Becerril Ángeles.
Calle Alondra 42, Col. El Rosedal, Delegación Coyoacán, 04330. México, D. F.
Correo electrónico: mbecer5@gmail.com