INTRODUCCION
La osteoporosis, una enfermedad caracterizada por una masa ósea baja y deterioro de la microarquitectura ósea, origina un aumento de la susceptibilidad a las fracturas, lo que supone un importante problema de salud pública especialmente en países industrializados1-3. En mujeres de raza blanca el riesgo acumulado de sufrir una o varias fracturas osteoporóticas (vértebras, antebrazo o cadera) durante la vida se aproxima al 50%4,5. En EE.UU. y Europa, alrededor del 30% de las mujeres posmenopáusicas de raza blanca tienen osteoporosis, definida por medio de la determinación de la densidad mineral ósea (DMO)1. La mayoría de las pacientes osteoporóticas no padecen otras enfermedades responsables de su trastorno y su pérdida ósea se encuentra ligada a dos factores: la menopausia y el envejecimiento. Por tanto, la deficiencia de estrógenos, propia del período postmenopáusico, origina un desequilibrio del remodelado óseo con predominio de la resorción6-8
El alendronato es un inhibidor muy potente de la resorción ósea mediada por osteoclastos, que normaliza la tasa de recambio óseo a niveles premenopaúsicos9. En estudios realizados en animales y seres humanos, la administración de alendronato aumenta la masa ósea manteniendo un hueso normal desde el punto de vista histológico10-13. Se dispone de datos de varios ensayos clínicos controlados y aleatorizados, de hasta 5 años de duración en pacientes con osteoporosis tratados con alendronato14. Estos estudios ponen de manifiesto que el alendronato aumenta la DMO entre un 5% y 10% en la columna vertebral y la cadera y reduce el riesgo de fractura en estas localizaciones de forma significativa.
El objetivo del estudio FOSIT15 doble ciego y controlado con placebo fue evaluar la eficacia y tolerabilidad del alendronato durante un año en una gran población multinacional de mujeres postmenopáusicas con baja masa ósea. En el presente artículo se analizan los resultados obtenidos específicamente por los investigadores españoles, así como la coherencia de dichos resultados con los globales del ensayo multinacional. Además, se muestran los resultados del estudio abierto de extensión de un año de duración realizado posteriormente en España, en el cual se administró alendronato 10 mg/día a todas las enfermas que participaron en el protocolo original, con la intención de evaluar la eficacia del fármaco hasta los 24 meses de tratamiento y el comportamiento del brazo placebo al pasar al grupo de intervención.
PACIENTES Y MÉTODOS
PACIENTES
En la fase multinacional se reclutaron pacientes procedentes de 153 centros en 34 países repartidos entre Europa, América Latina, Australia, Canadá, Sudáfrica y China. En España participaron catorce centros que incluyeron a 175 pacientes. Posteriormente, en el estudio de extensión español se incluyeron un total de 157 enfermas.
Las pacientes candidatas a participar en ambos estudios eran mujeres posmenopáusicas desde hacía al menos 3 años, con una edad inferior a 85 años y una DMO en columna lumbar (L2 a L4) al menos 2 desviaciones estándar por debajo de la media de la mujer premenopáusica adulta, un valor que corresponde aproximadamente a la mediana de la DMO de las mujeres de 65 años. La DMO de columna lumbar, determinada mediante absorciometría radiológica de doble energía (DEXA) fue ¾ 0,86 g/cm2 para densitómetros Hologic QDR (Hologic, Waltham, MA, EE.UU.) o ¾ 0,98 g/cm2 para densitómetros Lunar DPX (Lunar, Madison, WI, EE.UU.). Las candidatas mostraban buena salud y estaban entre el 20% por debajo y el 50% por encima del peso corporal ideal, definido por las tablas de peso y talla de la Metropolitan Life Insurance Company. Antes de entrar en el estudio se midieron los niveles de 25-hidroxivitamina D y se excluyeron aquellas pacientes cuyos valores basales eran inferiores a 12 ng/ml.
Se excluyeron mujeres con enfermedades metabólicas óseas distintas de la osteoporosis posmenopáusica; alteraciones de la función tiroidea o paratiroidea; enfermedades digestivas importantes recientes (ejemplos: ulcus péptico o malabsorción) en el año previo a la participación, o bien el uso de fármacos inhibidores de la secreción gástrica durante más de 2 semanas en los tres meses previos a la inclusión; con infarto de miocardio en el año previo a la inclusión en el estudio; hipertensión arterial o angor incontrolados; alteración significativa de la función renal (creatinina sérica > 1,6 mg/dl o aclaramiento de creatinina inferior a 30 ml/min); presencia de cualquier enfermedad grave en fase terminal. Se excluyeron también a aquellas mujeres que habían recibido un bifosfonato o fluoruro (> 8 mg/día) durante los 6 meses previos; estrógenos (excepto vaginales ¾ 3 veces/semana); ipriflavona o calcitonina durante los 6 meses previos. Las pacientes no podían recibir ningún fármaco que pudiera alterar el metabolismo óseo o mineral, incluida la vitamina A en una dosis superior a 10.000 U/día, vitamina D en dosis superiores a 1.000 U/día, anticonvulsivos o antiácidos quelantes de fosfato. No se excluyeron enfermas que tomaran de forma habitual antiinflamatorios no esteroideos (AINE).
Finalmente, debía ser posible evaluar al menos 3 vértebras desde L1 a L4 mediante la absorciometría por rayos X de doble energía (DEXA), para determinar la DMO en dicha región. No se obtuvieron radiografías de columna antes de la inclusión en el estudio.
Todos los comités éticos regionales o institucionales autorizaron tanto el protocolo original como la extensión de un año y todas las participantes firmaron por escrito un consentimiento informado.
DISEÑO DEL ESTUDIO
Multinacional
Tras un período de estudio de las condiciones basales de 2 a 4 semanas de duración, se asignó de forma aleatoria a las participantes en el ensayo a recibir 10 mg de alendronato o comprimidos de placebo de aspecto idéntico, una vez al día durante 12 meses. Se dieron instrucciones a las pacientes para que tomaran un comprimido del fármaco en estudio con un vaso lleno de agua una vez al día por la mañana, tras el ayuno nocturno y con la prohibición de tumbarse ni tomar ninguna otra bebida o alimento en al menos los siguientes 30 minutos. A todas las pacientes se les dispensaron también comprimidos que contenían 500 mg de calcio elemental en forma de sal (carbonato o citrato) con instrucciones para que tomaran, una vez
al día en la cena, uno de dichos comprimidos.
Estudio de extensión español
Todas las enfermas que completaron el estudio multinacional a los 12 meses eran elegibles para participar en el estudio de extensión. Las enfermas no incluidas en el segundo estudio, o bien pertenecían a centros que no participaron en la extensión, o bien abandonaron el estudio durante el primer año (9 pacientes).
Todas las pacientes participantes en el estudio de extensión fueron instruidas para tomar alendronato a la dosis de 10 mg una vez al día durante otros 12 meses (en total 24 meses de tratamiento) de forma idéntica a como habían tomado el fármaco del estudio en los 12 meses previos. Ni los investigadores ni las enfermas conocían la asignación de tratamiento previa, es decir, si habían recibido fármaco activo o placebo en los 12 meses que duró el estudio inicial.
CRITERIOS DE EFICACIA
La principal variable de eficacia fue el cambio porcentual de la DMO en las regiones analizadas en distintos tiempos predeterminados con relación a su valor basal. Se realizaron densitometrías óseas durante el período basal y a los 3, 6, 12 meses de comenzar el tratamiento, y a los 24 meses en las enfermas que participaron en el estudio de extensión. La DMO se midió utilizando densitómetros Hologic QDR (QDR-1000, 1000/W, 1500 o 2000; Hologic, Waltham, MA) o Lunar DPX (DPX, DPX-L, DPX-alfa; Lunar, Madison, WI). Se analizaron cuatro localizaciones: columna lumbar (criterio de valoración primario), cuello femoral, trocánter y cadera total. Para determinar la DMO en columna lumbar se utilizó la DMO media de al menos 3 vértebras evaluables de L1 a L4. Todas las medidas de la DMO se evaluaron en un laboratorio central de control de calidad.
CRITERIOS DE SEGURIDAD
Los acontecimientos adversos se registraron en cada visita utilizando preguntas no dirigidas. Además, se realizaron pruebas de laboratorio clínicas. Por otra parte, en la visita de selección y en la final se realizaron un electrocardiograma y una exploración física completa, mientras que en las intermedias se realizaron exámenes físicos dirigidos. Los resultados se presentan dentro de los globales del estudio multinacional FOSIT 15. En el estudio de extensión se sumaron a las previas, una visita intermedia a los 18 meses, en la que se procedió como en las visitas intermedias del protocolo original, y una visita final a los 24 meses, en la cual se realizaron los mismos procedimientos que a los 12 meses.
La incidencia de fracturas se determinó mediante la notificación de acontecimientos adversos. Para evaluar si las fracturas habían sido correctamente codificadas por los investigadores, al finalizar el estudio se recogió documentación de apoyo de todas las fracturas, incluidas radiografías y/o informes radiológicos, así como informes de alta donde figurase dicho diagnóstico clínico y/o confirmación del diagnóstico por el investigador o por el médico a cargo del tratamiento de dicha complicación.
MÉTODOS ESTADISTICOS
Población de estudio:
Para el análisis del cambio entre el final del estudio principal y el final del período de extensión se incluyeron (para cada una de las variables) aquellos individuos que presentaban valores de DMO, tanto en el mes 12 como en el final del período de extensión. Para el análisis del cambio entre el momento de entrada en el estudio randomizado y el final del período de extensión se incluyeron aquellos individuos que presentaban valores de DMO tanto en el mes 0 como en el final del período de extensión. Para el análisis del cambio entre el momento de entrada en el estudio randomizado y el final del estudio randomizado, se han incluido aquellos individuos que presentaban valores de DMO tanto en el mes 0 como en 12
Análisis estadístico
La evaluación de los datos sobre eficacia se basó en el principio de «intención de tratar» en el estudio multinacional FOSIT. Sin embargo, en el presente artículo se describe para cada una de las variables (columna lumbar, cuello femoral, cadera total y trocánter) una estadística descriptiva por protocolo de los valores en los meses 0, 12 y 24. El motivo de realizar una estadística descriptiva por protocolo fue realizar una estimación lo más ajustada a la realidad posible de los datos de DMO comparativos («análisis de cumplidores»), especialmente los correspondientes a los 24 meses en comparación con los datos a 12 meses, para comprobar lo sucedido con las enfermas que estaban con placebo el primer año y pasaron a alendronato el segundo año, así como las que recibieron alendronato de forma continua los dos años. Existen muchos estudios publicados (cuyo tipo de análisis ha sido ITT) que analizan el efecto del alendronato sobre la DMO frente a placebo o/u otros fármacos y que muestran de forma consistente la eficacia de este fármaco para incrementar la masa ósea. En este caso se consideró de un gran valor analizar los datos por protocolo con dos objetivos: 1) no sesgar los datos a 24 meses de los completadores del estudio de extensión con los que realizaron sólo el estudio inicial (cuyos datos a 12 meses tendrían que haberse incluido en todos los análisis a 24 meses de haberse realizado un análisis ITT) y 2) poder establecer comparativas reales de lo sucedido entre los 12 y los 24 meses.
Para evaluar la diferencia entre los valores de DMO en el mes 12 y en el mes 24 se calculó para cada individuo la diferencia absoluta (valor en el mes 24 menos valor en el mes 12) y la diferencia porcentual (diferencia absoluta dividida por el valor en el mes 12). Estos análisis se realizaron de manera separada para cada grupo de tratamiento (según asignación en el estudio principal) y conjuntamente para el global de los individuos. Una estrategia similar se utilizó para la comparación del mes 0 con los meses 12 y 24. Para el cálculo de la significación estadística de las diferencias encontradas se utilizó la prueba de la «t» de Student para muestras apareadas. Todas las comparaciones entre grupos fueron bilaterales y la significación estadística se definió como un valor de p ¾ 0,05. Se utilizó el paquete estadístico SAS frente a 6.12.
RESULTADOS
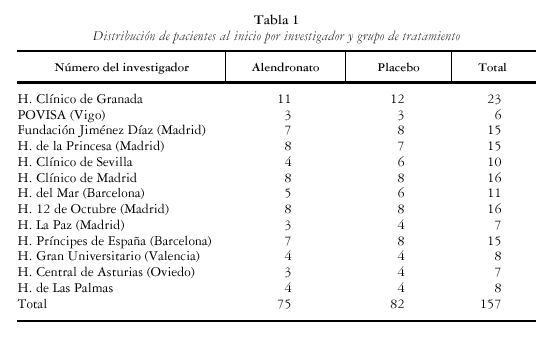
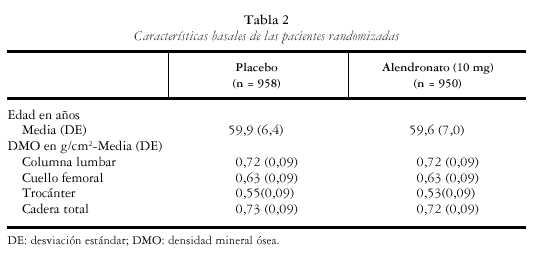
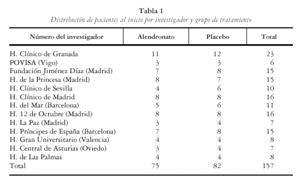
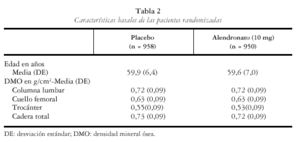
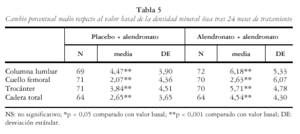
En el estudio multinacional se incluyeron 1908 pacientes distribuidas en dos grupos de 950 y 958 pacientes asignadas según el alendronato y el placebo, respectivamente. España contribuyó con 175 pacientes. En este artículo se muestran los resultados de la población española del estudio en la que se obtuvieron densitometrías basales, a los 12 meses (157) y también a los 24 meses (146) (tabla 1). En el estudio multinacional los dos grupos de tratamiento fueron comparables en el momento basal respecto a las características demográficas, los valores de DMO (tabla 2). Los resultados del grupo español no difieren del multinacional. Las pacientes españolas que no participaron en el estudio de extensión tenían unas características basales semejantes a las participantes.
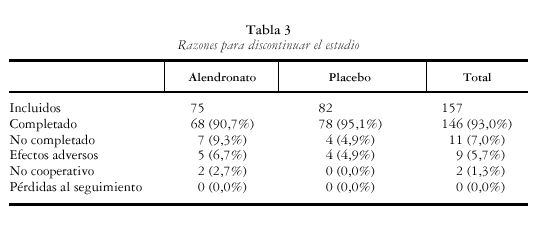
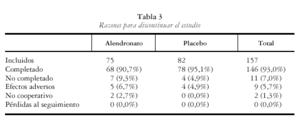
En conjunto completaron el estudio inicial más la extensión, un total de 146 enfermas (93%). Hubo 11 abandonos, 9 por efectos adversos y 2 por voluntad propia. No hubo pérdidas en el seguimiento (los detalles se muestran en la tabla 3). Esta tasa de abandonos es ligeramente inferior a la del estudio multinacional, en el cual un total de 1.697 mujeres (89%) completaron todas las visitas y procedimientos, 832 (88%) en el grupo placebo y 865 (90%) en el grupo alendronato.
DENSIDAD MINERAL ÓSEA
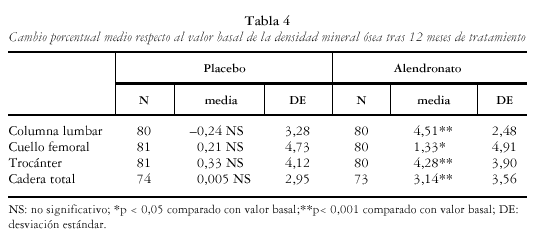
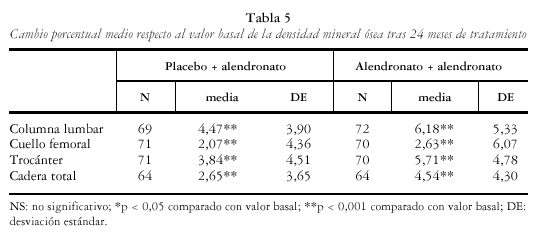
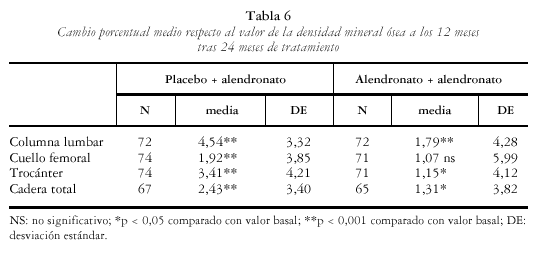
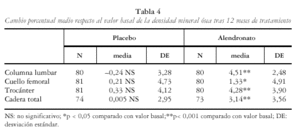
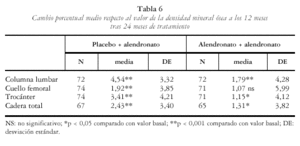
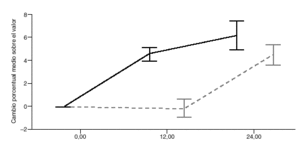
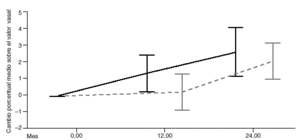
En las pacientes tratadas con alendronato se comprobó un aumento significativo y progresivo de la DMO. En las tablas 4-6 y figs. 1 y 2 se recogen los cambios de la DMO a los 12 y 24 meses con respecto al valor basal, así como entre los 12 y los 24 meses. Los incrementos de DMO son significativos en todas las localizaciones y en todos los tiempos estudiados. Como excepción, no se encontró significación estadística, en el grupo tratado con alendronato, al analizar el cambio porcentual de la DMO en el cuello femoral entre los meses 12 y 24, aunque sí en el mes 24 con respecto al valor basal (p< 0,001).
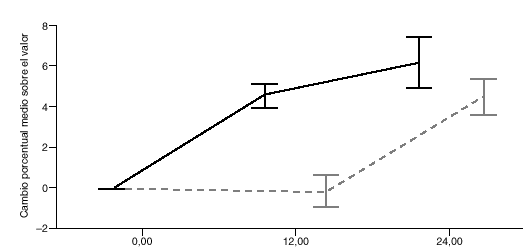
Fig. 1. Columna lumbar total. Cambio porcentual medio sobre el valor basal, e intervalo de confianza al 95%, por mes para ambos grupos de tratamiento.
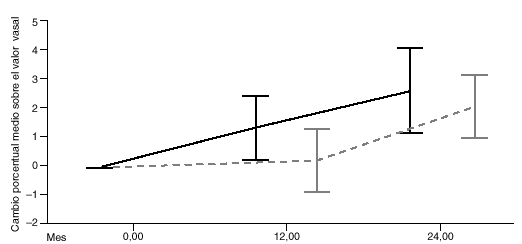
Fig. 2. Cuello femoral. Cambio porcentual medio sobre el valor basal, e intervalo de confianza al 95%, por mes para ambos grupos de tratamiento.
A los 12 meses de tratamiento, la diferencia entre los grupos de alendronato y placebo en el porcentaje medio de cambio de la DMO fue de 4,75% (IC:4,57-4,93) en columna lumbar; 1,12% (IC:1,08-1,18) en cuello femoral; 3,95% (IC:3,91-3,99) en trocánter y 3,09% (IC:2,94-3,24) en cadera total.
En las pacientes que recibieron placebo durante el primer año y alendronato el segundo, la diferencia entre el mes 12 y el mes 24 fue de 4,54% (3,75% a 5,34%) en columna lumbar; 1,92% (1,03% a 2,81%) en cuello femoral; 3,41% (2,43% a 4,39%) en trocánter y 2,43% (1,60% a 3,26%) en cadera total; todas ellas significativas (p< 0,001). Los incrementos finales de DMO conseguidos en estas pacientes son inferiores a los observados en aquellas tratadas durante los dos años con alendronato
FRACTURAS CLINICAS
Al cabo de los dos años, en el grupo analizado se produjeron cinco fracturas clínicas (una fractura de quinto dedo de la mano, otra de cuarto dedo de la mano y tres fracturas vertebrales). El pequeño tamaño muestral no permite obtener conclusiones válidas sobre este parámetro.
SEGURIDAD Y TOLERABILIDAD
El alendronato se toleró bien en general y los resultados de tolerabilidad no difirieron de los del estudio multinacional. En concreto, hubo un 11% de pacientes que refirieron algún efecto adverso posiblemente relacionado con el fármaco (nunca en una frecuencia superior al 2%) y en un 2% de las enfermas el efecto fue considerado grave (2 cardiovasculares, una fractura de dedo de la mano, una reacción alérgica, un quiste aracnoideo, y dos epigastralgias. Estas últimas fueron los únicos acontecimientos adversos graves relacionados con el fármaco).
DISCUSIÓN
Los resultados del estudio muestran que dos años de tratamiento con alendronato a dosis de 10 mg/día producen un aumento significativo de la DMO, con incrementos más acusados en el primer año y se mantienen de forma continua y progresiva durante el segundo.
Los aumentos registrados de DMO en la columna y cadera son similares a los observados tanto en estudios previos de un año de duración en población de EE.UU.16,17,18 como en el estudio multinacional FOSIT15. El efecto medio ponderado sobre la DMO en columna lumbar en las pacientes participantes en dichos ensayos clínicos fue de 5,06% y 5% respectivamente, valores comparables al 4,51% obtenido en el grupo español al cabo de un año. Igualmente sucede con los valores de cadera total, con incrementos del 3,1% en el multinacional y 3,14% en el español. La uniformidad de la respuesta es muy notable considerando las diferencias geográficas (EE.UU. solo, multinacional o España), la gran variabilidad en los tamaños muestrales (que inciden obviamente en la media obtenida) y las diferentes características de la población participante. En este estudio, a diferencia de los estudios FIT19,20, en los que se distribuía a las pacientes tanto por sus valores basales de DMO como por la historia previa de fractura, se han incluido enfermas exclusivamente en función de la DMO basal. El grupo es, por tanto, más heterogéneo, con criterios poco restrictivos en la selección de pacientes, lo que lo aproxima en gran medida a la práctica clínica real.
El estudio español añade sobre el multinacional un aspecto nuevo e interesante: la extensión en abierto un segundo año. Este diseño permite contrastar los resultados dentro de un mismo grupo de pacientes y evita sesgos de grupo, añadiendo, además, una prueba nueva de la eficacia del fármaco. En el primer año el brazo placebo fue un control convencional del grupo de intervención, pero en el segundo las enfermas pasaron a recibir alendronato; la experiencia y los datos recogidos en estos primeros 12 meses son el control ideal de la intervención posterior, puesto que cada enferma actúa como control de sí misma. Cabe destacar que las enfermas tratadas con placebo el primer año y alendronato en el segundo muestran ligeras pérdidas de DMO o cambios mínimos en los primeros 12 meses, mientras que en el periodo de tratamiento activo (de 12 a 24 meses) se observan incrementos significativos y acusados de la DMO en todas las localizaciones. Así, el incremento ponderado de la DMO en columna lumbar desde los 12 a los 24 meses de tratamiento en el grupo placebo es del 4,54%, cifra comparable a la del grupo alendronato tras un año de tratamiento (4,51%). Estos datos no sólo muestran la eficacia del fármaco, sino también la consistencia de los resultados.
En términos de medicina basada en la evidencia, el concepto de consistencia es de gran importancia y constituye la base de los metaanálisis21,22. El alendronato ha demostrado su consistencia en un metaanálisis realizado a nivel internacional23, y en otro realizado en España por Arboleya et al publicado recientemente en Medicina Clínica24. En este último se demuestra cómo los incrementos de DMO son consistentes en todos los ensayos clínicos realizados con alendronato que fueron analizados, y dicho efecto no era dependiente de ninguno de los estudios en particular. Los datos del presente estudio están también dentro del rango previsto por dicho análisis.
En el estudio multinacional, del que estas enfermas formaron parte, se demostró que el alendronato reduce el riesgo de fractura no vertebral en un 47% en tan sólo un año15. El tamaño muestral en el subgrupo español es demasiado pequeño como para realizar un análisis de cambio en el riesgo de fractura con la intervención. Sin embargo, los incrementos de DMO conseguidos permiten realizar una inferencia indirecta sobre la capacidad de reducción del riesgo de fractura, a tenor de los interesantes resultados publicados recientemente por Wasnish et al25, sobre la relación entre los cambios de DMO conseguidos con diferentes terapias y la modificación del riesgo de fractura En este trabajo se realizó un metaanálisis de los ECA publicados donde se relaciona, mediante regresión de Poisson, el riesgo relativo (RR) de fractura y el cambio porcentual medio en DMO. El modelo predice que cambios en la DMO del 8% se asocian a una reducción media del RR del 54%. La mayor parte de esta reducción del RR es debida al cambio en la DMO y el resto a errores de medida, sesgos de publicación o limitaciones de la tecnología actual. Otros estudios han mostrado que un mayor incremento de la DMO (> 3% en 12-24 meses) se asocia con un mayor descenso del riesgo de fractura26. Por tanto, la medición de la DMO representa el mejor método para cuantificar el riesgo de fractura en la actualidad5; y aquellos fármacos antiresortivos que producen un mayor aumento de la DMO debieran ser más efectivos en la reducción del riesgo de fractura que otros, si no existen alteraciones en la calidad ósea.
En conclusión, este estudio muestra que en una población española de mujeres posmenopáusicas con bajo nivel de masa ósea, el tratamiento durante dos años con alendronato aumenta la DMO de forma rápida en el primer año y que continúa sin alcanzar una meseta en el segundo. El aumento de DMO a un año es comparable al observado en la población multinacional del estudio FOSIT. Además, la consistencia de estos hallazgos se confirma con el idéntico incremento de DMO observado en las pacientes incluidas en el grupo placebo durante el primer año y posteriormente tratadas con alendronato durante el segundo.
Listado de investigadores del Grupo Español del Estudio FOSIT
M. Muñoz-Torres, M. Quesada, F. Escobar-Jiménez. Hospital Universitario San Cecilio, Granada.
D. Roig-Escofet, M. Romera, L. Mateo, A. Rozadilla, D. Roig Vilaseca. Hospital Príncipes de España, Ciudad Universitaria de Bellvitge, Barcelona.
C. Lozano, J. Jarreno. Hospital Universitario San Carlos, Madrid.
A. Rapado, M. Díaz Curiel, C. Turbí. Fundación Jiménez Díaz, Madrid.
A. García-Vadillo, S. Castanada. Hospital de la Princesa, Madrid.
F. Hawkins, E. Jodar, G. Martínez. Hospital 12 de Octubre, Madrid.
A. Díaz-Pérez, M. Martínez, X. Nogués. Hospital del Mar, Barcelona.
R. Pérez-Cano, M. Vázquez, M. Moruno. Hospital Clínico, Sevilla.
M. Sosa, R. de Castro. Hospital Universitario Insular, Las Palmas de Gran Canaria.
J. Calvo Catalá. Hospital General Universitario, Valencia.
A. Torrijos, J. Gijón. Hospital La Paz, Madrid.
J. Ferreiro, N. Gómez, J. Ibanex, L. Corral. Clínica Povisa, Pontevedra.
J. Cannata, C. Gómez Alonso. Hospital Central de Asturias, Oviedo.