INTRODUCCIÓN
En las últimas décadas, la tomografía computarizada (TC) se ha convertido en la principal herramienta diagnóstica para la estadificación inicial y el seguimiento del tratamiento de la patología oncológica. Sin embargo, tiene ciertas limitaciones que reducen su sensibilidad en la caracterización de ciertas lesiones, como adenopatías de tamaño normal que pueden ser patológicas o masas fibróticas postratamiento sin actividad tumoral. La tomografía por emisión de positrones (PET) ha venido empleándose también durante los últimos años para la estadificación y control del tratamiento de los pacientes con cáncer, proporcionando una información funcional, más que anatómica, que se basa en el grado de captación y metabolismo de glucosa por parte del tumor. Pero esta técnica también presenta limitaciones. La más importante es la escasa información anatómica que aporta frente a la TC y otros métodos radiológicos como la resonancia magnética (RM). Por otro lado, la captación del radiotrazador no es específica de los tumores y hay acumulación fisiológica en varios órganos normales, así como en procesos inflamatorios que pueden ocasionar falsos positivos con la PET1. En nuestro medio el isótopo radiactivo utilizado es el F18 y la molécula marcada o radiofármaco es la F18-2-fluoro-2-desoxi-D-glucosa.
El corregistro de estudios de medicina nuclear con información anatómica obtenida mediante métodos radiológicos permite una correlación exacta de datos moleculares y anatómicos en la misma imagen.
Tradicionalmente, para combinar imágenes PET y TC se utilizan dos métodos. Por una parte se obtienen las imágenes de forma separada en distintas sesiones y máquinas y posteriormente se realiza una correlación visual, comparando los datos de ambas modalidades y por otra, la fusión de ambas imágenes mediante un programa informático. El problema de este sistema es que no se produce una alineación exacta2,3.
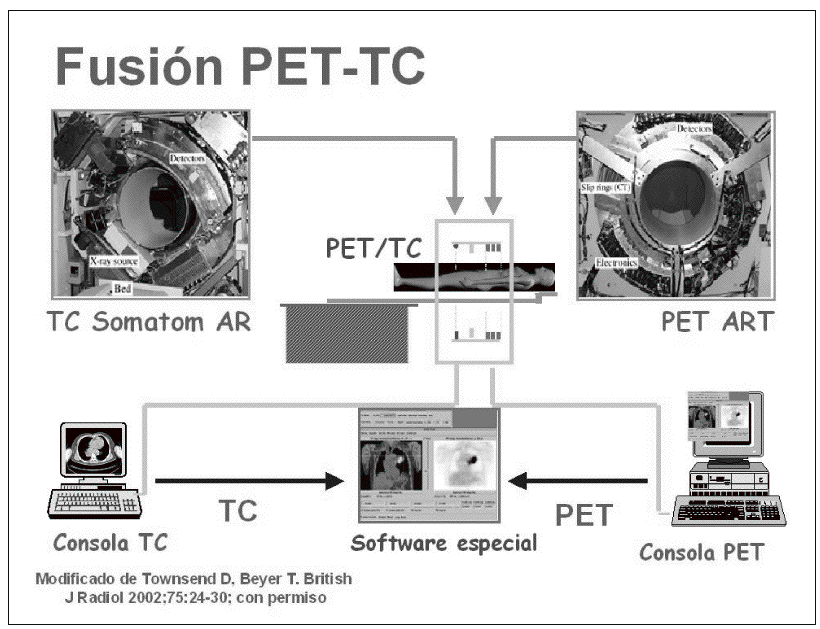
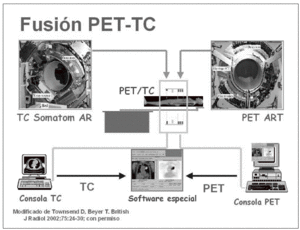
El nuevo sistema híbrido PET/TC integra en la misma máquina un escáner TC y otro PET situados en línea y que permiten la adquisición en una sola sesión de imágenes combinadas mientras el paciente permanece en la misma posición, se realiza la TC que se utiliza para corregir la atenuación de la PET y a continuación la PET. El primer sistema dual PET/TC se desarrolla en la Universidad de Pittsburg en 1998 por el Dr. David Townsend4,5 (fig. 1). En Europa el primer equipo PET/CT se instala en la Universidad de Zurich en marzo de 2001 y en España en el Hospital Universitario La Paz en julio de 2003, con ubicación y gestión en el servicio de Medicina Nuclear, aunque con la idea inicial de formar una Unidad de Imagen PET/TC donde no se diferenciaran médicos nucleares y radiólogos. Este inicio novedoso, no exento de problemas por los protagonismos de unos y otros, está resuelto en el momento actual en nuestro centro en el campo de la investigación exclusivamente y hoy es debate en todos los foros6,7.
Fig. 1.--Fusión PET/TC. Modificada de Townsend DW, Beyer T. A combined PET/CT scanner: the path to true image fusion. Br J Radiol. 2002;75:S24-S30.
El objetivo de este trabajo es describir la experiencia inicial del uso de la técnica combinada PET/TC en el manejo clínico de la patología oncológica en nuestro medio.
MATERIAL Y MÉTODO
Descripción de la técnica PET/TC
Método de estudio de PET/TC
Equipo
Características del equipo PET/TC: el equipo DISCOVERY LS consiste en un Gantry integrado que contiene un tubo de rayos X de TC multidetector de 4 coronas y un escáner de la PET que consta de dieciocho anillos detectores de cristales de germanato de bismuto (BGO). El equipo presenta un sistema electrónico de adquisición y reconstrucción. Los ejes mecánicos de los dos sistemas están alineados. Existen computadores diferentes para la adquisición de la PET y de la TC y hay también entre ambos una conexión para la transferencia de datos. Primero se efectúa la adquisición de la TC y a continuación la adquisición de la PET (emisión y transmisión).
Realización de la prueba
La técnica TC se realiza según el procedimiento habitual. Los parámetros empleados en la TC de baja dosis para la corrección de la atenuación son los siguientes: KVp / mAs / tiempo por rotación (seg): 140/80/0,5, colimación del detector 2,5 mm, grosor de corte 3 mm, intervalo de reconstrucción 2 mm, pitch 6. Si se realiza la TC diagnóstica (TC de alta dosis) con contraste intravenoso yodado entonces el miliamperaje se ajusta automáticamente y sube de acuerdo al peso del paciente hasta un máximo de 300 mAs. El contraste yodado utilizado es 140 ml de iobutrol (Xenetix 300 mg Guebert) con caudal de 3 ml/s, y un retraso de 45 a 60 segundos según la patología a estudiar.
La adquisición de los datos de la PET se realiza en respiración espontánea suave, obteniéndose seis volúmenes contiguos con una longitud transversal de 14,6 cm. El rastreo se efectúa desde cerebelo a suelo de la pelvis de forma general, aunque si la indicación es patología de cabeza-cuello y/o melanoma entonces el volumen de estudio varía. El campo de visión (FOV) es de 15,2 cm en el eje axial. La resolución final teórica (FWHM), después de la reconstrucción, se sitúa entre 4,8-6,2 mm. La duración de la adquisición de los datos de la PET varía de 30 a 40 minutos, según el volumen de estudio. Las imágenes se reconstruyen usando un algoritmo interactivo estándar.
Protocolo clínico de la PET/TC
A todos los pacientes, antes de realizar la prueba, se les efectúa una entrevista explicativa. Se solicita un consentimiento informado previo a la administración de 18FDG, así como una hoja específica validada por el comité ético a los pacientes a los que se realiza una PET/TC en el seno de un proyecto de investigación, y un consentimiento informado para la administración de contraste intravenoso yodado para la realización de la TC diagnóstica.
Preparación del paciente
Se requiere un ayuno de al menos cuatro horas, aunque el paciente puede tomar líquidos no azucarados. Se realiza la determinación de glucemia, posteriormente se administra la 18FDG (10-15 mCi o 370-555 MBq) vía intravenosa previa hidratación, 45-60 minutos antes de la adquisición de la PET/TC. Durante este periodo de tiempo, los pacientes deben permanecer en reposo e ingerir el contraste oral (1l de solución de amidotrizoato sodio y meglumina, gastrografin, diluido al 3%), cuando está indicado.
Posición del paciente
En decúbito supino sobre la mesa de exploración con los brazos por encima de la cabeza, permaneciendo en la máxima inmovilidad posible, excepto en los tumores de cabeza-cuello y siempre que el paciente no tolere esta posición, en cuyo caso los brazos se colocan a lo largo del cuerpo. Primero se efectúa la adquisición de la TC de baja dosis y a continuación la adquisición de la PET. Por último se realiza la fusión de la imagen PET/TC. Cuando la técnica se utiliza bajo la figura de uso tutelado del SNS como PET, la TC se efectúa a baja dosis con contraste oral y sin contraste intravenoso. En el momento actual en los proyectos de investigación cuyo objetivo son la validación de la técnica, se realiza después de terminar la PET una nueva TC en las mismas condiciones en las que se realizaría esta modalidad con fines diagnósticos (TC de alta dosis o diagnóstica). En este subgrupo de pacientes se efectúa en una única sesión la PET/TC y se excluyen aquellos pacientes que hayan sido sometidos a una TC previa. Se adecua el volumen de estudio a la indicación clínica. En el estudio específico del carcinoma no microcítico de pulmón, que estamos llevando a cabo, la TC se realiza con contraste intravenoso y se sustituye el contraste oral por la administración oral de agua.
Para la visualización de los estudios de la TC, PET y la fusión se utiliza una consola eNTEGRA y/o Xeleris (GE Medical Systems) que permite reformateos multiplanares de imágenes.
RESULTADOS
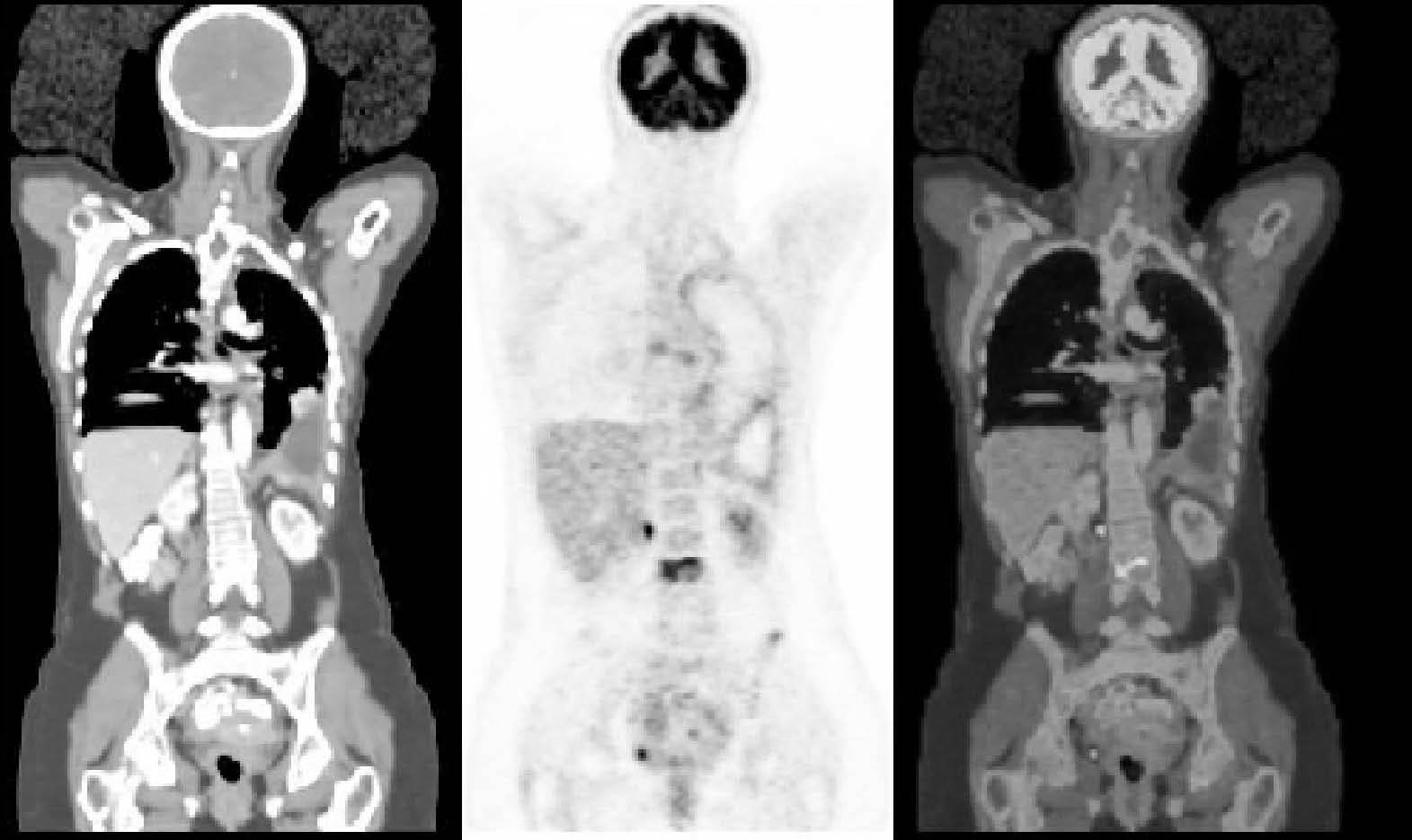
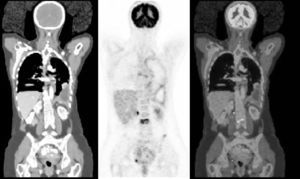
Desde el inicio de la actividad de la unidad PET/TC del Hospital Universitario La Paz, en septiembre de 2003 hasta agosto de 2005, se han realizado 2.459 exploraciones, de las cuales 2.200 se han efectuado bajo la figura de uso tutelado del Sistema Nacional de Salud (SNS) y como PET con TC de baja dosis, siguiendo las indicaciones aprobadas (tabla 1). El resto corresponden a pacientes incluidos en proyectos de investigación que no tenían un estudio de TC previo. Estos últimos incluyen: estudios de linfomas, carcinoma no microcítico de pulmón, carcinoma colorrectal y cáncer de cabeza-cuello. Todas estas exploraciones se han efectuado con contraste yodado intravenoso. Con la excepción de la indicación de patología de cabeza-cuello, estos estudios se han realizado con los brazos hacia arriba, desde el cerebelo a sínfisis del pubis con contraste oral e intravenoso (fig. 2). En el caso concreto del cáncer de pulmón y estudio de hígado en patología de colón y recto se ha utilizado agua como contraste negativo.
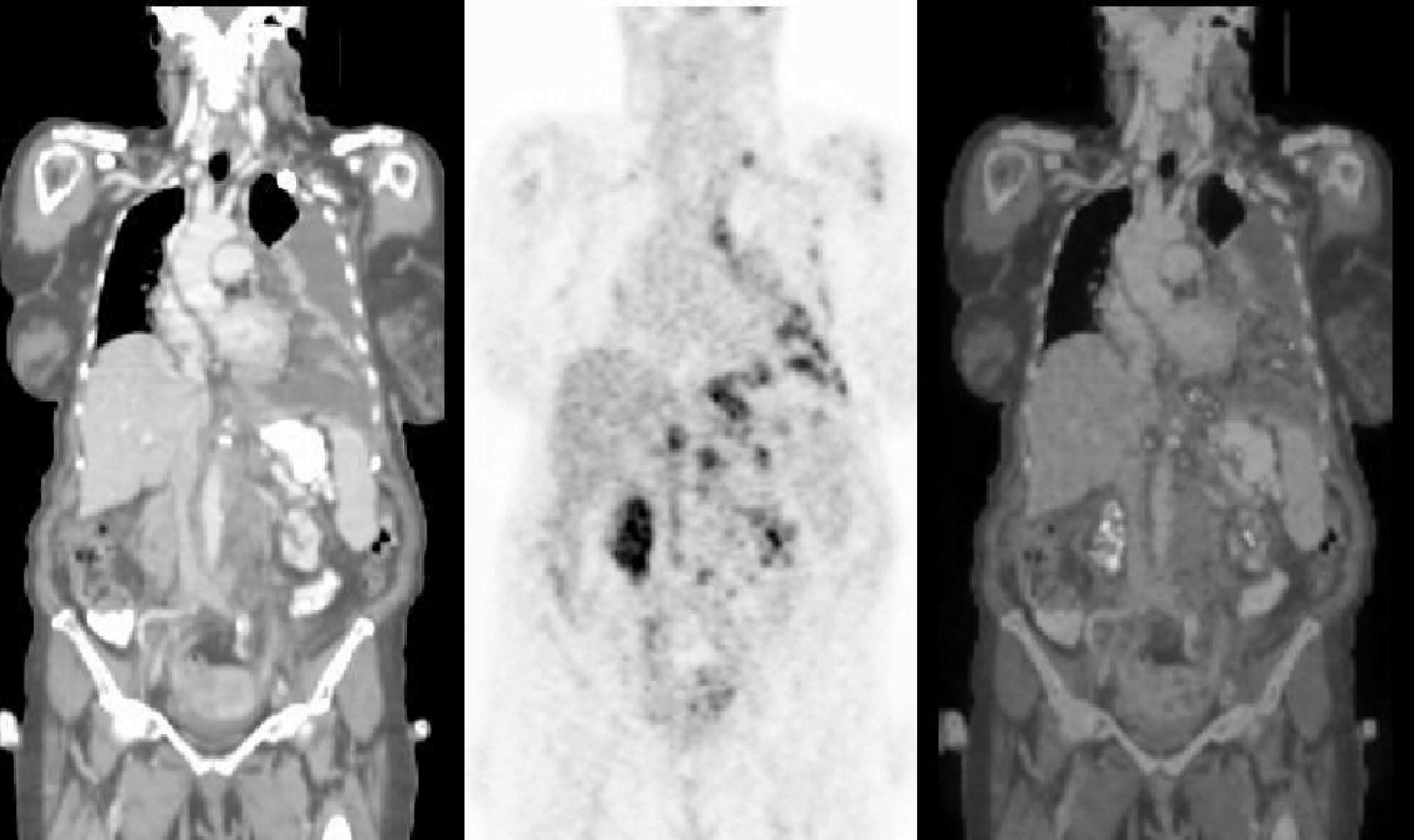
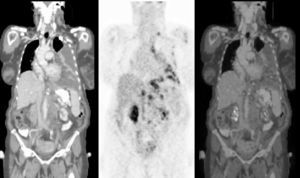
Fig. 2.--Técnica de estudio con contraste oral e intravenoso. A: TC coronal con contraste oral e intravenoso en una paciente con diagnóstico de carcinoma de mama. Los brazos se sitúan por encima de la cabeza para disminuir los artefactos por endurecimiento del haz en el tronco. B: la PET en el plano coronal con reconstrucción volumétrica muestra captación patológica del radiotrazador en mediastino, pleura y vértebra lumbar. C: fusión de las dos técnicas.
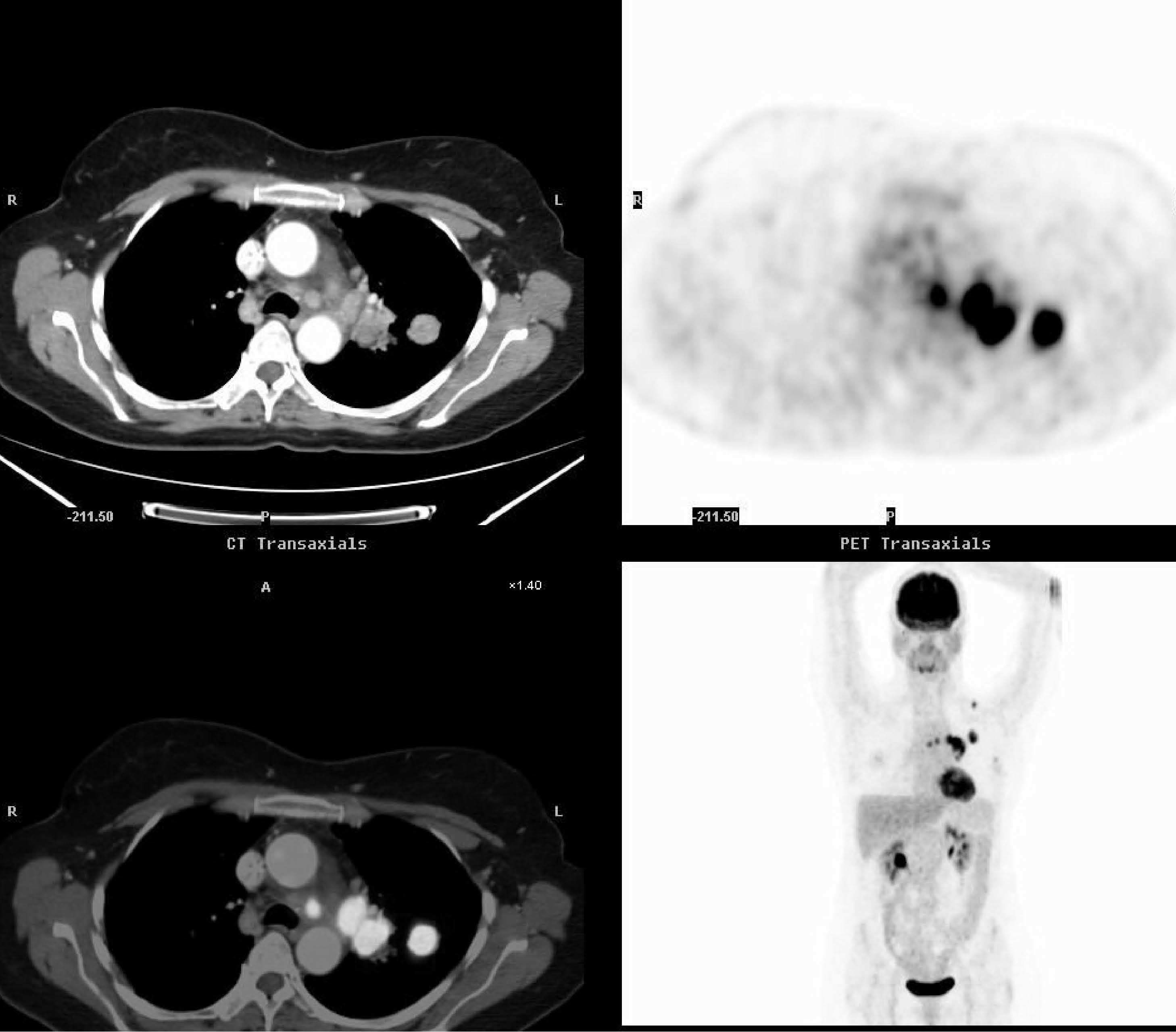
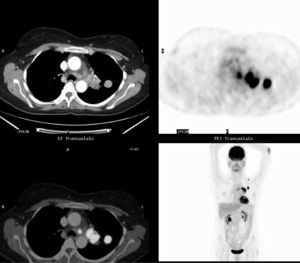
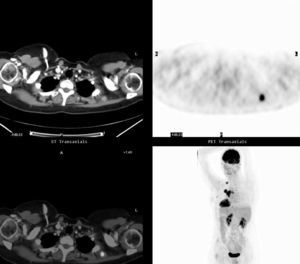
Los porcentajes globales de las patologías estudiadas en las 2.459 exploraciones son los siguientes: cáncer de pulmón en estadificación y reestadificación (14,7%) (figs. 3A y 3B) y caracterización del nódulo pulmonar solitario (7%) (fig. 4). En las neoplasias linfoides se ha evaluado la estadificación de la enfermedad, respuesta al tratamiento y la diferenciación entre fibrosis y/o recidiva, correspondiendo a linfoma no Hodgkin un 13% (fig. 5) y a la enfermedad de Hodgkin un 10,5% del total de la exploraciones (fig. 6).
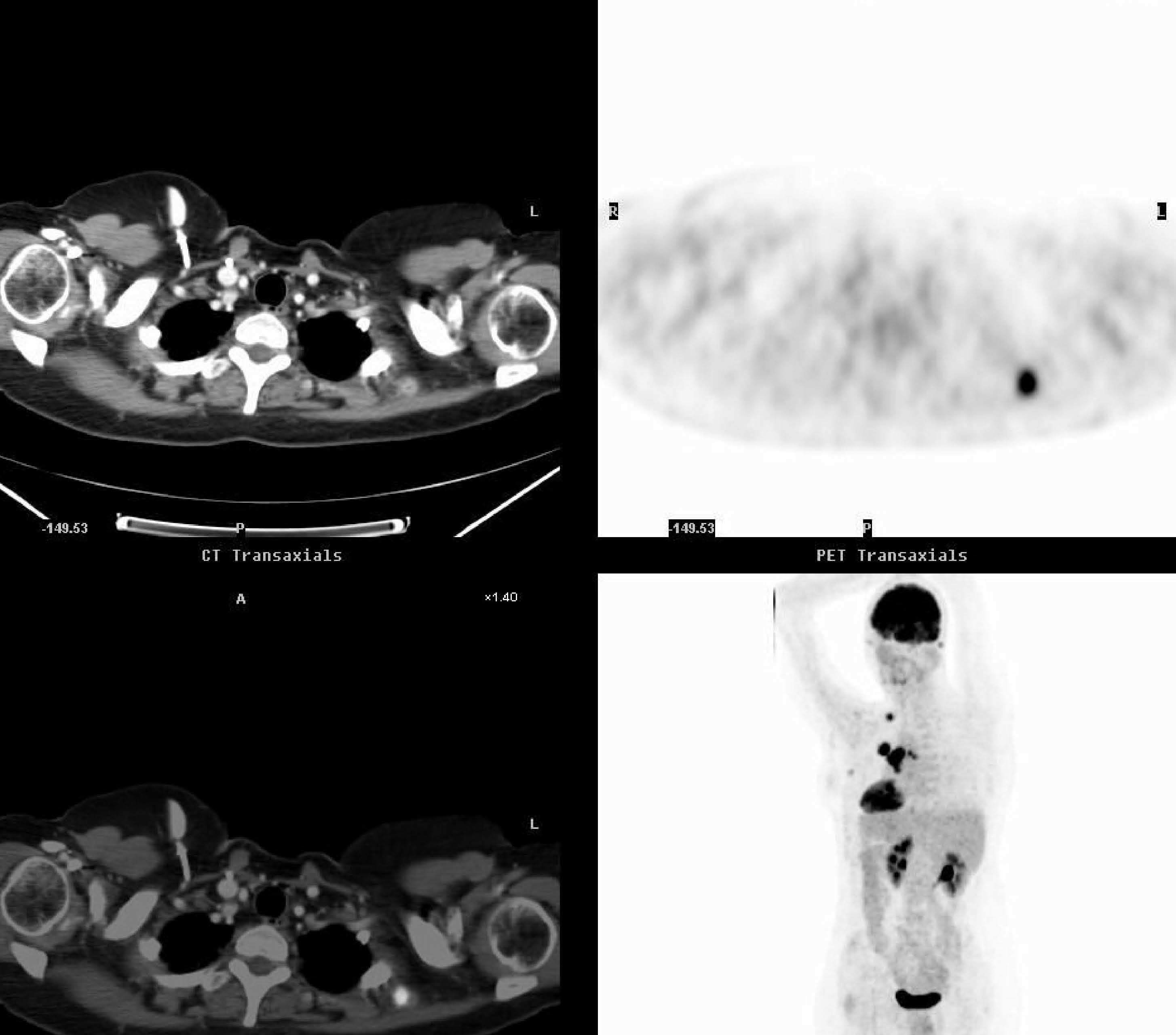
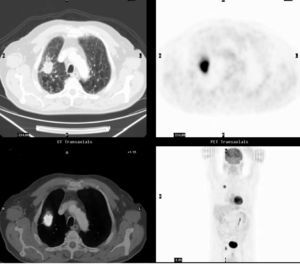
Fig. 3.--Estudio de extensión en una mujer de 50 años con adenocarcinoma pulmonar. A: masa en segmento posterior del lóbulo superior izquierdo asociada a adenopatías en hilio izquierdo y en ventana aortopulmonar que muestran intensa captación de 18FDG. B: en el mismo estudio se objetiva una captación patológica del radiotrazador adyacente al músculo trapecio izquierdo, no claramente identificado en la TC. La PAAF de la lesión demostró infiltración por adenocarcinoma, modificando la estadificación clínica de la paciente a un estadio IV. La PET en el plano coronal en la figura 3A y en el plano oblicuo en la figura 3B demuestran estos hallazgos.
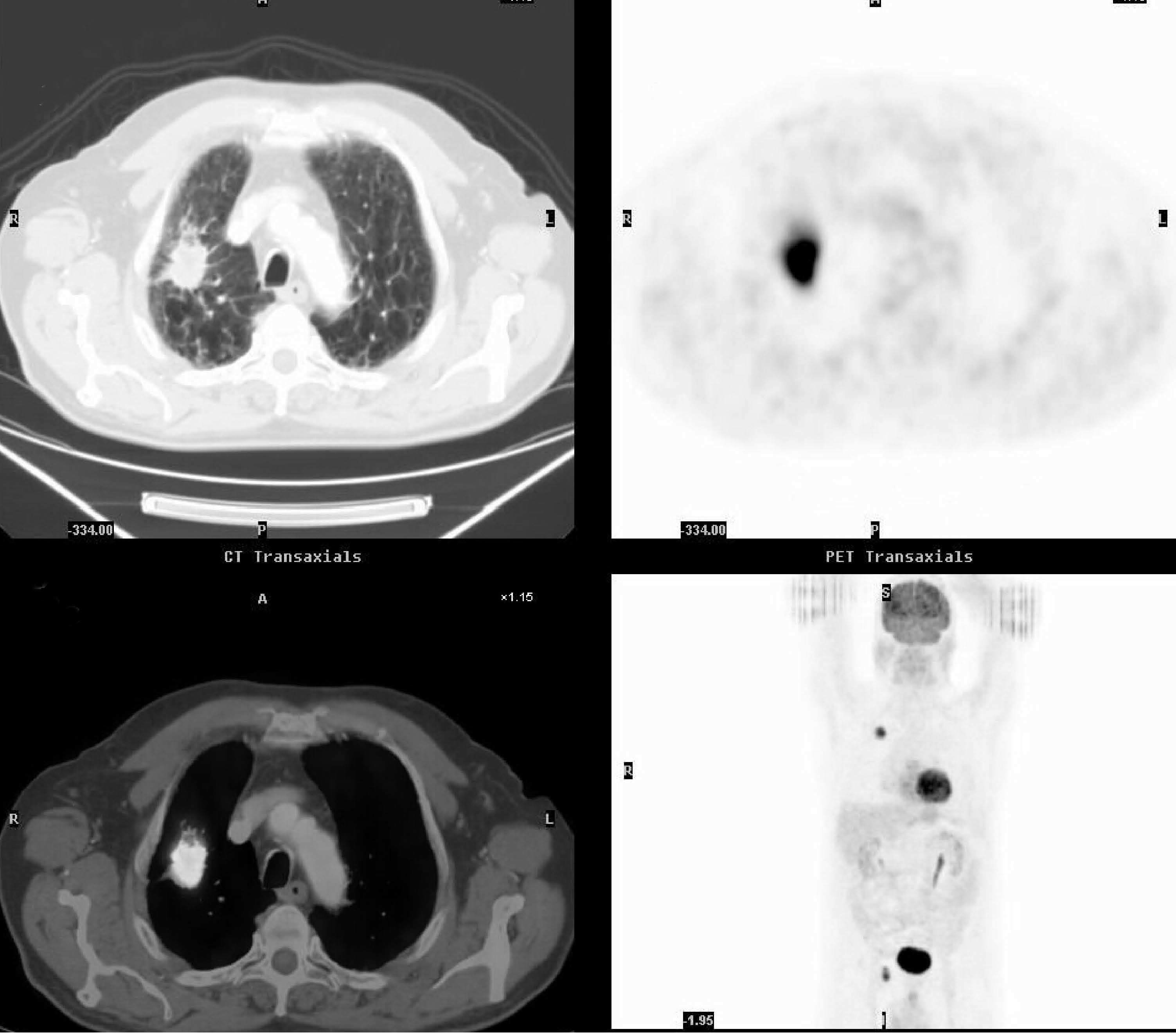
Fig. 4.--Caracterización de nódulo pulmonar solitario en un varón de 70 años. Nódulo espiculado de 28,8 mm de diámetro situado en el segmento apical del lóbulo superior derecho (A) con intensa captación del radiotrazador (B), sin visualización de adenopatías ni captación de 18FDG en cadenas ganglionares como se demuestra en la fusión PET/ TC (C) y en el plano coronal del estudio PET (D). La TC (A) identifica además áreas de enfisema pulmonar. La cirugía demostró carcinoma epidermoide sin afectación ganglionar.
Fig. 5.--Estudio con tomografía por emisión de positrones-tomografía computarizada (PET/TC) de estadificación en Linfoma no Hodgkin (LNH). Mujer de 65 años con el diagnóstico inicial de LNH de alto grado. El estudio se realizó con los brazos a lo largo del cuerpo por las condiciones clínicas de la paciente, que no toleró la posición de brazos por encima de la cabeza. La PET (B) presenta incremento de 18FDG en localización supra e infradiafragmática. La TC (A) y la fusión PET/ TC (C) muestran la afectación en cadena supraclavicular izquierda, mediastino, pleura y cadenas ganglionares paraórticas bilaterales.
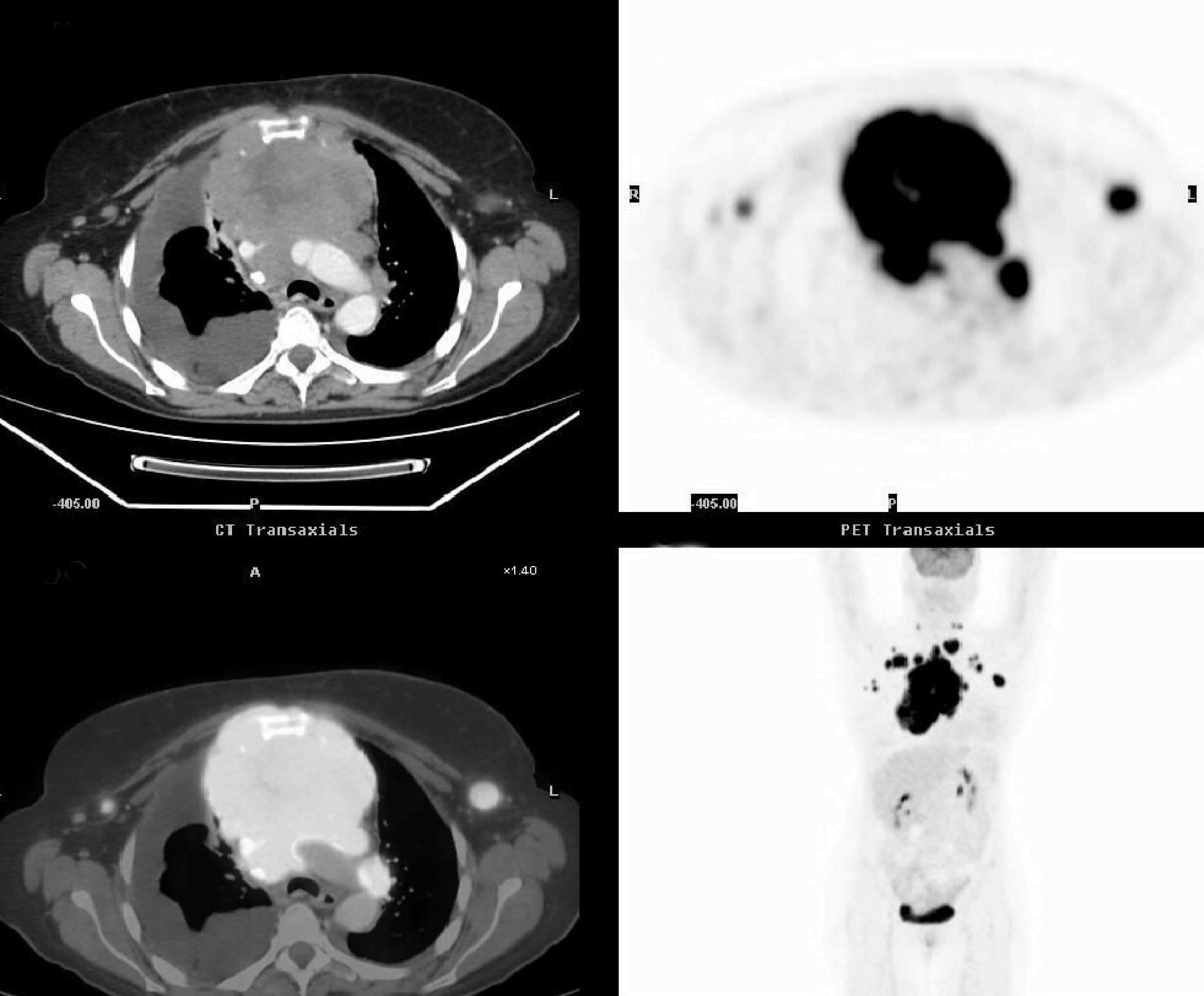
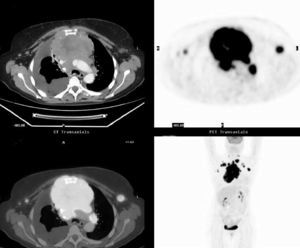
Fig. 6.--Estudio con tomografía por emisión de positrones-tomografía computarizada (PET/TC) de estadificación en linfoma Hodgkin. La PET en este corte axial (B) y en el coronal (D) muestra captación intensa de radiotrazador en el mediastino, así como en ambas axilas, que sugieren la presencia de adenopatías. La TC con contraste intravenoso (A) muestra la masa mediastínica de gran tamaño con una atenuación heterogénea y derrame pleural derecho; sin embargo los ganglios axilares derechos no tienen un tamaño significativo para malignidad. La fusión PET/TC (C) confirma que la actividad patológica de la 18FDG corresponde al conglomerado mediastino y a adenopatías axilares y muestra el derrame pleural derecho sin captación de radiotrazador.
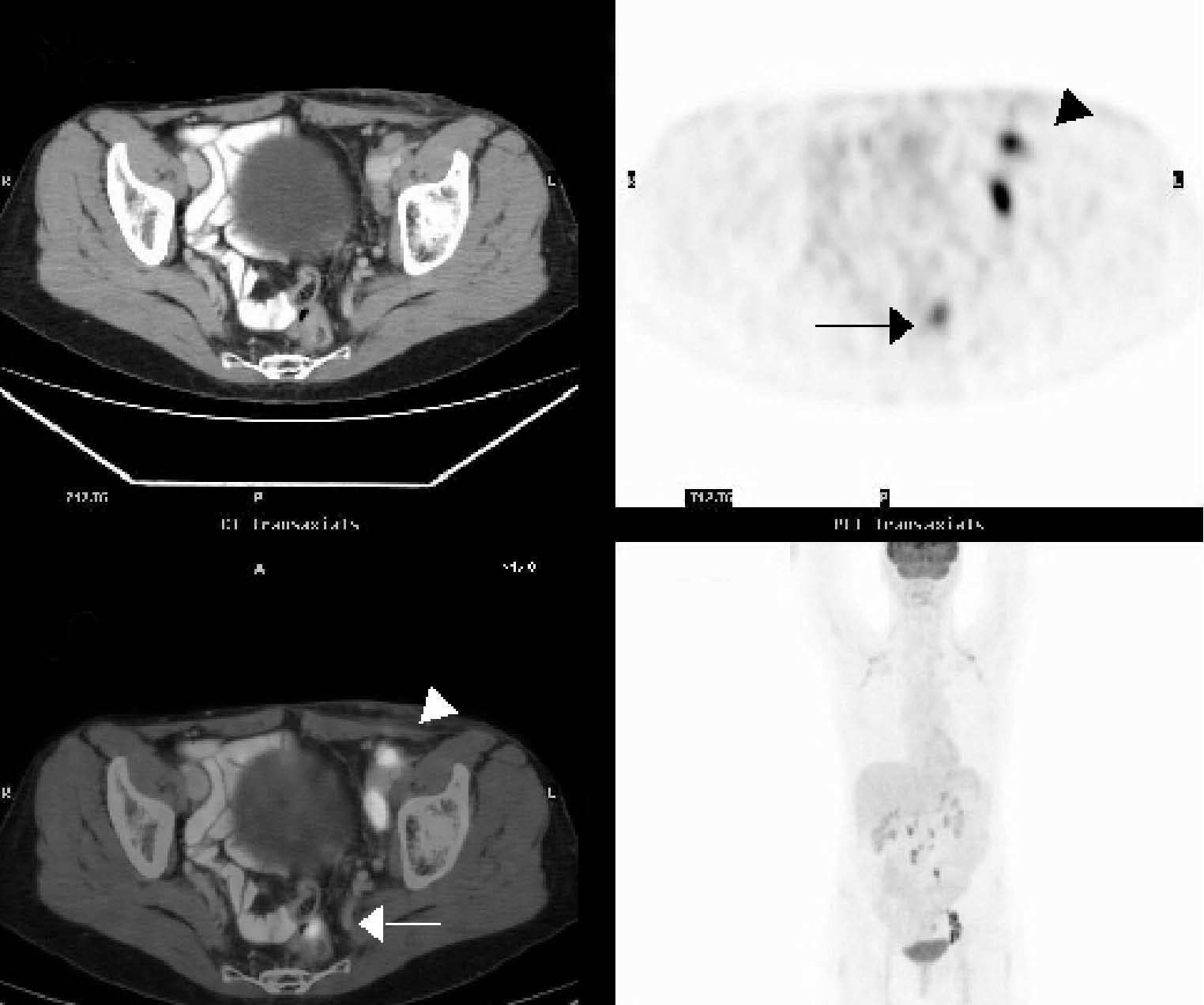
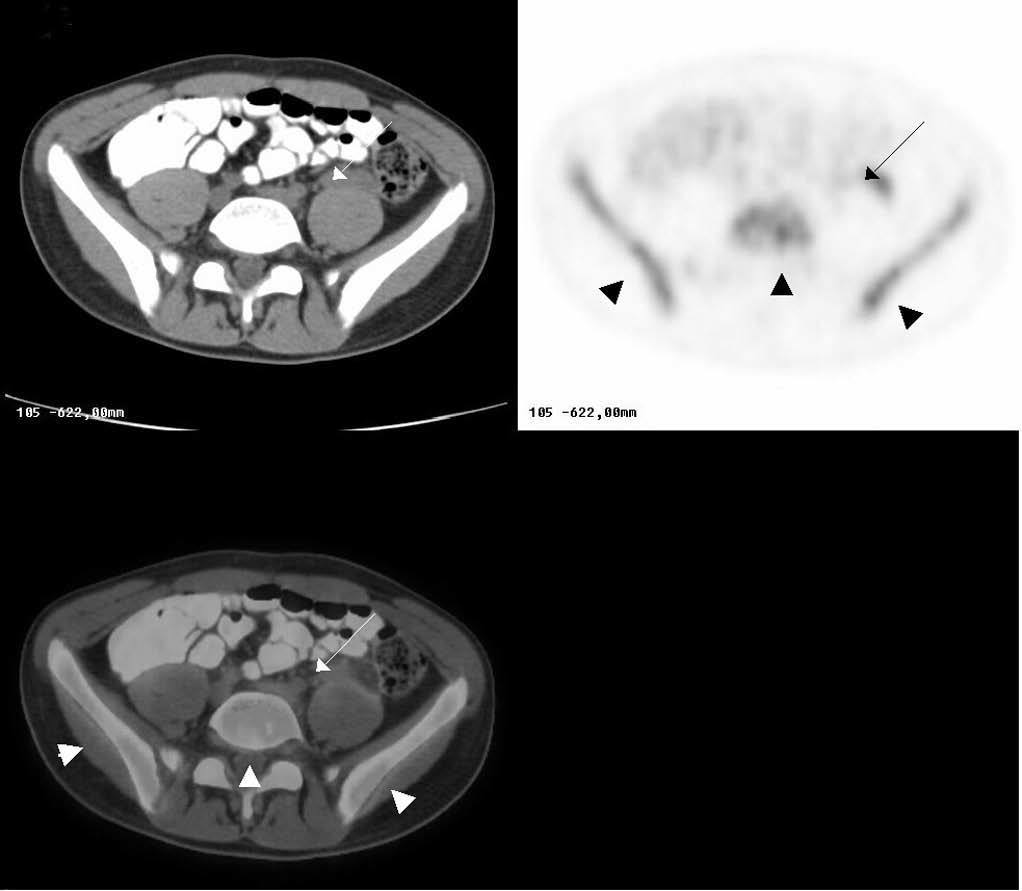
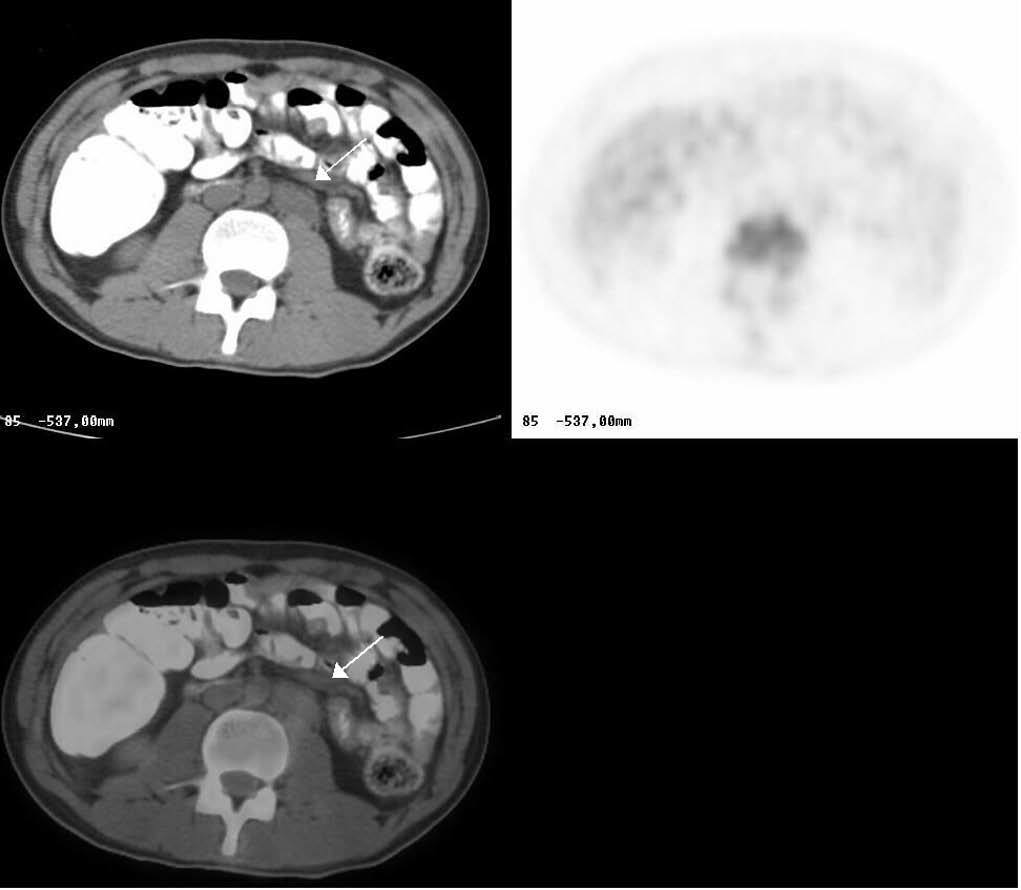
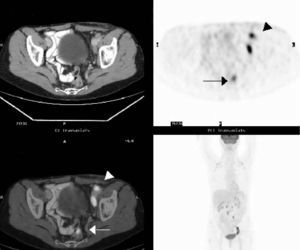
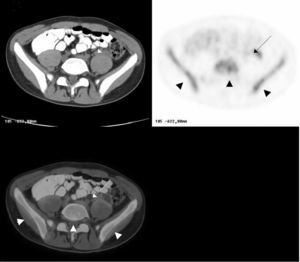
Fig. 7.--Estudio con tomografía por emisión de positrones-tomografía computarizada (PET/TC) de reevaluación postratamiento en una paciente de 47 años con carcinoma de ovario estadio IIIc. La PET (B y D) muestra captaciones que corresponden a adenopatías en cadena ilíaca externa izquierda (punta de flecha), así como otra captación patológica de radiotrazador en la pelvis (flecha), de difícil localización anatómica y sin clara visualización de la lesión en la TC (A). En la fusión PET/TC (C) esta captación de la 18FDG se localiza claramente en el sigma (flecha). Se confirman también las adenopatías en cadena ilíaca externa izquierda con captación patológica de radiotrazador (punta de flecha). En la colonoscopia se encontró un pólipo epitelial en el sigma.
Se ha evaluado la indicación clínica de restadificación y/o diferenciación entre cambios postratamiento de posible recidiva en los estudios de cáncer colorrectal en un 18,5% de las exploraciones. En el resto de la patología oncológica abdominal la distribución es la siguiente: el estudio de cáncer gástrico 1,9%, cáncer de esófago < 1%, cáncer de páncreas < 1%, hepatocarcinoma < 1%, cáncer de ovario < 1% (fig. 7), cáncer de testículo < 1%, sarcomas < 1% (figs. 8A y 8B). Los tumores cerebrales constituyen el 2,6%, y los tumores de cabeza-cuello representan el 5,5%, en las indicaciones clínicas de estadificación, reevaluación postratamiento y/o recidiva. El cáncer de tiroides constituye el 5%, el de mama el 4% y la búsqueda de tumor de origen desconocido el 4,3%. El estudio de epilepsia constituye el 1,4% y otras patologías el 8,6% de las exploraciones realizadas.
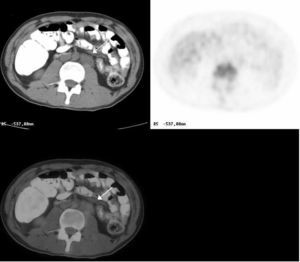
Fig. 8.--PET/TC en la evaluación del tratamiento de sarcoma. A: paciente diagnosticado de rabdomiosarcoma de epidídimo con respuesta parcial tras tratamiento con quimioterapia y radioterapia que es referido para evaluación pretrasplante autólogo de progenitores hematopoyéticos. Se observa persistencia, tras el tratamiento con quimiorradioterapia, de una masa retroperitoneal adyacente al psoas izquierdo con captación patológica del radiotrazador (flechas). La PET muestra un incremento moderado en la actividad de la 18FDG difuso y simétrico en la médula ósea de ambos huesos ilíacos y en el cuerpo vertebral (puntas de flecha) secundario a una hiperplasia de la médula hematopoyética postratamiento con quimioterapia y factor estimulante de las colonias granulocíticas. B: estudio PET/TC de reevaluación postrasplante del mismo paciente de la figura 8A que evidencia una buena evolución radiológica, con ausencia de captación de la 18FDG en la lesión, en relación a fibrosis residual (flecha).
Las edades de los pacientes varían entre 3 años y 80 años, aunque los pacientes pediátricos se han seleccionado muy cuidadosamente ya que a la complejidad multidisciplinar de la técnica hay que añadir la necesidad de anestesista pediátrico y una especial colaboración de los padres (fig. 9).
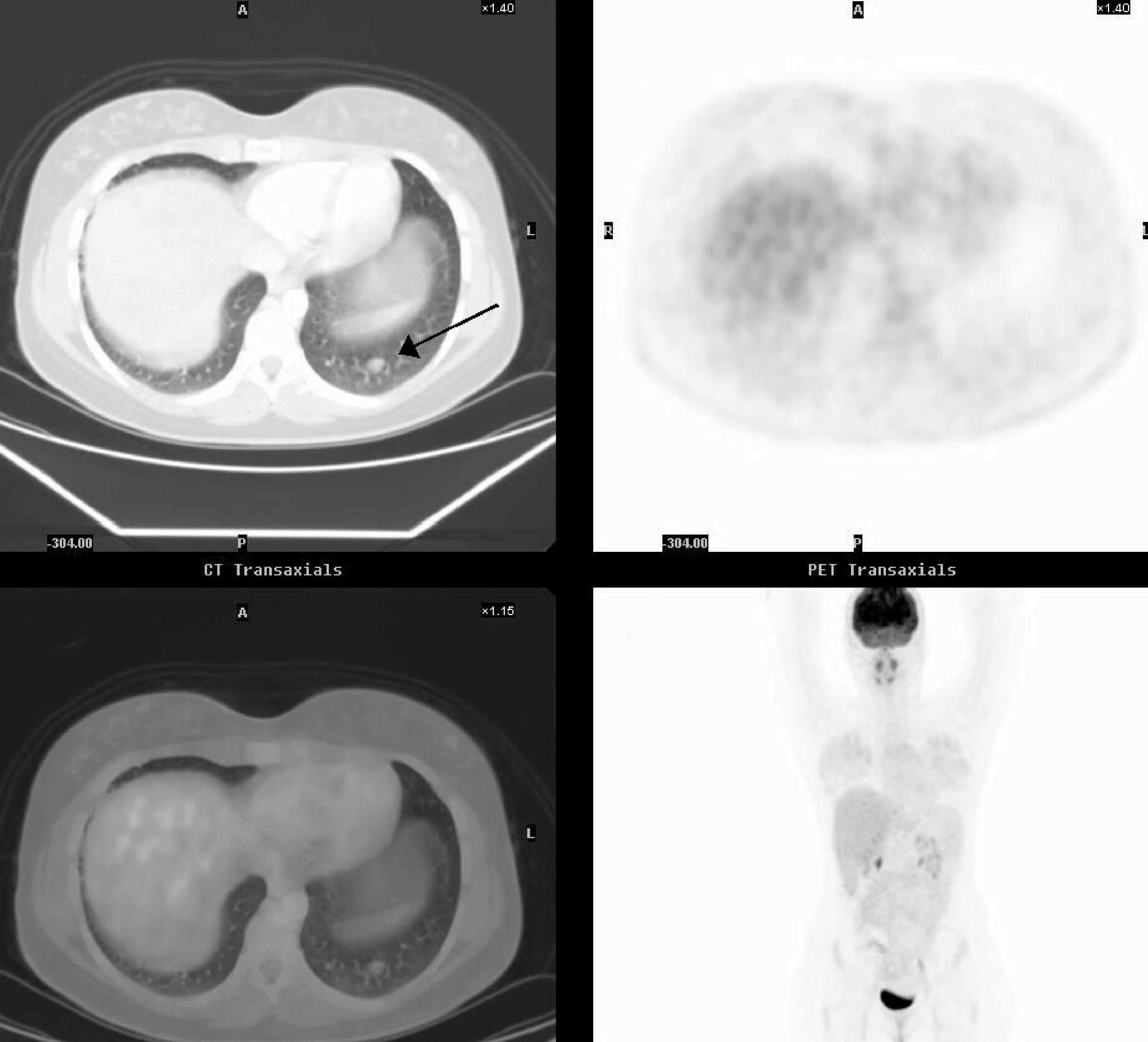
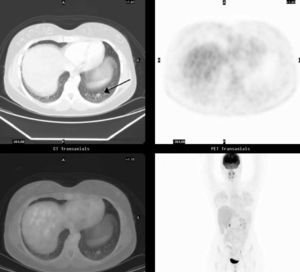
Fig. 9.--Trasplante hepático. Niña de 17 años receptora de un trasplante hepático cinco años antes como tratamiento de un hepatocarcinoma, referida para evaluación de nódulo pulmonar de reciente aparición en un control rutinario. A: la TC evidenció un nódulo pulmonar de menos de 1 cm en localización subpleural en el seno costodiafragmático izquierdo (flecha). B: la PET es negativa. Los nódulos menores de 1 cm y periféricos son una limitación de la PET. La cirugía demostró afectación metastásica.
DISCUSION
Los sistemas híbridos PET/TC integran en la misma maquina una TC y una PET situados en línea. Esto permite obtener simultáneamente información funcional y anatómica en una única exploración y sesión. La PET utiliza la inyección de moléculas marcadas con isótopos radiactivos emisores de positrones, proporcionando información metabólica. El proceso previo a la realización de la prueba diagnóstica consta de etapas sucesivas, como son: síntesis del isótopo radiactivo, síntesis del radio fármaco, transporte e inyección del mismo, reacción de los positrones con los electrones del organismo dando lugar a fotones de alta energía, adquisición de los datos tras la detección de dichos fotones, reconstrucción y fusión de las imágenes.
El primer prototipo dual PET/TC fue implantado en Pittsburg en abril de 1998 hasta agosto de 2001, cuando fue sustituido por el primer PET/TC comercial (Biograph, de Siemens Medical Solutions)2-5. Actualmente, se comercializan varios equipos híbridos Biograph Scanner (Siemens Medical Solutions), Discovery LS y ST (General Electric Medical Systems), Reveal (CTI), Gemeni (Phillips Medical Systems).Todos combinan los componentes de la PET ya sean cristales de ortosilicato de lutecio, germanato de bismuto y/o ortosilicato de gadolinio con una TC multidetector de 2, 4, 8 y de 16 coronas5-9. Existen dos tendencias de trabajo actualmente en revisión7. En EE.UU., el grupo de trabajo de Pittsburg, entre otros, inician el estudio con la TC con contraste intravenoso y posteriormente adquieren las imágenes de PET2,10.11. Otros autores adquieren TC de baja dosis primero, luego PET y posteriormente TC de alta dosis con contraste iv11-14. Es, al menos, curioso que en las publicaciones con el equipo de Biograph se realizan los estudios con la TC con contraste2,11. mientras que en las publicaciones con el Discovey se realizan con TC de baja dosis y sin contraste3.
La utilización de medios de contraste en esta técnica es controvertida debido a los potenciales aumentos artefactuales en la captación de 18-FDG que pueden producirse en diversos tejidos al realizar la corrección de la atenuación de la PET. Sin embargo, el contraste intravenoso y el contraste oral son necesarios a la hora de realizar la estadificación tumoral con TC. Los píxeles con contrastes se escalan incorrectamente a energías de 511 keV, por lo que pueden generar potenciales artefactos focales en las imágenes de PET corregidas. Los contrastes tienen un Z elevado, lo que resulta en un µ/* elevado a energías de Rx por absorción por efecto fotoeléctrico1515. Otra manera de obviar esto sería realizar dos TC, una de baja dosis y sin contraste, para la corrección de la atenuación y otra diagnóstico de alta dosis y con contraste iv, que es lo que hacemos nosotros en el marco exclusivo de la investigación. Algunas publicaciones afirman que el contraste intravenoso produce artefactos no significativos desde el punto de vista clínico a concentraciones normales en la imagen PET corregida10,12. En cuanto al contraste oral, como su rango de concentraciones es extenso y no controlable, puede generar sobrestimación a la hora de corregir la atenuación de los datos de emisión, si bien en algunos estudios también se ha visto que estos errores no son significativos en la práctica clínica diaria12,16,17. En nuestra experiencia personal no ha habido modificaciones en la fusión de la PET con el uso del contrate de la TC y sistemáticamente la fusión de las imágenes se realizan con la TC con contraste en los estudios de validación de la técnica. No obstante, la decisión técnica de realizar los estudios con o sin contraste deben estar basadas en la evidencia científica para reducir la variabilidad de la práctica clínica7.
En la práctica clínica diaria existen serios problemas en el trabajo y coordinación de todas las personas que trabajan en la unidad. Recientemente Wiley6 describe los problemas que nosotros hemos vivido desde hace dos años En este artículo de opinión se describen tres modelos de actuación con esta técnica. En la primera el estudio PET es interpretado por el médico nuclear con ayuda de la TC, pero solo se cobra la PET. En el segundo la PET se interpreta por un médico nuclear y la TC de calidad diagnóstica por el radiólogo y ambas técnicas se cobran. En ambos casos se realizan en el ámbito de hospitales universitarios. Sin embargo, en el sector puramente privado de la medicina americana sólo una persona interpreta las dos técnicas, ya que sus conocimientos son de ambas y por supuesto, se cobran las dos siendo la TC una TC diagnóstica (alta dosis). En nuestro centro hemos pasado por estas situaciones. Nuestra idea inicial fue crear una unidad de imagen PET/TC sin diferenciar especialistas de Medicina Nuclear y/o Radiología, pero surgieron problemas como la dependencia orgánica y funcional de los recursos humanos, el protagonismo de unos y otros que impidieron el trabajo en equipo, excluyendo a los radiofísicos y radiofarmacéuticos y la situación física del equipo (ubicada en el servicio de Medicina Nuclear). Además no disponíamos en el arranque inicial de referencias de otras unidades o experiencias previas, ni de la literatura. Aunque algunos de estos problemas persisten en la actualidad, intentamos resolverlos con el fin de optimizar la técnica y minimizar los protagonismos de unos y otros. Estamos aprendiendo de nuestros errores y, aunque esta opinión es personal y puede no ser compartida por muchos de los médicos nucleares y radiólogos de nuestro país, la técnica PET/TC es multidisciplinar, ya que es indiscutible que la PET es una técnica claramente de medicina nuclear, y la TC es una modalidad diagnóstica de Radiología. Ambas están validadas por separado, pero la modalidad híbrida PET/TC aún está siendo evaluada, hecho que se pone en evidencia en los informes de evaluación elaborados en las Agencias de Evaluación de Tecnologías Sanitarias. En España se han publicado dos revisiones sistemáticas8,18 y en Francia19 la revisión incluye una evaluación económica de la técnica. Tenemos una oportunidad en el sector académico única para validar la técnica híbrida si trabajamos en equipos multidisciplinares, como lo que estamos realizando con varios proyectos de investigación. Se ha publicado recientemente un estudio americano de los criterios de entrenamiento que deben cumplir aquellos profesionales que se dediquen a esta técnica donde intervienen el Colegio americano de radiología (ACR), la sociedad de TC, RM y de Medicina Nuclear7; nosotros en Europa y en España todavía ni lo planteamos.
De los estudios efectuados desde el 2003, 2.200 han sido realizados bajo la figura de uso tutelado y se realizan como PET con ayuda TC de baja dosis sin contraste intravenoso, para corregir la atenuación. Hasta ahora, para realizar una PET en la Comunidad de Madrid es necesaria la autorización por parte de la autoridad sanitaria, en un formulario donde consta el uso tutelado de la PET y donde está protocolizado que el paciente disponga de una TC previa. Esta situación no es acorde con la realidad de la técnica, en tanto que obliga a la previa realización de una TC para corregir la atenuación de la PET.
El resto de las exploraciones efectuadas, 259, se están realizando en el marco de proyectos de investigación que cuentan con financiación del fondo de investigación sanitaria y pretenden validar la técnica híbrida en varias indicaciones clínicas: linfomas, carcinoma no microcítico de pulmón, cabeza-cuello y metástasis de carcinoma de colon. En estos casos concretos todos los estudios TC se realizan en las mismas condiciones diagnósticas y con contraste intravenoso en las indicaciones ya apuntadas. En la actualidad ambos servicios Radiodiagnóstico y Medicina Nuclear, disponen de estación de trabajo que permite manipular los estudios y realizar los informes de forma más fluida. No obstante, se realiza un único informe PET/TC que facilita al clínico el manejo del paciente.
Las indicaciones clínicas aprobadas para la utilización de la técnica son similares entre las Comunidades Autónomas y también semejantes a las aceptadas por el Medicare20. Sin embargo, teniendo en cuenta el protocolo de uso tutelado de PET es necesario una TC previa a la realización de la PET, cuando utilizando la tecnología híbrida en una única sesión se obtienen las dos técnicas. La validación de la técnica híbrida PET/TC en grupos de pacientes con criterios de selección estrictos, en los que no se ha realizado una TC previa, para evaluar la exactitud diagnóstica de la PET/TC y su eficiencia en estas situaciones es una actividad claramente multidisciplinar. En breve ofreceremos resultados que aporten evidencia respecto a la efectividad y eficiencia de la PET/TC frente a la PET o la TC aisladamente, y por tanto, del impacto de esta tecnología en el manejo clínico y terapéutico de estos pacientes.