El síndrome de pseudotumor cerebral (SPTC) es una alteración caracterizada por el aumento de presión intracraneal que afecta predominantemente a mujeres jóvenes obesas. El objetivo del trabajo es definir los conceptos de SPTC primario, sin causa identificable y denominado también hipertensión intracraneal idiopática (HII), y de SPTC secundario, con etiología identificable. Se revisa el papel actual de las pruebas de imagen en su diagnóstico y los hallazgos por imagen típicos del SPTC, algunos de los cuales se incluyen entre los criterios diagnósticos propuestos en 2013. También se remarca el papel fundamental de la radiología intervencionista en el tratamiento, puesto que la colocación de stent en las estenosis de senos venosos constituye una alternativa terapéutica novedosa en pacientes resistentes al tratamiento clásico. Por último, se describen aquellos biomarcadores de imagen que han sido evaluados para aproximar el diagnóstico de la HII y predecir la respuesta al tratamiento.
Pseudotumor cerebri is a disorder characterized by increased intracranial pressure that predominantly affects obese young women. This paper aims to define the concepts of primary pseudotumor cerebri, in which the cause cannot be identified (also known as idiopathic intracranial hypertension), and secondary pseudotumor cerebri, in which the cause can be identified. We review the current role of imaging techniques in diagnosing pseudotumor cerebri and describe and illustrate the most characteristic imaging findings of the disorder, some of which are included in the diagnostic criteria proposed in 2013. We also consider the fundamental role of interventional radiology in the treatment of pseudotumor cerebri because placing a stent in stenosed venous sinuses is a novel treatment option in patients who are refractory to classical treatment. Finally, we describe the imaging biomarkers that have been evaluated for diagnosing primary pseudotumor cerebri and predicting the response to treatment.
El síndrome de pseudotumor cerebral (SPTC) consiste en el conjunto de signos y síntomas derivados del aumento de presión intracraneal (PIC) en ausencia de lesiones focales, hidrocefalia, infección o malignidad subyacente. En los casos en los que no se logra identificar la etiología se denomina hipertensión intracraneal idiopática (HII)1. Este cuadro afecta predominantemente a mujeres obesas en edad reproductiva. Su fisiopatología es compleja y multifactorial; una de las probables causas es la alteración en la homeostasis del líquido cefalorraquídeo (LCR). Las pruebas de imagen son fundamentales en el diagnóstico al permitir descartar causas de aumento de la PIC y porque algunos hallazgos por imagen se incluyen entre los criterios diagnósticos del SPTC propuestos en 20132. Asimismo, la neurorradiología tiene un papel importante en el tratamiento del SPTC, puesto que el abordaje intravascular por vía percutánea de la estenosis de senos venosos transversos mediante angioplastia y colocación de stent constituye una alternativa terapéutica novedosa en pacientes resistentes al tratamiento clásico3. Finalmente, se han propuesto diversos biomarcadores de imagen para diagnosticar la HII y para cuantificar la respuesta al tratamiento.
El objetivo de este artículo es revisar el estado actual del conocimiento respecto al SPTC, remarcando los hallazgos por imagen aceptados actualmente como signos de HII y describir el papel de la neurorradiología intervencionista en el tratamiento.
DefiniciónEl SPTC es un síndrome definido por signos y síntomas derivados del aumento de la PIC en ausencia de lesiones focales u otras causas identificables.
Previamente denominado hipertensión intracraneal benigna, en la actualidad se debe evitar esta nomenclatura ya que entre un 1% y un 2% de los pacientes evolucionará a ceguera durante el primer año del diagnóstico y hasta el 24% de pacientes presenta pérdida de visión permanente4. Actualmente, los términos utilizados son hipertensión intracraneal idiopática o pseudotumor cerebral. En 2013 se propuso la nueva terminología, SPTC, distinguiendo SPTC primario, sin causa identificable y también denominado HII, y SPTC secundario, con etiología identificable1.
Criterios diagnósticos en el síndrome de pseudotumor cerebralLos criterios diagnósticos del SPTC han evolucionado desde los primeros hallazgos clínicos descritos por Dandy en 1937 hasta los últimos criterios propuestos por Friedman et al. en 20131. El papel fundamental de las pruebas de imagen es descartar causas identificables de hipertensión intracraneal. No obstante, los hallazgos radiológicos se incluyen entre los últimos criterios diagnósticos propuestos. En ausencia de papiledema y parálisis del VI par podemos sugerir el diagnóstico de HII sumando los hallazgos por imagen a los criterios clínicos1 (tabla 1).
Criterios diagnósticos del pseudotumor cerebrala
| Requerido para el diagnóstico de pseudotumor cerebral |
| A. Papiledema |
| B. Examen neurológico normal (a excepción de alteraciones en pares craneales) |
| C. Neuroimagen: parénquima cerebral normal sin evidencia de hidrocefalia, masas, lesiones estructurales ni realces meníngeos en RM sin y con gadolinio en pacientes típicos (mujeres obesas), y en RM sin y con gadolinio con estudio venográfico en el resto; si no existe posibilidad de RM o está contraindicada, puede utilizarse la TC con contraste |
| D. Composición normal del LCR |
| E. Aumento de presión de apertura en la punción lumbar (≥250 mm H2O en adultos y ≥280 mm H2O en niños; 250 mm H2O si el niño no está sedado ni es obeso) |
| Diagnóstico del pseudotumor cerebral sin papiledema |
| En ausencia de papiledema: es posible realizar el diagnóstico de SPTC si se cumplen criterios B-E y se asocian a parálisis uni/bilateral de VI par craneal |
| En ausencia de papiledema y parálisis VI par: el diagnóstico de SPTC puede sugerirse, pero no realizarse, si se cumplen los criterios B-E y están presentes al menos 3 hallazgos de los siguientes en el estudio de imagen: |
| I. Silla turca vacía |
| II. Aplanamiento de la esclera posterior del globo ocular |
| III. Distensión del espacio subaracnoideo perióptico (con o sin tortuosidad del nervio óptico) |
| IV. Estenosis de senos venosos transversos |
SPTC: pseudotumor cerebral. LCR: líquido cefalorraquídeo.
El diagnóstico es definitivo si el paciente cumple los criterios A-E.
El diagnóstico es probable si cumple los criterios A-D, pero la presión de LCR medida es menor que la especificada para el diagnóstico definitivo.
La fisiopatología de este síndrome es multifactorial y no bien definida. La mayoría de teorías actuales se centran en la alteración en la homeostasis del LCR por aumento de resistencia a la salida/reabsorción del mismo y en la alteración de la hemodinámica venosa4.
La absorción de LCR depende del gradiente de presiones entre el sistema venoso y el espacio subaracnoideo, de modo que el aumento de presión venosa encefálica requiere del aumento de presión del LCR para mantener la tasa de absorción4. La hipótesis de la alteración hemodinámica venosa se apoya en que la trombosis de senos venosos durales produce clínica y signos similares a los identificados en pacientes con HII5.
Otros factores propuestos son el aumento de volumen cerebral, el aumento de presión arterial cerebral transmitida a capilares o el aumento de producción de LCR.
El SPTC primario se relaciona con otros factores como la obesidad y la ganancia ponderal reciente; aproximadamente el 70% de pacientes con HII son obesos y el 90% presentan sobrepeso6. Por su parte, el SPTC secundario se ha relacionado con causas identificables y factores agravantes: alteraciones venosas y/o cerebrales (trombosis de senos venosos o de venas yugulares y sobrecarga cardiaca derecha), fármacos (antibióticos como las tetraciclinas, vitamina A y retinoides), anemia o alteraciones endocrinológicas (Addison, hipoparatiroidismo)1.
EpidemiologíaEl concepto de paciente típico se ha acuñado en la HII, ya que más de un 90% de las personas afectadas son mujeres en edad reproductiva obesas o con ganancia ponderal rápida reciente4. La incidencia es de 12-20 casos/100.000 personas en este grupo, mientras que en la población general es de 1-2/100.000 personas4.
Menos frecuentemente, el SPTC puede afectar a personas delgadas, niños, varones o ancianos1,7. Se identifican menores tasas de obesidad en pacientes pediátricos con HII, de modo que, si bien el síndrome es más frecuente en adolescentes con sobrepeso, este no constituye un factor de riesgo en menores de 10 años7. Asimismo, no existe diferencia entre géneros en edad prepuberal8. De los adultos afectados, menos del 10% son hombres, típicamente obesos y con un pronóstico visual peor que el de las mujeres9.
ClínicaClásicamente, el diagnóstico de HII se considera ante la tríada de cefalea, cambios visuales y papiledema10.
El síntoma más frecuente es la cefalea, más del 90% de los pacientes la padecen, descrita generalmente como opresiva y manifestada al despertar. Otros pacientes refieren migraña pulsátil2.
Las alteraciones visuales transitorias, concretamente la pérdida de visión de menos de 60 segundos de duración o tras provocación postural, constituyen el segundo síntoma más frecuente, descrito en el 70% de los pacientes2. La pérdida de visión permanente es la complicación más grave en la HII, y en casos fulminantes puede tener lugar en un periodo inferior a un mes desde el inicio de los síntomas11. Otras alteraciones visuales descritas son reducción de la agudeza o del campo visual y diplopía por parálisis del VI par craneal10.
Hasta el 95% de pacientes pueden presentar papiledema, que puede conllevar pérdida permanente de la visión hasta en el 1-2% de pacientes sin tratamiento precoz4.
Otros síntomas referidos con frecuencia son tinnitus pulsátil, dolores de cuello o espalda, náuseas o vómitos11.
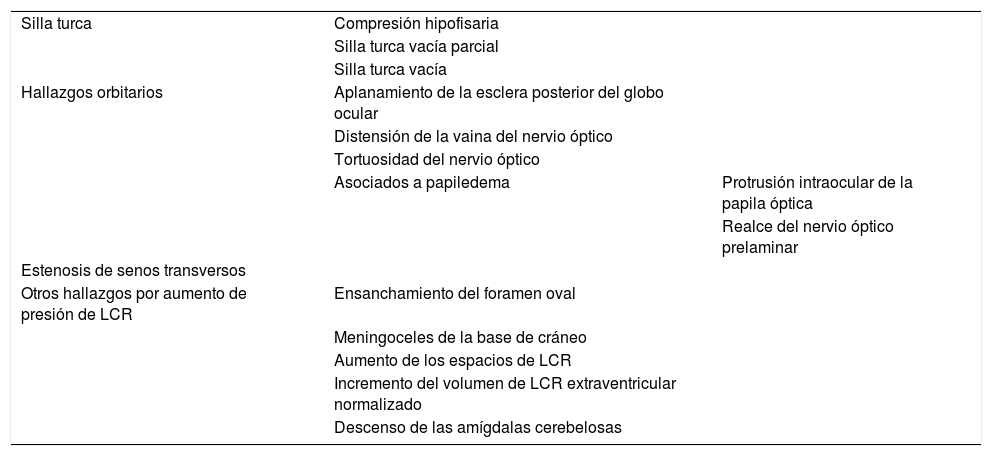
Hallazgos radiológicos en el síndrome de pseudotumor cerebralEl papel principal de las pruebas de imagen en la HII es excluir patologías que causen hipertensión intracraneal. Sin embargo, diversos hallazgos radiológicos han sido descritos en la HII con los avances de la neuroimagen, y algunos de ellos han sido aceptados como criterios diagnósticos, como se ha visto anteriormente. Los hallazgos radiológicos en el SPTC se caracterizan principalmente por su alta especificidad (>90%) y sensibilidad baja (tabla 2).
Resumen de los hallazgos radiológicos en el síndrome de pseudotumor cerebral
| Silla turca | Compresión hipofisaria | |
| Silla turca vacía parcial | ||
| Silla turca vacía | ||
| Hallazgos orbitarios | Aplanamiento de la esclera posterior del globo ocular | |
| Distensión de la vaina del nervio óptico | ||
| Tortuosidad del nervio óptico | ||
| Asociados a papiledema | Protrusión intraocular de la papila óptica | |
| Realce del nervio óptico prelaminar | ||
| Estenosis de senos transversos | ||
| Otros hallazgos por aumento de presión de LCR | Ensanchamiento del foramen oval | |
| Meningoceles de la base de cráneo | ||
| Aumento de los espacios de LCR | ||
| Incremento del volumen de LCR extraventricular normalizado | ||
| Descenso de las amígdalas cerebelosas |
LCR: líquido cefalorraquídeo.
Se trata de uno de los signos más prevalentes, hasta el 80%, con una especificidad aproximada del 70% y bajo valor en caso de ser un hallazgo aislado, ya que es frecuente en la población general12.
Este hallazgo radiológico es secundario a la pulsatilidad prolongada del LCR a alta presión que rellena la silla turca y produce un aracnoidocele a través del diafragma selar13. Algunos estudios morfométricos sugieren que el aumento y remodelación de la silla turca es la causa de la apariencia de silla vacía14.
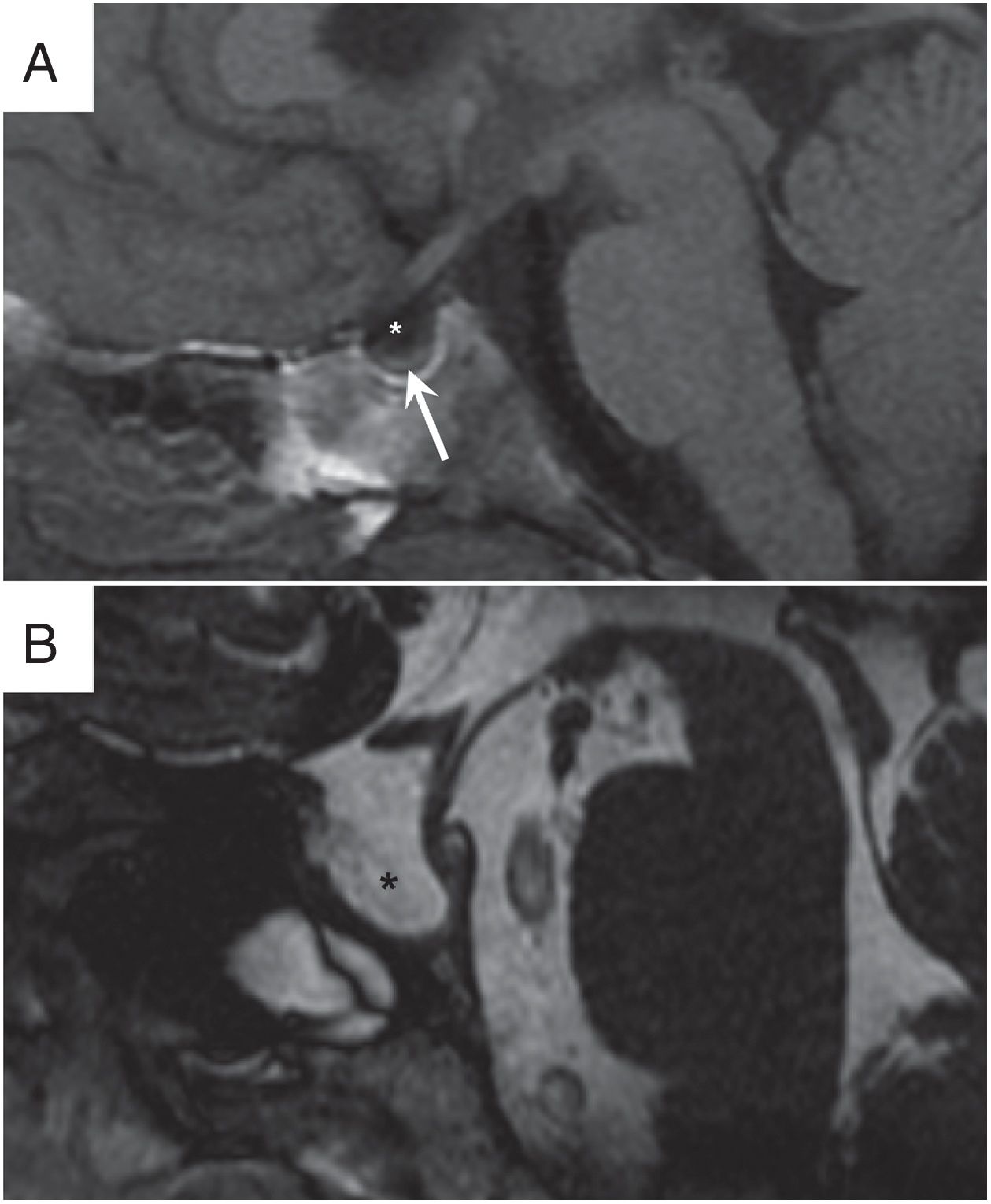
Puede verse, en grados variables, en cortes sagitales de resonancia magnética (RM) en línea media. Se considera silla turca vacía si se encuentra completamente llena de LCR sin glándula hipofisaria visible, y silla turca vacía parcial cuando la mayoría se rellena de LCR y la glándula es adelgazada en su base (fig. 1)12,15.
Hallazgos radiológicos en la silla turca. A) Silla turca parcialmente vacía, observada en secuencia T1 TSE sagital. Se observan las características típicas con la silla turca rellena casi completamente de líquido cefalorraquídeo (LCR) (*) y el adelgazamiento de la glándula hipofisaria (flecha). B) Silla turca vacía visualizada en secuencia T2 TSE sagital. Se identifica la silla turca remodelada y expandida completamente rellena por LCR (*) sin glándula hipofisaria visible.
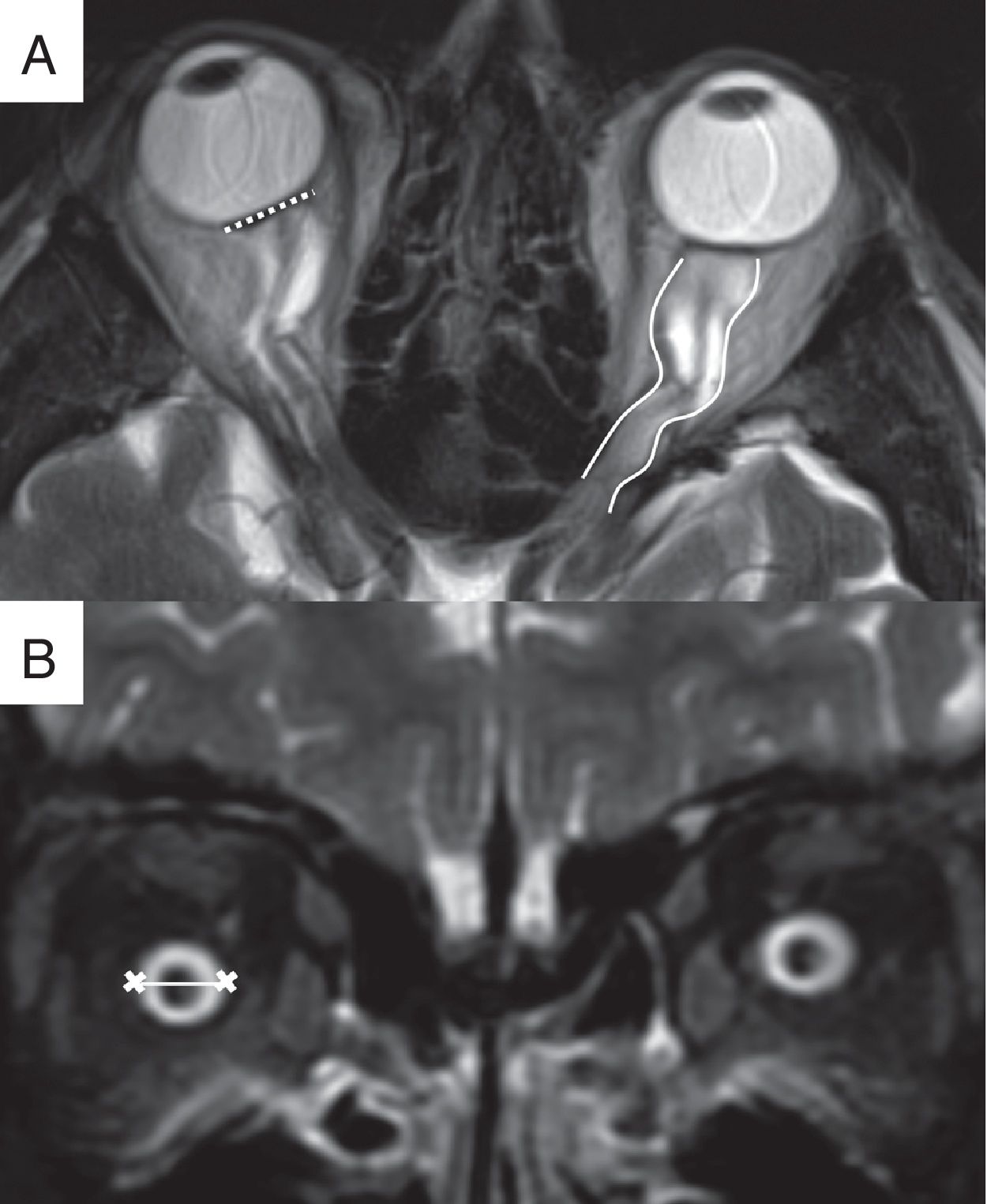
Se trata de un signo muy prevalente, con una sensibilidad variable y una especificidad cercana al 100% (fig. 2)13,16. La determinación de la presencia y el grado de alteración del globo ocular presentan marcada variabilidad interobservador, por lo que la cuantificación automatizada de la distorsión del globo ocular ha sido propuesta para mejorar la precisión diagnóstica17.
Hallazgos orbitarios. A) Imagen de resonancia magnética (RM), secuencia T2 FSE en el plano transversal, en la que se visualiza la distorsión de la morfología normal del globo ocular con aplanamiento de la esclera posterior bilateral (línea discontinua) así como la tortuosidad de los nervios ópticos en el plano horizontal (líneas continuas). B) Imagen de RM, secuencia STIR en el plano coronal, que demuestra la distensión de la vaina del nervio óptico tras el globo ocular (línea).
Mediante RM, las secuencias T2 con saturación de la grasa permiten evaluar correctamente la vaina del nervio óptico (NO) en la órbita18. En pacientes con papiledema se identifica un diámetro medio de la vaina del NO, medida tras el globo ocular, mayor que en pacientes sanos (7,54±1,05 mm frente a 5,52±1,11 mm respectivamente) (fig. 2)19,20. Este hallazgo presenta una sensibilidad del 45-66,7% y una especificidad del 82,1-95%, siendo la prevalencia del 65%14,21.
Tortuosidad del nervio ópticoEn la HII, la fijación del NO al anillo de Zinn y la esclera posterior del globo ocular producen elongación y tortuosidad intraorbitaria del NO. El desplazamiento puede producirse en el plano vertical o en el plano horizontal del nervio. La visualización de tortuosidad del NO en el plano vertical tiene mayor especificidad que en horizontal (fig. 2)18. Este hallazgo presenta una sensibilidad del 40% y una especificidad del 91%21.
Hallazgos orbitarios asociados al papiledemaEl papiledema se caracteriza en el fondo de ojo por la elevación del disco óptico, el borramiento de sus márgenes, la presencia de un halo peripapilar o la distensión venosa, entre otros hallazgos. Puede ser asimétrico o unilateral18.
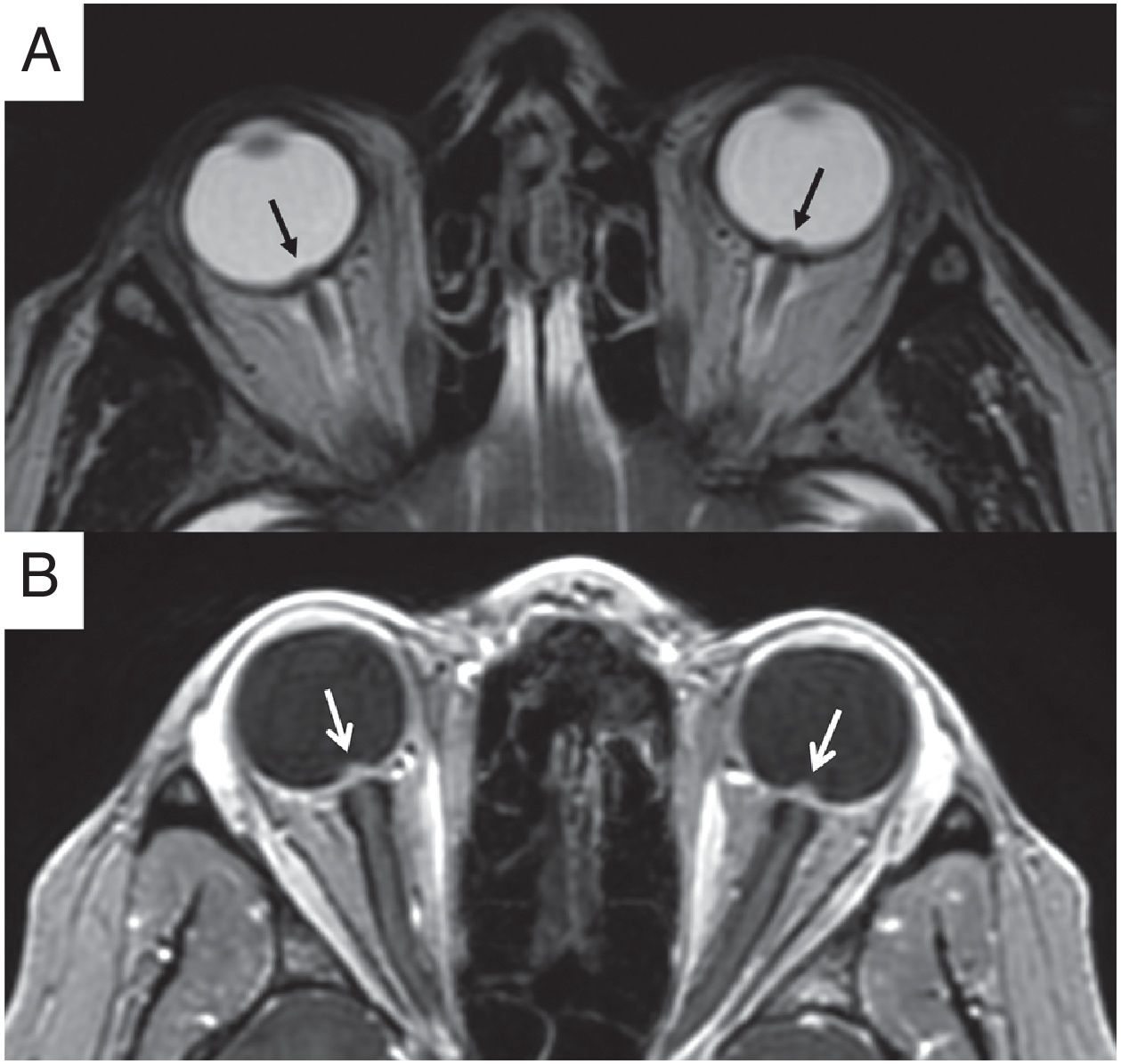
Protrusión intraocular de la papila ópticaSe ha observado protrusión de la papila óptica hasta en el 67% de pacientes con SPTC (fig. 3)22. Tiene un valor predictivo positivo elevado para valorar el papiledema y el grado clínico de este17.
Hallazgos orbitarios asociados al papiledema. A) Imagen de resonancia magnética (RM), secuencia T2 FSE en el plano transversal. Se identifica la protrusión intraocular bilateral de la papila óptica (flechas negras). B) Mismo paciente que en la imagen A. La imagen de RM, secuencia T1 gradiente 3D transversal con saturación de la grasa tras administrar contraste intravenoso, demuestra el realce bilateral y simétrico en la región prelaminar de los nervios ópticos (flechas blancas).
La región prelaminar del NO es una parte de la porción intraocular de la cabeza del nervio irrigada por el sistema vascular de la coroides. Su realce tras la administración de contraste en la RM presenta una sensibilidad baja (50%) con una especificidad del 100% (fig. 3). Se ha postulado que el realce se debe a la dificultad de flujo con estasis venoso del sistema coroideo por la protrusión papilar intraocular. No obstante, en muchos pacientes con HII y papiledema marcado, el realce prelaminar no se logra identificar13.
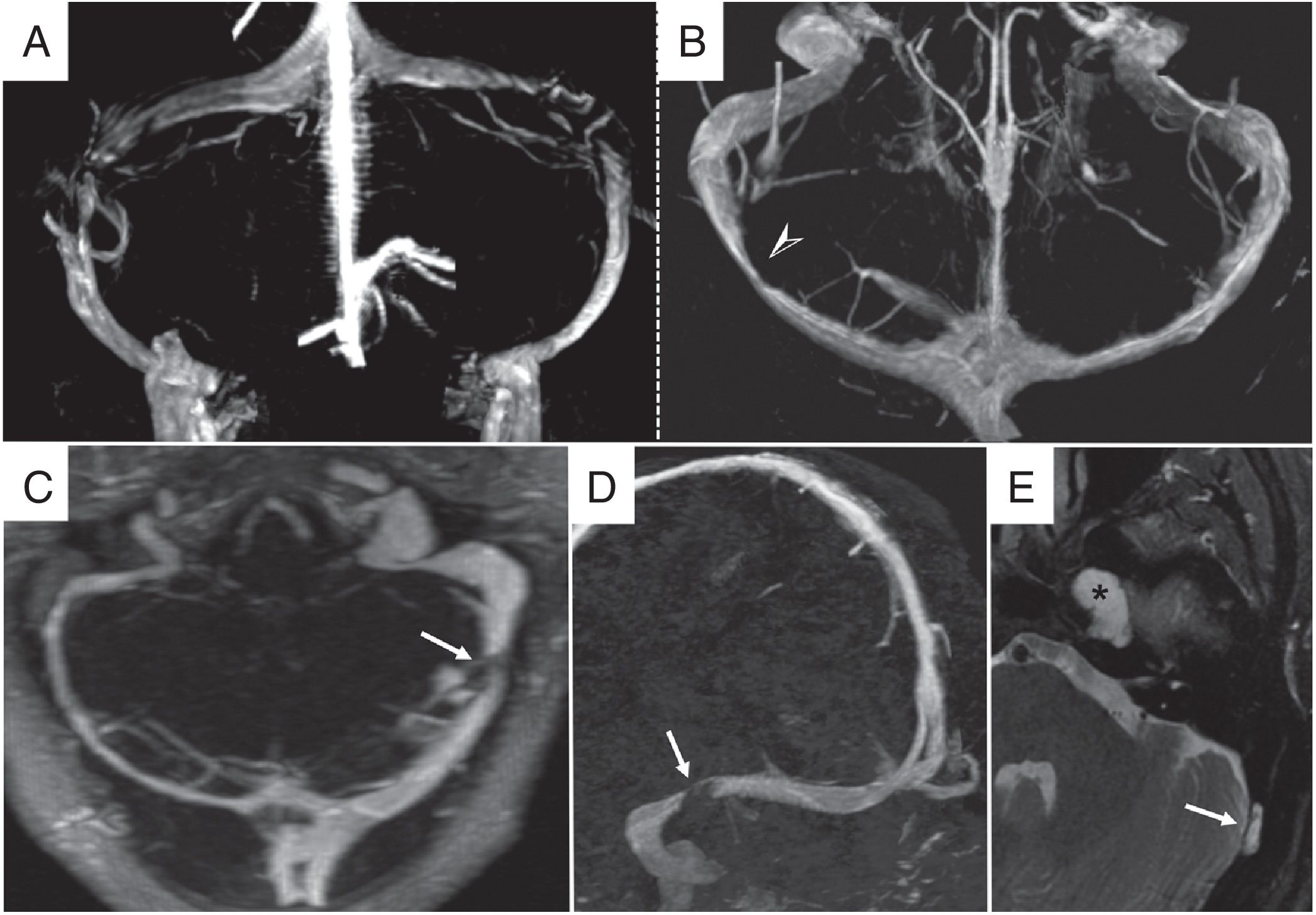
Estenosis de senos transversosLa estenosis de senos transversos presenta una prevalencia de hasta el 90% en pacientes con HII5. La localización más frecuente es en la región distal de los senos transversos o en su unión con los senos venosos sigmoides, de manera uni- o bilateral (fig. 4)23,24.
Estenosis de senos venosos transversos. Angio-RM venosa con contraste, reconstrucciones volumétricas 3D coronal (A) y transversal (B). A y B) Estenosis venosa extrínseca. A: estenosis bilateral típica en la región distal de los senos transversos. B: estenosis unilateral en el tercio medio del seno transverso derecho. C-E) Estenosis venosa intrínseca por granulación aracnoidea. C: angio-RM venosa con contraste con reconstrucción de máxima intensidad de proyección (MIP) en plano transversal en la que se visualiza hipoplasia del seno venoso transverso derecho y pequeño segmento estenótico significativo en tercio distal de seno transverso izquierdo. D: reconstrucción MIP en plano parasagital que demuestra los bordes bien delimitados de la estenosis (flecha blanca). E: secuencia STIR transversal en la que se identifica una granulación aracnoidea como causa de la estenosis (flecha blanca). Obsérvese también un meningocele del cavum de Meckel (asterisco) asociado a la HII.
La venografía por RM con contraste y técnica ATECO (Auto-Triggered Elliptic Centric-Ordered imaging) disminuye la pérdida de señal por artefactos con respecto a la técnica usada clásicamente (time-of-flight, venografía por RM) y permite una mejor detección de la estenosis de senos venosos, con una sensibilidad y especificidad del 93%5. Las estenosis de senos venosos pueden ser intrínsecas o extrínsecas.
Estenosis intrínseca de senos transversosSe han descrito alteraciones en los senos venosos que causan defectos focales en el relleno intraluminal, producen estenosis intrínseca y podrían contribuir a la producción de hipertensión intracraneal. Estas alteraciones incluyen septos, granulaciones aracnoideas y proyecciones de la matriz aracnoidea y el espacio subaracnoideo en la pared de los senos venosos durales24. Las granulaciones aracnoideas han sido descritas en un 24% de las tomografías computarizadas (TC) y en un 13% de los estudios de RM con contraste en poblaciones normales y aumentan en número con la edad. Frecuentemente se observan en los senos transversos y sigmoideos24,25.
Estenosis extrínseca de senos transversosSe trata de una estenosis de la luz de los senos venosos por compresión secundaria al aumento de PIC, que produce un “estado de colapso venoso automantenido”2. Este estado es considerado causa y consecuencia del aumento de PIC. El LCR se reabsorbe de forma pasiva a través de los espacios perivenulares y en las granulaciones aracnoideas hacia los senos venosos intracraneales. Una estenosis en un seno transverso dominante o una estenosis bilateral pueden dificultar el drenaje venoso y producir hipertensión venosa. Esta hipertensión dificulta y reduce la absorción de LCR causando aumento de la PIC y mayor compresión aún de los senos venosos2,3,26.
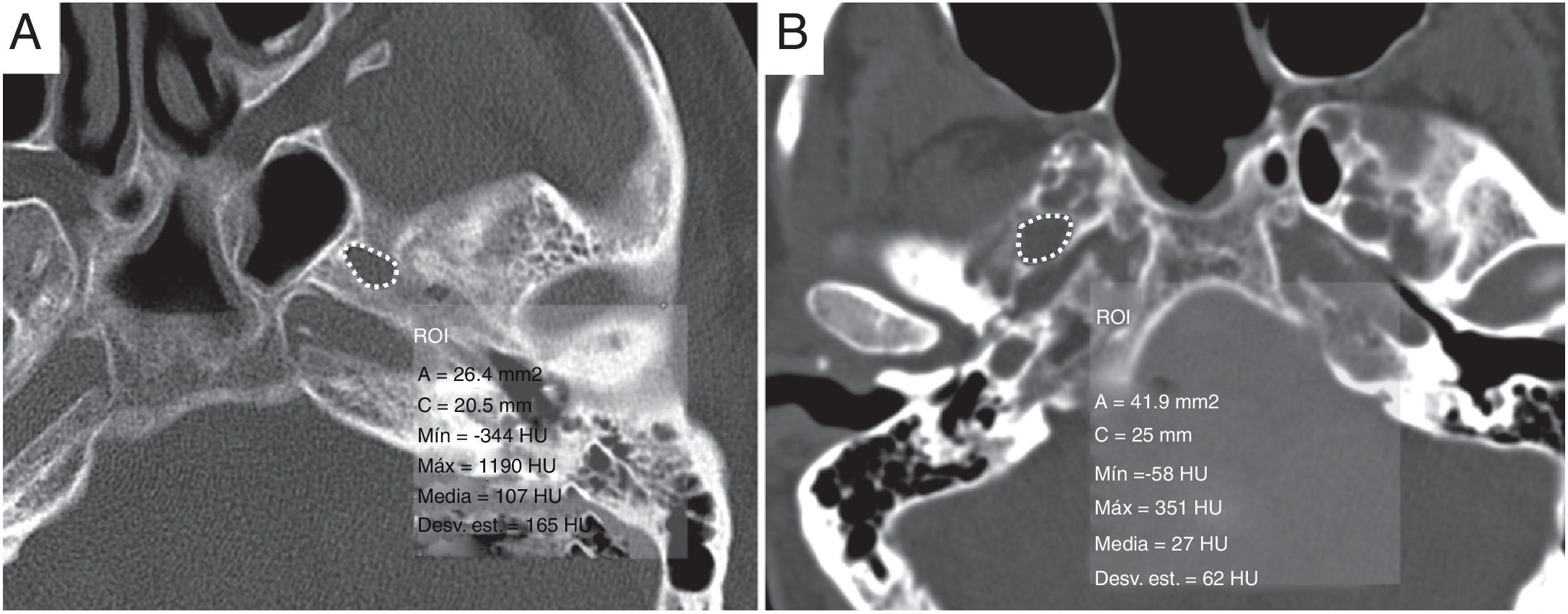
Otros hallazgos radiológicos asociados a aumento de presión del LCREnsanchamiento del foramen ovalLa presión de LCR elevada crónicamente puede producir remodelación y erosión ósea, hallazgo que se evidencia en el ensanchamiento del foramen oval (FO). El área media de este es mayor en pacientes con HII (fig. 5). Para un valor de corte de 30 mm2, la sensibilidad del área del FO para detectar HII es del 50%, con una especificidad del 81%. Para un valor de corte de 40 mm2, la especificidad y el valor predictivo positivo son del 100%15.
Aumento del área del foramen oval. A) Área del foramen oval en tomografía computarizada de cabeza sin contraste en paciente sano, con valor de 26,4 mm2. Compárese con un paciente con hipertensión intracraneal idiopática (B) en el que el área media del foramen oval es de 41,9 mm2, mayor de 40 mm2.
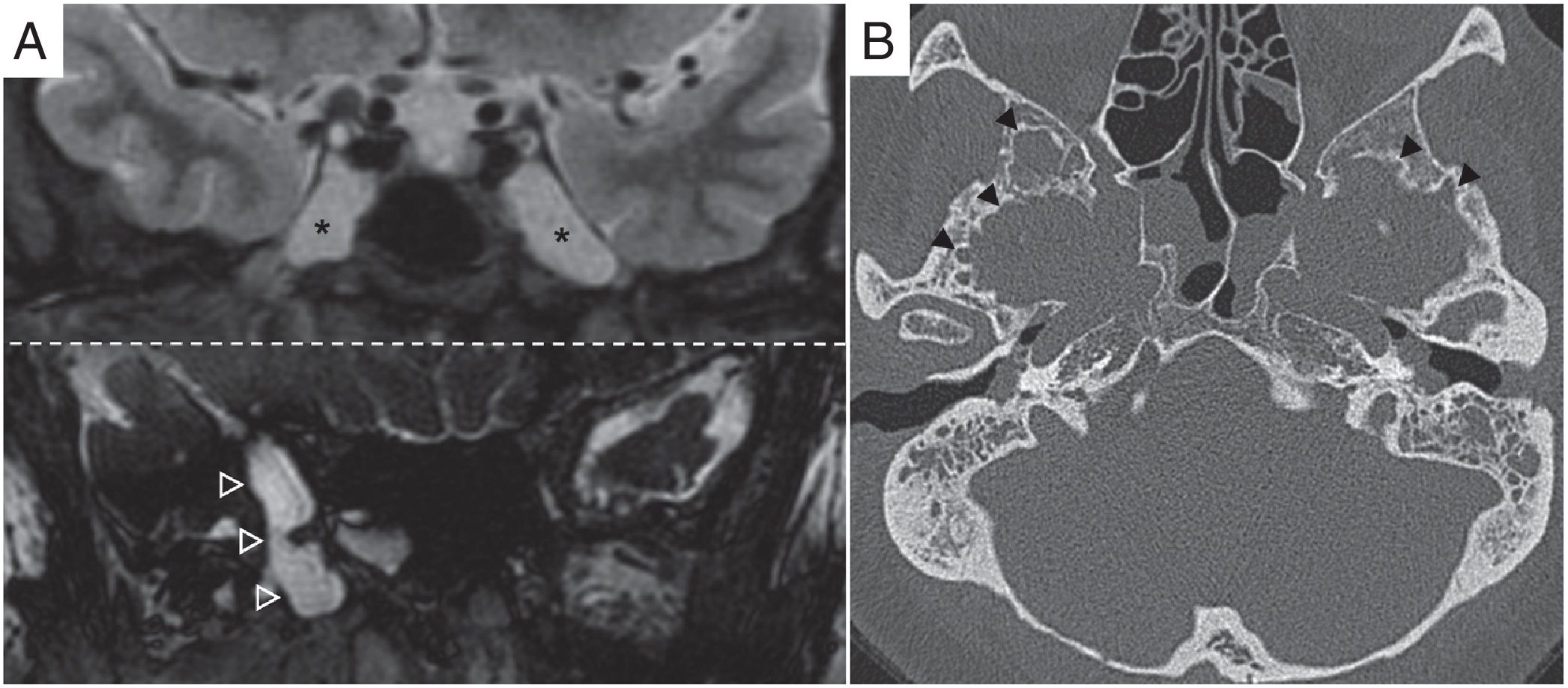
Pueden representar un signo adicional por imagen de la HII27. En el 11% de pacientes con HII se han identificado meningoceles en el cavum de Meckel o en el ápex petroso, y en un 9%, aumento del diámetro del cavum de Meckel (fig. 6)28. También se han descrito granulaciones aracnoideas intraóseas en el resto de la base de cráneo, predominantemente en las alas esfenoidales29. A través de las erosiones óseas y los defectos osteodurales pueden producirse fugas de LCR a oído medio o senos paranasales12.
Meningoceles y granulaciones aracnoideas en la base del cráneo. A) Secuencias STIR coronal y FIESTA (fast imaging employing steady-state) coronal en las que se identifica meningoceles del cavum de Meckel (asteriscos) y meningocele localizado en la zona medial del ala mayor derecha del esfenoides (puntas de flecha huecas). B) tomografía computarizada de peñascos, imagen transversal, donde se visualizan múltiples defectos óseos que afectan a la tabla interna de ambas alas esfenoidales correspondientes a granulaciones aracnoideas intraóseas (puntas de flecha negras).
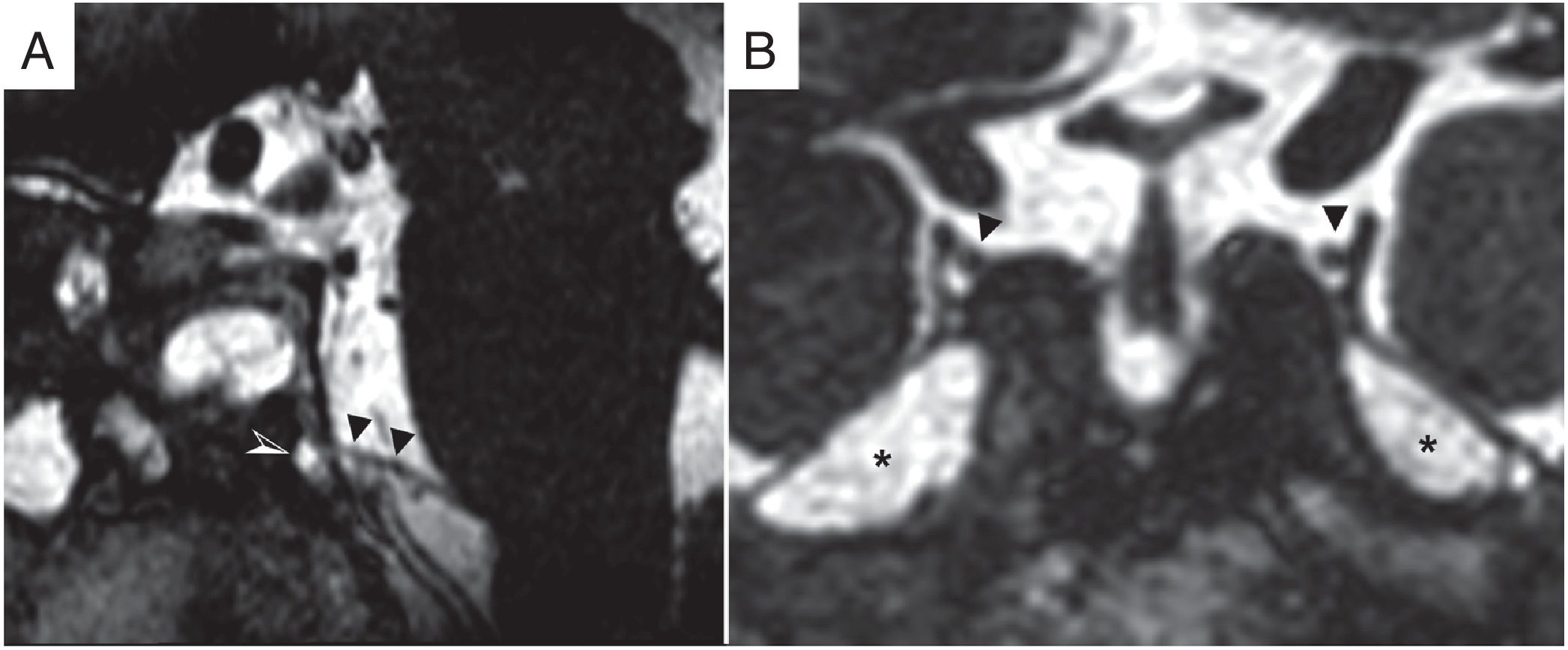
Se ha documentado el aumento bilateral y simétrico de los espacios de LCR alrededor de los nervios del III par en la pared lateral del espacio lateroselar o en la entrada del canal de Dorello del VI par (fig. 7)27. Son necesarios más estudios que evalúen su valor diagnóstico real.
Aumento de los espacios de líquido cefalorraquídeo (LCR). A) Secuencia balanceada fast imaging employing steady-state (FIESTA) en el plano sagital de un paciente con HII. Se demuestra el relleno por LCR del canal dural del VI par (canal de Dorello) (punta de flecha blanca y negra). B) Imagen coronal de secuencia FIESTA con un aumento bilateral y simétrico de los espacios de LCR (asteriscos) alrededor de los canales durales del III par (puntas de flecha negra) en la pared lateral del espacio lateroselar. Se identifican también meningocele del cavum de Meckel (asteriscos) asociados a la HII.
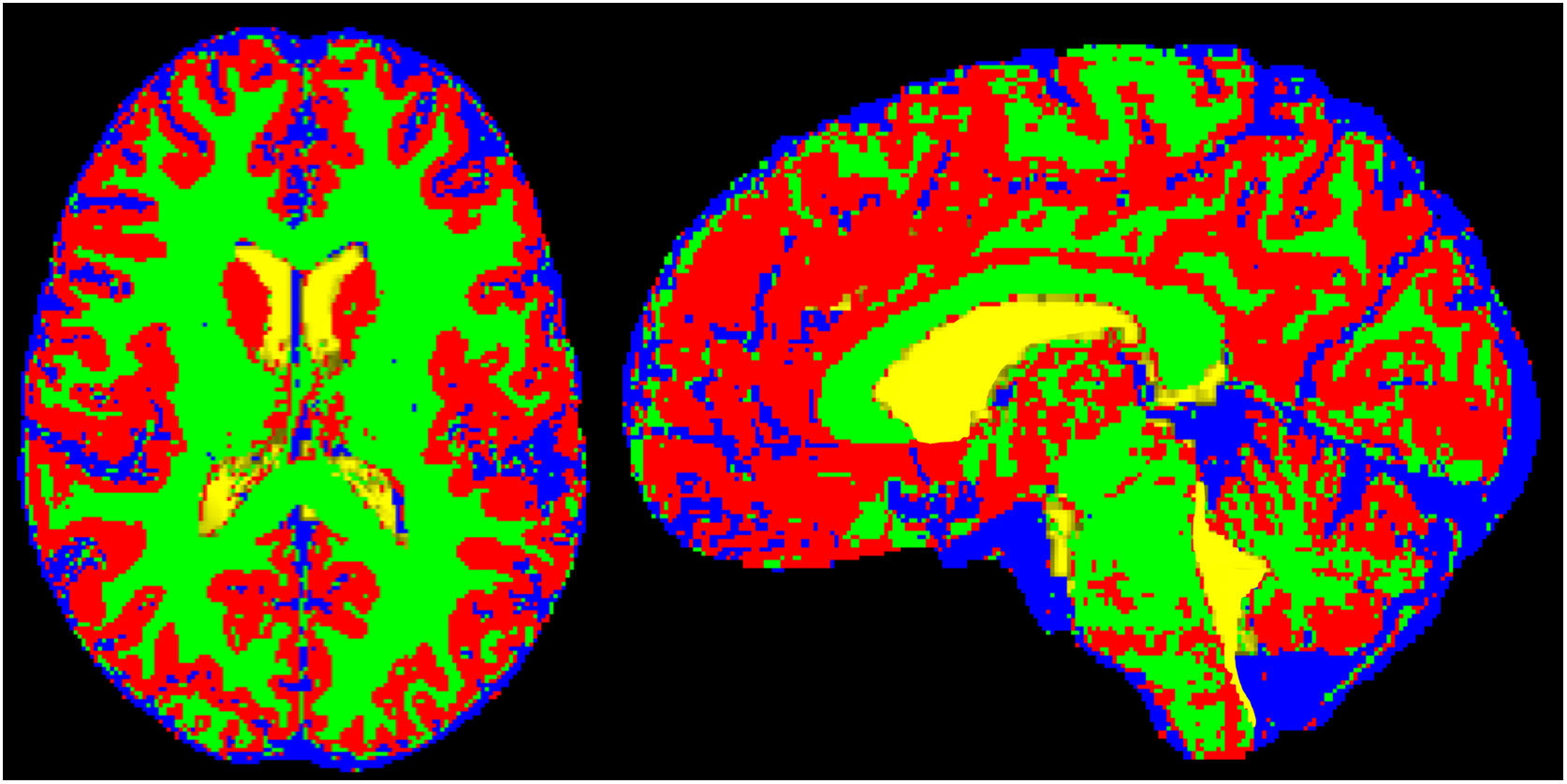
La cuantificación del volumen de LCR intracraneal extraventricular ha sido propuesta como un hallazgo útil para establecer el diagnóstico de HII (fig. 8). Alperin et al. han identificado el aumento de este volumen normalizado respecto al volumen total intracraneal, con un punto de corte de más del 18%, como un hallazgo radiológico que presenta una sensibilidad del 73% y una especificidad del 100%30.
Incremento del volumen de líquido cefalorraquídeo (LCR) extraventricular normalizado. Ejemplo de segmentación semiautomática de LCR extraventricular intracraneal en el que se demuestra la diferenciación del LCR intraventricular (en amarillo) del LCR extraventricular (azul). Sustancia gris y sustancia blanca segmentadas y diferenciadas en otros colores (rojo y verde, respectivamente).
El descenso o ectopia de las amígdalas cerebelosas a través del foramen magno, definido como un descenso mayor de 5 mm, tiene una incidencia significativa de entre el 10% y el 21% en pacientes con HII. Ante este hallazgo radiológico y en un contexto clínico adecuado, deben evaluarse otros signos radiológicos de HII para descartar entidades caracterizadas por descenso de amígdalas cerebelosas, sobre todo la malformación de Chiari 1 (además existe evidencia científica de coexistencia entre esta y la HII) y el síndrome de hipotensión intracraneal31.
Biomarcadores de imagenSe han descrito diversos biomarcadores de imagen para diagnosticar la HII y tratar de predecir la respuesta al tratamiento. La mayoría de los estudios analizan marcadores que establezcan de manera categórica la presencia o no de HII, como el área aumentada de la silla turca14,32, el área aumentada del foramen oval15 y el aumento del LCR extraventricular28,33. Diversos estudios abogan por la automatización de las medidas, como por ejemplo la elaboración de mapas de distancia del globo ocular para medir el aplanamiento de la esclera posterior17 o la valoración cuantitativa semiautomática en la venografía por RM del grado de estenosis de senos transversos34. Sin embargo, las publicaciones realizadas hasta la fecha presentan niveles de evidencia científica bajos y los biomarcadores de imagen propuestos no se han mostrado clínicamente útiles ni han sido validados. También se han evaluado los cambios por imagen tras tratamiento (acetazolamida o punción lumbar) en tres de los biomarcadores propuestos: el aumento del área de la glándula hipofisaria, el aplanamiento de la esclera posterior y la disminución del espacio extracerebral. Actualmente, ninguno de ellos permite predecir la respuesta al tratamiento, orientar la decisión de tratar o no tratar, ni seleccionar la mejor opción terapéutica.
TratamientoEl SPTC es un síndrome con una gran variabilidad clínica entre pacientes, por lo que no existe un enfoque terapéutico único. El manejo de cada paciente debe ser individualizado según las manifestaciones clínicas y abordado por un equipo multidisciplinar. El principal objetivo del tratamiento de la HII es aliviar los síntomas, restaurar la agudeza visual y prevenir la progresión de la pérdida visual33.
Estilo de vidaLa primera medida para el tratamiento de la HII es la pérdida de peso en pacientes obesos en un rango del 5-10% para la reversión de síntomas y signos6. El tratamiento puede variar desde dieta estricta a la necesidad de cirugía bariátrica35.
Tratamiento médicoLa acetazolamida es el fármaco más utilizado en el tratamiento médico y el único con un nivel de evidencia A para el tratamiento de pacientes con HII y pérdida de visión leve33. Disminuye la presión del LCR y el grado de papiledema al inhibir la anhidrasa carbónica de los plexos coroideos. Produce mejoría en el campo visual y en las escalas de medida de calidad de vida respecto al placebo36. Se han usado otros múltiples fármacos, como por ejemplo el topiramato o la furosemida.
Intervención quirúrgicaEn pacientes resistentes al tratamiento médico de la HII y con pérdida aguda progresiva de visión (HII fulminante) puede ser necesario usar opciones terapéuticas quirúrgicas que pretenden disminuir la PIC mediante la derivación del LCR. Estas opciones son la fenestración de la vaina del nervio óptico, la derivación de LCR (derivación lumboperitoneal o ventriculoperitoneal) y la colocación de stent en senos venosos. En la actualidad no existe una fuerte evidencia científica que demuestre la superioridad de una de las técnicas sobre el resto37.
Fenestración de la vaina del nervio ópticoEs la intervención de elección para los pacientes con HII resistentes al tratamiento médico que presentan pérdida visual grave pero escasa clínica de cefalea11. Consiste en la realización de fenestración en la vaina del NO retrobulbar para drenar LCR. Sin embargo, se han descrito complicaciones en el 26% de los pacientes y el fracaso en el tratamiento con necesidad de reintervención en un porcentaje aproximado de entre el 14,9% y 31% de los casos38.
Derivación de líquido cefalorraquídeoLa realización de punciones lumbares de repetición puede disminuir la PIC y la sintomatología. Este tratamiento suele ser una medida temporal hasta que se realiza un procedimiento definitivo para disminuir la presión de LCR, como la derivación ventriculoperitoneal (DVP) o lumboperitoneal (DLP)39. En los últimos años existe tendencia a utilizar más la DVP, aunque entre estas dos técnicas todavía existen dudas sobre cuál es la técnica óptima. Ambos procedimientos presentan buenos porcentajes de mejora en el campo y agudeza visual, en la cefalea y en el papiledema38. No obstante, existen tasas de fracaso elevadas con necesidad de revisión del procedimiento y reintervención en un porcentaje en torno al 38% en el caso de la DLP y del 41% en la DVP38.
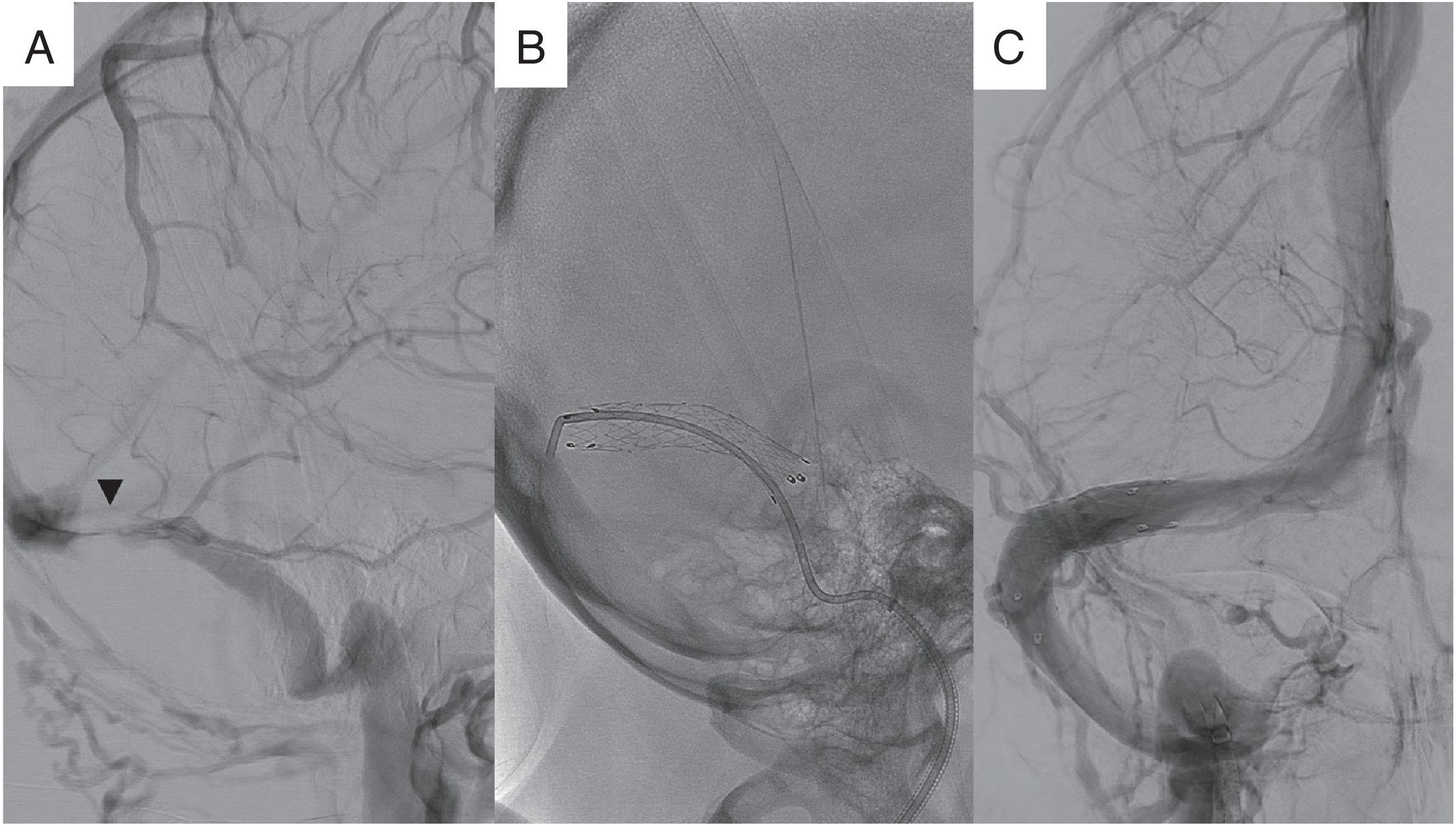
Colocación de stent en senos venosos cerebralesEl tratamiento con stent en la HII para resolver la estenosis de los senos venosos se basa en la teoría vascular/venosa de la fisiopatología. La apertura de la estenosis por el stent interrumpiría el estado de colapso venoso automantenido reduciendo la hipertensión venosa intracraneal y mejorando la absorción de LCR (fig. 9)33. Ha demostrado elevado éxito técnico con buenos resultados clínicos, con mejoría de la cefalea, el papiledema y la agudeza visual9.
Tratamiento mediante stent de la estenosis de un seno venoso. Imágenes de venografía digital. A) Imagen en el plano sagital y sustracción ósea digital que identifican segmento estenótico en seno transverso izquierdo (cabeza de flecha). B) Imagen de venografía sin sustracción digital donde observamos la liberación del stent en la región estenótica. C) Venografía con sustracción digital que muestra el resultado final. Seno transverso de calibre conservado identificando un calibre normal con paso de contraste a través del stent. Cortesía del Dr. Jordi Blasco Andaluz, Hospital de la Santa Creu i Sant Pau, Barcelona.
El objetivo de esta técnica es normalizar el gradiente de presiones pre- y postestenosis. Inicialmente es necesaria la realización de una venografía cerebral retrógrada con manometría para la evaluación de dicho gradiente. No existe consenso acerca del valor del gradiente de presiones requerido para la indicación de este tratamiento, si bien se evidencian mejores resultados clínicos cuanto mayor sea la diferencia de presiones pre- y postestenosis. Tras la implantación del stent se realiza otra manometría para valorar la disminución del gradiente. Se ha descrito una evolución clínica favorable cuanto mayor diferencia haya entre los gradientes de presión antes y después de la implantación del stent33. La angioplastia con balón no ha mostrado buenos resultados, con altas tasas de recurrencia de la estenosis11.
La indicación principal de colocación de stent de senos venosos es la HII con un curso resistente al tratamiento médico y quirúrgico. También existen estudios donde la indicación inicial es la intolerancia al tratamiento médico o ante la HII fulminante40.
Distintos estudios han evaluado los resultados tras este procedimiento. La revisión sistemática de la bibliografía llevada a cabo por Kalyvas et al.38 incluyó 11 estudios y un total de 155 de pacientes, de los cuales el 80,3% habían sido tratados mediante stent como primera opción terapéutica. Puso de manifiesto la mejoría del papiledema en el 98% de casos, de la agudeza visual en el 65% y del campo visual en el 75% de pacientes. La cefalea, por su parte, mejoró en el 77% de casos, empeorando únicamente en el 2%. La presión del LCR se normalizó en todos los pacientes estudiados. El 8% presentó recurrencia de los síntomas.
Entre las complicaciones destaca la cefalea transitoria tras el tratamiento con una frecuencia del 12%38. Se han notificado casos de reestenosis del stent, hematomas subdurales y otras complicaciones derivadas del procedimiento, como la presencia de pseudoaneurisma en el punto de punción11,34.
Entre los factores pronósticos se describe una peor evolución en pacientes jóvenes (media de edad de 30 años) y presión de apertura de LCR elevada, con mayores tasas de revisión del stent en pacientes con obesidad34.
ConclusiónEl SPTC se caracteriza por signos y síntomas derivados de un aumento de la PIC en ausencia de etiología identificable. Las pruebas de imagen tienen como objetivo en el diagnóstico identificar causas de aumento de la PIC. No obstante, existen hallazgos por imagen aceptados como signos de HII con alta especificidad y baja sensibilidad, hallazgos en la silla turca, hallazgos orbitarios asociados o no al papiledema o la estenosis de senos transversos, entre otros. El radiólogo debe estar familiarizado con la imagen de esta entidad, ya que algunos de estos signos se incluyen entre los criterios diagnósticos del SPTC propuestos en 2013. Los objetivos del tratamiento en el SPTC son preservar la visión y controlar los síntomas como la cefalea para mejorar la calidad de vida, de modo que el manejo individualizado de cada paciente permite adecuar el tratamiento. En este último aspecto, la neurorradiología tiene un papel importante, puesto que el abordaje intravascular por vía percutánea de la estenosis de senos venosos mediante la colocación de stent constituye una alternativa terapéutica novedosa con buenos resultados. Se han propuesto diversos biomarcadores de imagen para diagnosticar la HII, así como cuantificar y predecir la respuesta al tratamiento con baja evidencia en el momento actual. Por todo ello, el papel del radiólogo es fundamental tanto para el diagnóstico como para el manejo intervencionista. En el futuro será de interés la realización de estudios prospectivos que permitan adquirir mayor experiencia y conocimiento en esta entidad.
Autoría1. Responsable de la integridad del estudio: DVC, JCP 2. Concepción del estudio: JCP 3. Diseño del estudio: DVC, JCP 4. Obtención de los datos: DVC, JCP 5. Análisis e interpretación de los datos: DVC, JCP 6. Tratamiento estadístico: no procede 7. Búsqueda bibliográfica: DVC, JCP 8. Redacción del trabajo: DVC, JCP 9. Revisión crítica del manuscrito con aportaciones intelectualmente relevantes: DVC, JCP 10. Aprobación de la versión final: DVC, JCP
- 1.
El SPTC consiste en el conjunto de signos y síntomas derivados del aumento de PIC en ausencia de lesiones focales, hidrocefalia o infección o malignidad subyacente. En los casos en los que no se logra identificar etiología se denomina HII.
- 2.
El papel fundamental de las pruebas de imagen es descartar causas identificables de hipertensión intracraneal. No obstante, los hallazgos radiológicos se incluyen entre los últimos criterios diagnósticos propuestos. En ausencia de papiledema y parálisis del VI par podemos sugerir el diagnóstico de HII sumando los hallazgos por imagen a los criterios clínicos.
- 3.
Los hallazgos radiológicos en el SPTC están caracterizados principalmente por su alta especificidad y sensibilidad baja.
- 4.
El manejo de cada paciente debe ser individualizado según las manifestaciones clínicas y abordado por un equipo multidisciplinar. El principal objetivo del tratamiento de la HII es aliviar los síntomas y preservar la visión.
- 5.
La colocación de stent en los senos transversos ha demostrado elevado éxito técnico con buenos resultados clínicos, con mejoría de la cefalea, el papiledema y la agudeza visual.
Los autores declaran no tener conflicto de intereses.
Nuestro agradecimiento al Dr. Fernando Aparici Robles, jefe de la Sección de Neurorradiología del Hospital Universitari i Politècnic La Fe de València, por su participación en la revisión crítica del manuscrito, y al Dr. Juan Delgado Moraleda por su trabajo en la segmentación semiautomática del LCR extraventricular cerebral.