La fibrilación auricular (FA) es la arritmia cardíaca más frecuente globalmente. Se ha descrito previamente que algunas características clínicas como la edad, la obesidad, el tipo de FA y otras, obtenidas mediante estudios de imagen, como el volumen de la aurícula izquierda (AI), la densidad media (calculada a partir del promedio de los valores de unidades Hounsfield en una región de interés) y el volumen del tejido graso cardiaco podrían aumentar el riesgo de recurrencia tras la ablación de venas pulmonares, existiendo resultados contradictorios entre algunos estudios previos con respecto a las variables radiológicas. El objetivo de este estudio fue el de evaluar estos factores de riesgo clínicos y radiológicos obtenidos a partir de estudios de tomografía computarizada (TC).
Materiales y métodosEstudio retrospectivo de casos y controles incluyendo a todos los pacientes con FA sometidos a una primera ablación por radiofrecuencia o crioablación de venas pulmonares posterior a la realización de una TC con contraste entre 2017 y 2021. Se recopilaron variables clínicas como la edad, el sexo, las comorbilidades, las medicaciones empleadas tras la ablación, el tipo de FA y las imágenes radiológicas obtenidas a partir de la segmentación volumétrica de los estudios de TC, como el volumen de la AI, la densidad media y el volumen del tejido graso epicárdico, periauricular e interauricular, así como la aparición o no de recurrencia de la FA tras 12meses desde la ablación. Estas variables fueron sometidas a un análisis univariante y multivariante para evaluar el riesgo de recurrencia.
ResultadosDel total de pacientes incluidos, 40 tenían FA paroxística y 12 FA persistente. Doce (23,1%) mostraron recurrencia durante el periodo de seguimiento y 40 (76,9%) se mantuvieron con ritmo sinusal. Existieron diferencias estadísticamente significativas para el volumen de la AI según el tipo de FA, siendo mayor en los pacientes con FA persistente (119,16±32,38cc) respecto al resto (90,99±28,34cc). En cuanto a las diferencias entre los pacientes con y sin recurrencia tras la ablación, únicamente el volumen de la AI (p<0,05) y el volumen del tejido graso periauricular (p<0,01) fueron significativamente mayores en los pacientes con recurrencia.
ConclusiónEl tipo de FA, el aumento del volumen de la aurícula izquierda y del tejido graso periauricular son factores de riesgo para la recurrencia en pacientes con FA sometidos a ablación de venas pulmonares mediante crioablación o radiofrecuencia.
Atrial fibrillation (AF) is the most common cardiac arrhythmia worldwide. Previous studies have described that certain clinical characteristics such as age, obesity, the type of AF, and imaging-based factors, such as left atrial (LA) volume, mean density (calculated as the average of Hounsfield Units values in a certain region of interest), and volume of cardiac adipose tissue, may increase the risk of recurrence following pulmonary vein ablation. However, there have been contradictory results regarding radiological variables in previous studies. The objective of this study was to evaluate these clinical and radiological risk factors obtained from computed tomography (CT) studies.
Materials and methodsThis retrospective case-control study included all patients with AF who underwent initial radiofrequency or cryoablation of pulmonary veins after undergoing contrast-enhanced CT between 2017 and 2021. Clinical variables such as age, gender, comorbidities, medications used after ablation, type of AF, and radiological variables obtained from volumetric segmentation of CT studies were collected. Radiological variables included LA volume, mean density, and volume of epicardial, periatrial, and interatrial adipose tissue. The occurrence or absence of AF recurrence within 12months after ablation was also recorded. These variables were subjected to univariate and multivariate analysis to evaluate the risk of recurrence.
ResultsAmong the total number of included patients, 40 had paroxysmal AF and 12 had persistent AF. During the follow-up period, 12 patients (23.1%) experienced AF recurrence, while 40 patients (76.9%) remained in sinus rhythm. There were statistically significant differences in LA volume based on the type of AF, with higher volumes observed in patients with persistent AF (119.16±32.38cc) compared to the rest (90.99±28.34cc). Regarding the differences between patients with and without recurrence after ablation, only LA volume (P<.05) and periatrial adipose tissue volume (P<.01) were significantly higher in patients with recurrence.
ConclusionThe type of atrial fibrillation, increased left atrial volume, and increased periatrial adipose tissue volume are risk factors for recurrence in patients with atrial fibrillation undergoing pulmonary vein ablation using cryoablation or radiofrequency.
La fibrilación auricular (FA) es la arritmia cardíaca más frecuente globalmente, con una prevalencia variable que ha aumentado en las últimas décadas. Se estima que su incidencia aumenta según la edad, desde un 0,12- 0,16% en personas menores de 49años hasta un 10-17% en mayores de 79años1, y que para 2050, aproximadamente 17,9 millones de individuos en Europa desarrollarán FA2.
Dependiendo de la duración de los episodios de alteración del ritmo, la FA puede ser clasificada en paroxística, cuando dura menos de 7días, o persistente, entre 7días y 1año. La importancia de clasificarla según el tiempo de evolución tiene impacto sobre el pronóstico a largo plazo y sobre la terapéutica empleada para intentar restaurar el ritmo3,4.
El tratamiento se basa en la prevención de eventos cardioembólicos mediante anticoagulación o antiagregación y control del ritmo y/o de la frecuencia cardiaca mediante fármacos. En el caso de la FA paroxística los episodios pueden autolimitarse o tratarse mediante cardioversión, con el fin de restaurar el ritmo sinusal3. Debido a la frecuente recaída tras la cardioversión eléctrica o farmacológica y el auge de los procedimientos de cardiología intervencionista, la ablación por catéter de las venas pulmonares se ha convertido en una opción de tratamiento ampliamente aceptada para pacientes con FA sintomática resistente a medicamentos5, con una tasa de éxito a 12meses de aproximadamente el 59,9% al 65,4% tras la ablación por radiofrecuencia o la crioablación por catéter6.
Algunos factores, como el tipo de FA, se han relacionado con menores tasas de éxito tras la ablación. En un estudio realizado por Deng et al.7 la tasa de éxito en pacientes con FA paroxística fue del 70%, mientras que en pacientes con FA persistente fue del 50%.
Se ha propuesto que estas diferencias podrían ser secundarias a cambios morfológicos en la aurícula izquierda (AI), como la dilatación auricular y el grosor de la pared tras periodos continuos de alteración del ritmo. Otros factores que han sido relacionados con un mayor riesgo de recurrencia tras la ablación con catéter son la obesidad, el síndrome metabólico y la edad avanzada8-10.
En un trabajo previo, Mahajan et al.11 encontraron que la obesidad de larga evolución contribuye al remodelado auricular, caracterizado por aumento de volumen de la aurícula izquierda, anomalías de la conducción, fibrosis auricular y finalmente por un mayor riesgo de desarrollo de FA.
Se ha descrito, además, que el aumento de la cantidad y de la densidad media del tejido graso epicárdico (TGE), periauricular (TGP) e interauricular (TGI) podrían estar relacionados con el aumento del riesgo de desarrollo de FA y de recurrencia tras la ablación12-15. Esto ha sido evaluado mediante técnicas de segmentación tisular en estudios de resonancia magnética, tomografía computarizada (TC) y ecocardiografía, cuantificando el grosor, el volumen y la densidad de dichos tejidos, aunque con resultados contradictorios entre algunos de ellos16-25.
Por lo tanto, el objetivo de nuestro estudio fue el de evaluar en nuestro medio la asociación entre variables clínicas, volumétricas y densitométricas de la aurícula izquierda y de los TGE, TGP y TGI, obtenidas a partir de estudios de TC, y la recurrencia de la FA en pacientes sometidos a ablación de venas pulmonares.
MétodosEstudio retrospectivo de casos y controles que incluyó a todos los pacientes consecutivos con FA sometidos a una primera ablación por radiofrecuencia o crioablación de venas pulmonares posterior a la realización de una TC con contraste entre 2017 y 2021. Se excluyeron del estudio los pacientes cuyos estudios de TC presentaban artefactos de movimiento o un realce insuficiente de la aurícula izquierda. Se consideraron casos a todos los pacientes que presentaron recurrencia durante el periodo de seguimiento, y controles, a aquellos que permanecieron en ritmo sinusal.
Se recopilaron los datos demográficos y clínicos principales, incluyendo edad, sexo, índice de masa corporal (IMC) y comorbilidades (diabetes mellitus tipo2, dislipidemia e hipertensión arterial sistémica) a partir de las historias clínicas digitales. Se dividió a la muestra según el tipo de FA (paroxística o persistente) con el fin de comparar las características entre ambos grupos. También se recopiló la presencia de ritmo sinusal o recurrencia de la FA durante las visitas de seguimiento para cada paciente a los 3, 6 y 12meses. Todos los datos se trataron de manera confidencial y todos los pacientes firmaron un consentimiento informado antes del procedimiento. Se desestimó la necesidad de consentimiento informado para la participación en el estudio por el comité de ética de nuestro centro debido a la naturaleza retrospectiva, dependiente de la revisión de historias clínicas. El número del registro del protocolo fue PI2023-045.
Tomografías computarizadas y análisis del tejido adiposo cardíacoSe realizaron estudios de TC en pacientes utilizando un escáner de 64 coronas de detectores (Phillips Brilliance CT). Las imágenes se adquirieron a través de un protocolo de adquisición con sincronización electrocardiográfica retrospectiva con modulación de dosis con un kilovoltaje de 120kV, una colimación de 64×0,625mm y un tiempo de rotación de 0,35s. Se inyectó una dosis estándar de 80ml de contraste yodado con una concentración de 400mgI/ml a una velocidad de 4ml/s, seguido de 30ml de suero salino a la misma velocidad.
El estudio se realizó usando la técnica de seguimiento del bolo, colocando la región de interés en la aurícula izquierda y el umbral de disparo a 130unidades Hounsfield (UH), con adquisición del estudio 10s tras alcanzarse el umbral. Los conjuntos de datos de TC se reconstruyeron con un grosor de corte de 1mm.
La medición del volumen de la AI, del volumen y de la densidad de los TGE, TGP y TGI se realizó a partir de la fase del ciclo cardiaco que corresponde al 75% del intervalo R-R, mediante segmentación semiautomática, marcando manualmente el tejido correspondiente en el software Philips IntelliSpace versión 12.1. Todos los casos fueron evaluados y segmentados por un radiólogo de la sección de imagen cardiaca de nuestro hospital. El volumen del TGE se trazó manualmente desde el borde superior del cayado aórtico hasta el diafragma, mientras que el TGP se cuantificó desde el anillo mitral hasta el techo de la AI y el del TGI se realizó en la porción del tabique interauricular. La subsegmentación de tejido graso se basó en un rango de atenuación entre −195 y −15UH.
Análisis estadísticoSe determinó la normalidad de todas las variables cuantitativas incluidas en este estudio mediante el test de Kolmogorov Smirnov. Aquellas con distribución paramétrica fueron descritas mediante su media y desviación estándar, mientras que las no paramétricas se describieron mediante su mediana y cuartiles. Las variables cualitativas fueron descritas mediante su frecuencia absoluta y relativa.
Se realizó un primer análisis univariante comparando la presencia de recurrencia de FA y los factores de riesgo recopilados, tales como edad, sexo, IMC, tipo de FA (paroxística o persistente), volumen auricular izquierdo, volumen y densidad de tejido graso periauricular (TGP), interauricular (TGI) y epicárdico (TGE). Para ello, se empleó la prueba estadística χ2 en el caso de las variables cualitativas, la prueba t de Student para aquellas cuantitativas paramétricas y la prueba U de Mann-Whitney para las variables cuantitativas no paramétricas. Se consideró estadísticamente significativas a todas las variables con un resultado de valor p<0,05.
A partir de estos resultados, las variables estadísticamente significativas fueron sometidas a un análisis multivariante, realizado mediante la prueba estadística de regresión logística y de regresión de Cox.
Se realizó un segundo análisis univariante con el fin de comparar el volumen de la AI, la densidad media y el volumen de los TGP, TGI y TGE entre los pacientes con FA paroxística y persistente, empleando la prueba estadística t de Student para aquellas cuantitativas paramétricas y la prueba U de Mann-Whitney para las variables cuantitativas no paramétricas, considerándolas estadísticamente significativas cuando el resultado del valor p fuese menor a 0,05. El análisis estadístico fue llevado a cabo mediante el software Statistical Package for Social Sciences (SPSS) versión 22.0.
ResultadosSe recopilaron un total de 75 pacientes con FA tratados mediante ablación de venas pulmonares. De ellos, solo 52 tenían una TC con adecuada calidad diagnóstica, sin artefactos de movimiento y un seguimiento durante los siguientes 12meses. De estos pacientes, 21 eran mujeres y 31 hombres, con una mediana de edad de 60 (RIC: 54,5-66) y 58 (RIC: 53-63) años, respectivamente. Respecto a los 23 pacientes excluidos, 10 tenían FA persistente y 13 FA paroxística, siendo los motivos de exclusión la pérdida de seguimiento tras la ablación y los artefactos de movimiento en los estudios de TC.
Fibrilación auricular paroxística vs persistenteDel total de pacientes, 40 tenían FA paroxística y 12 FA persistente. No se encontraron diferencias significativas en la edad, el sexo, las comorbilidades y las medicaciones empleadas tras la ablación entre ambos grupos. Respecto a las variables obtenidas a partir de los estudios de TC (volumen de la AI, volumen y densidad media de los TGE, TGP o TGI), solo existieron diferencias estadísticamente significativas para el volumen de la AI, siendo mayor en los pacientes con FA persistente (119,16±32,38cc), respecto al resto (90,99±28,34cc) (p<0,01) (tabla 1).
Volumen de la aurícula izquierda y características del tejido graso epicárdico, periauricular e interauricular en pacientes con fibrilación auricular paroxística y persistente
| Variables | FA paroxística | FA persistente | OR (IC) | p |
|---|---|---|---|---|
| 28 (53,8%) | 24 (46,2%) | |||
| Volumen del tejido graso | ||||
| Epicárdico | 219,16±113,32 | 250,13±107,05 | − | >0,05 |
| Periauricular | 9,39±5,65 | 14,05±8,25 | − | >0,05 |
| Interauricular | 1,65 (p25: 0,65-p75: 3,04) | 1,94 (p25: 0,74-p75: 3,34) | − | >0,05 |
| Densidad media del tejido graso | ||||
| Epicárdico | −82,5±7,97 | −82,4±7,98 | − | >0,05 |
| Periauricular | −67,58±9,87 | −70,52±9,1 | − | >0,05 |
| Interauricular | −64,53±14,64 | −64,43±13,78 | − | >0,05 |
| Volumen AI | 90,99±28,34 | 119,16±32,38 | − | <0,01 |
AI: aurícula izquierda; FA: fibrilación auricular.
Del total de pacientes incluidos en este estudio, 12 (23,1%) mostraron recurrencia durante el periodo de seguimiento y 40 (76,9%) se mantuvieron con ritmo sinusal.
No existieron diferencias estadísticamente significativas al comparar la edad, el sexo, las comorbilidades, la medicación empleada, el tipo de procedimiento (crioablación vs. radiofrecuencia) y el espesor de la AI entre ambos grupos (tabla 2). Respecto al tipo de FA, 9 (75%) de los pacientes con recurrencia tenían FA persistente y 3 (25%) FA paroxística, mientras que en aquellos sin recidiva, 15 (37,5%) tenían FA persistente y 25 (62,5%) FA paroxística, con una OR de 2 (1,19-3,35, p<0,05) para los pacientes con FA persistente.
Características de la muestra y análisis univariante en pacientes con y sin recurrencia tras la ablación de venas pulmonares
| Variables | Pacientes con recidiva | Pacientes sin recidiva | OR (IC) | p |
|---|---|---|---|---|
| 12 (23,1%) | 40 (76,9%) | |||
| Edad | ||||
| Mayor de 60 años | 7 (58%) | 14 (35%) | 2,6 (0,69-9,72) | >0,05 |
| 60 años o menos | 5 (42%) | 26 (65%) | ||
| Sexo | ||||
| Mujer | 4 (33%) | 17 (42,5%) | ||
| Hombre | 8 (67%) | 23 (57,5%) | 0,37 (0,95-1,43) | >0,05 |
| Índice de masa corporal | 29,33 (± 1,15) | 29,12 (± 7,91) | − | >0,05 |
| Comorbilidades | ||||
| Diabetes mellitus | 4 (33%) | 5 (12,5%) | 3,5 (0,76-16,046) | >0,05 |
| Hipertensión arterial | 7 (58%) | 21 (52,5%) | 1,26 (0,34-4,67) | >0,05 |
| Dislipidemia | 5 (42%) | 21 (52,5%) | 0,64 (0,17-2,38) | >0,05 |
| Obesidad | 2 (16,7%) | 12 (30%) | 2,16 (0,17-27,07) | >0,05 |
| Síndrome metabólico | 1 (8,3%) | 5 (12,5%) | 0,5 (0,37-6,68) | >0,05 |
| Medicación postablación | ||||
| Beta-bloqueantes | 9 (75%) | 25 (62,5%) | 1,07 (0,27-4,21) | >0,05 |
| Calcioantagonistas | 3 (25%) | 5 (12,5%) | 2,33 (0,46-11,64) | >0,05 |
| IECA/ARA | 6 (50%) | 14 (35%) | 1,85 (0,5-6,84) | >0,05 |
| Anticoagulantes orales | 9(75%) | 19 (47,5%) | 3,31 (0,78-14,08) | >0,05 |
| Tipo de fibrilación auricular | ||||
| Paroxística | 3 (25%) | 25 (62,5%) | ||
| Persistente | 9 (75%) | 15 (37,5%) | 2,0 (1,19-3,35) | <0,05 |
| Volumen de la aurícula izquierda (AI) | 130,14±29,84 | 95,56±29,91 | − | <0,01 |
| Espesor de pared de la AI | 0,19 (p25: 0,15-p75: 0,21) | 0,18 (p25: 0,15-p75: 0,20) | − | >0,05 |
| Técnica de ablación | ||||
| Radiofrecuencia | 10 (83,3%) | 28 (70%) | >0,05 | |
| Crioablación | 2 (16,7%) | 12 (30%) | 0,46 (0,089-2,45) | >0,05 |
| Volumen del tejido graso | ||||
| Epicárdico | 270,85±94,46 | 222,23±113,54 | − | >0,05 |
| Periauricular | 17,37±8,32 | 9,79±6,025 | − | <0,01 |
| Interauricular | 2,25 (p25: 0,8-p75: 5,42) | 1,52 (p25: 0,63-p75: 3,04) | − | >0,05 |
| Densidad media del tejido graso | ||||
| Epicárdico | −82,38±6,87 | −82,47±8,26 | − | >0,05 |
| Periauricular | −67,11±7,98 | −68,89±10,06 | − | >0,05 |
| Interauricular | −64,29±14,39 | −64,54±14,21 | − | >0,05 |
Existieron diferencias estadísticamente significativas al comparar el volumen de la AI entre los pacientes que mostraron recurrencia y el resto, con mayores volúmenes en el primer grupo (130,14±29,84cc), respecto a los demás (95,56±29,91cc) (tabla 2).
Respecto al análisis del volumen del tejido graso, periauricular (TGP), epicárdico (TGE) e interauricular (TGI), las diferencias de estas dos últimas variables entre los pacientes con y sin recurrencia no alcanzaron la significación estadística, a pesar de que sus medias en los pacientes con recurrencia fueron mayores respecto al resto (tabla 2 y fig. 1). En cuanto al volumen del TGP entre los pacientes con y sin recurrencia, se hallaron diferencias significativas (p<0,01), con valores mayores en el grupo con recurrencia (17,37±8,32cc) respecto al resto (9,79±6,02cc) (figs. 2 y 3).
Al someter dichas variables a un análisis multivariante mediante regresión logística persistió la significación estadística para el volumen de la AI y el volumen del TGP (p<0,05) como factores de riesgo para recurrencia tras la ablación de venas pulmonares (tabla 3). Se sometieron las mismas variables a un segundo análisis multivariante mediante regresión de Cox, sin encontrar diferencias significativas en la tasa de riesgo (p>0,05).
Análisis multivariante y valores de corte de volumen de aurícula izquierda y tejido graso periauricular para la predicción de recurrencia tras ablación de venas pulmonares
| Variables | OR ajustada (IC) | p ajustada | Sensibilidad | Especificidad | VPP | VPN | |
|---|---|---|---|---|---|---|---|
| Volumen de la aurícula izquierda (AI) | 1,031 (1,003-1,061) | <0,05 | Mayor a 140 cc | 82,20% | 66,70% | 33,30% | 94,90% |
| Volumen del tejido graso periauricular | 1,14 (1,01-1,28) | <0,05 | Mayor a 20 cc | 84,40% | 71,40% | 41,70% | 95,00% |
| Tipo de fibrilación auricular | |||||||
| Paroxística | |||||||
| Persistente | 1,78 (0,28-11,1) | >0,05 |
AI: aurícula izquierda; VPN: valor predictivo negativo; VPP: valor predictivo positivo.
Con respecto a la densidad media del tejido graso epicárdico, periauricular e interauricular, no existieron diferencias estadísticamente significativas entre los pacientes con y sin recurrencia tras la ablación de venas pulmonares (tabla 2).
Finalmente, al analizar el volumen de la AI y el volumen del TGP mediante curvas ROC, el área bajo la curva fue de 0,78 y 0,79, respectivamente (fig. 4), con valores de sensibilidad del 82,2% y del 84,4% y de especificidad del 66,7% y del 71,4% para la predicción de recurrencia en aquellos pacientes que tenían un volumen de aurícula izquierda de más de 140cc y un volumen de TGP mayor a 20cc, respectivamente (tabla 3).
DiscusiónLos principales hallazgos de este estudio fueron, en primer lugar, que los pacientes con FA persistente tienen mayores volúmenes de AI que los pacientes con FA paroxística. En segundo lugar, que entre los pacientes con FA persistente, aquellos con mayor volumen de aurícula izquierda (AI) y del tejido graso periauricular tienen un mayor riesgo de recurrencia entre los 3 y los 12meses tras la ablación de venas pulmonares, mientras que no existen diferencias significativas en la densidad media del tejido graso periauricular, epicárdico e interauricular entre los pacientes con y sin recurrencia.
Se ha descrito previamente la existencia de diferencias morfológicas y volumétricas de la AI según el tipo de FA, con resultados similares a los nuestros. En el estudio realizado por Nagashima et al.14 los pacientes con FA persistente y paroxística tenían volúmenes de la aurícula izquierda, medidos por ecocardiografía, de 62,4±37,2 y 35,9±16,2ml, respectivamente. En nuestro estudio estos volúmenes fueron de 115,18cc (P25: 95,96 - P75: 139,82) y 89,96cc (P25: 72,33 - P75: 104,6). Estas diferencias podrían ser secundarias a las técnicas empleadas para la cuantificación del volumen entre ese estudio y el nuestro. A pesar de lo anterior, el volumen de AI reportado en pacientes con FA persistente fue mayor respecto al de los pacientes con FA paroxística. Este hallazgo podría relacionarse con el tiempo de evolución de la arritmia, que a su vez se ha descrito que influye en el desarrollo de mayor fibrosis parietal auricular19.
Al evaluar la densidad media y los volúmenes de tejido graso epicárdico, periauricular e interauricular según el tipo de FA, no hemos encontrado diferencias significativas; sin embargo, los volúmenes de los tres tipos de tejido fueron al menos 15% mayores en los pacientes con FA persistente comparados con los pacientes con FA paroxística (tabla 1).
Respecto a la evaluación de los factores de riesgo para la recurrencia tras la ablación de venas pulmonares, esta es más frecuente en pacientes con AI de mayor tamaño14,16-18,25-27. En el estudio prospectivo realizado por Straube et al.26 en 473 pacientes, se encontró que volúmenes de AI mayores o iguales a 122,7ml aportaban una sensibilidad y una especificidad del 53% y del 69% para determinar la recurrencia, respectivamente. A pesar de no describirse la fase del ciclo cardiaco en la que se ha cuantificado el volumen en dicho estudio, los resultados en nuestro estudio son similares, pues aquellos con volumen de AI mayor a 140ml durante la fase 75% del ciclo cardiaco aportaron una sensibilidad del 82,2% y una especificidad del 66,7% para la presencia de recurrencia.
En otro estudio16, el volumen de la AI cuantificado en la fase 75% del ciclo cardiaco y ajustado a la superficie corporal fue mayor en pacientes con recurrencia, con un incremento del cociente de riesgo (HR) ajustado del 3% respecto al resto de pacientes. Estos hallazgos refuerzan la existencia de diferencias en el tiempo hasta la recurrencia según el volumen de la AI.
Si bien la mayoría de estudios con los que hemos comparado nuestros resultados han empleado la fase 75% del ciclo cardiaco, el uso de otras fases del ciclo cardiaco podría condicionar la obtención de volúmenes de AI distintos.
En relación con el volumen de los tres tipos de tejido graso (TGE, TGP y TGI), existe gran heterogeneidad en la metodología utilizada para su cuantificación debido al empleo de distintos límites de densidad radiológica y respecto al análisis de los datos obtenidos, pues algunos estudios han analizado la diferencia entre la tasa de recurrencia mediante un análisis multivariante con regresión de Cox y otros la relación de riesgo mediante regresión logística en cierto punto temporal de corte.
En nuestro estudio, el tejido graso se ha cuantificado a partir de la franja de densidades entre −15 y −195UH, tal y como se hizo en un estudio previo27, mientras que otros autores han empleado valores distintos (tabla 4). Mediante este método de cuantificación, no hemos encontrado diferencias significativas respecto al volumen de la AI y del tejido graso periauricular entre los pacientes con y sin recurrencia al someter estas variables a un análisis mediante regresión de Cox, pero sí al evaluarlas mediante regresión logística. Esto podría ser debido a la escasa diferencia hallada al evaluar la velocidad de recurrencia en un periodo de tiempo corto.
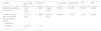
Comparación de características del tejido graso cardiaco evaluado en este estudio y en estudios previos
La significación estadística obtenida para la evaluación del volumen y/o densidad media de los distintos tipos de tejido graso se representa con cruces para el volumen y con círculos para la densidad media. Cada figura tiene un color distinto, acorde al tipo de tejido graso evaluado (rojo para epicárdico, azul para pericoronario, verde para el periauricular y negro para el interauricular).
La existencia de una asociación independiente entre el volumen del tejido graso epicárdico y la presencia de recurrencias más precoces se ha descrito previamente en algunos trabajos13,16,17,22,24,27. En nuestro caso, no hemos encontrado que el aumento del tejido epicárdico se asocie independientemente al riesgo de recurrencia. Estos hallazgos son similares a los de otros estudios20,23, que han empleado distintos límites de densidad para cuantificar el volumen (tabla 4). En uno de estos dos últimos, realizado con una muestra similar a la nuestra, de 53 pacientes23, no se encontró asociación para la existencia de recurrencia en periodos de entre 3 y 30meses tras la ablación, mientras que en el otro20, realizado de forma prospectiva con seguimiento de 55 pacientes durante 12meses, tampoco existieron diferencias estadísticamente significativas para el TGE entre los pacientes con y sin recurrencia.
Respecto al volumen del tejido graso periauricular, hemos encontrado un aumento significativo del riesgo de recurrencia en aquellos pacientes con volúmenes mayores. Estos hallazgos son similares a algunos estudios21,23, mientras que otros18,27 no han encontrado significación estadística para esta asociación. De estos últimos, uno de ellos27, realizado en 212 pacientes, con las mismas franjas de atenuación para definir al TGP (−15 a −195 UH) que el nuestro, ha analizado la tasa de riesgo (HR) a los 12meses sin identificar diferencias significativas en el volumen del TGP entre los pacientes con y sin recurrencia. Estos hallazgos podrían ser secundarios al corto tiempo de seguimiento para detectar diferencias en la tasa de recurrencia. En nuestro caso no hemos hallado diferencias en la tasa de riesgo (HR), pero sí en la relación de riesgo (OR) tras 12meses.
En cuanto al volumen del tejido graso interauricular, un estudio previo20 halló una asociación independiente de este último con el riesgo de recurrencia. Dicho estudio ha empleado un rango de atenuación distinto (−30 a −195 UH) al nuestro. En este estudio no hemos encontrado un aumento del riesgo secundario a un mayor volumen de tejido graso interauricular.
Tampoco hemos encontrado diferencias en la presencia de recurrencia tras la ablación respecto a la densidad media de los tejidos epicárdico, periauricular e interauricular, mientras que otros autores21 sí han encontrado asociación entre la densidad media del tejido graso periauricular con el riesgo de recurrencia al emplear rangos de densidad entre −50 y −190. Se ha propuesto que estos hallazgos podrían ser secundarios a cambios inflamatorios en el tejido graso con mayor cantidad de edema en el mismo.
Otros autores que han empleado una franja similar de atenuación18 no han encontrado estas diferencias con respecto a la densidad del tejido graso periauricular entre los pacientes con y sin recurrencia. Al emplear franjas más cercanas al cero, como en nuestro estudio (−15 a −195UH) y otro más27, tampoco se han encontrado diferencias entre ambos grupos.
Dentro de las limitaciones de nuestro estudio se encuentra la evaluación del volumen de los TGE, TGP y TGI mediante segmentación manual, ya que podrían existir diferencias al evaluarse por otro observador. A pesar no haber analizado estas diferencias en nuestro estudio, en un trabajo previo27 se ha encontrado una excelente correlación interobservador (0,99) mediante técnicas de segmentación manual como la que hemos empleado nosotros. Otra limitación posible en nuestro estudio es el empleo de franjas de atenuación distintas a las de otros estudios. No hemos encontrado una referencia apropiada que pudiese correlacionar la cuantificación del volumen del tejido graso mediante anatomía patológica con respecto a la radiológica con TC. Sin embargo, se ha mencionado que valores de −30 a −195UH representan al tejido graso libre de otros tipos de tejidos blandos, como el tejido conjuntivo28. En cuanto a la medición del volumen del tejido graso cardiaco, no hemos encontrado estudios previos que comparen su cuantificación en las distintas fases del ciclo cardiaco, lo que podría ser una limitación si existiesen diferencias. Finalmente, el tamaño de la muestra de nuestro estudio podría haber limitado la evaluación de algunas variables obtenidas a partir de las TC, como el volumen de los TGE, TGP y TGI, que si bien no fueron significativamente distintas, parecían no solaparse en un porcentaje de pacientes, por lo que ampliar la muestra podría destacar dichas diferencias.
ConclusiónEn nuestro medio, el tipo de fibrilación auricular, el aumento del volumen de la aurícula izquierda y del tejido graso periauricular son factores de riesgo para la recurrencia en pacientes con fibrilación auricular sometidos a ablación de venas pulmonares mediante crioablación y ablación por radiofrecuencia. Por otro lado, no existen diferencias en la densidad media del tejido graso interauricular, periauricular y epicárdico entre los pacientes con y sin recurrencia de la fibrilación auricular.
Autoría- 1.
Responsable de la integridad del estudio: JJAJ.
- 2.
Concepción del estudio: JMCG.
- 3.
Diseño del estudio: JMCG, JJAJ, AUV.
- 4.
Obtención de los datos: JMCG, MJGB, HTB.
- 5.
Análisis e interpretación de los datos: JMCG, JJAJ, AAC.
- 6.
Tratamiento estadístico: JMCG
- 7.
Búsqueda bibliográfica: AAC, JMCG.
- 8.
Redacción del trabajo: JMCG, AAC, JJAJ.
- 9.
Revisión crítica del manuscrito con aportaciones intelectualmente relevantes: JJAJ.
- 10.
Aprobación de la versión final: JJAJ.
Los autores declaran no tener conflicto de intereses.