Introducción
Los traumatismos arteriales posquirúrgicos o pospunción pueden generar pseudoaneurismas que suelen acompañarse de un cuadro hemorrágico inmediato o diferido. En estos casos es necesaria una actuación rápida que detenga el sangrado, adquiriendo el abordaje endovascular un papel muy importante.
En la bibliografía se refleja de forma extensa el tratamiento endovascular de los pseudoaneurismas con múltiples materiales de embolización1-9.
El desarrollo de microcatéteres y nuevos agentes de embolización, como el Onyx, han facilitado el tratamiento endovascular de las hemorragias arteriales espontáneas o secundarias a pseudoaneurismas
El Onyx es un agente de embolización líquido no adhesivo compuesto de un copolímero de alcohol etilen-vinílico (EVOH), disuelto en DMSO (sulfóxido de dimetilo), al que se le añade polvo de tantalio para su visualización fluoroscópica.
Fue diseñado para la embolización arterial de las malformaciones arteriovenosas cerebrales, y posteriormente se ha ido usando en el tratamiento endovascular de lesiones periféricas9-15.
El objetivo del presente trabajo es demostrar la utilidad del uso de Onyx en el tratamiento endovascular selectivo de las hemorragias arteriales traumáticas y cuadro clínico hemorrágico de diferente gravedad.
Material y métodos
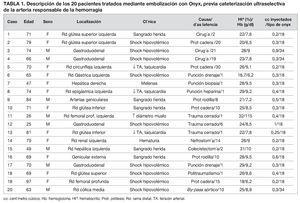
Realizamos una revisión retrospectiva y descriptiva de 20 casos embolizados con Onyx de sangrados arteriales periféricos secundarios a cirugía o punción, que describimos en la tabla 1.
Las embolizaciones, realizadas de forma consecutiva en un periodo de 6 meses, se llevaron a cabo en 12 mujeres con una edad media de 71,91 años y en 8 hombres con una edad media de 66,28 años.
La totalidad de los casos presentó descenso del hematocrito y de la hemoglobina, secundario a un cuadro hemorrágico agudo de diferente gravedad, 9 de ellos en shock hipovolémico. En todos ellos existió diferente grado de inestabilidad hemodinámica, que obligaba a una actuación rápida. En 7 casos el tiempo de latencia entre el traumatismo y el cuadro clínico hemorrágico fue menor de 24 horas, en dos de 48 horas y en los 11 restantes hubo un tiempo medio de latencia de 14,8 días, con un mínimo de 6 y un máximo de 30 días.
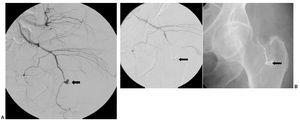
Once lesiones fueron roturas arteriales con formación de pseudoaneurisma de una arteria musculoesquelética (fig. 1) y 9 fueron lesiones en una arteria visceral (fig. 2), 4 de las cuales fueron lesiones de la arteria gastroduodenal (fig. 3), tres secundarias a complicaciones de una duodenopancreatectomía cefálica y otra a una punción directa con un catéter de drenaje 10 french de un absceso secundario a una colecistectomía.
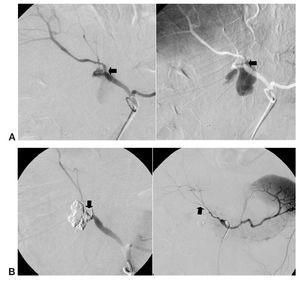
Fig. 1. (A) (caso 13) Arteriografía selectiva de arteria glútea inferior izquierda que pone de manifiesto la rotura arterial y el punto de sangrado activo (flecha). (B) Arteriografía selectiva de glútea inferior e imagen simple sin sustracción que muestran el molde de Onyx cerrando selectivamente el punto sangrante, permaneciendo permeables el resto de ramas arteriales (flecha).
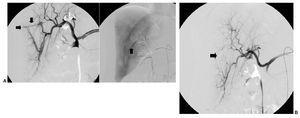
Fig. 2. (A) (caso 7). Arteriografía selectiva de arteria hepática en la que se aprecia la fístula arterio portal (flecha a la derecha), el tracto hepático de la biopsia (flecha hacia abajo) y en fase tardía el relleno de un radical biliar (flecha hacia arriba). (B) Arteriografía hepática en la que se objetiva el molde sustraído de Onyx y el cierre de la fístula con ausencia de llenado del árbol portal y biliar (flecha).
Fig. 3. (A) (caso 3). Extravasación de sangre por arteria gastroduodenal en paciente con fístula pancreática secundaria a duodenopancreatectomía cefálica, con pérdida de la sutura quirúrgica (flecha). (B) Oclusión con onyx 34 del muñón arterial y del pseudoaneurisma (flecha hacia abajo), estando conservada la vascularización hepática inicial (flecha hacia arriba).
El Onyx (ev3. Plymouth, USA) es un agente de embolización líquido no adhesivo compuesto de un copolímero EVOH, disuelto al 6% (onyx 18), 6,5% (onyx 20) y 8% (onyx 34) en DMSO, al que se le añade polvo de tantalio para su visualización fluoroscópica. Debido a que el disolvente puede estropear diferentes tipos de materiales, la casa comercial aconseja el uso de micro-catéteres compatibles con DMSO. En nuestro caso hemos utilizado en todos las situaciones un microcatéter Rebar (ev3. Plymouth, USA), inyectando primero el DMSO hasta rellenar el espacio muerto del microcatéter y posteriormente el Onyx. Ambos productos vienen precargados en envase estéril con jeringa de 1 ml compatible con el disolvente.
En los 20 pacientes hemos realizado un estudio previo con tomografía computarizada (TC), que demostró la localización del hematoma, y una angiografía selectiva con sustracción digital, que localizó exactamente la rama arterial rota responsable del sangrado. No realizamos angio TC por no disponer de esta tecnología. Siempre hemos hecho cateterismo ultraselectivo de la rama arterial responsable del sangrado, acercándonos lo más posible al punto de rotura arterial, donde se había formado un pseudoaneurisma de diferente tamaño, oscilando entre los 6 cm y los 3 mm. En la totalidad de los casos hemos llegado con el material de embolización hasta el propio pseudoaneurisma, realizando el cierre desde este nivel hacia atrás, con el fin de evitar reentradas. Con la embolización hemos procurado ser lo más conservadores posible en cuanto a preservar las ramas arteriales adyacentes no patológicas, y lo más agresivos posible a la hora de cerrar el punto sangrante, progresando en la embolización hasta estar seguros del cierre vascular del vaso responsable del sangrando y la ausencia de reentradas.
Para realizar el procedimiento, hecho por vía femoral en el 100% de los casos, hemos utilizado un introductor 4F y un catéter hidrofílico 4F con luz 0,038", de morfología cobra 1, simons 1 o vertebral (Terumo. Tokio, Japón) que lo utilizamos como catéter guía. Éste lo hemos colocado lo más próximo al vaso responsable de la hemorragia. Posteriormente, coaxial con este catéter, hemos introducido un microcatéter compatible con el DMSO, Rebar 0,18" o 0,10" (ev3. Plymouth, USA), que con la ayuda de una microguía hidrofílica 0,016" o 0,010" (Terumo. Tokio, Japón), hemos colocado lo más próximo posible al punto sangrante.
Una vez colocado el microcatéter en el punto desde el que decidimos realizar la embolización, rellenamos su espacio muerto con DMSO y posteriormente inyectamos Onyx. La cantidad de Onyx inyectada en cada caso, reflejada en la tabla 1, nunca superó 1 cc. El DMSO se disuelve en la sangre y en los fluidos intersticiales, causando la precipitación in situ del copolímero EVOH y del tantalio en él suspendido, que lo hace radioopaco y permite su correcta y precisa visualización con fluoroscopia. La precipitación produce un émbolo esponjoso y coherente que se solidifica desde la parte exterior hacia la interior, a la vez que progresa y se desplaza distalmente por el vaso, lo que permite "empujar" el émbolo y hacer una inyección controlada hasta el punto preciso que se desea, rellenando el tramo desde la punta del microcatéter hasta el punto de rotura vascular. Dado que el Onyx no es adhesivo, el microcatéter puede permanecer en la posición inicial mientras se realizan inyecciones lentas y controladas. Incluso se puede detener la inyección y realizar una angiografía de control posembolización por el catéter guía, así como inyecciones adicionales por el mismo microcatéter en caso de ser necesario. Esta maniobra la hemos realizado en la totalidad de los casos.
Una vez comprobado el cierre total del punto sangrante procedemos a retirar el microcatéter y realizamos una segunda comprobación por el catéter guía. Cuando estamos seguros de la correcta embolización con ausencia de sangrado activo, damos por finalizado el procedimiento.
A todos los enfermos se les realizó un control clínico inmediato, con TC en los 15 días siguientes a la embolización y un seguimiento clínico a los 6 meses.
Resultados
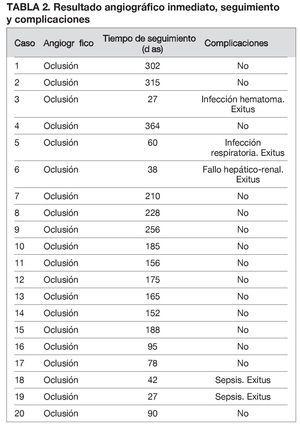
Como queda reflejado en la tabla 2 el éxito técnico y clínico lo conseguimos en el 100% de los casos, con el cierre del punto sangrante demostrado de forma inmediata mediante angiografía y con una buena evolución clínica.
El seguimiento medio ha sido de 157,65 días (rango: 27-364). En este tiempo no hemos tenido ningún caso con recidiva del sangrado. Tampoco hemos tenido complicaciones isquémicas secundarias a cierres arteriales no deseados.
El caso 4 se intentó resolver 24 horas antes con la colocación de una prótesis cubierta en la arteria hepática, que no se consiguió posicionar por la angulación del nacimiento del tronco celíaco que impedía su progresión. En ese momento se colocaron 3 coils electrolargables de platino en la arteria hepática común (GDC, Boston. Natick, USA). Dado que se mantenía la situación de inestabilidad hemodinámica del enfermo se repitió la angiografía, que demostró persistencia del sangrado. Por ello, decidimos cerrar la arteria inyectando Onyx 34 sobre los coils, con un resultado efectivo inmediato.
Hemos registrado 5 fallecimientos. Cuatro de ellos en los primeros 30 días, uno de los cuales ocurrió a las 48 horas de la embolización, sin constancia de resangrado. Cuatro fallecieron por problemas infecciosos y uno por fallo multiorgánico hepatorrenal.
En el enfermo 3, resuelto el problema hemorrágico y con el paciente perfectamente estable y recuperado, a los 10 días se le realizó una laparotomía para drenar el voluminoso hematoma intraperitoneal sobreinfectado. El paciente falleció por sepsis a los 27 días.
Discusión
Cuando, por la causa que sea, habitualmente traumática o infecciosa, ocurre una rotura en la continuidad de la pared arterial se produce una extravasación de sangre alrededor y habitualmente se genera una cápsula de tejido fibroso, formándose lo que denominamos un pseudoaneurisma16, que por definición nunca tiene las tres capas arteriales.
Los traumatismos arteriales pueden producir por este motivo serias complicaciones precoces o tardías, ya que el pseudoaneurisma puede y suele romperse, produciendo un extravasado de sangre con un cuadro hemorrágico. En nuestra serie el tiempo de latencia desde el antecedente traumático hasta el sangrado osciló entre una hora y 30 días.
Ante la sospecha de un traumatismo arterial, aunque se pueden realizar múltiples exploraciones no invasivas como la ecografía, la TC, la angio TC o la angiorresonancia, habitualmente es necesaria la realización de una angiografía, que sigue siendo la exploración fundamental en estos casos17. La presencia de pseudoaneurismas puede requerir de forma inmediata el tratamiento quirúrgico o endovascular, habiéndose mostrado este último menos agresivo y más fácil de realizar, ya que la exploración quirúrgica de una zona traumatizada habitualmente es muy compleja y difícil.
Desestimamos la cirugía de primera intención en todos los casos; en aquéllos en que la lesión asentaba sobre un vaso grande porque el acceso quirúrgico era complejo, sobre todo en enfermos ya intervenidos y en situación de fallo hemodinámico.
Cuando la lesión asienta sobre un vaso grande y superficial se puede hacer cirugía o tratamiento endovascular, siendo muy útil en estos casos la colocación de prótesis endovasculares cubiertas18 o agentes de embolización sólidos tales como coils18,19-21.
Cuando la lesión es de una rama profunda distal es siempre más fácil el tratamiento endovascular, y éste es más sencillo y seguro de realizar con agentes embolizantes líquidos, ya que el acceso directo al vaso distal para colocar agentes sólidos resulta muchas veces demasiado complicado, si no imposible. En la bibliografía los agentes de embolización más usados en el tratamiento de pseudoaneurismas son los coils y microcoils. En nuestra opinión, sobre todo cuando la lesión es distal, son muy difíciles de colocar abarcando el vaso distal y el propio pseudoaneurisma. Por ello, muchas veces se colocan proximales, en el vaso aferente, lo cual es causa de recidiva de la hemorragia por reentrada. En la totalidad de nuestros casos la lesión arterial se producía en vasos profundos y distales. Por ello hemos preferido la utilización de un agente líquido, más fácil de "empujar" por los vasos hasta el pseudoaneurisma.
En el caso 4 intentamos colocar una prótesis cubierta, y no lo conseguimos por problemas técnicos en la flexibilidad del material para adaptarse a la curvatura del tronco celíaco. Este problema, en nuestra opinión, es bastante frecuente y limita la utilización de estos dispositivos. Ante esta circunstancia se colocaron coils electrolargables sobre la arteria hepática derecha y en el nacimiento de la arteria gastroduodenal, no siendo oclusivos y manteniéndose el sangrado. A las 24 horas, con el enfermo hemodinámicamente inestable, decidimos elegir un agente embolizante líquido, denso y no adhesivo, que pudiéramos colocar entre los coils, lo que realizamos con 0,3 cc de onyx 34, con un resultado oclusivo inmediato. Esto nos ocurrió también en el caso 16, en el que habíamos colocado previamente coils que no consiguieron cerrar totalmente el pseudoaneurisma, manteniéndose el sangrado.
En nuestras manos el uso de prótesis cubiertas, agentes de embolización sólidos o agentes de embolización líquidos, como el N-butil cianoacrilato (NBCA) no resultan fáciles de usar. Nos ha ocurrido con cierta frecuencia que el agente embolizante ha quedado proximal, ha emigrado a sitios no deseados, o a pesar de estar colocado en el área que queríamos, no era oclusivo. En la bibliografía no hay referidas series grandes de tratamientos endovasculares de este tipo. Por ello, a pesar del precio (1.000 euros por vial), hemos elegido este material para la embolización; nunca hemos requerido más de 1 cc para completarla.
El principal inconveniente que hemos encontrado en la utilización de este material es que se deposita por precipitación en el fondo de los vasos, por lo que es necesario ser muy cautos en la valoración de cuándo hemos ocluido la totalidad de la luz del vaso.
Se han utilizado muchos agentes de embolización para ocluir los pseudoaneurismas de pequeñas y profundas arterias con buenos resultados técnicos y clínicos, tales como el NBCA22,23, coágulo autólogo, trombina18,24, gelfoam22,25, partículas22, coils19-21, microcoils25-27, etc. De ellos, probablemente el NBCA ha sido el más apropiado, y se ha usado solo o conjuntamente con coils. Sin embargo, la mezcla con lipiodol para su preparación, modificando la radioopacidad, viscosidad y tiempo de polimerización, así como su propiedad adhesiva y corto tiempo de aglutinación, que obliga a la retirada rápida del catéter para evitar la fijación de éste con la pared del vaso en el que está colocado, dificulta y limita su utilización. Cuanto más lipiodol se añade, la radioopacidad y el tiempo de polimerización aumentan, pero su baja viscosidad y el tiempo largo de aglutinación hacen que sea más fácil producir una embolización distal, embolizando vasos eferentes innecesarios, a veces sin conseguir embolizar el propio pseudoaneurisma e incluso, en ocasiones, embolizando el vaso aferente sin cerrar el punto de sangrado activo, permitiendo la recanalización retrógrada, lo que nos hace fracasar en el objetivo de la embolización. En el caso particular de la embolización con NBCA de pseudoaneurismas, a las limitaciones ya descritas hay que añadir la posibilidad de que el material se desplace por la pared superior del vaso aferente, produciendo reflujo a las ramas arteriales que no queremos embolizar28.
El Onyx (ev3. Plymouth, USA) es un agente de embolización líquido29. Cuando contacta con la sangre el DMSO se difunde rápidamente causando la precipitación y solidificación in situ del polímero y el tantalio, formando un émbolo esponjoso que no se adhiere a la pared vascular. Es por tanto un émbolo mecánicamente oclusivo, no adherente, que progresa por el vaso con el flujo y según la velocidad de inyección. Su visualización por radioscopia es buena, y permite controlar la progresión de la embolización en todo momento, pudiéndose incluso detener la inyección y retomarla pasado un tiempo. Ello hace posible la embolización selectiva del punto sangrante.
Su propiedad de ser no adhesivo, lo contrario que el NBCA, permite que los catéteres no se peguen a la pared del vaso, no siendo necesaria su rápida retirada, lo que aumenta mucho la tranquilidad del operador y el tiempo de manipulación. Su alta viscosidad y el tiempo largo de polimerización lo hacen de más fácil utilización que el NBCA, de muy baja viscosidad y polimerización muy rápida. Podemos decir que, en nuestras manos, es el agente líquido más fácil y seguro de manipulación, motivo por el cual lo hemos elegido en estos 20 casos que requerían una rápida y segura actuación.
El DMSO30 es un disolvente orgánico estable y seguro en el uso humano que puede causar degradación de algunos plásticos, lo que obliga a usar catéteres y materiales compatibles; nosotros elegimos siempre el Rebar.
En conslusión, nuestra experiencia en la embolización de sangrados arteriales con Onyx es positiva, ya que hemos solucionado el 100% de los casos. Nos parece un buen agente de embolización dadas sus propiedades de líquido, no adhesivo, alta viscosidad y tiempo largo de polimerización, lo que hace que sea muy controlable en su manejo.
Declaración de conflicto de intereses.Declaramos no tener ningún conflicto de intereses.
Correspondencia:
FERMÍN URTASUN GRIJALBA.
C/ Benjamín de Tudela, 26, 7D. 31008 Pamplona. Navarra. España.
furtasun@telefonica.net
Recibido: 18-VI-07
Aceptado: 6-XI-07