La rápida progresión de la neumonía COVID-19 puede implicar la necesidad de recurrir a sistemas de respiración asistida, como la ventilación mecánica no invasiva o la intubación endotraqueal. La introducción de herramientas que detecten la neumonía COVID-19 puede mejorar la atención sanitaria de los pacientes. Nuestro objetivo es evaluar la eficacia y la eficiencia de la herramienta de inteligencia artificial (IA) Thoracic Care Suite de GE Healthcare (que incorpora Lunit Insight CXR) para predecir la necesidad de recurrir a la respiración asistida en función de la progresión de la neumonía en la COVID-19 en radiografías torácicas consecutivas.
MétodosSe incluyó a pacientes ambulatorios con infección por SARS-CoV-2 confirmada, con hallazgos probables o indeterminados de neumonía COVID-19 en la radiografía torácica (RXT) y que necesitaron una segunda RXT debido a la evolución clínica desfavorable. En las 2RXT se evaluaron el número de campos pulmonares afectados mediante la herramienta de IA.
ResultadosSe incluyó a 114 pacientes (57,4±14,2 años; 65 de ellos varones, el 57%) de forma retrospectiva; 15 pacientes (el 13,2%) precisaron respiración asistida. La progresión de la diseminación neumónica ≥0,5 campos pulmonares al día en comparación con el inicio de la neumonía, detectada mediante la herramienta TCS, cuadruplicó el riesgo de precisar respiración asistida. El análisis de los resultados de IA precisó 26 segundos.
ConclusionesAplicar la herramienta de IA, Thoracic Care Suite, a la RXT de pacientes con neumonía COVID-19 nos permite predecir la necesidad de recurrir a la respiración asistida en menos de medio minuto.
Rapid progression of COVID-19 pneumonia may put patients at risk of requiring ventilatory support, such as non-invasive mechanical ventilation or endotracheal intubation. Implementing tools that detect COVID-19 pneumonia can improve the patient's healthcare. We aim to evaluate the efficacy and efficiency of the artificial intelligence (AI) tool GE Healthcare's Thoracic Care Suite (featuring Lunit Insight CXR, TCS) to predict the ventilatory support need based on pneumonic progression of COVID-19 on consecutive chest X-rays.
MethodsOutpatients with confirmed SARS-CoV-2 infection, with chest X-ray (CXR) findings probable or indeterminate for COVID-19 pneumonia, who required a second CXR due to unfavorable clinical course, were collected. The number of affected lung fields for the 2CXRs was assessed using the AI tool.
ResultsOne hundred fourteen patients (57.4±14.2 years; 65 of them were men, 57%) were retrospectively collected; and 15 (13.2%) required ventilatory support. Progression of pneumonic extension ≥ 0.5 lung fields per day compared to pneumonia onset, detected using the TCS tool, increased the risk of requiring ventilatory support by 4-fold. Analyzing the AI output required 26seconds of radiological time.
ConclusionsApplying the AI tool, Thoracic Care Suite, to CXR of patients with COVID-19 pneumonia allows us to anticipate ventilatory support requirements requiring less than half a minute.
La situación excepcional generada por la pandemia de SARS-CoV-2 (COVID-19) ha tensado los recursos de los sistemas sanitarios de todo el mundo hasta el límite, debido a la combinación de una sobrecarga de pacientes y las bajas por enfermedad de los profesionales sanitarios1,2. En aquellos casos en los que el SARS-CoV-2 afecta las vías respiratorias bajas y provoca neumonía, puede que el paciente precise respiración asistida, que puede variar desde la oxigenación con gafas nasales a los cuidados intensivos, como la ventilación mecánica e, incluso, la oxigenación mediante una membrana extracorpórea en las situaciones más extremas3. Predecir estas necesidades clínicas para evitar la sobrecarga de las unidades podría mejorar la atención de los pacientes y la organización de los servicios encargados de dicha atención4.
La radiografía torácica (RXT) ha sido la herramienta más utilizada para el diagnóstico y el seguimiento de la neumonía COVID-195. La progresión inicial de la neumonía en la RXT también es un indicador del pronóstico6. Así, por ejemplo, un aumento rápido de la puntuación Brixia en la RXT es un factor pronóstico independiente de la necesidad de recurrir a la respiración asistida6. Sin embargo, cuantificar de forma precisa las variaciones de la puntuación Brixia es un tarea que debe realizar un radiólogo experimentado7. Dada la falta actual de recursos8, debido a la escasez de radiólogos y a la sobrecarga de trabajo, no es posible solicitar a radiólogos expertos que calculen la puntuación Brixia, además de elaborar el informe radiológico completo. Las herramientas de inteligencia artificial (IA) podrían contribuir a ahorrar tiempo en cualquier tipo de situación pandémica que implique una posible afectación neumónica. Se han evaluado satisfactoriamente varios modelos de IA en el ámbito del laboratorio9. Sin embargo, la investigación sobre su eficacia en situaciones clínicas reales es escasa, probablemente debido a las dificultades inherentes de integrar estos sistemas en la práctica diaria y evaluar sus resultados. Los problemas para superar estos obstáculos retrasarán o impedirán que los servicios sanitarios se beneficien de estas herramientas en la práctica clínica, lo que sería, sin duda, una oportunidad perdida, teniendo en cuenta que estos recursos podrían ayudarnos tanto en la pandemia actual como en posibles pandemias futuras.
Por otra parte, los servicios radiológicos pueden proveerse de herramientas de IA comercializadas por distintos proveedores sanitarios, pero dichas herramientas de IA no están preparadas ni centradas específicamente en el diagnóstico de COVID-19. Aun así, podrían ser de ayuda si los resultados diagnósticos se demostraran en el ámbito científico. Es por este motivo por el que este estudio pretende valorar el rendimiento de la herramienta de IA comercial Thoracic Care Suite (TCS) en la vida real, aplicada a las RXT (RXT-IA) en el seguimiento inicial de la neumonía COVID-19, con el fin de prever la necesidad de respiración asistida. Nuestra hipótesis, tal como hicimos anteriormente sin IA6, es que podría ayudarnos a prever una evolución desfavorable y la progresión de la enfermedad. Como objetivo secundario, al valorar la eficiencia del flujo de trabajo con la integración de TCS, cuantificaremos el tiempo que necesita el radiólogo para integrar el resultado en el informe radiológico.
Materiales y métodosRealizamos un estudio retrospectivo observacional en un solo centro, aprobado por el Comité de Ética de nuestro centro (código interno EST: 38/20), según la declaración STROBE. No se consideró necesario el consentimiento informado del paciente.
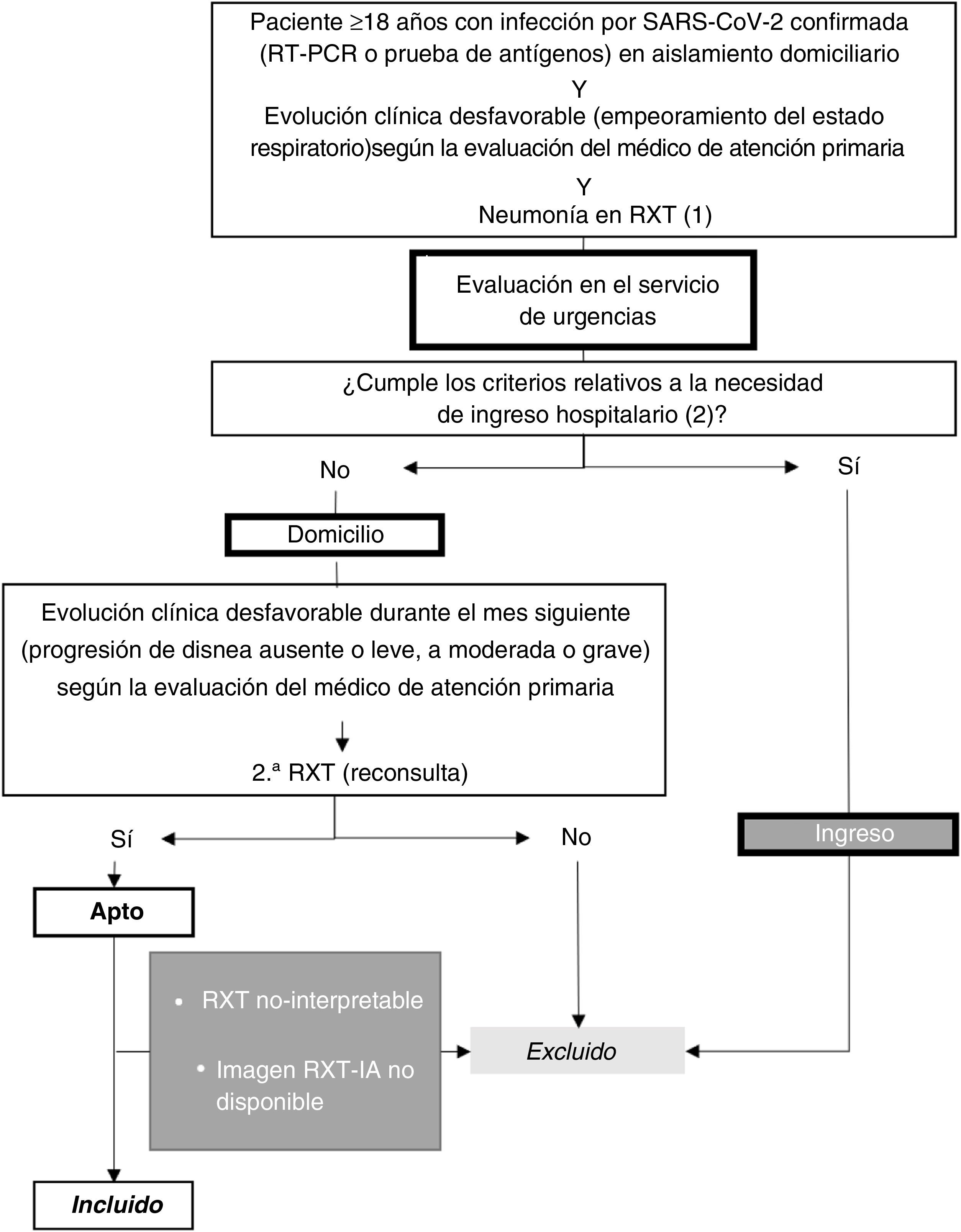
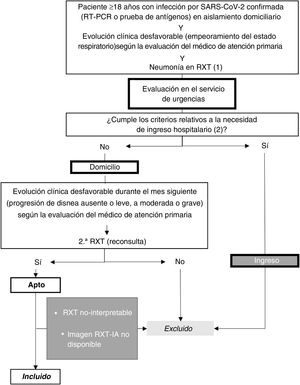
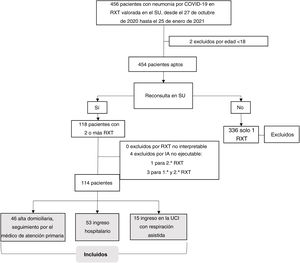
Entorno y selección de la muestraLos criterios de selección fueron: a) pacientes de ≥18 años; b) prueba positiva de la reacción en cadena de la polimerasa con retrotranscripción (RT-PCR) o de antígenos para la infección por SARS-CoV-2; c) evaluación respiratoria desfavorable y primera RXT (RXT1) con opacidades pulmonares, hallazgos probables o indeterminados de neumonía COVID-1910; d) sin criterios que hagan necesario el ingreso hospitalario en el momento de la RXT1 (sin disnea, frecuencia respiratoria <22, saturación de oxígeno ≥95 %, puntuación Brixia <14 y sin riesgo de progresión teniendo en cuenta las enfermedades concomitantes); e) y que precisen una segunda consulta y una nueva RXT (RXT2) por presentar una evolución clínica desfavorable en el domicilio durante el mes posterior a la primera RXT (fig. 1).
Selección de la muestra con criterios de inclusión y exclusión.
(1) Neumonía en radiografía torácica: opacidades pulmonares, hallazgos probables o indeterminados de neumonía COVID-19.
(2) Criterios de hospitalización:
Criterios principales:
-Disnea.
-Frecuencia respiratoria ≥ 22.
-Saturación de O2 basal <94%.
Criterios adicionales que tener en cuenta:
-Puntuación Brixia en radiografía torácica:
-0-4: paciente de bajo riesgo.
-5-13: la necesidad de ingreso debe correlacionarse con los antecedentes clínicos e históricos.
-14-18: paciente de riesgo elevado.
-Pacientes de riesgo elevado según las enfermedades concomitantes.
RT-PCR: reacción en cadena de la polimerasa en tiempo real con retrotranscripción (real-time reverse transcription polymerase chain reaction); RXT-IA: RXT procesada con la herramienta de IA; RXT: radiografía torácica.
Los pacientes se excluyeron si las imágenes radiológicas no eran diagnósticas debido a una mala calidad técnica o si no se disponía de imágenes de RXT-IA (fig. 1).
El médico de atención primaria confirmó la infección por SARS-CoV-2 antes de solicitar la RXT1 o lo hizo el médico de urgencias poco después de la RXT1. El ingreso en la unidad de cuidados intensivos se determinó en función de la gravedad de la insuficiencia respiratoria, con requerimiento de respiración asistida (documento suplementario).
Variables radiológicasRecopilamos datos de la RXT1 y la RXT2 para determinar la evolución radiológica. La RXT1 fue la primera RXT en que se observan opacidades pulmonares, hallazgos probables o indeterminados de neumonía COVID-1910. La RXT2 fue la primera RXT de seguimiento después de la RXT1. En ambas exploraciones evaluamos la proyección posteroanterior habitual y, en pacientes encamados, la radiografía hecha en la cama.
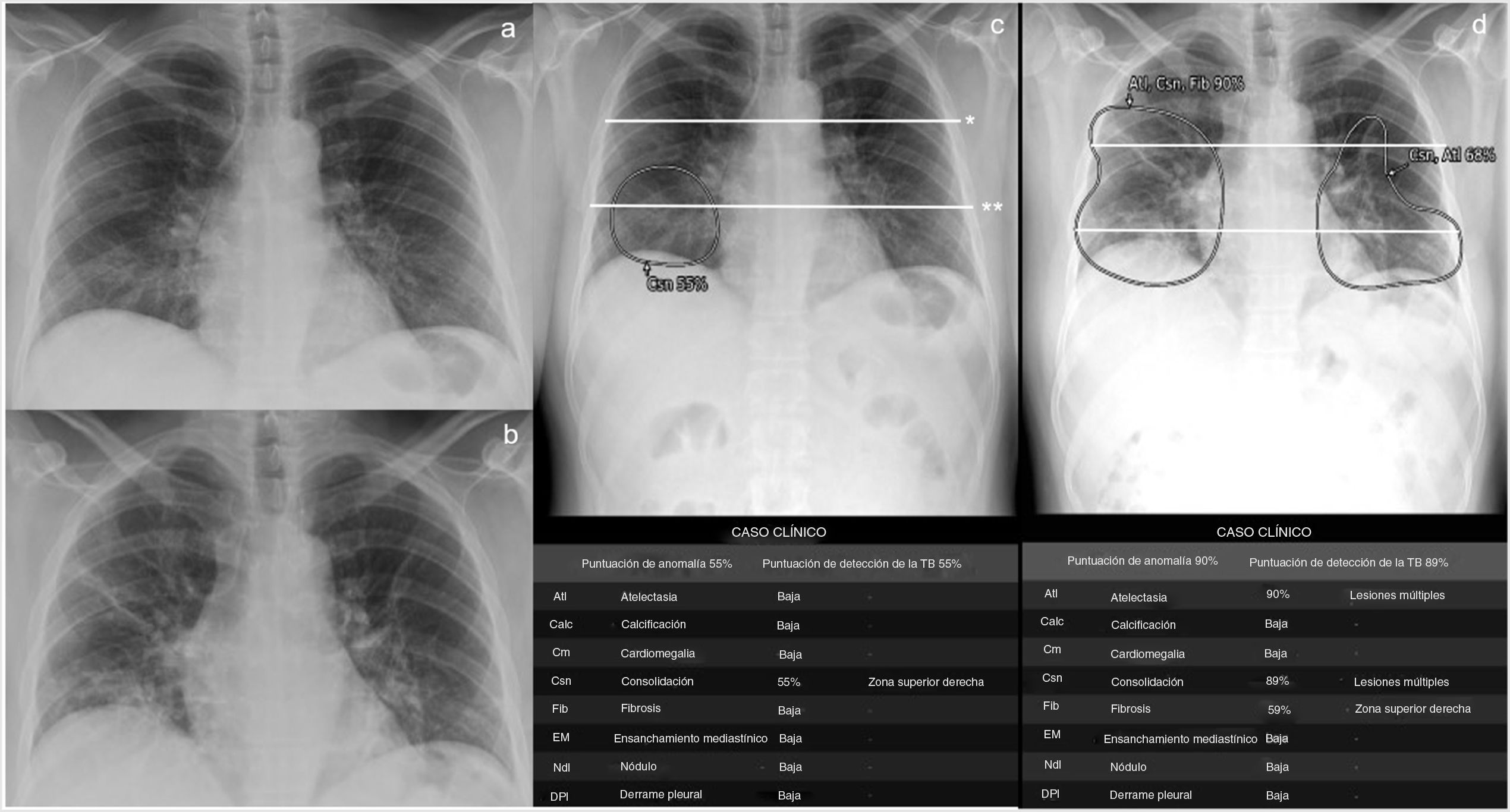
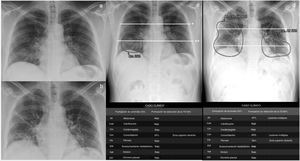
Thoracic Care Suite (que incorpora Lunit Insight CXR, GE Healthcare, Milwaukee, WI, Estados Unidos) es un algoritmo de IA comercial preparado para detectar 8hallazgos radiológicos anómalos relacionados con afecciones torácicas (fig. 2). En nuestro centro, el TCS está configurado con un umbral predeterminado y considera positivo cualquiera de estos hallazgos si su probabilidad es superior al 30%. En este estudio, solo los hallazgos pulmonares de TCS denominados por el programa como «consolidación», «nódulo» y «atelectasia» se consideraron hallazgos indicativos de neumonía COVID-19. La neumonía COVID-19 provoca una consolidación con morfología nodular11, especialmente al inicio, algo que el TCS interpreta como nódulos. Por consiguiente, si los nódulos detectados por TCS presentaban unos márgenes mal definidos según la interpretación del radiólogo (consolidaciones con morfología nodular, a diferencia de los nódulos intersticiales, con márgenes precisos), se incluían como hallazgos indicativos de neumonía COVID-19. Si el programa detectaba atelectasia en el interior de las consolidaciones, también se incluía como hallazgo indicativo de neumonía COVID-19 (fig. 2). En cambio, no lo incluimos si se trataba de un hallazgo aislado de atelectasia fuera del área de consolidación.
Paciente con febrícula, mialgia, malestar general y una semana de evolución con RT-PCR positiva para SARS-CoV-2 y neumonía visible en la radiografía torácica (RXT) en proyección posteroanterior, obtenida en días consecutivos (a y b) y detectada con la herramienta Thoracic Care Suite de GE Healthcare (que incorpora Lunit Insight CXR) (c y d). Los pulmones se dividen en 6campos dibujando una línea manual que atraviesa el margen inferior del cayado aórtico (*) y otra (**), que divide el pulmón por debajo de la primera en 2partes de tamaño superior-inferior lo más similar posible. El área de consolidación detectada por la herramienta, que afecta 2campos pulmonares en la primera RXT, está rodeada con un círculo en c. En el estudio de RXT realizado el día siguiente, la herramienta detecta un aumento de la extensión de las consolidaciones, con atelectasia entre ellas (d). La extensión de la afectación progresó de 2 a 6 campos pulmonares, es decir, 4 campos pulmonares en un día. El paciente precisó ventilación mecánica. Los datos que se presentan en las tablas siguientes, a saber, probabilidad (%) de cada resultado, ubicación de los resultados, resultados distintos a «consolidaciones», «atelectasia» y «nódulos» y la «puntuación de detección de tuberculosis» no se tuvieron en cuenta para este estudio.
Para cuantificar la extensión de la neumonía COVID-19, cada pulmón se dividió en 3campos pulmonares (fig. 2), según referencias previas7. El número de campos pulmonares afectados determinados por TCS con hallazgos indicativos de neumonía COVID-19 fue nuestra variable radiológica principal. El radiólogo comprobó las anomalías radiológicas identificadas por la herramienta de IA dentro de los campos pulmonares, con el fin de incluir únicamente hallazgos indicativos de neumonía COVID-19. El evaluador no corrigió el número de campos pulmonares afectados por hallazgos indicativos de neumonía COVID-19, obtenido según el resultado de IA. Se contabilizaron el número de campos pulmonares afectados en la primera (CP-RXT-IA1) y la segunda (CP-RXT-IA2) RXT. También se valoró la progresión o la mejoría dividiendo la diferencia entre CP-RXT-IA1 y CP-RXT-IA2 por los días entre ambas RXT y se definió como tasa de empeoramiento radiológico diario en RXT-IA=CP-RXT-IA2–CP-RXT-IA1 / días entre RXT1 y RXT2.
El proceso fue el siguiente: el radiólogo mostró la imagen de la RXT-IA en la estación de trabajo, representó líneas para dividir los campos pulmonares de forma manual (fig. 2) e interpretó si la semiología radiológica en las áreas descritas por la herramienta de IA eran hallazgos indicativos de neumonía COVID-19 en cada campo pulmonar. El número de campos afectados por hallazgos indicativos de neumonía COVID-19 se registró en una base de datos Excel. Se midió el tiempo necesario para completar todo el proceso del informe radiológico. En este caso, el tiempo usado por la herramienta de IA durante el periodo posterior al procesamiento de la imagen no se incluyó, ya que este procesamiento posterior ya se había realizado antes de recopilar los datos para este estudio. Sin embargo, en una situación clínica, la herramienta puede aplicarse de forma directa a la radiografía digital inmediatamente después de su obtención, y el resultado de IA se envía al sistema de comunicación y archivado de imágenes (PACS). Básicamente, la IA no precisa tiempo posterior al procesamiento. Un radiólogo con 12 años de experiencia en radiología torácica y de urgencias evaluó las imágenes RXT-IA incluidas en este estudio.
Variables no radiológicasEl criterio principal de valoración fue la necesidad de recurrir a la respiración asistida, en términos de ventilación mecánica no invasiva o intubación endotraqueal (criterios requeridos en el documento suplementario). También recopilamos datos sobre el sexo, las enfermedades concomitantes, el tratamiento inmunosupresor y los días transcurridos desde el inicio de los síntomas hasta la RXT1 y la RXT2.
Métodos estadísticosSegún un artículo previo6, asumiendo una proporción de necesidad de respiración asistida del 17%, una precisión del 6,5% y una tasa de sustitución del 10%, se calculó que el tamaño de la muestra teniendo en cuenta un intervalo de confianza del 95% era de 109 pacientes.
Las variables cuantitativas se expresaron como media±desviación estándar o mediana (rango intercuartílico, RIC) según la distribución normal o no normal, y las variables cualitativas mediante frecuencias absolutas y relativas. Se utilizaron las pruebas de la χ2, de Kruskal-Wallis y ANOVA para la comparación bivariante.
El rendimiento diagnóstico de las variables radiológicas se determinó mediante el área bajo la curva (area under the curve, AUC) en la curva operador-receptor (receiver operating characteristic, ROC), la sensibilidad y la especificidad, los cocientes de probabilidad positivo (CPP) y negativo (CPN), los valores pronósticos positivo (VPP) y negativo (VPN), todos con un intervalo de confianza del 95% (IC del 95%) y la prueba de DeLong para la comparación por pares de las curvas ROC.
El análisis multivariante mediante regresión logística binaria se realizó para determinar la asociación entre la necesidad de respiración asistida y los efectos principales de las variables no radiológicas.
Las diferencias se consideraron estadísticamente significativas si p<0,05 con IBM-SPSS-Statistics v 20 y Med-Calc v 12.7.0. JMPM (radiólogo) fue la persona que realizó el análisis.
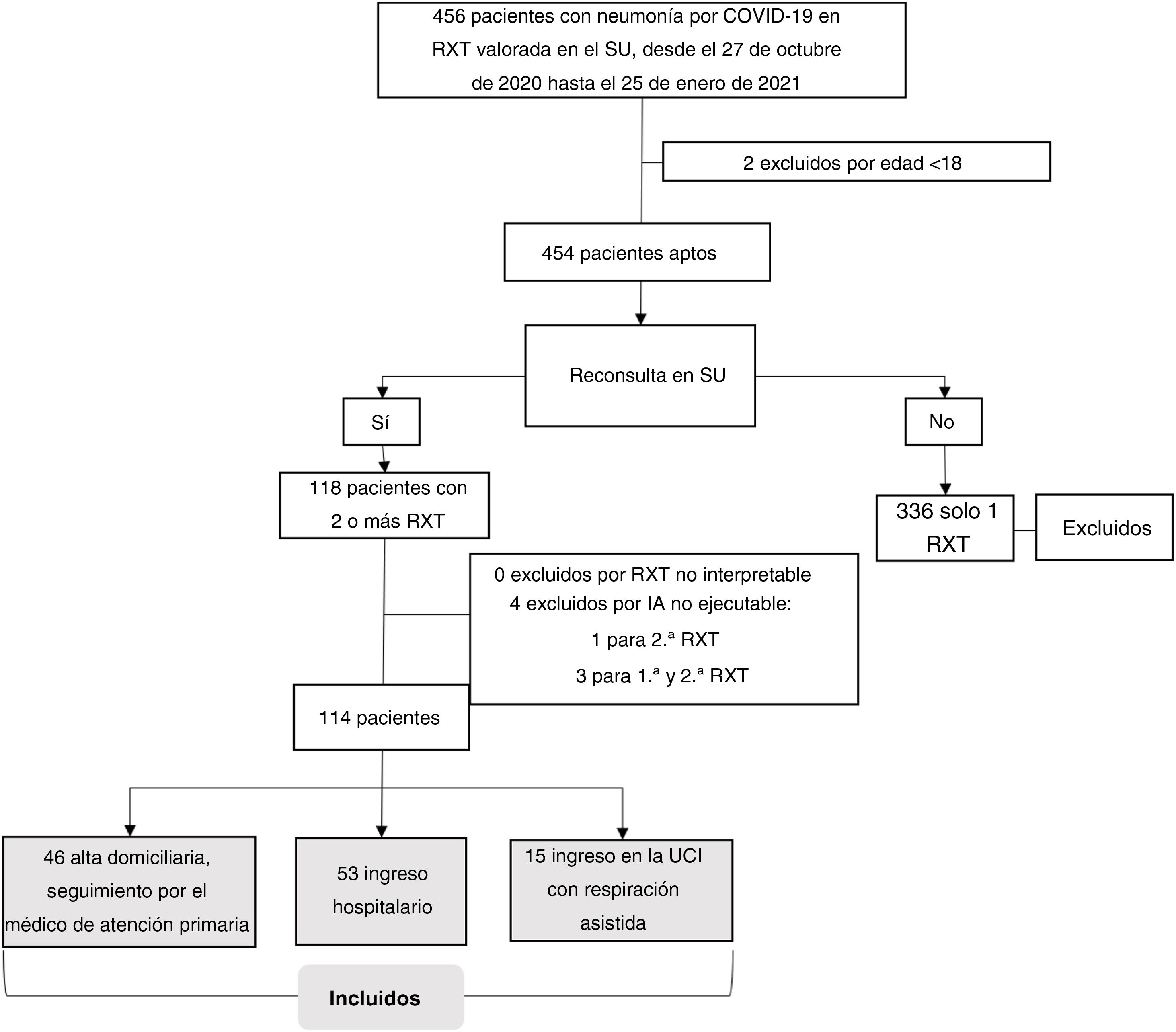
ResultadosMuestraSe incluyó a pacientes ambulatorios con COVID-19 considerados aptos de forma consecutiva desde el 27 de octubre de 2020 hasta el 25 de enero de 2021. La muestra inicial estuvo compuesta por 118 pacientes con RXT1 y RXT2. Fueron excluidos 4 pacientes por no poder obtenerse las imágenes de RXT-IA por cuestiones técnicas. En total se incluyó a 114 pacientes (57,4±14,2; 65 varones), 53 (46,5 %) precisaron ingreso hospitalario y 15 (13,2%) respiración asistida en la UCI (fig. 3). Las características de la muestra se presentan en la tabla 1.
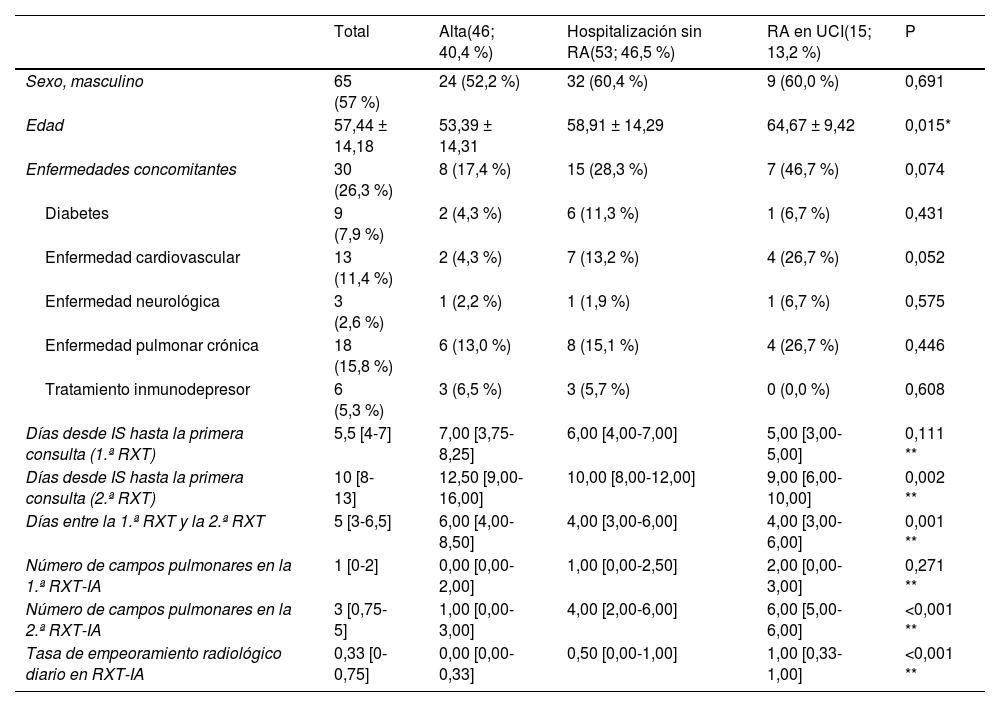
Características de la muestra
| Total | Alta(46; 40,4 %) | Hospitalización sin RA(53; 46,5 %) | RA en UCI(15; 13,2 %) | P | |
|---|---|---|---|---|---|
| Sexo, masculino | 65 (57 %) | 24 (52,2 %) | 32 (60,4 %) | 9 (60,0 %) | 0,691 |
| Edad | 57,44 ± 14,18 | 53,39 ± 14,31 | 58,91 ± 14,29 | 64,67 ± 9,42 | 0,015* |
| Enfermedades concomitantes | 30 (26,3 %) | 8 (17,4 %) | 15 (28,3 %) | 7 (46,7 %) | 0,074 |
| Diabetes | 9 (7,9 %) | 2 (4,3 %) | 6 (11,3 %) | 1 (6,7 %) | 0,431 |
| Enfermedad cardiovascular | 13 (11,4 %) | 2 (4,3 %) | 7 (13,2 %) | 4 (26,7 %) | 0,052 |
| Enfermedad neurológica | 3 (2,6 %) | 1 (2,2 %) | 1 (1,9 %) | 1 (6,7 %) | 0,575 |
| Enfermedad pulmonar crónica | 18 (15,8 %) | 6 (13,0 %) | 8 (15,1 %) | 4 (26,7 %) | 0,446 |
| Tratamiento inmunodepresor | 6 (5,3 %) | 3 (6,5 %) | 3 (5,7 %) | 0 (0,0 %) | 0,608 |
| Días desde IS hasta la primera consulta (1.ª RXT) | 5,5 [4-7] | 7,00 [3,75-8,25] | 6,00 [4,00-7,00] | 5,00 [3,00-5,00] | 0,111 ** |
| Días desde IS hasta la primera consulta (2.ª RXT) | 10 [8-13] | 12,50 [9,00-16,00] | 10,00 [8,00-12,00] | 9,00 [6,00-10,00] | 0,002 ** |
| Días entre la 1.ª RXT y la 2.ª RXT | 5 [3-6,5] | 6,00 [4,00-8,50] | 4,00 [3,00-6,00] | 4,00 [3,00-6,00] | 0,001 ** |
| Número de campos pulmonares en la 1.ª RXT-IA | 1 [0-2] | 0,00 [0,00-2,00] | 1,00 [0,00-2,50] | 2,00 [0,00-3,00] | 0,271 ** |
| Número de campos pulmonares en la 2.ª RXT-IA | 3 [0,75-5] | 1,00 [0,00-3,00] | 4,00 [2,00-6,00] | 6,00 [5,00-6,00] | <0,001 ** |
| Tasa de empeoramiento radiológico diario en RXT-IA | 0,33 [0-0,75] | 0,00 [0,00-0,33] | 0,50 [0,00-1,00] | 1,00 [0,33-1,00] | <0,001 ** |
Los resultados se muestran en función de frecuencia absoluta (porcentaje), media±desviación estándar si distribución normal, y mediana (cuartiles 25 y 75) en caso de distribución no normal. Respiración asistida significa necesidad de ventilación no invasiva o intubación endotraqueal. Pruebas de la χ2, prueba *ANOVA, prueba de **Kruskal-Wallis.
La respiración asistida y el ingreso en la unidad de cuidados intensivos no fueron consecuencia directa de la segunda evaluación clínica del paciente, sino del resultado final después de un periodo de hospitalización.
Abreviaturas
UCI: unidad de cuidados intensivos
IS: inicio de los síntomas
RA: respiración asistida
El número de campos pulmonares afectados en RXT-IA fue mayor en pacientes que precisaron respiración asistida, pero la significación estadística solo se alcanzó en RXT-IA2 (6,00 RIC: 5,00-6,00; 4,00 RIC: 2,00-6,00 y 1,00 RIC: 0,00-3,00 con respecto a la necesidad de respiración asistida, el ingreso y el alta hospitalaria, respectivamente; p<0,001). El momento de realización de la RXT2 desde el inicio de los síntomas osciló entre 8 y 13 días (RIC), con una mayor variabilidad en los pacientes más leves dados de alta de nuevo, con un RIC de 9 a 16 días (tabla 1). La mediana de tiempo transcurrido entre la RXT1 y la RXT2 fue de 5 días (RIC: 3,0-6,5), pero disminuyó a 4 (RIC: 3,00-6,00) en los pacientes que precisaron ingreso hospitalario o respiración asistida (p=0,001).
La progresión de los campos pulmonares afectados entre RXT-IA1 y RXT-IA2 fue un factor de riesgo independiente para la necesidad de respiración asistida. De hecho, la tasa de empeoramiento radiológico diario de RXT-IA fue superior en los pacientes que precisaron respiración asistida, con valores de 1,00 (RIC: 0,33-1,00); 0,50 (RIC: 0,00-1,00) y 0,00 (RIC: 0,00-0,33) para la necesidad de respiración asistida, el ingreso y el alta hospitalaria, respectivamente (p<0,001; tabla 1). El AUC de la tasa de empeoramiento radiológico diario en la RXT-IA para predecir la necesidad de respiración asistida fue de 0,771 (IC del 95%: 0,683-0,845; p<0,001; tabla 2). Cuando la neumonía progresó ≥0,5 campos pulmonares al día, se produjo un aumento de 4,2 veces en la necesidad de recurrir a la respiración asistida según la regresión logística binaria (IC del 95%: 1,19-14,52; p=0,025, tabla 3) con cifras de sensibilidad del 66,67 (IC del 95%: 38,4-88,2), especificidad del 74,75 (IC del 95%: 65,0-82,9), CPP del 2,64 (IC del 95%: 1,6-4,3), CPN del 0,45 (IC del 95%: 0,2-0,9), VPP de 28,6 (IC del 95%: 14,6-46,3) y VPN de 93,7 (IC del 95%: 85,8-97,9) para la necesidad de respiración asistida (tabla 2). Cuando la neumonía progresó en 0,67 campos pulmonares al día, la especificidad alcanzó 80,81 (IC del 95%: 71,7-88,0) y el VPN 94,1 (IC del 95%: 86,8-98,1), manteniendo la cifra de sensibilidad en 66,67 (38,4-88,2) (tabla 2).
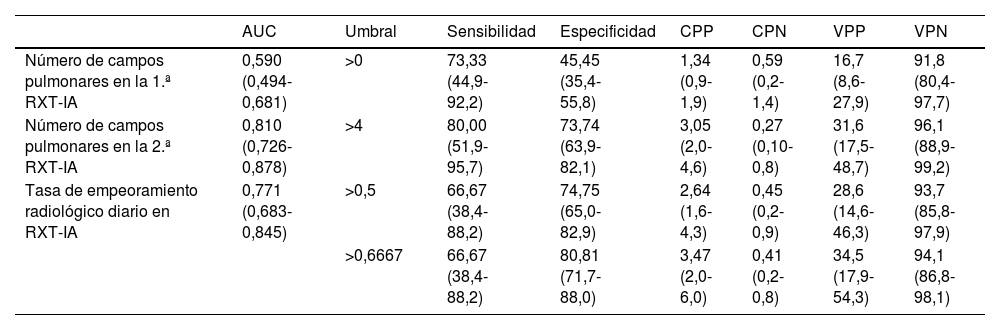
Rendimiento diagnóstico del número de campos pulmonares en la primera y segunda RXT-IA y tasa de empeoramiento radiológico diario en RXT-IA
| AUC | Umbral | Sensibilidad | Especificidad | CPP | CPN | VPP | VPN | |
|---|---|---|---|---|---|---|---|---|
| Número de campos pulmonares en la 1.ª RXT-IA | 0,590 (0,494-0,681) | >0 | 73,33 (44,9-92,2) | 45,45 (35,4-55,8) | 1,34 (0,9-1,9) | 0,59 (0,2-1,4) | 16,7 (8,6-27,9) | 91,8 (80,4-97,7) |
| Número de campos pulmonares en la 2.ª RXT-IA | 0,810 (0,726-0,878) | >4 | 80,00 (51,9-95,7) | 73,74 (63,9-82,1) | 3,05 (2,0-4,6) | 0,27 (0,10-0,8) | 31,6 (17,5-48,7) | 96,1 (88,9-99,2) |
| Tasa de empeoramiento radiológico diario en RXT-IA | 0,771 (0,683-0,845) | >0,5 | 66,67 (38,4-88,2) | 74,75 (65,0-82,9) | 2,64 (1,6-4,3) | 0,45 (0,2-0,9) | 28,6 (14,6-46,3) | 93,7 (85,8-97,9) |
| >0,6667 | 66,67 (38,4-88,2) | 80,81 (71,7-88,0) | 3,47 (2,0-6,0) | 0,41 (0,2-0,8) | 34,5 (17,9-54,3) | 94,1 (86,8-98,1) |
Los datos entre paréntesis son intervalos de confianza del 95 %.
AUC: área bajo la curva (area under the curve); CPN: cocientes de probabilidad negativa; CPP: cocientes de probabilidad positiva; RXT-IA: RXT procesada con la herramienta de IA; VPN: valor pronóstico negativo; VPP: valor pronóstico positivo.
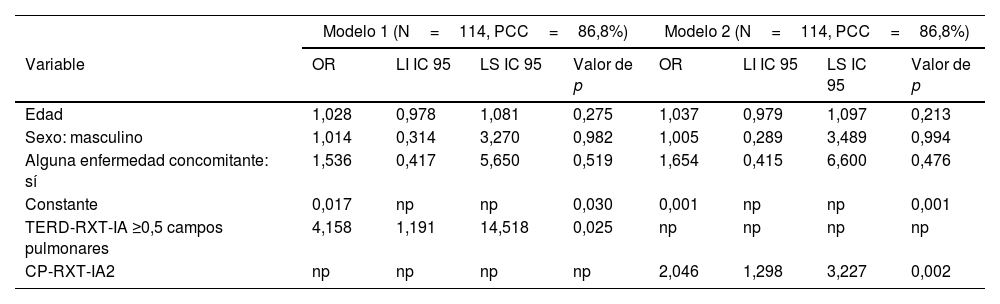
Modelos de regresión logística binaria para la tasa de empeoramiento radiológico de la RXT procesada con la herramienta de IA ≥0,5 campos pulmonares (modelo 1) y número de campos pulmonares afectados en la segunda RXT procesada con la herramienta IA (modelo 2)
| Modelo 1 (N=114, PCC=86,8%) | Modelo 2 (N=114, PCC=86,8%) | |||||||
|---|---|---|---|---|---|---|---|---|
| Variable | OR | LI IC 95 | LS IC 95 | Valor de p | OR | LI IC 95 | LS IC 95 | Valor de p |
| Edad | 1,028 | 0,978 | 1,081 | 0,275 | 1,037 | 0,979 | 1,097 | 0,213 |
| Sexo: masculino | 1,014 | 0,314 | 3,270 | 0,982 | 1,005 | 0,289 | 3,489 | 0,994 |
| Alguna enfermedad concomitante: sí | 1,536 | 0,417 | 5,650 | 0,519 | 1,654 | 0,415 | 6,600 | 0,476 |
| Constante | 0,017 | np | np | 0,030 | 0,001 | np | np | 0,001 |
| TERD-RXT-IA ≥0,5 campos pulmonares | 4,158 | 1,191 | 14,518 | 0,025 | np | np | np | np |
| CP-RXT-IA2 | np | np | np | np | 2,046 | 1,298 | 3,227 | 0,002 |
Las categorías de referencia para variables cualitativas dicotómicas fueron «sexo: femenino», «alguna enfermedad concomitante: no».
CP-RXT-IA2: número de campos pulmonares en la segunda RXT-IA; IC 95: intervalo de confianza del 95%; LI: límite inferior; LS: límite superior; np: no procede; OR: oportunidad relativa; PCC: porcentaje de clasificación correcta; RXT-IA: RXT procesada con la herramienta de IA; TERD-RXT-IA: tasa de empeoramiento radiológico diario de la RXT procesada con la herramienta de IA.
A pesar de que el CP-RXT-IA2 alcanzó mejor AUC (0,810; IC del 95 %: 0,657-0,886; tabla 2), no se obtuvieron diferencias significativas entre CP-RXT-IA2 y la tasa de empeoramiento radiológico diario de RXT-IA en la comparación por pares de las curvas ROC (p=0,550), y la capacidad pronóstica de la necesidad de respiración asistida del CP-RXT-IA2 fue peor de acuerdo con el análisis de regresión logística binaria, con un riesgo relativo de 2,05 (IC del 95%: 1,30-3,23; p=0,002, tabla 3).
Tiempo transcurrido hasta obtener los datos de RXT-IALas imágenes de RXT-IA incluidas en este estudio se evaluaron en una única sesión. Se evaluaron 2imágenes de RXT-IA en cada paciente, es decir, 228 imágenes (114×2). Cada imagen de RXT se cargó en el visor, la existencia de consolidaciones o nódulos con márgenes mal definidos se interpretó al ser detectadas mediante TCS y se anotó el número de campos pulmonares afectados por estos resultados. La sesión entera duró 98 min, es decir, se destinaron 25,78 segundos a cada imagen RXT-IA (98×60=5.880/228) o, en otras palabras, se evaluaron 2,33 imágenes de RXT-IA por minuto (228/98).
Variables no radiológicasAunque la edad de los pacientes que precisaron respiración asistida fue mayor en el análisis univariante (64,67±9,42; 58,91±14,29 y 57,44±14,18 años con respecto a la necesidad de respiración asistida, el ingreso y el alta hospitalarios, respectivamente; p=0,015) y tuvieron más tendencia a padecer enfermedades concomitantes (46,7%; 28,3%; 17,4%, respectivamente; p=0,074), estas variables no influyeron de forma independiente en el resultado de respiración asistida en el análisis multivariante (tablas 1 y 3).
DiscusiónEn este estudio observamos que el uso de la herramienta TCS para determinar la progresión inicial de las consolidaciones pulmonares en la neumonía COVID-19 es factible. En los casos que progresaron a una tasa de al menos «medio campo pulmonar al día», el riesgo de respiración asistida se cuadruplicó a corto plazo. El proceso radiológico completo para obtener el resultado de la extensión de la neumonía COVID-19 precisó, de promedio, 26 segundos por radiografía. Aunque el número de campos pulmonares afectados en la RXT2 obtuvo mejores cifras de AUC en nuestro análisis, la mejor capacidad pronóstica de la tasa de empeoramiento radiológico diario de RXT-IA puede verse influida por el valor añadido de la velocidad de empeoramiento, incluida en la ecuación para la última. Por el contrario, el momento en que se realizó la segunda radiografía varió entre los pacientes, dependiendo de su propia percepción del empeoramiento o de la percepción del médico de cabecera tras haber hablado con el paciente por teléfono.
En muchos centros, el informe de la RXT no se realiza debido a los escasos recursos humanos12. Por otro lado, durante la pandemia, la necesidad de elaborar informes radiológicos de una gran cantidad de pacientes con sospecha de neumonía COVID-19ha impulsado cambios para mejorar los resultados en radiología4. En estas circunstancias, los servicios de radiología están interesados en herramientas que proporcionen información diagnóstica y pronóstica útil de manera rápida, a pesar de no estar específicamente preparadas para la evaluación de la COVID-19. En este estudio hemos mostrado la eficacia de una herramienta de IA comercializada, inicialmente desarrollada para otras enfermedades pulmonares, aplicada a pacientes con neumonía COVID-19. Los radiólogos solo tendrían que invertir 26 segundos por resultado de RXT-IA para determinar el número de campos pulmonares afectados detectados por el algoritmo. Aplicar esta herramienta de forma sistemática ayudaría a detectar la progresión rápida de la neumonía. Otros trabajos sobre la aplicación de la IA al pronóstico de la COVID-19 a partir de pruebas de diagnóstico por la imagen, como la tomografía computarizada13, son menos intuitivos para los seres humanos y solo se han desarrollado en el laboratorio.
Según las revisiones sistemáticas y la valoración crítica de los modelos pronósticos de la COVID-1914, los únicos que han mostrado pruebas de fiabilidad para este fin no incluían variables radiológicas14,15. Sin embargo, hemos mostrado previamente que el uso sistemático de datos de seguimiento proporcionados por RXT en pacientes con COVID-19 proporcionaría información pronóstica crítica6. Por todos estos motivos, creemos que en muchos centros sobrecargados por la escasez de recursos, enormes cargas de trabajo, o ambas cosas al mismo tiempo, los algoritmos comercializados, a pesar de no estar específicamente preparados para estos resultados, pueden representar una ayuda significativa.
En varios estudios de IA se han registrado buenos resultados para predecir la necesidad de respiración asistida en función de la primera RXT realizada en el servicio de urgencias en pacientes con sospecha de neumonía COVID-1916-18. Sin embargo, no pueden compararse fácilmente con nuestros resultados debido a diferencias metodológicas. La forma en que proporcionamos asistencia radiológica a los pacientes de atención primaria en nuestro centro4 probablemente facilitó el hecho de realizar la RXT antes que en otros lugares. Si se demuestra que esto es cierto, podríamos haber detectado un mayor número de neumonías leves con la RXT1 y la diferencia entre los hallazgos radiológicos de la RXT1 y la RXT2 podría tener una mejor capacidad pronóstica que los hallazgos encontrados en nuestra RXT1. Sin embargo, seguimos pensando que la capacidad pronóstica de la diferencia entre RXT sería útil incluso en pacientes con neumonía más avanzada en el momento del diagnóstico. De hecho, la especificidad registrada (58,8%) fue peor cuando la IA se aplicó a la RXT117 que en nuestro enfoque de RXT1 frente a RXT2 (75%-81%). Esto significa que los pacientes que progresan rápidamente no se detectarían contando solo con los resultados de la RXT1. Por otro lado, a pesar de haber demostrado el valor pronóstico de las herramientas de IA también en TC torácicas realizadas en pacientes con neumonía COVID-1913,19, su utilidad es mucho más limitada, ya que la TC se limita a pacientes con sospecha de complicaciones20. Además, debido a la carga de trabajo actual de muchos servicios de radiología, no sería factible hacer una TC a todos los pacientes con sospecha de neumonía COVID-19 en el servicio de urgencias, en especial, cuando los resultados de la IA deben ser validados por un radiólogo.
Nuestro estudio tiene algunas limitaciones. Una primera limitación es que la sensibilidad y la especificidad de la progresión pulmonar de las lesiones específicas de la neumonía COVID-19 mediante 0,5 campos o más al día para predecir la necesidad de respiración mecánica es del 66% y el 74%, respectivamente. Aunque en nuestro caso, el rendimiento de la herramienta de IA fue inferior al de un evaluador humano para determinar la gravedad de la afectación pulmonar6, la ventaja de la herramienta en comparación con el evaluador humano es que se puede aplicar a todas las RXT debido a sus rápidos resultados. Otra limitación es que la progresión en el número de campos pulmonares solo se ha tenido en cuenta cuando un campo pulmonar afectado no se encontraba afectado en la RXT previa, pero no si su progresión se había producido dentro del mismo campo previamente afectado. Aunque se podría extrapolar a un empeoramiento en el mismo campo pulmonar, consideramos que la afectación de un nuevo campo pulmonar es más pertinente ya que, excepto en áreas contiguas a campos ya afectados, lo más probable es que la aparición de consolidaciones en un campo nuevo implique más afectación pulmonar que la progresión en un campo ya afectado. Por otro lado, no hemos medido si la progresión de la neumonía COVID-19 detectada con la RXT-IA predice la progresión antes de lo que lo haría el empeoramiento de los marcadores inflamatorios o la oxigenación. Sin embargo, la información de nuestro estudio puede obtenerse a partir de RXT realizadas durante el seguimiento de la neumonía, es decir, sin pruebas adicionales. Por último, la edad y las enfermedades concomitantes pueden no haber influido en el pronóstico debido al pequeño tamaño de nuestra muestra, pero creemos que es improbable que esto haya modificado la capacidad pronóstica independiente de la variable radiológica utilizada en este estudio.
De hecho, la escasez estructural de recursos humanos, las políticas de los servicios de radiología relativas a los informes de RXT o las enormes cargas de trabajo en momentos de epidemia podrían tener un impacto relevante en la forma en que la herramienta de IA podría usarse en el ámbito de urgencias. Sea cual sea la razón, las consecuencias potenciales no deberían ignorarse. En particular, en momentos de epidemia en los que los radiólogos no pueden garantizar una rápida evaluación de los resultados de IA antes de que estén disponibles para el médico que solicita la prueba, los resultados de RXT-IA falsos positivos podrían dar lugar a procedimientos innecesarios. Del mismo modo, los falsos negativos en RXT-IA (p. ej., en nuestro caso, el riesgo de progresión no se detectaría en el 33,3 % [100-66,7%] de los pacientes) probablemente darían lugar a decisiones insuficientes de seguimiento. Es por este motivo por lo que necesitamos soluciones de IA mucho más sensibles en el futuro. Confiar en los resultados de IA negativos posiblemente reducirá la carga de trabajo del radiólogo, ya que evitará la evaluación de RXT clasificadas como normales.
En resumen, la progresión inicial de la neumonía COVID-19 en medio campo pulmonar al día o más, tal como se muestra mediante la herramienta TCS, cuadruplica el riesgo de insuficiencia respiratoria que requiere ventilación mecánica. Con esta información proporcionada por la IA, el radiólogo tarda un promedio de 26 segundos en registrar el número de campos pulmonares afectados.
FinanciaciónEste estudio no ha recibido ninguna subvención específica de organismos de financiación del sector público, comercial o sin ánimo de lucro. Los autores se limitan a valorar el rendimiento del programa proporcionado por la empresa General Electric, específicamente para este estudio, sin ninguna relación contractual ni remuneración por los servicios.
Autoría- •
Responsable de la integridad del estudio: JMPM.
- •
Concepción del estudio: JMPM, JMGS.
- •
Diseño del estudio: JMPM.
- •
Recopilación de los datos: JMPM, RPC.
- •
Análisis e interpretación de los datos: JMPM.
- •
Procesamiento estadístico: JMPM; MBR.
- •
Búsqueda bibliográfica: JMPM.
- •
Redacción del artículo: JMPM.
- •
Revisión crítica del manuscrito y contribución significativa a nivel intelectual: JMPM, JMGS, MBR, RPC.
- •
Aprobación de la versión final: JMPM, JMGS, MBR, RPC.
Los autores declaran no tener ningún conflicto de intereses.