En los dientes que han sido sometidos a tratamiento endodóncico resulta imperativo sellar las cavidades de acceso con materiales provisionales, para evitar la recontaminación por microorganismos entre visitas, mientras se espera a la restauración final1-4. Los materiales más empleados son los que contienen sulfato de calcio-oxido de zinc (Cavit, 3M ESPE) y oxido de zinc-eugenol reforzado con resina de polimetilmetacrilato (IRM, Caulk/ De Trey Dentsply). También se usan con frecuencia los materiales que contienen ionómero de vidrio (Ketac, 3M ESPE). Un material provisional de fraguado dual relativamente nuevo, DuoTemp (Coltène/Whale-dent), contiene oxido de zinc/sulfato de zinc modificado con resina de metacrilato y libre de eugenol. Su fabricante defiende que DuoTemp presenta una adecuada resistencia a la carga después de 40 segundos de fotopolimerización y que exhibe unas excelentes propiedades de sellado. DuoTemp contiene además fluoruro sódico, lo que es considerado por el fabricante como una ventaja adicional del material.
Los materiales de restauración provisional para endodoncia, además de sellar bien la cavidad de acceso, deben ser resistentes a las fuerzas mecánicas y a los cambios térmicos, no presentar toxicidad, y no afectar a la adhesión futura de los materiales de restauración a la estructura dentaria. Ketac ha demostrado comportarse bien bajo carga; sin embargo, su capacidad de sellado se ha demostrado inferior a la de Cavit en varios estudios5-7. Se ha demostrado que Cavit presenta unas cualidades de sellado superiores, incluso en cavidades de acceso complejas8. Sin embargo, la capacidad de sellado de Cavit, se ve limitada por su baja resistencia a la carga mecánica9. Otro estudio5 investigó la técnica de sándwich con IRM y Cavit, y obtuvo resultados de filtración favorables con esta combinación empleando un modelo de filtración mediante tinción. IRM, con y sin carga mecánica, ha demostrado un mal comportamiento a la filtración6,10.
El uso de IRM como material de restauración provisional se ve limitado por su contenido en eugenol que interfiere con la capacidad de algunos materiales de restauración para adherirse a la estructura dentaria11.
Resulta necesario investigar nuevos materiales o combinaciones de ellos, dado que ninguno de los actuales materiales de restauración provisional, solos o en combinación, ha demostrado unas propiedades de sellado buenas y predecibles. Este estudio fue diseñado para investigar la capacidad de sellado de una técnica que combinaba los materiales Ketac y Cavit y comparar los resultados obtenidos con los de otros materiales de restauración provisional comúnmente empleados. La idea fue determinar si esta combinación permitiría aprovechar las ventajas de ambos materiales. El propósito de este estudio de filtración bacteriana fue evaluar el sellado de Cavit, Ketac, DuoTemp, y una técnica combinada con Ketac y Cavit.
Método y materiales
Cien molares mandibulares humanos que habían sido extraídos recientemente fueron asignados aleatoriamente a uno de los cuatro grupos experimentales (n = 20 por grupo) y a los dos grupos control (n = 10 por grupo). Los molares seleccionados presentaban unas coronas intactas con una altura mínima de 10 mm. Ninguno de los dientes presentaba restauraciones anteriores. La dimensión mesiodistal de la corona era de al menos 10 mm, y la vestíbulolingual de al menos 8 mm. Las cavidades de acceso presentaban unas dimensiones aproximadas de 5 mm en sentido vestibuloingual y 8 mm en sentido mesiodistal. En los 10 dientes control negativos no se preparó ninguna cavidad de acceso, y en los 10 dientes control positivos se preparó cavidad de acceso pero esta no se restauró con ningún material. Cada molar de los cuatro grupos experimentales se preparó con una cavidad de acceso, y a continuación se colocó una bolita de algodón pellet (Richmond Dental) en el suelo de la cámara.
Los materiales provisionales se mezclaron siguiendo las instrucciones de los fabricantes, y a continuación se procedió a obturar con ellos las cavidades de acceso hasta el algodón. Las cavidades de acceso se prepararon de forma que el grosor de cada muestra fuera de aproximadamente 4 mm (Cavit). Después se seccionó la corona de cada diente justo por debajo de la furca de forma que la estructura radicular quedara en contacto con el medio de cultivo preparado en la cámara inferior.
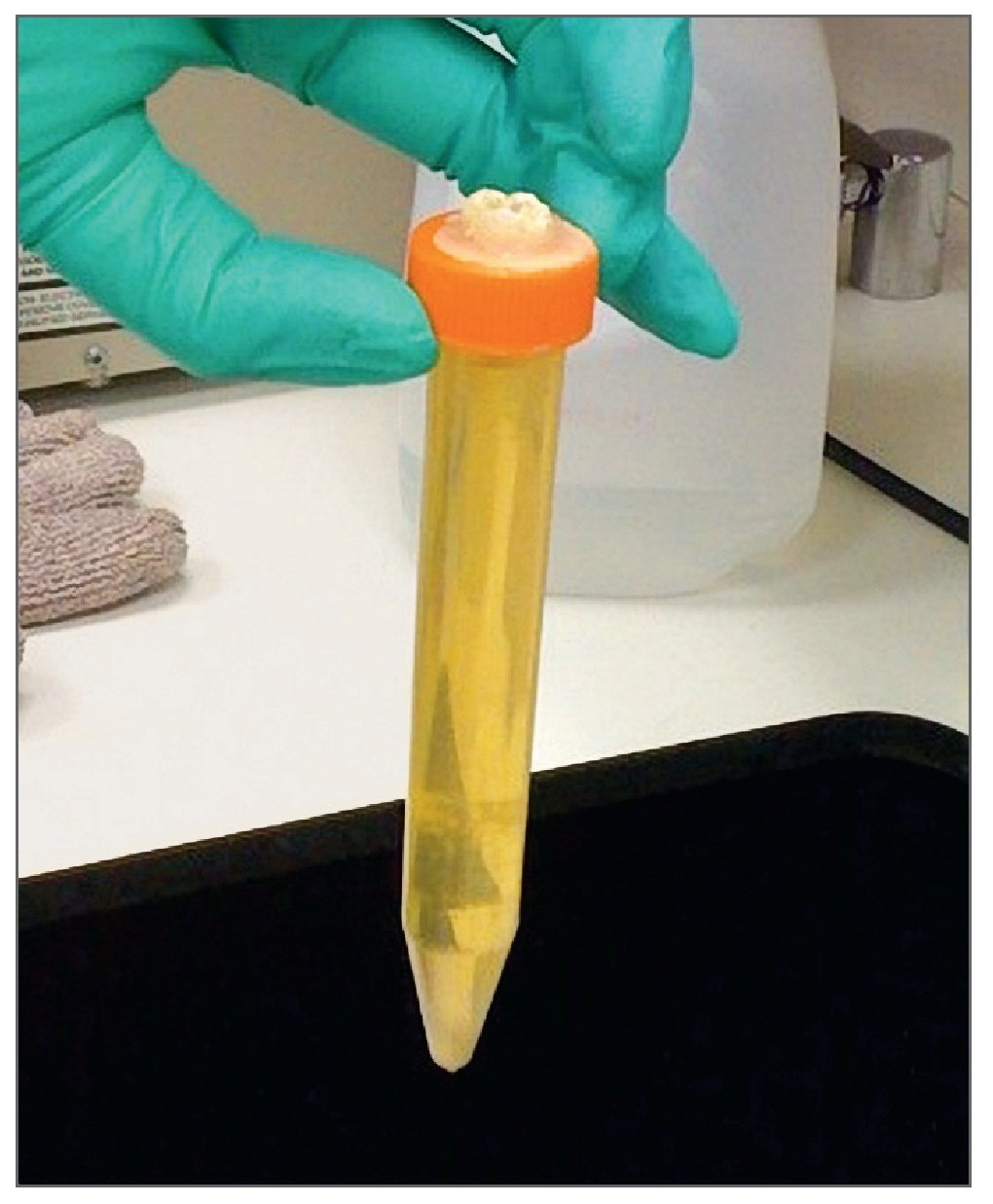
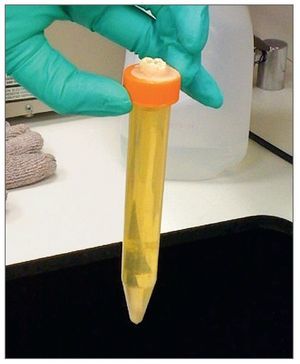
Cada corona seccionada se pegó a la tapa de un tubo de ensayo de plástico estéril (Fisher Scientific) mediante metilmetacrilato (Dentsply/Caulk), y a continuación se le dio una capa final de sellado con cianocrilato (Krazy Blue). A continuación se esterilizó todo el montaje (fig. 1) empleando gas de oxido de etileno (ASP). El interior del tubo de ensayo se rellenó con una infusión de agar cerebro-corazón (BD) mediante pipetas estériles (Fisher Scientific). A continuación se aplicó, dos veces al día, Streptococcus mutans (ATCC) sobre la corona seccionada. Las muestras se almacenaron a 37 ºC y 100% de humedad. La filtración bacteriana se determinó por la presencia de turbidez, lo que indicaba crecimiento bacteriano en la infusión de agar cerebro-corazón. La presencia o ausencia de turbidez fue determinada por un único observador a los 7, 14, 21 y 28 días.
Figura 1. Vista lateral del dispositivo.
Se empleó la prueba exacta de Fisher para analizar los datos recogidos en todos los grupos experimentales en cada periodo de tiempo. El nivel de significación alfa se estableció a p < 0,05.
Resultados
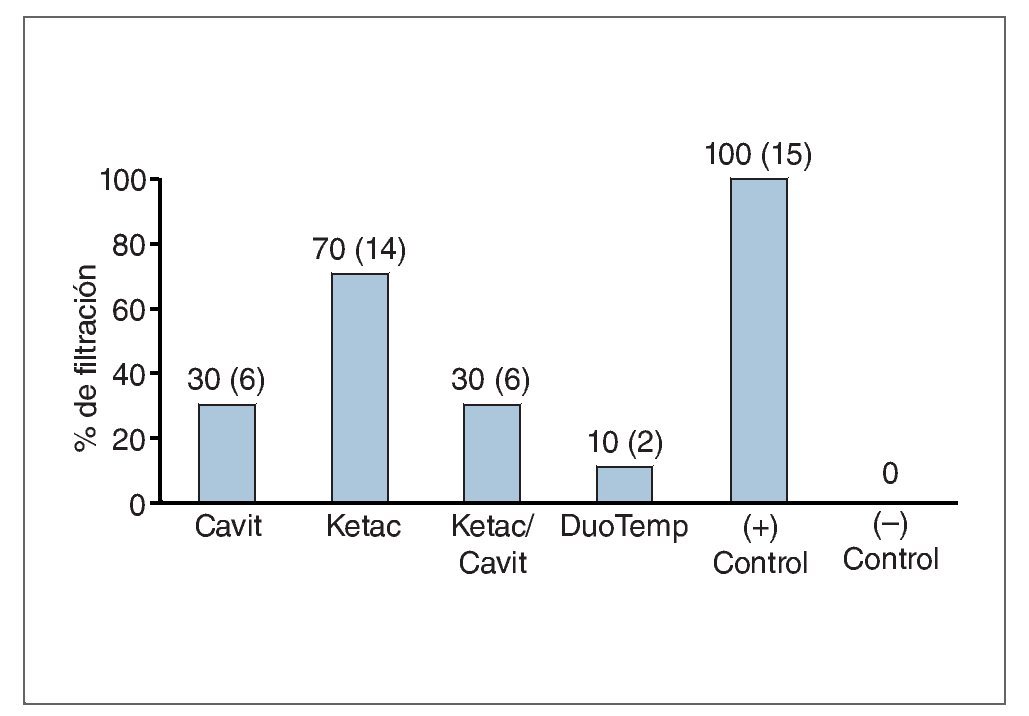
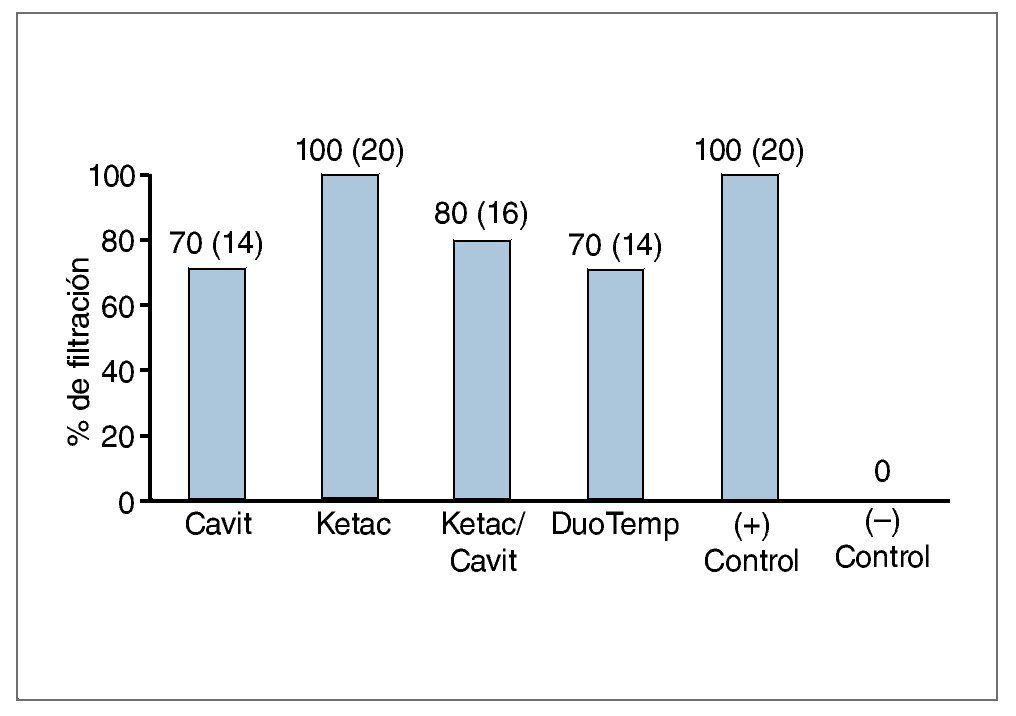
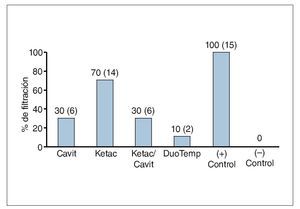
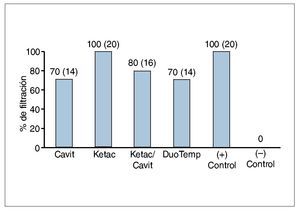
Transcurridos 14 días, y durante el resto del periodo de observación no se encontraron ya más muestras filtradas. Todos los controles positivos resultaron filtrados en todos los periodos de tiempo, y ninguno de los controles negativos resultó filtrado en ningún momento. El número de muestras filtradas en cada grupo experimental en todos los periodos de tiempo se muestra en las figuras 2 y 3. Cuando se compararon los grupos de diferentes periodos de tiempo mediante la prueba exacta de Fisher, Ketac, empleado solo, no resultó significativamente diferente desde el punto de vista estadístico de los controles positivos a los 7 días. Se detectaron diferencias estadísticamente significativas (p < 0,05) en todos los periodos de tiempo entre los grupos de Cavit y Ketac, así como entre Ketac y DuoTemp. Se detectaron diferencias significativas entre el grupo de Ketac y el de la combinación de Ketac/Cavit solo en el periodo inicial de 7 días (fig. 2). No se detectaron diferencias estadísticamente significativas entre DuoTemp y Cavit ni entre DuoTemp y la combinación Ketac/cavit en ninguno de los periodos de tiempo (fig. 3). A excepción del grupo de Ketac solo, a los 7 días, ninguno de los otros grupos presentó diferencias estadísticamente significativas respecto a los controles positivos en todos los periodos de tiempo.
Figura 2. Porcentaje de filtración de las muestras medido a los 7 días (número de muestras entre paréntesis).
Figura 3. Porcentaje de filtración de las muestras medido a los 14, 21 y 28 días (número de muestras entre paréntesis). No se registró ningún cambio entre los 14 y los 28 días.
Discusión
Resulta importante determinar la filtración bacteriana asociada a los materiales de restauración provisional que se emplean en los tratamientos endodóncicos, ya que una de las propiedades fundamentales que estos materiales deben cumplir es la prevención de la recontaminación del sistema de conductos por las bacterias orales entre visitas y después de terminar el tratamiento de endodoncia mientras se espera a la restauración final definitiva. En este estudio, se seleccionó S mutans por ser un microorganismo que se encuentra de forma habitual en la cavidad oral y que se ha empleado con frecuencia en otros estudios sobre filtración bacteriana. Se ha demostrado que después de un tratamiento endodóncico, uno de los factores más importantes para el éxito del tratamiento y para la conservación del diente tratado, es la colocación de la restauración final12. No existe ningún material de obturación totalmente inmune a la filtración bacteriana, y se ha demostrado que cuando después de terminar el tratamiento de conductos radiculares no quirúrgico no se coloca pronto la restauración permanente, el sistema de conductos radiculares se contamina antes de 60 días13. Cualquier grado de filtración contribuye a la contaminación global y conduce en último término al fracaso del tratamiento de conductos radiculares no quirúrgico completado.
Cavit ha demostrado presentar unas excelentes propiedades de sellado siempre y cuando se utilice con un grosor mínimo de 3,5 mm14. En el presente estudio, ninguno de los materiales de restauración provisional resultó totalmente resistente a la filtración bacteriana. Un 60% de los especimenes en los cuatro grupos experimentales demostró filtración a los 14 días. El periodo de 14 días para la filtración, es similar al de un reciente estudio que investigó IRM, Cavit, y Dyract como materiales de restauración provisional en un modelo de filtración bacteriana15. Existe una gran variedad de materiales de restauración provisional, cada uno con su propia composición. Algunos se recomiendan para uso en tratamientos endodóncicos; otros no8,16,17. Algunos estudios han reseñado que Cavit o una técnica de sándwich con Ketac y otros materiales permiten conseguir propiedades de sellado mejores que Ketac solo5. Otros han sugerido que ni siquiera la restauración final aporta un sellado adecuado18. Esto ha inducido a algunos investigadores a sugerir el empleo de barreras del orificio coronal para añadir otra capa protectora frente a la filtración19. Sin embargo estas barreras del orificio no resuelven completamente el problema ya que crean obstáculos al dentista restaurador cuando quiere colocar una restauración de muñón y poste. Por todo ello, hasta el momento de colocar la restauración permanente, el clínico que realiza el tratamiento endodóncico debe seguir confiando en algunos de los materiales de restauración provisional actualmente disponibles como barrera principal frente a la filtración. Aunque esto no representa un problema en las clínicas pequeñas, en las clínicas grandes y facultades de odontología se debe seguir informando a los pacientes de que cuánto antes se reemplace la restauración provisional mayores son las posibilidades de éxito del tratamiento endodóncico. Los retrasos en la colocación de restauraciones permanentes en los dientes endodonciados son la razón por la que los investigadores siguen buscando un material provisional que sea: capaz de prevenir la filtración, fácil de colocar y retirar, y suficientemente fuerte como para resistir las fuerzas oclusales generadas durante la masticación.
Una limitación de este estudio es que se trata de un estudio ex vivo. La extrapolación de este estudio a un modelo in vivo tendría un alcance muy limitado, ya que no resultaría ético realizar un estudio verdaderamente aleatorio. En lugar de ello lo que se puede llevar a cabo es un estudio de cohorte prospectivo. El diseño de este último sería más aceptable desde el punto de vista ético siempre y cuando hubiera suficiente evidencia de que las barreras de orificio protegen de forma suficiente de la contaminación coronal. La filtración/contaminación se comprobaría después mediante el análisis de la reacción en cadena de la polimerasa (PCR), que evalúa el ADN tanto de las bacterias vivas como de las muertas presentes, en la cámara de la preparación dentaria y por encima del orificio de barrera. De esta manera, los investigadores podrían estudiar adecuadamente la filtración de estas restauraciones provisionales (teóricamente sin colocar al paciente en riesgo de contaminación). Así, se podrían estudiar las restauraciones provisionales en funcionamiento frente a múltiples factores como las fuerzas de la masticación, el flujo salival, y el posible compromiso de los ácidos bacterianos, pero sin limitarse a ellos.
Este presente estudio examinó el insulto mínimo esperado de filtración bacteriana respecto a los materiales de restauración provisional Cavit, Ketac, y DuoTemp. Por lo tanto este estudio resulta útil para establecer directrices sobre el empleo de DuoTemp en un modelo in vivo.
Conclusión
Dentro de las limitaciones de este estudio de filtración bacteriana ex vivo, ninguno de los materiales estudiado consiguió un sellado fiable después de 14 días. Más de un 60% de los especimenes de los cuatro grupos experimentales demostró filtración a los 14, 21 y 28 días. Los grupos de Cavit y DuoTemp fueron los que obtuvieron el mejor sellado a lo largo del estudio. Estos resultados sugieren que después de los tratamientos endodóncicos, para minimizar la microfiltración coronaria, los pacientes deben recibir la restauración final o por lo menos el muñón de reconstrucción antes de dos semanas.
Correspondencia: G.R. Hartwell.
University of Medicine and Dentistry of New Jersey. Department of Endodontics. 110 Bergen Street. Room C-790. PO Box 1709. Newark. NJ 07101-1709. Estados Unidos.
Correo electrónico: hartwega@umdnj.edu
Presentado en la sesión anual de la American Association of Endodontics, Orlando, Florida, 1 de mayo de 2009.