Cariprazina es un antipsicótico de nueva generación que actúa como agonista parcial de los receptores de la dopamina D2 y D3, y de los receptores de serotonina 5HT1A. Actualmente, la cariprazina está aprobada por la Asociación Española del Medicamento para el tratamiento de la esquizofrenia, y por la Food and Drug Administration para el tratamiento de las fases maníacas, depresivas y mixtas asociadas al trastorno bipolar. La evidencia científica disponible, así como varias guías clínicas internacionales, acreditan la eficacia, seguridad y tolerabilidad de este fármaco y avalan su uso en cualquier tipo de episodio agudo del TB, con o sin síntomas mixtos. Los efectos adversos más frecuentes son los síntomas extrapiramidales, especialmente la acatisia. En dichos estudios se propone individualizar la dosis de cariprazina en función del tipo y la gravedad del episodio, así como de la tolerabilidad del paciente. Los estudios más recientes parecen indicar también un potencial beneficio para la prevención de recaídas en la fase de eutimia, y actualmente se están llevando a cabo ensayos clínicos para evaluar tanto este aspecto como el impacto del fármaco en la esfera cognitiva y en la funcionalidad de los pacientes. En conclusión, el uso de cariprazina en el TB está plenamente justificado desde un punto de vista científico, con unos beneficios globales que sobrepasan ampliamente el perfil de efectos adversos.
Cariprazine is a new generation antipsychotic that acts as a partial agonist of dopamine D2 and D3 receptors and serotonin 5HT1A receptors.
Cariprazine has now been approved by the Spanish Medicines Association (Asociación Española del Medicamento (AEM)) for the treatment of schizophrenia, and by the Food and Drug Administration (FDA) for the treatment of the manic, depressive, and mixed states associated with bipolar disorder (BD). The available scientific evidence, and several international guidelines attest to the efficacy, safety, and tolerability of this drug and endorse its use in any type of acute BD episode, with or without mixed symptoms.
The most frequent adverse effects are extrapyramidal symptoms, especially akithisia. Studies propose individualising the dose of cariprazine to the type and severity of the episode, and the patient’s tolerability. The most recent studies also seem to indicate a potential benefit in the prevention of relapse in the euthymia phase, and clinical trials are currently underway to evaluate this and the impact of the drug on patients’ cognitive sphere and functionality. To conclude, the use of cariprazine in bipolar disorder is fully justified from a scientific perspective, with overall benefits that far outweigh the adverse effects profile.
El trastorno bipolar (TB) es una enfermedad psiquiátrica que se caracteriza por episodios maníacos, hipomaníacos, depresivos o mixtos alternados con períodos de eutimia1. El TB tiene una prevalencia en la población general del 2%2 y se asocia a nivel global, a una pérdida de funcionalidad con consecuencias significativas en la esfera personal y sociolaboral, un aumento de la comorbilidad médica y psiquiátrica, y un incremento de los casos de suicidio3. A nivel clínico es posible distinguir entre el TB tipo I, cuyo diagnóstico requiere la presencia de al menos un episodio maníaco a lo largo de la vida, y el TB tipo II, definido por la existencia de al menos un episodio hipomaníaco y uno depresivo, pudiéndose asociar ambos a la presencia de episodios depresivos o mixtos1. Concretamente, los episodios depresivos y en particular los episodios con síntomas mixtos suponen un factor de riesgo relevante para la conducta suicida4–6.
Las guías de tratamiento actuales diferencian entre intervenciones de primera, segunda y tercera línea para el TB7, las cuales tienen en cuenta la evidencia disponible en cuanto a eficacia, seguridad, tolerabilidad y riesgo de viraje relacionado con los tratamientos. A la vez, existen recomendaciones centradas en el tratamiento del episodio maníaco agudo, el episodio depresivo agudo y el tratamiento de mantenimiento, enfocándose este último en la prevención de recurrencias7.
Los tratamientos psicosociales forman parte del plan de manejo individualizado en el TB; algunos de estos, como la terapia cognitivo-conductual o la terapia familiar, han mostrado resultados en la recuperación del episodio agudo y en la prevención de recaídas3.
A nivel farmacológico, existen diferencias en cuanto a las estrategias recomendadas en función de la fase de la enfermedad. En el tratamiento de los episodios maníacos, las guías del Canadian Network for Mood and Anxiety Treatments (CANMAT) recomiendan como tratamiento de primera línea el uso de estabilizadores del estado de ánimo, como el litio o el ácido valproico, así como antipsicóticos como la quetiapina, asenapina, aripiprazol, paliperidona, risperidona y cariprazina, en monoterapia o bien en combinación7. Las últimas guías de práctica clínica españolas, por otra parte, recomiendan el uso de risperidona, olanzapina, quetiapina, aripiprazol o litio como tratamiento de primera elección8, pero están pendientes de actualización, ya que se publicaron hace algo más de 10 años. En los pacientes que se encuentren bajo tratamiento con litio o valproato, deben revisarse los niveles plasmáticos correspondientes y optimizarse la dosis en caso de ser necesario. En caso de inefectividad del litio en monoterapia, podría considerarse añadir tratamiento con un antipsicótico9.
Por otro lado, el tratamiento de primera línea recomendado por las guías CANMAT en los episodios depresivos incluye el uso de antipsicóticos atípicos como quetiapina o lurasidona, así como estabilizadores del estado de ánimo como litio o lamotrigina. Estos antipsicóticos, incluyendo cariprazina, son actualmente los únicos fármacos aprobados por la United States Food and Drug Administration (FDA) para el tratamiento a corto plazo de los episodios depresivos en el TB10. Las combinaciones de lurasidona con litio o ácido valproico, o de lamotrigina junto con otro de los fármacos mencionados, también se consideran de primera elección7. Cabe destacar que cariprazina se recomienda como alternativa farmacológica de segunda línea, ya que su aprobación por la FDA en dicha indicación es muy reciente. Por su parte, las guías de práctica clínica española recomiendan el uso de quetiapina como tratamiento de primera línea8. En caso de encontrarse con una medicación eutimizante, debe revisarse la adherencia a esta y si los niveles plasmáticos son adecuados, optimizar la dosis si es necesario, pudiéndose además plantear la adición de otros fármacos antipsicóticos o eutimizantes9. En este sentido, el tratamiento de combinación suele ser la norma en el manejo de la depresión bipolar11.
Por otra parte, el uso de antidepresivos no está recomendado en primera instancia en la depresión bipolar por su potencial para inducir episodios maníacos o hipomaníacos y para aumentar la frecuencia de ciclación de episodios3,12. Otros tratamientos recomendados en el tratamiento de la depresión bipolar incluyen la terapia electroconvulsiva y la estimulación magnética transcraneal11,.
Generalmente, es recomendable como tratamiento de mantenimiento, continuar con la estrategia farmacológica iniciada en la fase aguda; no obstante, existen excepciones, como es el caso del tratamiento con antidepresivos. En los pacientes en fase de eutimia, las guías CANMAT recomiendan el tratamiento en monoterapia o bien, en combinación con litio, ácido valproico, quetiapina, lamotrigina, asenapina o aripiprazol7. Las guías clínicas españolas recomiendan como tratamiento de mantenimiento el uso de litio o la combinación de este con valproato para la prevención de episodios de cualquier tipo. De igual modo, se recomienda añadir quetiapina a cualquiera de estos 2 eutimizantes en el caso de haber asociado respuesta previa a este antipsicótico. También se recomienda el uso de lamotrigina en monoterapia para la prevención de episodios depresivos y de olanzapina para la prevención de episodios maníacos. Otros expertos recomiendan como tratamiento de mantenimiento de primera elección únicamente el litio, y considerar alternativas, como valproato, olanzapina o quetiapina, cuando este no sea bien tolerado9. Generalmente, los antipsicóticos recomendados muestran una eficacia clínicamente relevante, pero limitaciones a nivel de tolerabilidad. No obstante, recientemente han surgido estudios con antipsicóticos atípicos de nueva generación con un mejor perfil de tolerabilidad que apoyan su eficacia en la depresión bipolar13.
CariprazinaCariprazina es un derivado de la piperazina que actúa como agonista parcial de los receptores de dopamina D2 y D3, y de los receptores de serotonina 5HT1A14,15. También presenta un antagonismo 5HT2B, 5HT2A y de los receptores de histamina H114,16. No se une a los receptores colinérgicos y presenta una baja unión a los receptores 5HT2C y α-1 adrenérgicos14,17,18.
En comparación con aripiprazol y brexpiprazol, que también son agonistas parciales D2 y D3, la característica más diferencial de cariprazina es su alta afinidad por los receptores D3, más elevada que la de la propia molécula de dopamina19. En situaciones de baja actividad dopaminérgica, se comporta como un agonista parcial, mientras que, en situaciones de actividad dopaminérgica alta, actúa como antagonista14. Los receptores D3 están localizados sobre todo en el sistema límbico, el hipotálamo, el área tegmental ventral y la sustancia negra20. Su acción sobre estos receptores parece mediar una parte significativa de sus efectos procognitivos, antidepresivos y antianhedónicos, observados tanto en modelos animales como en humanos21–25. Una hipótesis plantea que el agonismo parcial en los autorreceptores presinápticos D3 del área tegmental ventral y sustancia negra desinhibe la liberación de dopamina en el córtex prefrontal, promoviendo un ambiente pro-dopaminérgico en esta área y explicando sus efectos beneficiosos26. Además, la actividad agonista parcial sobre los receptores 5HT1A también podría contribuir a los efectos antidepresivos15 y, juntamente con un bajo potencial de inhibición de la transmisión dopaminérgica en el estriado, a una incidencia de síntomas extrapiramidales (SEP) más baja que otros antipsicóticos18. Las acciones sobre el receptor D3 también podrían explicar un potencial efecto sobre el sistema de recompensa27, hecho que podría ser relevante en el tratamiento del TB, frecuentemente asociado al abuso de sustancias tóxicas28. Finalmente, la actividad agonista parcial/antagonista sobre los receptores D2 podría explicar las propiedades antimaníacas y antipsicóticas de la molécula29.
En relación con sus características farmacocinéticas, cariprazina se absorbe rápidamente por vía oral de manera independiente a la toma de alimentos30, y llega a una concentración plasmática máxima entre las 3 y 5 horas después de su administración31. Tiene un gran volumen de distribución y se puede encontrar en varios tejidos del organismo32. Una característica destacable es su potencial como tratamiento oral de larga duración. Cariprazina se metaboliza por el citocromo P450 3A4 (CYP3A4) y, en menor medida, por el citocromo CYP2D6, presentando una semivida de eliminación de entre 2 y 4 días14. Sus 2 metabolitos principales, la desmetil cariprazina y la didesmetil cariprazina, son farmacológicamente equipotentes a la cariprazina33,34 y presentan una semivida de eliminación de entre una y 3 semanas35, la más prolongada de entre todos los antipsicóticos atípicos. En consecuencia, el equilibrio estacionario puede tardar varias semanas en alcanzarse36. Por esta misma razón, la omisión de una dosis de cariprazina puede que no tenga unas consecuencias clínicas adversas significativas36. La cariprazina no necesita ajuste de dosis al combinarla con litio o ácido valproico, pero sí con el uso concurrente con inhibidores o inductores (como la carbamazepina) del CYP3A437. La eliminación renal de la cariprazina y de sus metabolitos es mínima32, y se puede usar de forma segura en los pacientes con insuficiencia renal o hepática leve o moderada37. De igual manera, su metabolismo no está afectado por el sexo, etnia o consumo de tabaco37. Los estudios en los pacientes de más de 65 años tratados con cariprazina no son suficientes para conocer con detalle su respuesta a la molécula, por lo que se recomienda un ajuste cuidadoso38.
En la actualidad, la cariprazina está aprobada por la Agencia Europea del Medicamento (AEM) como tratamiento agudo y de mantenimiento de la esquizofrenia en los adultos38, asociando un efecto procognitivo y una mejoría en los síntomas negativos propios de la enfermedad39. Además, la molécula está aprobada por la FDA para el tratamiento de episodios maníacos, mixtos y depresivos asociados al TB tipo I (TBI) en los adultos, en un rango de dosis de 3-6 mg/día para los 2 primeros tipos y de 1,5-3 mg/día para el último40. A la vez, las guías CANMAT[7] recomiendan su uso como tratamiento de primera línea en episodios de manía, y de segunda línea en episodios depresivos, en consonancia con las indicaciones aprobadas por la FDA en 2018. Finalmente, hasta el momento no ha habido evidencia suficiente como para recomendar su uso como tratamiento de mantenimiento en el TB, ya que el ensayo clínico controlado con placebo todavía está en fase de reclutamiento.
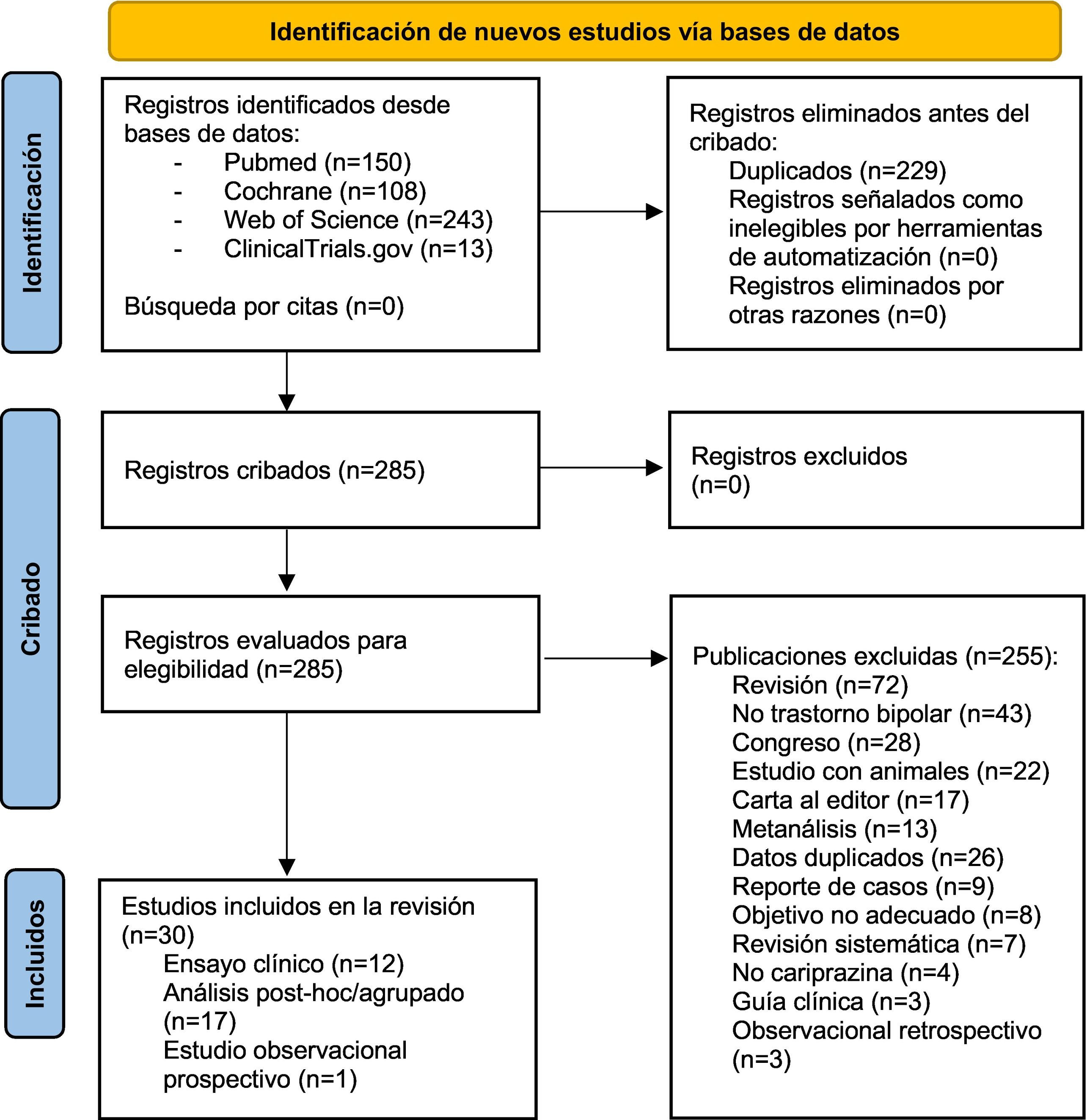
MétodosEstrategia de búsqueda e identificación de estudiosEsta revisión sistemática se realizó siguiendo las recomendaciones de la declaración Preferred Reporting Items for Systematic reviews and Meta-Analyses (PRISMA) 2020, y se registró en PROSPERO (ID: CRD42022351999). El diagrama de flujo PRISMA se muestra en la figura 1 y la lista de verificación PRISMA se encuentra en la tabla 1. Los autores utilizaron las bases de datos PubMed, Cochrane, Web of Science y ClinicalTrials.gov para la búsqueda de estudios publicados en cualquier idioma hasta el mes de agosto de 2022. Para ello, se utilizó el algoritmo (cariprazin* OR «vraylar» OR «rgh-188» OR «reagila») AND (bipolar* OR mani*). También se llevó a cabo una búsqueda manual de las referencias disponibles en la sección de bibliografía de los artículos seleccionados para identificar artículos relevantes para el estudio. No se buscó literatura gris.
Ensayos clínicos aleatorizados finalizados basados en el tratamiento de cariprazina en trastorno bipolar
| Primer autor (año) | Tipo de estudio | Número de ensayo clínico | Diseño | Rango de edad | Sexo femenino (%) | Número de brazos | Comparador | Tamaño muestral | Duración del tratamiento (semanas) | Dosis de cariprazina (mg) | Diagnóstico | Medida principal | Medidas secundarias | Herramienta de medida | Resultados principales |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Calabrese (2014) | ECA, doble ciego, fase III | NCT01058668 | Multicéntrico | 18-65 | - | 3 | Placebo | 497 | 3 | 3-6, 6-12 | TBI, episodio maníaco o mixto | Eficacia | Seguridad, tolerabilidad | YMRS, CGI-S, MADRS, PANSS | Mayor eficacia respecto a placebo en ambos grupos de cariprazina. En cuanto a tolerabilidad, solamente hay diferencias significativas en SEP; mayor frecuencia con cariprazina |
| Durgam (2014) | ECA, doble ciego, fase II | NCT00488618 | Multicéntrico | 18-65 | 33,5 | 2 | Placebo | 236 | 3 | 3-12 | TBI, episodio maníaco o mixto | Eficacia | Seguridad, tolerabilidad | YMRS, CGI-S | Diferencias significativas a favor de cariprazina en todos los ítems de YMRS. Mayor incidencia de SEP con cariprazina |
| Sachs (2015) | ECA, doble ciego, fase III | NCT01058096 | Multicéntrico | 18-65 | 35,9 | 2 | Placebo | 312 | 3 | 3-12 | TBI, episodio maníaco | Eficacia | Seguridad, tolerabilidad | YMRS | Mayor eficacia de cariprazina respecto al placebo. Mayor incidencia de SEP en el grupo tratado con cariprazina |
| Durgam (2016) | ECA, doble ciego, fase II | NCT01396447 | Multicéntrico | 18-65 | 61,4 | 4 | Placebo | 584 | 6 | 0,75; 1,5; 3 | TBI, episodio depresivo | Eficacia | Seguridad, tolerabilidad | MADRS, CGI-S | Mayor eficacia con cariprazina 1,5 mg/día respecto a 0,75 mg/día, 3 mg/día y placebo. Menor incidencia de EA con dosis inferiores a 3 mg/día |
| Earley (2017) | ECA, doble ciego, fase III | NCT02670551 | Multicéntrico | 18-65 | 59,2 | 3 | Placebo | 488 | 6 | 1,5; 3 | TBI, episodio depresivo | Eficacia | Seguridad, tolerabilidad | MADRS | Mayor eficacia respecto al placebo en los pacientes tratados con cariprazina tanto a 1,5 mg/día como a 3 mg/día. Buen perfil de tolerabilidad con cariprazina |
| Earley (2020) | ECA, doble ciego, fase III | NCT02670538 | Multicéntrico | 18-65 | 62,7 | 3 | Placebo | 493 | 6 | 1,5; 3 | TBI, episodio depresivo | Eficacia | Seguridad, tolerabilidad | MADRS | Diferencias estadísticamente significativas en cuanto a la eficacia con cariprazina 1,5 mg/día, pero no con cariprazina 3 mg/día, en comparación con el placebo. Un estudio previo con las mismas dosis muestra mayor eficacia en ambos grupos respecto al placebo |
| Yatham (2020) | ECA, doble ciego, fase II | NCT00852202 | Multicéntrico | 18-65 | 63,9 | 3 | Placebo | 224 | 8 | 0,25-0,75, 1,5–3 | TBI o TBII, episodio depresivo | Eficacia | Seguridad, tolerabilidad | MADRS | Diferencias no significativas en cuanto a la eficacia, con elevada incidencia de la respuesta al placebo como factor de confusión. Un análisis post-hoc posterior muestra una mayor eficacia en el grupo de cariprazina. Similar perfil de efectos adversos en ambos grupos de tratamiento |
CGI-S: Clinical Global Impression-Severity; EA: efectos adversos; ECA: ensayo clínico aleatorizado; MADRS: Montgomery-Asberg Depression Rating Scale; PANSS: Positive and Negative Syndrome Scale; SEP: sintomatología extrapiramidal; TBI: trastorno bipolar tipo I; TBII: trastorno bipolar tipo II; YMRS: Young Mania Rating Scale.
Los autores utilizaron el programa Rayyan para eliminar registros duplicados y realizar el cribado de artículos. Los títulos y resúmenes de los artículos identificados se examinaron para determinar la elegibilidad para la revisión sistemática. Dos autores (Ana Giménez-Palomo y Cristian-Daniel Llach) realizaron este proceso de manera independiente y después acordaron conjuntamente los estudios a incluir. En caso de discrepancia, ambos autores discutieron cada caso hasta lograr un consenso. El proceso fue supervisado por Eduard Vieta.
Los criterios de inclusión fueron ensayos clínicos, estudios post-hoc, y estudios observacionales prospectivos, que midieran parámetros de eficacia, seguridad y tolerabilidad de la cariprazina como tratamiento en las poblaciones de los pacientes diagnosticados de TB según los criterios del DSM o la CIE. La búsqueda se realizó teniendo en cuenta todas las fases del tratamiento del TB: episodios de manía o depresión aguda, mantenimiento y prevención de recaídas. Además, solo se incluyeron aquellos artículos que utilizaran escalas de valoración validadas, como la Young Mania Rating Scale (YMRS), la Montgomery-Asberg Depression Rating Scale (MADRS) o la Hamilton Depression Rating Scale (HDRS).
Se excluyeron revisiones, metaanálisis, estudios observacionales retrospectivos, editoriales, capítulos de libro, extractos de conferencias, resúmenes de presentación de pósteres y reportes de casos o de series de casos.
Extracción y análisis de datosDos de los autores (Ana Giménez-Palomo y Cristian-Daniel Llach) crearon una base de datos en el programa Excel para extraer la información de los artículos seleccionados. Se extrajeron los siguientes datos: nombre del primer autor, año de publicación, tipo de estudio, número de registro de ensayo clínico, duración del ensayo, edad media o rango, porcentaje de mujeres, criterios de inclusión, criterios de exclusión, variable principal, variables secundarias, número y tipo de brazos de tratamiento, población incluida, dosis utilizadas, puntuación basal de la población en las escalas de valoración, resultados, efectos adversos, y número de abandonos.
Tras la búsqueda en las diferentes bases de datos mencionadas se obtuvieron un total de 514 registros, siendo 229 de estos duplicados, los cuales se eliminaron durante la revisión. Con la revisión individual de títulos y resúmenes, se eliminaron registros según los criterios de inclusión y exclusión establecidos, obteniéndose finalmente 30 registros distintos.
ResultadosEficacia en manía y episodios mixtosSe han realizado numerosos ensayos clínicos aleatorizados (ECA) con cariprazina para evaluar la eficacia de este fármaco en la esquizofrenia. Sin embargo, otros estudios centran su atención en el tratamiento con cariprazina de las diferentes fases del TB. La tabla 1 muestra los diferentes ECA finalizados hasta la fecha.
Diferentes ECA en fase III han comparado la eficacia de cariprazina con placebo en el tratamiento de la manía o de los episodios mixtos (según la definición del DSM-IV-TR) en función de cambios en la escala Young Mania Rating Scale (YMRS), habiendo demostrado diferencias significativas41–43.
Uno de los ECA (NCT01058668) evaluaba la eficacia de cariprazina en los pacientes con TB tipo I que presentaran un episodio agudo maníaco o mixto, distinguiendo un grupo de pacientes tratados con dosis de cariprazina de 3-6 mg/día y otro grupo tratado con dosis de 6-12 mg/día. Al comparar la eficacia de este fármaco con el placebo, la cariprazina mostró mayor eficacia en ambos grupos42.
Otro de los ECA (NCT01058096) evaluó mediante un estudio multicéntrico la eficacia de la cariprazina en el tratamiento de los episodios maníacos, en dosis de entre 3 y 12 mg al día, en comparación con el placebo, mostrando una mejoría significativa de la sintomatología maniforme respecto a placebo41. Por otro lado, otro ECA (NCT00488618) consistió en un estudio multicéntrico que incluyó a los pacientes con un episodio maníaco o mixto43, comparando la eficacia de cariprazina en dosis de 3-12 mg al día con la de placebo, mostrando diferencias estadísticamente significativas en la puntuación de la escala YMRS a las 3 semanas.
Un estudio post-hoc44 que incluyó los resultados agrupados de los 3 ECA disponibles sobre manía (NCT01058096, NCT01058668 y NCT00488618) mostró una reducción significativa respecto a placebo en la escala YMRS (p < 0,001). Otro estudio post-hoc45 incluyó a 3 ECA (NCT00488618, NCT01058096 y NCT01058668) que evaluaban la eficacia de cariprazina en episodios maníacos en dosis de entre 3 y 12 mg, y mostró que el porcentaje de los pacientes con un cambio de sintomatología en la escala YMRS de moderada/severa (puntuación igual o superior a 2 en ítems puntuados del 0 al 4 o puntuación igual o superior a 4 en aquellos puntuados de 0 a 8) a leve o ausencia de síntomas en 3 semanas era superior en cariprazina en comparación al placebo en los 11 ítems (p < 0,001 en todos ellos). A las 3 semanas, el porcentaje de pacientes con síntomas leves o sin síntomas maniformes era de 22,5% en los pacientes tratados con cariprazina y 13,5% en individuos tratados con el placebo (p < 0,001). En esta línea, otro estudio post-hoc de los mismos ECA mostró unas tasas de respuesta y remisión significativamente superiores en aquellos pacientes tratados con cariprazina, que a la vez no asociaban un viraje depresivo. Finalmente, un estudio exploratorio46 apoya una mejoría en los 11 ítems de la escala YMRS en los pacientes con TB tipo I que presentaban un episodio maníaco o mixto, así como un mayor porcentaje en los pacientes tratados con cariprazina con síntomas leves o ausencia de síntomas respecto a placebo (p < 0,001).
La eficacia de cariprazina en los pacientes con manía y episodios mixtos también se ha evaluado en relación con la impresión clínica global. En primer lugar, cabe destacar que la mejoría en la puntuación de la escala de impresión clínica global (CGI-S) fue generalmente significativa en los 3 ECA disponibles (NCT01058096, NCT01058668 y NCT00488618), estudiándose como parámetros secundarios de eficacia. En esta línea, un estudio post-hoc47 que incluyó estos 3 ECA corroboró que los pacientes tratados con cariprazina mostraban una mejor impresión clínica global respecto a placebo, mejorando la puntuación media de la escala y asociando un mayor porcentaje de pacientes que pasaba a una categoría de enfermedad menos severa.
Finalmente, un estudio post-hoc en los pacientes con TB y un episodio agudo maníaco o mixto mostró que, en los 3 estudios incluidos (NCT01058668, NCT00488618, NCT01058096), cariprazina en dosis de entre 3 y 12 mg/día presentaba una eficacia significativamente superior a placebo en la reducción de la puntuación de la escala YMRS y en todos sus ítems, así como en la mejoría en la CGI-S48.
Eficacia en la depresión bipolarA pesar de que la mayoría de los estudios de cariprazina se centraron inicialmente en el tratamiento de los episodios de manía, otros ensayos más recientes han aportado evidencia científica acerca de su potencial utilidad en la depresión bipolar. Un total de cuatro ECA (2 de fase II y 2 de fase III) seleccionaron a los pacientes con un episodio depresivo en contexto de un TB.
Un primer ECA multicéntrico de fase II (NCT00852202)49, llevado a cabo entre 2009 y 2010, reclutó a un total de 224 participantes diagnosticados tanto con TBI como con TB tipo II (TBII), comparando un brazo de placebo con 2 brazos de tratamiento activo en dosis flexibles: uno a dosis bajas (0,25-0,75mg/día) y otro a dosis altas (1,5-3 mg/día). La variable principal fue el cambio en la puntuación de la escala MADRS a las 8 semanas de tratamiento. Ningún grupo de tratamiento activo logró diferenciarse de los resultados del placebo en relación con la variable primaria (cambio en la puntuación de la escala MADRS) ni secundaria (cambio en la puntuación de la escala CGI-I) a las 8 semanas de tratamiento. Las posibles razones que explicaron la ausencia de eficacia fueron una elevada proporción de respuesta a placebo en algunos centros participantes, la inclusión de una muestra heterogénea (pacientes con TBI y TBII), y una titulación del fármaco demasiado rápida que conllevó una alta tasa de efectos adversos en el grupo de dosis altas y, en consecuencia, un posible efecto negativo sobre las variables de eficacia. El efecto adverso más significativo fue la acatisia, presente hasta en el 17% de los pacientes en el grupo tratado con dosis altas (en comparación con el 4% del grupo placebo).
La experiencia obtenida en el primer ECA sirvió posteriormente para llevar a cabo 3 estudios con un diseño más adecuado a los objetivos planteados. Un segundo ECA multicéntrico de fase II (NCT01396447) reclutó a más del doble de los pacientes que el anterior (un total de 571 pacientes), incluyendo solo a los pacientes con TBI, y comparó un brazo del placebo con 3 brazos del tratamiento activo en dosis fijas con 0,75 mg/día, 1,5 mg/día y 3 mg/día de cariprazina respectivamente. Este estudio demostró una mayor eficacia de 1,5 mg/día de cariprazina en el tratamiento de la depresión bipolar, con una reducción significativa de la variable principal (puntuación de la escala MADRS a las 6 semanas de tratamiento) respecto a placebo (LSMD - 4.0 [CI 95%: -6,3 a -1,6; p-valor ajustado de 0,003]). El resto de las dosis de tratamiento con cariprazina no lograron diferenciarse de los resultados del placebo. De manera parecida, el brazo de 1,5 mg/día de cariprazina fue el único que presentó una reducción significativa de ambas tasas de respuesta y remisión según los criterios MADRS en comparación con el placebo, y el brazo de 3 mg/día mostró superioridad solo en la tasa de respuesta. En este estudio también se mostró una mejor tolerabilidad al fármaco en comparación con el primer ECA, disminuyendo la proporción de los pacientes incluidos en los brazos del tratamiento activo con un total de efectos adversos del 77 al 60%50.
En la misma línea, el estudio NCT0267055151 fue un ECA multicéntrico de fase III realizado entre 2016 y 2017 que incluyó un total de 478 pacientes con TBI. En este caso, los pacientes se distribuyeron aleatoriamente en 3 brazos de tratamiento en dosis fijas: placebo, cariprazina 1,5 mg/día y cariprazina 3 mg/día. De nuevo, solo el brazo de cariprazina 1,5mg/día mostró una reducción significativa de la variable principal (puntuación de la escala MADRS a las 6 semanas de tratamiento) respecto a placebo. Por otra parte, el grupo tratado con 3 mg/día de cariprazina mostró una reducción en la puntuación de la escala MADRS, que no supuso una diferencia estadísticamente significativa (p = 0,1051). Ningún brazo de tratamiento con cariprazina mostró una reducción significativa en las tasas de respuesta o remisión según los criterios MADRS en comparación con el placebo.
Finalmente, en otro ECA multicéntrico de fase III (NCT02670538)52 se aleatorizaron un total de 475 pacientes con TBI en los mismos grupos que el anterior: placebo, cariprazina 1,5 mg/día y cariprazina 3 mg/día. En este caso, no obstante, ambos grupos de tratamiento activo mostraron una reducción estadísticamente significativa en la variable principal, idéntica también al anterior estudio para el brazo de cariprazina 1,5 mg/día y el de 3 mg/día. En comparación con el placebo, también se consiguieron tasas de respuesta (en el caso del brazo de 3 mg/día de cariprazina) y de remisión (en ambos brazos de tratamiento activo) significativamente más elevadas, siempre según los criterios MADRS.
La eficacia de amplio espectro se evaluó en un estudio post-hoc53 que incluyó 3 ECA sobre depresión en TBI (NCT01396447, NCT02670551 y NCT02670538) con un total de 1.383 pacientes, y excluyendo un cuarto estudio que había incluido a los pacientes con TBII (NCT00852202). Los resultados agrupados mostraron una diferencia estadísticamente significativa en la puntuación de la escala MADRS a la semana 6 desde el inicio del tratamiento en aquellos pacientes tratados con cualquier dosis de cariprazina comprendida entre 1,5 y 3 mg/día. Por otra parte, se reportó una mejoría significativa en todos los síntomas depresivos considerados como ítems individuales en la escala MADRS en los pacientes tratados con cariprazina, incluyendo el ítem de ideación suicida, y solo con una excepción: el ítem de tensión interna. Considerando los brazos de 1,5 mg/día y 3 mg/día por separado, también se objetivó una mejoría en la mayoría de los ítems analizados. Este estudio también analizó los resultados de seguridad y tolerabilidad, que fueron consistentes con otros estudios descritos más adelante.
Finalmente, otro estudio post-hoc sobre los mismos ECA (NCT01396447, NCT02670551 y NCT02670538) mostró que cariprazina es eficaz en la depresión bipolar independientemente de las características basales de los pacientes, incluyendo los determinantes sociodemográficos (edad, sexo, etnia, índice de masa corporal), la duración del episodio a tratar, el número de episodios maníacos o depresivos previos, la polaridad predominante, la gravedad de la enfermedad al inicio del tratamiento, y la toma previa de medicación para el TB.
Más allá de la evidencia de la efectividad de cariprazina en la depresión bipolar generada en los últimos años, actualmente existen nuevos estudios que pretenden obtener resultados en la misma línea. Uno de ellos (NCT050605499) se centra en el estudio mediante PET-Scan antes y durante el tratamiento para objetivar el rol del receptor de dopamina D3, sobre el que actúa cariprazina, en casos de depresión bipolar.
Seguridad y tolerabilidadEn primer lugar, cabe destacar que cariprazina fue generalmente segura y bien tolerada en cada uno de los ECA que se llevaron a cabo para estudiar su eficacia tanto en manía como en depresión bipolar. Tres estudios post-hoc analizaron los resultados de seguridad y tolerabilidad de dichos ECA de forma agrupada.
Un primer estudio post-hoc44 analizó los resultados agrupados de los 3 ECA centrados en el tratamiento de los episodios maníacos (NCT01058096, NCT01058668 y NCT00488618), incluyendo un total de 1.065 pacientes. En este estudio, cariprazina asoció una mayor tasa de efectos adversos (79,6%, similar en todos los grupos de dosis) que el placebo (67,4%), siendo los más frecuentes la acatisia (19,8% para el brazo de 3-6 mg/día y 20,6% para el brazo de 9-12 mg/día, en comparación con el 4,8% en el placebo), los SEP (26,2% para el brazo de 3-6 mg/día y 29,2% para el brazo de 9-12 mg/día, en comparación con el 11,5% en el placebo), la inquietud (6,7% para cariprazina, similar entre todos los grupos de dosis, en comparación con el 2,3% en el placebo) y los vómitos, generalmente de intensidad leve o moderada. Solo los SEP y el estreñimiento mostraron una relación dosis-respuesta con cariprazina. No se observaron casos de viraje depresivo, y la tasa de EA severos fue baja y similar para todos los grupos. Finalmente, no se objetivaron diferencias relevantes a nivel metabólico: no hubo cambios en el peso o en los parámetros de laboratorio analizados, a excepción de la glucemia (que aumentó en 7 mg/dL en comparación a los 1,7 mg/dL en el placebo) y de los triglicéridos (que aumentaron en 3,1 mg/dL en comparación con una disminución de 4,4 mg/dL con el placebo). Los niveles medios de prolactina se vieron reducidos en ambos grupos, y no se asociaron cambios electrocardiográficos en ninguno de ellos, a pesar de que un mayor porcentaje de pacientes tratado con 9-12 mg/día de cariprazina (12,2%) pasó de cifras de normotensión a hipertensión arterial, en comparación con el placebo (5,3%).
Un segundo estudio post-hoc54 se centró en los resultados de seguridad y tolerabilidad de la cariprazina en los 4 ECA de depresión bipolar disponibles (NCT00852202, NCT01396447, NCT02670551 y NCT02670538), incluyendo 1.775 pacientes en el análisis por dosis más frecuente (todos los ECA) y 970 en el análisis por dosis fijas (ECA de fase III). En el primer análisis, las tasas de efectos adversos fueron similares entre los grupos de pacientes tratados con placebo (54,7%), cariprazina < 1,5 mg/día (63,8%), 1,5 mg/día (59,3%) y cariprazina 3 mg/día (57,5%). Los efectos adversos más reportados fueron acatisia (2,4% en el placebo, 3,4% en el brazo de < 1,5 mg/día, 7,3% en el brazo de 1,5 mg/día y 9,4% en el brazo de 3 mg/día) y náuseas, mientras que las incidencias de sedación fueron ligeramente más elevadas en el grupo de cariprazina. No se reportaron casos de viraje maníaco, y de manera parecida al primer estudio post-hoc, los EA fueron globalmente de intensidad leve y moderada, y la tasa de EA severos fue incluso más baja en los grupos de cariprazina que en el de placebo. La cariprazina no se asoció a cambios clínicamente relevantes a nivel de peso, parámetros electrocardiográficos o metabólicos en comparación con el placebo, incluyendo en este caso la glucemia y los triglicéridos, así como la prolactina. Los efectos discretos de cariprazina sobre esta última también se corroboraron en un estudio post-hoc adicional55.
Finalmente, un tercer estudio post-hoc56 se centró en las características de la acatisia y los SEP en los pacientes con TBI y un episodio depresivo tratados con cariprazina. Para ello, analizó los datos agrupados de 3 ECA sobre depresión bipolar (NCT01396447, NCT02670551 y NCT02670538), con un total de 1.407 pacientes, y excluyendo uno de ellos (NCT00852202) por el hecho de no presentar un diseño de dosis fijas e incluir a los pacientes con TBII. Se describió una incidencia global de acatisia con cariprazina del 7,6%, en comparación con el 2,1% en placebo. Además, esta relación fue dosis-dependiente, mostrando los pacientes tratados con 1,5 mg/día una tasa del 5,5% y los pacientes tratados con 3 mg/día una tasa del 9,6%. Por otra parte, la incidencia de SEP (excluyendo acatisia) fue del 4,5% (en comparación con el 2,1% en el placebo). El Número Necesario para Dañar (NND) de la acatisia fue de 19 (30 para la dosis de 1,5 mg/día y 14 para la dosis de 3 mg/día), mientras que el NND de los SEP fue de 43 (60 para la dosis de 1,5 mg/día y 34 para la dosis de 3 mg/día). En general, la acatisia y los SEP detectados se iniciaron dentro de las primeras 3 semanas desde el inicio del tratamiento, fueron de leve o moderada intensidad en más del 95% de los pacientes y raramente conllevaron el abandono del estudio.
Más allá de los ECA y los estudios post-hoc correspondientes, se han publicado los resultados de un ensayo clínico abierto y no controlado57, en el que se administró cariprazina 1,5 mg/día, 3 mg/día o 4 mg/día durante 16 semanas a 402 pacientes con un episodio maníaco o mixto para valorar la seguridad, tolerabilidad y eficacia en un período de tiempo más largo que en los ECA pivotales. El estudio reportó resultados similares: cariprazina fue generalmente bien tolerada a todas las dosis ensayadas, el EA más frecuente fue la acatisia (aunque raramente conllevó el abandono del estudio) seguida de cefalea, estreñimiento y náuseas, y los parámetros de laboratorio no experimentaron cambios significativos. Solo se reportaron 9 pacientes con EA severos, en las categorías de acatisia, SEP y ansiedad. Las tasas de somnolencia fueron relativamente bajas, hecho que es congruente con los resultados de otro estudio sobre incidencia y características de la sedación asociada a los nuevos antipsicóticos, que clasificó cariprazina en el grupo farmacológico de baja somnolencia58.
En general, cariprazina ha mostrado una adecuada tolerabilidad a lo largo de los ECA que la han estudiado como tratamiento para el TB, con un perfil de efectos adversos discreto y de intensidad leve o moderada, en el que destaca una mayor presencia de síntomas extrapiramidales, como la acatisia y el parkinsonismo, respecto a placebo.
Dada la falta de datos acerca de seguridad y tolerabilidad de cariprazina en población pediátrica, existe un ensayo abierto (NCT04578756) aún en fase de reclutamiento, para evaluarlas en población infantil con diagnósticos de esquizofrenia, trastorno del espectro autista o TBI. Existe otro ensayo clínico en curso en fase III centrado en población pediátrica (NCT04777357) que tiene como objetivo principal evaluar la seguridad y tolerabilidad de cariprazina en los pacientes con TBI que presenten un episodio depresivo.
Otros estudios post-hocManía con síntomas mixtosUn estudio post-hoc59 analizó los resultados de 3 ECA (NCT00488618, NCT01058096 y NCT01058668) para evaluar la eficacia de cariprazina en episodios maníacos con síntomas mixtos, utilizando 3 tipos de criterios para definirlos: a) episodio maníaco con ≥ 3 síntomas depresivos (definición operativa del nuevo DSM-5), b) episodio maníaco con ≥ 2 síntomas depresivos, y c) episodio maníaco con una puntuación de la escala MADRS ≥ 10. Cariprazina fue superior a placebo a la hora de reducir la escala YMRS en todos los criterios utilizados, obteniendo también mayores tasas de respuesta y remisión para los criterios b y c. Por otra parte, la reducción de la puntuación en la escala MADRS respecto a placebo solo fue estadísticamente significativa teniendo en cuenta el criterio c, aunque la tendencia fue similar en el resto de los criterios. Una posible causa para estas observaciones negativas fue que las puntuaciones basales de la escala MADRS fueron relativamente bajas, de forma congruente con el diseño del propio estudio.
Depresión con síntomas mixtosUn estudio post-hoc60agrupó los resultados de 3 ECA de cariprazina (NCT01396447, NCT02670551 y NCT02670538), con un total de 1.383 pacientes, con el objetivo de evaluar la eficacia del fármaco en los pacientes diagnosticados con depresión bipolar, con o sin síntomas mixtos. El criterio para definir un episodio depresivo con síntomas mixtos fue una puntuación en la escala YMRS igual o mayor a 4. Cariprazina 1,5 mg/día fue superior a placebo en la reducción de la puntuación en la escala MADRS a las 6 semanas, tanto si los pacientes presentaban síntomas mixtos como si no. También se observaron mayores tasas de respuesta y remisión respecto a placebo en ambos grupos y bajo este tratamiento. Por otra parte, cariprazina 3 mg/día fue superior al placebo en el grupo de pacientes con síntomas mixtos, pero no en los pacientes sin estos. Finalmente, los síntomas maníacos, medidos por la escala YMRS, mejoraron en ambos grupos de tratamiento en los pacientes con y sin síntomas mixtos.
Cognición y funcionalidadActualmente, no se han diseñado ECA cuyo objetivo primario sea evaluar la cognición o la funcionalidad de los pacientes con TB tratados con cariprazina. No obstante, se han realizado estudios post-hoc con base en los datos disponibles de los ECA sobre eficacia.
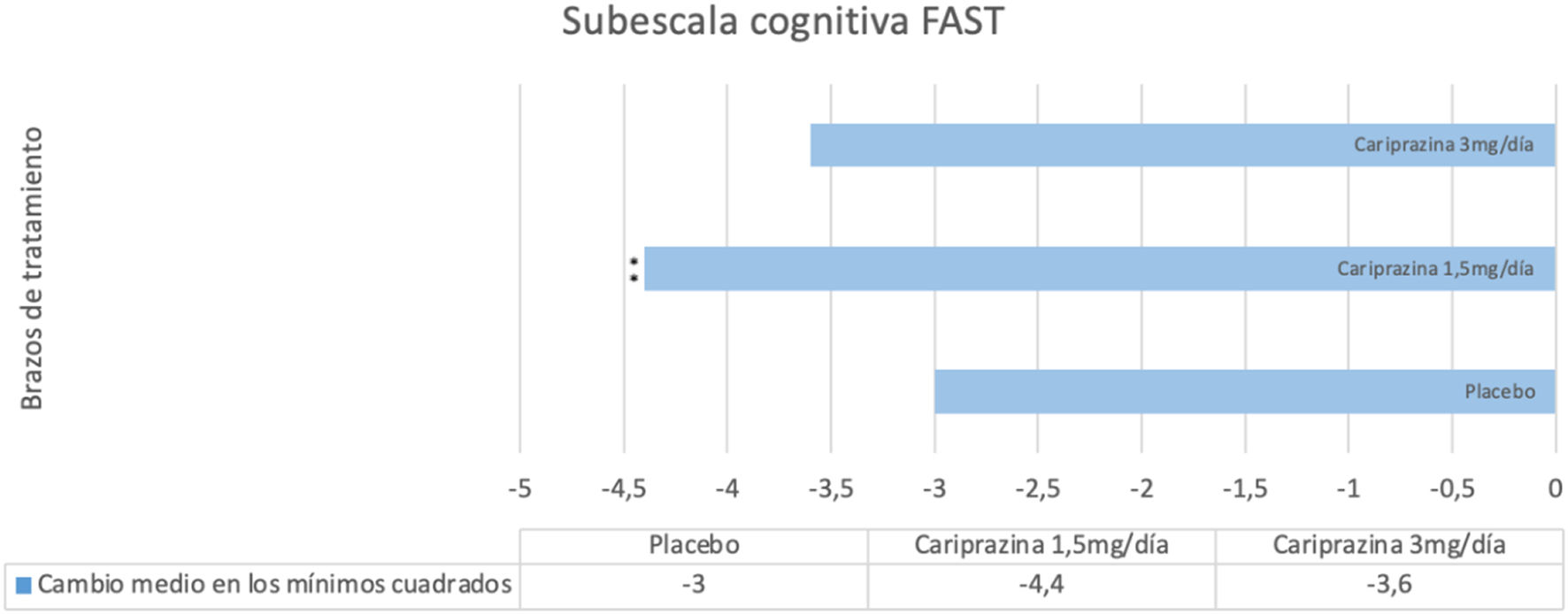
Un estudio post-hoc61 evaluó la eficacia de la cariprazina a la hora de mejorar los síntomas cognitivos en los pacientes diagnosticados tanto con depresión bipolar como con manía. En primer lugar, se analizó el cambio a las 6 semanas de tratamiento en la puntuación agrupada del ítem 6 de la escala MADRS en 3 ECA sobre depresión bipolar (NCT01396447, NCT02670551 y NCT02670538). Cariprazina mostró una mejoría significativa en los pacientes con presencia de síntomas cognitivos al inicio del tratamiento (puntuación de ≥ 3 del ítem 6), y en comparación a placebo. Por otra parte, también se reportaron unos cambios favorables a cariprazina 1,5 mg/día (pero no para 3 mg/día) respecto a placebo en la puntuación de la escala Functional Assessment Short Test (FAST) y en la subescala de funcionamiento cognitivo de la FAST en los pacientes con síntomas cognitivos basales (puntuación de ≥ 2 en 2 o más ítems de la subescala) en un único ECA centrado en depresión bipolar (fig. 2). En este caso, la medida de las variables se realizó a las 8 semanas de haberse iniciado el tratamiento.
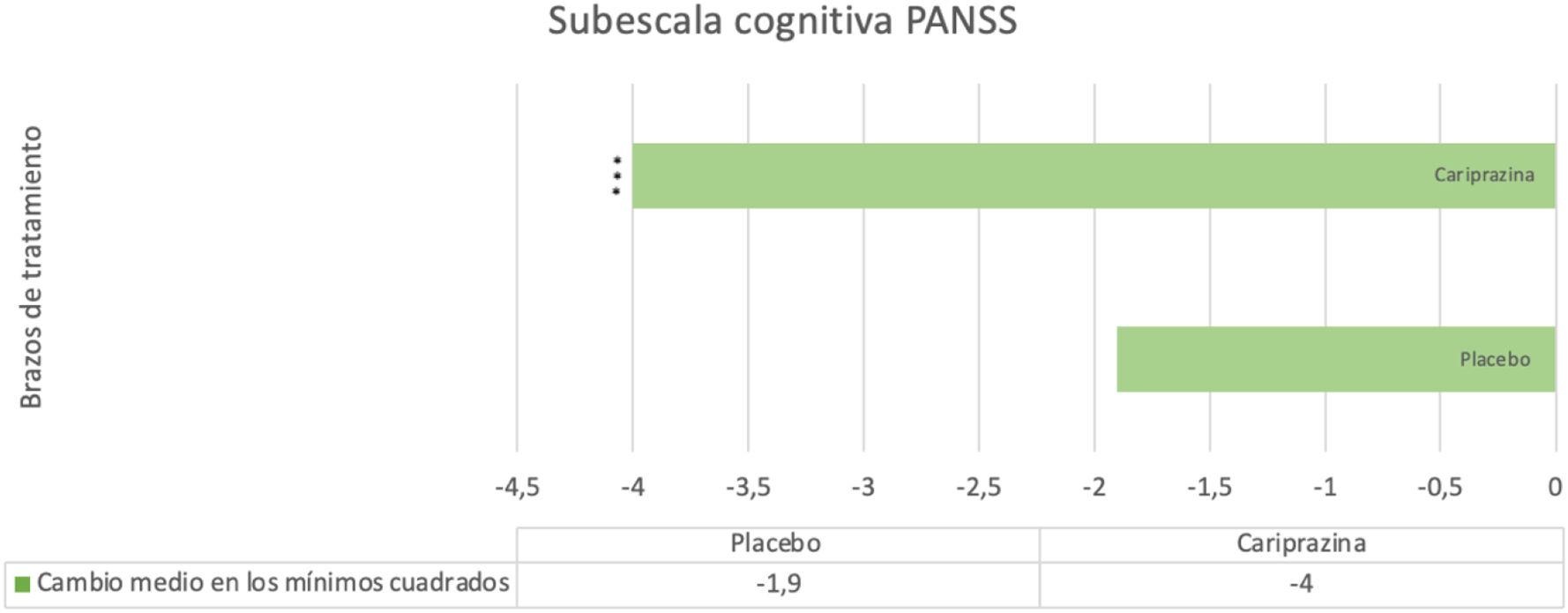
En segundo lugar, se reportaron los resultados a las 3 semanas de tratamiento en los 3 ECA realizados en manía aguda. La puntuación agrupada de la subescala de cognición de la PANSS mostró una disminución significativa con el tratamiento activo en comparación al placebo en los pacientes con presencia de síntomas cognitivos al inicio del tratamiento (puntuación basal ≥ 15) (fig. 3). En concreto, se produjo una mejoría en todos los ítems individuales de la subescala, excepto para el ítem «desorientación».
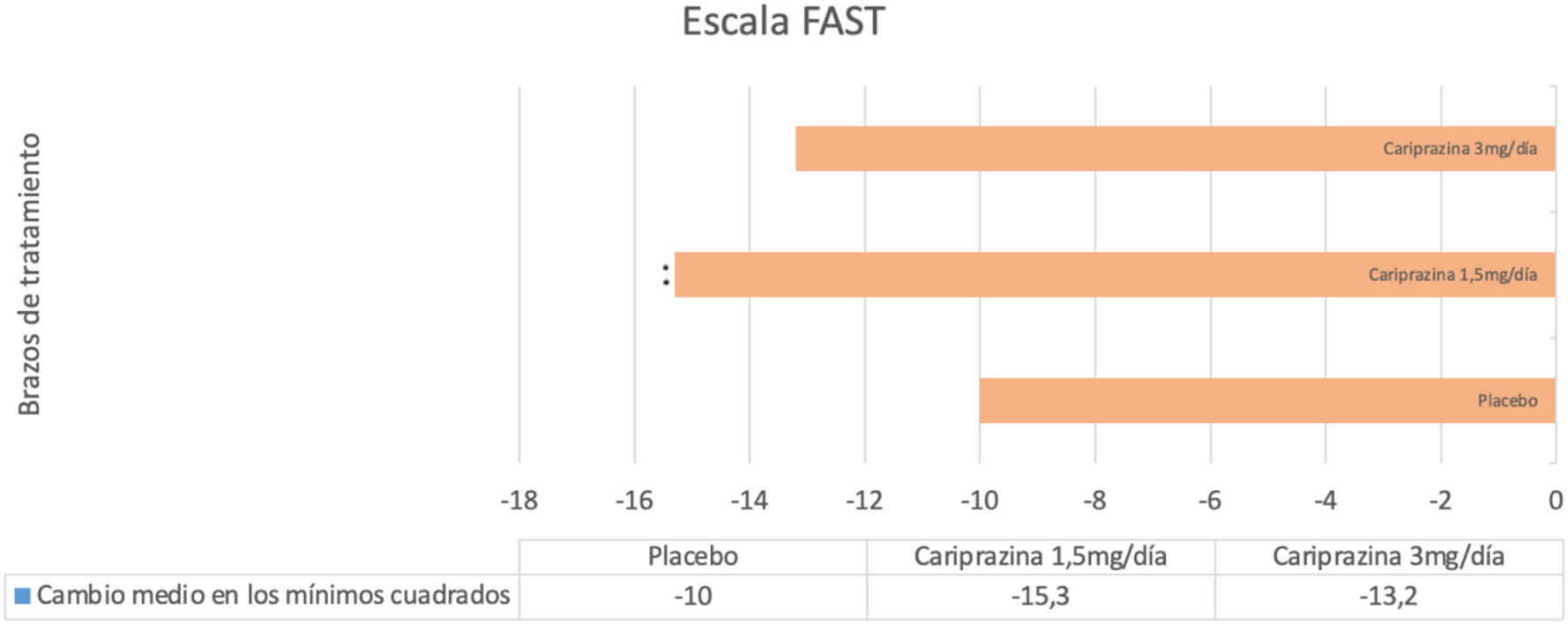
Otro estudio post-hoc62 analizó la eficacia de cariprazina en la funcionalidad de los pacientes con depresión bipolar. Para ello, se consideraron los cambios en la escala FAST a las 8 semanas de tratamiento, reportados en uno de los ECA descritos (NCT01396447). Cariprazina 1,5 mg/día se relacionó con una mejoría significativa respecto a placebo, tanto respecto a la puntuación de la escala global (fig. 4), como en todas las subescalas a excepción de la de finanzas, así como en las tasas de respuesta (43,28 vs. 24,81%), remisión (47,01 vs. 29,46%) y recuperación (25,37 vs. 13,95%). La mejoría asociada a cariprazina 3 mg/día solo fue estadísticamente significativa en las tasas de remisión parcial (30% de mejoría respecto a la puntuación basal).
Finalmente, existe un ECA de fase III en período de reclutamiento que tiene como objetivo principal evaluar la mejoría en el rendimiento cognitivo en los pacientes con TBI en fase eutímica que reciban tratamiento con cariprazina en comparación con los pacientes tratados con placebo. Este estudio pretende asimismo evaluar la mejoría en la funcionalidad en la misma muestra de los pacientes.
Otros estudios activos sin resultados publicadosActualmente hay varios estudios activos, que aún no han publicado sus resultados.
Todavía existe escasa evidencia acerca del uso de cariprazina como tratamiento de mantenimiento en el TB, si bien hay estudios activos que pretenden evaluarlo. Uno de ellos (NCT03573297), el cual se encuentra todavía en curso, tiene como objetivo evaluar la eficacia y seguridad de este a una dosis de 3 mg/día y compararlo con placebo en los pacientes con TB tipo I con un episodio maníaco o depresivo, con o sin características mixtas, así como comparar la dosis de 1,5 mg/día como tratamiento de mantenimiento para la prevención de recaídas, los cuales hayan sido estabilizados con una dosis de 3 mg/día.
Un ECA de fase III (NCT03573297) ha reclutado a 822 pacientes con TBI y un episodio maníaco o depresivo agudo con el objetivo de estudiar la eficacia y la seguridad de cariprazina 1,5 mg/día y 3 mg/día en la prevención de recaídas en contexto del mismo TBI. El estudio tiene previsto completarse a finales de 2022, y puede aportar datos importantes de cara a la indicación de cariprazina para su uso en fase de mantenimiento del TBI.
Un ECA de fase III (NCT04771299) prevé seleccionar a 30 pacientes con TBI con el objetivo de valorar el impacto del tratamiento con cariprazina 1,5 mg/día en la cognición y funcionalidad de los pacientes en fase de eutimia. Se espera que el estudio se complete en septiembre de 2026.
DiscusiónEn los últimos años, con el desarrollo de nuevos psicofármacos, existe un creciente interés en el perfil de tolerabilidad, lo cual ocurre especialmente con los antipsicóticos. Si bien los antipsicóticos típicos son conocidos por su incidencia en los SEP, los atípicos han mostrado mayores efectos adversos metabólicos. Por otro lado, conociendo que algunos trastornos mentales graves, como son la esquizofrenia y el TB, presentan una evolución negativa en cuanto a reserva cognitiva y funcionalidad63, también ha aumentado el interés en el desarrollo de fármacos que no causen un mayor perjuicio en dichas esferas y que en cambio puedan tener un efecto beneficioso.
La cariprazina es un antipsicótico de nueva generación que ha sido aprobado por la AEM como tratamiento agudo y de mantenimiento de la esquizofrenia en los adultos38, a la cual se le han atribuido efectos procognitivos y en la mejoría de los síntomas negativos39. Por otro lado, ha sido aprobada por la FDA para el tratamiento de episodios maníacos, mixtos y depresivos asociados al TBI en los adultos, en un rango de dosis de 3-6 mg/día para los 2 primeros tipos y de 1,5-3 mg/día para el último40. Existen recomendaciones en las guías clínicas más recientes que incluyen la cariprazina como tratamiento de primera línea en episodios de manía, y de segunda línea en episodios depresivos, sin existir por el momento evidencia suficiente para poder ser recomendado como tratamiento de mantenimiento.
En primer lugar, existen diferentes ECA que apoyan la eficacia de cariprazina en episodios maníacos y mixtos, dado que han demostrado una reducción significativamente mayor al placebo en la puntuación de la escala YMRS a las 3 semanas41–43. Un estudio post-hoc45 también muestra unas mayores tasas de respuesta respecto al placebo (Número Necesario para Tratar [NNT] = 5) y remisión (NNT = 7 para YMRS ≤ 12 y NNT = 9 para YMRS ≤ 8) asociadas al fármaco, que cobran importancia al tener en cuenta la elevada prevalencia de síntomas residuales después de los episodios afectivos, que según algunos estudios puede llegar al 50% de los días del año64, asociando un mayor deterioro funcional y riesgo de recaída, así como una reducción en la calidad de vida de estos pacientes45. Para poner estos resultados en su contexto, un metaanálisis65 mostró que el NNT de los antipsicóticos de segunda generación para respuesta y remisión (YMRS ≤ 12) en manía fue de 6 y 8, respectivamente. Además, un estudio exploratorio sugirió la eficacia de cariprazina en los pacientes maníacos con síntomas mixtos, de acuerdo con la conceptualización correspondiente al DSM-5. Este hecho reviste gran importancia, ya que este tipo de episodios están frecuentemente subdiagnosticados, asocian una mayor comorbilidad y presentan un curso menos favorable que los que no presentan síntomas mixtos59.
Complementariamente, cariprazina también parece asociar una mejoría de la impresión clínica global en estos pacientes47. Esta es una dimensión que informa sobre el impacto clínico general de una enfermedad, teniendo en cuenta la gravedad de los síntomas y el estrés, discapacidad e impacto funcional que asocian, y que puede ser de especial relevancia en trastornos que suponen un elevado deterioro funcional como el TB o la esquizofrenia47.
Mientras que el TBI se puede diagnosticar con tan solo la presencia de un episodio maníaco, la mayor parte de los episodios y síntomas que experimentan los pacientes son de polo depresivo, y son los que acaban definiendo el curso y pronóstico de la enfermedad66. No obstante, las alternativas terapéuticas para tratar la depresión bipolar son escasas: del total de 23 ECA que han evaluado hasta 9 fármacos para la indicación de depresión bipolar, solo olanzapina, lurasidona, quetiapina y cariprazina han mostrado superioridad respecto a placebo67. En consecuencia, aún es necesario el diseño y comercialización de nuevos agentes farmacológicos. En este contexto, cariprazina ha mostrado una eficacia significativa en el tratamiento de los episodios depresivos, y de manera especialmente consistente a dosis de 1,5 mg/día. Esta observación es congruente con un estudio realizado con tomografía por emisión de positrones en los pacientes con esquizofrenia, en el que se analizaron los cambios en la ocupación de los receptores dopaminérgicos por parte de la cariprazina en función de la dosis usada68. Así, a 1 mg/día, solo el 45% de los receptores D2 quedan ocupados, mientras que a 3mg/día el porcentaje de ocupación aumenta hasta el 79%. La tasa de ocupación de los receptores D3 varía mucho menos entre ambas dosis (76 y 92%, respectivamente). Así, una elevada especificidad D3 en dosis de 1,5 mg/día contribuiría a una mayor eficacia antidepresiva de cariprazina, mientras que una ocupación de receptores D2 y D3 más equilibrada a dosis más elevadas explicaría un mayor beneficio en los episodios maníacos.
Según los resultados de un estudio post-hoc, la eficacia de la cariprazina en los episodios depresivos parece ser independiente de las características basales sociodemográficas o clínicas del paciente. Esto es importante dado que el TB afecta a un espectro muy diverso de los pacientes, y que algunas variables concretas (como una menor edad o la presencia de síntomas mixtos) se han asociado a un peor pronóstico e incluso a una peor respuesta al tratamiento. Por ejemplo, algunos estudios post-hoc reportaron que aripiprazol pierde eficacia en los pacientes que presentan una depresión menos grave69, así como que la olanzapina es menos eficaz en los pacientes con un episodio depresivo sin características melancólicas70.
Además, un estudio exploratorio sugirió que la eficacia de cariprazina se mantiene en los episodios depresivos con síntomas mixtos. Esto es destacable ya que este tipo de episodios comportan síntomas más graves, mayores tasas de recurrencia de episodios afectivos y de refractariedad al tratamiento, además de mayor comorbilidad y un riesgo incrementado de suicidio71. Cabe destacar que actualmente no hay ningún fármaco comercializado para el tratamiento de los episodios mixtos, pero un panel de expertos ha recomendado considerar los antipsicóticos atípicos como tratamiento de primera línea en estos casos72.
Varios estudios indican que en los pacientes con TBI los déficit cognitivos y funcionales se extienden más allá de la remisión de los síntomas depresivos, asociando una reducción en su calidad de vida73. Hasta el momento, no se han publicado resultados de ECA con cariprazina diseñados para la evaluación formal de dichos déficit en los pacientes con TB, por lo que la evidencia en este sentido es limitada. No obstante, los estudios exploratorios sobre síntomas cognitivos y funcionalidad sugieren una eficacia significativa en este sentido, sobre todo para la dosis de 1,5 mg/día de cariprazina, lo cual es congruente con la evidencia de la que se dispone a partir de estudios en los pacientes con esquizofrenia74–76. En efecto, el mecanismo de acción de la cariprazina, basado en una mayor afinidad para los receptores D3 que para los receptores D2, se ha relacionado con un efecto procognitivo en estudios preclínicos25 y con una potencial mejoría de los déficit cognitivos en los pacientes21. Otros agentes del mismo grupo farmacológico, como la lurasidona o el brexpiprazol, también han demostrado efectos procognitivos77. En resumen, el perfil de unión a receptores de la cariprazina favorecería una mayor remisión de los síntomas depresivos y cognitivos que, juntamente con una mejoría funcional y en la calidad de vida, conllevarían mayores tasas de recuperación en los pacientes con TB. Algunos ensayos clínicos que se encuentran activos en la actualidad permitirán evaluar de forma más adecuada la eficacia de cariprazina en la funcionalidad y en la función cognitiva (NCT04771299) (Jayasree Basivireddy, 2021), hecho que podría plantear futuros estudios que analicen el posible beneficio global de cariprazina como tratamiento de mantenimiento en esta enfermedad.
En cuanto a la seguridad y tolerabilidad, los estudios realizados hasta el momento demuestran que la cariprazina es segura y generalmente bien tolerada como tratamiento para el TB. En ambos tipos de episodio afectivo, los EA más frecuentes fueron los SEP, especialmente la acatisia, y los gastrointestinales, y no hubo un aumento significativo de EA severos respecto a placebo. Como punto a destacar, la tolerabilidad de cariprazina fue sustancialmente mejor en los ensayos de depresión bipolar que en los de manía, probablemente a causa del uso de dosis menores y de unas estrategias de titulación más progresivas, como sugiere un estudio de relación entre exposición a fármaco y efectos clínicos78. Así, se reportaron mejores resultados para depresión en comparación con la manía en la tasa de efectos adversos (59,5 vs. 79,6%), efectos adversos severos (1,3 vs. 5,5%), acatisia (7,3 vs. 20,2%) y SEP (14,3 vs. 27,9%).
En esta línea, la efectividad comparable de los grupos de 3-6 mg/día y de 9-12 mg/día de cariprazina a la hora de tratar los episodios maníacos, junto con un perfil de efectos adversos más favorable en el primer grupo, llevaron a la FDA a aprobar la indicación del fármaco para dicho tratamiento a dosis de entre 3-6 mg/día.
Profundizando en la relación entre cariprazina y los SEP, se objetivó una posible relación dosis-respuesta tanto en manía como en depresión. Si bien se tratan de efectos adversos que en ocasiones requerirían un cambio de tratamiento para su resolución, no se consideran efectos adversos graves, y en ocasiones podrían ser resueltos mediante un tratamiento concomitante.
Un estudio post-hoc con datos agrupados56 reportó un NND para acatisia en la depresión bipolar de 30 para la dosis de 1,5 mg/día y de 14 para la dosis de 3 mg/día. De nuevo, la diferente tasa de ocupación de los receptores D2 y D3 en función de la dosis de cariprazina explicaría la incidencia de aparición de los SEP68. El uso de dosis más bajas y titulaciones más progresivas podría minimizar la aparición de SEP y de otros EA. No obstante, en función de la severidad del EA, un NND superior a 10 se considera generalmente tolerable79. En comparación, los NND para acatisia en depresión bipolar fueron similares para los antipsicóticos con la misma indicación terapéutica: quetiapina de liberación prolongada33 y lurasidona14,80.
Finalmente, las diferencias entre los grupos de placebo y tratamiento activo para el resto de los parámetros de seguridad (virajes maníacos o depresivos, ideación suicida, parámetros electrocardiográficos, hemodinámicos, metabólicos) fueron nulas o clínicamente irrelevantes tanto en los estudios de manía como los de depresión. Los pacientes con TB presentan una elevada comorbilidad con enfermedad médica, como las enfermedades cardiovasculares, la hipertensión, la obesidad, la diabetes y el síndrome metabólico66, causando una mayor mortalidad en comparación con controles sanos81. Además, y dado que los antipsicóticos son una clase de fármacos tradicionalmente asociada al aumento de peso, la sedación, los SEP, la hiperprolactinemia y a las alteraciones en parámetros cardiovasculares y metabólicos, conllevando una baja adherencia al tratamiento y una reducción en la calidad de vida de los pacientes82, el perfil de seguridad y tolerabilidad de la cariprazina resulta interesante a la hora de tratar el TB.
En general, las limitaciones de los estudios de cariprazina incluyen la falta de comparadores activos y la exclusión de los pacientes con enfermedad médica y/o psiquiátrica sustancial (incluyendo a los pacientes con historia de ciclación rápida, depresión resistente al tratamiento o ideación suicida), hecho que puede asociar una falta de validez externa en los resultados de los estudios descritos. La corta duración de los ensayos también puede afectar a la capacidad de interpretar algunos resultados de seguridad, como el aumento ponderal. Este hecho es especialmente importante dada la semivida de eliminación de la cariprazina y sus metabolitos, por lo que algunos efectos adversos podrían aparecer más allá de los tiempos de observación de los ensayos. En este sentido, es recomendable una estrecha monitorización durante las semanas posteriores al inicio o cambio de dosis del tratamiento.
Cabe destacar que aún no se han publicado resultados de cariprazina como tratamiento de mantenimiento en el TB, a pesar de que actualmente hay dos ECA al respecto en desarrollo. A pesar de disponer de suficiente evidencia que apuntan a un beneficio con cariprazina en episodios afectivos del TB, estos nuevos estudios permitirán apoyar dicha evidencia y ampliar el estudio de este fármaco no solo en la eficacia en la sintomatología afectiva, sino también en otros aspectos relacionados con la enfermedad, como son la prevención de recaídas, el rendimiento cognitivo y la funcionalidad. Un enfoque ampliado en el estudio de cariprazina en el TB podría suponer, junto con el perfil beneficioso de efectos adversos que presenta este fármaco, un beneficio global en el tratamiento de la enfermedad.
ConclusionesLa cariprazina es un antipsicótico de nueva generación aprobado por la AEM para el tratamiento de la esquizofrenia, y por la FDA para el tratamiento de los episodios maníacos, depresivos y mixtos asociados al TB. Las guías clínicas más recientes incluyen este fármaco como tratamiento eficaz del TB, tanto en episodios de manía aguda como en episodios depresivos, con cierta evidencia también para su uso en episodios mixtos y a medio y largo plazo, a la espera del ensayo clínico actualmente en marcha para la indicación de mantenimiento. Con base en los estudios disponibles, las guías clínicas recomiendan dosis de 3-6 mg al día para el tratamiento de episodios maníacos y de 1,5-3 mg al día en episodios depresivos. La experiencia clínica demuestra que las dosis deben individualizarse en función de la gravedad del episodio (episodios maníacos graves podrían requerir dosis superiores) y de la tolerabilidad, especialmente para el manejo de las fases depresivas, dónde algunos pacientes sóolo toleran dosis bastante bajas. Cariprazina es un fármaco seguro y generalmente bien tolerado. Sus EA más frecuentes son los SEP, especialmente la acatisia, y aparecen con menor frecuencia en dosis bajas y con una titulación progresiva. La acatisia raramente es causa de discontinuación del tratamiento, pero puede requerir una titulación lenta y la adición de alguna medicación que la mitigue, como una benzodiacepina a dosis bajas al inicio del tratamiento.
A pesar de no existir resultados de ECA que evalúen cambios en sintomatología cognitiva y funcionalidad en TB con cariprazina, los estudios exploratorios sugieren una eficacia significativa en este sentido. Los datos son particularmente buenos en depresión bipolar, especialmente a dosis de 1,5 mg/día.
Teniendo en cuenta el perfil de seguridad y el mecanismo de acción de cariprazina, y el hecho de estar aprobada para el tratamiento del TB tanto en sus fases maníacas como depresivas en Estados Unidos y muchos otros países, su utilización está plenamente justificada desde el punto de vista científico. Los beneficios son especialmente notables a medio y largo plazo, por el perfil de seguridad respecto a efectos metabólicos y neurológicos respecto a otros fármacos, y su impacto en la calidad de vida y la funcionalidad.
Conflicto de interesesLos autores han realizado actividades docentes o investigadoras no relacionadas con este trabajo para AB-Biotics, AbbVie, Adamed, Angelini, Biogen, Boehringer-Ingelheim, Casen-Recordati, Celon Pharma, Compass, Dainippon Sumitomo Pharma, Ferrer, Gedeon Richter, GH Research, Glaxo-Smith Kline, Janssen, Lundbeck, Medincell, Merck, Novartis, Orion Corporation, Organon, Otsuka, Rovi, Sage, Sanofi-Aventis, Sunovion, Takeda, y Viatris.
AgradecimientosAna Giménez-Palomo recibe soporte financiero de un contrato Río Hortega procedente del Ministerio Español de Sanidad, Instituto de Salud Carlos III (CM21/00094) y del Fondo Social Europeo Plus (FSE+). Los autores de este estudio agradecen el apoyo del Ministerio de Ciencia e Innovación de España e Innovación (PI18/00805, PI21/00787) integrado en el Plan Nacional de I+D+I y cofinanciado por el ISCIII-Subdirección General de Evaluación y el Fondo Europeo de Desarrollo Regional (FEDER); el Instituto de Salud Carlos III; el CIBER de Salud Mental (CIBERSAM); la Secretaria d'Universitats i Recerca del Departament d'Economia i Coneixement (2017 SGR 1365) y el Programa CERCA.
Resumen- •
Cariprazina es un antipsicótico de nueva generación que actúa como agonista parcial de los receptores de dopamina D2 y D3, y de los receptores de serotonina 5HT1A.
- •
Ha mostrado ser eficaz en el tratamiento de la esquizofrenia y de las diferentes fases del trastorno bipolar.
- •
En el trastorno bipolar, se recomienda su uso en dosis de 1,5-3 mg al día para el tratamiento de episodios depresivos y de 3-6 mg al día en caso de episodios maníacos.
- •
Presenta un correcto perfil de seguridad y tolerabilidad, siendo su efecto adverso más frecuente la acatisia.
- •
Algunos estudios sugieren un beneficio de cariprazina sobre la función cognitiva y la funcionalidad.
- •
El uso de cariprazina en trastorno bipolar puede suponer un beneficio global en cuanto a eficacia, seguridad y funcionalidad.