La atrofia vaginal es una enfermedad crónica, a menudo no diagnosticada, que tiene un importante impacto en la salud sexual y la calidad de vida. La atrofia vaginal está causada por los cambios fisiológicos debidos a la disminución de estrógenos y son la base de una serie de síntomas que incluyen sequedad vaginal, dispareunia, prurito e irritación reportados en un 40-60% de las mujeres posmenopáusicas en Europa. El porcentaje de mujeres tratadas es menor del 30% y con un cumplimiento menor del 10% al año. El tratamiento de primera línea para la atrofia vaginal moderada-severa son los estrógenos locales.
Recientemente, ha aparecido en España un nuevo tratamiento local de estrógenos, que consiste en un anillo de silicona flexible con un núcleo que contiene 2mg de hemihidrato de estradiol. El estradiol se libera en cantidades mínimas pero continuas, con una liberación de 6,5 a 9,5 μg/día durante, al menos, 90 días. El anillo vaginal ha demostrado ser efectivo en el alivio de la sintomatología local (vaginal y urológica) y mejorando la mucosa vaginal desde el punto de vista de los hallazgos visuales exploratorios (palidez, turgencia, rugosidad, grosor), así como en cuanto al índice de maduración citológica (mayor proporción de células superficiales y una disminución de células basales, parabasales e intermedias) y pH.
El anillo muestra los mismos efectos secundarios que otros tipos de estrógenos locales y es el método más elegido por las pacientes debido a la facilidad de su uso, la comodidad y la satisfacción en general.
Vaginal atrophy is a chronic disease that is often undiagnosed and has a major impact on sexual health and quality of life. Vaginal atrophy is caused by physiological changes due to a decrease of estrogens. These changes are the basis of a number of symptoms including vaginal dryness, dyspareunia, itching and irritation reported in 40-60% of postmenopausal women in Europe. The percentage of treated women is less than 30%, and compliance is less than 10% per year. Local estrogens are the first-line treatment for moderate-to-severe vaginal atrophy.
A new local estrogen treatment has recently become available in Spain, consisting of a flexible silicone ring with a core containing 2mg of estradiol hemihydrate. The amount of estradiol released is minimal but in continuous quantities, with a release of 6.5 to 9.5 mcg/day for at least 90 days. The vaginal ring has been proven to be effective in relieving local symptoms (vaginal and urological), improving the vaginal mucosa based on visual examination (pale color, turgor, roughness, and thickness) and on the rate of cytologic maturation (a greater proportion of surface cells and a decrease in basal, parabasal and intermediate cells) and pH.
The ring produces the same side effects as other types of local estrogen and is the most frequently chosen method by patients because of its ease of use and comfort, and the general satisfaction produced.
Los estrógenos son necesarios para mantener la estructura y la función de la vagina1. La disminución de los niveles de estrógenos se ha asociado a cambios en la fisiología de la vagina, tales como disminución del epitelio y un aumento del nivel de pH vaginal2. Estos cambios en la fisiología son la base de una serie de síntomas que incluyen sequedad vaginal, dispareunia, prurito e irritación1,2, que definen a la atrofia vaginal (AV).
La AV es una enfermedad crónica, a menudo no diagnosticada, que tiene un importante impacto en la salud sexual y la calidad de vida3. Los síntomas de AV se han reportado hasta en un 40-60% de las mujeres posmenopáusicas en Europa y los EE. UU.4. Incluso mujeres que reciben terapia hormonal sustitutiva presentan síntomas locales (hasta un 25%)5 y tan solo una cuarta parte de estas mujeres se lo comunica a su especialista y reclama algún tipo de tratamiento6.
A diferencia de los síntomas vasomotores, los síntomas de AV, en ausencia de tratamiento, generalmente persisten o aumentan con el tiempo1,5. La sequedad vaginal y dispareunia son los síntomas más molestos y los síntomas más comunes reportados por las mujeres posmenopáusicas con AV3,4,7. Los tratamientos para la AV buscan aliviar estos síntomas6. Las terapias de primera línea incluyen el uso de hidratantes vaginales no hormonales, lubricantes en el momento de la relación sexual y dosis bajas o ultra bajas de estrógenos locales6. Sin embargo, tanto los posibles efectos secundarios indeseables que puedan producirse en el uso de dosis incorrectas de estrógenos y la incomodidad de la aplicación local de forma constante de cremas, óvulos o tabletas8 pueden tener repercusiones en un bajo cumplimiento y en la irregularidad de su administración.
El anillo vaginal con liberación de ultrabajas dosis de estrógeno (Estring®) de forma continua es una alternativa hormonal vaginal para la AV9. Es un anillo liberador de estradiol del que se tiene una amplia experiencia9. El uso del anillo ha demostrado ser seguro, así como reducir los síntomas de dispareunia y sequedad vaginal10-12. En esta revisión, se presentan datos de conjunto de su farmacocinética, eficacia, seguridad y experiencia en su uso clínico.
FarmacocinéticaEs un anillo de silicona flexible, de 55mm de diámetro y 9mm de espesor, con un núcleo que contiene 2mg de hemihidrato de estradiol. El estradiol se libera en cantidades mínimas pero continuas, con una liberación de 6,5 a 9,5 μg/día durante, al menos, 90 días.
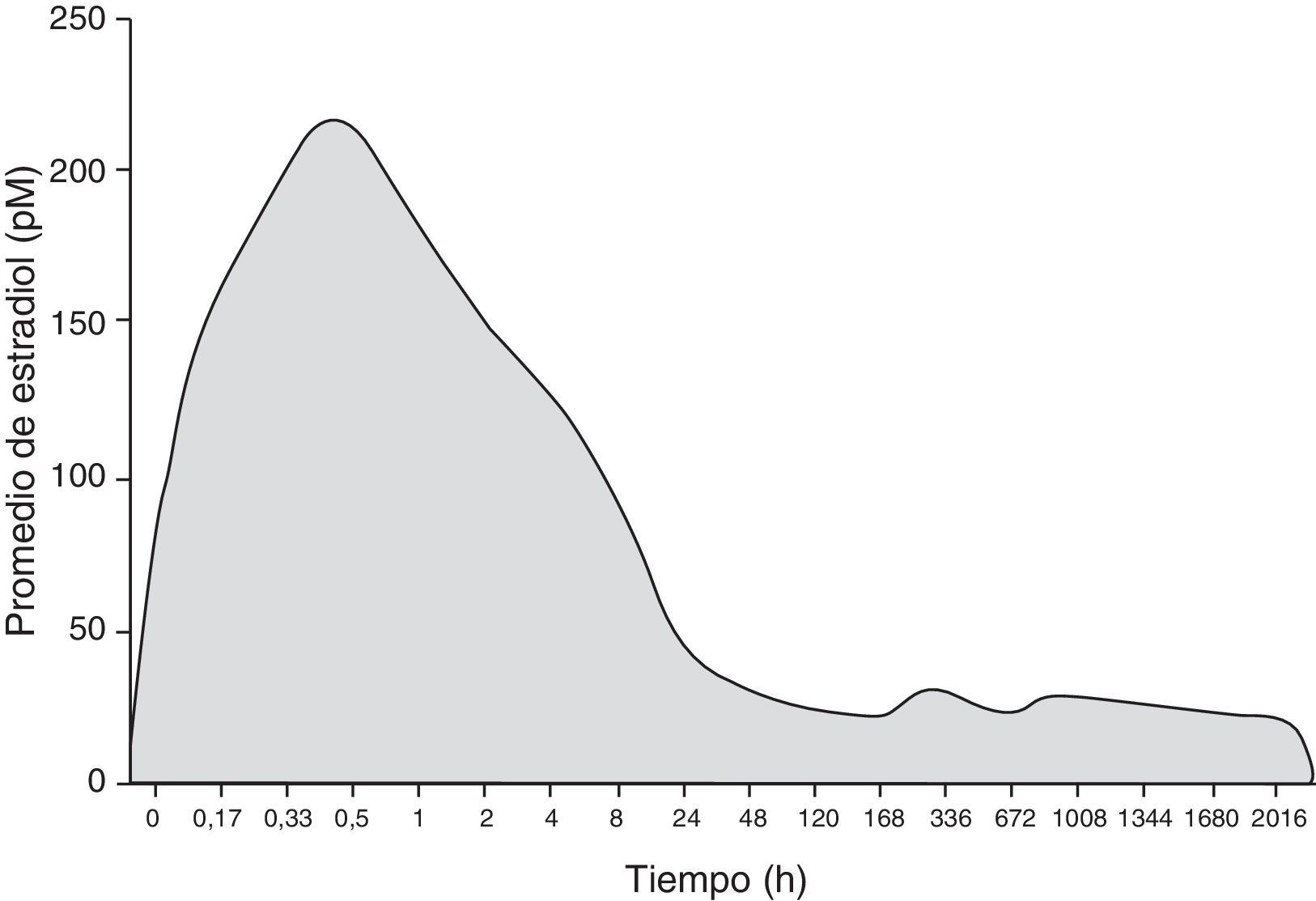
Tres estudios clínicos10,11,13 han demostrado que esta dosis ultrabaja solo crea aumentos mínimos en los niveles de estradiol en plasma, excepto durante las primeras 8h, donde hay un aumento inicial por la rápida absorción. Durante esta primera fase de uso, la velocidad de liberación se incrementa debido a la acumulación de esteroides en la superficie del anillo durante el almacenamiento y debido a que la mucosa vaginal, cuanto más atrófica, más absorbe14. El estradiol plasmático va desde valores pretratamiento de 15-25pmol/l (4 a 7pg/ml) a 20-30pmol/l (5,5-9pg/ml), durante la fase de tratamiento, siendo equivalente a la observada en las mujeres posmenopáusicas sin tratamiento 20-70pmol/l (5,5-20pg/ml). La contribución relativa de esta cantidad inicial a la exposición de estradiol en general en los 90 días es mínima (< 2%). En los 3 estudios, en el día 14, los niveles de estradiol en suero estaban dentro del rango normal de estradiol que se observa en las mujeres posmenopáusicas, permaneciendo sin cambios (fig. 1)15.
Un aumento inicial de estradiol en plasma se ve de nuevo con la inserción de un segundo anillo. Este aumento se debe a la acumulación de esteroides en la superficie del anillo durante el almacenamiento, pero es más fugaz si lo comparamos con el aumento en la absorción de estradiol en plasma con el primer anillo; esto es debido a que la mucosa vaginal ya no es atrófica15.
Por lo tanto, el tratamiento con estrógenos locales a dosis ultrabajas tiene la ventaja de evitar concentraciones elevadas de estrógenos séricos, manteniéndolos en el rango posmenopáusico normal7. Este hecho permite obviar las limitaciones en su uso debido a sus potenciales efectos adversos sistémicos e incluso evitar la necesidad de la oposición gestagénica en mujeres con útero intacto, tal y como la European Menopause and Andropause Society pone de manifiesto en un posicionamiento reciente relativo al manejo de la AV16.
EficaciaLa eficacia de los tratamientos de AV se basan en medidas directas tanto objetivas (pH vaginal y citología vaginal con estudio del índice de maduración) como subjetivas (percepción de alivio de la sintomatología por parte del paciente y por la exploración clínica del profesional).
Tres estudios descriptivos10-12, con un total de más de 350 mujeres, mostraron consistentemente que la maduración del epitelio vaginal mejoró significativamente durante el tratamiento con el anillo vaginal de dosis ultrabaja de estradiol. En el estudio de Henriksson et al., de 136 mujeres con síntomas y signos de atrofia urogenital, el 90% tenía una clara mejoría en el valor del índice de maduración en la mucosa vaginal después de un año de tratamiento12. Además, todos los estudios mostraron una mejora en los síntomas de atrofia urogenital después del tratamiento. Smith et al.11 estudiaron a 222 mujeres con síntomas y signos de atrofia urogenital y encontraron que cada síntoma (sequedad vaginal, prurito vulvar, dispareunia, disuria y urgencia urinaria) había mejorado o curado en el 85% de las mujeres.
Se realizó otro ensayo clínico doble ciego, aleatorizado, controlado con placebo17, en el que se incluyó a 84 pacientes asignados o al anillo vaginal con dosis ultrabaja o a un anillo vaginal placebo. El estudio de 24 semanas fue completado por 67 pacientes. No se encontraron diferencias estadísticamente significativas entre los 2 grupos en los signos de atrofia genital al inicio del tratamiento. El valor medio de maduración de las evaluaciones citológicas de frotis vaginales fue significativamente mayor en los usuarios de Estring® en comparación con el placebo (p=0,004) y el pH vaginal fue significativamente menor en los usuarios del anillo con estradiol en comparación con el placebo (p=0,0006). También existieron más mujeres libres de síntomas o mejoría con respecto a los síntomas de AV en el grupo de Estring® que el grupo de anillo de placebo. Además, existió una diferencia estadísticamente significativa para el alivio de dispareunia (90% en el grupo anillo con estradiol frente al 45% en el grupo de anillo de placebo, p=0,028).
Otro estudio abierto, aleatorizado, de grupos paralelos en la prevención del efecto de Estring® en las infecciones recurrentes del tracto urinario en las mujeres posmenopáusicas mostró que la proporción de mujeres que quedan libres de ITU fue significativamente mayor en el grupo Estring® en comparación con los controles (45 y 20%, respectivamente, p=0,008)18.
Los estudios que compararon la dosis ultrabaja del anillo vaginal de estradiol vaginales vs. óvulos o cremas vaginales de estrógenos también han mostrado de forma consistente que el anillo vaginal es tan eficaz como otros tratamientos establecidos en términos de alivio de los síntomas (vaginal y urinario) y la mejora de los índices de maduración de la mucosa vaginal19-22.
La mayor revisión publicada hasta la fecha sobre tratamientos locales para la AV ha sido la realizada por la Cochrane Database en 2006. Incluyó 19 ensayos que gozaban de buena calidad metodológica, con un total de 4.162 mujeres. Se evaluaron la eficacia, la seguridad y la aceptabilidad de distintos preparados de estrógenos locales entre sí (anillo vaginal, comprimidos, crema y óvulos) y frente a placebo. Se encontró que todos ellos eran eficaces a la hora de la mejora tanto de los parámetros objetivos como en la sintomatología clínica, y más eficaces que frente a placebo23.
En resumen, el anillo vaginal liberador de dosis ultrabaja de estradiol ha demostrado ser efectivo en el alivio de la sintomatología local (vaginal y urológica) y mejorando la mucosa vaginal desde el punto de vista de los hallazgos visuales exploratorios (palidez, turgencia, rugosidad, grosor), así como en cuanto al índice de maduración citológica (mayor proporción de células superficiales y una disminución de células basales, parabasales e intermedias) y pH.
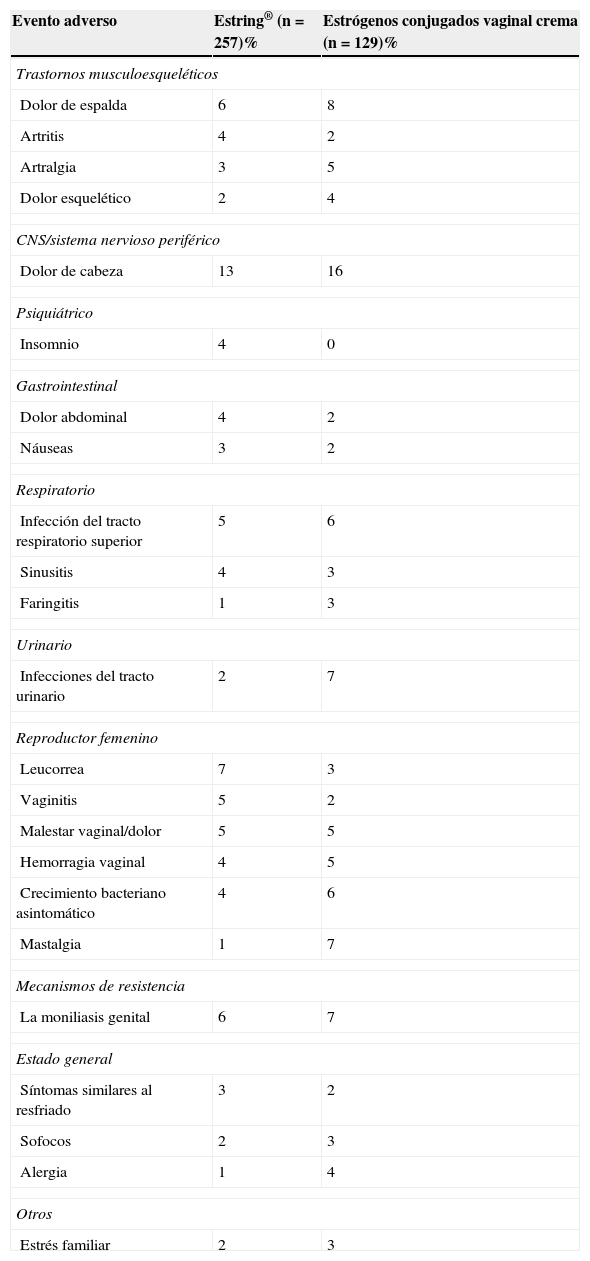
SeguridadLos estudios pivotales o de fase 310-12,19-22 que tienen por objeto valorar la eficacia clínica, la seguridad y la tolerabilidad del fármaco demostraron la eficacia y la seguridad del fármaco. Así, en un estudio comparativo, la interrupción del tratamiento debido a un evento adverso se dio en el 5,4% de los pacientes que recibieron Estring® y en el 3,9% de los pacientes que recibieron estrógenos conjugados en crema vaginal. Las razones más comunes para la suspensión del tratamiento en el grupo de Estring® fueron un malestar vaginal y síntomas gastrointestinales20 (tabla 1).
Eventos adversos informados en un 3% o más de los pacientes que recibieron ya sea Estring® o crema de estrógenos conjugados vaginal en los 2 estudios pivotales controlados
| Evento adverso | Estring® (n=257)% | Estrógenos conjugados vaginal crema (n=129)% |
|---|---|---|
| Trastornos musculoesqueléticos | ||
| Dolor de espalda | 6 | 8 |
| Artritis | 4 | 2 |
| Artralgia | 3 | 5 |
| Dolor esquelético | 2 | 4 |
| CNS/sistema nervioso periférico | ||
| Dolor de cabeza | 13 | 16 |
| Psiquiátrico | ||
| Insomnio | 4 | 0 |
| Gastrointestinal | ||
| Dolor abdominal | 4 | 2 |
| Náuseas | 3 | 2 |
| Respiratorio | ||
| Infección del tracto respiratorio superior | 5 | 6 |
| Sinusitis | 4 | 3 |
| Faringitis | 1 | 3 |
| Urinario | ||
| Infecciones del tracto urinario | 2 | 7 |
| Reproductor femenino | ||
| Leucorrea | 7 | 3 |
| Vaginitis | 5 | 2 |
| Malestar vaginal/dolor | 5 | 5 |
| Hemorragia vaginal | 4 | 5 |
| Crecimiento bacteriano asintomático | 4 | 6 |
| Mastalgia | 1 | 7 |
| Mecanismos de resistencia | ||
| La moniliasis genital | 6 | 7 |
| Estado general | ||
| Síntomas similares al resfriado | 3 | 2 |
| Sofocos | 2 | 3 |
| Alergia | 1 | 4 |
| Otros | ||
| Estrés familiar | 2 | 3 |
Tomado de Ayton et al.20.
En 201023, la Cochrane concluyó que el anillo mostraba los mismos efectos secundarios que otros tipos de estrógenos locales y que era el método más elegido por las pacientes debido a la facilidad de su uso, su comodidad y satisfacción en general.
Seguridad endometrialUna de las principales preocupaciones del tratamiento con estrógenos sin oposición de gestágenos es el riesgo de aparición de patología endometrial. En uno de los estudios pivotales20 se realizó ecografía pélvica a las pacientes y se les sometió a la prueba de provocación con progestágenos para valorar la posibilidad de hiperestimulación endometrial. En ninguna de las 58 pacientes del grupo de Estring® se produjeron cambios significativos en el espesor endometrial ni se llegó a superar el límite considerado normal (5mm). Tampoco se informó de sangrado espontáneo o tras la administración de progestágenos; sin embargo, sí se produjo hemorragia en 4 de las 35 (11%) pacientes del grupo de la crema con estrógenos conjugados.
Un estudio multicéntrico aleatorizado comparó la seguridad endometrial del anillo con los comprimidos vaginales de estradiol de 25 μg. El seguimiento fue de un año, basándose en la medida por ecografía del espesor endometrial y la presencia de sangrado genital espontáneo o tras el test de progesterona24. El estudio no mostró diferencias en cuanto a la medida del espesor endometrial entre ambos grupos pero sí en la proporción de hemorragia genital con resultados desfavorables para el grupo que utilizaba comprimidos vaginales. Ninguna de las usuarias del anillo presentó sangrado ni patología endometrial en caso de realizarse biopsia por indicación ecográfica, por lo que se concluye que Estring® es un tratamiento seguro a nivel endometrial tras un año de tratamiento, ya que no induce cambios proliferativos, hiperplasia o aumento de riesgo de cáncer de endometrio.
Por todo ello, se considera que no es necesario administrar de forma adicional progestágenos durante el tratamiento con Estring® ni realizar cribado de patología endometrial. En cualquier caso, si durante el tratamiento con el anillo la paciente presenta sangrado vaginal, será necesario poner en marcha el protocolo habitual de estudio endometrial.
Síntomas vaginales localesPueden existir en un porcentaje pequeño de pacientes que refieren irritación, leucorrea o molestia vaginal durante el tratamiento con Estring®, tal y como muestran los estudios pivotales (tabla 1). Se considera que el anillo no provoca clínica local llamativa y que la aparición de úlceras, erosiones severas o adherencias vaginales son un hecho raro25.
En conclusión, Estring® se presenta como una alternativa segura para el tratamiento de la atrofia urogenital con efectos adversos infrecuentes y que no suponen graves implicaciones clínicas, y con buen perfil de seguridad endometrial, ya que no incrementa el riesgo de hiperplasia ni carcinoma.
Aceptación y satisfacción de la pacienteLas pacientes incluidas en los ensayos han destacado la comodidad de uso, obteniendo los niveles de aceptabilidad más altos al ser comparados con el tratamiento con cremas locales u óvulos vaginales estrogénicos. Esto ha sido fundamentado principalmente por la facilidad de la aplicación, la comodidad en su patrón trimestral de recambio y su comodidad durante el uso17,18.
En el ensayo clínico estadounidense realizado por Nachtigall se compara el uso del anillo vaginal estrogénico con la aplicación de crema de estradiol, obteniéndose claros resultados a favor del anillo, siendo catalogado como excelente y muy bueno en cuanto a su facilidad de colocación (95 vs. 88%) y su comodidad en el uso (95 vs. 65%) frente a la crema local, con diferencias estadísticamente significativas26.
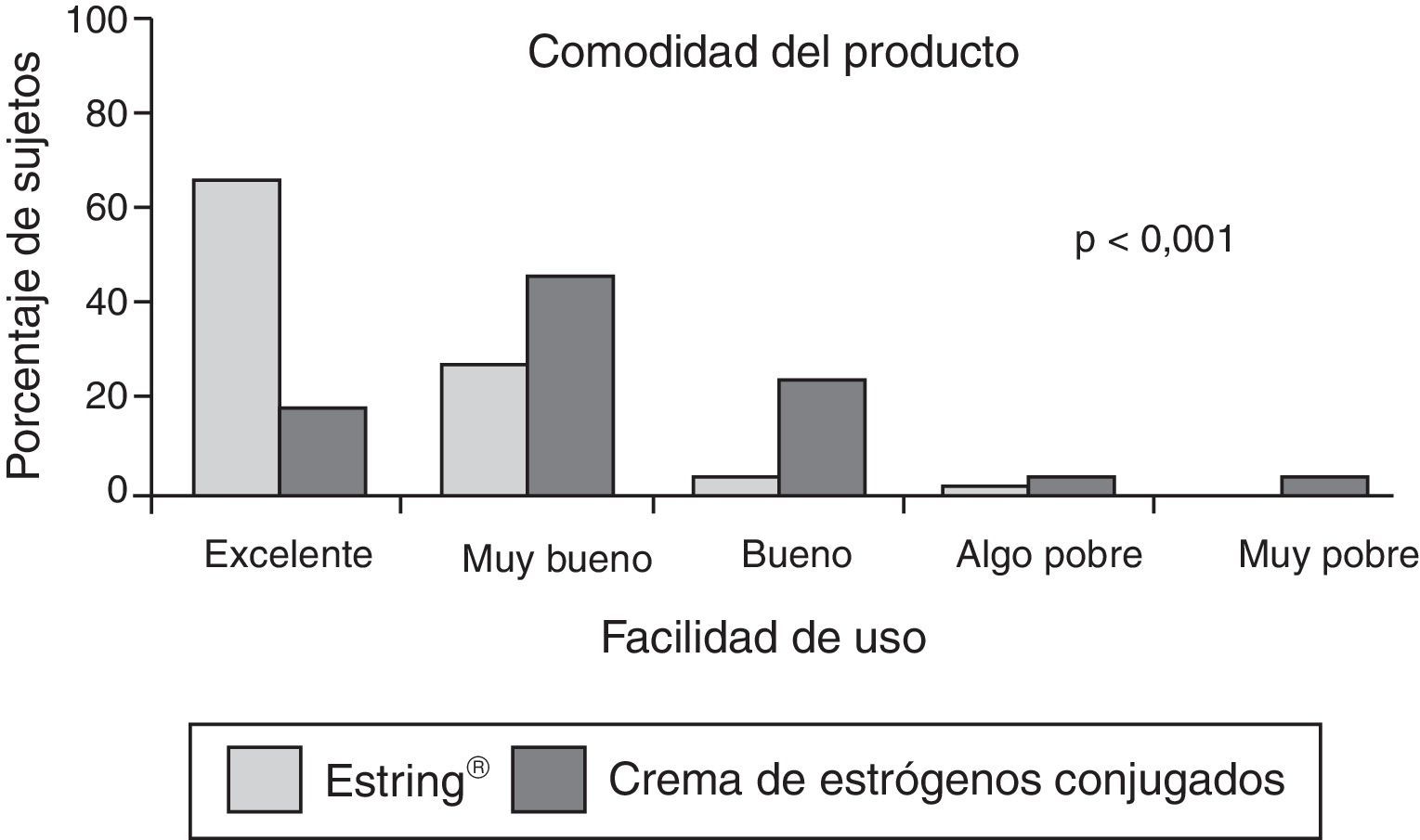
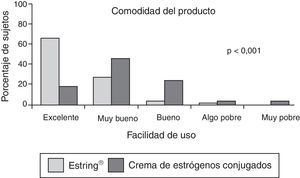
Los resultados descritos por Bachmann et al.27 en un ensayo multicéntrico con 192 pacientes y 10 centros participantes tras aplicar crema de estradiol en uno de los grupos y el anillo vaginal estrogénico en el otro, durante 12 semanas, fueron los siguientes: el 88% de las pacientes referían que el anillo vaginal no se desplazó en ningún momento, no precisando su extracción de forma voluntaria ni detectando su movilización mientras que solo un 66% de las pacientes que usaron la crema refirieron haberla administrado de forma correcta en su pauta de administración indicada; un 66% de las pacientes catalogaron el anillo como producto excelente frente a un 18% de las usuarias de la crema, y un 86% de las pacientes catalogaron el anillo vaginal como «muy fácil de usar» frente a un 35% en las usuarias de la crema vaginal (fig. 2)27.
Los datos aportados en otro estudio pivotal fueron muy contundentes. Realizaron un estudio sobre 165 mujeres, donde 83 iniciaron tratamiento con el anillo estrogénico y 82 con crema de estradiol de forma aleatorizada. Estudiaron las preferencias de las pacientes tras ser sometidas al tratamiento estrogénico local a través del anillo en primer lugar y, posteriormente, mediante la crema local en un grupo y en otro grupo a la inversa. Los resultados fueron claramente favorecedores para el anillo vaginal; las pacientes prefirieron el uso del anillo como forma de administración con unas diferencias estadísticamente significativas, sobre todo destacando como principal ventaja la facilidad de uso21.
Eugster-Hausmann et al.28, tras 12 semanas de uso, además de demostrar la eficacia en el tratamiento de los síntomas urogenitales y la seguridad del fármaco por su menor exposición estrogénica sistémica, destacan que las pacientes refieren no haberlo notado durante el tiempo de uso ni durante las relaciones sexuales28.
La aceptabilidad y la preferencia de la paciente son parámetros especialmente importantes cuando hablamos del tratamiento de los síntomas urogenitales, ya que son de larga duración, posiblemente sin fecha límite, para aumentar la adherencia y evitar abandonos por motivos de comodidad o de olvido.
Manejo clínico¿Cómo debo utilizarlo?Lo normal en la mujer posmenopáusica es utilizarlo de forma continua, es decir, que cuando finalicen los 3 meses, se retira y se coloca otro. En cualquier momento se puede descansar durante el tiempo que se estime oportuno y volver a colocarlo posteriormente. Si por cualquier motivo la paciente mancha, y se ha descartado patología endometrial, no existe ningún problema en retirarlo en ese momento y volver a colocarlo cuando haya finalizado el sangrado. En ocasiones, puede prescribirse el anillo a pacientes que tienen aún la menstruación de forma regular o que están con terapia hormonal sustitutiva cíclica. En estos casos, y coincidiendo con la menstruación, se puede retirar 3-7 días el anillo y volverlo a colocar tras finalizar la misma2.
Colocación del anilloEl tamaño de estos anillos, como hemos mencionado antes, es de 55mm de diámetro exterior y el 9mm en sección transversal y, por lo tanto, mucho más pequeñas que los anillos y pesarios utilizados para el tratamiento del prolapso. Se colocan en el fondo de saco posterior de la vagina o alrededor del cuello del útero. Las mujeres pueden insertar y quitar fácilmente los anillos por sí mismas. En personas con grandes dificultades (ejemplo artritis, obesidad, etc.), puede colocarlo el médico y, en caso necesario, repetir la intervención cada 3 meses.
¿Pueden expulsarse o caerse fácilmente?Ocasionalmente, puede expulsarse algún anillo y raras veces puede pasar inadvertida. La mayoría de las expulsiones de anillo están asociadas a un aumento de la presión abdominal, por ejemplo, con la defecación. En caso de duda, la paciente debe asegurarse que lo conserva. También el anillo puede caerse. En el estudio de Smith et al.11, de 222 mujeres, había 18 casos reportados de expulsión de anillo. La mayoría de los casos se produjeron en pacientes con prolapso uterino y no existieron dificultades en volverlo a poner. En el estudio del Population Council, el 24% de las mujeres histerectomizadas reportó una sensación de deslizamiento del anillo o la expulsión del anillo en algún momento durante el estudio de 6 meses. La mitad de estas mujeres reportaron más de un episodio29.
¿Cuando hay relaciones sexuales se deja o se quita?No es necesario quitar el anillo durante las relaciones sexuales. En el estudio de Henriksson et al.12, el 3% de las mujeres y el 8% de las parejas reportaron problemas con el anillo cuando fue dejado in situ durante el coito. En estos casos, debe de retirarse el anillo y, finalizada la relación sexual, volver a reinsertarlo. Se debe destacar que los retrasos en la reinserción del anillo podrían conducir a un mayor riesgo de sangrado.
¿Tener colocado un anillo 3 meses o más puede producir alteraciones en la mucosa vaginal?Ha habido preocupación de que los anillos vaginales puedan, a veces, producir erosiones superficiales en la mucosa vaginal. La evidencia indica que, de hecho, los anillos protegen contra erosiones superficiales, presumiblemente por mejorar el epitelio vaginal. En el estudio de Eriksen (anillo vs. ningún tratamiento para la profilaxis UTI)18, el 30% del grupo con anillo y el 29% de los controles tenían irritación vaginal al comienzo del estudio. En la visita de la terminación, no se observó irritación vaginal en ninguno de los sujetos tratados con Estring® vs. un 28% en el grupo control. La disminución en la aparición de irritación durante el periodo de estudio fue significativamente diferente entre los grupos de estudio (p=0,001).
ConclusiónEl anillo vaginal que libera ultrabaja dosis de 17-beta-estradiol es una opción muy interesante para el tratamiento de la AV. La experiencia clínica en otros países ha sido muy buena, refiriendo una gran aceptación y cumplimiento por parte de las pacientes.
La eficacia encontrada ha sido semejante a otros estrógenos locales y ha demostrado ser segura, en particular con respecto a la no predisposición de hiperplasia o carcinoma endometrial. La ultrabaja dosis y la comodidad de su uso han hecho que sea preferida por la mayoría de las usuarias.
Conflicto de interesesSantiago Palacios declara que ha sido ponente o miembro de consejos consultivos o advisor board de Servier, Pfizer, GSK, Abbot, Ferrer, Bioibérica, Shionogi, Amgen y Novo Nordisk. Además, ha recibido honorarios de investigación u honorarios de consultoría por Pfizer, Serviern Amgen, MSD, Preglem, Leon Farma, Gynea, Sandoz y Bayer. El resto de autores declaran no tener ningún conflicto de intereses.