INTRODUCCIÓN
El citomegalovirus (CMV) pertenece a la familia Herpesviridiae que, en el adulto inmunocompetente, produce una infección asintomática o levemente sintomática; sin embargo, es la causa de infección congénita viral más frecuente, con una incidencia en los neonatos que oscila entre el 0,3 y el 2,4%1. Su seroprevalencia es variable. En Europa occidental, alrededor del 50% de las gestantes es inmune al CMV al inicio de la gestación, pero esta cifra puede alcanzar el 90% en función de la etnia, la condición socioeconómica, el comportamiento sexual o la profesión2,3.
Tras la infección primaria materna, la transmisión fetal se produce en torno al 40% de los casos, con variaciónes en función de la edad gestacional (el 25% hasta la semana 23 y el 50% a partir de las 23 semanas)4,5 y con un 10-15% de recién nacidos sintomáticos al nacimiento. Del 85-90% de los nacidos asintomáticos, el 10% presentará secuelas tardías, básicamente defectos auditivos6. La afección fetal grave se produce sobre todo en las infecciones adquiridas antes de las 20 semanas, incluido el período periconcepcional7-9.
La infección materna no primaria incluye la reactivación endógena del virus o la reinfección por una nueva cepa, con una incidencia en gestantes con inmunidad previa entre el 0,4 y el 1%6,10. Aunque éstas representan el 18-25% de las infecciones congénitas por CMV, producen pocos casos de enfermedad sintomática grave, y en el 8% de los casos puede producir secuelas a largo plazo, sobre todo defectos auditivos10,11.
CASO CLÍNICO
Presentamos el caso de una paciente de 36 años de edad, con un patrón de paridad de 1-0-1-1, remitida a nuestra unidad de diagnóstico prenatal a las 17 semanas de gestación para realizar una amniocentesis por riesgo de aneuploidía estimado de 1/258 en el cribado bioquímico de segundo trimestre, realizado en su laboratorio de referencia.
La paciente no presentaba antecedentes médicos de interés, ni hábitos tóxicos, y permaneció asintomática hasta las 17 semanas de gestación. Aportaba una analítica de primer trimestre con hemograma normal, grupo O Rh positivo, serologías de virus de la inmunodeficiencia humana (VIH) y luética negativas, e inmunidad frente a toxoplasma (IgG positiva con IgM negativa) y rubéola.
El estudio ecográfico practicado el día de la amniocentesis mostró un feto con biometrías acordes con las 17 semanas de amenorrea, y llamaba la atención la presencia de hiperecogenicidad intestinal y disminución de líquido amniótico (LA), con una columna máxima de 3 cm. El resultado del cariotipo fue normal (46,XY). Se indicó un seguimiento ecográfico y en la semana 18 se objetivó un pie equino varo unilateral y un franco oligoamnios (columna máxima de 2 cm), sin que la paciente hubiera observado pérdida de LA. A las 21 semanas, las biometrías correspondían a la edad gestacional, persistía la hiperecogenicidad intestinal y se evidenció además una ventriculomegalia bilateral de 11 mm, con sospecha de agenesia del cuerpo calloso y una columna máxima de LA de 3 cm.
Ante la elevada sospecha de infección fetal, se solicitó serología materna para CMV y se decidió ofrecer una nueva amniocentesis en el momento óptimo (a partir de las 21 semanas) para estudio de la reacción en cadena de la polimerasa en la LA. La IgG de CMV en suero fue positiva y la IgM negativa. El estudio de ADN de CMV en LA por PCR resultó positivo. Se solicitó al laboratorio de microbiología que realizara análisis del ADN del LA obtenido en la primera amniocentesis realizada en la semana 17, del que se conservaba una muestra congelada, que mostraba igualmente positividad para ADN-CMV. La repetición de la serología materna reveló una persistencia de negatividad para la IgM. Paralelamente, los marcadores ecográficos iban empeorando, con aparición de dilatación del tercer ventrículo, ascitis, hepatomegalia y persistencia del oligoamnios. Ante el diagnóstico de infección fetal por CMV con afección ecográfica grave y elevado riesgo de secuelas, la paciente solicitó una interrupción legal de la gestación, que se practicó a las 22 semanas sin incidencias.
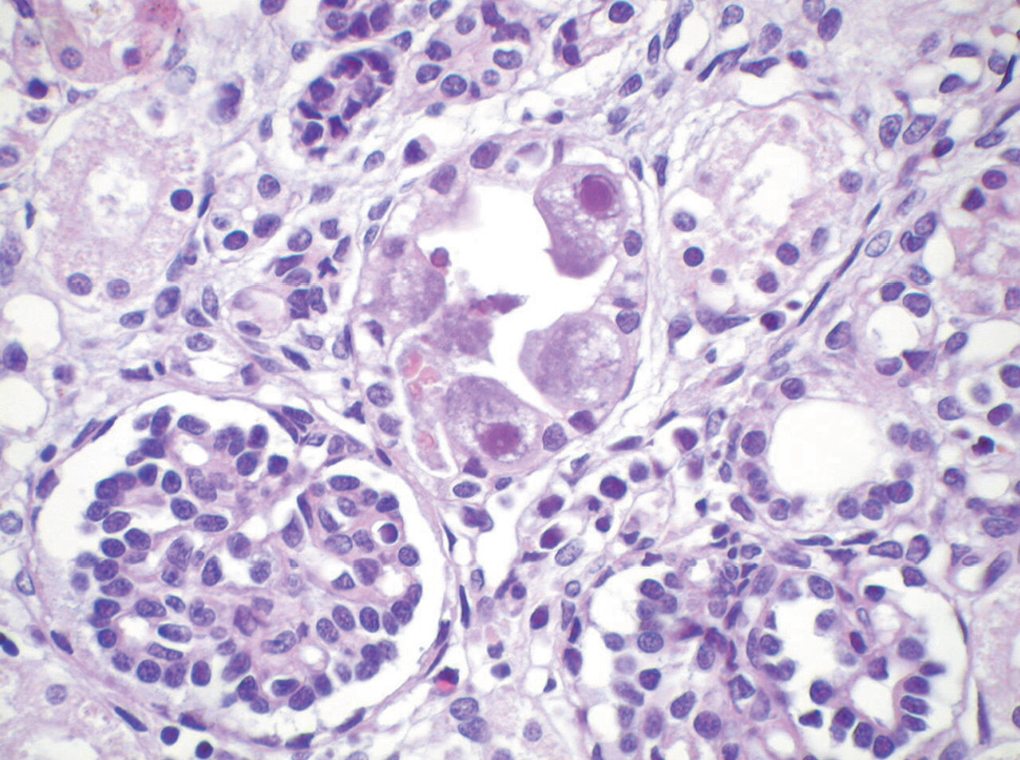
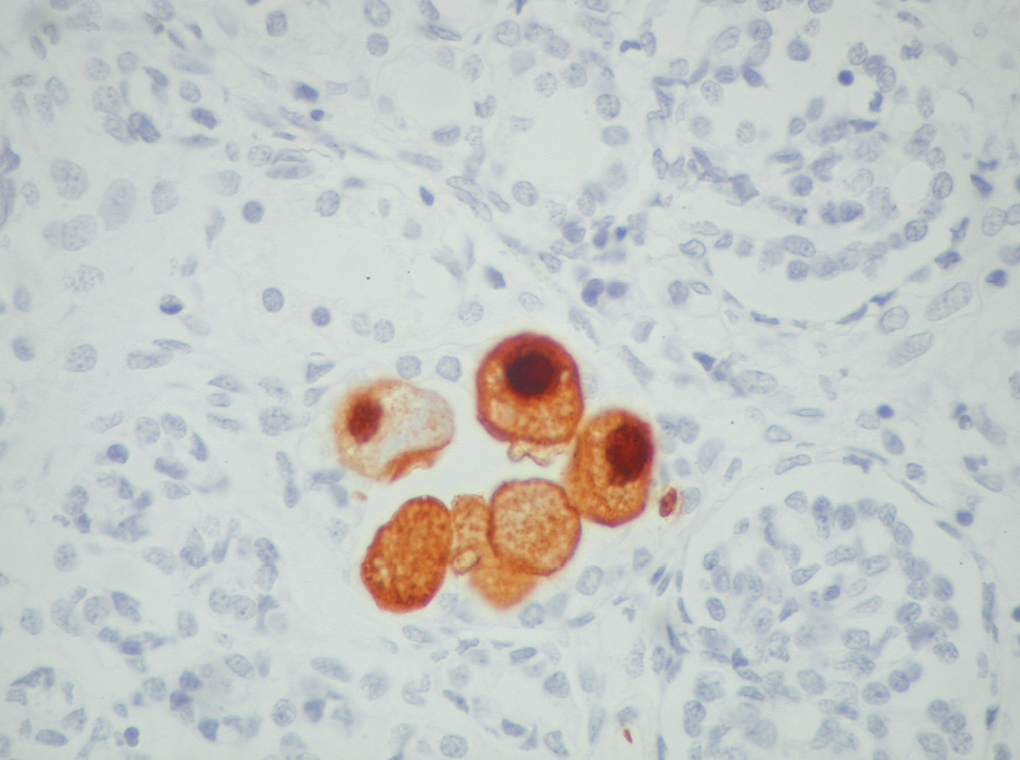
El estudio necrópsico informó de un feto masculino de dimensiones concordantes con la edad gestacional estimada, varismo podal bilateral, orejas de implantación baja, microrretrognatia y esplenomegalia. Histológicamente, se observó una encefalitis por CMV con presencia de células diagnósticas en el propio encéfalo, pulmones, riñones (fig. 1), hígado, glándulas suprarrenales, bazo, glándula tiroides, páncreas, testículos y lengua. En la placenta se observó villitis crónica con focos de necrosis e infiltrado inflamatorio de predominio linfoplasmocitario. La inmunohistoquímica demostró positividad en las células diagnósticas (fig. 2).
Figura 1. Células tubulares renales con inclusiones diagnósticas de infección por citomegalovirus. Las células se hacen más grandes (citomegalia) y muestran una inclusión eosinófila intranuclear con un halo claro periférico (en ojo de búho) y múltiples inclusiones intracitoplasmáticas basófilas (HE, x60).
Figura 2.La inmunohistoquímica demuestra la presencia de antígenos de citomegalovirus en las células diagnósticas (HE, x60).
DISCUSIÓN
A pesar de que el CMV produce la infección congénita más frecuente, con una afección fetal grave y con secuelas en el recién nacido y posnatales, las sociedades científicas no recomiendan el cribado sistemático de CMV durante la gestación. Sin duda, hay factores que inclinan a desaconsejar el cribado universal, como la escasa eficacia de la prevención primaria, la posibilidad de presentar una infección recurrente, la ausencia de un tratamiento efectivo, el riesgo de que el cribado lleve a la interrupción de gestaciones con feto no afectado o la ansiedad que puede generar en la gestante. No obstante, se han producido avances importantes en el diagnóstico de la transmisión fetal y parece discutible no ofrecer una información adecuada para que la gestante pueda decidir someterse o no al cribado4,8,12.
Actualmente, la mayoría de infecciones congénitas por CMV se detecta en fase de afección fetal grave durante una exploración ecográfica de rutina, tal como ocurrió en el caso que aquí se presenta. El 10% de los neonatos infectados son sintomáticos al nacer, ya sea con manifestaciones de «enfermedad por inclusiones citomegálicas» (petequias, hepatosplenomegalia, ictericia, neumopatía intersticial, enterocolitis, restricción de crecimiento), en fase de secuelas (microcefalia, calcificaciones periventriculares, ventriculomegalia, hipotonía, coriorretinitis, atrofia óptica) o formas mixtas. Algunos de estos signos tienen una interpretación ecográfica precoz, pero otros son silentes o pueden aparecer tardíamente.
Cuando aparecen alteraciones ecográficas, la afección fetal suele ser grave, a excepción de los focos intestinales hiperecogénicos, que se pueden deber a una enterocolitis viral transitoria12. Los signos ecográficos más frecuentes son: ventriculomegalia, microcefalia, calcificaciones intracraneales, hepatosplenomegalia, ascitis, hidrops y restricción de crecimiento4,13. La sospecha de agenesia del cuerpo calloso, que no se confirmó en la necropsia del caso aquí descrito, ha sido referida por otros autores y se debe al especial tropismo del virus sobre el sistema nervioso central y a su capacidad destructiva14,15. El 25% de las infecciones sintomáticas se acompaña de oligoamnios, probablemente secundario a nefropatía, ya que el CMV tiene también un especial tropismo por el riñón12. En el caso descrito, el oligoamnios de larga evolución pudo ser causa de la mala posición de los pies.
El diagnóstico de primoinfección materna durante la gestación puede ser dificultoso, salvo en los casos de seroconversión en pacientes con serología negativa previa. La IgM es un marcador de infección primaria, pero tiene distintos patrones de descenso, y puede desaparecer en 2-3 meses o persistir hasta 12 meses8. En pacientes inmunocompetentes no suele positivizarse en las reinfecciones. La existencia de baja avidez de la IgG es el marcador serológico más sensible de una primoinfección reciente, aunque en el caso que presentamos carecíamos de dicho marcador (no siempre disponible en los laboratorios), así como de serologías previas de la paciente. La ausencia de IgM en el momento del diagnóstico, en la semana 21, permite suponer que se trataba de una primoinfección adquirida unos meses antes, al inicio de la gestación o en el período periconcepcional, lo que explicaría la gravedad de las lesiones. No obstante, podría deberse también a una infección recurrente, ya que hay casos descritos de afección fetal grave16, aunque esta segunda opción parece menos probable.
La detección de ADN viral en LA mediante PCR permite el diagnóstico de transmisión vertical. Tiene una especificidad del 100% y una sensibilidad superior al 80%, siempre y cuando el procedimiento diagnóstico se realice por lo menos 7 semanas después de la infección materna y a partir de las 21 semanas de gestación8,17. No obstante, en el caso que presentamos, el ADN viral ya era positivo a las 17 semanas, lo que revela que la infección se produjo muy al inicio de la gestación.
Se recomienda realizar la amniocentesis ante el hallazgo de anomalías ecográficas compatibles y de serología sospechosa de primoinfección. La positividad del ADN viral en LA permite informar a la paciente de un feto infectado, con un riesgo del 10% de afección con sintomatología grave y un 10% de probables secuelas más leves a largo plazo. Sin embargo, la cuantificación de la carga viral en LA no parece guardar relación con la gravedad de la afección fetal8. Además de la edad gestacional temprana en el momento de la infección y de la evidencia de anomalías ecográficas, se considera también de mal pronóstico la detección de IgM o de una carga viral elevada en sangre fetal4,18. Recientemente se ha relacionado la gravedad de la infección con factores genéticos propios del huésped, particularmente de su respuesta inmune, que condicionarían una mayor afección en los fetos de sexo femenino13.
En el caso presentado, la aparición de signos ecográficos evolutivos en el segundo trimestre motivó la sospecha de infección por CMV que se confirmó mediante PCR en LA. Cabe destacar que no se detectó la positividad de la IgM en suero materno cuando los signos ecográficos fueron evidentes. Al no realizarse un cribado sistemático durante la gestación, las infecciones congénitas por CMV adquiridas a partir de las 20 semanas, o las de escasa definición ecográfica, no se suelen diagnosticar prenatalmente.