La definición de hemorragia posparto (HPP) no está consensuada. Prichard et al1 demostraron que la pérdida hemática media tras un parto por vía vaginal es de 500ml, mientras que tras una cesárea esa cantidad asciende a 1.000ml. Por ello, algunos autores definen la HPP como cualquier pérdida superior a esta cantidad2. Esta definición parece imprecisa, pues la apreciación clínica habitualmente subestima la pérdida hemática hasta en un 50%3. Además, algunas mujeres se afectan con pequeñas hemáticas pérdidas, como es el caso de las que presentan hipertensión y proteinuria, anemia, deshidratación o son de baja estatura4. Como alternativa, se ha propuesto definir la HPP como la que produce un descenso en el hematocrito del 10% o aquella que requiere transfusión5. Ambas definiciones son retrospectivas y, por tanto, de poca ayuda.
Pensamos que la HPP se debe definir como el sangrado vaginal > 500ml tras un parto vaginal o > 1.000ml tras una cesárea6 o aquella hemorragia que amenaza con ocasionar una inestabilidad hemodinámica en la parturienta (grado de recomendación C)4.
EPIDEMIOLOGÍALa HPP complica el 5-15% de todos los partos4. Es la causa aislada más importante de mortalidad materna. La mitad de las HPP son precoces (las que ocurren en las primeras 24h posparto)7 y son las que trataremos en este protocolo por que son, generalmente, las más agudas y graves.
La Organización Mundial de la Salud (OMS) estima en 150.000 el número de muertes anuales por HPP en el Tercer Mundo8, mientras que en algunos países como Francia esta mortalidad se calcula en 1-2/100.000 nacimientos, y de ellas, 8–9 de cada 10 serían evitables9.
En España, se ha registrado una incidencia moderada: la mortalidad materna se estima en 7,15 mujeres/100.000 nacidos vivos y la HPP es la causa del 23,07% de ésta10.
La HPP tiende a repetirse en sucesivos partos11.
FACTORES DE RIESGOAunque en dos tercios de los casos de HPP no se encuentra ningún factor de riesgo11, los obstetras debemos buscarlos y tenerlos en cuenta en el manejo del parto (grado de recomendación C)4.
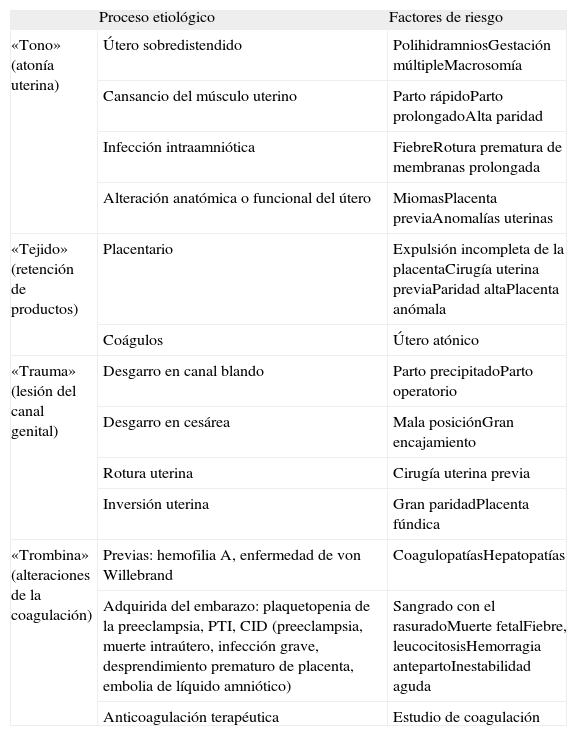
Las causas de la HPP se agrupan en 4 categorías que responden a la regla nemotécnica de las 4 «t»: tono (atonía uterina), tejido (retención de productos de la concepción), trauma (en el tracto genital) y trombina (en relación con las alteraciones de la coagulación)4. Los factores de riesgo se relacionan con las distintas causas y se exponen en la tabla 1.
Factores de riesgo de la hemorragia posparto4
| Proceso etiológico | Factores de riesgo | |
| «Tono» (atonía uterina) | Útero sobredistendido | PolihidramniosGestación múltipleMacrosomía |
| Cansancio del músculo uterino | Parto rápidoParto prolongadoAlta paridad | |
| Infección intraamniótica | FiebreRotura prematura de membranas prolongada | |
| Alteración anatómica o funcional del útero | MiomasPlacenta previaAnomalías uterinas | |
| «Tejido» (retención de productos) | Placentario | Expulsión incompleta de la placentaCirugía uterina previaParidad altaPlacenta anómala |
| Coágulos | Útero atónico | |
| «Trauma» (lesión del canal genital) | Desgarro en canal blando | Parto precipitadoParto operatorio |
| Desgarro en cesárea | Mala posiciónGran encajamiento | |
| Rotura uterina | Cirugía uterina previa | |
| Inversión uterina | Gran paridadPlacenta fúndica | |
| «Trombina» (alteraciones de la coagulación) | Previas: hemofilia A, enfermedad de von Willebrand | CoagulopatíasHepatopatías |
| Adquirida del embarazo: plaquetopenia de la preeclampsia, PTI, CID (preeclampsia, muerte intraútero, infección grave, desprendimiento prematuro de placenta, embolia de líquido amniótico) | Sangrado con el rasuradoMuerte fetalFiebre, leucocitosisHemorragia antepartoInestabilidad aguda | |
| Anticoagulación terapéutica | Estudio de coagulación |
La atonía uterina es la causa más frecuente de HPP, dado que está implicada en más de la mitad de los casos y causa el 4% de las muertes maternas12.
La placenta adherente (acretismo placentario) se presenta en 1/2.500 partos. Sin embargo, merece una mención especial por su gravedad y la tendencia ascendente de su frecuencia. En mujeres con placenta previa y útero con una o más cicatrices, el riesgo de placenta accreta puede llegar a ser ≥ 25%3.
Se ha demostrado que una actitud activa durante el alumbramiento disminuye la frecuencia de presentación de la HPP más de un 40%13. Por ello se debe recomendar la prevención de ésta de forma sistemática en todos los partos (nivel de evidencia Ia; grado de recomendación A).
DIAGNÓSTICOEl diagnóstico de la HPP es clínico y subjetivo11 y se basa tanto en la cuantificación de la pérdida hemática6 como en la sensación de que la estabilidad hemodinámica de la puérpera está en riesgo4.
Antes de empezar a actuar, es conveniente calcular la afectación hemodinámica de la mujer, para lo cual se ha propuesto la gradación reflejada en la tabla 24.
Afección hemodinámica en la hemorragia posparto4
| Sin repercusión | Leve | Moderada | Grave | |
| Pérdida hemática | 500–1.000ml10-15% | 1.000-1.500ml15-25% | 1.500-2.000ml25-35% | 2.000-3.000ml35-45% |
| Caída presión arterial sistólica | Ninguna | Ligera80–100mmHg | Marcada70–80mmHg | Profunda50–70mmHg |
| Síntomas/signos | PalpitacionesMareoTaquicardia | DebilidadSudorTaquicardia | InquietudPalidezOliguria | ColapsoDisneaAnuria |
Una vez diagnosticada la HPP, se debe actuar de manera secuencial y rápida (grado de recomendación C). La actuación ha de ser lógica y reglada. Por ello se recomienda disponer de un plan de acción previamente establecido y que resulte familiar al personal de la maternidad4.
Inicialmente, se debe realizar un soporte vital de la paciente y simultáneamente cohibir la hemorragia. Para esto último es necesario conocer y tratar la causa de ésta, para lo que es de ayuda saber si ya ha ocurrido o no el alumbramiento placentario.
MEDIDAS BÁSICAS (grado de recomendación C)4,11Son imprescindibles en la HPP en la que haya una afectación hemodinámica moderada o grave:
- –
Buscar ayuda: avisar al personal disponible (enfermera, médico de reanimación, personal auxiliar y compañero obstetra si fuese necesario), para trabajar en equipo, asignando un médico responsable, encargado de coordinar las diversas maniobras.
- –
Valorar la hemorragia.
- –
Monitorizar, si es posible con monitor automático, la presión arterial, el pulso y la saturación arterial de oxígeno.
- –
Instaurar oxigenoterapia de soporte con mascarilla.
- –
Colocar una sonda urinaria permanente con control horario de diuresis. Esto favorece la contracción del útero y sirve para evaluar la función renal. Se considera adecuada la diuresis horaria > 30ml/h.
- –
Reevaluar en la historia clínica los datos de interés, como análisis previos, evolución y características del parto, características obstétricas y personales, etc.
- –
Extracción de un hemograma y un estudio de coagulación. Petición de grupo sanguíneo y pruebas cruzadas de sangre en caso de no haberlos solicitado con anterioridad.
- –
Establecer una vía venosa de calibre adecuado o en su defecto una segunda vía.
- –
Comenzar la reposición rápida de fluidos a razón de 3:1 (300ml de reposición por cada 100 perdidos). Un metaanálisis de la Librería Cochrane recomienda la utilización de cristaloides (suero salino fisiológico o Ringer lactato) (grado de recomendación A)14.
- –
Valorar la reposición de sangre y de factores de coagulación.
- –
Registrar la medicación administrada, así como los fluidos administrados y recogidos.
Si no se ha desprendido la placenta (poco frecuente), habrá que proceder a su extracción:
- –
Si se observa una inversión uterina, habrá que reponer el útero a su localización con la ayuda del puño, presionando hacia el interior de la cavidad, siempre con ayuda de una relajación del miometrio bajo anestesia, preferentemente con gases10.
- –
Como siguiente paso se realiza un masaje uterino, presionando con una mano en el fondo del útero, para comprobar su grado de contracción y favorecer su vaciamiento. Hay que recordar que la atonía uterina es la causa más frecuente de HPP precoz. Por ello, si nos encontramos un útero blando, comenzaremos la administración de fármacos uterotónicos como se explica posteriormente. La presencia de coágulos en el útero o en la vagina nos informa de una buena coagulación en ese momento.
- –
Si continúa la HPP, para descartar traumatismos en el útero y en el canal blando, así como retención de tejidos dentro del útero, se considera imprescindible que el personal más cualificado disponible en el momento realice bajo anestesia una revisión sistemática del canal blando del parto. Se comenzará desde el fondo del útero hacia el segmento uterino y por todas las caras del útero para comprobar que la cavidad está vacía. Se debe realizar una revisión manual de la cicatriz de cesárea previa si ésta existiera. En caso de persistir restos intraútero, se debe realizar un legrado uterino. Habrá que ser especialmente cuidadoso con la posibilidad de perforación del útero puerperal grande y blando. A continuación, se realiza una revisión de ambos ángulos del cuello y de todas las caras de la vagina. Si hay desgarros se procederá a su sutura.
- –
Si se recibe el estudio de coagulación alterado, habrá que realizar el tratamiento específico de la alteración. En caso necesario, se realizará una transfusión sanguínea. Si es preciso, se pedirá ayuda al hematólogo, si está disponible.
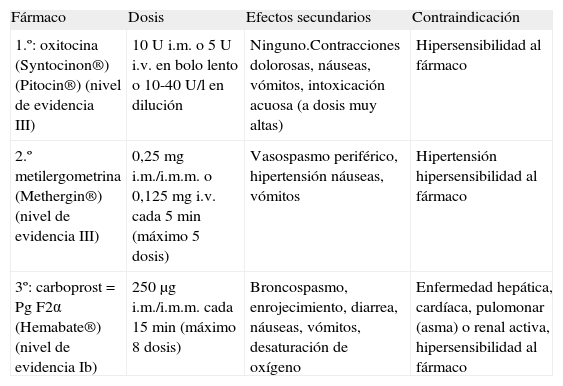
Simultáneamente a la realización de un masaje continuado del útero, se procede a la administración vía parenteral de fármacos uterotónicos de manera secuencial, salvo contraindicaciones y hasta agotar las dosis (tabla 3)3,4.
Fármacos uterotónicos3,4
| Fármaco | Dosis | Efectos secundarios | Contraindicación |
| 1.º: oxitocina (Syntocinon®) (Pitocin®) (nivel de evidencia III) | 10 U i.m. o 5 U i.v. en bolo lento o 10-40 U/l en dilución | Ninguno.Contracciones dolorosas, náuseas, vómitos, intoxicación acuosa (a dosis muy altas) | Hipersensibilidad al fármaco |
| 2.º metilergometrina (Methergin®) (nivel de evidencia III) | 0,25mg i.m./i.m.m. o 0,125mg i.v. cada 5min (máximo 5 dosis) | Vasospasmo periférico, hipertensión náuseas, vómitos | Hipertensión hipersensibilidad al fármaco |
| 3º: carboprost = Pg F2α (Hemabate®) (nivel de evidencia Ib) | 250μg i.m./i.m.m. cada 15min (máximo 8 dosis) | Broncospasmo, enrojecimiento, diarrea, náuseas, vómitos, desaturación de oxígeno | Enfermedad hepática, cardíaca, pulomonar (asma) o renal activa, hipersensibilidad al fármaco |
i.m.: intramuscular; i.m.m: intramiometrial; i.v.: intravenoso; Pg: prostaglandina; U: unidades.
Una alternativa al carboprost es el misoprostol (prostaglandina E1), si bien la indicación de HPP no figura en la ficha técnica del fármaco en España. En una reciente revisión sistemática, 200μg por vía oral asociados a 400μg por vía sublingual o rectal redujeron significativamente la incidencia de HPP > 500ml una vez instaurada la hemorragia15.
Una reciente revisión Cochrane demuestra que el misoprostol a dosis de 800μg por vía rectal es un fármaco de mayor efectividad que la oxitocina o que la combinación de oxitocina con metilergometrina (nivel de evidencia Ia)16. Se acepta su uso como tratamiento de primera línea en países del Tercer Mundo porque es un fármaco muy barato y que se conserva a temperatura ambiente, a diferencia de la oxitocina y la metilergometrina, que requieren refrigeración11.
TRATAMIENTO DE LA HEMORRAGIA POSPARTO PERSISTENTESi tras las medidas previas la HPP no cede, se procede a un abordaje más agresivo. Según la estabilidad de la puérpera, la disponibilidad y el conocimiento de la técnica que se debe realizar, y siempre favoreciendo los procedimientos menos agresivos y valorando los deseos genésicos de la mujer, se puede optar a realizar alguno de los siguientes procedimientos:
- –
Taponamiento uterino (nivel de evidencia III, grado de recomendación B). Se puede utilizar una sonda-balón de Sengstaken-Blakemore17 o un balón específico de Bakri18, o una tira de gasa ancha que rellene toda la cavidad uterina y que se deja ubicada dentro del útero. Estos procedimientos perdieron popularidad porque se pensó que ocultaban la hemorragia y causaban infección, pero estas suposiciones no se han demostrado16,19.
- –
Embolización arterial selectiva (nivel de evidencia III, grado de recomendación B). Consiste en la cateterización, a través de radiología intervencionista, de los vasos sangrantes con el objetivo de realizar la oclusión de éstos de la forma más selectiva y distal4. Como lo habitual es que ambas arterias uterinas estén implicadas, es frecuente su embolización bilateral. Su objetivo, al igual que el de las ligaduras vasculares, consiste en disminuir de manera transitoria la presión de perfusión, con objeto de que los mecanismos fisiológicos de la hemostasia y la coagulación detengan la hemorragia. Ambos procedimientos preservan la fertilidad. De hecho, se han comunicado varios casos de embarazos posteriores, incluso tras la exclusión de la vascularización ovárica9. Esta técnica requiere disponer de radiología intervencionista con experiencia. El éxito de la técnica se estima en el 70-100%9, pero su realización se ve dificultada tras la práctica de ligaduras vasculares.
- –
Ligaduras vasculares (nivel de evidencia III; grado de recomendación B)9. Cuando las maniobras anteriores fracasan o no son utilizables, se deben considerar las ligaduras vasculares, ya que son fáciles y rápidas de realizar4.
- –
Ligadura uterina bilateral. Por vía abdominal, se realiza traccionando del útero hacia arriba. Consiste en ligar en masa la rama ascendente de la arteria uterina y la vena que le acompaña en profundidad, cogiendo parte del miometrio subyacente con una aguja atraumática y sutura reabsorbible. La altura ideal sería unos 2–3cm por debajo de la histerotomía de una cesárea. Por vía vaginal, es posible el acceso a los vasos uterinos si se realiza una incisión horizontal en el labio anterior del cuello, a un centímetro por debajo del pliegue cervicovaginal y se rechaza la vejiga hacia arriba. La eficacia por ambas vías es superior al 90% y la causa principal de fracaso son las anomalías de inserción placentaria9.
- –
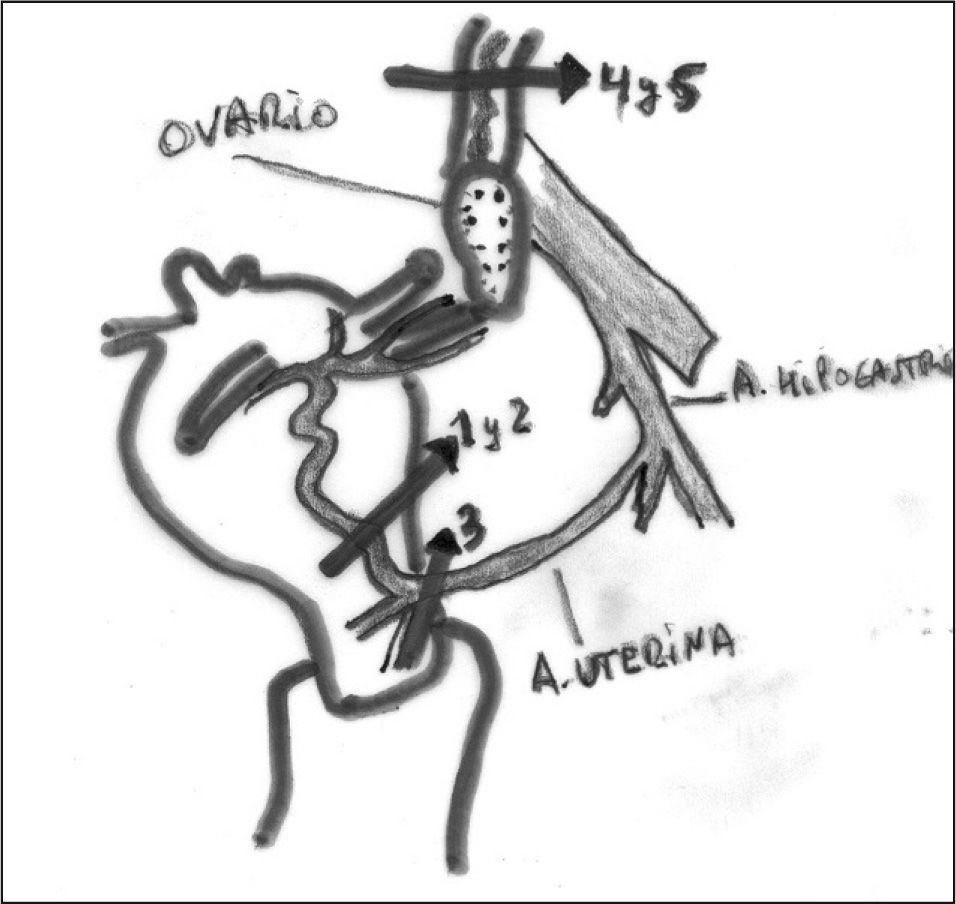
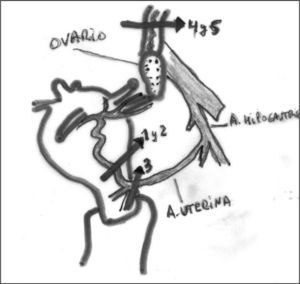
Ligadura arterial progresiva. Se trata de la desvascularización progresiva de los pedículos vasculares aferentes al útero. Cada etapa sólo se realiza si la anterior no ha cohibido la hemorragia tras 10min. Las etapas son: a) ligadura unilateral de la rama ascendente de la arteria uterina; b) ligadura de la arteria uterina contralateral; c) ligadura baja de las 2 uterinas y de sus ramas cervicovaginales, 3–5cm por debajo de las ligaduras precedentes y una vez que se ha despegado la plica vesicouterina; d) ligadura unilateral de un pedículo lumboovárico, y e) ligadura del pedículo contralateral. El tercer paso implica la desvascularización del segmento uterino inferior y la parte alta del cuello. Un estudio de 123 casos demuestra una eficacia del 100%20. La atonía uterina fue la principal indicación. El tercer paso únicamente fue necesario para las anomalías de inserción y el quinto sólo para las coagulopatías20. Los pasos se pueden ver en la figura 1.
- –
Ligadura bilateral de las arterias hipogástricas. El lugar de elección para ligar las arterias ilíacas internas es a unos 2cm por debajo de su bifurcación de la arteria ilíaca común, para evitar la ligadura de ramas posteriores que irrigan la región glútea. Su realización es técnicamente difícil, su morbilidad es elevada y, porque es una ligadura proximal, su eficacia es inconstante (42-100%). Además los estudios son de series poco extensas, por lo que la efectividad se puede considerar poco documentada4.
- –
Plicatura/capitonaje (nivel de evidencia III; grado de recomendación B). Son técnicas que consiguen la compresión del útero mediante suturas reabsorbibles transmurales.
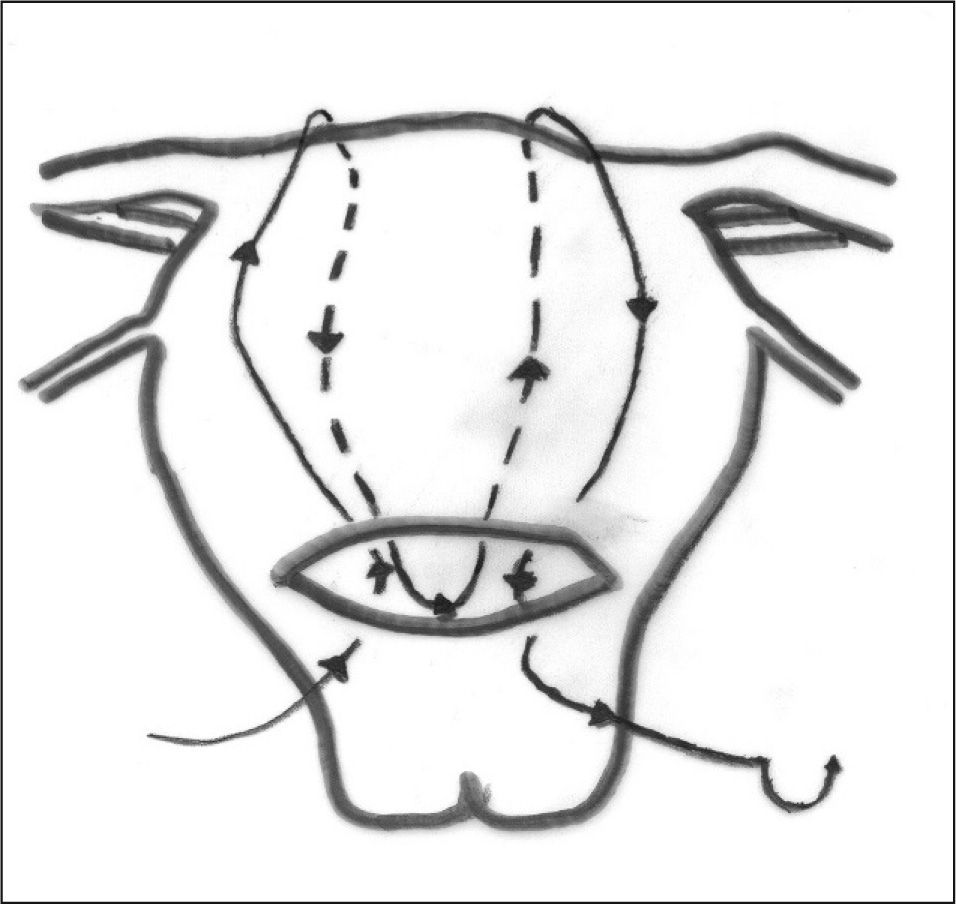
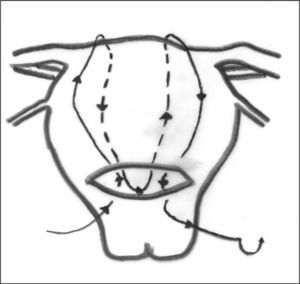
Cuando la indicación es la atonía uterina poscesárea, la técnica más conocida es la de B-Lynch21. Previo a su realización, se comprueba que el útero deja de sangrar al realizar una compresión manual desde el fondo uterino con una mano. La sutura, que es continua, comienza en la cara anterior, en un lateral del labio inferior de la histerotomía, a unos 2cm por dentro del ángulo de ésta. Desde fuera entra en la cavidad uterina, sale por el labio superior, rodea la superficie uterina por arriba y penetra en cavidad por la cara posterior a nivel de segmento. Desde allí, sale por la cara posterior en el otro lado del útero y sigue un recorrido paralelo en el lado contralateral, como se observa en la figura 2, hasta anudar ambos extremos en el borde inferior de la histerotomía.
Para cuando no se ha realizado una cesárea, se ha descrito una técnica similar con aguja recta para poder atravesar el útero en sentido anteroposterior, rodearlo y suturar en la zona del segmento uterino22.
Las técnicas de capitonaje son suturas transmurales que, mediante puntos simples o en marco, buscan la hemostasia comprimiendo la cara anterior con la posterior del útero de forma localizada. Su indicación ideal es en las anomalías de placentación9. La casuística publicada de todas estas técnicas es escasa, pero los resultados son buenos.
- –
Histerectomía (nivel de evidencia III; grado de recomendación B). Debido a la realización de las otras técnicas antes descritas, la histerectomía posparto tiene unas indicaciones cada vez más restrictivas9. Estaría indicada cuando falla el tratamiento conservador, cuando haya un gran destrozo uterino (sobre todo en caso de rotura extensa) o en casos de placenta accreta extensa; esta última es la indicación más frecuente hoy día. Además, el tratamiento conservador puede estar cuestionado en mujeres mayores, en multíparas, o en aquellas que no desean más hijos, o si presentan un útero patológico9. La técnica de elección es la histerectomía total conservando anejos, pues no se ha podido demostrar que la histerectomía subtotal acorte el tiempo quirúrgico ni la pérdida de sangre y sí que puede dejar zonas vasculares sangrantes2,4. No obstante, la elección de la técnica que se realizará depende de factores difícilmente explicables sobre el papel y que requieren la toma de decisión durante el propio acto quirúrgico.
- –
Taponamiento pélvico. Está indicado tras la histerectomía, en casos de coagulopatías de consumo o en hemorragias difusas. Se realiza un taponamiento con múltiples compresas que compriman la pelvis y se dejan 24h más desde la corrección de la coagulopatía4. También se puede utilizar un paquete de compresas con tracción transvaginal. En estos casos, se requiere sonda urinaria permanente para descartar la obstrucción urinaria, drenajes pélvicos para valorar la evolución y antibióticos profilácticos de amplio espectro19. La eficacia se limita a la descripción de su uso en casos aislados y no es esperable un estudio comparativo con otras técnicas (nivel de evidencia III).
- –
Factor VII recombinante. En caso de hemorragia por coagulopatía con afectación vital, puede considerarse, si está disponible, la administración de factor VII recombinante23, aunque no existen estudios suficientes que avalen su seguridad.
El mejor tratamiento de la HPP es, sin duda, su prevención. La identificación de los factores de riesgo será de gran ayuda, pero la prevención de la HPP se debe realizar de forma sistemática en todos los partos, existan o no factores de riesgo (nivel de evidencia Ia; grado de recomendación A)24.
Está demostrado que el uso rutinario de oxitocina tras la salida del hombro anterior reduce el riesgo de hemorragia posparto > 40% y tan sólo es preciso tratar profilácticamente a 22 mujeres para evitar una HPP13. Las principales ventajas son su rápido mecanismo de acción y que, a diferencia de la metilergometrina, no eleva la presión arterial ni produce contracciones tetánicas del útero. Además, no se ha demostrado un aumento de la retención placentaria. Existen diversos protocolos efectivos: 10 unidades intramusculares o 5 unidades por vía intravenosa lento o 10–20 U/l a 100–150ml/h. No se ha demostrado que ninguno de estos protocolos sea superior a otro en cuanto a vía, dosis, pauta o momento de administración4. De todas formas, la oxitocina tiene una vida media corta y para mantener su eficacia y evitar atonías secundarias es preciso proseguir su administración por perfusión por vía intravenosa durante 4–6h o asociándola a otros uterotónicos.
Esquema de actuación ante la hemorragia posparto precoz4
| Paso 1Manejo inicial | |
| Medidas básicas: | Buscar etiología |
| Solicitar ayuda; valorar sangrado; medir presión arterial, pulso, SaO2; oxigenoterapia; sonda urinaria; valorar historia clínica; hemograma, coagulación, grupo de sangre, pruebas cruzadas; vía venosa de buen calibre; reponer fluidos, sangre y factores coagulación; registrar fluidos y fármacos | 1. Extracción placenta (si procede)2. Reposición uterina (si procede)3. Masaje uterino4. Revisión sistemática de cavidad y del canal blando |
| Paso 2Tratamiento etiológico | |||
| Tono | Tejido | Trauma | Trombina |
| – Masaje | – Retirada manual | – Corregir inversión | – Tratamiento específico |
| – Compresión | – Legrado | – Reparar desgarro y/o rotura | |
| – Fármacos (tabla 3) | |||
| Paso 3Tratamiento de la hemorragia posparto refractaria |
|
La asociación de metilergometrina mejora un poco la eficacia en comparación con el empleo de oxitocina sola en el manejo activo del alumbramiento. Sin embargo, la tasa de complicaciones es mayor (nivel de evidencia Ia)25. El misoprostol no es tan efectivo como la oxitocina en la prevención de la HPP y posee más efectos secundarios. Los más frecuentes son los temblores y la fiebre, y se relacionan con la dosis administrada (nivel de evidencia Ia)26.
La carbetocina, un análogo sintético de la oxitocina pendiente de comercializar en España en 2007, tiene un inicio de acción rápido y una vida media prolongada de 40min. Los estudios existentes demuestran que es bien tolerada y tan efectiva o más que la oxitocina (nivel de evidencia Ib)27,28.
Como ya hemos reseñado, en todos los partos es preceptivo mantener una conducta activa en el alumbramiento para evitar la HPP. Ésta suele incluir la administración de oxitócicos continuados junto con el pinzamiento y el corte temprano del cordón y la tracción controlada de éste. Estas maniobras asociadas han demostrado disminuir la pérdida media de sangre, la incidencia de HPP y el alumbramiento prolongado, sin afectar al recién nacido, aunque con algún efecto secundario para la madre cuando se emplea ergometrina (hipertensión, náuseas y vómitos) (nivel de evidencia Ia)29.
Aunque el corte temprano del cordón parece que reduce la duración del alumbramiento, no hay evidencia de que esta práctica sola disminuya el riesgo de HPP4. La tracción controlada del cordón umbilical no ha sido estudiada independientemente, por lo que el efecto de la denominada conducta activa del alumbramiento puede deberse en exclusiva a la acción de la oxitocina4. Sin embargo, mientras no se distinga qué parte del protocolo es prescindible, éste se debe realizar preferentemente en su totalidad7, si bien se puede considerar el uso sólo de oxitocina cuando la paciente rechace la manipulación del cordón.
Una vez aplicadas estas maniobras, la placenta debe expulsarse de forma espontánea. Si esto no ocurre, se administrará oxitocina. Una vez expulsada la placenta, se comprobará que el útero está bien contraído y se revisará la placenta para comprobar su integridad (grado de recomendación A)4.
Clasificación de las recomendaciones en función del nivel de evidencia disponible
| Ia La evidencia científica procede a partir de metaanálisis de ensayos clínicos controlados y aleatorizados |
| Ib La evidencia científica procede de al menos un ensayo clínico controlado y aleatorizado |
| IIa La evidencia científica procede de al menos un estudio prospectivo controlado, bien diseñado y sin aleatorizar |
| IIb La evidencia científica procede de al menos un estudio casi experimental, bien diseñado |
| III La evidencia científica procede de estudios descriptivos no experimentales, bien diseñados como estudios comparativos, de correlación o de casos y controles |
| IV La evidencia científica procede de documentos u opiniones de expertos y/o experiencias clínicas de autoridades de prestigio |
Grados de recomendación
| A Existe buena evidencia a partir de la investigación para apoyar la recomendación. (Recoge los niveles de evidencia científica Ia y Ib) |
| B Existe moderada evidencia a partir de la investigación para apoyar la recomendación (Recoge los niveles de evidencia científica IIa, IIb y III) |
| C La recomendación se basa en la opinión de expertos o en un panel de consenso. (Recoge el nivel de evidencia IV) |
Los Protocolos Asistenciales en Ginecología y Obstetricia y los Protocolos de Procedimientos Diagnósticos y Terapéuticos de la Sociedad Española de Ginecología y Obstetricia pretenden contribuir al buen quehacer profesional de todos los ginecólogos, especialmente los más alejados de los grandes hospitales y clínicas universitarias. Presentan métodos y técnicas de atención clínica aceptadas y utilizadas por especialistas en cada tema. Estos protocolos no deben interpretarse de forma rígida ni excluyente, sino que deben servir de guía para la atención individualizada a las pacientes. No agotan todas las posibilidades ni pretenden sustituir a los protocolos ya existentes en Departamentos y Servicios Hospitalarios.