Investigar mediante un estudio observacional, prospectivo y multicéntrico la eficacia y la seguridad de un extracto isopropanólico estandarizado de Cimicifuga racemosa (CR) (Remifemin®) para tratar la clínica climatérica.
Material y métodoEstudio multicéntrico, observacional y prospectivo en el que participaron 483 mujeres posmenopáusicas (menopausia natural), entre abril y agosto de 2004. Todas las pacientes registraron, en un cuestionario al inicio y a los 3 meses de tratamiento, la presencia e intensidad (leve, moderada y severa) de sofocos, crisis de sudoración, irritabilidad, nerviosismo y depresión. Las pacientes recibieron 40 mg/día de CR durante 12 semanas. Se comparó la evolución de los síntomas antes y después del tratamiento. El estudio estadístico se realizó mediante la prueba de la χ2.
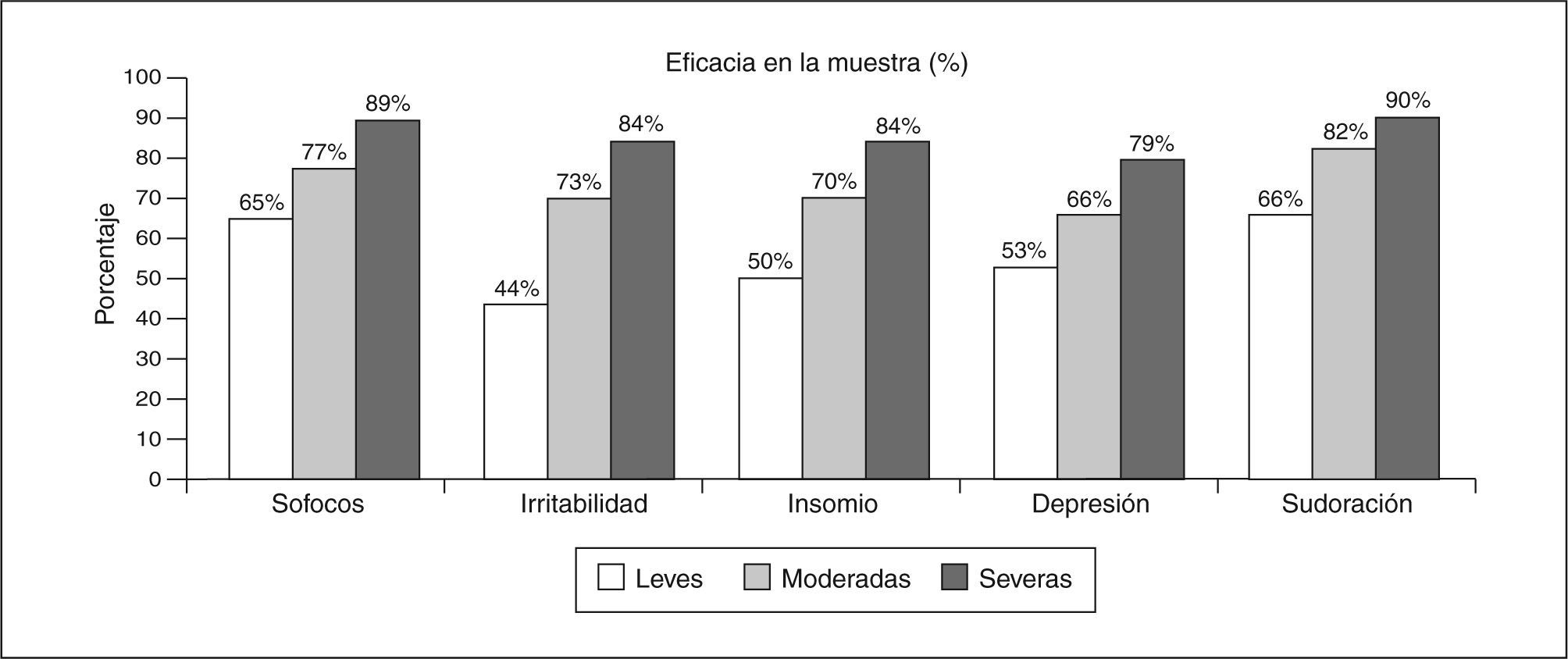
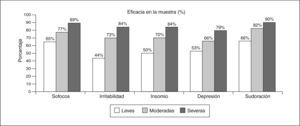
ResultadosLa tolerancia fue excelente: ninguna paciente abandonó el tratamiento debido a efectos secundarios. La eficacia del tratamiento con CM se consideró buena por la mayoría de los clínicos. De las 483 pacientes enroladas, 471 acudieron a la segunda visita (las 12 mujeres que no acudieron a la segunda visita fueron consideradas dentro del grupo de mujeres que no mejoraron); de las 483 mujeres con sofocos, el 77% mejoró. Atendiendo a la intensidad de los sofocos, el 85, el 76 y el 64% de las pacientes con síntomas severos, moderados y leves, respectivamente, mejoraron. Los sofocos y las crisis de sudoración fueron los síntomas que presentaron más mejoría. Un 78% de las crisis de sudoración mejoró: severas, 85%; moderadas, 81%, y leves, 65%. Las tasas de mejoría respecto a síntomas psíquicos estuvieron por encima del 70%: irritabilidad severa, 77%; moderada, 72%, y leve, 43%; depresión severa 78%; moderada, 64%, y leve, 51%, e insomnio severo 78%, moderado 69%, y leve, 49%.
ConclusionesEl tratamiento con CM (40 mg/día) de las pacientes con clínica climatérica es una alternativa segura y eficaz en los casos en que las pacientes no puedan o no quieran recibir terapia hormonal.
To evaluate the safety and efficacy of a standardized isopropanolic extract of Cimicifuga racemosa (CR) (Remifemin®) in the treatment of climacteric symptoms.
Material and methodWe performed a multicenter observational prospective study in 483 postmenopausal women (natural menopause) between April and August 2004. In all patients, the presence and intensity (mild, moderate, severe) of hot flashes, sweating, irritability, nervousness, and depression were registered in a questionnaire administered at the beginning of treatment and 3 months later. The patients received 40 mg/day of CR for 12 weeks. Symptoms were evaluated before and after treatment. The statistical analysis was performed using the chi-squared test.
ResultsTolerance was excellent with no treatment withdrawals due to adverse effects. Efficacy was considered good by most of the clinicians. Of the 483 patients enrolled, 471 attended the second visit (the 12 women not attending the second visit were included in the group of women showing no improvement). Of the 483 women with hot flashes, 77% improved. The intensity of hot flashes was reduced in 85%, 76% and 64% of the patients with severe, moderate, and mild symptoms, respectively. The symptoms showing greatest improvement were hot flashes and sweating: sweating improved in 78% (severe 85%, moderate 81% mild 65%). Rates of improvement were over 70% for psychic symptoms: irritability (severe 77%, moderate 72%, mild 43%), depression (severe 78%, moderate 64%, mild 51%) and insomnia (severe 78%, moderate 69%, mild 49%).
ConclusionsCM (40 mg/day) is a safe and effective alternative for the treatment of climacteric symptoms in women who cannot or do not wish to receive hormone replacement therapy.
Los síntomas vasomotores observados durante el climaterio mejoran con la terapia hormonal sustitutiva (THS) (con o sin progesterona) y existen datos suficientes para afirmar el efecto beneficioso de este tratamiento para mantener la masa ósea1 y contribuir a la normalización del perfil lipídico2. La THS, sin embargo, aumenta el riesgo de cáncer de mama y de accidentes tromboembólicos2. La decisión de administrar THS deberá tener en cuenta, individualizadamente, los beneficios y los riesgos de esa terapia. Son las pacientes con riesgos que superan a los beneficios y aquellas que no desean ser tratadas con estrógenos las que demandan tratamientos alternativos para combatir sus síntomas.
En los últimos años, numerosos ensayos clínicos han demostrado la eficacia y seguridad del extracto isopropanólico estandarizado de Cimicifuga racemosa (CR) en el alivio de los síntomas climatéricos3, tales como sofocos, ansiedad, depresión y otras molestias ginecológicas4.
Liske et al5 confirman la ausencia de acción estrogénica de CR, incluso con dosis 3 veces superior a la recomendada. Estudios in vivo e in vitro confirman la ausencia de acción estrogénica en muestras de tejido uterino y vaginal6,7, así como una acción estrogénica en otros tejidos como hueso8; esto haría de CM un moduladores selectivos de los receptores de estrógenos (SERM) natural.
Para explicar la actividad biológica de los extractos de CR en los síntomas psíquicos y vasomotores, se han postulado otros mecanismos de acción relacionados con la modulación de las funciones dopaminérgicas y serotoninérgicas9,10.
Nuestro objetivo, en el presente estudio observacional, es investigar si aparece mejoría en síntomas como sudoración, irritabilidad, insomnio y depresión, después de 3 meses de tratamiento con 40mg/día del extracto isopropanólico de CR en mujeres climatéricas; éste es el estudio más amplio hecho hasta la fecha en España con CR.
MATERIAL Y MÉTODOEstudio multicéntrico, observacional y prospectivo en el que participaron 50 ginecólogos españoles elegidos aleatoriamente. El 75% de los ginecólogos desempeñaba su actividad profesional en el ámbito de la medicina privada y el 25%, en la medicina pública. Se solicitó a cada uno de los 50 ginecólogos que reclutase hasta 10 pacientes posmenopáusicas (menopausia natural), con edades comprendidas entre los 45 y los 65 años. Ninguna de las pacientes reclutadas debía haber sido tratada previamente con THS ni con otros tratamientos para combatir la clínica menopáusica. El período de reclutamiento se extendió entre abril y agosto de 2004.
Se respetaron los requerimientos de la guía de buenas prácticas médicas y la declaración de Helsinki. Antes de su inclusión, se informó a las pacientes de las características del estudio y éstas dieron su consentimiento.
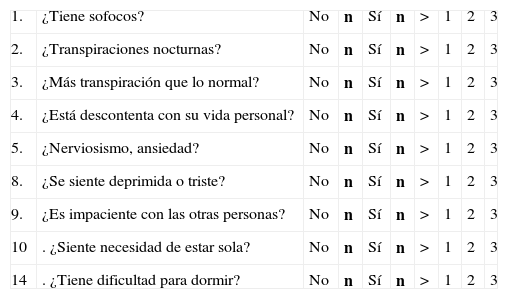
En la primera visita, cada paciente completó un cuestionario en la consulta del ginecólogo. En este cuestionario se valoraba la presencia y la intensidad de varios síntomas vasomotores y psíquicos (anexo 1). Si bien no se trataba de una escala validada, se optó por ella debido a su facilidad de uso y su comodidad, tanto para el clínico como para las pacientes. El cuestionario valoraba la intensidad de los síntomas mediante una escala numérica: 1: ausencia de síntomas; 2: síntomas leves; 3: síntomas moderados, y 4: síntomas severos. Cada síntoma fue evaluado de forma independiente. Una vez completado el primer cuestionario, las pacientes iniciaron tratamiento con CR (Remifemin®) a dosis de 20mg cada 12h durante 12 semanas. Tras finalizar este período de tratamiento, se pidió a las pacientes que completasen de nuevo el mismo cuestionario. El médico valoró la eficacia del tratamiento en buena o mala.
Cuestionario específico de sintomatología en la menopausia
La CR (Remifemin®) redujo significativamente la intensidad de los sofocos (p < 0,00001) y los síntomas vasomotores (p < 0,00001). Remifemin® fue más eficaz en las mujeres con síntomas severos en la reducción de sofocos y síntomas climatéricos.
La tolerancia al tratamiento fue muy buena; sólo 4 (1%) mujeres presentaron efectos adversos. Liske et al5 presentan datos similares a los obtenidos en nuestro estudio. Osmers11 (2006), en un estudio aleatorizado, multicéntrico y doble ciego en el que se evalúa la eficacia y seguridad de CR en 304 mujeres tratadas con CR (40mg/día) durante 12 semanas, refieren 8 mujeres con problemas gastrointestinales frente a 7 en el grupo tratado con placebo, lo que confirma los escasos efectos adversos de CR4,11,12.
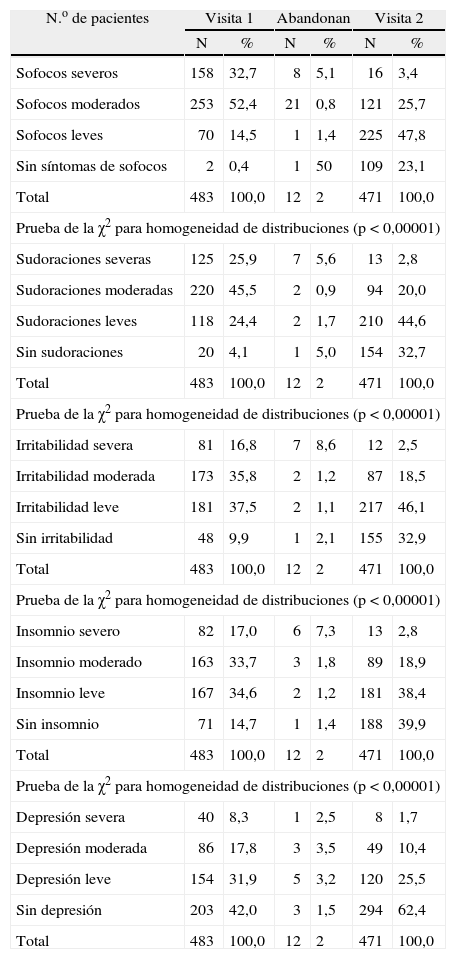
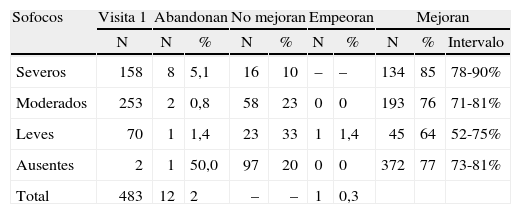
La tabla 1 recoge los datos demográficos de las mujeres estudiadas. La tabla 2 muestra los resultados obtenidos en ambos cuestionarios. De las 483 mujeres enroladas sólo 12 abandonaron (considerando a este grupo dentro de las mujeres que no mejoraron). La tabla 3 refleja la mejoría en función de la intensidad de los síntomas.
Resultados del cuestionario antes y después de las 12 semanas de tratamiento con Cimicifuga racemosa
| N.o de pacientes | Visita 1 | Abandonan | Visita 2 | |||
| N | % | N | % | N | % | |
| Sofocos severos | 158 | 32,7 | 8 | 5,1 | 16 | 3,4 |
| Sofocos moderados | 253 | 52,4 | 21 | 0,8 | 121 | 25,7 |
| Sofocos leves | 70 | 14,5 | 1 | 1,4 | 225 | 47,8 |
| Sin síntomas de sofocos | 2 | 0,4 | 1 | 50 | 109 | 23,1 |
| Total | 483 | 100,0 | 12 | 2 | 471 | 100,0 |
| Prueba de la χ2 para homogeneidad de distribuciones (p < 0,00001) | ||||||
| Sudoraciones severas | 125 | 25,9 | 7 | 5,6 | 13 | 2,8 |
| Sudoraciones moderadas | 220 | 45,5 | 2 | 0,9 | 94 | 20,0 |
| Sudoraciones leves | 118 | 24,4 | 2 | 1,7 | 210 | 44,6 |
| Sin sudoraciones | 20 | 4,1 | 1 | 5,0 | 154 | 32,7 |
| Total | 483 | 100,0 | 12 | 2 | 471 | 100,0 |
| Prueba de la χ2 para homogeneidad de distribuciones (p < 0,00001) | ||||||
| Irritabilidad severa | 81 | 16,8 | 7 | 8,6 | 12 | 2,5 |
| Irritabilidad moderada | 173 | 35,8 | 2 | 1,2 | 87 | 18,5 |
| Irritabilidad leve | 181 | 37,5 | 2 | 1,1 | 217 | 46,1 |
| Sin irritabilidad | 48 | 9,9 | 1 | 2,1 | 155 | 32,9 |
| Total | 483 | 100,0 | 12 | 2 | 471 | 100,0 |
| Prueba de la χ2 para homogeneidad de distribuciones (p < 0,00001) | ||||||
| Insomnio severo | 82 | 17,0 | 6 | 7,3 | 13 | 2,8 |
| Insomnio moderado | 163 | 33,7 | 3 | 1,8 | 89 | 18,9 |
| Insomnio leve | 167 | 34,6 | 2 | 1,2 | 181 | 38,4 |
| Sin insomnio | 71 | 14,7 | 1 | 1,4 | 188 | 39,9 |
| Total | 483 | 100,0 | 12 | 2 | 471 | 100,0 |
| Prueba de la χ2 para homogeneidad de distribuciones (p < 0,00001) | ||||||
| Depresión severa | 40 | 8,3 | 1 | 2,5 | 8 | 1,7 |
| Depresión moderada | 86 | 17,8 | 3 | 3,5 | 49 | 10,4 |
| Depresión leve | 154 | 31,9 | 5 | 3,2 | 120 | 25,5 |
| Sin depresión | 203 | 42,0 | 3 | 1,5 | 294 | 62,4 |
| Total | 483 | 100,0 | 12 | 2 | 471 | 100,0 |
Prueba de la χ2 para homogeneidad de distribuciones (p < 0,00001)
Tasa de mejoría en función de la intensidad de los síntomas
| Sofocos | Visita 1 | Abandonan | No mejoran | Empeoran | Mejoran | |||||
| N | N | % | N | % | N | % | N | % | Intervalo | |
| Severos | 158 | 8 | 5,1 | 16 | 10 | – | – | 134 | 85 | 78-90% |
| Moderados | 253 | 2 | 0,8 | 58 | 23 | 0 | 0 | 193 | 76 | 71-81% |
| Leves | 70 | 1 | 1,4 | 23 | 33 | 1 | 1,4 | 45 | 64 | 52-75% |
| Ausentes | 2 | 1 | 50,0 | 97 | 20 | 0 | 0 | 372 | 77 | 73-81% |
| Total | 483 | 12 | 2 | – | – | 1 | 0,3 | |||
| Irritabilidad | Visita 1 | Abandonan | No mejoran | Empeoran | Mejoran | |||||
| N | N | % | N | % | N | % | N | % | Intervalo | |
| Severos | 81 | 7 | 8,6 | 12 | 15 | – | – | 62 | 77 | 66-85% |
| Moderados | 173 | 2 | 1,2 | 47 | 27 | 0 | 0 | 124 | 72 | 64-78% |
| Leves | 181 | 2 | 1,1 | 94 | 52 | 7 | 3,9 | 78 | 43 | 36-51% |
| Ausentes | 48 | 1 | 2,1 | 153 | 35 | 3 | 6 | 264 | 61 | 56-65% |
| Total | 483 | 12 | 2 | – | – | 10 | 2,5 | |||
| Insomnio | Visita 1 | Abandonan | No | mejoran | Empeoran | Mejoran Peor escenario | ||||
| N | N | % | N | % | N | % | N | % | Intervalo | |
| Severos | 82 | 6 | 7,3 | 12 | 15 | 64 | 78 | 68-86% | ||
| Moderados | 163 | 3 | 1,8 | 48 | 29 | 0 | 0,0 | 112 | 69 | 61-76% |
| Leves | 167 | 2 | 1,2 | 80 | 48 | 3 | 1,8 | 82 | 49 | 41-57% |
| Ausentes | 71 | 1 | 1,4 | 140 | 34 | 2 | 3 | 258 | 63 | 58-67% |
| Total | 483 | 12 | 2 | 5 | 1,2 | |||||
| Depresión | Visita 1 | Abandonan | No | mejoran | Empeoran | Mejoran Peor escenario | ||||
| N | N | % | N | % | N | % | N | % | Intervalo | |
| Severos | 40 | 1 | 2,5 | 8 | 20 | 31 | 78 | 62-89% | ||
| Moderados | 86 | 3 | 3,5 | 28 | 33 | 0 | 0,0 | 55 | 64 | 53-74% |
| Leves | 154 | 5 | 3,2 | 66 | 43 | 4 | 2,6 | 79 | 51 | 43-59% |
| Ausentes | 203 | 3 | 1,5 | 102 | 36 | 9 | 4,4 | 165 | 59 | 53-65% |
| Total | 483 | 12 | 2 | 13 | 2,9 | |||||
| Sudor | Visita 1 | Abandonan | No | mejoran | Empeoran | Mejoran Peor escenario | ||||
| N | N | % | N | % | N | % | N | % | Intervalo | |
| Severos | 125 | 7 | 5,6 | 12 | 10 | 106 | 85 | 77-91% | ||
| Moderados | 220 | 2 | 0,9 | 39 | 18 | 0 | 0,0 | 179 | 81 | 75-86% |
| Leves | 118 | 2 | 1,7 | 38 | 32 | 1 | 0,8 | 77 | 65 | 56-74% |
| Ausentes | 20 | 1 | 5,0 | 89 | 19 | 1 | 5,0 | 362 | 78 | 74-82% |
| Total | 483 | 12 | 2 | 2 | 0,6 | |||||
Se realizó un análisis descriptivo comparando los resultados entre la primera y la segunda visitas mediante la prueba de la χ2 para homogeneidad de distribuciones (p < 0,00001); se consideró la falta de eficacia cuando la distribución de la primera y la segunda visitas eran iguales (similares proporciones en cada estado de intensidad). En cada uno de los estratos de gravedad se calculó el porcentaje de mujeres que mejoraban, con un intervalo de confianza (IC) del 95%. Para valorar la seguridad se registraron todos los acontecimientos adversos: 4 mujeres presentaron molestias gástricas, pero ninguna necesitó abandonar el tratamiento.
De las 483 mujeres que fueron incluidas, 12 no acudieron a la segunda visita y se consideraron como mujeres que no mejoraron.
DISCUSIÓNEn la actualidad se dispone de muchos productos para el tratamiento de la clínica climatérica. Sin duda, la opción más conocida y eficaz es la THS. Sin embargo, la terapia con estrógenos, como se ha demostrado recientemente en el estudio WHI13, se relaciona con un aumento en la incidencia de cáncer de mama y muchas mujeres no aceptan el tratamiento con TSH.
Algunas opciones terapéuticas «naturales» se han propuesto como alternativa a la THS. Las isoflavonas, el clavo rojo y la CR son las más empleadas por que se consideran SERM y terapias seguras sin efecto estrogénico. Sin embargo, la evidencia de que éste sea el caso, en el caso de isoflavonas y clavo rojo14, es muy escasa.
Bodinet8 evaluó la influencia de diferentes productos naturales que contenían soja, trébol rojo y CR sobre la proliferación de células cancerosas estrógeno-dependientes (MCF-7) para poder valorar si la utilización de este tipo de productos, en mujeres con riesgo de presentar cáncer de mama dependiente de estrógenos, era apropiada.
Los resultados indicaron que los productos comercializados que contenían soja, trébol rojo y otras combinaciones de productos vegetales inducían un incremento en la proliferación de las células MCF-7 en ausencia de estradiol, lo que sugiere que estos preparados tenían actividad estrógeno-agonista. En cambio, el extracto isopropanólico de CR (Remifemin®) no sólo no estimuló el crecimiento de las células MCF-7, sino que ejerció un efecto inhibitorio de la proliferación celular8.
Otros autores confirman la seguridad y eficacia de CR, y demuestran la ausencia de efecto estrogénico15,16.
Nuestro estudio obtiene resultados de eficacia y seguridad similares a otros estudios realizados con CR y confirma que el extracto isopropanólico estandarizado de CR (Remifemin®) mejora la sintomatología vasomotora y psíquica del síndrome climatérico5; las mujeres con síntomas severos son las más beneficiadas.
La mejoría en los síntomas, o lo que es lo mismo, la mejoría en la calidad de vida de la mujer climatérica, justifica el empleo de CR. Además, el extracto isopropanólico de CR presenta muchos de los beneficios del 17 betaestradiol, como el efecto beneficioso sobre el hueso en la prevención de osteoporosis14.
Rosella et al17 demostraron la eficacia del extracto isopropanólico estandarizado de CR en el alivio de los síntomas climatéricos, en comparación con dosis bajas de estradiol transdérmico (TTSE2). Tanto CR como TTSE2 a dosis bajas redujeron significativamente el número de sofocos por día (p < 0,001) y los síntomas vasomotores (p < 0,001), desde el primer mes de tratamiento. Este efecto positivo se mantuvo durante los 3 meses de observación, sin ninguna diferencia significativa entre ambos tratamientos.
Cuando se comparan los efectos terapéuticos del extracto isopropanólico estandarizado de CR frente a estrógenos conjugados en los síntomas vasomotores, el metabolismo óseo y el endometrio, encontramos que CR tiene una eficacia equivalente a los estrógenos conjugados y superior a placebo en la reducción de los síntomas climatéricos10, pero sin acción estrogénica, y se diferencia de los estrógenos en su seguridad.
Los datos obtenidos de estudios clínicos y de los programas de información de organismos nacionales e internacionales sugieren que los efectos adversos asociados a CR son poco frecuentes, poco severos y reversibles. CR es una alternativa eficaz y segura para la sintomatología vasomotora de la mujer menopáusica.
Aunque en España la CR es relativamente nueva (se comercializa en el mercado español desde el 2002), en el resto de Europa viene utilizándose desde principios de los años cincuenta, y lo que es más importante, en Europa se utiliza bajo diversas y muy variadas presentaciones y categorías: suplementos alimenticios, preparados de herbolario, productos combinados con otras plantas medicinales, etc.
Es importante resaltar el hecho de que los productos que no están registrados como especialidad farmacéutica publicitaria (EFP) no están sujetos a los mismos controles por parte de las autoridades sanitarias, ni obligados a cumplir los mismos estándares de calidad y control de farmacovigilancia que los productos EFP.
Remifemin® es una EFP, registrada como tal en la Agencia Española del Medicamento, y aunque en los ensayos clínicos realizados con este producto no se ha dado ningún caso de daño hepático ni se ha registrado ninguna alteración de las enzimas hepáticas, el Comité de Expertos en Productos Vegetales Medicinales de la EMEA ha presentado en 2006 algunos casos clínicos de pacientes con daño hepático que utilizaban raíz de black cohosh (CR), y alertado tanto a los usuarios de black cohosh como a los profesionales de la salud sobre la necesidad de prestar atención en la aparición de ciertos síntomas que podrían ser indicio de daño hepático.
De los 42 casos informados en todo el mundo, sólo se ha clasificado como causa probable a 2 de ellos, y otros 2 se clasificaron como «causa posible».
Los productos consumidos en estos 4 casos eran complementos alimentarios y no medicamentos registrados (en uno de ellos se desconoce el preparado concreto de black cohosh).
Además se sabe que en dos de estos casos la ingesta de black cohosh fue superior a la recomendada en la posología del producto en 12 y 25 veces, respectivamente.
La relación causal establecida por la Agencia Europea del Medicamento de «causa posible» o «causa probable» se refiere más al tipo de producto utilizado y no indica un riesgo general asociado a la ingesta de productos controlados que contengan CR. Si éste fuera el caso, o si la EMEA tuviera la más mínima duda acerca de una relación beneficio-riesgo positiva, el comité de expertos habría impuesto medidas restrictivas y la retirada del producto.
CONCLUSIONESRemifenin® es una alternativa eficaz y segura para las mujeres que no quieren o no pueden emplear terapia hormonal. Los resultados confirman la eficacia del producto y demuestran que la sudoración fue el síntoma con mejor respuesta. Los aspectos psíquicos presentaron mejoría en el 50% de los casos; los efectos adversos fueron escasos, lo que confirma que Remifemin® es una opción segura y bien tolerada.