Comparar el tiempo medio de expulsión de dos protocolos de misoprostol vaginal en abortos de segundo trimestre.
Material y métodosEstudio retrospectivo de 281 casos entre enero de 2000 y diciembre de 2005 (protocolo A: 800μg/24h) y junio de 2007 y diciembre de 2008 (protocolo B: 400μg/4h). Se recogió como variable principal el tiempo de expulsión.
ResultadosEl tiempo medio de expulsión fue similar para los dos protocolos (19,7h para el A y 17,7h para el B). Tampoco encontramos diferencias significativas en cuanto a las tasas de expulsión a las 12, 24 y 48h. El efecto adverso observado con mayor frecuencia fue la fiebre, siendo más frecuente en el protocolo B. No hubo efectos adversos mayores como rotura uterina o hemorragia severa.
ConclusionesNo existen diferencias significativas entre los dos protocolos en cuánto a tiempo medio de expulsión fetal, aunque sí mayor porcentaje de fiebre en el protocolo B.
To compare the mean induction-expulsion times in two regimens of vaginal misoprostol for second-trimester pregnancy termination.
Material and methodsWe performed a retrospective study of 281 pregnancies between January 2000 and December 2005 (regimen A: 800μg /24h) and between June 2007 and December 2008 (regimen B: 400μg /4h). Induction-expulsion time was taken as the main outcome.
ResultsThe mean expulsion time was similar in both regimens (19.7h for A and 17.7h for B). No significant differences were found in the expulsion rate at 12, 24 and 48h. The most commonly observed adverse effect was fever, which was more frequent in regimen B. No major adverse effects such as uterine rupture or severe hemorrhage were observed.
ConclusionsNo significant differences were found between regimens A and B in the mean fetal expulsion time, although fever was more common in regimen B.
Las técnicas de diagnóstico prenatal han aumentado el número de patologías fetales diagnosticadas que pueden comprometer la vida del recién nacido y que, por tanto, hacen que antes de la semana 24 se pueda optar por una interrupción de la gestación. Además, muchas de las muertes fetales de segundo trimestre requieren tratamiento para conseguir la expulsión fetal y placentaria. En ambos casos, el tratamiento médico se considera el más adecuado aunque no queda exento de complicaciones maternas graves1. En los países en los que la mifepristona (RU-486) no está comercializada, el fármaco que más se usa para esta indicación es el misoprostol2.
El tratamiento quirúrgico mediante dilatación y evacuación en estas situaciones proporciona resultados más rápidos pero se asocia a mayor morbimortalidad materna, como la perforación uterina, las sinequias, la incompetencia cervical o incluso la muerte1,2.
El misoprostol es un análogo sintético de la prostaglandina E1 (PGE1) comercializado con el nombre de Cytotec® y está indicado para la prevención y el tratamiento de la enfermedad ulcerosa péptica. Sin embargo, como acción adicional estimula el miometrio, induciendo contracciones uterinas y es efectivo en la maduración cervical. Es un fármaco estable a temperatura ambiente, económico, fácil de obtener en España y de uso cómodo, y tiene eficacia similar o superior a otras prostaglandinas1–4.
Sabemos que para su uso obstétrico, las dosis de misoprostol son diferentes en función de la edad gestacional y se ha establecido la vía vaginal como la más eficaz y que presenta menores efectos secundarios5,6. Sin embargo, y aunque se han analizado distintos protocolos, la dosis óptima todavía no ha estado definida1,2.
El protocolo usado en nuestro centro hasta mayo de 2007 fue de 800μg cada 24h. Revisando la literatura encontramos estudios que usando protocolos con menor dosis e intervalo conseguían mayores tasas de abortos completos, por lo que diseñamos este estudio con la hipótesis de que la respuesta al misoprostol vaginal sería mejor con dosis de 400μg cada 4h que con 800μg cada 24h, sin que ello comportase un aumento de los efectos adversos.
El objetivo principal de nuestro estudio fue comparar el tiempo medio de expulsión de dos protocolos de misoprostol vaginal en interrupciones legales del embarazo y en abortos de segundo trimestre.
Como objetivos secundarios se valoraron las diferencias entre los dos protocolos, estudiando el porcentaje de expulsiones en 12, 24 y 48h, la tasa de abortos completos, la dosis total de PGE1, los métodos complementarios utilizados y los efectos secundarios debidos al tratamiento.
Material y métodosRealizamos un estudio retrospectivo de 281 casos de finalización de la gestación de segundo trimestre (13-24 semanas) en el Hospital de Sabadell durante el periodo comprendido entre enero de 2000 y diciembre de 2005 para el protocolo A y entre junio de 2007 y diciembre de 2008 para el protocolo B. Se excluyeron las gestaciones gemelares.
El protocolo A consistió en la administración de 800μg de misoprostol (PGE1) por vía vaginal cada 24h (4 comprimidos), mientras que en el protocolo B, se colocaron 400μg por vía vaginal (2 comprimidos) cada 4h. La administración de la medicación se realizó mediante tacto vaginal en la planta de hospitalización.
La variable principal del estudio fue el tiempo de expulsión, calculado en horas, considerándose desde la administración de la primera dosis de misoprostol vaginal hasta la expulsión del feto, independientemente del uso de métodos adicionales.
Como variables secundarias se consideraron la tasa de expulsión en 12, 24 y 48h, los abortos completos, las retenciones placentarias, los métodos complementarios utilizados para la expulsión fetal, la dosis total de PGE1 y los efectos adversos. Se definió como aborto completo aquél en el que se consiguió la expulsión fetal y placentaria mediante misoprostol vaginal y sin ningún tratamiento adicional. En los casos de expulsión fetal y retención placentaria se practicó un legrado uterino. No se estableció ningún protocolo específico en cuanto a qué métodos complementarios utilizar en caso de falta de expulsión ni cómo hacerlo, siendo el criterio del clínico presente en aquel momento el factor decisivo en estos casos. Los métodos complementarios utilizados fueron oxitocina IV, laminarias endocervicales, dinoprostona (endocervical, intraamniótica o intramuscular) y balón endocervical. Como efectos adversos se recogieron los que figuran en la ficha técnica de misoprostol (fiebre, náuseas, vómitos, diarrea e hipotensión), considerando el dolor abdominal una consecuencia del efecto deseado de las prostaglandinas.
Además, se recogieron las siguientes variables descriptivas: edad, paridad, cesárea anterior y semanas de gestación.
Los casos se obtuvieron del registro de anatomía patológica y del registro de ILE de nuestro centro. Los datos se recogieron a partir de una revisión de la historia clínica de las pacientes, siendo posteriormente introducidos en una base de datos (Access 2003).
Para el análisis estadístico de los resultados se utilizó el paquete estadístico SPSS 17.0. Se realizó un análisis descriptivo univariante de las distintas variables mediante tablas de frecuencia absoluta y porcentajes para las variables categóricas. Para las cuantitativas analizamos la media, la desviación típica y los valores mínimo y máximo. La comparación entre variables cuantitativas se realizó con la prueba de la t de Student, mientras que las variables categóricas se analizaron con la prueba de la chi al cuadrado. Se estableció como significación estadística una p<0,05.
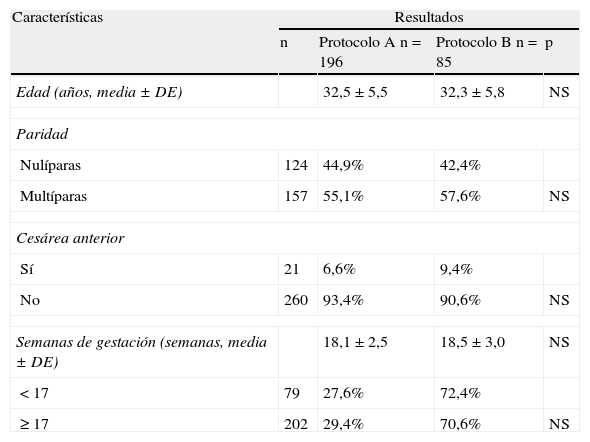
ResultadosDurante los periodos de enero de 2000 a diciembre de 2005 y de junio de 2007 a diciembre de 2008 se realizaron 281 abortos de segundo trimestre en el Hospital de Sabadell (196 en el primer periodo y 85 en el segundo). Las características de las pacientes de ambos grupos se resumen en la tabla 1.
Características de las pacientes y gestaciones (n=281)
| Características | Resultados | |||
| n | Protocolo A n=196 | Protocolo B n=85 | p | |
| Edad (años, media±DE) | 32,5±5,5 | 32,3±5,8 | NS | |
| Paridad | ||||
| Nulíparas | 124 | 44,9% | 42,4% | |
| Multíparas | 157 | 55,1% | 57,6% | NS |
| Cesárea anterior | ||||
| Sí | 21 | 6,6% | 9,4% | |
| No | 260 | 93,4% | 90,6% | NS |
| Semanas de gestación (semanas, media±DE) | 18,1±2,5 | 18,5±3,0 | NS | |
| < 17 | 79 | 27,6% | 72,4% | |
| ≥ 17 | 202 | 29,4% | 70,6% | NS |
La indicación de finalización de la gestación fue por muerte fetal de segundo trimestre en 88 casos (69 del protocolo A y 19 del B) e ILE en 196 casos (127 del protocolo A y 66 del B).
El tiempo medio de expulsión del feto fue de 19,7±21,7h (intervalo 1-168) para el protocolo A y 17,7±19,8h (intervalo 2-147) para el B. En el subgrupo de pacientes nulíparas, el tiempo medio de expulsión fue de 24,4±26,6h (25,4±26,1h en el protocolo A y 22,0±27,9h en el B), mientras que en las multíparas fue de 14,9±14,3h (15,0±16,1h en el protocolo A y 14,6±9,5h en el B). Para el subgrupo de muertes fetales se obtuvieron unos tiempos medios de expulsión de 13,9±20,0h (14,9±22,2h en el protocolo A y 10,2±6,5h en el B) y para el subgrupo de interrupciones legales del embarazo de 21,5±21,3h (22,3±21,1h en el protocolo A y 19,9±21,7h en el B).
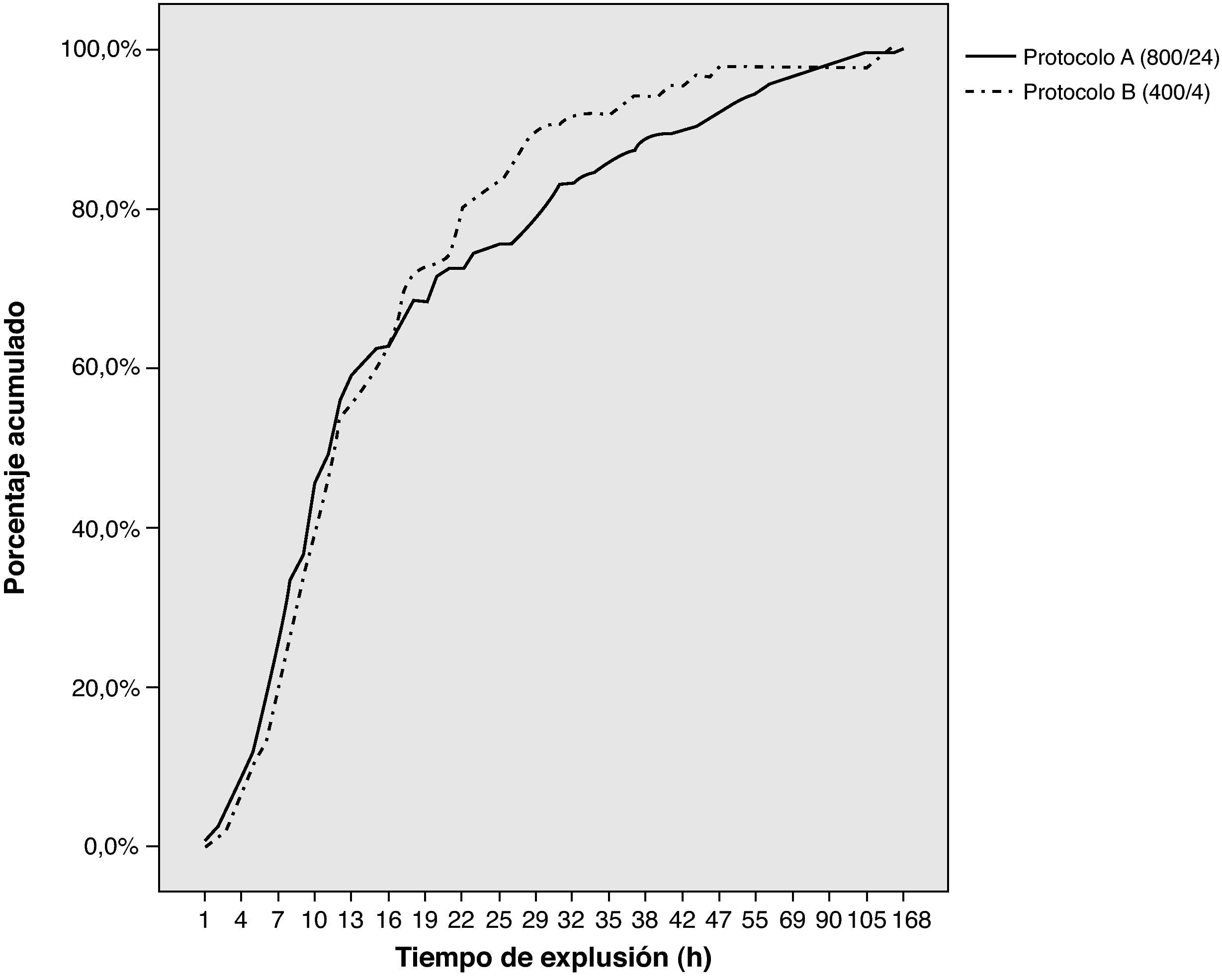
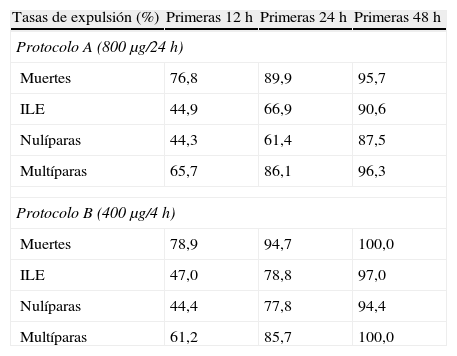
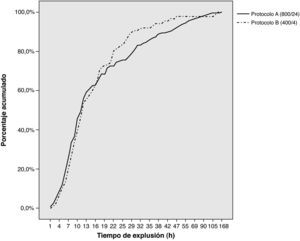
En la figura 1 se pueden observar las tasas acumulativas de expulsión fetal para ambos protocolos, siendo del 56,1% para el protocolo A y del 54,1% para el protocolo B antes de las 12h, del 75% para el protocolo A y del 82,4% para el protocolo B antes de las 24h y, finalmente, del 92,3% para el protocolo A y del 97,6% para el protocolo B antes de las 48h. En la tabla 2 se comparan las tasas de expulsión a las 12, 24 y 48h para los subgrupos óbitos fetales de segundo trimestre e interrupciones legales del embarazo, así como para los subgrupos nulíparas y multíparas.
Tasa de expulsión a las 12, 24 y 48h en los distintos subgrupos
| Tasas de expulsión (%) | Primeras 12 h | Primeras 24 h | Primeras 48 h |
| Protocolo A (800μg/24 h) | |||
| Muertes | 76,8 | 89,9 | 95,7 |
| ILE | 44,9 | 66,9 | 90,6 |
| Nulíparas | 44,3 | 61,4 | 87,5 |
| Multíparas | 65,7 | 86,1 | 96,3 |
| Protocolo B (400μg/4 h) | |||
| Muertes | 78,9 | 94,7 | 100,0 |
| ILE | 47,0 | 78,8 | 97,0 |
| Nulíparas | 44,4 | 77,8 | 94,4 |
| Multíparas | 61,2 | 85,7 | 100,0 |
La dosis total media necesaria para la expulsión del feto fue 1.100μg en el protocolo A y 1.515μg en el B. El número medio de dosis administradas en cada protocolo fue 1,38±0,80 en el A y 3,71±2,79 en el B.
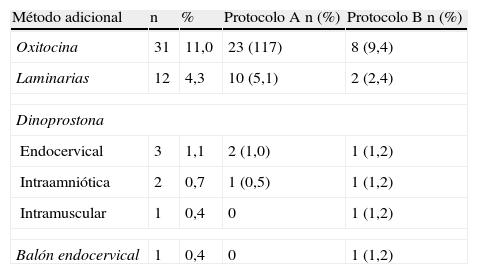
El porcentaje de abortos completos fue del 64,8% para el protocolo A y del 69,4% para el B. En las gestaciones de menos de 17 semanas, el porcentaje abortos completos fue del 55,7%, mientras que en el subgrupo de gestaciones de 17 semanas o más, fue del 70,3%. Se diagnosticaron un 24,5% de retenciones placentarias usando el protocolo A y un 18,8% usando el B, que se solucionaron mediante legrado uterino en la mayoría de los casos (57) o alumbramiento manual bajo sedación (7 casos). En la tabla 3 se muestran los casos que requirieron algún tipo de tratamiento adicional.
Métodos adicionales usados para la expulsión fetal
| Método adicional | n | % | Protocolo A n (%) | Protocolo B n (%) |
| Oxitocina | 31 | 11,0 | 23 (117) | 8 (9,4) |
| Laminarias | 12 | 4,3 | 10 (5,1) | 2 (2,4) |
| Dinoprostona | ||||
| Endocervical | 3 | 1,1 | 2 (1,0) | 1 (1,2) |
| Intraamniótica | 2 | 0,7 | 1 (0,5) | 1 (1,2) |
| Intramuscular | 1 | 0,4 | 0 | 1 (1,2) |
| Balón endocervical | 1 | 0,4 | 0 | 1 (1,2) |
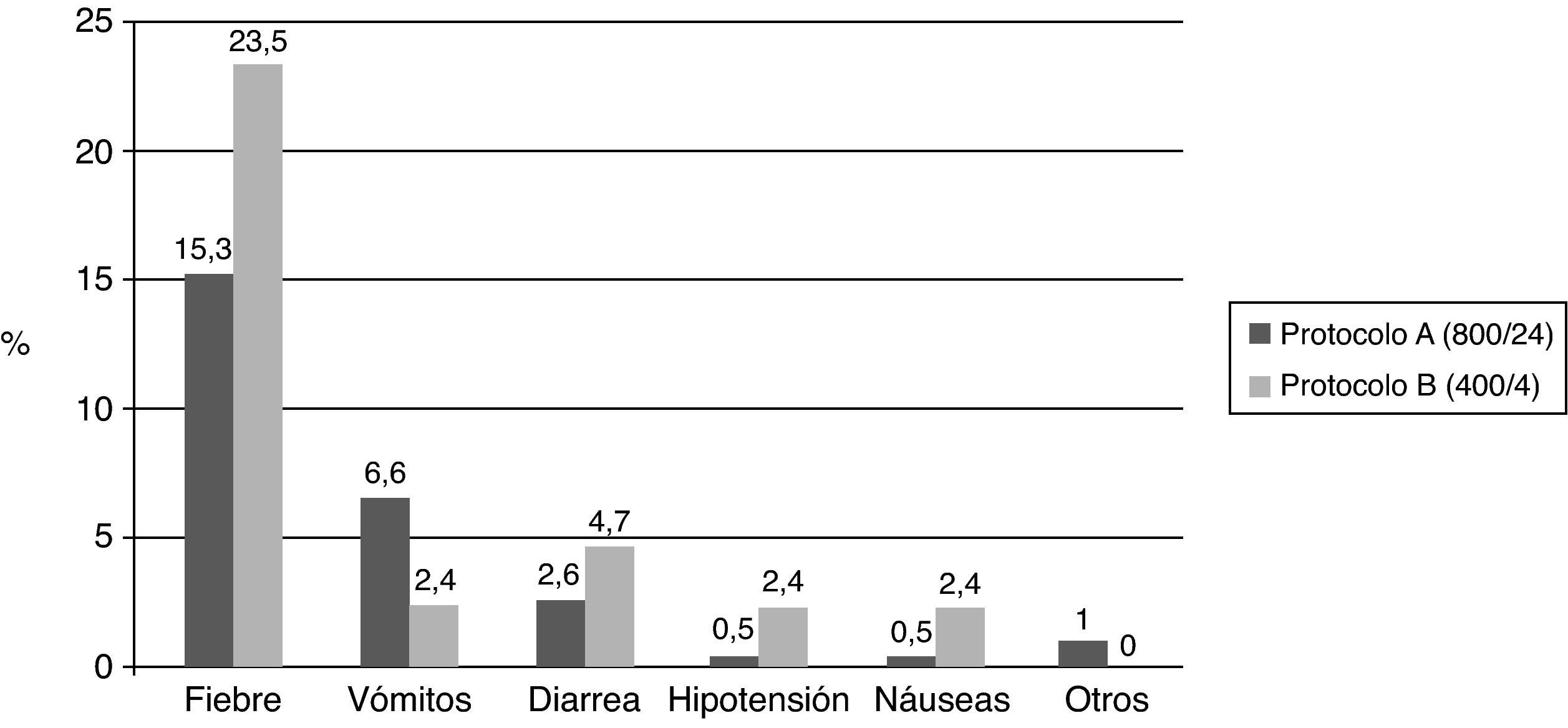
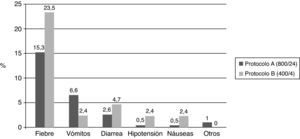
El efecto adverso observado con mayor frecuencia fue la fiebre (50 casos), que representa el 15,3% en el protocolo A y el 23,5% en el B. El resto de efectos adversos observados se describen en la figura 2 en función del protocolo usado. No hubo efectos adversos graves como rotura uterina o hemorragia severa. Una paciente fue diagnosticada de edema agudo de pulmón que requirió ingreso en la unidad de cuidados intensivos para tratamiento, aunque ya presentaba clínica de disnea y ortopnea antes del ingreso.
La mayoría de las pacientes refirieron algún grado de dolor abdominal, precisando analgesia el 80%. Los fármacos administrados fueron dolantina IM, metamizol IV, paracetamol IV y diclofenaco IM. En 9 pacientes se realizó analgesia peridural.
DiscusiónEn el presente estudio, el tiempo medio de expulsión del feto fue similar para los dos grupos (19,7±21,7h para el protocolo A y 17,7±19,8h para el B). Al comparar las tasas de expulsión a las 12, 24 y 48h, tampoco se encontraron diferencias estadísticamente significativas a favor de ningún protocolo. La dosis total media necesaria para la expulsión fetal fue mayor en el protocolo B 1515μg vs. 1.100μg en el A (p<0,05), con un número de dosis superior para el protocolo B y, por consiguiente, mayor número de tactos vaginales en este grupo.
El método complementario usado con más frecuencia fue la oxitocina IV en 23 casos del protocolo A (11,7%) y 8 del B (9,4%).
En el protocolo B observamos que las pacientes a las que se les había administrado mayor dosis de misoprostol presentaban más efectos adversos (p<0,05), sin encontrar estas diferencias cuando se usó el protocolo A. El efecto adverso observado con mayor frecuencia fue la fiebre, siendo más frecuente en el protocolo B (23,5%), probablemente relacionado con el mayor número de dosis total de misoprostol (protocolo A 15,3%), aunque estas diferencias no fueron significativas. Los porcentajes de fiebre en los protocolos A y B (15,3% y 23,5%, respectivamente), vómitos (6,6% y 2,4%) y diarrea (2,6% y 4,7%) obtenidos en nuestro estudio son similares a los descritos en los estudios revisados. Sin embargo, al tratarse de un estudio retrospectivo, en nuestro caso puede existir un infradiagnóstico de los efectos secundarios, dado que los datos se recogieron del curso clínico de las historias de las pacientes. No sería éste el caso de la fiebre, pues la temperatura se obtuvo de las gráficas de constantes.
Al comparar los subgrupos en función de la paridad se observaron tiempos medios de expulsión fetal significativamente mayores para las nulíparas respecto a las multíparas (M), así como tasas de expulsión a las 12, 24 y 48h superiores para el subgrupo M. Estas diferencias no fueron significativas para la pauta B, probablemente debido al número limitado de casos.
Analizando los subgrupos en función de la indicación del proceso (óbitos fetales [O] e interrupciones legales del embarazo), encontramos tiempos medios de expulsión significativamente menores para el subgrupo O y tasas de expulsión fetal a las 12 y 24h superiores para este subgrupo.
La respuesta al misoprostol es muy variable, con un tiempo de expulsión de 1 a 168h en nuestra serie. La paridad y la indicación de la finalización de la gestación son variables importantes, pues como hemos podido confirmar en nuestro estudio, las multíparas y los casos en que finalización fue por aborto tuvieron menor tiempo medio de expulsión que las nulíparas y las interrupciones por malformación fetal7,8. Además, otros estudios muestran que la edad gestacional constituye otra variable importante, con mayor probabilidad de expulsión completa a menor edad gestacional7. En nuestro estudio hemos encontrado resultados contrarios con un porcentaje de abortos completos superior en gestaciones de 17 semanas o más (70,3%) respecto a las gestaciones de menos de 17 semanas (55,7%), siendo estas diferencias significativas. El estudio de Lo et al9 muestra los mismos resultados y los atribuye a la sensibilidad uterina a los agentes uterotónicos, que aumenta a mayor edad gestacional.
En algún estudio10 se recomienda una dilatación y evacuación sistemática después de la expulsión fetal para asegurar que la cavidad uterina esté vacía y evitar así hemorragias graves. Sin embargo, en la mayoría, se aconseja realizarlo sólo cuando existe una evidencia clínica de aborto incompleto o una hemorragia posterior al aborto2. Haciéndolo de esta forma, en nuestra serie se realizaron un 20,3% de legrados uterinos por retención placentaria sin registrar ningún caso de hemorragia grave.
Algunas de las limitaciones de nuestro estudio fueron el número limitado de casos, la obtención de datos del curso clínico de forma retrospectiva, así como la falta de un protocolo de actuación a partir del segundo día de tratamiento si no se consigue la expulsión fetal con misoprostol.
La comparación de los múltiples estudios publicados es difícil de realizar, ya que difieren en varios aspectos (semanas de gestación, dosis y vías de administración, uso de métodos adicionales, indicación de la finalización, etc.)11–24.
Revisando los estudios que analizan protocolos con vía de administración vaginal, vemos que el tiempo medio de expulsión varía entre 10,7 y 22,5h, sin observar ninguna relación con la dosis ni los intervalos. En estos casos, las tasas de expulsión fetal en las primeras 24h varían entre el 54% y 100%, siendo más elevadas en los estudios que utilizan regímenes de administración en intervalos de 3-6h (la mayoría superiores al 90%). Sin embargo, cuando los intervalos se alargan (más de 6h) las tasas disminuyen hasta 54-67%10,11,13–21,23,24.
Algunos estudios analizan protocolos combinados vaginal (vag) y oral (vo), consiguiendo también buenas tasas de expulsión en las primeras 24h, como Dilbaz et al7 (200μg vag + 100μg/2h vo) del 98% y Langer et al8 (800μg vag + 400μg/3h vo) del 91%. Otros comparan protocolos con distintas vías de administración (vag vs vo o sublingual) concluyendo que no existen diferencias a favor de ninguna vía ni tampoco en cuanto a la incidencia de efectos adversos11,16,21,23,24; sin embargo, estos estudios tienen escasa validez.
En un metaanálisis publicado en abril del 20091 donde se incluyen 14 estudios que comparan distintos protocolos de tratamiento, los autores concluyen que la vía vaginal es menos efectiva que la oral para la expulsión antes de las 24h, pero no para las 48h; sin embargo, la vía oral se asocia con más efectos adversos.
El hecho de no haber hallado mejores resultados en uno de los dos protocolos estudiados nos sugiere que tal vez modificando el intervalo o la vía de administración de la medicación podríamos conseguir mejores resultados y mejorar el confort de nuestras pacientes. En esta línea, en un futuro cercano, dispondremos de mifepristona que incorporaremos a nuestro protocolo.
Pese al gran número de estudios publicados al respecto, son necesarios más estudios controlados para determinar la dosis y la pauta de misoprostol con mejores resultados para la finalización de la gestación en el segundo trimestre, aunque es bien sabido que los protocolos que asocian mifepristona y misoprostol muestran múltiples ventajas respecto a los que usan misoprostol solo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.