La hiperhidrosis afecta a aproximadamente el 5% de la población. Se puede clasificar dependiendo de su etiología en hiperhidrosis primaria (HPr), la más frecuente (>90%), o secundaria. La HPr está caracterizada por excesiva sudación debido a una excesiva actividad neurogénica sobre las glándulas ecrinas normales. La hiperhidrosis focal es la forma más frecuente de HPr y afecta la zona axilar, palmoplantar, inguinal, craneofacial o el pliegue inframamario.
La hiperhidrosis secundaria puede ser debida a enfermedades endocrinas (lo más frecuente) como la diabetes mellitus, el hipertiroidismo y el hiperpituitarismo, seguida de alteraciones neurológicas o neurodegenerativas1. Otras causas menos frecuentes incluyen diversos fármacos, tóxicos o neoplasias1. Es importante sospecharla en casos de inicio tardío (>25 años de edad), compromiso generalizado, distribución asimétrica o unilateral, afectación nocturna (durante el sueño) o ante la presencia de síntomas sistémicos como fiebre y la bajada de peso, entre otros (tabla 1)2.
Hiperhidrosis secundaria
| Frecuencia | Aproximadamente un 10% de las hiperhidrosis |
|---|---|
| Historia familiar | No |
| Edad de debut | Variable (es sospechoso un inicio después de los 25 años de edad) |
| Distribución corporal | Puede ser unilateral y asimétrica.Usualmente es generalizada |
| Relación con el ciclo sueño/vigilia | Puede desencadenarse tanto en la vigilia, como en el sueño |
| Presencia de síntomas sistémicos | Pueden presentar disminución de peso, fiebre, adenopatías palpables, diarrea o flushing, dependiendo de la causa subyacente |
| Causas | Trastornos endocrinosDiabetes mellitus, hipertiroidismo, hiperpituitarismo, diabetes insípida, feocromocitoma, síndrome carcinoideAlteraciones neurológicasEnfermedad de Parkinson, accidente vascular encefálicoLesiones neurológicas focales o neuropatía periféricaInfeccionesBacterianas o víricas agudas/crónicas, tuberculosis, VIH, brucelosis, endocarditis, malariaEnfermedades cardiorrespiratoriasInsuficiencia cardiaca, insuficiencia respiratoriaDrogasAlcohol, cocaína, heroínaFármacosAntidepresivos, ansiolíticos, antipsicóticos, AINE, triptanos, ciprofloxacino, aciclovir, insulina e hipoglicemiantes oralesNeoplasiasLinfoma, trastornos mieloproliferativos |
AINE: antiinflamatorios no esteroideos; VIH: virus de la inmunodeficiencia humana.
La HPr produce un gran detrimento en la calidad de vida, alterando el ámbito social, laboral, de estudios y la actividad física3–5, y puede producir altas tasas de ansiedad y depresión4. El manejo de la HPr puede ser difícil. Existen diversas alternativas farmacológicas, entre las que destacan los anticolinérgicos tópicos y orales, y la toxina botulínica; así como procedimientos invasivos o mínimamente invasivos como la iontoforesis, la radiofrecuencia, la termólisis por microondas, los ultrasonidos o la cirugía (simpatectomía). Muchas de estas terapias están limitadas por su disponibilidad y alto coste. Además, resulta fundamental evaluar cuidadosamente los riesgos y beneficios antes de indicar un tratamiento determinado, especialmente en los niños. En este artículo revisaremos los tratamientos farmacológicos disponibles para la HPr en los adultos y en la población pediátrica.
Evaluación de la hiperhidrosisExisten diversos métodos objetivos y subjetivos para evaluar el impacto de la HPr. Entre los primeros, se destaca la medición de la producción de sudor por gravimetría. Dentro de los subjetivos, la escala más utilizada es la escala de gravedad de la hiperhidrosis (Hyperhidrosis Disease Severity Scale) (HDSS) (tabla 2)5. En esta se pregunta por la interferencia de la sudación en la vida diaria. La puntuación oscila entre 1 y 4 (máxima afectación). Se considera una hiperhidrosis moderada o grave con una puntuación ≥3. La reducción de un punto se correlacionaría con una disminución de la sudación de un 50% y la reducción de 2 puntos, de un 80%. Habitualmente se considera que una reducción de 2 puntos corresponde a una respuesta clínica excelente y que una disminución de un punto equivale a una respuesta parcial6. Para evaluar el impacto de la HPr en la calidad de vida se suele utilizar el índice de calidad de vida en dermatología (Dermatology life Quality Index) (DLQI)5. El índice de calidad de vida en hiperhidrosis (Hyperhidrosis Quality of Life Index[HidroQoL]) es otro cuestionario disponible.
Escala de gravedad de la hiperhidrosis (Hyperhidrosis Disease Severity Scale)
| ¿Cómo calificaría la intensidad de su hiperhidrosis? | |
|---|---|
| Puntuación | Respuesta |
| 1 | Mi sudación nunca es perceptible y nunca interfiere con mis actividades diarias |
| 2 | Mi sudación es tolerable, pero en ocasiones interfiere con mis actividades diarias |
| 3 | Mi sudación apenas es tolerable y con frecuencia interfiere con mis actividades diarias |
| 4 | Mi sudación es intolerable y siempre interfiere con mis actividades diarias |
La HPr en los adultos se inicia frecuentemente entre los 14 y 25 años de edad2. Las áreas corporales más frecuentemente afectas son las axilas (50%), las plantas (30%), las palmas (24%) y la zona craneofacial (10%), y es frecuente encontrar varias zonas involucradas en un mismo individuo2. Los pacientes con hiperhidrosis palmar (HP) pueden ser los más afectados en cuanto a calidad de vida7. En los ancianos, la HPr puede ser poco prevalente2; sin embargo, en nuestra experiencia, no es infrecuente que consulten por HPr de largo tiempo de evolución.
TratamientoExisten una serie de recomendaciones generales que pueden ayudar a los pacientes como: evitar la ropa ajustada, prendas sintéticas y calzado oclusivo, usar talco secante, utilizar una primera capa de ropa para disimular el sudor, evitar los alimentos condimentados y el alcohol, y ambientes o situaciones que generen respuestas emocionales que agraven la enfermedad; en la hiperhidrosis plantar (HPL), cambiar frecuentemente los calcetines y los zapatos, y usar plantillas absorbentes.
Terapia tópicaAntitranspirantes tópicosLos antitranspirantes contienen diversos metales, más frecuentemente sales de aluminio en concentraciones variables (6 a 30%). Ejercen su acción al obstruir la luz de las glándulas sudoríparas ecrinas. Múltiples ensayos clínicos (EC)8–10 y estudios prospectivos11–14 realizados en adultos, han demostrado su utilidad en la hiperhidrosis axilar (HA), así como en HP13–16 e HPL17. Sin embargo, tienden a ser efectivos solo en las formas leves y pueden ocasionar irritación local y miliaria. Es importante aplicarlos sobre la piel seca (generalmente se recomiendan antes de dormir) y mantener 8 horas antes de lavar la zona. Se aplican a diario las primeras semanas hasta observar una disminución de la sudación y luego se reducen a una o 2 veces por semana.
Anticolinérgicos tópicosGlicopirronio tópicoEl glicopirronio tópico está aprobado por la Food and Drug Administration (FDA) y por la European Medicines Agency (EMA) para el tratamiento de la HA en los adultos. Múltiples EC aleatorizados (ECA) avalan su efectividad y seguridad en el manejo de la HPr (tabla 3). El estudio más amplio y con seguimiento más prolongado corresponde a un recientemente publicado ECA fase-3b que incluyó a 518 pacientes con HA. Se evaluó la efectividad y seguridad a las 72 semanas del bromuro de glicopirronio 1%, demostrándose una disminución significativa del HDSS y de la sudación medida por gravimetría; además de una reducción promedio de 10 puntos del DLQI en la semana 72. Se reportaron EA mayoritariamente leves como xerostomía, y el tratamiento debió suspenderse en 14 individuos (2,7%)18. Previamente se habían reportado resultados similares en 2 ECA: uno fase-3a (n = 171)19 y otro fase-1b (n = 30)20. Este agente también ha mostrado ser efectivo en la hiperhidrosis facial (HF), según los resultados de 2 ECA con 39 y 25 pacientes, respectivamente21,22. De hecho, un ECA reciente (n = 24) reveló que tanto el glicopirrolato 2% tópico como las inyecciones de toxina botulínica (TB) produjeron resultados similares en los pacientes con HF (respuesta completa en el 75% de los casos)23 (tabla 4).
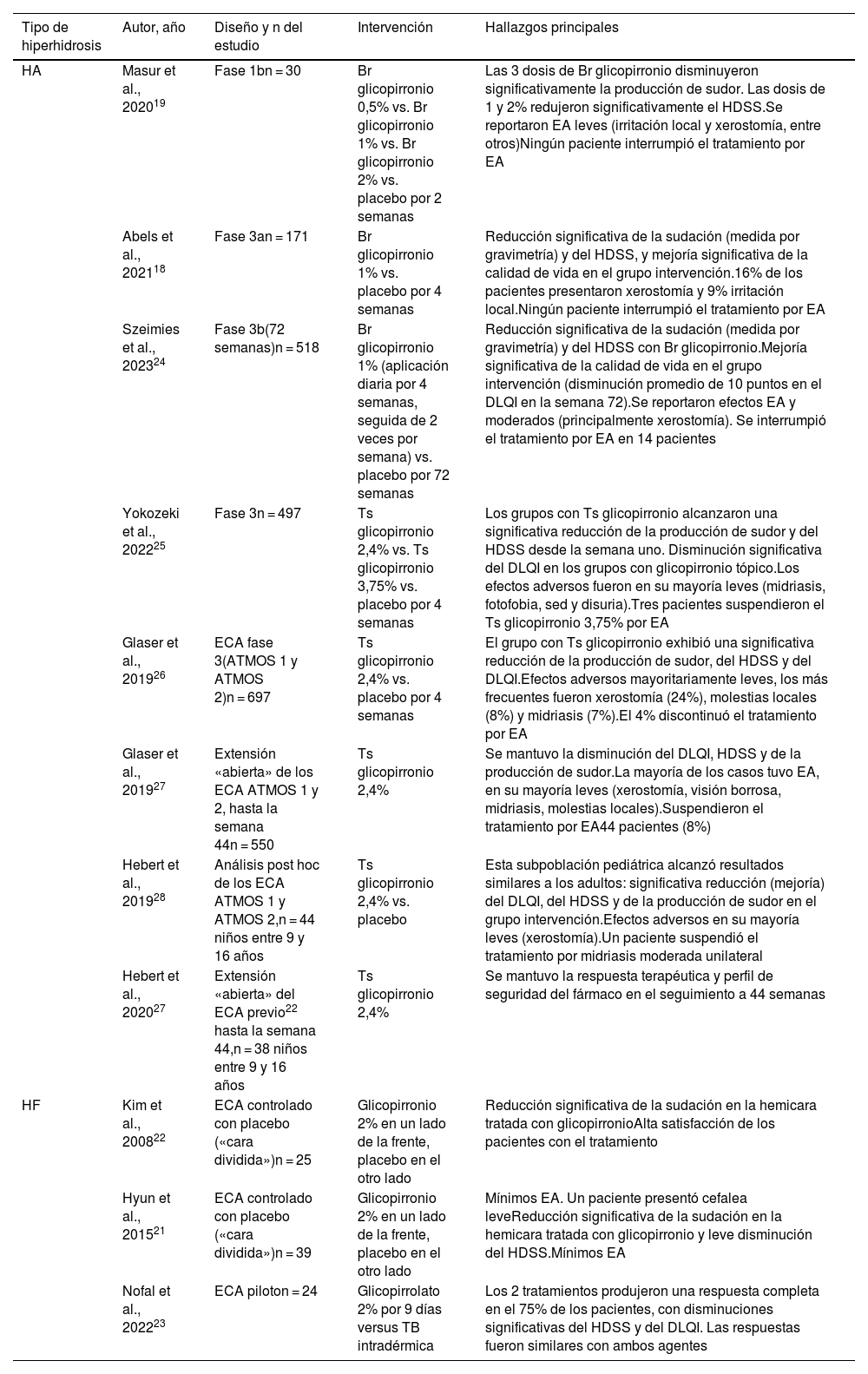
Ensayos clínicos sobre la efectividad del glicopirronio tópico en la hiperhidrosis primaria
| Tipo de hiperhidrosis | Autor, año | Diseño y n del estudio | Intervención | Hallazgos principales |
|---|---|---|---|---|
| HA | Masur et al., 202019 | Fase 1bn = 30 | Br glicopirronio 0,5% vs. Br glicopirronio 1% vs. Br glicopirronio 2% vs. placebo por 2 semanas | Las 3 dosis de Br glicopirronio disminuyeron significativamente la producción de sudor. Las dosis de 1 y 2% redujeron significativamente el HDSS.Se reportaron EA leves (irritación local y xerostomía, entre otros)Ningún paciente interrumpió el tratamiento por EA |
| Abels et al., 202118 | Fase 3an = 171 | Br glicopirronio 1% vs. placebo por 4 semanas | Reducción significativa de la sudación (medida por gravimetría) y del HDSS, y mejoría significativa de la calidad de vida en el grupo intervención.16% de los pacientes presentaron xerostomía y 9% irritación local.Ningún paciente interrumpió el tratamiento por EA | |
| Szeimies et al., 202324 | Fase 3b(72 semanas)n = 518 | Br glicopirronio 1% (aplicación diaria por 4 semanas, seguida de 2 veces por semana) vs. placebo por 72 semanas | Reducción significativa de la sudación (medida por gravimetría) y del HDSS con Br glicopirronio.Mejoría significativa de la calidad de vida en el grupo intervención (disminución promedio de 10 puntos en el DLQI en la semana 72).Se reportaron efectos EA y moderados (principalmente xerostomía). Se interrumpió el tratamiento por EA en 14 pacientes | |
| Yokozeki et al., 202225 | Fase 3n = 497 | Ts glicopirronio 2,4% vs. Ts glicopirronio 3,75% vs. placebo por 4 semanas | Los grupos con Ts glicopirronio alcanzaron una significativa reducción de la producción de sudor y del HDSS desde la semana uno. Disminución significativa del DLQI en los grupos con glicopirronio tópico.Los efectos adversos fueron en su mayoría leves (midriasis, fotofobia, sed y disuria).Tres pacientes suspendieron el Ts glicopirronio 3,75% por EA | |
| Glaser et al., 201926 | ECA fase 3(ATMOS 1 y ATMOS 2)n = 697 | Ts glicopirronio 2,4% vs. placebo por 4 semanas | El grupo con Ts glicopirronio exhibió una significativa reducción de la producción de sudor, del HDSS y del DLQI.Efectos adversos mayoritariamente leves, los más frecuentes fueron xerostomía (24%), molestias locales (8%) y midriasis (7%).El 4% discontinuó el tratamiento por EA | |
| Glaser et al., 201927 | Extensión «abierta» de los ECA ATMOS 1 y 2, hasta la semana 44n = 550 | Ts glicopirronio 2,4% | Se mantuvo la disminución del DLQI, HDSS y de la producción de sudor.La mayoría de los casos tuvo EA, en su mayoría leves (xerostomía, visión borrosa, midriasis, molestias locales).Suspendieron el tratamiento por EA44 pacientes (8%) | |
| Hebert et al., 201928 | Análisis post hoc de los ECA ATMOS 1 y ATMOS 2,n = 44 niños entre 9 y 16 años | Ts glicopirronio 2,4% vs. placebo | Esta subpoblación pediátrica alcanzó resultados similares a los adultos: significativa reducción (mejoría) del DLQI, del HDSS y de la producción de sudor en el grupo intervención.Efectos adversos en su mayoría leves (xerostomía).Un paciente suspendió el tratamiento por midriasis moderada unilateral | |
| Hebert et al., 202027 | Extensión «abierta» del ECA previo22 hasta la semana 44,n = 38 niños entre 9 y 16 años | Ts glicopirronio 2,4% | Se mantuvo la respuesta terapéutica y perfil de seguridad del fármaco en el seguimiento a 44 semanas | |
| HF | Kim et al., 200822 | ECA controlado con placebo («cara dividida»)n = 25 | Glicopirronio 2% en un lado de la frente, placebo en el otro lado | Reducción significativa de la sudación en la hemicara tratada con glicopirronioAlta satisfacción de los pacientes con el tratamiento |
| Hyun et al., 201521 | ECA controlado con placebo («cara dividida»)n = 39 | Glicopirronio 2% en un lado de la frente, placebo en el otro lado | Mínimos EA. Un paciente presentó cefalea leveReducción significativa de la sudación en la hemicara tratada con glicopirronio y leve disminución del HDSS.Mínimos EA | |
| Nofal et al., 202223 | ECA piloton = 24 | Glicopirrolato 2% por 9 días versus TB intradérmica | Los 2 tratamientos produjeron una respuesta completa en el 75% de los pacientes, con disminuciones significativas del HDSS y del DLQI. Las respuestas fueron similares con ambos agentes |
Br: bromuro; DLQI: Dermatology Life Quality Index; EA: efectos adversos; ECA: ensayo clínico aleatorizado; HA: hiperhidrosis axilar; HDSS: Hyperhidrosis Disease Severity Scale; HF: hiperhidrosis facial; HP: hiperhidrosis palmar; TB: toxina botulínica; Ts: tosilato.
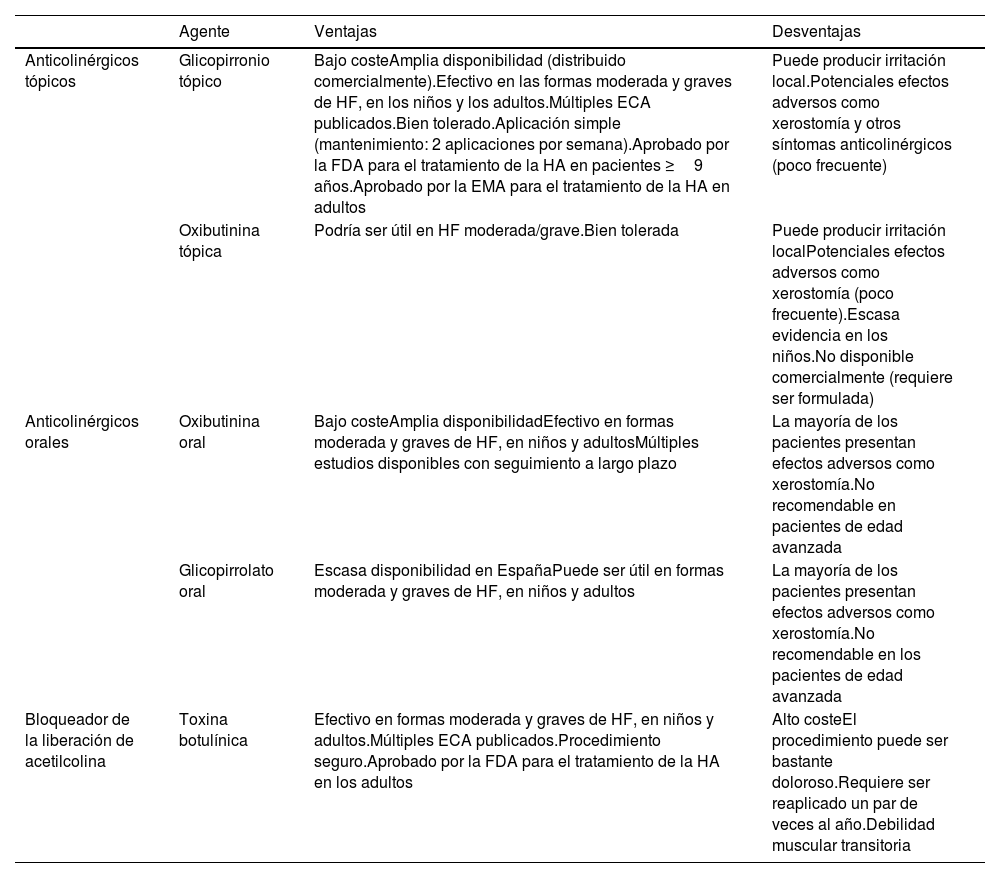
Terapia farmacológica de la hiperhidrosis primaria
| Agente | Ventajas | Desventajas | |
|---|---|---|---|
| Anticolinérgicos tópicos | Glicopirronio tópico | Bajo costeAmplia disponibilidad (distribuido comercialmente).Efectivo en las formas moderada y graves de HF, en los niños y los adultos.Múltiples ECA publicados.Bien tolerado.Aplicación simple (mantenimiento: 2 aplicaciones por semana).Aprobado por la FDA para el tratamiento de la HA en pacientes ≥9 años.Aprobado por la EMA para el tratamiento de la HA en adultos | Puede producir irritación local.Potenciales efectos adversos como xerostomía y otros síntomas anticolinérgicos (poco frecuente) |
| Oxibutinina tópica | Podría ser útil en HF moderada/grave.Bien tolerada | Puede producir irritación localPotenciales efectos adversos como xerostomía (poco frecuente).Escasa evidencia en los niños.No disponible comercialmente (requiere ser formulada) | |
| Anticolinérgicos orales | Oxibutinina oral | Bajo costeAmplia disponibilidadEfectivo en formas moderada y graves de HF, en niños y adultosMúltiples estudios disponibles con seguimiento a largo plazo | La mayoría de los pacientes presentan efectos adversos como xerostomía.No recomendable en pacientes de edad avanzada |
| Glicopirrolato oral | Escasa disponibilidad en EspañaPuede ser útil en formas moderada y graves de HF, en niños y adultos | La mayoría de los pacientes presentan efectos adversos como xerostomía.No recomendable en los pacientes de edad avanzada | |
| Bloqueador de la liberación de acetilcolina | Toxina botulínica | Efectivo en formas moderada y graves de HF, en niños y adultos.Múltiples ECA publicados.Procedimiento seguro.Aprobado por la FDA para el tratamiento de la HA en los adultos | Alto costeEl procedimiento puede ser bastante doloroso.Requiere ser reaplicado un par de veces al año.Debilidad muscular transitoria |
HF: hiperhidrosis focal; HA, hiperhidrosis axilar; ECA, ensayos clínicos aleatorizados; FDA, Food and Drug Administration; EMA, European Medicines Agency.
Un reciente ECA realizado en Japón, que incluyó 497 pacientes con HA, reveló que tanto el tosilato de glicopirronio al 2,4% como al 3,75% indujeron una mejoría clínica significativa, con disminución del HDSS y de la sudación, con un excelente perfil de seguridad24. Previamente, 2 ECA con 697 pacientes en total habían alcanzado resultados similares con tosilato de glicopirronio 2,4%5,29. La respuesta favorable se mantuvo durante la fase de extensión de estos estudios por 44 semanas26.
En cuanto a la HP, un estudio prospectivo (n = 120) mostró que el tosilato de glicopirronio a diversas concentraciones podría ser útil30. El glicopirronio tópico también podría ser una alternativa a considerar en el manejo de la bromohidrosis axilar, según los resultados de un estudio prospectivo con 19 individuos31.
Oxibutinina tópicaAl menos 3 ECA han evaluado la utilidad de diversas formulaciones de oxibutinina tópica: un ECA fase 3 (n = 244) mostró que una loción de oxibutinina al 20% disminuyó significativamente el sudor y el DLQI en pacientes con HP. No se reportaron EA graves32. Resultados similares se observaron en otro ECA con 61 pacientes con HA, HP o HPL al utilizar oxibutinina tópica 10%33, y en un ECA (n = 30) con oxibutinina en gel 1% versus oxibutinina en nanoemulgel 1%34.
Terapia sistémicaSe han utilizado diversos psicofármacos como el clonazepam, paroxetina, topiramato y quetiapina, y antihipertensivos como el propanolol, la clonidina y diltiazem, pero la evidencia es limitada35. Los anticolinérgicos son el grupo farmacológico más ampliamente utilizado.
Anticolinérgicos sistémicosOxibutininaLa oxibutinina está indicada en los adultos para el manejo de la vejiga hiperactiva e incontinencia urinaria, y para reducir la frecuencia miccional. Una reciente revisión sistemática y metaanálisis que incluyó 6 ECA36-37 con 239 pacientes en total con HPr en diversas áreas corporales, mostró que la oxibutinina oral entre 2,5 y 10 mg/día redujo significativamente el HDSS y el DLQI38. Resultados similares se reportaron en 2 revisiones sistemáticas previas: una de ellas incluyó 16 estudios de diseño experimental u observacional, y reveló que la oxibutinina oral produjo una mejoría de la sintomatología y de la calidad de vida en >75% de los pacientes39; en la otra revisión sistemática se evaluó el uso de oxibutinina en HP, incluyéndose 2 estudios prospectivos con un total de 750 pacientes, observándose buenas repuestas en la mayoría de casos40. La oxibutinina fue bien tolerada en la mayoría de estudios, pero con una alta tasa de xerostomía, y con un mayor riesgo de presentar dificultad para orinar, visión borrosa, astenia o mareos38.
En un amplio estudio retrospectivo con seguimiento a largo plazo, que incluyó a 1.658 individuos con HA, HP, HPL o HF en tratamiento con oxibutinina oral, se reportó que aproximadamente el 70% de los pacientes alcanzaron una mejoría clínica subjetiva moderada u óptima, mejoría de la calidad de vida y reducción del HDSS7. La oxibutinina también se ha utilizado satisfactoriamente en forma transdérmica (en parches de 36 mg/semana) en 2 pequeños estudios prospectivos41,42.
Glicopirrolato oralUn estudio prospectivo con 58 individuos con HPr no respondedores a oxibutinina oral, reportó que el glicopirrolato oral (2-6 mg/día) redujo significativamente el HDSS en >50% de los casos. Sin embargo, suspendieron el tratamiento 27 pacientes43. En 2 estudios retrospectivos previos44,45 (83 pacientes en total) se observó una reducción significativa de la sudación en el 67% de los individuos.
Metantelina oralUn ECA con 337 individuos con HA e HP describió que el uso de metantelina 150 mg/día disminuyó significativamente la producción de sudor, el HDSS y el DLQI. Se reportaron EA transitorios graves en 21 casos46.
Terapia intralesionalToxina botulínicaLa toxina botulínica (TB) A (TB-A) está aprobada por la FDA para el manejo de la HA en los adultos. Una reciente revisión sistemática que incluyó 6 ECA con un total de 663 pacientes con HA, reportó que la TB-A redujo significativamente el HDSS, y mejoró la calidad de vida47. Así mismo, múltiples estudios han demostrado que la TB-A reduce significativamente la sudación en HA, HP, HPL y HF, con una duración del efecto de aproximadamente 4 a 9 meses48,49, y EA mayoritariamente leves48,49.
Una reciente revisión de la literatura encontró 14 estudios prospectivos, fundamentalmente ECA de pequeño tamaño, que demostraban la efectividad de la TB-B en HA, HP e HF, y en hiperhidrosis residual y compensatoria. Al parecer, produciría mayor dolor asociado a las inyecciones y mayor tasa de EA que la TB-A50.
Hiperhidrosis primaria en los niños y adolescentesEn los niños, la HP es frecuentemente infradiagnosticada e infratratada, pese a que puede ocasionar un grave impacto en la calidad de vida, incluso en los pacientes menores de 12 años51. En esta población, la HP se inicia alrededor de los 11 años de edad27. Su localización más frecuente es la palmoplantar (90%), seguida de la axilar (15%) y facial (6%)2,52.
Terapia tópicaAntitranspirantes tópicosLos productos tópicos con sales de aluminio son indicados en la práctica clínica como tratamiento de primera línea; sin embargo, no hemos encontrado estudios sobre su efectividad y tolerabilidad en población pediátrica.
Anticolinérgicos tópicosGlicopirronio tópicoEl glicopirronio tópico está aprobado por la FDA para el tratamiento de la HA en pacientes ≥9 años. Un análisis post-hoc de 2 ECA con 44 individuos (entre 9 y 16 años) con HA en tratamiento con tosilato de glicopirronio al 2,4%, reveló que presentaban respuestas clínicas similares a los adultos, reduciendo significativamente el DLQI, el HDSS y la producción de sudor. El producto fue bien tolerado y en solo un caso se suspendió el fármaco por midriasis moderada unilateral27. En la extensión de este estudio a las 44 semanas, que incluyó a 38 niños, se mantuvieron estos resultados28.
Terapia sistémicaAnticolinérgicos oralesOxibutininaLa oxibutinina está aprobada por la FDA para el tratamiento de la enuresis en los niños ≥5 años. Dos estudios prospectivos (uno de ellos con seguimiento a largo plazo) con 95 niños de entre 7 y 14 años con HPr, describieron una disminución significativa de la sudación y del DLQI y aproximadamente el 90% alcanzó una mejoría clínica moderada o excelente. La mayoría presentó EA leves, fundamentalmente xerostomía52,53. Resultados similares se observaron en un estudio retrospectivo con 50 niños o adolescentes54. En estos estudios se ha utilizado una dosis progresiva: inicio con 2,5 mg por la noche y aumento paulatino hasta un máximo de 5 mg/12 h en los niños >40 kg o a 2,5 mg/12 h en <40 kg52,54.
Glicopirrolato oralUn estudio retrospectivo con 31 niños con una dosis aproximada de 2 mg de glicopirrolato, mostró que el 90% presentó una mejoría clínica significativa de la hiperhidrosis. El fármaco fue bien tolerado; sin embargo, casi el 30% presentó xerostomía y/o xeroftalmia55.
Terapia intralesionalToxina botulínicaUn EC con 151 niños o adolescentes de entre 12 y 17 años con HA, mostró que la inyección de TB-A disminuyó la sudación y el HDSS en la mayoría de los pacientes. El efecto se prolongó por una media de 4,5 meses. Ningún paciente suspendió la terapia por EA56.
DiscusiónLa HPr produce un impacto en la vida del paciente equiparable al producido por la psoriasis, dermatitis atópica o artritis reumatoide5; sin embargo, solo un pequeño porcentaje de los individuos buscan atención médica y el 50% lo hace después de >10 años de enfermedad5. Además, la falta de conocimiento de los profesionales del real impacto de la HPr y de las alternativas terapéuticas disponibles dificultan el acceso a tratamientos efectivos5. Múltiples ECA avalan la efectividad del glicopirronio tópico en el manejo de la HPr en los adultos18,20,24,29-30,57 y niños27,28 y ha demostrado ser coste-efectivo58. Dada su amplia disponibilidad (está comercializado en España desde abril del 2023), bajo coste y excelente perfil de seguridad, consideramos que puede ser indicado en primera línea terapéutica en HPr moderada o grave. Otras alternativas como la oxibutinina tópica ofrecen resultados prometedores32, pero requieren estudios más amplios para realizar recomendaciones. Dentro de la terapia sistémica, los anticolinérgicos orales como la oxibutinina pueden ser una alternativa muy útil36,37,59–61, pero presentan una alta tasa de EA (mayoritariamente leves), por lo que se podrían considerar en segunda línea. La TB es altamente efectiva, pero con limitaciones importantes como su alto coste y el dolor asociado al procedimiento.
ConclusionesLa HPr es una enfermedad frecuente y ocasiona un grave impacto en la calidad de vida. El glicopirronio tópico es un anticolinérgico de bajo coste, excelente perfil de seguridad y de efectividad demostrada en múltiples ECA, por lo que podría ser considerado un tratamiento de primera línea en HPr moderada/grave en los adultos y los niños. La oxibutinina oral y la toxina botulínica podrían indicarse en los no respondedores al tratamiento tópico.
- •
La hiperhidrosis primaria es la causa más frecuente de hiperhidrosis.
- •
La hiperhidrosis primaria produce un gran impacto en la calidad de vida, en la actividad social, laboral y física.
- •
La hiperhidrosis primaria se asocia a altas tasas de ansiedad, de depresión y de fobia social.
- •
Los antitranspirantes tópicos son efectivos en las formas leves de hiperhidrosis.
- •
El glicopirronio tópico es un anticolinérgico de bajo coste, excelente perfil de seguridad y efectividad contrastada en múltiples ensayos clínicos.
- •
El glicopirronio tópico está aprobado por la FDA para el tratamiento de la hiperhidrosis axilar en pacientes ≥9 años.
- •
La toxina botulínica está aprobada por la FDA para el tratamiento de la hiperhidrosis axilar en adultos.
- •
La toxina botulínica presenta una elevada efectividad en la hiperhidrosis primaria, pero tiene un alto coste, limitada disponibilidad y el procedimiento puede ser doloroso.
- •
La oxibutinina oral puede ser un tratamiento efectivo y bien tolerado, y múltiples estudios avalan su utilidad en los niños y los adultos.
- •
Es fundamental titular adecuadamente la dosis de oxibutinina, incrementándola lenta y progresivamente para disminuir los efectos adversos asociados.
Ninguna.
Conflicto de interesesDaniel Morgado-Carrasco y Raúl de Lucas han recibido honorarios de Cantabria Labs.