La mola hidatidiforme (MH) consiste en un embarazo anormal caracterizado por la degeneración hidrópica de las vellosidades coriales e hiperplasia trofoblástica. Se clasifica en mola hidatidiforme parcial (MHP) y mola hidatidiforme completa (MHC). Tiene una incidencia de 1-3:1,000 embarazos en Norteamérica y Europa, y de 2.4:1,000 en México. Entre el 10-30% se complican con enfermedad gestacional trofoblástica persistente. El 75% de los embarazos molares se clasifican como MHC, la cual de manera general tiene un complemento cromosómico diploide androgenético. Histopatológicamente se caracteriza por edema hidrópico difuso e hiperplasia del sinciciotrofoblasto, citotrofoblasto y trofoblasto intermedio; el restante 25% se clasifica como MHP, con complemento cromosómico triploide e histopatológicamente se caracteriza por la presencia de dos poblaciones de vellosidades coriales, y existe hiperplasia del sinciciotrofoblasto y citotrofoblasto. La mayoría de las MHs son esporádicas, recurriendo de manera general del 0.6-2.57% de los casos. Se considera mola recurrente (MR) la ocurrencia de dos o más embarazos molares en una misma paciente, en este caso se identifican dos grupos de pacientes, aquellas con MR de origen androgenético y aquellas con MR con complemento diploide y origen biparental (MDBP), en el primer caso es raro que ocurra un tercer embarazo molar y el pronóstico reproductivo es más favorable. En aquellas pacientes con MDBP, su etiología se ha relacionado con alteraciones en la metilación materna del tejido molar por mutaciones en los genes NLRP7 y KHCD3L, el pronóstico reproductivo para estas pacientes es adverso, con probabilidad de lograr un embarazo normal a término solo del 5 al 7%.
The hydatidiform mole (HM) consists in an abnormal pregnancy, featured by hydropic degeneration of the chorionic villi and trophoblastic hyperplasia. It is classified as complete hydatidiform mole (CHM) and partial hydatidiform mole (PHM) and has an incidence in Europe and North America of 1-3:1,000 pregnancies, in Mexico the incidence has been estimated in 2.4:1,000 pregnancies. From 10 to 30% of the HM complicate with persistent trophoblastic gestational disease. Almost 75% are classified as CHM, which have a diploid androgenetic chromosome complement; histopathological features are diffuse hydropic edema, and trophoblastic hyperplasia of the syncytiotrophoblast, cytotrophoblast and intermediate trophoblast. The remaining 25% are classified as PHM, with a triploid chromosome complement; histopathological features are the presence of two villi populations, and syncytiotrophoblast and cytotrophoblast hyperplasia. Most of the HMs are sporadic, with general recurrence in 0.6 to 2.57% of total cases. The occurrence of two or more molar pregnancies in the same patient is known as recurrent mole, in this case there are two groups: those with RM of androgenetic origin and those with a diploid complement and biparental origin (DCBP). In the first case it's rare to have a third molar pregnancy and reproductive outcome is better, in those patients with DCBP, their etiology has been related with maternal metilation alterations in molar tissue, the majority of patients with this type of molar pregnancy have mutations in NLRP7 and KHCD3L genes, the reproductive outcome is adverse, with a probability of a normal term pregnancy of 5-7%.
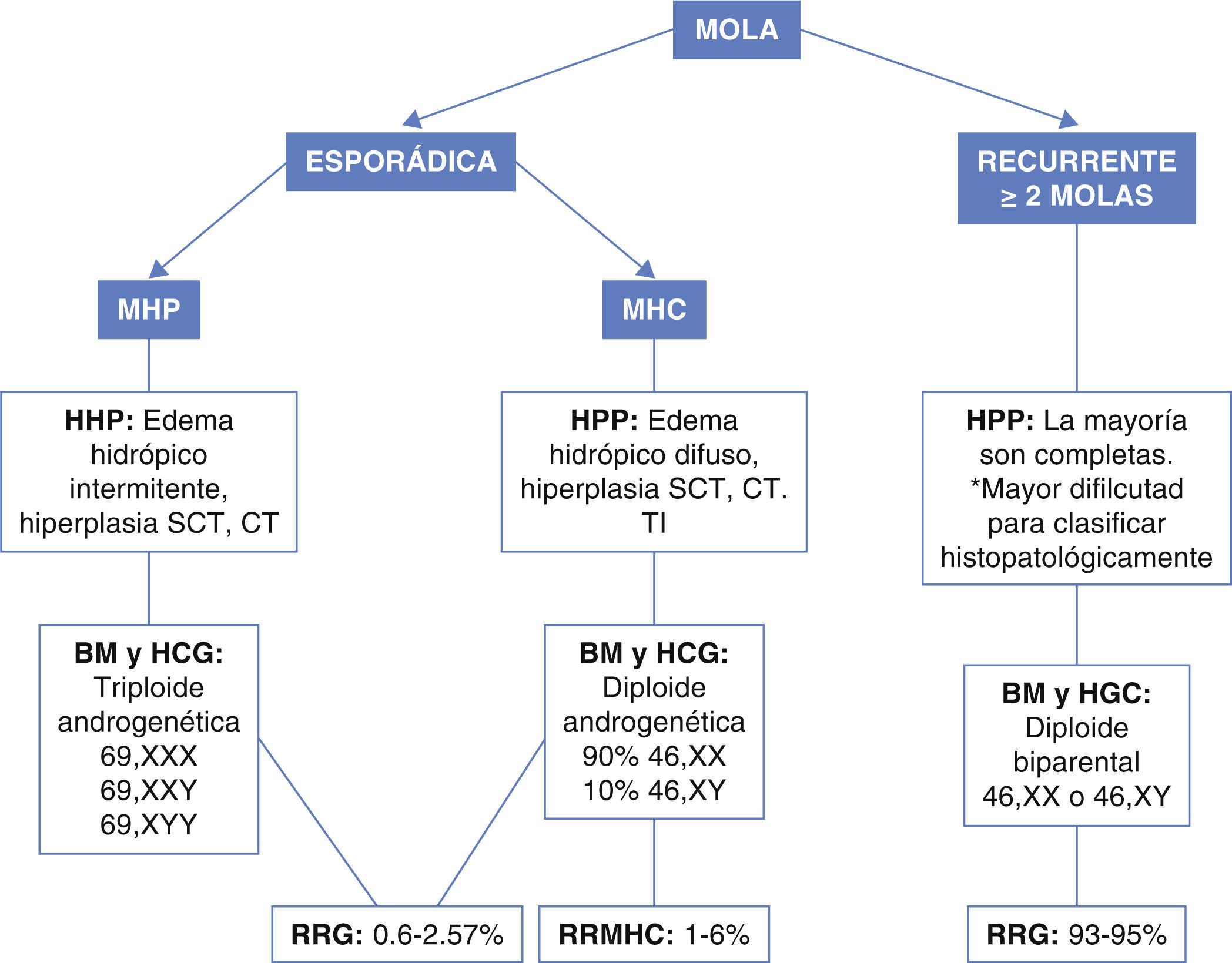
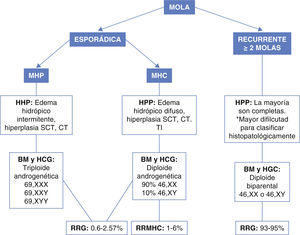
La mola hidatidiforme (MH) forma parte del grupo de enfermedades trofoblásticas de la gestación, consiste en un embarazo anormal caracterizado por degeneración hidrópica de las vellosidades coriales y proliferación trofoblástica con desarrollo embrionario anormal o ausente1. Se clasifica como MH completa (MHC) o parcial (MHP) de acuerdo a sus hallazgos histopatológicos y citogenéticos2 (fig. 1). El 75% de los embarazos molares clínicamente reconocidos son clasificados como MHC y 25% como MHP3.
Clasificación de la mola hidatidiforme. MHP: mola hidatidiforme parcial; MHC: mola hidatidiforme completa; HHP: hallazgos histopatológicos; BM: bases moleculares; SCT: sinciciotrofoblasto; CT: citotrofoblasto; TI: trofoblasto intermedio; HCG: hallazgos citogenéticos; RRG: riesgo de recurrencia general; RRMHC: riesgo de recurrencia mola hidatidiforme completa.
Esta enfermedad tiene una incidencia en Europa y en Norteamérica del 1 a 3 por 1,000 embarazos, observándose de forma más frecuente en países del Medio Oriente, América Latina, África y Lejano Oriente. Se ha reportado una incidencia de 1 en 500 en Japón y China, y de hasta 1 en 80 embarazos en Indonesia. La frecuencia de embarazos molares en México es de 2.4 por cada 1,000 embarazos3–5.
El factor de riesgo mejor establecido es la edad materna2, existe una relación entre el riesgo de embarazo molar y los extremos de edad materna; con un riesgo aumentado de 10 veces en mujeres mayores de 40 años y 1.3 veces en adolescentes. Otros factores predisponentes son la gravidez y uso de anticonceptivos3. Es también reconocido que un embarazo molar previo aumenta el riesgo de presentar un nuevo embarazo molar en futuras concepciones6, así como el antecedente de aborto espontáneo, el cual aumenta el riesgo de presentar un embarazo molar de 2 a 3 veces7.
Presentación clínicaLas pacientes con MH suelen ser detectadas de forma inicial en el primer trimestre, por la apariencia ultrasonografía característica3,8. Posterior al diagnóstico, las molas deben ser evacuadas y debe seguirse a la paciente con una serie de mediciones de la fracción beta de la hormona gonadotropina coriónica humana (β-hCG), hasta que se presenten las cifras normales de esta hormona. Un porcentaje de pacientes evoluciona a enfermedad gestacional trofoblástica persistente o residual (EGTP), la cual se manifiesta principalmente con sangrado irregular, útero agrandado con forma irregular y crecimiento ovárico bilateral acompañado de niveles elevados de β-hCG8.
El riesgo de enfermedad gestacional trofoblástica persistente posterior a un embarazo molar varía de 10 al 30%9–11, siendo más frecuente en los casos de mola completa en comparación a las pacientes con un caso de mola parcial (10 vs 0.2-4%)11.
La EGTP más frecuente es la mola invasora, seguida del coriocarcinoma. El riesgo de presentar coriocarcinoma es 1,000 veces mayor después de un embarazo molar, en comparación a otro evento obstétrico, el riesgo aumenta si se trata de mola completa y en casos de edad materna avanzada8.
La coexistencia de un feto normal y una MH es un evento poco frecuente en la práctica clínica, con una incidencia de 1 caso por cada 22,000 a 100,000 embarazos12.
Hallazgos histopatológicos y citogenéticosLa mayoría de las MHCs son diploides androgenéticas (dos conjuntos cromosómicos de origen paterno) y no presentan desarrollo embrionario. Se ha propuesto que el 90% surge de forma secundaria a la fertilización de un óvulo vacío con duplicación del contenido espermático, resultando en un complemento cromosómico 46 XX. En el 10% de los casos restante, se cree que existe una fertilización de un óvulo vacío por dos espermatozoides con la misma probabilidad de ser 46 XX o 46 XY (3).
Ante la ausencia de óvulos vacíos en los procedimientos de biología de la reproducción, se ha propuesto como mecanismo de formación, la reducción del contenido cromosómico a dos conjuntos de cromosomas (diploidización) posterior a una concepción triploide (tres conjuntos de cromosomas). La teoría se origina con la formación de una concepción con tres complementos cromosómicos, siendo dos de origen paterno y uno de origen materno (triploide diándrica), usualmente por la fertilización de un solo óvulo por dos espermatozoides o por un espermatozoide diploide (dos complementos cromosómicos). El cigoto triploide con tres pronúcleos puede mantener el estado de triploidía o puede tener una división celular anormal resultado en una mola completa diploide androgenética por pérdida del pronúcleo materno13.
La mayoría de las MHPs son triploides diándricas con desarrollo embrionario anormal. Diferentes mecanismos de formación de MHPs han sido descritos, entre los que se señalan:
Mola recurrenteLa MH se presenta generalmente de forma esporádica, sin embargo algunas mujeres presentan recurrencia.
Se define como mola recurrente (MR) a la ocurrencia de al menos dos MH en la misma paciente4. Las pacientes con MR pueden clasificarse dentro de dos grupos:
- 1.
Pacientes con MH completa androgenéticas o MH parcial triploides.
- 2.
Pacientes con molas diploides de origen biparental (MDBP)6 (fig. 1).
Ocasionalmente las pacientes con MR tienen familiares con embarazos molares y estos casos se definen como MR familiar14. Los casos familiares se consideran poco frecuentes, aunque hay una tendencia creciente a pensar que se encuentran subdiagnosticados3.
Aspectos moleculares de la mola recurrenteSe ha observado que las mujeres con mola recurrente de origen biparental generalmente no logran un embarazo normal, por lo que se ha sugerido un defecto genético materno como el responsable de esta entidad15,16.
Se ha sugerido que las MDBP resultan de una falla para reprogramar la impronta materna de regiones diferencialmente metiladas en línea germinal17.
Varios estudios independientes reportan pacientes con mutaciones homocigotas y heterocigotas compuestas en el gen NLRP7, con aparente relación etiológica a la MR, confiriéndoles predisposición a embarazos molares diploides de origen biparental18. Se han identificado mutaciones en este gen en 88% de los casos familiares y 66% de los casos únicos de MR17. Su asociación con molas androgenéticas, triploidía, abortos y óbitos de etiología desconocida, es controversial19.
Un segundo gen con efecto materno, el KHDC3L, ha sido asociado con MR20. Se considera un gen menor con mutaciones en el 10 al 14% de las pacientes con MR que no presentan mutaciones en el gen NLRP74.
Asesoramiento genéticoEl antecedente de un embarazo molar por sí solo aumenta el riesgo de un subsecuente embarazo molar, recurriendo en general en el 0.6 al 2.6% de los casos. El riesgo de presentar un segundo embarazo es mayor si se trata de una mola completa6,9, este riesgo aumenta después de un segundo embarazo molar y disminuye después de un embarazo normal3,9.
En la población general un tercer embarazo molar es raro, con excepción de aquellas pacientes con predisposición genética a múltiples embarazos molares, siendo difícilmente distinguible por hallazgos patológicos de aquellos casos de embarazo molar de origen adrogenético con bajo riesgo de recurrencia. En estas pacientes con mayor predisposición, las molas suelen ser diploides y de origen biparental6.
A diferencia de pacientes con molas de origen androgenético, las pacientes con MR-MDBP tienen un riesgo de 93 a 95% de volver a presentar un nuevo embarazo molar. En algunos casos el embarazo se ha logrado por medio de ovodonación4 (fig. 1).
La identificación de pacientes con MR-MDBP es importante no solo por la baja posibilidad de lograr un embarazo normal a término, sino también por el riesgo que conlleva cada embarazo molar de malignizar. El riesgo del embarazo MR-MDBP de progresar a EGTP es el mismo que el riesgo de la mola de origen androgenético. Sin embargo, el pronóstico reproductivo de las pacientes con MR es malo. Una complicación en cada embarazo molar mucho más grave puede ser la muerte, aun cuando el manejo oncológico de tumores trofoblásticos es exitoso en la mayoría de los casos, hasta un 10% fallece por esta causa13.
Abordaje de pacientes con embarazo molar recurrenteEs importante realizar una adecuada genealogía e historia clínica en cualquier paciente que curse con un embarazo molar para poder identificar aquellos casos de embarazo molar recurrente, así como casos familiares, con el fin de recibir un abordaje óptimo y beneficiarse de asesoramiento genético.
El abordaje ideal posterior a dos embarazos molares es el análisis molecular por secuenciación de los genes NLRP7 y KHCD3L en la mujer afectada. Se sugiere iniciar el estudio con el gen mayormente asociado a MR-MDBP (NLRP7), en caso de tener un resultado negativo se debe analizar el gen KHCD3L. En aquellos casos sin evidencia de mutaciones en ambos genes, o en aquellos centros que no cuenten con los recursos o infraestructura para este estudio, las pacientes con MR pueden beneficiarse en base al conocimiento de su pronóstico reproductivo mediante análisis del origen biparental de los tejidos molares. Una herramienta útil que puede utilizarse para determinar el contenido cromosómico de los tejidos molares es el cariotipo o el FISH (hibridación in situ con fluorescencia) en el tejido molar. En caso de que el tejido sea diploide se sugiere determinar el origen parental del mismo. Se considera como mal pronóstico reproductivo a todos aquellos casos con molas de origen biparental o en aquellas pacientes positivas a mutaciones en cualquiera de los dos genes previamente mencionados.
Existen varios reportes de ovodonación exitosa en pacientes con MR-MDBP, lo cual debe ser informado como una posible opción reproductiva21,22.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.