En 2006, se autorizó en Estados Unidos una nueva vacuna para la prevención de la gastroenteritis aguda (GEA) causada por el rotavirus (RotaTeq; Merck, Whitehouse Station, NJ), que fue recomendada por el US Advisory Committee on Immunization Practices y la American Academy of Pediatrics para la vacunación rutinaria de todos los niños estadounidenses1. Esta decisión se basó, en parte, en la considerable carga de GEA relacionada con el rotavirus en el sistema estadounidense de atención sanitaria2-7, evaluada principalmente mediante el cruce de grandes bases de datos (como los datos nacionales de alta hospitalaria) y el empleo de abordajes indirectos para estimar la proporción de episodios de GEA atribuibles al rotavirus. Al contar con limitados datos poblacionales, confirmados por laboratorio, de supervisión activa sobre la infección grave por rotavirus8, la New Vaccine Surveillance Network (NVSN) de los Centers for Disease Control and Prevention (CDC) acometió este esfuerzo. Esta supervisión es necesaria para evaluar la eficacia de la vacunación mediante la monitorización prospectiva directa de la carga de enfermedad causada por el rotavirus y los genotipos de las cepas de rotavirus circulantes. Este artículo presenta los resultados de la primera estación de revisión de la GEA en la NVSN, que también fue la última estación de rotavirus antes de la instauración generalizada de la vacuna contra el rotavirus.
MÉTODOSLa NVSN realizó una revisión prospectiva, poblacional, de la GEA en 3 condados estadounidenses entre el 1 de enero de 2006 y el 30 de junio de 2006. La supervisión se realizó en hospitales, servicios de urgencia (SU) y consultas externas, con laaprobación del comité de Ética del CDC y de cada centro participante en la NVSN. Estos centros de la NVSN son el Vanderbilt University Medical Center (Davidson County, Tennessee), Cincinnati Children’s Hospital Medical Center (Hamilton County, Ohio), y el University of Rochester Medical Center (Monroe County, Nueva York).
Los niños de 14 días a 3 años de edad se consideraron elegibles para la inclusión si acudieron a estas instalaciones de asistencia sanitaria con una GEA, definida como µ3 deposiciones desligadas, µ1 episodio de vómitos, o ambas circunstancias, en 24 h. Debían residir en los condados indicados, haber iniciado los síntomas de gastroenteritis µ10 días antes de pedir asistencia médica, y que los padres o tutores otorgasen el consentimiento informado. Los niños no fueron elegibles si padecían una enfermedad no infecciosa, estaban inmunodeprimidos, habían sido incluidos anteriormente en el mismo episodio de gastroenteritis o habían sido trasladados desde otro hospital tras un ingreso de > 48 h. Los niños incluidos como pacientes del SU y que luego llegaron a la hospitalización durante la supervisión se clasificaron como hospitalizados.
Un cuestionario normalizado, administrado a los padres o tutores que dieron el consentimiento, recogió datos demográficos, de la historia clínica y socioeconómicos, y la revisión de las historias clínicas detectó datos clínicos y el estado de la vacunación. Intentamos tomar una muestra de heces antes de transcurridos 14 días del inicio de la enfermedad, que se estudiaron mediante una determinación inmunoenzimática (EIA) comercial de rotavirus. Los CDC analizaron las muestras positivas a EIA para determinar el genotipo del rotavirus mediante la reacción en cadena de la polimerasa (PCR) de transcripción inversa (TI) múltiple y la secuenciación de nucleótidos9-12. Los análisis estadísticos se realizaron mediante SAS 9.1 (SAS Institute, Cary, NC). Las comparaciones se realizaron con el test µ2 de Pearson y el test t de Student.
Los hospitales de la NVSN participantes reciben > 95% de los ingresos hospitalarios pediátricos en sus respectivos condados. En estos 3 condados viven µ85.000 niños de < 3 años de edad. Las tasas poblacionales de hospitalización se calcularon como el número ponderado de hospitalizaciones por GEA con rotavirus confirmado por el laboratorio dividido por el número de niños de la cohorte de edad en la población del condado (según el censo estadounidense de 2000), multiplicado por 10.000. Los pesos se calcularon para tener en cuenta el número de días en que se realizó la supervisión de la GEA, la proporción de niños elegibles incluidos en el estudio y las distintas tasas de recogida de muestras en los centros de NVSN. Se determinaron los intervalos de confianza (IC) del 95% mediante 1.000 muestras bootstrap de cada tasa, con los consiguientes valores de los percentiles 2,5 y 97,5 como límites inferior y superior, respectivamente, de los IC13.
Las tasas poblacionales de visita al SU por rotavirus se estimaron corrigiendo el número de visitas al SU relacionadas con la GEA por niños de < 3 años de edad por los períodos de supervisión durante 24 h, para tener en cuenta los días en que no se realizó la supervisión en una semana concreta y las proporciones estimadas de visitas al SU en la NVSN en los 3 condados (Davidson County, Tennessee, 54% en el SU del Vanderbilt University Medical Center; Hamilton County, Ohio, 95% en el SU del Cincinnati Children’s Hospital Medical Center; Monroe County, Nueva York, 70% en el SU del Strong Memorial y 25% en el SU del Rochester General). Los totales ponderados del mes se multiplicaron por la proporción mensual de muestras positivas al rotavirus de los participantes en el estudio en cada SU del NVSN para obtener la cifra estimada de visitas al SU relacionadas con el rotavirus14. Las tasas poblacionales en el SU se calcularon aplicando el método descrito para las tasas poblacionales de hospitalización.
Para la comparación con nuestras tasas de las visitas al SU relacionadas con el rotavirus en la NVSN calculamos de forma indirecta las tasas de visita al SU relacionadas con el rotavirus aplicando los datos de la National Hospital Ambulatory Medical Care Survey (NHAMCS). Se identificaron todas las visitas al SU del NHAMCS atribuibles a GEA en niños de < 3 años de edad, entre el 1 de enero y el 30 de junio, desde 2003 a 200515. Estas visitas al SU se identificaron seleccionando los códigos de GEA de la Clasificación Internacional de Enfermedades, 9.ª revisión, Modificación Clínica, en cualquiera de los 3 campos de diagnóstico médico. El EE de las estimaciones ponderadas se calculó mediante SUDAAN 9.0 (Research Triangle Institute, Research Triangle Park, NC). La estimación ponderada de visitas por GEA en los niños de < 3 años de edad se multiplicó por la proporción de muestras positivas a rotavirus observada en los centros de la NVSN durante el período coincidente del 1 de enero al 30 de junio de 2006 para obtener la cifra estimada y la tasa estadounidense de visitas al SU atribuibles a una GEA relacionada con el rotavirus. En nuestros cálculos de la tasa se utilizó como denominador las estimaciones intercensales por raza de los niños estadounidenses de < 3 años de edad entre 2003 y 2005 del National Center for Health Statistics16.
Los datos ambulatorios de la NVSN no son poblacionales, como nuestros datos del SU y de hospitalización, pero representan un componente importante de la carga estimada de gastroenteritis intensa por rotavirus. Estimamos una tasa ambulatoria de rotavirus en Estados Unidos multiplicando la proporción de visitas ambulatorias con rotavirus confirmado por laboratorio de nuestro período de 6 meses (enero a junio) de supervisión de la GEA en la NVSN por el número de visitas ambulatorias al SU (NHAMCS, 2003-2005) más las visitas a la consulta (National Ambulatory Medical Care Survey, 2003-2005) de los niños estadounidenses de < 3 años de edad entre enero y junio. Luego calculamos la tasa estadounidense con el método utilizado para las tasas estadounidenses del SU. Todas las tasas se anualizaron como visitas por 10.000 niños por año, excepto las tasas mensuales, que se presentan por 10.000 niños/año. Las extrapolaciones a la población estadounidense se calcularon aplicando las tasas de la NVSN a la cohorte anual de nacimientos estadounidenses, de µ4 millones.
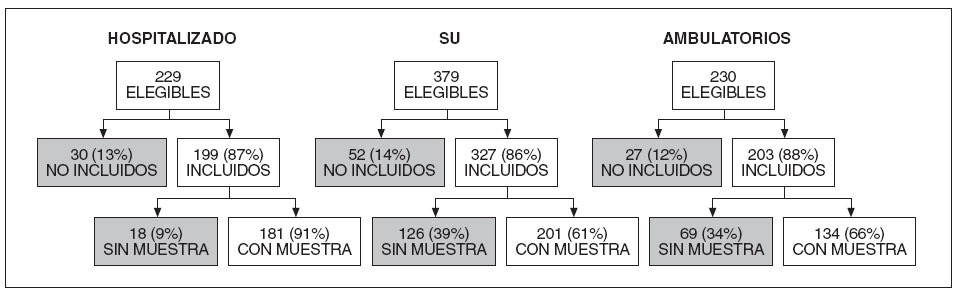
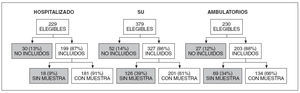
RESULTADOSGrupo de estudioDe los 1.042 niños hospitalizados, vistos en el SU y ambulatorios estudiados sistemáticamente para su participación en este estudio, resultaron elegibles 838 (80%). Obtuvimos el consentimiento para 730 de estos niños (87%), que luego se incluyeron en el estudio de supervisión de la GEA de la NVSN. Se tomaron muestras de heces de 517 (71%) de los 730 participantes en el estudio, es decir, 182 de los hospitalizados, 201 de los SU y 134 de las consultas ambulatorias centinela (fig. 1). Ninguno de los niños había recibido la vacuna contra el rotavirus.
Fig. 1. Organigrama de los sujetos elegibles para la revisión del NVSN, su inclusión y las muestras tomadas, según el tipo de profesional. SU: servicios de urgencia.
Comparación de los participantes en el estudioHubo más posibilidades de tomar muestras de heces de los sujetos incluidos hospitalizados (91%) que de los incluidos y visitados en el ED y de forma ambulatoria (61% y 66%, respectivamente, p < 0,001). Los participantes incluidos en el estudio fueron estadísticamente similares a los sujetos no incluidos respecto al tipo de profesional, la edad y el sexo, aunque hubo diferencias significativas respecto a la etnia y la cobertura de seguro; el 27% de los sujetos no incluidos era hispanoamericano, frente al 10% de los participantes incluidos en el estudio (p < 0,001), y el 18% de los sujetos no incluidos no estaba asegurado, comparado con el 6% de los participantes incluidos en el estudio (p < 0,001). Las razones de la falta de inclusión fueron las siguientes: rechazo de los padres o tutores (47%), idioma distinto al inglés (30%), falta de progenitor o tutor (19%) y paciente dado de alta antes de la inclusión (4%).
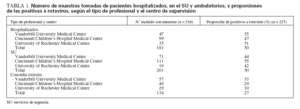
Detección del rotavirus mediante EIAEn todos los centros de revisión y tipos de profesional, el 44% de las muestras de heces de la NVSN (227 de 517 mues-tras) fueron positivas al rotavirus. Las tasas de detección de rotavirus en las visitas por GEA a los hospitalizados y al SU fueron, en ambos casos, del 50% y la tasa de detección en la consulta externa fue del 27%, estadísticamente menor (P < 0,001). Las proporciones de muestras de pacientes hospitalizados, del SU y ambulatorios que fueron positivas al rotavirus no fueron estadísticamente distintas entre los 3 centros de supervisión (hospitalizado: P = 0,631; SU: P = 0,259; ambulatorio: P = 0,068) (tabla 1).
TABLA 1. Número de muestras tomadas de pacientes hospitalizados, en el SU y ambulatorios, y proporciones de las positivas a rotavirus, según el tipo de profesional y el centro de supervisión
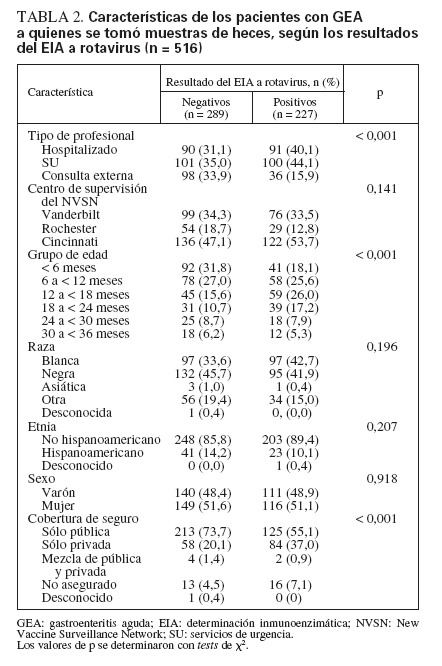
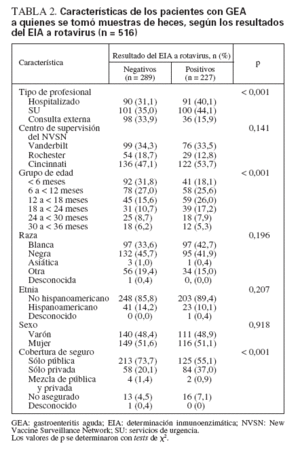
Los sujetos positivos a rotavirus fueron estadística-mente distintos a los sujetos rotavirus negativos respecto al grupo de edad (P < 0,001) y la cobertura de seguro (P < 0,001) (tabla 2). La edad media de los niños positivos a rotavirus fue de 13,6 meses (DE: 8,2 meses), comparado con una edad media de 11,7 meses (DE: 9,4 meses) en los niños negativos al rotavirus. Las muestras de heces de los niños de 6 a 12 meses de edad tuvieron estadísticamente más probabilidades de ser positivas al rotavirus que las de los lactantes de < 6 meses de edad (43% frente a 31%; P = 0,013). Los sujetos positivos al rotavirus tuvieron más probabilidades de contar con un seguro privado que los pacientes negativos al rotavirus (37,0% frente a 20,0%). No hubo diferencias estadísticas de los resultados del EIA a rotavirus según la raza (P = 0,214), la etnia (P = 0,212) o el sexo (P = 0,888).
TABLA 2. Características de los pacientes con GEA a quienes se tomó muestras de heces, según los resultados del EIA a rotavirus (n = 516)
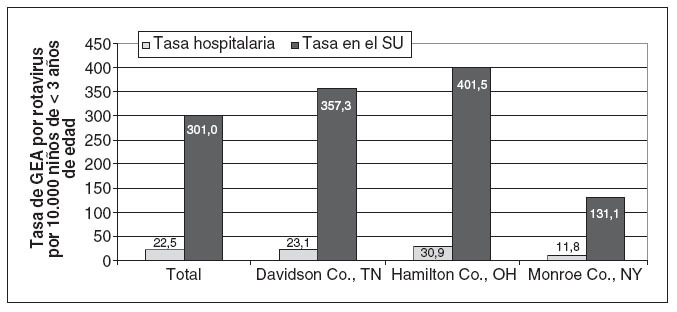
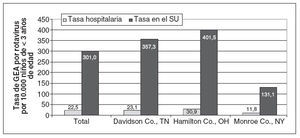
Tasa de hospitalización relacionada con el rotavirusLa tasa estimada de hospitalización relacionada con el rotavirus fue de 22,4 ingresos por 10.000 niños de < 3 años de edad en los 3 condados de la supervisión, con un IC 95% de 19,1 a 25,5 ingresos por 10.000 niños. Las tasas de hospitalización variaron según el centro de la NVSN, con 23,1 ingresos por 10.000 niños de < 3 años de edad (IC 95%: 17,2-28,7 ingresos por 10.000 niños) en Davidson County, Tennessee (Vanderbilt), 30,6 ingresos por 10.000 niños de < 3 años de edad (IC 95%: 24,5-36,6 ingresos por 10.000 niños) en Hamilton County, Ohio (Cincinnati), y 11,8 ingresos por 10.000 niños de < 3 años de edad (IC 95%: 8,1-15,1 ingresos por 10.000 niños) en Monroe County, Nueva York (Rochester) (fig. 2).
Fig. 2. Tasas de hospitalización y visita al SU por GEA relacionada con el rotavirus por 10.000 niños de < 3 años de edad, según el centro del NVSN. GEA: gastroenteritis aguda; NVSN: New Vaccine Surveillance Network; SU: servicios de urgencia.
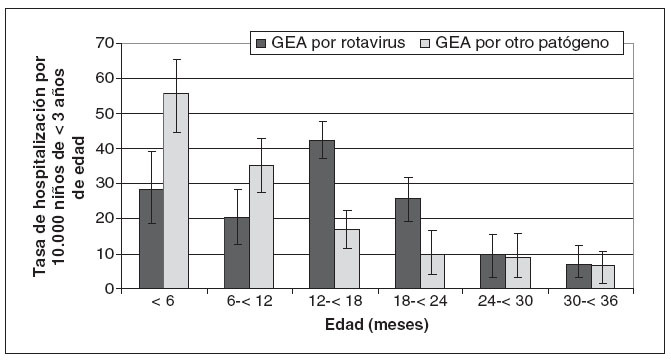
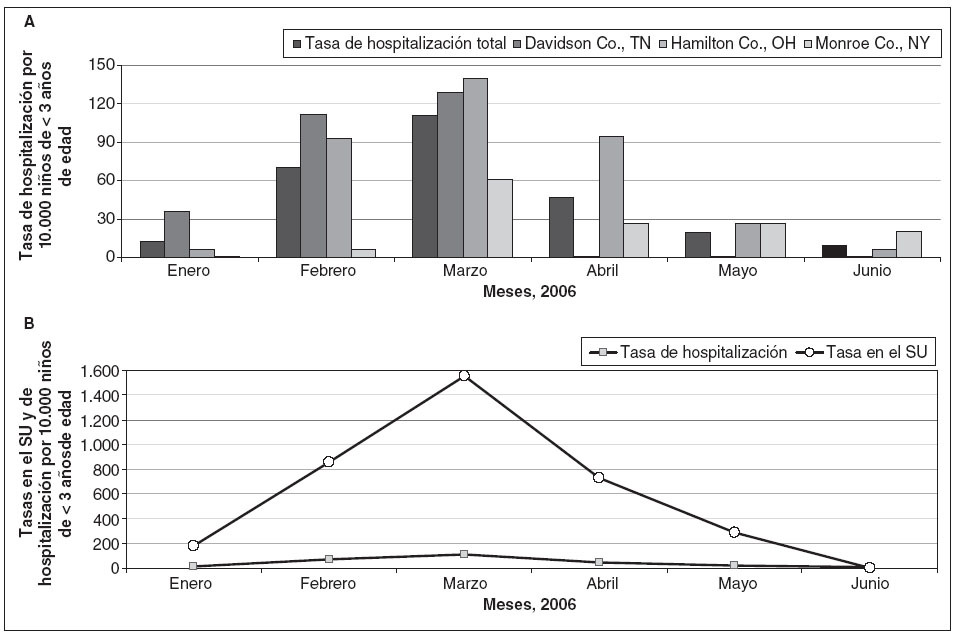
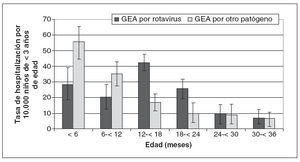
Respecto a la categoría de edad, las tasas ponderadas de hospitalización por rotavirus fueron mínimas para los niños de 30 a 36 meses de edad (7,1 ingresos por 10.000 niños) y máximas para los de 12 a 18 meses de edad (42,3 ingresos por 10.000 niños) (fig. 3). Comparativamente, la categoría de 30 a 36 meses de edad también tuvo la mínima tasa de hospitalización para la GEA negativa a rotavirus (6,9 ingresos por 10.000 niños), pero las tasas hospitalarias de infección por patógenos distintos al rotavirus fueron máximas en los 6 primeros meses de vida (55,6 ingresos por 10.000 niños). La tasa de hospitalización atribuida al rotavirus fue máxima durante los meses de febrero (69,9 ingresos por 10.000 niños/año), marzo (110,8 ingresos por 10.000 niños/año) y abril (46,5 ingresos por 10.000 ni-ños/año), mientras que la supervisión en los meses de enero, mayo y junio promedió 13,8 ingresos por 10.000 ni-ños/año (fig. 4).
Fig. 3. Tasas de hospitalización por GEA, relacionada o no con el rotavirus, por 10.000 niños de < 3 años de edad, con IC 95%, según el grupo de edad. GEA: gastroenteritis aguda.
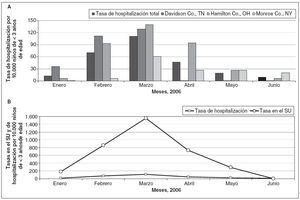
Fig. 4. Tasas de hospitalización por GEA relacionada con rotavirus por 10.000 niños/año en niños de < 3 años de edad, según el mes y el centro del NVSN (A) y comparación de las tasas de hospitalización y en el SU por 10.000 niños/año en niños de < 3 años de edad, según el mes (B). SU: servicios de urgencia.
Tasas de visitas ambulatorias y al SU relacionadas con el rotavirusEn la revisión poblacional activa de la NVSN, 301,0 de cada 10.000 niños de < 3 años de edad acudieron al SU por una GEA relacionada con el rotavirus. Nuestra tasa, obtenida directamente, fue mayor que la tasa media durante 3 años calculada de los datos del NHAMCS (171,7 visitas al SU por 10.000 niños de < 3 años de edad entre enero y junio, 2003-2005; IC 95%: 136,5-207,0 visitas al SU por 10.000 niños). Entre 2005 y 2003, las tasas anuales nacionales de visitas al SU según los datos del NHAMCS oscilaron entre 140,0 visitas al SU por 10.000 niños (IC 95%: 78,7-201,2 visitas al SU por 10.000 niños) y 205,9 visitas al SU por 10.000 niños (IC 95%: 136,7-275,1 visitas al SU por 10.000 niños).
Las tasas de visita al SU de la NVSN por una GEA relacionada con el rotavirus en los niños de < 3 años de edad variaron entre los centros de la NVSN, es decir, 357,3 visitas al SU por 10.000 niños en Davidson County, Tennessee, 401,5 visitas al SU por 10.000 niños en Hamilton County, Ohio, y 131,1 visitas al SU por 10.000 niños en Monroe County, Nueva York (fig. 2). De forma congruente con el patrón estacional de la hospitalización por rotavirus, la tasa de visita al SU por GEA relacionada con rotavirus fue máxima durante los meses de febrero (858,3 visitas al SU por 10.000 niños), marzo (1.557,1 visitas al SU por 10.000 niños) y abril (727,0 visitas al SU por 10.000 niños), comparado con una tasa media de 156,7 visitas al SU por 10.000 niños en enero, mayo y junio (fig. 4). En las consultas externas centinela de la NVSN, la tasa de visitas ambulatorias atribuibles a una gastroenteritis por rotavirus fue de 311,9 visitas ambulatorias por 10.000 niños de < 3 años de edad (IC 95%: 199,0-424,9 visitas ambulatorias por 10.000 niños).
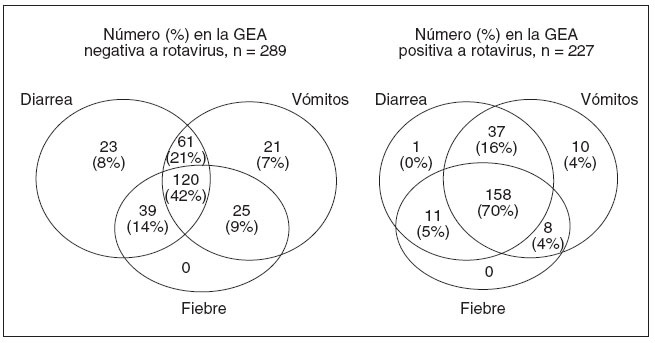
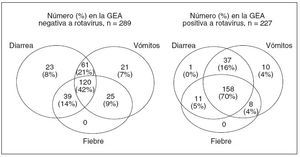
Gravedad del rotavirusLos síntomas de la GEA relacionada con el rotavirus fueron, por lo general, más graves que los de la GEA no relacionada con el rotavirus e incluyeron con mayor probabilidad los vómitos (95% frente al 79%; P < 0,001), la diarrea (92% frente al 84%; P = 0,007), la fiebre (78% frente al 63%; P = 0,001) y la letargia (53% frente al 27%; P < 0,001). La cifra media de episodios diarios de vómito fue mayor en los casos de GEA relacionados con rotavirus, comparados con los casos de GEA no relacionados con rotavirus (7,5 frente a 5,6 episodios diarios; P < 0,001), así como la cifra media de episodios diarreicos diarios (8,0 frente a 6,3 episodios diarios; P = 0,002). La figura 5 muestra los síntomas de la enfermedad de GEA en los sujetos positivos y negativos al rotavirus de la supervisión (cabe destacar que la fiebre no fue requisito de inclusión en la supervisión). Más del 70% de los sujetos positivos a rotavirus presentó la combinación de síntomas de diarrea, vómitos y fiebre, comparado con el 41,5% de los sujetos de la revisión con GEA negativa a rotavirus. Fue rara la presentación de diarrea aislada positiva a rotavirus (0,4%), aunque este síntoma se presentó de forma aislada en el 8% de los sujetos de la revisión negativos al rotavirus. No hubo fallecimientos en nuestros sujetos de la revisión.
Fig. 5. Diagrama de Venn de la diarrea, los vómitos y la fiebre en los sujetos de revisión con GEA negativa a rotavirus frente a los sujetos positivos a rotavirus. GEA: gastroenteritis aguda.
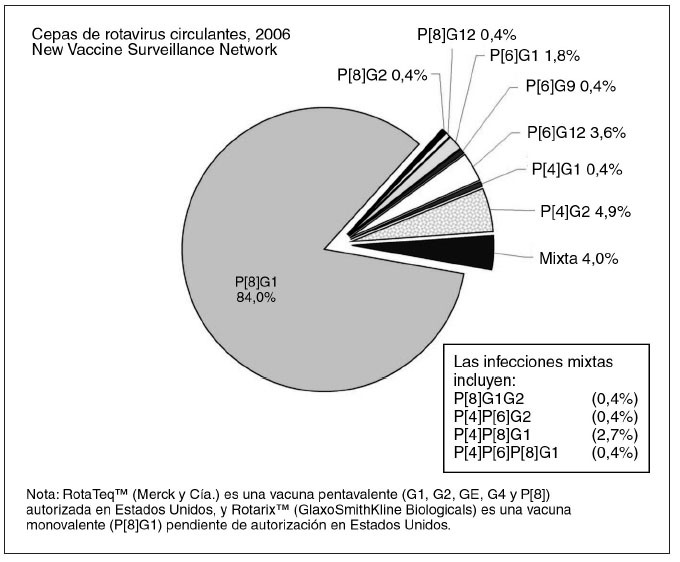
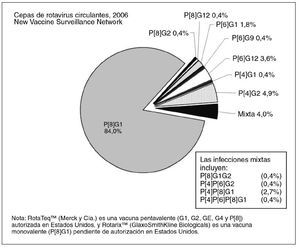
Detección de cepasEntre las 225 muestras positivas al rotavirus remitidas a los CDC para la identificación de la cepa mediante técnicas de PCR-TI, la cepa de mayor prevalencia fue la del genotipo P[8]G1 (189 muestras, 84,0%), seguida a distancia por P[4]G2 (11 muestras, 4,9%) y P[6]G12 (8 muestras, 3,6%). P[6]G1 se detectó con menor frecuencia (4 muestras, 1,8%), y hubo 1 sola observación (0,4%) de cada uno de los siguientes: P[8]G2, P[8]G12, P[6]G9 y P[4]G1. El 4% de nuestra muestra presentó infecciones mixtas por rotavirus con > 1 genotipo (fig. 6).
Fig. 6. Serotipos de rotavirus detectados en las muestras positivas a rotavirus (n = 225).
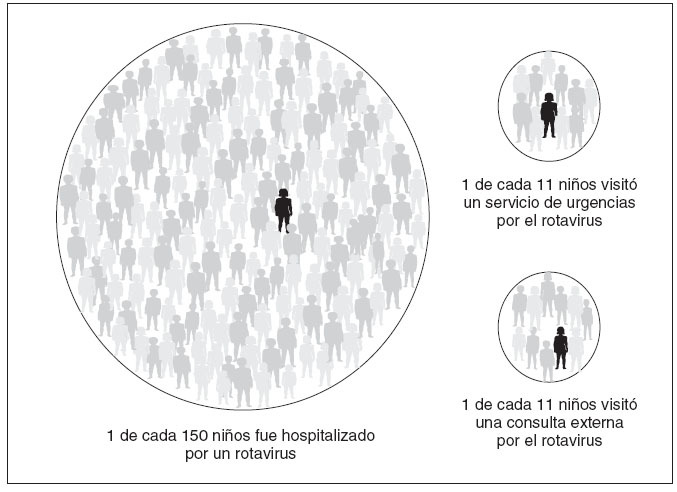
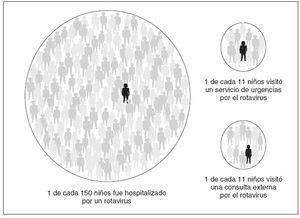
ANÁLISISEste estudio ilustra claramente la sustancial carga sanitaria de la GEA relacionada con el rotavirus en los niños estadounidenses y los posibles beneficios de la vacunación. Las infecciones por rotavirus confirmadas por laboratorio explicaron el 50% de las hospitalizaciones y de las visitas al SU por GEA y el 27% de las visitas ambulatorias durante los 6 meses de nuestra supervisión activa. Al extrapolar nuestros hallazgos poblacionales de estos 3 condados a los niños estadounidenses de < 3 años de edad a efectos de comparación, nuestra tasa global de hospitalización, de 22,4 por 10.000 niños se traduciría en µ27.000 hospitalizaciones anuales por rotavirus y nuestra tasa de 301,0 visitas al SU por 10.000 niños equivaldría a µ361.000 visitas anuales al SU. Nuestra tasa de consulta ambulatoria centinela de 311,9 visitas por 10.000 significaría unas 374.000 visitas ambulatorias anuales atribuibles a una GEA relacionada con el rotavirus en los niños estadounidenses de < 3 años de edad. Si lo aplicamos a una cohorte de nacimientos estadounidenses de 4 millones, sería de esperar que la GEA relacionada con el rotavirus originase anualmente la hospitalización de 1 de cada 150 niños estadounidenses de < 3 años de edad y la visita al SU o a la consulta ambulatoria de 1 de cada 11 (fig. 7). Además, los niños con GEA relacionada con el rotavirus mostraron síntomas (diarrea, vómitos, fiebre y letargia) con una frecuencia e intensidad significativamente mayores que los que sufrieron una GEA no relacionada con el rotavirus, lo que subraya la gravedad y la carga sanitaria de esta enfermedad. Más de 8 de cada 10 de nuestros pacientes con rotavirus confirmado por el laboratorio, ninguno de ellos vacunado en este año de la revisión inicial, tenía > 6 meses de edad, edad a la que debería haberse completado la vacunación, lo que indica que una vacuna eficaz podría prevenir una sustancial proporción de enfermedad grave relacionada con el rota-virus.
Fig. 7. Estimaciones de la carga anual de infección por rotavirus en los niños estadounidenses de < 3 años de edad, a partir de los datos del CDC NVSN, 2006.
Nuestro hallazgo de que el 50% de los niños de > 3 años de edad hospitalizados por una GEA entre enero y junio tenía un rotavirus confirmado por laboratorio demuestra, como habíamos sospechado, que el código específico de rotavirus de la Clasificación Internacional de Enfermedades, 9.ª revisión, Modificación Clínica, probablemente sólo engloba a una fracción de las hos-pitalizaciones relacionadas con el rotavirus. Estudios anteriores, que utilizaron los datos del consumo de asistencia sanitaria, informaron de unas proporciones sustancialmente menores (11,8%-19,6%) de altas hospitalarias por GEA codificadas de rotavirus17,18. Sin embargo, Staat et al8, en una revisión directa de niños de < 5 años de edad hospitalizados por una GEA, observaron una tasa de detección de rotavirus del 56% durante la estación del rotavirus, y la supervisión canadiense indicó que µ40% de las visitas al SU atribuibles a una GEA durante la estación invernal del rotavirus eran positivas a este patógeno19. Nuestras tasas de detección de rotavirus son congruentes con ambos estudios. Además, ofrecemos las primeras estimaciones poblacionales de las incidencias de hospitalizaciones y visitas al SU atribuibles a una infección por rotavirus confirmada por laboratorio en los niños estadounidenses. Nuestro informe de que el 27% de las visitas ambulatorias centinelas por GEA de los niños de < 3 años de edad eran atribuibles a una infección por rotavirus confirmada por laboratorio es menor que el valor del 40% notificado por Coffin et al20 pero todavía indica una notable carga de rotavirus en las consultas ambulatorias pediátricas, similar a la carga nacional estimada por Parashar et al1.
Cuando extrapolamos nuestros datos de supervisión poblacional activa a los niños estadounidenses de < 3 años de edad, observamos que nuestra estimación de las tasas estadounidenses de hospitalización atribuible al rotavirus, aun siendo sustancial, fue menor que las recientes mediciones indirectas de los conjuntos de datos nacionales, que calcularon unas tasas estadounidenses para los niños de < 5 años de edad de 47.000 a 67.000 hospitalizaciones anuales4,5,18,21; sería de esperar que la diferencia de edad resultara en unas tasas de hospitalización del NVSN µ10% al 15% menores que estos valores nacionales. Parte de la variación podría deberse a las presunciones subyacentes utilizadas para el análisis del conjunto nacional de datos, como las presunciones acerca de las proporciones de los casos de GEA atendidos médicamente y que son positivos a rotavirus. No obstante, nuestra medición de la carga de hospitalización por rotavirus parece estar considerablemente compensada por nuestro hallazgo estimado de 346.000 visitas anuales al SU en Estados Unidos atribuibles al rotavirus, cifra mayor que las estimaciones nacionales publicadas1 (205.000-272.000 visitas anuales al SU). En nuestra comparación, nuestra tasa NVSN de visitas al SU atribuibles al rotavirus fue mayor que las tasas indirectas de visitas al SU calculadas a partir de los datos nacionales más recientes de los niños de < 3 años de edad (NHAMCS, enero a junio, 2003-2005), aunque hubo una importante fluctuación de las tasas nacionales durante este período de 3 años (140,0-205,9 visitas al SU por 10.000 niños de < 3 años de edad). Nuestra observación durante un solo año de los datos del NVSN podría reflejar las considerables fluctuaciones de la tasa anual nacional observadas o indicar otra dinámica de utilización de la asistencia sanitaria, como la posible sustitución de la carga de la enfermedad entre el hospital y el SU en los centros del NVSN. Las tasas de hospitalización y visita en el SU variaron sustancialmente según el centro del NVSN, pero los cocientes entre las tasas de visita al SU y las de hospitalización siguieron siendo similares (las tasas de visita al SU fueron 1115 veces mayores que las de hospitalización). Destaca que las tasas de visitas al SU y a la consulta externa atribuibles a una GEA relacionada con el rotavirus fueron similares, y que nuestros datos retratan al rotavirus como causa de una muy importante, y típicamente inadvertida, carga de enfermedad en el SU. En conjunto, estos datos confirman que es necesario determinar las tasas de enfermedad tanto en la hospitalización como en el SU para calibrar con exactitud la carga de GEA grave relacionada con el rotavirus, e indican que vale la pena seguir estudiando la carga en el SU relacionada con el rotavirus.
Cerca del 96% de las cepas circulantes tienen el antígeno G o P incluido en RotaTeq, la actual vacuna contra el rotavirus autorizada en Estados Unidos. Una vacuna monovalente contra el rotavirus, en la actualidad pendiente de autorización en Estados Unidos, Rotarix (GlaxoSmith-Kline Biologicals), contiene una sola cepa atenuada de rotavirus humano (P[8]G1) que se observó directamente en el 84% de nuestras muestras y correspondió a un antígeno G o P en µ91% de nuestras cepas circulantes. Los ensayos clínicos han indicado cierto grado de protección contra la infección grave por otros tipos de rotavirus22.
Comparado con los resultados de revisión nacional de cepas de rotavirus en los laboratorios estadounidenses en 1996-199923, detectamos con mayor frecuencia la cepa P[8]G1 (84,0% frente al 75,5%). Encontramos una proporción comparativamente menor de P[4]G2 (4,9% frente a 10,9%). De las cepas habitualmente descritas como “poco frecuentes” en Estados Unidos, informamos de menos resultados positivos a P[6]G9 (0,4% frente a 3,2%), aunque por otro lado nuestros resultados fueron comparables a los datos de la supervisión nacional. Detectamos 2 cepas que se ha sugerido que representan serotipos emergentes de forma global, por su creciente detección en los últimos años11,24, P[8]G12 (0,4%) y P[6]G12 (3,6%). El caso de P[8]G12 se observó en Hamilton County, Ohio (Cincinnati), y los casos de P[6]G12 se observaron en las 3 áreas de revisión. Los niños en que se detectaron infecciones mixtas por rota-virus (4,0%) podrían haber tenido infecciones concomitantes por rotavirus o una GEA relacionada con un rota-virus activo combinada con la diseminación de rotavirus por una infección previa. Es necesario mantener la supervisión para medir las tendencias anuales de los rota-virus circulantes, controlar los posibles cambios resultantes de la instauración de la vacunación y evaluar la eficacia de la vacunación contra distintas cepas.
Se debe tener en cuenta ciertas limitaciones en la interpretación de nuestros hallazgos. En primer lugar, este informe resume los resultados de una sola estación de supervisión de la GEA. Es conocida la considerable variación geográfica y temporal de la actividad del rotavirus25,26, y observamos esta aparente variabilidad natural en los 3 puntos de supervisión. Queda por determinar cómo el impacto de una vacunación generalizada puede modificar este fenómeno geográfico y temporal en futuras estaciones del rotavirus. En segundo lugar, aunque realizamos una supervisión poblacional en condados localizados en estados del sur, el medio oeste y el noreste, se han aplicado extrapolaciones a la población estadounidense a efectos comparativos, y estas localidades pueden no ser representativas de toda la población estadounidense. Comparados con la población estadounidense de niños de < 3 años de edad del censo estadounidense de 2000, los µ85.000 niños que viven en los 3 condados del NVSN tuvieron una distribución similar respecto a la edad, el sexo y la raza blanca. Sin embargo, los niños de estas áreas de captación del NVSN tuvieron menos probabilidades de ser hispanoamericanos (6% en las áreas del NVSN, comparado con el 20% en Estados Unidos) y más de ser de raza negra (27% en las áreas del NVSN, comparado con el 14% en Estados Unidos). En tercer lugar, la inclusión en el estudio se limitó a los niños cuyos padres o tutores dieron el consentimiento al estudio en lengua inglesa. La diferencia observada de inclusión según la etnia latinoamericana nos llevó a desarrollar un impreso de consentimiento y una entrevista en español para facilitar la inclusión de padres o tutores hispanoamericanos que no hablen inglés en las futuras supervisiones. En cuarto lugar, debido a restricciones logísticas, realizamos la supervisión durante 6 meses de calendario que incluyen la estación invernal, en la que el rotavirus suele mostrar gran predominio. Según los patrones estacionales históricos de la enfermedad por rotavirus en Estados Unidos, confiamos en haber captado la inmensa mayoría de los casos de rota-virus en estos 3 puntos de revisión, aunque nuestras tasas de GEA relacionada con rotavirus probablemente constituyan infravaloraciones si no hubiéramos podido captar los casos fuera del período de revisión. En quinto lugar, nuestra demostración de la gravedad de la enfermedad no incluyó la evaluación clínica del estado de deshidratación.
En agosto de 2008 se habían distribuido > 21 millones de dosis de la vacuna contra el rotavirus en Estados Unidos27. A medida que aumenta la proporción de lactantes estadounidenses vacunados contra el rotavirus, nuestra plataforma de supervisión del NVSN sigue recogiendo prospectivamente datos epidemiológicos, clínicos y de laboratorio en el hospital y en el SU, así como en consultas ambulatorias centinela. Mediante entrevistas a los padres, resúmenes de historias clínicas, la confirmación de laboratorio de la enfermedad por rotavirus y la identificación de los genotipos del rotavirus utilizando la PCR-TI, el NVSN está singularmente preparado para controlar el impacto de la vacunación sobre las tendencias epidemiológicas y clínicas de la enfermedad, detectar cambios de los genotipos virales circulantes y realizar sólidas valoraciones poblacionales de la eficacia de la vacuna tras la comercialización. La supervisión del NVSN ofrece la confirmación directa de que la GEA relacionada con el rotavirus impone una importante carga sanitaria a los niños estadounidenses y ofrece una importante información inicial sobre los aspectos epidemiológicos y clínicos de la GEA grave relacionada con el rotavirus, lo que debiera permitir la futura valoración del impacto de la vacunación.
AGRADECIMIENTOSDamos especialmente las gracias a Elizabeth Teel y Jennifer Hull (CDC), que determinaron el genotipo del rotavirus, a la Dra. Marika Iwane (CDC), por la experiencia metodológica y técnica del NVSN y a los coordinadores de los centros del NVSN para la supervisión de la GEA, Diane Kent (Vanderbilt University Medical Center), Michol Holloway (Cincinnati Chil-dren’s Hospital Medical Center) y Dr. Gerry Loftus (University of Rochester School of Medicine and Dentistry), que dirigieron la inclusión en el estudio, la recogida de datos y la coordinación del laboratorio en los centros del data NVSN.
Los hallazgos y las opiniones expresadas en este informe son los de los autores y no necesariamente los de los Centers for Disease Control and Prevention.
Correspondencia: Daniel C. Payne, PhD, MSPH, Epidemiology Branch, Division of Viral Diseases, National Center for Immunizations and Respiratory Disease, Centers for Disease Control and Prevention, 1600 Clifton Rd, NE, MS-A34, Atlanta, GA 30333, Estados Unidos.
Correo electrónico: dvp6@cdc.gov