¡La púrpura de Schönlein Henoch (PSH) es la vasculitis más frecuente de la infancia, afecta cada año a de 8 a 20 por 100.000 niños y abarca el 49% de las vasculitis infantiles de Estados Unidos1,2. Aunque típicamente es autolimitada, la PSH puede causar hemorragia gastrointestinal, invaginación y nefropatía terminal (NT). La afectación renal, manifiesta por hematuria, proteinuria, síndrome nefrótico o insuficiencia renal, puede aparecer en el 60% de los niños3. En un estudio reciente, el 54% de los pacientes desarrolló manifestaciones renales a los 3 meses del diagnóstico, el 11,6% tenía anomalías persistentes al cabo de 7 años y ninguno de los pacientes desarrolló nefropatía terminal4 (NT). Sin embargo, los estudios anteriores informan que hasta el 21% de los niños con nefritis asociada con PSH desarrolla una glomerulonefritis de rápida progresión5 (GNRP); el 15% de estos niños con GNRP asociada a la PSH, es decir, el 2% de los pacientes con PSH, puede progresar a uremia o a NT6. Además, incluso la PSH aparentemente benigna puede tener efectos a largo plazo: 2 estudios informaron que el 40% y el 70% de los embarazos a término de mujeres con antecedentes de PSH de inicio infantil estuvo complicado por hipertensión, proteinuria o preeclampsia7,8.
Los objetivos del tratamiento de la PSH son típicamente: 1) mejorar los síntomas agudos, 2) mitigar la morbilidad a corto plazo (como las complicaciones abdominales que necesitan de intervención quirúrgica) y 3) prevenir la insuficiencia renal crónica. Como la PSH se caracteriza por la infiltración leucocitaria de las paredes del vaso sanguíneo con deposición de IgA (y la consiguiente lesión vascular y necrosis), y dado que los corticoides inhiben los procesos inflamatorios, se ha postulado que el tratamiento temprano con corticoides es eficaz en los 3 objetivos terapéuticos, aunque persiste gran controversia9-13. Aunque la bibliografía está llena de estudios retrospectivos que evalúan el empleo de corticoides en la PSH, en la actualidad sólo existen 3 estudios prospectivos, controlados con placebo sobre este tema, y sus conclusiones acerca de la utilidad de la administración temprana de corticoides son distintas9,11,14.
Mediante una revisión sistemática y el metaanálisis, tratamos de comparar y contrastar los datos experimentales y de observación acerca del empleo de corticoides, y cuando fue adecuado, sintetizar los datos de las 5 preguntas clínicas fundamentales. Los corticoides: 1) ¿acortan la duración de los síntomas abdominales en la PSH?; 2) ¿disminuyen las posibilidades de intervención quirúrgica en la PSH?; 3) ¿disminuyen las posibilidades de recurrencia de la enfermedad?; 4) ¿disminuyen las posibilidades de enfermedad renal (transitoria y persistente) en la PSH?, y 5) ¿disminuyen las posibilidades de desarrollar una nefropatía persistente en la PSH?
MÉTODOSFuentes de datosSe revisó la bibliografía mediante el Cochrane Controlled Trials Register (CCTR) y la base de datos Medline. La búsqueda incluyó artículos escritos en todas las lenguas, obteniéndose la traducción cuando fue necesario.
La búsqueda en CCTR y Medline utilizó las expresiones MeSH “steroids”, “methylprednisolone”, “dexmethasone” y las palabras clave “Henoch” y “corticosteroids”. “Henoch” y “purpura, Schönlein-Henoch” se agruparon mediante “OR”. “Steroids”, “methylprednisolone”, “dexamethasone” y “corticosteroids” se agruparon mediante “OR”. Ambos grupos de expresiones se agruparon mediante “AND”. El único límite aplicado a la búsqueda fue “sólo niños: 0-18 años”.
Por el gran número de estudios obtenidos en la búsqueda bibliográfica (n = 201), en este informe sólo citamos los estudios escogidos para la inclusión. En http://www.pediatric-gene-ralists.org/weiss.htm se encuentra la lista completa de publicaciones.
Selección para el estudioLos estudios elegibles se limitaron a los trabajos que examinaron el empleo de corticoides para el tratamiento de la PSH; fueron incluidos tanto ensayos de observación como los controlados aleatorizados. Los artículos fueron excluidos si: 1) eran una revisión, 2) examinaban el tratamiento con un fármaco distinto a los corticoides, 3) mostraban una serie de menos de 5 sujetos con PSH, 4) se centraban en personas de más de 18 años de edad, 5) no estudiaban el tratamiento con corticoides, 6) incluían sólo a pacientes con nefritis al inicio del estudio, 7) no evaluaban resultados definidos u 8) no estudiaban la PSH.
Selección del estudioLa búsqueda bibliográfica inicial del CCTR y la base de datos Medline obtuvo 201 artículos, escritos en 14 idiomas. Se revisaron los títulos para determinar su selección. Si el título no ofrecía datos suficientes para determinar si un estudio era o no elegible, se obtuvo y revisó el resumen. Los trabajos sin suficiente información en el resumen o sin un resumen accesible fueron examinados por completo. Intérpretes familiarizados con el lenguaje médico y los diseños de estudio evaluaron todos los artículos escritos en idiomas distintos al inglés.
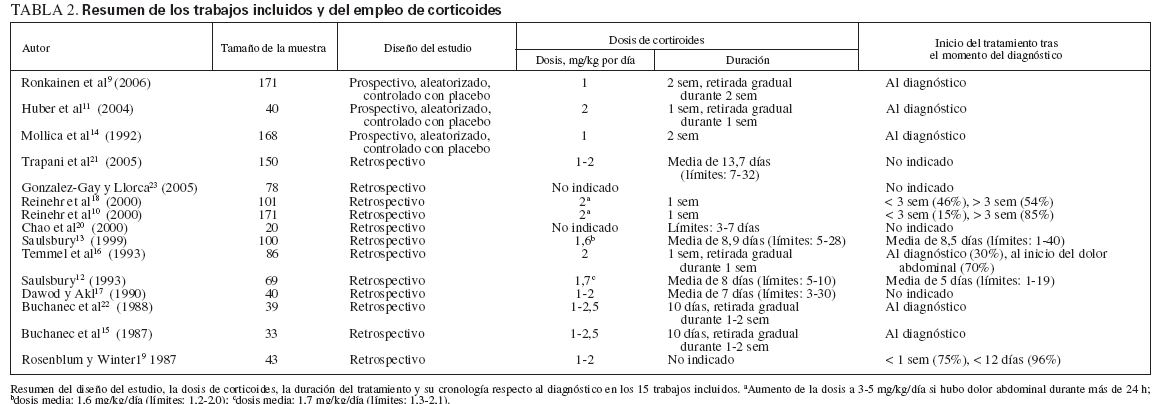
Dos autores (P.F.W. y J.A.F.) escrutaron de forma independiente cada uno de los títulos, resúmenes y artículos para determinar su inclusión. Las discrepancias fueron resueltas mediante discusión y acuerdo mediado por un tercer autor (C.F.). La tabla 1 presenta las razones para la exclusión del artículo. Tras aplicar todas las exclusiones quedaron 15 artículos para el análisis posterior (tabla 2).
TABLA 1. Razones para la exclusión de artículos
TABLA 2. Resumen de los trabajos incluidos y del empleo de corticoides
En un intento por encontrar todos los artículos relevantes se investigaron las listas de bibliografía de los artículos incluidos, con lo que se consiguieron otros 2 trabajos para su posible in-clusión15,16. Sin embargo, ninguno de ellos fue incluido porque no se pudo resumir los resultados. Además, nos comunicamos con los autores de los artículos incluidos para saber si había algún estudio o ensayo no publicado adicional.
Extracción de los datosDos de los autores (P.F.W. y J.A.F.) resumieron de forma independiente los datos de los artículos. Las discordancias fueron resueltas mediante discusión y acuerdo mediado por un tercer autor (C.F.). Los datos extraídos de los artículos incluyeron información acerca de la población de estudio, la existencia de un grupo de control, las limitaciones del estudio y la información relativa a la resolución del dolor abdominal, la intervención quirúrgica, la recurrencia y la incidencia de secuelas renales.
Análisis estadísticoLas razones de posibilidades agrupadas se obtuvieron aplicando la orden metan de Stata (versión 9.2, Statacorp, College Station, TX, Estados Unidos) para cada uno de los 5 resultados clínicos: 1) resolución del dolor abdominal, 2) intervención quirúrgica por dolor abdominal grave o invaginación, 3) recurren-cia, 4) anomalías renales acumulativas, 5) anomalías renales persistentes. Las posibilidades de obtener cada uno de los resultados en los pacientes tratados con corticoides se comparó con los pacientes tratados con cuidados rutinarios de sostén, tanto en los estudios prospectivos como en los retrospectivos. Se presentan los resultados de los modelos de efectos fijos. Se realizaron pruebas de heterogeneidad de cada análisis como forma de valorar hasta qué punto los resultados fueron consistentes y adecuados al modelo de efecto fijo. Si la prueba de heterogeneidad resultó significativa, no calculamos una OR agrupada. Se realizó la prueba del sesgo de Egger y los gráficos en embudo de cada uno de los resultados clínicos para valorar el sesgo de publicación. Todos los gráficos en embudo fueron simétricos, sugiriendo la ausencia de un sesgo de publicación. La prueba del sesgo de Egger sólo se pudo aplicar a los análisis con más de 2 estudios.
RESULTADOS¿Acortan los corticoides la duración de los síntomas abdominales en la PSH?
Aunque no existe acuerdo acerca de la indicación del empleo de corticoides en la PSH, el dolor abdominal es, curiosamente, la razón más habitual de la prescripción de los corticoides. Los estudios prospectivos de Huber et al y Ronkainen et al evaluaron el efecto de los corticoides sobre el dolor abdominal utilizando diarios de síntomas de 14 días. Huber et al utilizaron corticoides a 2 mg/kg/día durante 1 semana, con disminución gradual durante 2 semanas, mientras que Ronkainen et al utilizaron corticoides a 1 mg/kg/día durante 2 semanas, con disminución gradual durante las semanas 3 y 4 (tabla 2). Mediante el empleo de los valores de la mediana de la duración total del dolor abdominal, Huber et al no encontraron diferencia entre los grupos de tratamiento y de control11 (p = 0,8) (fig. 1A). Por el contrario, Ronkainen et al encontraron una disminución de 1,2 días de dolor en los pacientes tratados con corticoides9 (p = 0,03) (fig. 1A). Tres estudios retrospectivos informan de estos efectos en las primeras 24 h tras la administración de corticoides17-19. Sin embargo, al analizarla fue evidente la heterogeneidad entre los estudios incluidos (p = 0,015). Una probable fuente de heterogeneidad fue la cronología de la administración de corticoides en relación con el inicio de la enfermedad. En el estudio de Rheiner et al, 31 de los 57 pacientes recibieron corticoides más de 21 días después del inicio de la PSH, mientras que, en los otros 2 estudios, el grupo de tratamiento recibió corticoides unos días después del diagnóstico. El análisis tras la exclusión del estudio de Rheiner et al mostró un efecto positivo, estadísticamente significativo, del corticoide, sin heterogeneidad significativa (OR 5,42; IC 95%: 1,60, 18,29; p = 0,476) (fig. 1B).
Fig. 1. Tratamiento corticoide de la PSH y resolución del dolor abdominal. A. Intervalo hasta la resolución del dolor abdominal (días), expresado en medias y medianas. A, prospectivo; B, retrospectivo. B. OR e IC 95% de la resolución del dolor abdominal a las 24 h de la administración de corticoides. El tamaño de la caja es proporcional al inverso de la magnitud de la varianza. IC: intervalo de confianza; OR: odds ratio; PSH: púrpura de Schönlein Henoch.
Un estudio de Chao et al se centró en un grupo singular de pacientes con PSH con afectación hepatobiliar. La afectación estuvo definida por unas transaminasas hepáticas elevadas y una ecografía abdominal anormal20. De los tratados con corticoides, el 90% con afectación hepática, el 100% con colecistitis y el 100% con barro biliar se recuperaron al cabo de 7 días. Por el contrario, en el grupo no tratado, el 25% de los que tenían afectación hepática, ninguno de los afectados por colecistitis y sólo el 50% con barro biliar mostraron resolución a los 7 días. Sin embargo, todos los pacientes de ambos grupos mostraron la resolución de los síntomas a los 14 días.
¿Disminuyen los corticoides la incidencia de intervención quirúrgica en la PSH?
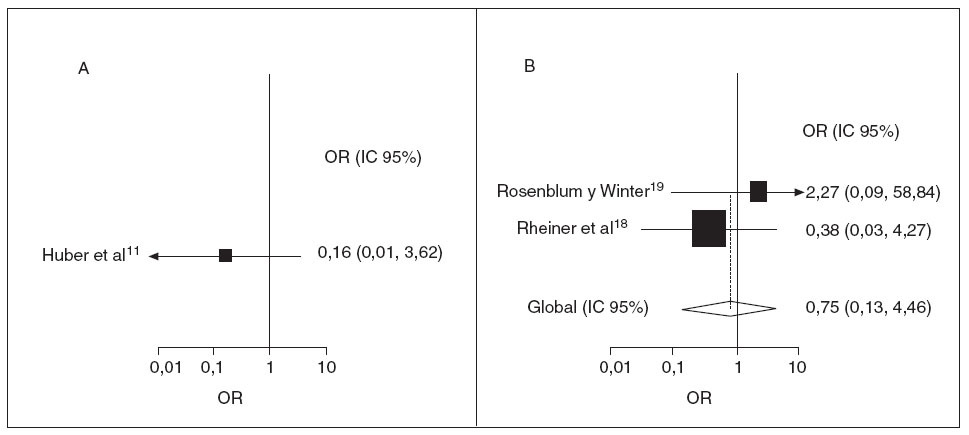
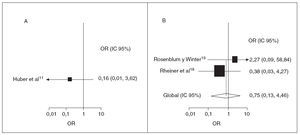
Sólo 3 estudios (1 ensayo aleatorizado controlado y 2 ensayos de observación) informaron de invaginación, una rara complicación abdominal que puede amenazar la vida durante la fase aguda de la PSH11,18,19. El de Huber et al11 fue el único estudio prospectivo que informó de la incidencia de invaginación; el riesgo de invaginación disminuyó, pero no de forma significativa, en el grupo de corticoides (OR 0,16; IC 95%: 0,01, 3,62). Los dos estudios retrospectivos sugirieron, en conjunto, un efecto protector de la exposición a corticoides (OR 0,75; IC 95%: 0,13, 4,46) (fig. 2). No hubo evidencia de heterogeneidad entre los estudios (p = 0,39).
Fig. 2. Tratamiento corticoide y posibilidades de intervención quirúrgica. OR e IC 95% de intervención quirúrgica posterior por dolor abdominal intenso, invaginación o ambas situaciones. A, prospectivo; B, retrospectivo. El tamaño de la caja del cuadro B es proporcional al inverso de la magnitud de la varianza. IC: intervalo de confianza; OR: odds ratio.
¿Disminuye el tratamiento temprano con corticoides las posibilidades de recurrencia de la PSH?
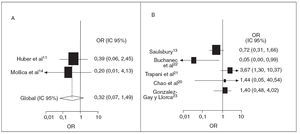
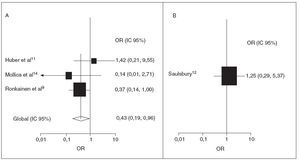
Las recurrencias afectan hasta la tercera parte de los niños con PSH13,21. Muchos de estos niños necesitan ingresos hospitalarios adicionales y farmacoterapia. Los 2 estudios prospectivos con datos de recurrencia indican un efecto positivo de los corticoides (OR 0,32; IC 95%: 0,07, 1,49) y la ausencia de heterogeneidad significati-11,14 (p = 0,70) (fig. 3). Los 5 estudios de observación retrospectivos que examinaron la recurrencia de PSH mostraron heterogeneidad (p < 0,01), de forma que no se indica una razón de posibilidades agrupada11,13,14,20-23. Se indican la razón de posibilidades y los intervalos de confianza del 95% de cada estudio (fig. 3). No se encontró evidencia de sesgo de publicación (prueba de Egger, p = 0,55).
Fig. 3. Tratamiento corticoide de la PSH y posibilidades de recurrencia. OR e IC 95% de recurrencia de PSH. A, prospectivo; B, retrospectivo. El tamaño de la caja de ambos cuadros es proporcional al inverso de la magnitud de la varianza. En el cuadro B no se muestra la OR global por la heterogeneidad de los estudios. IC: intervalo de confianza; OR: odds ratio; PSH: púrpura de Schönlein Henoch.
¿Disminuyen los corticoides la probabilidad de desarrollar anomalías renales acumulativas en la PSH?
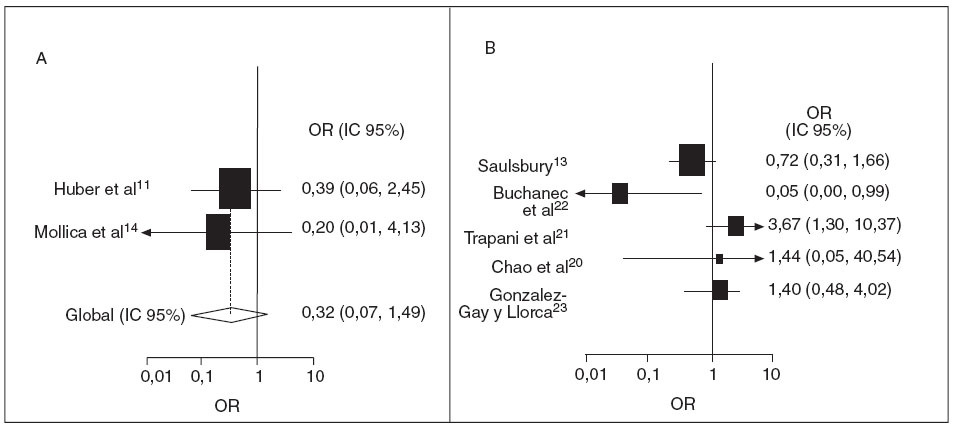
Ocho estudios presentan datos sobre las anomalías renales acumulativas (transitorias o persistentes) durante el año posterior al diagnóstico9-14,17,24. Hubo heterogeneidad entre los estudios, tanto prospectivos como retrospectivos (p = 0,03 y < 0,01, respectivamente), de forma que no se presenta la razón de posibilidades agrupada. En cambio, se muestra la razón de posibilidades individual y los intervalos de confianza del 95% de cada estudio (fig. 4). No se encontró señal de sesgo de publicación (prueba de Egger, p = 0,59 y p = 0,66, estudios prospectivos y retrospectivos, respectivamente).
Fig. 4. Tratamiento corticoide y posibilidades de incidencia acumulativa de nefropatía. OR e IC 95% de que los pacientes con PSH muestren una afectación renal (transitoria o permanente) acumulativa si reciben tratamiento temprano con corticoides. A, prospectivo; B, retrospectivo. El tamaño de la caja de ambos cuadros es proporcional al inverso de la magnitud de la varianza. No se muestra la OR global por la heterogeneidad de los estudios. IC: intervalo de confianza; OR: odds ratio; PSH: púrpura de Schönlein Henoch.
¿Disminuyen los corticoides la probabilidad de desarrollar anomalías renales persistentes?
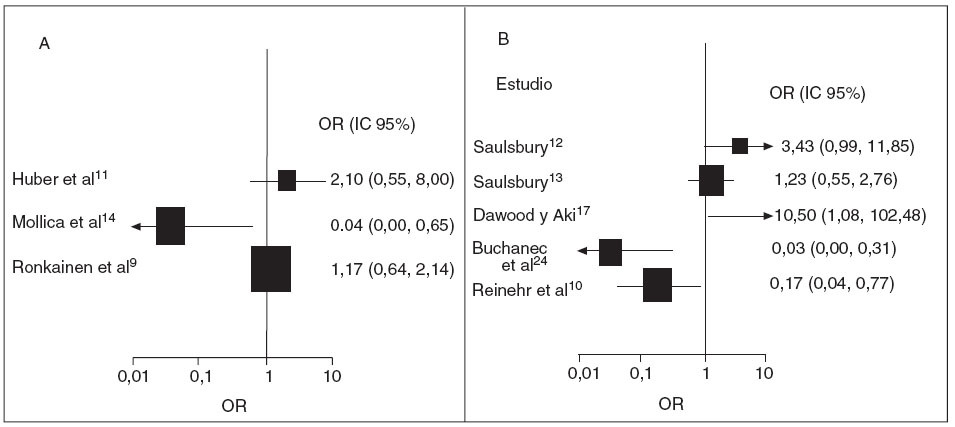
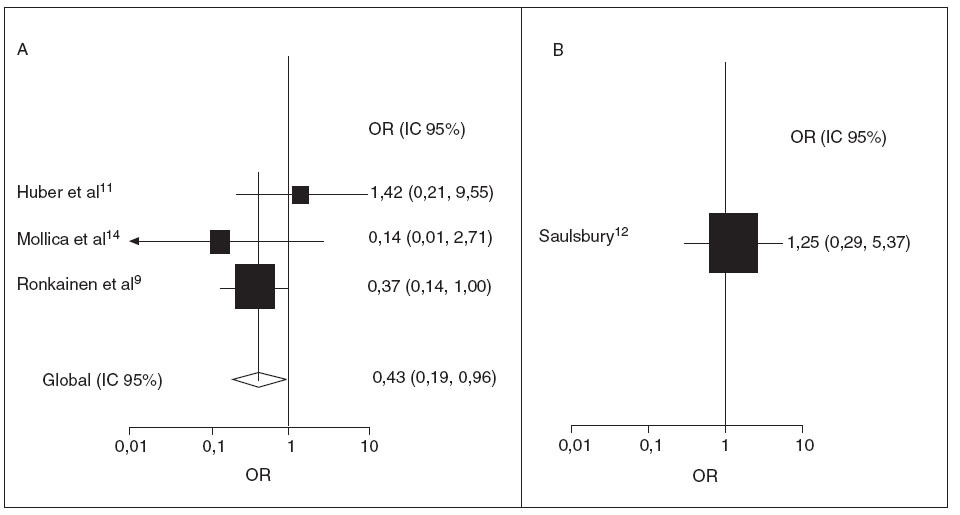
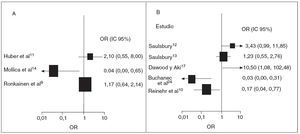
El tratamiento corticoideo temprano disminuyó significativamente las posibilidades de desarrollar una nefropatía persistente en los 3 estudios prospectivos8,10,13 (OR 0,43; IC 95%: 0,19, 0,96) (fig. 5A). No hubo pruebas de marcada heterogeneidad entre los estudios (p = 0,341). Además, no se encontraron indicios de sesgo de publicación (prueba de Egger, p = 0,99). El estudio retrospectivo de Saulsbury et al12 no mostró una diferencia estadísticamente significativa del resultado renal entre los pacientes expuestos y los no expuestos (OR 1,25; IC 95%: 0,29, 5,37) (fig. 5B).
Fig. 5. Tratamiento corticoide y posibilidades de nefropatía persistente. OR e IC 95% de afectación renal persistente tras el diagnóstico de PSH. A, prospectivo; B, retrospectivo. Para los estudios de Huber et al11 y de Mollica et al14 se utilizó un plazo de 1 año y para el de Ronkainen et al9 de 6 meses. El tamaño de la caja, en el cuadro A, es proporcional al inverso de la magnitud de la varianza. IC: intervalo de confianza; OR: odds ratio; PSH: púrpura de Schönlein Henoch.
Análisis de sensibilidad¿Importa la dosis de corticoides?
Investigamos si la dosis de corticoides afecta a la probabilidad de desarrollar una nefropatía persistente mediante modelos de regresión restringidos y no restringidos y la prueba de la razón de probabilidades. La tabla 2 muestra las dosis y la duración del tratamiento en cada estudio. Este análisis excluyó a 2 estudios por no indicar la dosis de corticoides20,23. La prueba de la razón de probabilidad no fue estadísticamente significativa (p = 0,07), por lo que señaló, pero no pudo identificar, un efecto significativo de proporcionalidad de respuesta a la dosis.
¿Qué futuro estudio revocará los hallazgos de este metaanálisis?
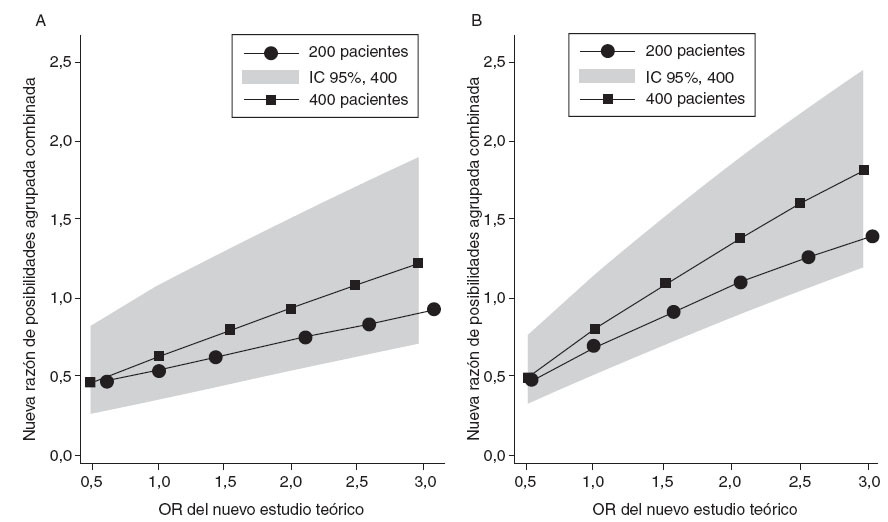
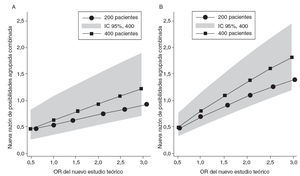
Se realizaron análisis de sensibilidad para determinar el tamaño de la muestra y la magnitud del efecto que necesitará un teórico estudio futuro para revocar los hallazgos de los estudios prospectivos respecto al beneficio del corticoide para disminuir la nefropatía persistente presentada en este metaanálisis. Realizamos análisis de sensibilidad mediante muestras teóricas de 200 y 400 pacientes y suponiendo una incidencia de afectación renal persistente del 5% y del 20% en el grupo de control (fig. 6). Si el riesgo inicial de afectación renal en los controles es del 5%, un nuevo estudio con 200 pacientes necesitaría un tamaño del efecto superior a una OR de 3 para que la OR agrupada llegase a 1. Un estudio con 400 pacientes necesitaría un tamaño de efecto superior a una OR de 2,25 para que la nueva OR agrupada llegase a 1; para que la nueva OR agrupada fuera estadísticamente significativa, el efecto de tamaño debería ser mayor que 3 (fig. 6A). Si el riesgo inicial de afectación renal en los controles es del 20%, la OR de un nuevo estudio con 200 pacientes debería ser mayor que 1,75 para aumentar la OR agrupada a 1 y mayor que 3,0 para conseguir la significación. Un nuevo estudio con 400 pacientes necesitaría una OR mayor que 1,4 para aumentar la OR agrupada a 1 y mayor que 2,25 para alcanzar la significación estadística (fig. 6B).
Fig. 6. Análisis de sensibilidad del tamaño del efecto de futuros estudios teóricos para la probabilidad de la afectación renal persistente. Nueva OR agrupada combinada frente a una OR de un teórico nuevo estudio con tamaño de muestra de 200 y 400. La prevalencia de afectación renal persistente en el grupo de control se calculó al 5% (A) o al 20% (B). IC: intervalo de confianza; OR: odds ratio.
DISCUSIÓNEsta revisión sistemática y resumen de los datos de 5 artículos elegibles indica que el tratamiento temprano con corticoides de los niños con PSH se asocia con un aumento estadísticamente significativo de la resolución del dolor abdominal a las 24 h y una disminución de las posibilidades de nefropatía persistente. Además, aun cuando los análisis carecieron de suficiente precisión estadística, la probabilidad de intervención quirúrgica y de recurrencia de PSH también puede disminuir. En conjunto, el patrón del efecto en los análisis tiende a favorecer el empleo de corticoides; ninguno de los análisis indica daño.
Esta revisión subraya la necesidad de un conocimiento más completo de las formas en que los corticoides inciden sobre el curso de la PSH, tanto en el marco agudo como en el crónico. En los años cincuenta se propuso por primera vez que los corticoides benefician a los niños con PSH, y son eficaces en el tratamiento de otras vasculitis de los niños y los adultos25. Los corticoides constituyen la piedra angular de la mayoría de las vasculitis juveniles, como el lupus eritematoso sistémico, la granulomatosis de Wegener, la poliarteritis nodosa y la arteritis de Takayasu. Por el contrario, se debate el tratamiento corticoide en la enfermedad de Kawasaki, otra vasculitis aguda infantil con posible morbilidad y mortalidad; un informe reciente no encontró efecto del corticoide26 mientras que otros anuncian los efectos beneficiosos de los corticoides27,28. Según esta información, ¿se debe administrar corticoides a los niños que acuden al hospital con una PSH de nueva aparición? La rigurosa respuesta a esta pregunta tendría sustanciales consecuencias clínicas. Pese al empleo generalizado de corticoides en las vasculitis, hasta ahora no hay acuerdo entre los médicos sobre si se debe administrar corticoides para la PSH, y en este caso, en qué indicaciones.
Las pruebas que presentamos tienen algunas limitaciones importantes. En primer lugar, la definición de afectación renal difirió entre los estudios, por lo que pudo captar distintas dimensiones o grados de la gravedad de la PSH. Por ejemplo, la definición de proteinuria en los 3 estudios prospectivos osciló entre 200 y 400 mg/l, y la de hematuria entre 5 y 10 hematíes por campo. En segundo lugar, los regímenes de dosificación y el modo de administración de los corticoides no fueron iguales en cada estudio (tabla 2). Al estratificar el tratamiento corticoide según dosis elevada frente a baja de corticoides para cada uno de los resultados clínicos no hubo diferencias estadísticas entre los 2 grupos (datos no ofrecidos). Aunque distintas dosis de corticoides o el método de administración (oral frente a i.v.) pueden afectar al tamaño de la disminución del riesgo, no es probable que estos cambios de dosis o vía inviertan la dirección de los efectos. En tercer lugar, los estudios no clasificaron de manera uniforme los casos de PSH como incidentes o recurrentes. Así pues, es posible que se haya agrupado inadecuadamente recurrencias graves con otras más leves, como una erupción aislada. Del mismo modo, dada la incertidumbre acerca de la pérdida de seguimiento, especialmente en el grupo tratado con corticoides, el efecto protector de los corticoides probablemente constituya una infravaloración.
Al interpretar estos datos se debe tener en cuenta otras dos limitaciones. En primer lugar, nuestra capacidad de extraer conclusiones robustas estuvo dificultada por el limitado número de pacientes en los estudios, lo que a menudo resultó en mediciones imprecisas de los efectos del tratamiento. Aunque el efecto del corticoide sobre varios de los resultados alcanzó un grado de beneficio estadísticamente significativo, el fallo en demostrar beneficio acerca de otros resultados y en mostrar un significativo efecto de proporcionalidad de respuesta a la dosis puede reflejar o bien la naturaleza, todavía relativamente carente de poder, de los estudios combinados existentes o bien una verdadera ausencia de impacto. En segundo lugar, los efectos apreciados en los estudios retrospectivos de observación probablemente incluyen cierto grado de confusión por indicación, por el que los pacientes con mayor gravedad de la enfermedad tuvieron más probabilidades de recibir corticoides. Dado que la mayoría de los estudios retrospectivos siguen mostrando un beneficio pese a todo, los resultados en todos los estudios son más tranquilizadores.
A pesar de estas precauciones, nuestros hallazgos indican que el posible beneficio de la administración temprana de corticoides en el curso de la enfermedad puede ser mayor que lo anteriormente sugerido, tanto en las complicaciones agudas (dolor, intervención quirúrgica) como en las crónicas (recurrencia, nefropatía) de la enfermedad. Si el tratamiento corticoide es verdaderamente tan eficaz como indica este metaanálisis, el más amplio empleo de corticoides probablemente disminuiría la hospitalización prolongada, el riesgo de cirugía o la nefropatía crónica y puede, por extensión, mostrarse beneficioso incluso en los casos aparentemente benignos en las mujeres que posteriormente desarrollan complicaciones durante el embarazo. Como demuestran los análisis de sensibilidad, nuestros hallazgos acerca del posible beneficio de los corticoides para disminuir la nefropatía crónica son robustos; para revocar nuestros hallazgos no sólo sería necesaria una muestra mayor que las de cualquier estudio publicado hasta la fecha sobre PSH, sino que debería mostrar una razón de posibilidades de daño por la administración de corticoides superior a 2,25, lo que es poco probable. Para evaluar todos los resultados clínicamente relevantes son necesarios estudios retrospectivos mejor diseñados con normalización de la exposición a corticoides teniendo en cuenta la probabilidad de que cualquier paciente reciba corticoides, y ensayos prospectivos, aleatorizados controlados de mayor tamaño. El conocimiento originado en estos estudios es esencial para guiar nuestras intervenciones en el curso temprano de la PSH y mejora los resultados del paciente, tanto en los niños como en los adultos.
AGRADECIMIENTOSPamela Weiss está financiada, en parte, por una T32 en farmacoepidemiología de los NIH.
Los autores agradecen la traducción de resúmenes y artículos a: Frank Pessler, Eric Hanson, Alba Hanson, Jan Boswinkel, Keri Cohn, Eva Lynch, Anna Genin, Kaoru Saijo y Lorenza Frisoni. Los autores también dan las gracias a David D. Sherry y James Guevara por su lectura crítica de este manuscrito.
Correspondencia: Pamela F. Weiss, MD, Division of Rheumatology, Children’s Hospital of Philadelphia, Children’s Seashore House Room 236, 34th and Civic Center Boulevard, Filadelfia, PA 19104-4399, Estados Unidos.
Correo electrónico: weisspa@email.chop.edu