Tras la aprobación del activador de plasminógeno tisular recombinante para el tratamiento del accidente cerebrovascular (ACV) isquémico en su fase aguda en el año 1995, el siguiente gran hito en el tratamiento de esta patología en su fase aguda fue el advenimiento de la trombectomía mecánica (TM). Sin embargo, la experiencia con dicho tratamiento en nuestro país ha sido escasamente reportada.
ObjetivoOfrecer un resumen de nuestra experiencia en el tratamiento del ACV isquémico con TM en un centro de alta complejidad en la Ciudad de Buenos Aires, Argentina.
PacientesSe describen los antecedentes, características clínicas y evolución de 11 pacientes sometidos a TM como parte del tratamiento del ACV isquémico en su fase aguda.
ResultadosEn nuestra serie de pacientes la tasa de recanalización exitosa con la TM fue del 73%, alcanzando un 80% para los dispositivos stent retriever. La mortalidad a los 3 meses fue del 27,3%.
ConclusionesLa tasa de recanalización de nuestra serie se aproximó a la reportada en la bibliografía. El desafío a futuro implicará incentivar políticas de salud, con el objetivo de sistematizar la atención en la fase prehospitalaria y hospitalaria, dado que la TM requiere de una adecuada implementación previa de la trombólisis sistémica.
After the approval of recombinant tissue plasminogen activator for the treatment of ischemic stroke (IS) in its acute phase in the year 1995, the next milestone was the advent of mechanical thrombectomy (MT), which received the highest recommendation grade in the latest Guidelines of the American Stroke Association. However, the experience with this treatment in our country has been scarcely reported.
ObjectiveTo present our experience with MT in the treatment of acute IS in a high-complexity medical center in the city of Buenos Aires, Argentina.
PatientsThis paper describes the relevant medical backgrounds, clinical features and outcomes of 11 patients that received MT as a part of the treatment of acute IS.
ResultsIn our series, the global successful recanalization rate was 73%, and when considering stent retriever devices alone, it rose to 80%. The 90-day mortality was 27.3%.
ConclusionsThe successful recanalization rate in our patients was comparable to the rate reported in the literature. The next challenge implies promoting health policies aimed at systematizing the medical care in the pre-hospital and hospital settings, given that the use of MT at a given institution requires the adequate previous implementation of systemic intravenous thrombolysis.
El accidente cerebrovascular (ACV) constituye la cuarta causa de muerte y la primera causa de morbilidad en Argentina1. En el año 1995, se publica el primer estudio que demuestra la utilidad del uso de activador tisular del plasminógeno (TPA) por vía intravenosa para reducir el grado de discapacidad con una ventana terapéutica de 3 h desde el inicio de los síntomas2, y en el año 2008 el estudio ECASS-3 aporta evidencia de su efectividad en la llamada «ventana extendida» (ACV isquémico entre 3 y 4,5 h de evolución)3. Tiempo después se observó que el beneficio del TPA era mayor en pacientes con ACV que no presentaban obstrucciones proximales del polígono de Willis o de la carótida interna intracraneana4. Esto motivó el desarrollo de terapias endovasculares para el tratamiento de estos pacientes. Recientemente, la publicación de 5 ensayos clínicos (MR-CLEAN5, ESCAPE6, EXTEND-IA7, REVASCAT8 y SWIFT-PRIME9) evidenció beneficio de la trombectomía mecánica (TM) por vía endovascular con una ventana de 6 hasta 12 h (de acuerdo con distintos criterios de inclusión de cada estudio), luego de la aplicación del TPA en pacientes con obstrucciones arteriales proximales del circuito anterior cerebral. La TM también constituye una terapia alternativa en los pacientes con contraindicación para el uso del TPA y que presentan un ACV con evidencia de obstrucción proximal en las imágenes.
En la Argentina, la terapia trombolítica sistémica tiene serias dificultades para su implementación en la práctica habitual; 2 registros nacionales de base hospitalaria (ARENAS10 y RENACER11) demostraron que solamente del 1 a 1,2% de los pacientes acceden a ese tratamiento. Vale la pena aclarar que esta terapia se emplea fundamentalmente en centros privados, como lo demuestra el registro ARENAS. La experiencia con TM es aún menor en nuestro medio; son pocas las instituciones que actualmente realizan dicho procedimiento para los pacientes que persisten con obstrucción arterial luego del TPA sistémico.
ObjetivoReportar el uso de la TM como tratamiento del ACV isquémico en un hospital universitario de alta complejidad en Argentina.
Pacientes y métodosSe analizó en forma retrospectiva los pacientes con ACV isquémico que se les efectuó una TM en el Hospital Italiano de Buenos Aires. Se registraron los siguientes datos a partir de la historia clínica electrónica: edad, sexo, factores de riesgo vascular, tiempo transcurrido entre inicio de los síntomas e inicio de TM, el Alberta Stroke Program Early CT score (ASPECTS)12 de la tomografía cerebral de ingreso, el CTA-Score13 (puntaje de angiotomografía) de ingreso, el empleo de TPA previo a la TM, la National Institute of Health Stroke Scale (NIHSS)14 previa a la TM, el sitio de obstrucción, el grado de recanalización posterior mediante la escala Thrombolysis in Cerebral Infarction score (TICI)15 y la Modified Rankin Scale (mRS)16 a los 90 días.
Definición de escalas y puntajes- –
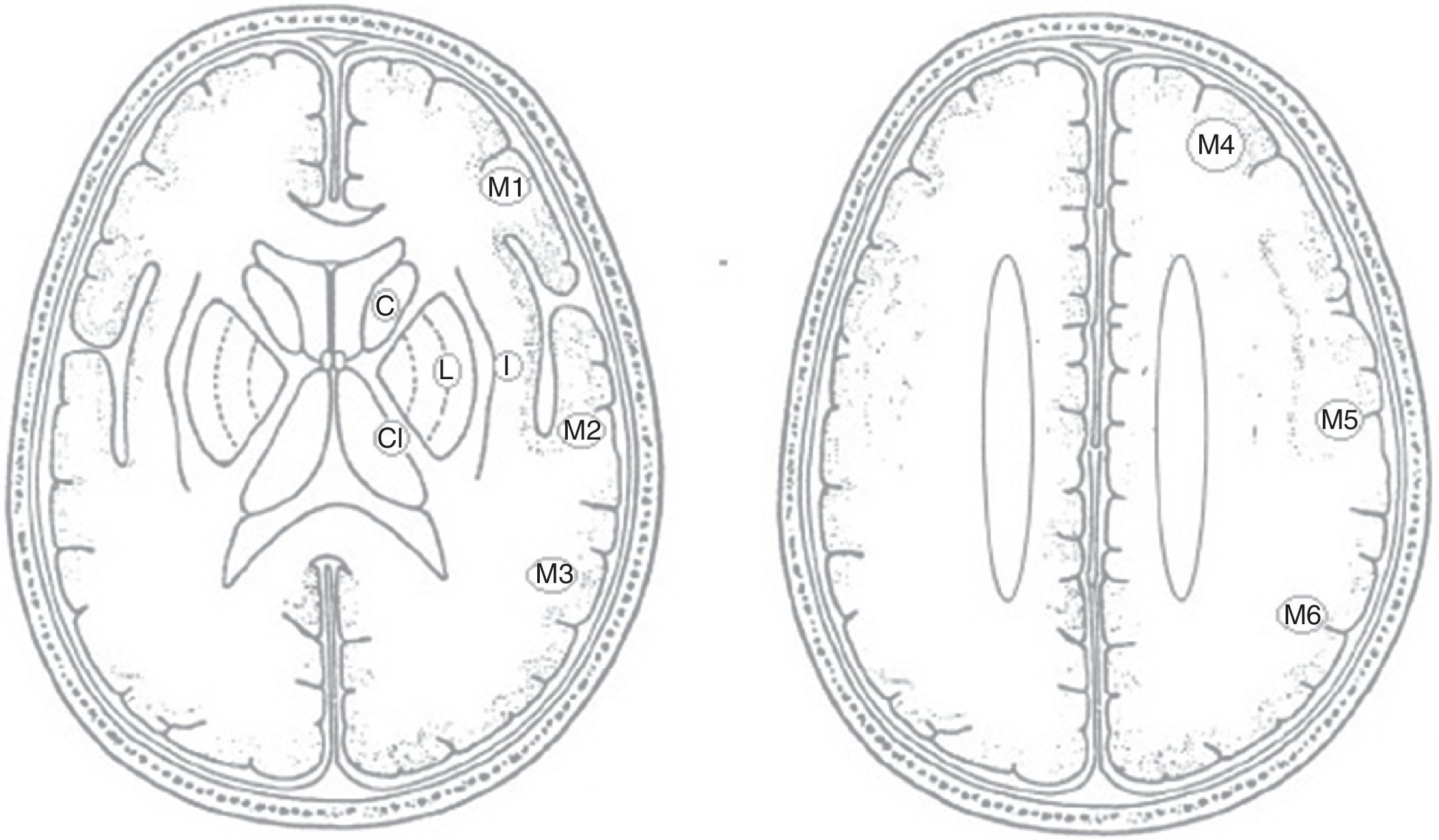
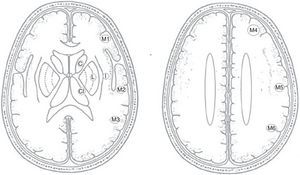
ASPECTS: sistema de puntaje empleado para establecer la presencia de cambios radiológicos precoces en la tomografía cerebral en pacientes con ACV isquémico (en el territorio de la arteria cerebral media) en su fase hiperaguda. El puntaje ideal que corresponde a la ausencia de cambios precoces es 10. En 2 cortes tomográficos, uno a la altura de los ganglios basales y otro a la altura de los centros semiovales, se definieron 10 puntos anatómicos: cabeza del núcleo caudado, cápsula interna, núcleo lenticular, ínsula y 6 regiones del territorio córtico-subcortical de la arteria cerebral media (fig. 1). Por cada territorio que presenta hipodensidad se le sustrae un punto al puntaje inicial ideal. A menor puntaje, más territorios demostrarán cambios isquémicos precoces.
Figura 1.Planos de corte de la escala de ASPECTS.
C: cabeza del núcleo caudado); CI: cápsula interna; I: ínsula; L: núcleo lenticular.
Tomado de: http://www.aspectsinstroke.com/training-for-aspects/test/
- –
CTA-Score: sistema de puntaje que observa el grado de vasos colaterales permeables. Se clasifica en grado 0 (sin ningún vaso colateral abierto), 1 (los vasos colaterales abiertos rellenan ≤ 50% del territorio de la arteria cerebral media ocluida proximalmente), 2 (los vasos colaterales abiertos rellenan > 50% pero<100% del territorio de la arteria cerebral media ocluida proximalmente) y 3 (los vasos colaterales rellenan el 100% de la arteria cerebral media ocluida proximalmente).
- –
Escala TICI: sistema de puntaje que categoriza el grado de reperfusión de un vaso tras una intervención trombolítica en el contexto de un ACV. Los puntajes son: 0 (sin flujo anterógrado), 1 (flujo que es posterior a la oclusión, pero sin reperfusión tisular), 2A (reperfusión tisular parcial en<66% del territorio de la arteria ocluida), 2B (reperfusión tisular completa del territorio de la arteria ocluida pero enlentecida respecto a la arteria homóloga contralateral) y 3 (reperfusión tisular completa y sin retraso).
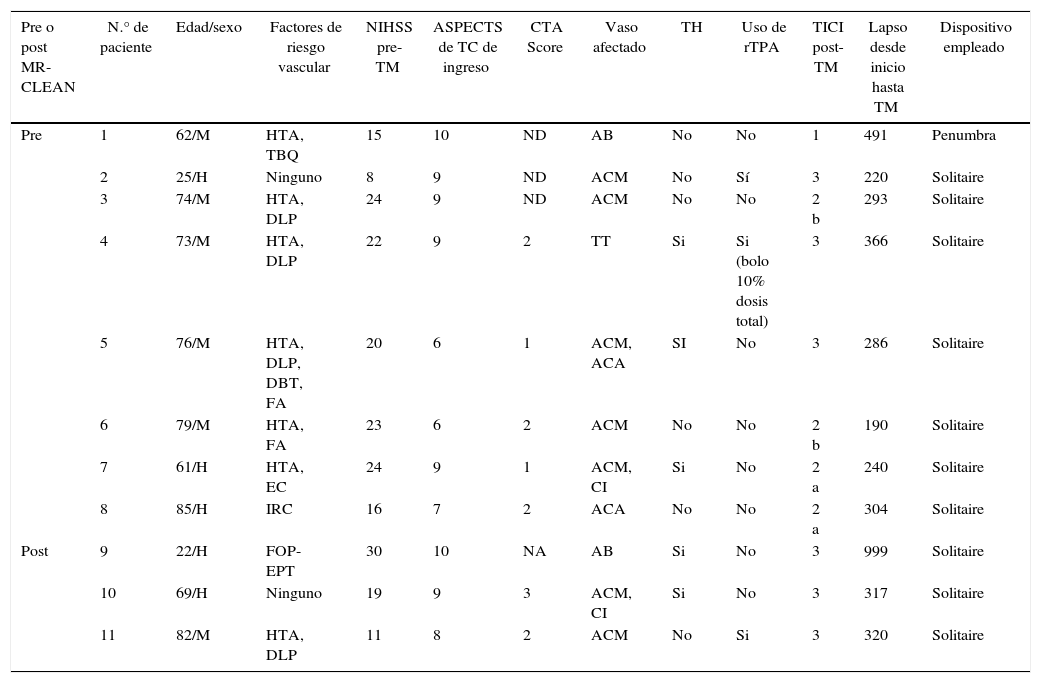
Sobre un total de 410 pacientes ingresados con diagnóstico de ACV isquémico desde octubre del 2013 hasta diciembre del 2015, el 2,6% (n=11) de los casos cumplieron criterios para TM. En la tabla 1 se resumen las características clínicas y de imágenes de los casos que fueron sometidos a TM como parte del tratamiento del ACV isquémico, presentados en orden cronológico. La edad promedio de los pacientes fue de 64±21 años y el 55% fueron mujeres. El NIHSS promedio antes de la TM fue de 19±6 y el puntaje ASPECTS promedio fue de 8±1. El 82% de los pacientes (n=9) presentaba oclusiones en el circuito anterior y en 7 de ellos se pudo estimar un puntaje CTA-Score (6 de estos pacientes presentaban puntaje de 1-2 y el paciente restante fue 3). El 45% de los pacientes (n=5) presentó un sangrado posterior a la TM. Los últimos 3 pacientes de la tabla 1 fueron tratados antes de conocerse los resultados del estudio MR-CLEAN.
Características clínicas y de imágenes de los pacientes con TM
| Pre o post MR-CLEAN | N.° de paciente | Edad/sexo | Factores de riesgo vascular | NIHSS pre-TM | ASPECTS de TC de ingreso | CTA Score | Vaso afectado | TH | Uso de rTPA | TICI post-TM | Lapso desde inicio hasta TM | Dispositivo empleado |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Pre | 1 | 62/M | HTA, TBQ | 15 | 10 | ND | AB | No | No | 1 | 491 | Penumbra |
| 2 | 25/H | Ninguno | 8 | 9 | ND | ACM | No | Sí | 3 | 220 | Solitaire | |
| 3 | 74/M | HTA, DLP | 24 | 9 | ND | ACM | No | No | 2 b | 293 | Solitaire | |
| 4 | 73/M | HTA, DLP | 22 | 9 | 2 | TT | Si | Si (bolo 10% dosis total) | 3 | 366 | Solitaire | |
| 5 | 76/M | HTA, DLP, DBT, FA | 20 | 6 | 1 | ACM, ACA | SI | No | 3 | 286 | Solitaire | |
| 6 | 79/M | HTA, FA | 23 | 6 | 2 | ACM | No | No | 2 b | 190 | Solitaire | |
| 7 | 61/H | HTA, EC | 24 | 9 | 1 | ACM, CI | Si | No | 2 a | 240 | Solitaire | |
| 8 | 85/H | IRC | 16 | 7 | 2 | ACA | No | No | 2 a | 304 | Solitaire | |
| Post | 9 | 22/H | FOP- EPT | 30 | 10 | NA | AB | Si | No | 3 | 999 | Solitaire |
| 10 | 69/H | Ninguno | 19 | 9 | 3 | ACM, CI | Si | No | 3 | 317 | Solitaire | |
| 11 | 82/M | HTA, DLP | 11 | 8 | 2 | ACM | No | Si | 3 | 320 | Solitaire |
AB: arteria basilar; ACA: arteria cerebral anterior; ACM: arteria cerebral media; ASPECTS: Alberta Stroke Program Early CT Score; CI: carótida interna; CTA score: Computed Tomography Angiography Score; DBT: diabetes; DLP: dislipidemia; EC: enfermedad coronaria; EPT: estado protrombótico; FA: fibrilación auricular; FOP: foramen oval permeable; H: hombre; HTA: hipertensión arterial; IRC: insuficiencia renal crónica; M: mujer; NA: no aplicable; ND: no disponible; NIHSS: National Institute of Health Stroke Scale; TC: tomografía computarizada cerebral; TH: transformación hemorrágica; TICI: Thrombolysis in Cerebral Infarction; TM: trombectomía mecánica; TT: trombo en T.
Para el análisis de los tiempos se excluyó el caso 9, ya que el mismo fue una trombosis total de la arteria basilar en un paciente joven, al cual se le realizó la TM con una ventana de 16 h, como terapia compasiva independientemente de la recomendación de las guías. El promedio de tiempo entre el inicio de los síntomas y la recanalización fue de 302±84 min y el tiempo puerta-inicio de trombectomía fue de 156±48 min.
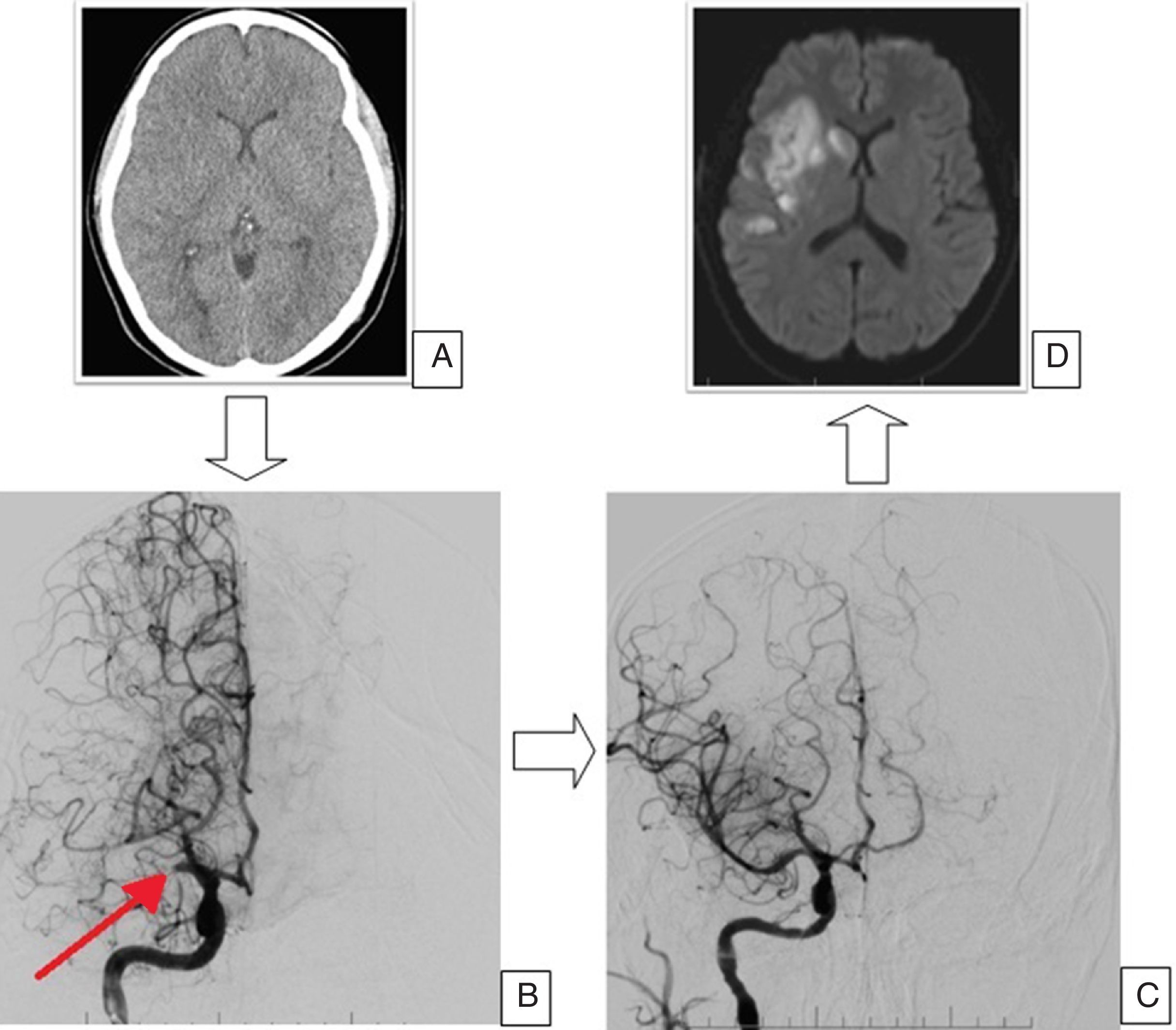
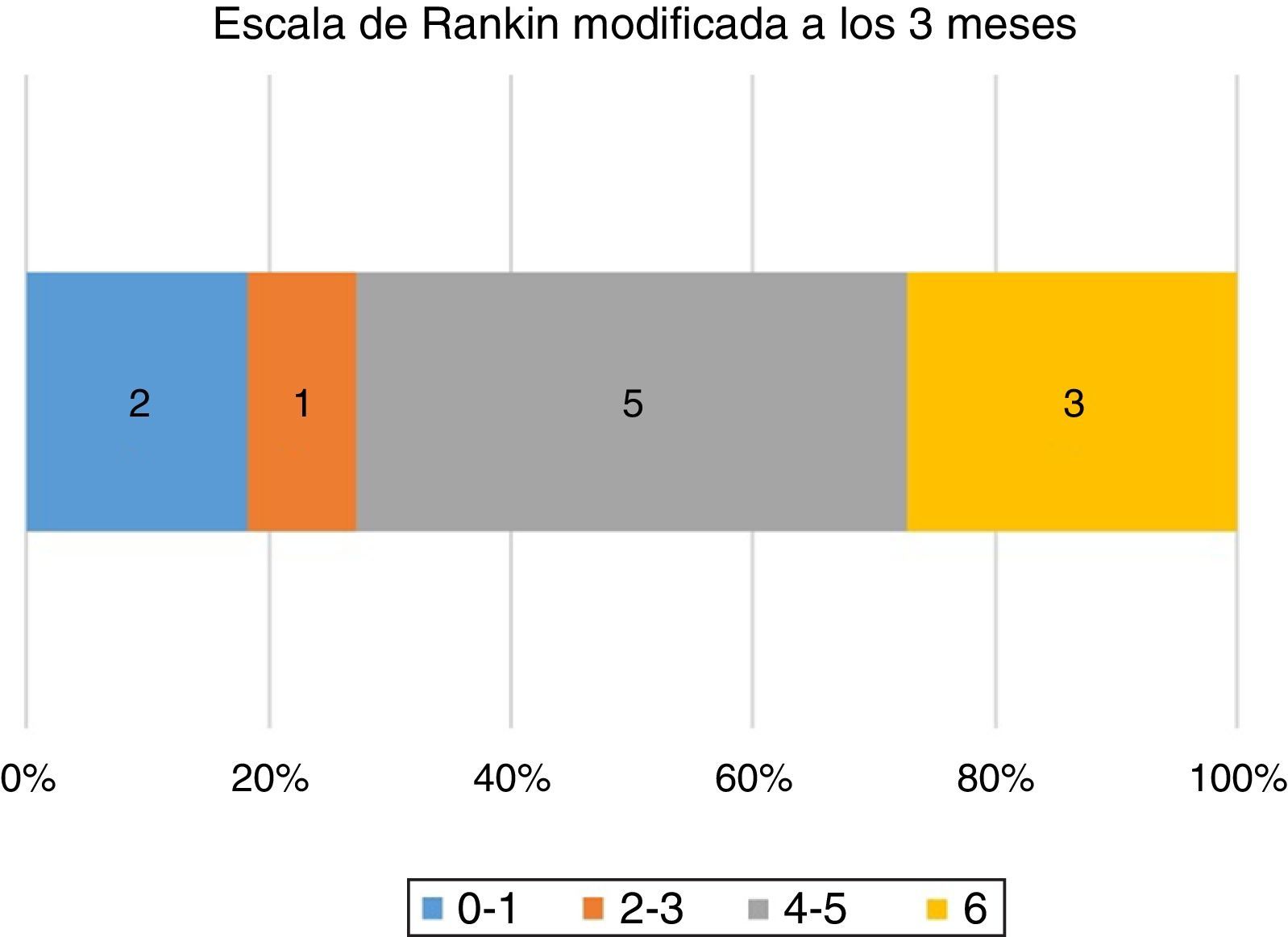
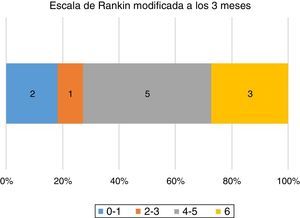
En 8 pacientes (73%) se logró una recanalización exitosa (definida como un grado 2B o 3 de la escala TICI). En el 91% de los pacientes se empleó el dispositivo Solitaire (la tasa de recanalización exitosa con dicho dispositivo fue del 80%). Dos pacientes recibieron TPA en dosis completa de acuerdo con las recomendaciones actuales, como se muestra en la tabla 1 (uno de los casos se detalla en la figura 2). En un paciente se empleó TPA en dosis «puente» (10% de la dosis total calculada por peso) antes de la TM, dado que tras la demora a la admisión y el lapso transcurrido para realizar estudios pertinentes, se hallaba próxima a terminar la ventana extendida (este único caso ocurrió antes de la publicación del estudio MR-CLEAN5). La mortalidad a los 3 meses fue del 27,3% (3 pacientes). El puntaje mRS a los 90 días se halla representado en la figura 3.
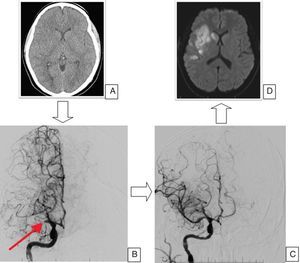
Caso clínico radiológico. Paciente de 26 años que presenta debilidad en el hemicuerpo izquierdo de 30 min de evolución. NIHSS al ingreso de 12 puntos. Trombólisis sistémica seguida de trombectomía mecánica. NIHSS al alta de 0 puntos. A) Tomografía de cerebro sin contraste. Borramiento del núcleo lenticular derecho. B) Angiografía digital cerebral. Inyección de carótida interna derecha. Amputación proximal de la arteria cerebral media derecha. C) Angiografía digital cerebral. Inyección de carótida interna derecha posterior a trombectomía mecánica. Recuperación del flujo distal (TICI 3). D) Resonancia magnética cerebral. Secuencia de difusión. Volumen final del infarto.
La instauración de la terapia trombolítica en el ACV isquémico constituyó un punto importante en la historia de la enfermedad para disminuir el grado de discapacidad. El tratamiento del ACV isquémico se tornó una tarea multidisciplinaria y que requiere de profesionales idóneos disponibles las 24 h del día, además de cierta infraestructura. Se estableció la importancia en la cadena de atención. Esto incluye el reconocimiento precoz de los síntomas, la notificación temprana a los sistemas de urgencia, el traslado rápido a un centro asistencial de complejidad y, por último, la importancia de tener protocolos de tratamiento en el hospital con el objetivo de completar los estudios y el tratamiento en menos de 1 h. En la Argentina, al igual que en otros países, la implementación del tratamiento con TPA no fue fácil. En un relevamiento publicado en el año 201517, en Argentina, con un total de 26 centros con capacidad operativa para la realización de trombólisis endovenosa, 14 de ellos se concentran en 4 provincias, poniendo de manifiesto la desigualdad en la distribución geográfica de los recursos. Los 2 principales registros de ACV con base hospitalaria en nuestro país, el ARENAS (2003) y el RENACER (2008), mostraron dificultades en el estudio y la evaluación inicial de los pacientes, con una baja tasa de indicación de terapia trombolítica. En la actualidad, el registro ARENAS realiza un nuevo relevamiento sobre las características de la atención del ACV en las primeras 24 h. En la década pasada se trabajó en la concientización de la población en relación con los síntomas del ACV y la Sociedad Neurológica Argentina18 y la Sociedad Argentina de Cardiología19 publicaron guías de tratamiento de la patología. Desde hace 20 años20 en nuestro hospital se desarrolla un programa de trombólisis sistémica en el ACV el cual funciona las 24 h los 7 días de la semana. La implementación de la TM es más reciente y se desarrolló a partir de observar una peor evolución de los pacientes que presentaban una obstrucción proximal. Estos pacientes cursan con formas clínicas más graves con NIHSS de más de 10 puntos. La TM consiste en la lisis del trombo por medios físicos (disrupción, aspiración, extracción con stents recuperables) en los segmentos proximales de las principales ramas del polígono (segmentos A1, M1, M2 y P1), carótida interna intracerebral y en la arteria basilar. El dispositivo Merci© (Concentric Medical Inc., California, Estados Unidos de América) fue el primero en obtener aprobación por la Food and Drugs Administration de Estados Unidos. Siguieron, en orden de aparición, los dispositivos Penumbra© (Penumbra Inc., California, Estados Unidos de América), Solitaire© (eV3 Endovascular) (Micro Therapeutics Inc., California, Estados Unidos de América) y Trevo Pro© (Stryker neurovascular, California, Estados Unidos de América). En el año 2012 fueron publicados 2 ensayos clínicos, el SWIFT y el TREVO 2; en ambos se evidenció la superioridad de los dispositivos Solitaire y Trevo Pro frente al dispositivo Merci, mientras que ningún estudio comparó directamente estos 2 dispositivos con el Penumbra. En el año 2013 se publican los ensayos SYNTHESIS21, IMS III22 y MR RESCUE23, enfocados a comparar la evolución en pacientes tratados exclusivamente con TPA por vía intravenosa con aquellos que eran sometidos a TM, con o sin uso previo de TPA. Estos 3 ensayos empleaban diversos tipos de dispositivos, no era necesario demostrar la obstrucción para la asignación del tratamiento y los tiempos de recanalización fueron muy prolongados en la rama de tratamiento endovascular. Lo previamente mencionado podría haber influenciado en los resultados negativos para el uso de la TM. El MR RESCUE incluyó a pacientes hasta las 8 h de evolución, mientras que el SYNTHESIS lo hizo hasta las 4 h y media. La guía de tratamiento del ACV publicada por la American Stroke Association (ASA) en el año 2013, luego de la publicación de los estudios SWIFT, TREVO 2 e IMS III, recomienda la TM para pacientes con contraindicación para recibir TPA (recomendación clase iia, nivel de evidencia C). Es una alternativa razonable cuando el paciente con obstrucción de gran vaso intracraneal no respondió al TPA por vía intravenosa (recomendación clase iib, nivel de evidencia B)24. De la comparación directa entre los stent retriever y los dispositivos tipo Merci y Multi-Merci, se objetivó superioridad de los primeros con evidencia clase 1, nivel A.
En los últimos 2 años 5 ensayos clínicos (MR-CLEAN5, ESCAPE6, EXTEND-IA7, REVASCAT8 y SWIFT-PRIME25) mostraron el beneficio del uso de la TM en pacientes con ACV isquémico que persisten con obstrucción proximal de circulación anterior luego del uso de TPA sistémico. En estos estudios se utilizó mayormente dispositivos de tipo stent retriever luego del tratamiento con TPA por vía intravenosa en dosis plena; la evaluación inicial de las imágenes en la mayoría de los trabajos incluyó un protocolo de CTA-score para la detección de obstrucciones proximales y esto permitió acortar los tiempos a la recanalización. Con el uso de los dispositivos tipo stent retriever se apreció un mayor grado de recanalización que con otros dispositivos, así como una menor incidencia de sangrado intracraneal26. Actualmente, y en función del análisis de estos estudios, la TM constituye una indicación de clase 1 y nivel A en los siguientes criterios: mRS previa al evento de 0-1, pretratamiento con TPA dentro de las 4 h y media de evolución, oclusión de la arteria cerebral media en su segmento M1 o carótida interna intracraneana, edad ≥ 18 años, NIHSS ≥ 6, ASPECTS ≥ 6 e inicio de la TM dentro de las 6 h del inicio del cuadra. Los pacientes que cumplen los criterios previamente mencionados representan entre el 5 y el 8% del total de los pacientes que ingresan con ACV en el periodo de ventana25.
En nuestro centro, desde el año 2013 se inició el uso de TM en los pacientes con obstrucciones proximales. La mayoría de los casos de nuestra serie fueron del territorio anterior y en pacientes con un NIHSS superior a 10 puntos. Salvo 2 pacientes, a los cuales se les administró dosis completa de TPA previamente (y tuvieron buena evolución, quedando con mRS de 0 y 1, respectivamente), el resto de los casos fue TM directa. Los tiempos internos fueron similares a lo reportado en la literatura. En un caso se empleó el dispositivo Penumbra, mientras que en los 10 casos restantes el dispositivo utilizado fue el Solitaire©, el cual ya había mostrado superioridad en comparación con el Merci o Multi-Merci27. El 73% de los pacientes (8 de los 11) sometidos a TM demostraron una recanalización exitosa, pero si se analiza la tasa de recanalización exitosa en los casos en los que se empleó un dispositivo stent retriever, la misma asciende al 80%: esto se halla próximo al 84,5% de tasa de recanalización reportada en un metaanálisis de 20 ensayos que emplearon dispositivos stent retriever27.
La implementación de este tipo de terapia en el ACV isquémico es compleja, tanto para países desarrollados, como para economías en vías de desarrollo. Un análisis de los resultados del programa Get With The Guidelines, enfocado en la optimización de la terapia trombolítica en los Estados Unidos, observó que la proporción de hospitales que ofrecían tratamiento endovascular aumentó del 12,9% en el año 2003 al 28,9% en el año 2013, lo que significa que menos de un tercio de las instituciones ofrecen este tratamiento en la actualidad28. En nuestro país esta situación es aún peor, existiendo una distribución asimétrica de los recursos en salud para la atención de este tipo de pacientes. En nuestro hospital, la protocolización de la trombólisis sistémica acortó los tiempos de evaluación y diagnóstico de los pacientes con ACV. En forma paralela, y en concordancia con los trabajos más recientes de TM, se implementó la evaluación del árbol vascular durante la imagen inicial del ACV, tanto en protocolos de tomografía como de resonancia magnética. Esto permitió acortar los tiempos y poder realizar la TM en menos de 6 h en la gran mayoría de los pacientes.
El desafío a futuro implicará incentivar políticas de salud que obren en virtud de la evidencia científica e implementen estándares de atención del ACV isquémico agudo, tanto a nivel público como privado, con el objetivo de sistematizar la atención en la fase prehospitalaria y hospitalaria. Esto es indispensable dado que la TM requiere de una adecuada implementación previa de la trombólisis sistémica. La TM no reemplaza a la trombólisis sistémica, dado que la evidencia actual demuestra que se complementan, siendo de elección para un escaso número de pacientes con formas clínicas graves y obstrucción proximal.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.