La revisión 2010 de criterios McDonald (RC2010) para esclerosis múltiple (EM) lleva a implicaciones importantes al aplicarse en síndromes clínicamente aislados(SCA), modificándose evidencias paraclínicas de diseminación en espacio (DE) y tiempo (DT).
ObjetivosEvaluar: a) el diagnóstico de EM aplicando estos criterios en pacientes con SCA; y b) las implicaciones que causa la RC2010 en los SCA al aplicarse en ellos.
Material y métodosSe analizaron retrospectivamente 51 SCA típicos ocurridos desde el año 2001 seguidos hasta 2010 inclusive; a todos se les realizó imagen de resonancia magnética (basal) (IRMB) de cerebro, sin y con gadolinio, evaluándose en ellas quiénes cumplían DE según los criterios de Barkhof y Tintoré.
Retrospectivamente se estratificaron los mismos SCA aplicando la RC2010.
ResultadosDe 51 SCA —edad media 32 años— hubo 36 mujeres (70,6%), 48 con SCA de tipo monofocal (94%) y 31 (60,8%) con alto riesgo de conversión (ARC). Aplicando retrospectivamente la RC2010 se obtuvo que de 31 SCA con ARC 11 (35,5%) cumplían criterios de DE y DT en IRMB.
ConclusionesAplicando RC2010 aumentó la sensibilidad para un diagnóstico precoz de EM al haber un 35,5% de pacientes con SCA que ya eran EM convertidos por IRMB desde el primer ataque.
La RC2010 lleva a implicaciones (entre otras) consistentes de que existen pacientes con SCA convertidos de entrada.
Ante un paciente con SCA típico y una IRMB cumpliendo criterios de DE y DT se puede establecer el diagnóstico de EM con un valor predictivo positivo del 79%. Se postula una clasificación de los SCA según IRMB.
2010 Revisions to the McDonald Criteria (2010RMcDC) for diagnosis of multiple sclerosis (MS) lead to important implicances when it applies in the clinically isolated syndromes (CIS), modifying paraclinical evidences of dissemination in space (DIS) and time (DIT).
ObjetivesEvaluate: a) the diagnosis of MS applying these criteria in patients with CIS; and b) the implicances that causes the 2010RMcDC in the CIS when it applies in them.
Material and methodsThere have been analysed retrospectively 51 typical CIS, that took place from year 2001 and followed up to 2010 inclusive.Initial magnetic resonance image (IMRI) of brain without and with gadolinium was made to all of them, evaluating who fulfilled DIS according to criteria of Barkhof and Tintoré. Retrospectively the same CIS were stratified applying the 2010RMcDC.
ResultsFrom 51 CIS (mean 32 years) there were 36 women (70,6%),48 monofocal CIS (94%) and 31 (60,8%) with higher risk of conversion.
Applying retrospectively the 2010RMcDC it was obtained that from 31 CIS with higher risk of conversion, 11 (35,5%) fulfilled criteria of DIS and DIT in the IMRI.
ConclusionsApplying 2010RMcDC increased the sensitivity for an early diagnosis of MS because there were 35,5% of patients with CIS who already were MS converted by IMRI from the first clinical demyelinating event. The 2010RMcDC lead to implicances (between others) which consider that exist patients with CIS converted from the beginning. In the presence of patients with typical CIS and a IMRI that fulfill DIS and DIT criteria it is possible to establish the diagnosis of MS with a positive predictive value of 79%. Besides this leads to classification of the CIS according to IMRI.
Los criterios diagnósticos (CD) en Medicina surgen y basan su utilidad cuando no existe una prueba diagnóstica segura o un marcador específico de una enfermedad. Los mismos dan un marco de diagnóstico probable interpretando los síntomas y signos clínicos o de estudios complementarios que presentan los pacientes en distintas patologías.
Los CD a través del tiempo pueden modificarse a la luz de la aparición de nuevos conocimientos de una enfermedad.
Esto es lo que ha sucedido en la esclerosis múltiple (EM); los CD de esta enfermedad han ido evolucionando o modificándose a través del tiempo hasta llegar a la revisión de CD realizada en marzo de 2010 (RC2010)1. En ellos se han modificado las evidencias paraclínicas que se requieren con el fin de demostrar la diseminación en el espacio (DE) y en el tiempo (DT) en los síndromes clínicamente aislados (SCA).
Los SCA, también conocidos como clinically isolated syndromes (CIS), también se denominan síndromes desmielinizantes aislados (SDA) e incluso evento desmielinizante inicial (EDI), esta última denominación para West et al.2 identifica mejor el primer episodio de EM, pues se considera en el comienzo su localización y severidad. Así el término EDI caracteriza el comienzo de EM recaída-remisión, pudiendo ser la presentación y clasificando la misma en: monosintomática, polisintomática o polirregional, reflejando la heterogeneidad de la EM2,3.
El término SCA/CIS para algunos expertos es inadecuado4 porque engloba distintas situaciones de presentación clínica, y el mismo ha sido empleado en grupos variables de pacientes con:
- 1.
Un único evento clínico y signos que indican solamente una única lesión (de este modo existe diseminación aislada en el espacio y en el tiempo).
- 2.
Episodios recurrentes en una única localización (así habrá diseminación aislada en el espacio, pero no en el tiempo, por ejemplo: las neuritis ópticas recurrentes)5.
- 3.
Un único evento clínico, pero que los hallazgos del examen neurológico sugieren la presencia de 2 o más lesiones en lugares separados (así habrá diseminación aislada en el tiempo, pero no en el espacio).
Por estas ambigüedades en la denominación e interpretación hay opiniones2 o acuerdo de expertos4 en que un SCA puede ser definido como una presentación monofásica, con alta sospecha del comienzo de una enfermedad desmielinizante inflamatoria.
Una presentación monofásica implica un único y primer episodio clínico neurológico de relativa rápida aparición (agudo/subagudo) que dura más de 24 h. Presentaciones simultáneas múltiples clínicas o paraclínicas que representan DE también son posibles, aunque la DT no debería ser evidente4. Dos tipos de SCA pueden definirse en función de la presentación topográfica clínica: monofocales o multifocales, y si a ello le agregamos las evidencias que puedan aparecer en la primera resonancia o imagen de resonancia magnética basal (IRMB) tendremos 4 tipos de SCA según la clasificación de Miller D et al.4:
- 1.
SCA tipo i: clínica monofocal y en la IRMB al menos una lesión asintomática
- 2.
SCA tipo ii: clínica multifocal y en la IRMB al menos una lesión asintomática.
- 3.
SCA tipo iii: clínica monofocal e IRMB normal (sin lesiones asintomáticas).
- 4.
SCA tipo iv: clínica multifocal e IRMB normal (sin lesiones asintomáticas).
Las lesiones asintomáticas en la IRM deben ser típicas de desmielinización y en lugares también típicos para EM.
Esta clasificación de Miller et al. también agrega otro tipo de SCA (tipo v), en el que no existe una presentación clínica sugestiva de enfermedad desmielinizante; son pacientes que no tienen síntomas, o si los tienen no son específicos de EM (por ejemplo cefalea), pero en cambio en la IRM se evidencia anormalidades típicas de desmielinización. Esta situación clínica radiológica también se conoce como síndrome radiológicamente aislado.
Los SCA tipo i y ii son los que tienen mayor alto riesgo de conversión a EM.
Existen otras definiciones de SCA: trastorno agudo/subagudo neurológico que traduce lesión de la sustancia blanca que dura más de 24 h, primera manifestación clínica de inflamación de la mielina con evidencias de daño axonal o primer ataque desmielinizante sugestivo de EM.
Las presentaciones más comunes de aparición de los SCA son las que involucran al nervio óptico, la médula espinal y el tronco encefálico; otros síndromes aislados pueden ocurrir, como aquellos que afectan a los hemisferios cerebrales (por ejemplo hemiparesia)4.
Miller et al.4 establecen 3 categorías clínicas de presentación de los SCA con síntomas y signos correspondientes a cada una de ellas: a) SCA llamado típico: es aquel que se presenta con genuinos síntomas y signos correspondientes a EM; b) SCA con presentaciones menos comunes para EM; y c) SCA atípicos con presentaciones que difícilmente correspondan a EM.
En otra publicación referente a la presentación de los SCA de Kelly et al.6, estos autores refieren que los SCA atípicos tienen una sensibilidad del 84%, una especificidad del 90% y un cociente de probabilidad positiva de 8,4, así como un cociente de probabilidad negativa de 0,18 para no ser EM.
Incluso se concluye que las presentaciones atípicas tienen mayor sensibilidad, especificidad y cociente de probabilidad positiva que las llamadas banderas rojas para refutar el diagnóstico de SCA sugestivo de EM.
Estos datos relacionados con la presentación clínica consideramos que son relevantes ante la aparición de un SCA, por lo tanto son en primer lugar los síntomas y signos clínicos de presentación a los que hay que considerar con especial atención.
Un 85% de pacientes con EM comienza con un SCA, pero estos por sí solos no definen EM, aunque el riesgo de conversión a ella es alto y esto obliga a realizar un diagnóstico diferencial.
La conversión de un SCA a EM se puede realizar por 2 vías alternativas: por aparición de un segundo ataque clínico, y si esto ocurre se denominará EM clínicamente definida (EMCD) —se cumple así con los criterios de Poser7— y por IRM de control, y se ha denominado esclerosis radiológicamente definida (EMRD)8.
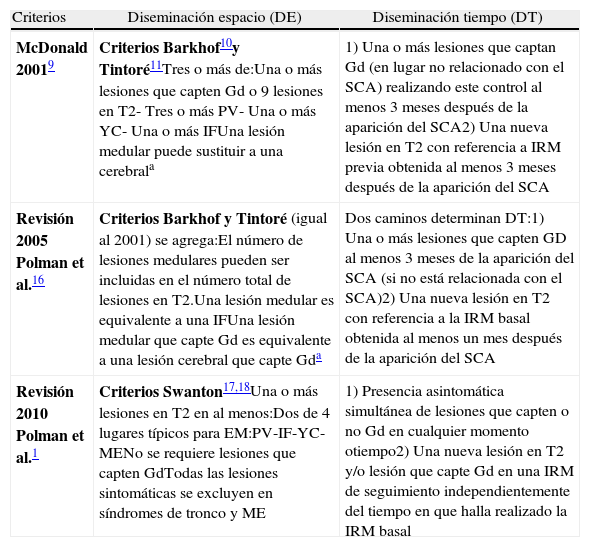
Desde el año 2001, con la aparición de los criterios de McDonald et al. publicados en julio de ese año9, aparece este nuevo concepto sobre la conversión, no solo por un segundo ataque clínico, sino a expensas de un examen radiológico, que implicó un diagnóstico más temprano de la enfermedad, siendo los requerimientos para la conversión cumplir con la DT establecida en estos nuevos criterios (tabla 1).
Comparación criterios de IRM para diseminación en espacio y tiempo
| Criterios | Diseminación espacio (DE) | Diseminación tiempo (DT) |
| McDonald 20019 | Criterios Barkhof10y Tintoré11Tres o más de:Una o más lesiones que capten Gd o 9 lesiones en T2- Tres o más PV- Una o más YC- Una o más IFUna lesión medular puede sustituir a una cerebrala | 1) Una o más lesiones que captan Gd (en lugar no relacionado con el SCA) realizando este control al menos 3 meses después de la aparición del SCA2) Una nueva lesión en T2 con referencia a IRM previa obtenida al menos 3 meses después de la aparición del SCA |
| Revisión 2005 Polman et al.16 | Criterios Barkhof y Tintoré (igual al 2001) se agrega:El número de lesiones medulares pueden ser incluidas en el número total de lesiones en T2.Una lesión medular es equivalente a una IFUna lesión medular que capte Gd es equivalente a una lesión cerebral que capte Gda | Dos caminos determinan DT:1) Una o más lesiones que capten GD al menos 3 meses de la aparición del SCA (si no está relacionada con el SCA)2) Una nueva lesión en T2 con referencia a la IRM basal obtenida al menos un mes después de la aparición del SCA |
| Revisión 2010 Polman et al.1 | Criterios Swanton17,18Una o más lesiones en T2 en al menos:Dos de 4 lugares típicos para EM:PV-IF-YC-MENo se requiere lesiones que capten GdTodas las lesiones sintomáticas se excluyen en síndromes de tronco y ME | 1) Presencia asintomática simultánea de lesiones que capten o no Gd en cualquier momento otiempo2) Una nueva lesión en T2 y/o lesión que capte Gd en una IRM de seguimiento independientemente del tiempo en que halla realizado la IRM basal |
Gd: gadolinio; IF: infratentorial; ME: médula espinal; PV: periventricular; SCA: síindrome clínicamente aislado; YC: yuxtacortical.
Pasaron así más de 18 años a partir de la publicación, en 1983, de los criterios de Poser para incorporar nuevos conceptos con el fin de encarar el diagnóstico de la EM, donde las IRM desempeñan un papel crucial tanto para la DE como para la DT.
Las implicaciones de los nuevos criterios de McDonald et al.9 fueron varias: un diagnóstico más temprano con apropiados niveles de sensibilidad, especificidad, precisión y valor predictivo positivo en predecir la conversión a EMCD.
La incorporación de las IRM en estos nuevos criterios aplicados a los SCA sirvió para que estos se puedan ordenar o clasificar en SCA de bajo o alto riesgo de conversión a EM, según los hallazgos de las IRM de inicio o basales y de acuerdo con los criterios de resonancia de Barkhof10 y Tintoré11 que los criterios de McDonald utilizaron para la DE. Es decir, que la DE en las IRM basales realizadas en los SCA fueron las que determinaron un riesgo bajo o alto de conversión a EM. Así, un SCA típico de alto riesgo de conversión será aquel que en la IRM basal cumpla por lo menos 3 de 4 criterios de DE requeridos por Barkhof y Tintoré (DE completa).
Diversos estudios observacionales12,13, e incluso ensayos terapéuticos de SDA para retrasar la conversión a EM, como el estudio BENEFIT14, realizado para evaluar el retraso de la conversión de SCA a EM con interferón beta 1b 250 μg día por medio, confirmaron que los criterios de McDonald 2001 anticipaban el diagnóstico de EM en relación con los criterios de Poser.
Tintoré et al.12 refieren que dichos criterios anticipan el diagnóstico de EM en más de 3 veces en el primer año.
En nuestra experiencia también pudimos observar que los nuevos criterios aplicados a los SCA, y comparándolos con los de Poser a un año desde la aparición del SCA, anticipaban el diagnóstico de EM15.
Pero estos criterios de McDonald fueron revisados y evaluados nuevamente en marzo de 2005 por un panel internacional, y como resultado surge la revisión de los mismos, publicándose en el año 200516.
Otra vez nuevos conceptos e implicaciones, pues si bien se mantiene la DE de acuerdo a los criterios de Barkhoff y Tintoré a ellos se suman la imágenes que pudieran hallarse en las IRM de la médula espinal y además se cambia y se simplifica la DT, habiendo dos caminos para su determinación y por lo tanto cumplirse la conversión a EM por IRM (tabla 1).
Esta revisión fue más útil para anticipar la conversión a EM por IRM, e incluso se observó que la misma tuvo mayor sensibilidad y precisión, pero menor especificidad y menor valor predictivo positivo respecto a los criterios de 2001.
No obstante lo anterior, la revisión de 2005 volvió a evaluarse por el Grupo Colaborativo Europeo Multicéntrico del llamado Magnetic Resonance Network in Multiple Sclerosis (MAGNIMS) en Dublín, Irlanda, en mayo de 2010, y así surge otra revisión de los criterios de McDonald que se publica en el año 20111.
Esta última revisión tiene como fundamento principal la evolución de las imágenes en RM, y los cambios producidos en el rol de las IRM de la médula espinal en el diagnóstico, e incluso las definiciones de DE y DT que se han simplificado merced a trabajos y propuestas de varios de ellos desde el año 2006, como los criterios de Swanton et al. de los años 2006 17y 200718, que hacen más simples los criterios de resonancia de DE de Barkhof y Tintoré, con el objetivo de una aplicación más práctica o menos complicada, pero manteniendo la sensibilidad y especificidad de los mismos.
Los requerimientos para la DT también se modifican en función de lo establecido por Montalban et al.19.
En la tabla 1 se pueden apreciar las diferencias referentes a los criterios de resonancia de DE y DT utilizados en los criterios de McDonald 2001, revisión de 2005 y revisión de 2010.
La RC2010 está principalmente dirigida para su aplicación en los SCA, pues la validación de los mismos se ha restringido prácticamente a este tipo de presentación.
Esta revisión y sus implicaciones son las que motivan nuestro trabajo, pues consideramos que al aplicarse en los SCA se producen cambios importantes y conceptos diferentes que consideramos relevantes.
Se aclara que también se presentaron cambios y modificaciones en las formas primarias progresivas que no se analizan en este trabajo, pues el mismo está enfocado a los SCA.
ObjetivoEvaluar el diagnóstico de EM aplicando estos criterios en pacientes con SCA y las implicaciones que causa la RC2010 aplicada a los SCA.
Material y métodosSe analizaron retrospectivamente 51 pacientes que presentaron SCA típicos desde el año 2001, que fueron seguidos en un principio durante 44 meses; dichos casos fueron presentados en Congreso ECTRIMS 200520 con el objetivo, en ese entonces, de evaluar el riesgo de conversión según la topografía lesional y los criterios de McDonald 2001.
Posterior a esa presentación dichos pacientes continuaron en seguimiento hasta el año 2010 incluido (total 9 años; media: 7 años y 5 meses).
Los criterios de inclusión fueron pacientes con un primer evento desmielinizante sugestivo de EM, es decir con síntomas de presentación típicos para dicha enfermedad, no atribuibles a otras enfermedades, sin antecedentes de enfermedades neurológicas y de edad no mayor de 50 años.
No se incluyeron pacientes con neuritis óptica bilateral (presentación menos común para EM4), ni mielitis transversa completa total hiperaguda (presentación atípica para EM4). A todos se les realizó una IRMB de 1,5 tesla de cerebro, sin y con gadolinio, dentro de los primeros 7 días de ocurrido el SDA, evaluándose quiénes cumplían DE según los criterios de IRM de Barkhof y Tintoré (por lo menos 3 de 4 criterios). En los casos en los que la DE fuera incompleta (solo 2 criterios) se completó la DE con LCR, si este era positivo (presencia de 2 o más bandas oligoclonales o aumento del índice de IgG) se cumplía la DE.
El índice de IgG se realizó por inmunonefelometría, y la determinación de las bandas por inmunoelectroforesis proteica con alta concentración (por 100), y en caso de no hallarse bandas por este método se repitió el estudio por isoelectro-enfoque tanto en el LCR como en el suero.
La DT fue establecida siguiendo las pautas de los criterios de McDonald 2001: aparición de un segundo ataque clínico o por IRM de control según los tiempos establecidos por dichos criterios (tabla 1). Se realizaron controles de IRM a los 3, 6, 9 y 12 meses desde el inicio del SCA.
De acuerdo a los resultados de la IRMB y el LCR se clasificó a los pacientes en SCA con bajo o alto riesgo de conversión.
Sobre la base de estos 51 pacientes con SCA se realizó una revisión y estratificación de los mismos, aplicando la revisión de los CD de 2010 que consistió esencialmente en la evaluación de las IRMB.
ResultadosLa edad promedio fue entre 18 y 50 años con una media de 32, una mediana de 31 y con una distribución por sexo de 36 mujeres (70,6%).
La forma de presentación clínica fue monofocal en 48 pacientes (94%), distribuidos en la siguiente forma: neuritis óptica 22 (43,1%), síndrome tronco 14 (27,4%), síndrome medular parcial 12 (23,5%) y forma de presentación multifocal 3 pacientes (6%).
De los 51 pacientes 20 (39,2%) presentaron BRC, pues 16 tuvieron IRMB de cerebro normal (31,4%) y 4 (7,8%) no cumplían la DE debido a que tenían menos de 2 criterios de Barkhof y Tintoré (DE incompleta).
Del resto de los pacientes 31 (60,8%) presentaron ARC, de los cuales 27 pacientes (53%) cumplían 3 o 4 criterios de Barkhof y Tintoré para DE y 4 (7,8%) cumplían solo 2 de estos criterios, ante lo cual se realizó LCR, que al ser positivo en ellos se completaron los criterios para DE (tabla 2).
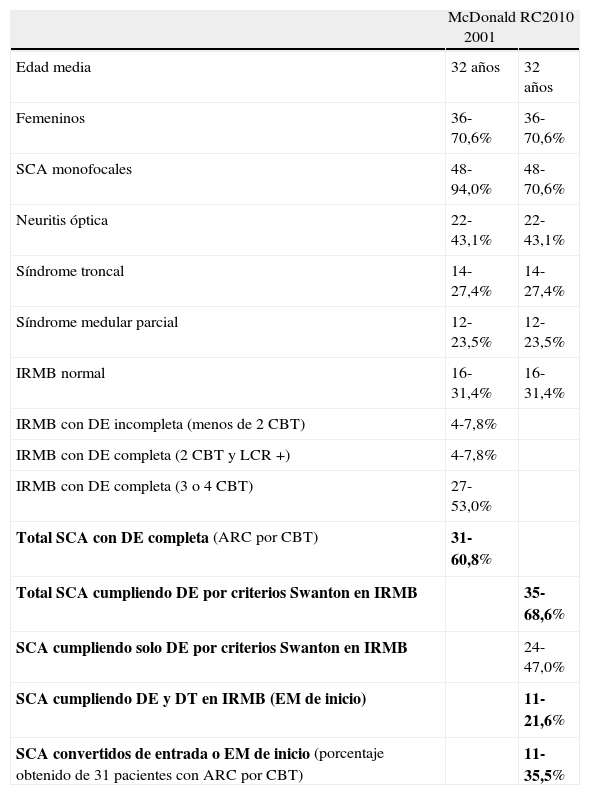
Características/resultados en 51 pacientes con SCA por criterios McDonald 2001 y aplicando RC2010
| McDonald 2001 | RC2010 | |
| Edad media | 32 años | 32 años |
| Femeninos | 36-70,6% | 36-70,6% |
| SCA monofocales | 48-94,0% | 48-70,6% |
| Neuritis óptica | 22-43,1% | 22-43,1% |
| Síndrome troncal | 14-27,4% | 14-27,4% |
| Síndrome medular parcial | 12-23,5% | 12-23,5% |
| IRMB normal | 16-31,4% | 16-31,4% |
| IRMB con DE incompleta (menos de 2 CBT) | 4-7,8% | |
| IRMB con DE completa (2 CBT y LCR+) | 4-7,8% | |
| IRMB con DE completa (3 o 4 CBT) | 27-53,0% | |
| Total SCA con DE completa (ARC por CBT) | 31-60,8% | |
| Total SCA cumpliendo DE por criterios Swanton en IRMB | 35-68,6% | |
| SCA cumpliendo solo DE por criterios Swanton en IRMB | 24-47,0% | |
| SCA cumpliendo DE y DT en IRMB (EM de inicio) | 11-21,6% | |
| SCA convertidos de entrada o EM de inicio (porcentaje obtenido de 31 pacientes con ARC por CBT) | 11-35,5% |
ARC: alto riesgo de conversión; CBT: criterios de Barkhof y Tintoré; DE: diseminación en espacio; DT: diseminación en tiempo; EM: esclerosis multiple; IRMB: imagen de resonancia magnética basal; LCR: líquido cefalorraquídeo; RC2010: revisión criterios 2010; SCA: síndrome clínicamente aislado.
En negrita: se realizaron para remarcar las diferencias entre los criterios de McDonald 2001 y la Revisión de criterios del 2010.
Como el objetivo de este estudio fue aplicar retrospectivamente la RC2010, se obtuvo que de los 31 pacientes con ARC por Barkhof y Tintoré 11 (35,5%) presentaron en la IRMB DE y DT, pues cumplían los criterios de Swanton para DE, evidenciándose además lesión asintomática captante con gadolinio, cumpliendo así los criterios nuevos para DT en esta primera resonancia cerebral, lo que significó de acuerdo a la RC2010 que ya eran EM desde el inicio o SCA convertidos de entrada.
De estos 11 pacientes ya convertidos a EM por IRMB, 8 (72,7%) tuvieron un segundo ataque clínico, es decir que evolucionaron a EMCD con una media de tiempo de 32 meses. Debe aclararse que este dato sobre el tiempo de conversión no se puede tomar como historia natural de estos, pues todos los pacientes con ARC fueron medicados con fármacos inmunomoduladores.
Otros cambios producidos al seguir la RC2010 en nuestros pacientes fueron que al aplicar los criterios de DE de Swanton en las IRMB 35 (68,6%) de ellos cumplían los mismos, de los cuales 24 (47,0%) solo cumplían DE y 11 DE y DT (21,6%).
Por lo tanto, al realizar la aplicación retrospectiva de la RC2010 en nuestros pacientes se obtuvo, al estratificar los mismos, los siguientes resultados del total de pacientes con SCA típicos (n=51) (tabla 2): 16 (31,4%) con IRMB normal 35 (68,6%) en donde en la IRMB se evidenció DE, 24 (47,0%) en donde en IRMB solo se cumplía la DE, 11 (21,6%) en donde en la IRMB se cumplía la DE y DT, considerándose EM desde el inicio o SCA convertido de entrada.
Los 11 pacientes con DE y DT en la primera resonancia (IRMB) constituyeron el 35,5% de los SCA de ARC por Barkhof y Tintoré.
Otro resultado a señalar es que aplicando los criterios de Swanton se obtuvo mayor número de pacientes con DE en su IRMB: 35 (68,6%); en cambio, aplicando los criterios de DE de Barkhof y Tintoré se obtuvo 31(60,8%) pacientes con DE (tabla 2).
Conclusiones y discusiónEn nuestra muestra de pacientes con SCA la aplicación de la RC2010 reveló un aumento importante de la sensibilidad para un diagnóstico mucho más temprano de EM, pues el 35,5% de pacientes con SCA que por criterios de McDonald 2001 fueron SCA de ARC, eran EM desde el inicio.
Estos resultados coinciden con otros estudios que también realizaron una revisión retrospectiva de pacientes con SCA aplicando RC2010.
Entre estos estudios podemos mencionar el estudio REFLEX21, ensayo realizado para evaluar la eficacia de interferón beta 1 a 44 mcg libre de albúmina, subcutáneo 3 veces por semana o igual dosis, pero una vez por semana, en retrasar la conversión a EM de los pacientes con SCA, según los criterios de McDonald 2005.
Al terminar dicho ensayo se hizo una revisión de los pacientes con SCA aplicando la RC201022; en dicha revisión se obtuvo que de 517 pacientes con SCA 195 (37,7%) eran EM de entrada, pues en su IRMB se encontró DE y DT.
Otro estudio realizado en nuestro país por Silva et al., del Hospital Ramos Mejía, en el XLVIII Congreso Argentino de Neurología 201123, presentó 58 pacientes con SCA que tenían ARC, 21 de ellos (36,2%) presentaron DE y DT en IRMB. Los autores refieren que en su población al aplicar RC2010 aumentó la sensibilidad para un diagnóstico más temprano de EM.
En el último evento ECTRIMS del mes de octubre de 2012, llevado a cabo en Lyon, Francia, Montalban et al.24 presentaron la revisión de criterios de 2010 aplicada al estudio BENEFIT (realizado para retrasar la conversión de SCA a EM por criterios de McDonald 2001 o por segundo ataque clínico). De dicha revisión se evidenció que de 468 pacientes con SCA 157(33,5%) eran EM también desde su inicio.
Si bien el objetivo de nuestro trabajo fue evaluar qué se obtenía al aplicar la RC2010 en los pacientes con SCA, consideramos que la RC2010 produce además implicaciones importantes y conceptos nuevos que consideramos que no se pueden dejar de mencionar o de evaluar.
¿Cuáles son esas implicaciones y nuevos conceptos?
- 1.
Aplicando RC2010 un número importante de pacientes con SCA serán EM desde el inicio, siempre que en la IRMB se encuentre DE y DT al mismo tiempo (la DT se establece por la existencia de por lo menos una lesión asintomática que refuerce o no con gadolinio) es decir, que nos podremos encontrar con SCA convertidos de entrada o EM convertidas de inicio que se han producido por las IRMB denominándose EMRD, aclarando que no son EMCD, pues no se ha producido un segundo ataque clínico. Evidentemente esto abrevia el desarrollo diagnóstico de EM, y al mismo tiempo reduce los falsos positivos, pues los criterios de DE utilizados por Swanton están referidos principalmente al lugar donde están las lesiones, y en menor importancia al número de ellas. Ante lo anterior el diagnóstico de EM es mucho más precoz, mucho más en comparación con los criterios de McDonald 2001 y la revisión de 2005, y manifiesta cambios notables y de mayor repercusión de estos nuevos criterios ante la posibilidad de establecer un diagnóstico de EM certero, partiendo de una primera y única resonancia sin necesidad de esperar un espacio de tiempo o de una segunda resonancia para poder concretar un diagnóstico definitivo. Los objetivos de los nuevos criterios son simplificar, unificar las normas diagnósticas y buscar la forma de hacer un diagnóstico más precoz a partir de una única IRM.
- 2.
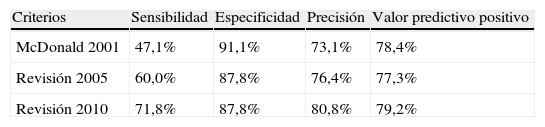
Si se evalúa la precisión diagnóstica de los criterios de McDonald de 2001, la revisión de ellos de 2005 y la de 2010 producida por el grupo MAGNIMS, se puede observar que la última revisión que origina los nuevos criterios perfecciona la sensibilidad, sin disminuir de manera importante la especificidad, mejora la precisión e incluso se obtiene un valor predictivo positivo mayor24 (tabla 3).
Tabla 3.Precisión diagnóstica de nuevos criterios de DE y DT (2010)
Criterios Sensibilidad Especificidad Precisión Valor predictivo positivo McDonald 2001 47,1% 91,1% 73,1% 78,4% Revisión 2005 60,0% 87,8% 76,4% 77,3% Revisión 2010 71,8% 87,8% 80,8% 79,2% Fuente: Montalban X et al.24.DE: diseminación en el espacio; DT: diseminación en el tiempo.
- 3.
Evidentemente surge que, por ejemplo, en los ensayos realizados con inmunomoduladores para retrasar la conversión a EM, tanto por resonancia como por un segundo ataque clínico, si se hubiera aplicado la RC2010 es altamente probable que un importante porcentaje de pacientes con SCA ya fueran EM convertidas desde el inicio. Así ocurrió en los ensayos REFLEX y BENEFIT al realizarse una revisión de los pacientes incluidos aplicando la RC201022,24.
- 4.
En futuros ensayos con nuevos fármacos, a los efectos de retrasar la conversión de SCA a EM, y si los mismos se realizan con la RC2010, se deberá considerar que un porcentaje de pacientes ya son EM convertidos por resonancia desde el inicio. De acuerdo con las revisiones que se han realizado este porcentaje oscila alrededor del 35%.
- 5.
El concepto de que en SCA típicos y una IRMB que cumpla criterios de DE y DT se pueda establecer el diagnóstico de EM lleva a una nueva clasificación de los SCA.
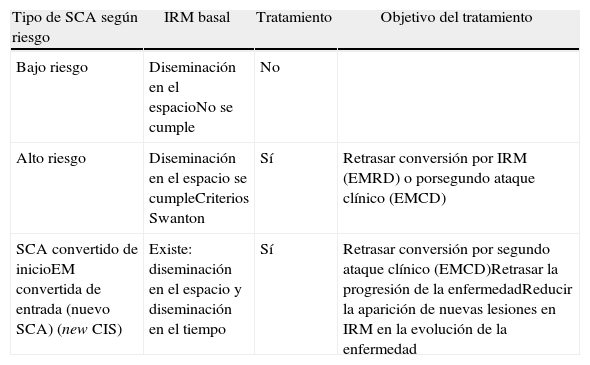
De acuerdo con ello, y según lo que se observe en la IRMB, habrá: a) SCA de bajo riesgo de conversión, donde no se cumple la DE; b) SCA de alto riesgo de conversión donde sí se cumple la DE; c) SCA convertidos de entrada o EM convertida desde el inicio, pues la DE y la DT están presentes en la IRMB (tabla 4).
Clasificación de los SCA según riesgo de conversión de acuerdo a la revisión de criterios 2010 y conducta terapéutica
| Tipo de SCA según riesgo | IRM basal | Tratamiento | Objetivo del tratamiento |
| Bajo riesgo | Diseminación en el espacioNo se cumple | No | |
| Alto riesgo | Diseminación en el espacio se cumpleCriterios Swanton | Sí | Retrasar conversión por IRM (EMRD) o porsegundo ataque clínico (EMCD) |
| SCA convertido de inicioEM convertida de entrada (nuevo SCA) (new CIS) | Existe: diseminación en el espacio y diseminación en el tiempo | Sí | Retrasar conversión por segundo ataque clínico (EMCD)Retrasar la progresión de la enfermedadReducir la aparición de nuevas lesiones en IRM en la evolución de la enfermedad |
CIS: clinically isolated syndrome; EMCD: esclerosis múltiple clínicamente definida; EMRD: esclerosis múltiple radiológicamente definida; IRM: imagen de resonancia magnética; SCA: síndrome clínicamente aislado.
Este planteamiento de un nuevo ordenamiento/clasificación de los SCA lleva además a proponer conductas de control y terapéuticas diferentes a lo que se tenía con los criterios de McDonald 2001 y revisión de 2005.
En SCA típico con IRMB, donde la DE no existe o no se cumple, la conducta es de control clínico, también de control con IRM, y aun cuando sea típico habrá que buscar otras alternativas diagnósticas, incluso examen del LCR. Por supuesto esta categoría de SCA no tiene indicación de tratamiento.
En SCA típico con ARC (en IRMB se observa DE) tiene indicación de tratamiento inmunomodulador a los efectos de retrasar la conversión a EM, ya sea por resonancia o por un segundo ataque clínico.
En SCA típico convertido desde el inicio, y considerado como EM de entrada, estos «nuevos SCA» tienen indicación de tratamiento, pero los objetivos del tratamiento son diferentes. Se tratan para retrasar la conversión por un segundo ataque clínico, es decir, para retrasar la conversión a EMCD y disminuir la frecuencia o número de futuras recaídas. En estos últimos no se busca retrasar la conversión por resonancia, pues ella ya ocurrió desde el inicio. Otro objetivo será disminuir la aparición de nuevas imágenes en la RM de control.
Se plantea si un SCA típico donde solo se cumple la DE por criterios de Swanton vs un SCA convertido de entrada tienen el mismo pronóstico y evolución, e incluso si deben recibir un tratamiento diferente, pues el primero todavía se tiene que convertir y el segundo ya es EM por lo menos por IRM.
Además, un SCA convertido de entrada y considerado como EM, indica ya que desde el inicio se presenta una enfermedad con mayor agresividad.
Los nuevos criterios no dejan de lado el concepto de que el diagnóstico de EM es de exclusión, y que indefectiblemente se deben cumplir los criterios de DE y DT.
Estos nuevos criterios solo deben ser aplicados a pacientes con SCA típicos, teniendo una especial atención a los hallazgos de eventuales lesiones inespecíficas en la IRMB y que puedan ser confundidas con imágenes típicas de EM.
Concluyendo, a pesar de la experiencia clínica e incluso en IRM, los SCA se presentan como un desafío diagnóstico.
La RC2010 se puede considerar que tiene como uno de los resultados principales y más relevantes que ante un paciente con un SCA típico, donde en la IRMB se cumplan los criterios de DE y DT, se puede determinar el diagnóstico de EM con un valor predictivo positivo mayor al 79%25.
No obstante lo anterior, consideramos necesario realizar un mayor número de evaluaciones retrospectivas y prospectivas de seguimiento de historia natural de los SCA aplicando la revisión de los criterios de 2010, a los efectos de establecer y confirmar la sensibilidad, especificidad y precisión diagnóstica de los mismos, principalmente para evaluar si estos criterios son también aplicables en poblaciones como la de América Latina y países asiáticos, e incluso pediátricas, donde estos criterios aún no están validados.
Aunque un aporte importante para su validación latinoamericana ha sido efectuado en nuestro país por Patrucco et al.26, presentado en la Academia Americana de Neurología 2012 y también en el Congreso ECTRIMS 2012, obteniendo en un estudio de 101 pacientes con SCA al aplicar la RC2010 una sensibilidad del 84%, especificidad del 80%, precisión del 82% y un valor predictivo positivo del 88%. Estos datos se consideran que pueden contribuir a su validación internacional.
Con la aplicación de la RC2010 se ha abierto un nuevo horizonte basado en que la RC2010 tiene mayor sensibilidad, se mantiene la especificidad, aumenta la precisión y el valor predictivo positivo para el diagnóstico precoz de EM, y por lo tanto permite comenzar con un tratamiento mucho más temprano.
No obstante, nuevos estudios terapéuticos aplicando la revisión de criterios de McDonald 2010 son necesarios para valorar el beneficio que se puede obtener para los pacientes que presentan SCA.
Conflicto de interesesLos autores declaran que no existe ningún conflicto de intereses.