: Bevacizumab es un anticuerpo monoclonal IgG1 humanizado recombinante que se une e inhibe la actividad biológica del factor de crecimiento endotelial vascular humano (FCEV) en sistemas de análisis in vitro e in vivo. Ha sido aprobado por la FDA como un agente adyuvante para el tratamiento del carcinoma colorrectal metastático y el cáncer pulmonar de células no pequeñas no escamosas. Actualmente es utilizado en diversas patologías oculares del segmento posterior, incluidas la degeneración macular retiniana relacionada con la edad y el edema macular secundario a trombosis venosa retiniana.
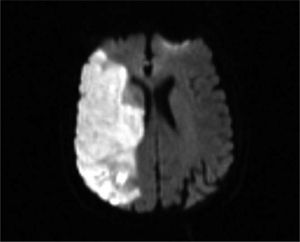
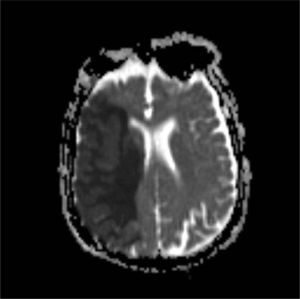
Caso clínico: Mujer de 81 años, con antecedentes patológicos de dislipemia, trombosis de la vena central de la retina del ojo derecho, seis meses previos al ingreso. Bajo tratamiento con inyecciones intravítreas de bevacizumab. Aproximadamente 4 h tras la segunda dosis de bevacizumab presenta de forma súbita debilidad en hemicuerpo izquierdo asociada a disartria. Ingresa en el servicio de emergencias, donde se realiza RM de cráneo que evidencia lesión compatible con infarto agudo de la cerebral media derecha.
Conclusión: Teniendo en cuenta la bibliografía actual, aún no existen reportes publicados provenientes de ensayos clínicos controlados, por lo que no puede analizarse apropiadamente su eficacia y su perfil de seguridad. Por lo tanto, se debería administrar sólo bajo condiciones de protocolo y con consentimiento informado, con especial precaución en pacientes mayores de 65 años, y también con antecedentes de arteriopatía.
: Bevacizumab is a recombinant humanized IgG1 monoclonal antibody that binds and inhibits the biological activity of vascular endothelial growth factor in human (VEGF) analysis systems in vitro and in vivo. Approved by the FDA as an adjuvant agent for the treatment of metastatic colorectal carcinoma and lung cancer non-small cell carcinoma. Currently, using it in various posterior segment eye diseases, including retinal macular degeneration related to age (AMD) and retinal vein thrombosis.
Case report: Female patient, 81 years with clinical history of dyslipidemia, thrombosis, central retinal vein of the right eye, six months prior to admission. Treated with intravitreal injections of bevacizumab. Approximately four hours after the second dose of bevacizumab presents fairly sudden weakness in the left hemisphere associated with dysarthria. Login to the emergency room where RMI is made of skull that shows lesion compatible with acute right middle cerebral.
Conclusion: Given the current evidence, although there are no published reports from controlled clinical trials and therefore can not properly analyze their effectiveness and safety profile. Therefore should be administered only under conditions of protocol and informed consent. With particular caution in patients over 65 years as well as a history of artery disease.
Bevacizumab es un anticuerpo monoclonal IgG1 humanizado recombinante que se une e inhibe la actividad biológica del factor de crecimiento endotelial vascular (VEGF) humano en sistemas de análisis in vitro e in vivo1. Bevacizumab fue aprobado por varias agencias reguladoras, entre ellas la Food and Drug Administration (FDA) y la Agencia Reguladora de la Unión Europea (EMEA)2,3 como un agente adyuvante para el tratamiento del carcinoma colorrectal metastático y el cáncer pulmonar de células no pequeñas no escamosas. Hasta la fecha no está regulado su uso para el tratamiento del edema macular en la trombosis venosa retiniana, aunque su empleo fuera de indicación (off label) se ha universalizado y constituye una práctica frecuente4–6. Recientes estudios muestran la inyección intraocular de bevacizumab como tratamiento alternativo en pacientes con trombosis de la vena central de la retina, con evidencia de escasos efectos adversos6,7.
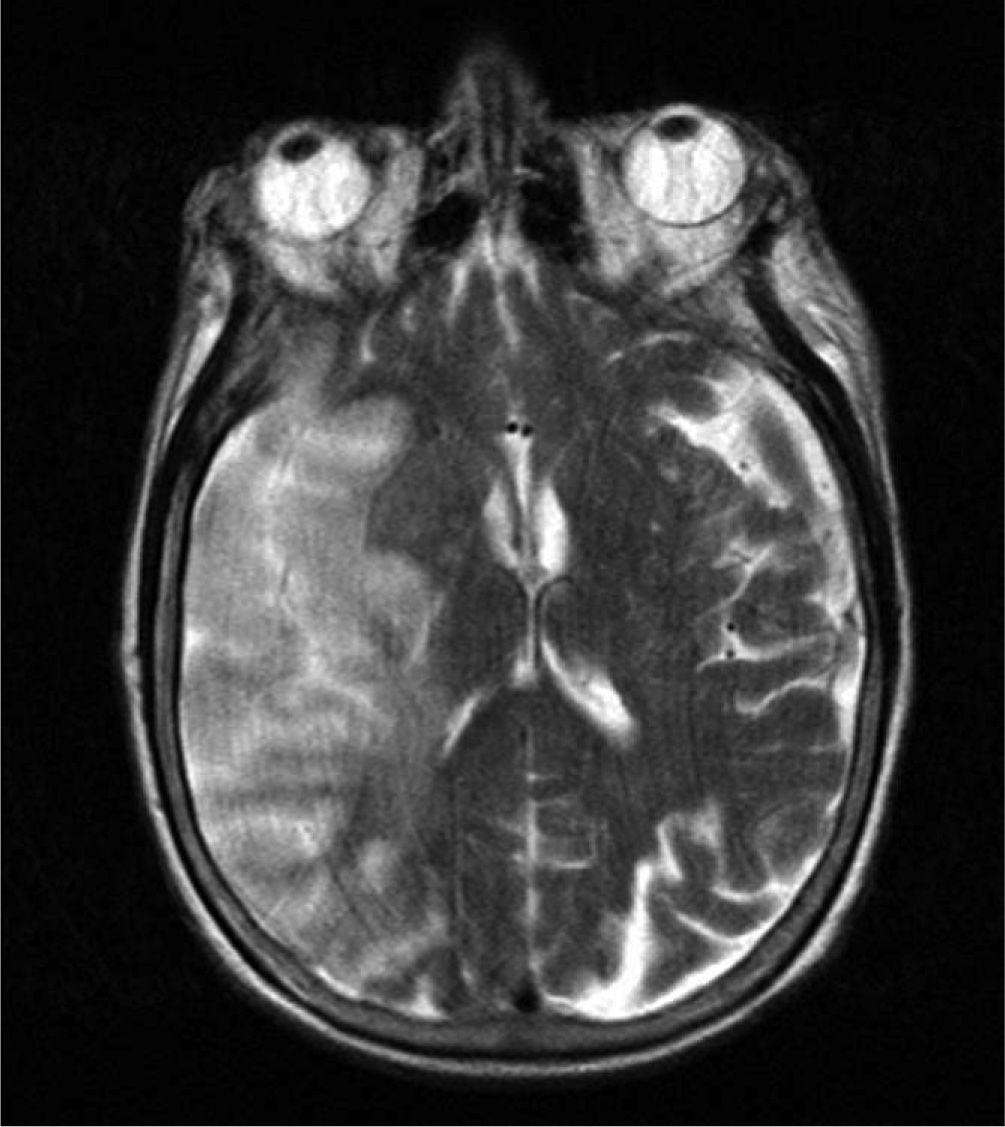
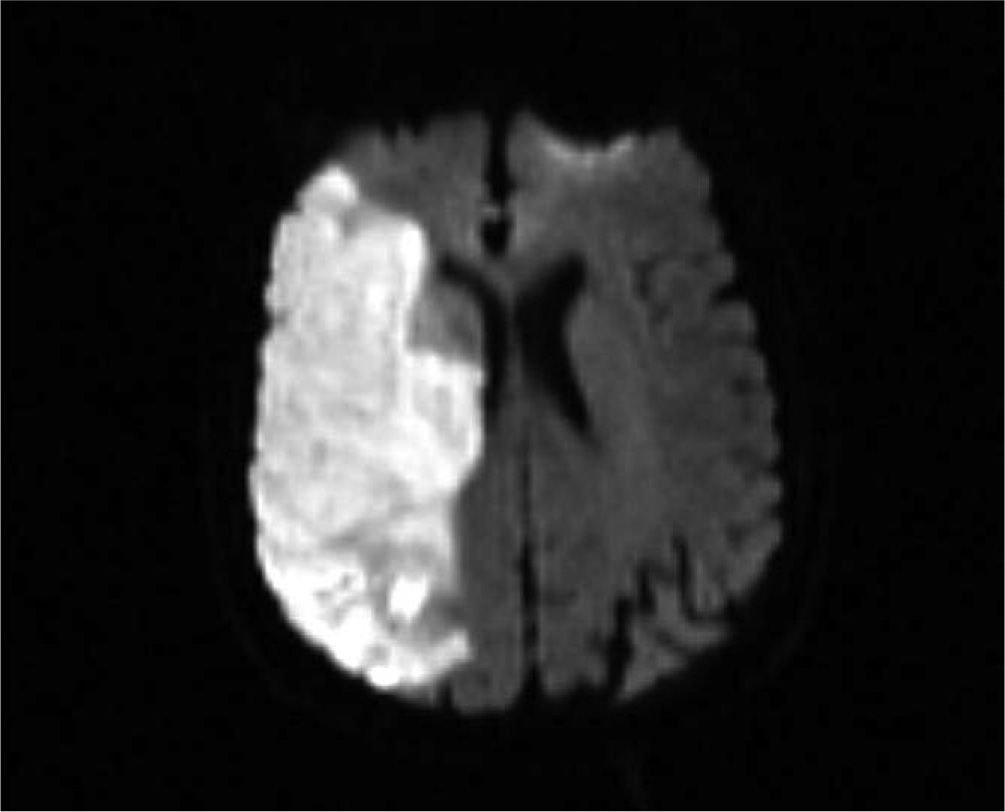
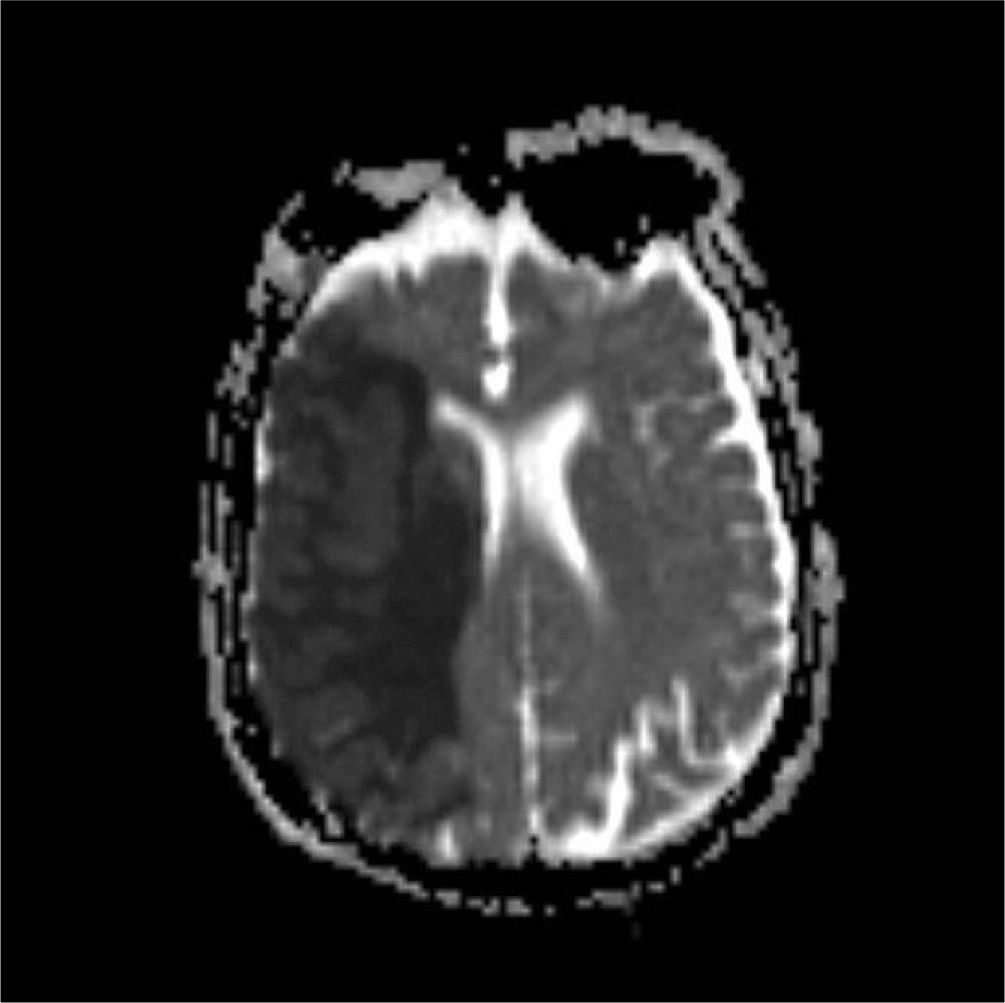
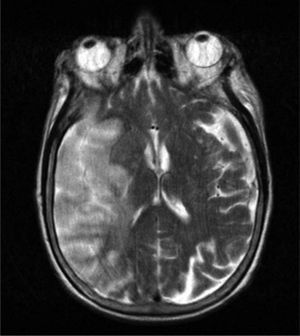
Caso clínicoMujer de 81 años de edad con antecedentes patológicos de dislipemia con diagnóstico de trombosis de la vena central de la retina en el ojo derecho (OD), 6 meses previos al ingreso. Recibió inicialmente tratamiento con láser y posteriormente inyección intravítrea de bevacizumab en el OD. La paciente recibe una segunda dosis de bevacizumab, presentado a las 4h de forma súbita debilidad muscular en hemicuerpo izquierdo asociada a trastorno en el lenguaje. Es trasladada a emergencias, donde se constata hemiparesia facial 1/2 braquial 0/5 crural 1/5 izquierda, disartria moderada, desviación forzada de la mirada hacia la derecha, hemianestesia, anosognosia y Babinsky izquierdo. ECG: ritmo sinusal. Se realiza una resonancia magnética (RM) del cráneo, que muestra signos de leucoaraiosis asociada a una extensa área córtico-subcortical hipointensa en T1 e hipertintensa en T2, y FLAIR en la región frontotemporal derecha, que borra los surcos y provoca leve efecto de masa sobre el sistema ventricular adyacente (fig. 1-3). Hiperintensa en difusión / hipotensa en mapa de coeficiente de difusión aparente (ADC), compatible con infarto agudo de la arteria cerebral media derecha. En la angiorresonancia extracraneal la arteria carótida interna derecha muestra moderada ateromatosis, y la arteria carótida primitiva izquierda, ateromatosis moderada con imagen sugerente de placa ulcerada en porción bulbar.
Bevacizumab ha sido aprobado por varias agencias reguladoras, entre ellas la FDA, la EMEA y la Administración Nacional de Medicamentos, Alimentos y tecnología (ANMAT), como un agente adyuvante para el tratamiento del carcinoma colorrectal metastático y el cáncer pulmonar de células no pequeñas no escamosas2,3. Desde octubre del 2005, los investigadores del grupo PACORES (Pan-American Collaborative Retina Study Group)8 han utilizado el bevacizumab intravítreo en diferentes patologías vitreorretinianas. Sin embargo, actualmente no está aprobado para su utilización en inyecciones intraoculares por los organismos de gobierno que controlan y regulan la ultimación de drogas en humanos (ANMAT y FDA).
Según resultados de estudios recientes, demuestra eficacia en el uso de inhibidores de VEGF para la disminución del edema macular secundario a trombosis venosa retiniana, por lo tanto se plantea su uso como posible opción terapéutica9–12.
El bloqueo sistémico del VEGF puede llegar a causar complicaciones sistémicas, como hipertensión arterial13, eventos tromboembólicos o aun la muerte14. En un estudio oncológico, la hipertensión arterial sistémica se observó en el 22,4% de los pacientes tratados con quimioterapia y bevacizumab, en comparación con el 8,3% de pacientes tratados únicamente con quimioterapia15. Hasta el 5% de los pacientes tratados con bevacizumab en combinación con quimioterapia pueden desarrollar eventos tromboembólicas, inclusive tromboembolismos arteriales fatales16.
Los posibles efectos adversos sistémicos asociados al uso de bevacizumab (intravítreo o sistémico) incluye accidente cerebrovascular, hipertensión arterial, trombosis venosa profunda, hemorragias y alucinaciones visuales17–20.
Por otro lado, teniendo en cuenta la relación temporal entre la inyección y el evento vascular, existen estudios que demuestran que en aproximadamente los 30min posteriores a la administración de bevacizumab intravítreo existe una elevación de la presión intraocular. Hay evidencias de que este incremento se asocia con daño en las células retinales, y también con oclusiones vasculares. Como probable mecanismo fisiopatológico involucrado en este fenómeno se propone una alteración en la autorregulación de la microcirculación, debido a que el VEGF actúa como vasodilatador al estimular la síntesis de óxido nítrico21.
Existen reportes de casos que demuestran lesiones isquémicas agudas dentro de las 24h postadministración, sin embargo la evidencia es limitada22.
Un análisis ongoing de subgrupo en el estudio SAILOR muestra un riesgo de ACV del 1,2% para dosis intraoculares de 0,5mg versus 0,3% en el grupo de 0,3mg (p=0,02)23. Sin embargo, no está claro si la tendencia hacia un mayor riesgo de ACV en los pacientes que recibieron dosis de 0,5mg se mantendrá en el análisis final. Los riesgos de uso intraocular de bevacizumab siguen actualmente siendo ampliamente desconocidos.
El amplio uso de bevacizumab en pacientes no sólo con degeneración macular retiniana relacionada con la edad, sino también en condiciones de compromiso vascular severo, no sólo regional sino también sistémico, incrementa significativamente los riesgos de eventos isquémicos y hemorrágicos.
Por lo tanto, la administración de bevacizumab intravítrea como sistémica puede asociarse a lesiones isquémicas oculares o cerebrales, sobre todo en pacientes de alto riesgo (ancianos: arteriopatía).
Conflicto de interesesNo se recibió apoyo financiero para la realización del trabajo. El envío a publicación de este trabajo ha sido aprobado por sus autores, por el Departamento de Docencia e Investigación y por el Servicio de Neurología del Hospital Privado de Comunidad. Transferimos los derechos de publicación a la revista Neurología Argentina.