En general se considera anemia la presencia de unos valores de hemoglobina por debajo de 12 g/dl con hematócrito inferior al 36% para mujeres y 14 g/dl con hematócrito menor de 41% para varones. Si bien la anemia se acompaña siempre de una disminución de la masa eritrocitaria, no es obligado un descenso del número de hematíes. Así, podrán darse situaciones en que la disminución de hemoglobina se asocie a una cifra normal o aumentada de eritrocitos y, por el contrario, una cifra disminuida de hematíes puede coexistir con una concentración de hemoglobina normal. Deben tenerse en cuenta en la interpretación de los valores de hemoglobina las posibles variaciones del volumen plasmático, ya que pueden inducir a error al apuntar a una falsa anemia en situaciones de hemodilución, y vice versa.
Anamnesis y exploración física
Los signos y síntomas de la anemia varían según la etiología, intensidad y rapidez de instauración del cuadro. En la tabla 1 se recogen las principales manifestaciones clínicas del síndrome anémico.
Anamnesis
La historia clínica resulta fundamental a la hora de comenzar y orientar el estudio. Deben tenerse en cuenta la edad del paciente, la forma de presentación, el tiempo de evolución y la existencia de ciertos antecedentes personales o la historia familiar. El momento de aparición de los primeros síntomas ayudará a distinguir entre un defecto adquirido o una enfermedad congénita. La raza del paciente puede orientar asimismo hacia determinadas patologías, como algunas hemoglobinopatías hereditarias frecuentes en la raza negra. Tiene interés reseñar los hábitos alimenticios, consumo de alcohol, ingestión reciente de fármacos o de determinados alimentos, como las habas (déficit de G6PDH), o la exposición a tóxicos ambientales o laborales. Debe interrogarse sobre posibles pérdidas digestivas y recoger una historia ginecológica completa. La existencia de antecedentes de tiroiditis, vitíligo u otras enfermedades autoinmunes orienta hacia la presencia de anemia perniciosa.
Ciertos síntomas pueden proporcionar datos para el diagnóstico de formas específicas de anemia. La presencia de fiebre u otros signos inflamatorios pueden indicar asociación a una enfermedad del colágeno. Los pacientes con anemia de células falciformes suelen referir historia de larga evolución de dolores óseos y articulares intensos y periódicos. El déficit grave de hierro suele provocar úlceras orales, dificultad para la deglución y un deseo incontenible de comer hielo o tierra (pica). La existencia de manifestaciones neurológicas, como la pérdida de sensibilidad vibratoria y postural en extremidades, orienta hacia una degeneración combinada subaguda por déficit de cobalamina.
Algunas neoplasias pueden manifestarse con un período de evolución subclínica prolongado en que los únicos síntomas sean tan inespecíficos como fiebre de origen indeterminado, pérdida de peso o anemia. Es el caso del hipernefroma, del cáncer de páncreas o de los linfomas. En niños y jóvenes, una anemia de larga evolución con antecedentes de ictericia recurrente, muchas veces atribuida a hepatitis, es indicativa de un origen congénito.
Exploración física
En la exploración clínica de un paciente con anemia debe evaluarse, en primer lugar, la situación de oxigenación tisular y de pérdida de volumen, sobre todo en los síndromes anémicos de instauración aguda. Si son muy graves, el paciente presentará datos de shock hipovo-
lémico, con disminución del nivel de conciencia, taquicardia con pulso muy débil, hipotensión, sudación fría, palidez y disnea. Cuando la instauración de la anemia es más gradual, los mecanismos compensatorios retrasan la aparición de síntomas y se podrá objetivar palidez o ictericia según el origen del cuadro, taquicardia, soplos cardíacos funcionales e hipotensión ortostática.
Según se trate de uno u otro origen, podrán asociarse distintos datos de exploración, como las rágades y uñas frágiles en la ferropenia; lengua depapilada, tinte subictérico conjuntival y alteraciones atáxicas de la marcha en las anemias megaloblásticas y otros hallazgos que se comentan en el apartado correspondiente.
Pruebas de laboratorio
Las pruebas analíticas que deben formar parte del primer escalón diagnóstico del síndrome anémico se recogen en la tabla 2.
Hemograma. El hemograma completo confirma la existencia de la anemia y proporciona información sobre su gravedad y la posible afección de las otras series, que permite una orientación diagnóstica. Los índices eritrocitarios, sobre todo el volumen corpuscular medio (VCM), resultan útiles para detectar macro o microci tosis, y la hemoglobina corpuscular media (HCM) es sensible a las alteraciones en la producción de hemo-
globina.
Bioquímica. La bioquímica sanguínea también puede aportar datos sobre la existencia de hemólisis, por el aumento de los valores de bilirrubina o de lactatodeshidrogenasa (LDH) séricos, así como descartar una posible alteración de la función renal.
Extensión de sangre. Es importante la realización de una extensión de sangre periférica, que detecta alteraciones en el tamaño y la forma de las células sanguí neas y puede indicar defectos en la proliferación o maduración de los precursores eritrocitarios o una destrucción en la circulación periférica. El frotis puede evidenciar la existencia de policromasia, indicadora de la salida a la circulación de reticulocitos (con gran cantidad de ARN y ribosomas en su interior) desde la médula ósea (MO), lo que informa de la idoneidad de la respuesta a la eritropoyetina (EPO). La visualización en el frotis de determinadas formas celulares resulta orientadora de ciertos procesos patológicos, como se expone en la tabla 3.
Reticulocitos. El recuento de reticulocitos es útil para realizar una clasificación inicial del síndrome anémico. Los valores normales oscilan entre el 5 y el 15%o en valor relativo o 25.000-80.000/µl en números absolutos. El porcentaje de cada paciente debe corregirse en función del hematócrito. El índice reticulocitario (IR) proporciona información fiable de la respuesta a la EPO, de una respuesta medular correcta y de unas concentraciones suficientes de hierro para afrontar la mayor producción de eritrocitos. Se calcula mediante la
siguiente fórmula:
IR = n.o de reticulocitos * hematócrito del paciente/hematocrito normal / 2
Un IR superior al 2-3% es marcador de anemia regenerativa y si es inferior al 2% indica un componente hiporegenerativo.
Metabolismo férrico. El estudio del metabolismo férrico ofrece una importante información en el abordaje inicial del paciente con anemia. Los valores normales se reflejan en la tabla 4.
Médula ósea. Puede ser necesario realizar estudio de la médula ósea (MO) obtenida por biopsia/aspiración, especialmente si los resultados de las pruebas previas orientan hacia un origen hiporregenerativo o a una alteración en la maduración de los hematíes. Proporciona información sobre la arquitectura y celularidad de la médula, así como de la proliferación y maduración de los precursores eritroides. El cociente entre los precursores eritroides y granulocíticos (E/G) se usa para valorar la capacidad proliferativa de los primeros: un paciente con anemia hiporregenerativa presentará un índice E/G inferior a un tercio o la mitad, mientras que si la anemia es hemolítica o posthemorrágica el cociente E/G será de 1:1. Si el cociente E/G es normal y sin embargo el índice reticulocitario es bajo, se tratará de una anemia con trastornos en la maduración intramedular de los hematíes ya formados.
Clasificación inicial de la anemia
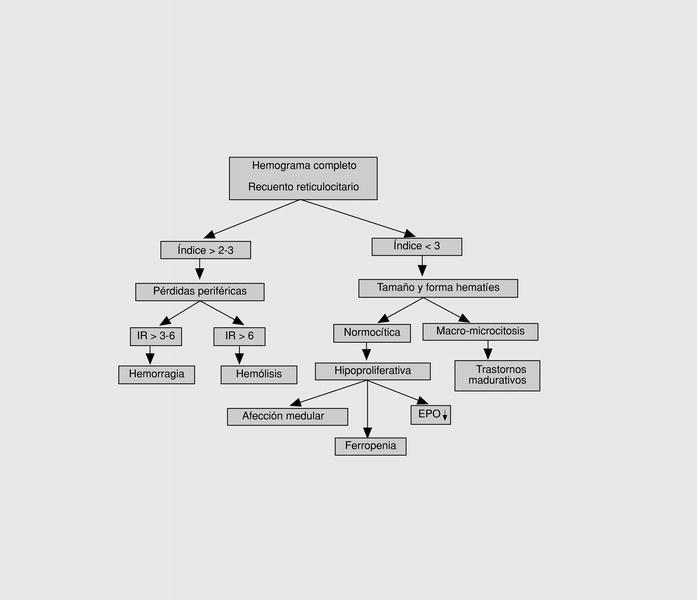
Los resultados de las primeras pruebas de laboratorio permiten orientar el diagnóstico y establecer una primera clasificación fisiopatológica para continuar el estudio de una forma dirigida. Como queda esquematizado en la figura 1, combinando los datos del hemograma con la VCM y la amplitud de distribución eritrocitaria (ADE) y el índice reticulocitario, se pueden definir los tres grupos principales de anemias: a) las hipoproliferativas, debidas a un defecto en la respuesta de la MO; b) las secundarias a un defecto en la maduración de los precursores a pesar de una producción eficaz, y c) las debidas a un aumento de la destrucción o pérdida de los hematíes en la circulación periférica.
Fig. 1. Algoritmo diagnóstico de una anemia. IR: índice reticu locitario, y EPO: eritropoyetina.
Anemias hipoproliferativas
Constituyen el mayor grupo de anemias en la práctica clínica. Se deben a una respuesta insuficiente de la médula frente a la falta de células maduras en sangre periférica. Dentro de este grupo se distinguen tres subgrupos, según su mecanismo fisiopatológico:
Afección medular primaria
Las anemias hipoproliferativas causadas por lesiones medulares engloban la anemia aplásica, la aplasia eritrocitaria pura, los síndromes mielodisplásicos y la mieloptisis.
Anemia aplásica. Está afectada la producción de todos los precursores eritroides, granulocíticos y megacariocíticos, lo que se traduce en una pancitopenia periférica. Es más frecuente entre jóvenes (de 15 a 30 años) o en personas mayores de 60, y fundamentalmente son de causa adquirida. En la tabla 5 se reseñan las principales etiologías.
A las manifestaciones del síndrome anémico se unen los síntomas derivados de la afección de las otras series.
El diagnóstico comienza por constatar en el hemograma la presencia de pancitopenia, con normocromía y normocitosis, junto a un IR inferior a 2, que confirma la situación hipoproliferativa. Debe confirmarse mediante estudio morfológico y citogenético de MO, para distinguir entre las causas adquiridas y congénitas. El diagnóstico diferencial debe realizarse con el síndrome displásico hipocelular (el frotis puede ser de gran utilidad), la leucemia aguda paucicelular (según la presencia o no de blastos) y la leucemia de células peludas (por la morfología de las mismas).
En el tratamiento, es fundamental la retirada del agente etiológico sospechoso. Si no existiera, el tratamiento definitivo será el trasplante de MO de un familiar histocompatible. La terapia de soporte (transfusiones, antibioterapia, etc.) es importante en el mantenimiento de los pacientes hasta la realización del trasplante. En los pacientes no candidatos a trasplante se han usado inmunodepresores, como la ciclofosfamida, la ciclosporina o los corticoides. Los ensayos clínicos con factores de crecimiento hematopoyético han dado resultados insatisfactorios.
Aplasia eritrocitaria pura. Se trata de una ausencia exclusiva de precursores eritroides. Como el grupo anterior, pueden ser hereditarias o adquiridas, bien idiopáticas o asociadas a otros procesos como linfomas, timomas, enfermedades autoinmunes (LES o anemia refractaria simple) o infecciones, sobre todo víricas (VIH, Parvovirus B19, virus de Epstein-Barr [VEB]). También pueden producirla algunos fármacos e, incluso, el embarazo. Para el diagnóstico se siguen los mismos pasos que en el grupo anterior. El tratamiento se basa en la supresión del agente etiológico si existe. Si se asocia a in fección por Parvovirus B19 resultará eficaz el tratamiento con inmunoglobulinas; si se considera la causa inmune, se utilizarán inmunodepresores.
Síndromes mielodisplásicos. Son un grupo de procesos adquiridos que suelen cursar con pancitopenia, IR bajo y médula normo o hipercelular, pero con formas claramente displásicas. Son trastornos clonales cuya etiología no está bien aclarada. Suelen evolucionar a leucemias agudas.
Su presentación clínica suele ser insidiosa, con síntomas derivados de la afección de las tres series. Para confirmar el diagnóstico se valorarán el grado de celularidad de la médula, el número de blastos y sideroblastos en anillo y la existencia de cambios displásicos. Puede ser de ayuda la realización de un estudio citogenético de las células medulares. Existen 5 tipos de procesos mielodisplásicos: la anemia refractaria simple (AR), la anemia refractaria con sideroblastos en anillo (ARSA), la anemia refracta ria con exceso de blastos (AREB), la anemia refractaria con exceso de blastos en transformación (AREB-t) y la leucemia mielomonocítica crónica (LMMC). La descripción de cada grupo queda fuera del propósito de este trabajo. El diagnóstico diferencial debe establecerse con determinadas carencias vitamínicas que pueden producir cuadros similares (B6, B12 o ácido fólico), con la anemia aplásica, la hemoglobinuria paroxística nocturna (HPN), la leucemia aguda aleucémica en la que no se ven blastos circulantes, la mielofibrosis aguda y crónica y la anemia mieloptísica.
El trasplante de MO es la única terapia curativa. En los pacientes no candidatos se deben administrar transfusiones periódicas de hematíes (intentando evitar el desarrollo de hemocromatosis con quelantes, como la desferroxamina), plaquetas, antibióticos, factores de crecimiento hematopoyético, vitaminas, corticoides, inmunodepresores, etc.
Anemias ferropénicas
Se caracterizan por un descenso de la masa eritrocitaria secundaria a un déficit de hierro que puede ser debido a un aporte insuficiente, a un aumento del consumo o a un exceso de pérdidas, como se resume en la tabla 6.
Las pérdidas digestivas crónicas son la causa más frecuente de ferropenia, bien por hernia de hiato, gastritis, úlcera gastroduodenal, hemorroides, neoplasias, enfermedad inflamatoria, lesiones vasculares, etc. Determinados fármacos, como la aspirina, los antiinflamatorios o los corticoides, pueden contribuir a la lesión de la mucosa favoreciendo la hemorragia.
Las manifestaciones clínicas suelen aparecer de forma lenta y progresiva, lo que justifica que las cifras de hemoglobina puedan llegar a ser muy bajas en el momento del diagnóstico. Los signos y síntomas que orientan al déficit de hierro se dan en todos los tejidos de alto recambio celular. Se observarán glositis, queilitis, trastornos tróficos de la piel, fragilidad de pelo y uñas, las cuales a su vez pueden adoptar una forma típica en cuchara, etc.
El diagnóstico se basa en el hemograma, el recuento de reticulocitos y la determinación de los valores de hierro, ferritina, transferrina, índice de saturación y capacidad total del transporte de hierro. Los hematíes son microcíticos e hipocrómicos. La ADE está aumentada (> 14-15%) como expresión de la heterogenicidad existente entre la población eritrocitaria. Este dato es útil para diferenciar una anemia ferropénica de las talasemias, ya que en éstas la ADE es menor, al ser la morfología eritrocitaria más homogénea. Cuando el déficit de hierro se perpetúa, disminuye la formación de reticulocitos; de ahí que este grupo forme parte de las anemias hiporregenerativas.
La investigación y el tratamiento de la causa de la ferropenia es fundamental en su tratamiento. Las transfusiones de hematíes se reservan para los casos de anemia grave con clínica manifiesta. La reposición del hierro, para corregir el déficit y reponer los depósitos, se realiza con la administración oral de sales ferrosas, siendo el más utilizado el sulfato ferroso por su mejor tolerancia digestiva. La absorción es mayor en ayunas, y debe tenerse en cuenta posibles situaciones de malabsorción, aclorhidria u otras que puedan hacer ineficaz el tratamiento por vía oral. La dosis habitual para un adulto oscila entre 200-250 mg de hierro diario. En los niños la dosis es de 3 mg/kg/día. Los efectos secundarios más frecuentes son los gastrointestinales, como náuseas, vómitos, diarrea, etc. La respuesta al tratamiento se valora con un hemograma a los 7 días de comenzar el tratamiento, comprobando el aumento en la cifra de reticulocitos. En uno o dos meses, y según la gravedad de la anemia, la hemoglobina deberá haber alcanzado valores normales, y a partir de ese momento se continuará el tratamiento otros 6 meses como mínimo para replecionar los depósitos de hierro.
Si existe una causa que impida el aporte por vía oral, se puede recurrir al hierro parenteral, que se administra en forma de hierro dextrano. La dosis se calcula mediante la siguiente fórmula:
Dosis total (mg) = peso (kg) * 2,3 * (hemoglobina deseada hemoglobina del paciente en g/dl)
A esto se añadirán entre 500 y 1.000 mg más hasta reponer los depósitos.
Otras anemias hipoproliferativas
La falta de respuesta medular se produce por la coexistencia de distintos factores; son varios los procesos y entidades en que podemos encontrarlas.
Anemia de los procesos inflamatorios. Los mediadores de inflamación (TNF, Il-1, IFN, etc.) son capaces de inhibir la proliferación de precursores eritroides a nivel medular, la liberación de EPO por el riñón y la liberación del hierro por las células del sistema reticuloendotelial.
Es una anemia generalmente moderada, normocítica y normocrómica o microcítica e hipocroma según predomine o no la falta de disponibilidad de hierro. Los depósitos de hierro en la médula son normales o elevados. La sideremia y la capacidad de fijación de la transferrina están disminuidas y la ferritina está aumentada como reactante de fase aguda. Estos datos permiten diferenciarlas de otras anemias hipoproliferativas.
Anemia de la insuficiencia renal. Es secundaria a la disminución de la vida media de los hematíes por la hiperazoemia sumada a la deficiente producción de EPO por el riñón enfermo. El grado de anemia suele ser paralelo al de insuficiencia renal. Los parámetros de laboratorio son similares a los del resto del grupo, excepto los del metabolismo férrico, que se mantienen normales en la nefropatía incipiente, a diferencia de los otros grupos. La determinación de EPO sérica no resulta de utilidad, ya que puede ser normal, puesto que el defecto se debe a una respuesta inadecuada a la intensidad de la anemia, y no a una pérdida absoluta de formación de EPO.
Otros. En los estados que cursan con disminución del metabolismo parece que la menor respuesta de EPO a la anemia indica una menor necesidad de oxígeno. Esto ocurre en varones sometidos a supresión hormonal, en el hipotiroidismo y en la insuficiencia suprarrenal. También es normal la existencia de anemia en pacientes con carencias proteicas y en hepatopatías, sobre todo de origen alcohólico, por acumulación de colesterol en el hematíe o por efecto tóxico directo del alcohol sobre el mismo.
El tratamiento en estos procesos debe ser individualizado y comienza por un correcto diagnóstico y control de la causa subyacente, en ocasiones suficiente para corregir la anemia. Sólo se recurrirá a las transfusiones en caso de anemias muy graves o sintomáticas, sobre todo en personas de edad avanzada. El tratamiento con EPO (50-150 U/kg por vía subcutánea, tres veces en semana) se ha demostrado eficaz en pacientes con nefropatía terminal. Si el paciente llegara a hacerse refractario al tratamiento, cuando aumentan demasiado las necesidades de EPO, se recurrirá a las transfusiones.
Trastornos en la maduración celular
En este grupo de anemias se combina un IR bajo con una morfología eritrocitaria característica: puede existir macrocitosis si el defecto se produce en la maduración nuclear y microcitosis cuando el fallo de maduración se da en el citoplasma. El estudio morfológico de la médula objetiva un incremento del cociente E/G hasta valores superiores a 1:1, lo que indica una correcta producción intramedular de precursores eritroides. Los dos grupos fundamentales son:
Defectos citoplasmáticos
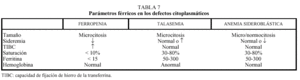
Dentro de este grupo hay tres posibles orígenes, cuyas diferencias se resumen en la tabla 7.
Déficit de hierro. Ya descrito por pertenecer también al grupo fisiopatológico anterior.
Alteraciones de la hemoglobina. Cuando el defecto consiste en la producción de cadenas anormales de hemoglobina, se habla de hemoglobinopatías. Sin embargo, si la alteración supone una reducción del número de estas cadenas se conocen como talasemias. La diferencia entre ellas no siempre es completa.
En las hemoglobinopatías se producen mutaciones en los genes de la globina que pueden alterar la estabilidad de la hemoglobina en situaciones de bajo nivel de oxígeno, haciendo que ésta precipite en el citoplasma (cuerpos de Heinz) y produzca la deformación de los hematíes. Dentro de estos trastornos el más representativo es la anemia de células falciformes o drepanocitosis. En ella, los hematíes deformados en situaciones de hipoxemia atraviesan poco o nada los vasos pequeños, lo que provoca infartos repetidos, sobre todo en el bazo, pulmón, riñón y cerebro.
Además de los signos y síntomas propios de la anemia, los pacientes suelen presentar ictericia por la hemólisis y predisposición a la formación de cálculos biliares. Otros síntomas dependen directamente de la oclusión de los vasos pequeños, con desprendimientos de retina, afección renal por necrosis papilar, úlceras en las piernas, priapismo, infartos pulmonares con desarrollo de hipertensión pulmonar e infartos esplénicos que pueden llegar a producir una situación de asplenia funcional con mayor susceptibilidad a infecciones. En niños pueden darse ictus con graves secuelas neurológicas. La insuficiencia renal y pulmonar es progresiva y muchas veces es causa de muerte en estos pacientes. En ocasiones pueden aparecer crisis agudas de dolores óseos por infartos en estas zonas, de secuestro esplénico de los hematíes y de hemólisis agudas e intensas.
El diagnóstico se basa en la existencia de hemoglobina falciforme, que se confirma sometiendo a los hematíes a un agente reductor, el metabisulfito sódico, y comprobando que éstos adoptan la forma característica. La realización de una electroforesis permitirá identificar a la hemoglobina S responsable del proceso.
Es fundamental en el tratamiento evitar las situaciones que pueden desencadenar las complicaciones. La hidroxicarbamida, un fármaco que inhibe la eritropoyesis normal favoreciendo la formación de cadenas gamma, con lo que aumenta la hemoglobina fetal, que interfiere con la falciformación, disminuye las crisis. El único tratamiento definitivo es el trasplante alogénico de médula ósea.
Entre las talasemias se distinguen varios tipos (alfa y beta), según la globina defectuosa, y dentro de éstos, varios grados de gravedad según los genes afectados. El más leve dentro de las alfatalasemias es el rasgo talasémico alfa, en el que los pacientes presentan una discreta anemia con microcitosis e hipocromía. En el otro extremo estarían las formas incompatibles con la vida. En las betatalasemias la gravedad depende de la afec-ción (deleción o mutación) de uno o varios genes, y la clínica también será distinta en uno u otro caso.
El diagnóstico, una vez sospechado el trastorno con los datos presentes en la tabla 7, se comprueba realizando un estudio electroforético de las cadenas de la hemoglobina. El tratamiento consiste en transfusiones repetidas, teniendo en cuenta las posibles sobrecargas de hierro y, en ocasiones, la esplenectomía.
Defectos a nivel nuclear
Los defectos de la maduración nuclear comportan una disminución de la síntesis de ADN. Las alteraciones en la eritropoyesis asociadas a este defecto se conocen como anemias megaloblásticas y pueden deberse a un déficit de vitamina B12 o cobalamina, de ácido fólico o de ambos. Las distintas causas del déficit de uno u otro varían según las distintas zonas geográficas (tabla 8). Una de las más frecuentes es la anemia perniciosa, debida a un déficit de factor intrínseco por atrofia de la mucosa gástrica. Asociada a alteraciones inmunes, se pueden demostrar anticuerpos anticélulas parietales gástricas en el 90% y antifactor intrínseco en el 60% de los pacientes.
En el déficit de cobalamina, además del síndrome anémico y de la clínica propia de cada proceso, coinciden manifestaciones gastrointestinales (lengua dolorosa y depapilada, anorexia, pérdida de peso, diarrea o estreñimiento) y del sistema nervioso por desmielinización y degeneración axonal, como parestesias, ataxia, trastornos esfinterianos, etc. En el déficit de folatos es más frecuente encontrar al paciente en situación de malnutrición importante; sin embargo, no suele haber manifestaciones neurológicas.
Una macrocitosis importante (VCM > 110) hace verosímil el diagnóstico de anemia megaloblástica. El IR es bajo y con frecuencia se pueden ver afectadas las otras series, según la gravedad del proceso. Es muy típico el hallazgo de neutrófilos hipersegmentados, y su presencia debe indicar el diagnóstico de megaloblastosis. En la extensión de sangre periférica podrán verse anisocitosis, poiquilocitosis, macroovalocitos, punteado basófilo, hematíes nucleados y cuerpos de Howell-Jolly. El examen de la médula ósea objetiva hipercelularidad con cociente E/G bajo, hierro abundante, precursores eritroides grandes con asincronía nucleocitoplásmica y conformación anormal de la cromatina con mitosis también anormales.
La hemólisis intramedular de precursores produce aumento de LDH y bilirrubina no conjugada, con haptoglobina disminuida. La determinación de los valores de vitamina B12 y ácido fólico confirmarán el diagnóstico. Cifras menores de 100 pg/ml de cobalamina y de 4 ng/ml de folatos indican un déficit importante. También pueden medirse en sangre los metabolitos de la cobalamina (homocisteína o ácido metilmalónico).
Tras la confirmación del déficit de cobalamina, su etiología puede intentar filiarse mediante el test de Schilling: tras la administración de vitamina B12 marcada por vía oral, a la vez que una cantidad de la misma por vía parenteral, se comprueba 24 h después su excreción en orina. Si la causa del déficit es la malabsorción, la excreción urinaria será baja. En la segunda parte de la prueba se administra la vitamina B12 marcada más factor intrínseco. Si existe anemia perniciosa, se comprobará un aumento de cobalamina radiactiva en orina. Si la prueba sigue siendo anormal, indicará malabsorción de otro origen, como un síndrome del asa ciega o una enfermedad del íleon terminal.
Su tratamiento exige el de la causa subyacente en cada caso. Además, será necesario administrar los suplementos del elemento deficitario. La vitamina B12 se administra en forma de cianocobalamina intramuscular. Se comienza con 100 µg/día en la primera semana, pasando a 100 µg dos veces en semana en la segunda. En las 4 semanas siguientes se administrarán 100 µg semanales y posteriormente una dosis mensual de por vida. Periódicamente debe realizarse endoscopia digestiva por el riesgo de adenocarcinoma gástrico.
El déficit de ácido fólico se repone con dosis de 1- 5 µg/día por vía oral. Si el componente de malabsorción es muy importante, puede recurrirse a la vía parenteral. Si la anemia es secundaria a fármacos antagonistas de los folatos se utilizará el ácido folínico.
Aumento de destrucción de hematíes
Este grupo se caracteriza por un IR elevado (> 3) que representa intacta la capacidad regenerativa de la médula. Suele deberse a hemorragia o a hemólisis.
Hemorragia
La pérdida aguda de sangre suele ser clínicamente evidente, por lo que resulta difícil que plantee un problema diagnóstico. La pérdida de hierro con los hematíes hace que la capacidad de respuesta de la médula sea moderada (IR = 3) y menos duradera que en el siguiente grupo. El tratamiento dependerá de la cuantía de la sangre perdida y de la gravedad de la anemia, y el pilar básico serán las transfusiones de hematíes.
Hemólisis
Las anemias por destrucción de los hematíes se caracterizan por un aumento importante del IR (mayor de tres veces el valor normal), lo que conduce a macrocitosis.
Las anemias hemolíticas pueden presentarse como cuadros agudos y autolimitados que, a su vez, pueden ser intra o extravasculares, o como formas crónicas de larga evolución. Las distintas formas de anemias hemolíticas se recogen en la tabla 9.
Anemias hemolíticas congénitas. Dentro de las hemólisis hereditarias se encuentran aquellas producidas por defectos en la membrana del hematíe, que alteran su forma normal y su capacidad de deformación al atravesar determinadas zonas de la circulación, principalmente el bazo, donde quedan atrapados y son destruidos. Otra causa de hemólisis congénita son las alteraciones enzimáticas del hematíe, como el déficit de piruvato-cinasa o de glucosa-6-fosfato-deshidrogenasa (G6PD).
La clínica en ambos grupos suele ser la superposición del síndrome anémico, esplenomegalia e ictericia por el aumento de bilirrubina no conjugada. Se genera mayor cantidad de pigmento biliar y, por tanto, es frecuente la historia familiar de cálculos biliares desde la infancia. La hiperplasia eritroide puede ser tan intensa que a veces se ven masas paravertebrales de focos de eritropoyesis extramedular. El diagnóstico se basa en un IR aumentado, un VCM normal o alto y valores de bilirrubina no conjugada y LDH elevados que apuntan al diagnóstico de hemólisis. El frotis de sangre periférica evidencia la presencia de esferocitos, eliptocitos, estomatocitos y cuerpos de Heinz. Otras pruebas, como la fragilidad osmótica de los hematíes o la autohemólisis (incubando los hematíes 48 h y comprobando su hemólisis espontánea), ayudan a confirmar el diagnóstico. El tratamiento, cuando la hemólisis es importante, suele ser la esplenectomía, aunque en ocasiones las crisis pueden ceder espontáneamente tras desaparecer la situación desencadenante. En casos graves pueden requerirse transfusiones, en espera del tratamiento definitivo.
Anemias hemolíticas adquiridas. Las anemias hemolíticas de mecanismo inmune están mediadas por anticuerpos, ya sean alo o autoanticuerpos. El grupo de las autoinmunes es muy heterogéneo, y son muy variados los anticuerpos dirigidos contra los antígenos de superficie de los hematíes. Los autoanticuerpos calientes, reactivos a temperaturas cercanas a 37 oC, originan en la mayoría de los casos una hemólisis extravascular por atrapamiento de los hematíes en el bazo o hígado. Por lo general suelen ser crónicas, poco intensas, y cursan con anemias leves o moderadas. En el hemograma se objetivará una anemia normocítica y normocrómica aunque, si está elevado el número de reticulocitos, puede ser macrocítica. El frotis de sangre periférica objetivará esferocitos, policromasia, punteado basófilo y hematíes nucleados en los casos graves. El estudio de la médula ósea pone de manifiesto hiperplasia de la serie roja con megaloblastosis y puede ayudar al diagnóstico de un síndrome linfo o mieloproliferativo al que van frecuentemente asociados. La positividad del test de Coombs directo permite diferenciar este tipo de hemólisis de las no autoinmunes, aunque puede existir un porcentaje mínimo con un resultado negativo. El Coombs indirecto es positivo hasta en un 80% de los pacientes.
El tratamiento dependerá de que se trate de un cuadro primario o secundario, en cuyo caso resulta fundamental tratar la enfermedad de base. Deben evitarse las transfusiones o recurrir a ellas solamente en caso de anemia grave, para lo cual se transfundirá isogrupo ABO y D. La base del tratamiento son los corticoides a dosis iniciales de 1 mg/kg/día de metilprednisolona, que se irán reduciendo hasta 20-30 mg/día cuando se compruebe el ascenso de la hemoglobina. A partir de ahí se continuará la reducción de dosis paulatinamente. La esplenectomía se reserva para el fracaso de los corticoides. Si fracasa se emplearán fármacos inmunodepresores, como la ciclofosfamida a dosis de 60 mg/m2 o la azatioprina a 80 mg/m2. El uso de gammaglobulinas i.v. no resulta tan eficaz como en otros procesos.
La hemólisis también puede ser debida a anticuerpos fríos o crioaglutininas, que producen aglutinación intravascular (acrocianosis) y hemólisis a temperaturas bajas. Pueden ir asociados a procesos linfoproliferativos o infecciosos y la anemia suele ser leve o moderada. El hemograma puede objetivar un «falso aumento» del VCM por la aglutinación, pero la extensión de sangre periférica a 37 oC permite distinguirlo de una verdadera macrocitosis. El diagnóstico se establece demostrando la existencia de crioaglutininas, que son bastante específicas de estos procesos.
En el tratamiento de las formas leves puede ser suficiente con evitar la exposición al frío. Los glucocorticoides y la esplenectomía no son tan eficaces como en el grupo anterior, por lo que si es necesario se re curre a plasmaféresis o al tratamiento de la enfermedad de base. En las formas idiopáticas puede resultar eficaz el interferón alfa a dosis de 3 a 5 millones U sema nales.
La hemoglobinuria paroxística a frigore es un tipo de anemia hemolítica autoinmune poco frecuente que suele ir asociada a procesos víricos (sobre todo en niños) y cursa con brotes de dolor abdominal, fiebre y escalo fríos que aparecen con el frío, duran 2 o 3 semanas y son autolimitados. En estos casos los test de Coombs directo e indirecto suelen ser negativos. La incubación de hematíes normales con suero del paciente a 4 oC y la comprobación de hemólisis, junto con el cuadro clínico compatible, suelen ser diagnósticas. En el tratamiento es básico evitar la exposición al frío hasta que el brote se autolimite.
La anemia hemolítica inmune inducida por fármacos puede obedecer a un doble mecanismo: como en la hemólisis inducida por anticuerpos calientes, cuyo mejor ejemplo es la alfametildopa, o como haptenos que se unen a la superficie del hematíe induciendo la formación de anticuerpos contra el complejo hematíe-fármaco, caso de la penicilina y la quinidina. El diagnóstico es sobre todo clínico, aunque puede confirmarse con un test de Coombs directo e indirecto, que será positivo siempre en el primer caso y sólo si se añade el fármaco en el segundo. Basta con suspender el fármaco implicado para controlar el cuadro.
En el grupo de anemias hemolíticas de causa mecánica, la rotura de los hematíes se produce por embates sufridos en la circulación, con la consiguiente hemólisis intravascular. Cuando la causa es macrovascular la anemia puede ser intensa y se observarán valores elevados de reticulocitos, esquistocitos, bilirrubina y descenso de la haptoglobina. El test de Coombs suele ser negativo y el tratamiento es el de la causa subyacente.
El grupo de mecanismo microangiopático es muy heterogéneo, y a la hemólisis se añaden los síntomas propios de cada proceso: en la púrpura trombótica trombocitopénica (PTT) y en el síndrome hemolítico urémico (SHU) las manifestaciones clínicas típicas, la anemia hemolítica con esquistocitos y test de Coombs negativo, trombopenia, insuficiencia renal y pruebas de coagulación normales deben hacer sospechar el diagnóstico. La plasmaféresis proporciona buenos resultados, aunque en ocasiones hay que mantener las sesiones durante varios meses. La utilidad de los corticoides es dudosa, y se puede recurrir a los inmunodepresores y esplenectomía si no se controla el cuadro con la plasmaféresis.
Las restantes causas de hemólisis descritas en la tabla 9 son poco frecuentes y deben sospecharse por la clínica y la relación directa con el agente causal. Así mismo el tratamiento suele ser la retirada de ese agente.
Por último, la hemoglobinuria paroxística nocturna (HPN) es una entidad producida por un defecto intracorpuscular adquirido de las células madre. Se caracteriza por anemia hemolítica, trombosis venosas y hematopoyesis ineficaz que, incluso, puede pasar por fases de verdadera anemia aplásica. El diagnóstico se sospecha en un paciente con clínica compatible, datos de hemólisis intravascular y un test de Ham y de lisis con sacarosa positivos. La confirmación se realiza con la determinación por citometría de flujo de las proteínas CD59 y CD55, que estarán disminuidas. En cuanto al manejo, las transfusiones se realizan tanto para aumentar las cifras de hemoglobina como para disminuir la producción de hematíes por la médula ósea. El uso de andrógenos y corticoides (15-30 mg de prednisona en días alternos) puede disminuir la hemólisis. Si la pérdida de hierro por orina es importante, puede ser necesario un aporte adicional, pero a veces debe administrarse asociado a corticoides o transfusiones para evitar la crisis hemolítica que comporta la formación de hematíes jóvenes. Los cuadros trombóticos se tratan igual que los de cualquier otra etiología, y para la hipoplasia medular se administrará globulina antitimocito a dosis de 150 mg/kg, 4 a 10 días, asociándola a corticoides. La única forma de erradicar completamente el clon anormal es el trasplante de médula ósea.
Bibliografía recomendada
Acedo Gutiérrez MS, Hernández Ruiz B, Giménez Mesa E. Anemias. En: Acedo Gutiérrez MS, Barrios Blandino A, Díaz Simón R, Orche Galindo S, Sanz García RM, editores. Manual de diagnóstico y terapéutica médica (4.ª ed.). Madrid: Hospital Universitario 12 de Octubre. Grupo MSD, 1998; 683-693.
Andrews NC. Disorders of Iron Metabolism. N Eng J Med 1999; 341: 1986-1995.
Babior BM, Bunn HF. Anemias megaloblásticas. En: Fauci AS, Braunwald E, Isselbacher KJ, Wilson JD, Martin JB, Kasper DL et al, editores. Harrison, principios de medicina interna (14.ª ed.). Madrid: McGraw Hill, 1998; 1: 745-753.
Barrett J, Saunthararajah Y, Molldrem J. Myelodysplastic syndrome and aplastic anemia: distinct entities or diseases linked by a common pathophysiology? Semin Haematol 2000; 37: 15-29.
Beutler E. Alteraciones de la hemoglobina. En: Fauci AS, Braunwald E, Isselbacher KJ, Wilson JD, Martin JB, Kasper DL et al, editores. Harrison, principios de medicina interna (14.ª ed.). Madrid: McGraw Hill, 1998; 1: 737-745.
Gilsanz Rodríguez F. Anemia: manifestaciones clínicas y clasificación. En: Enfermedades de la sangre. Medicine 7: 1169-1171.
Hillman RS. Anemia. En: Fauci AS, Braunwald E, Isselbacher KJ, Wilson JD, Martin JB, Kasper DL et al, editores. Harrison, principios de medicina interna (14.ª ed.). Madrid: McGraw Hill, 1998; 1: 379-84.
Hillman RS. Anemia ferropénica y otras anemias hipoproliferativas. En: Fauci AS, Braunwald E, Isselbacher KJ, Wilson JD, Martin JB, Kasper DL et al, editores. Harrison, principios de medicina interna (14.ª ed.). Madrid: McGraw Hill, 1998; 1: 729-737.
Provan D, Weatherall D. Red cells II: acquired anaemias and polycythaemia. Lancet 2000; 355: 1260-1268.
Rosse W, Bunn HF. Anemias hemolíticas y por pérdida aguda de sangre. En: Fauci AS, Braunwald E, Isselbacher KJ, Wilson JD, Martin JB, Kasper DL et al, editores. Harrison, principios de medicina interna (14.ª ed.). Madrid: McGraw Hill, 1998; 1: 753-767.
Spivak JL. The blood in systemic disorders. Lancet 2000; 355: 1707-1712.
Weatherall DJ, Provan AB. Red cells I: inherited anaemias. Lancet 2000; 355: 1169-1175.