El asma bronquial es un importante problema de salud mundial que consiste en un proceso inflamatorio crónico de las vías aéreas cuyos principales hallazgos inmunopatológicos son: edema; activación de los mastocitos; infiltración por células inflamatorias: neutrófilos (especialmente las agudizaciones), eosinófilos y linfocitos (tipo Th2); descamación del epitelio bronquial y, por último, depósito de colágeno bajo la membrana basal.
Esta inflamación contribuye a la hiperreactividad bronquial y a la limitación al flujo aéreo y, por lo tanto, a la presencia de signos y síntomas respiratorios como las sibilancias, la tos y la disnea y la cronificación del proceso, pudiéndose llegar a una remodelación o cambio permanente de la pared bronquial.
La atopia, entendida como la predisposición genética para la puesta en marcha de una respuesta mediada por IgE ante la inhalación de alergenos comunes, es el factor predisponente que se ha relacionado con más fuerza para desarrollar asma.
Es conocida la complejidad que comporta el abordaje y el tratamiento crónico del paciente asmático. Dicho tratamiento se debe basar en el reconocimiento y valoración de los síntomas, con el fin de establecer el grado de gravedad personalizado para cada paciente.
La evaluación global del paciente con asma debe incluir una historia médica y ambiental detalladas, centradas en los posibles desencadenantes alérgicos y no alérgicos, así como descartar otras enfermedades que puedan cursar con síntomas similares como, por ejemplo, infecciones respiratorias, bronquiectasias, enfermedad pulmonar obstructiva crónica (EPOC), insuficiencia cardíaca, disfunción de cuerdas vocales, etc. Asimismo, es necesaria la evaluación de la gravedad del proceso en función de una serie de parámetros.
La evaluación de la función pulmonar es esencial, no sólo para el diagnóstico, sino también para establecer la conducta terapéutica, ya que, aunque en ocasiones la correlación entre el grado de obstrucción bronquial y la gravedad clínica es pobre, un progresivo descenso de los valores espirométricos indica una mala evolución de la enfermedad. Especialmente en los pacien tes con un asma persistente moderada o grave, puede resultar útil la monitorización del flujo espirado máximo (FEM) con medidores portátiles, cuya variabilidad superior al 20% es indicativa de inestabilidad de la vía aérea.
Además de una exhaustiva valoración por parte del médico de los factores anteriormente citados, en los pacientes con asma se deben contemplar siempre otros aspectos que pueden contribuir a la gravedad del proceso, como presencia de tabaquismo (activo y pasivo); identificación de exposición a alergenos, o realización de estudios alergológicos. Esto debe incluir también posibles exposiciones laborales y la sensibilidad a los sulfitos; utilización de otros medicamentos, especialmente bloqueantes beta (incluidos los preparados oftalmológicos); investigar la historia de sensibilidad a la aspirina y los antiinflamatorios no esteroides (AINE), que están desaconsejados en algunos pacientes con asma, especialmente en aquellos con sospecha o historia de intolerancia a los AINE, asma moderada-grave y/o rinosinusitis poliposa, y tratamiento, si es necesario, de otros procesos como el reflujo gastroesofágico, que contribuyen a la gravedad del asma.
Clasificación del asma (por escalones de gravedad)1,2
Asma leve intermitente
Este grupo engloba el 60-70% de los asmáticos. Las características son: sintomatología intermitente inferior a una vez al mes; agudizaciones escasas (¾ cuatro por año) y breves (pocas horas o días), y síntomas nocturnos menos de dos veces al mes.
Las características funcionales son: exploración funcional normal entre agudizaciones; FEM o FEV1 superiores al 80% del valor de referencia; variabilidad de los valores del FEM menores del 20%.
Asma leve persistente
Los síntomas son intermitentes, aparecen más de una vez por semana y menos de una vez al día. Cursa con agudizaciones que pueden afectar la actividad diaria y aparecen síntomas nocturnos más de dos veces al mes.
Las características funcionales son: FEM o FEV1 superior al 80% del valor de referencia y variabilidad del FEM entre el 20 y el 30%.
Asma moderada
Los síntomas son intermitentes y diarios con agudizaciones que afectan a la actividad diaria y los síntomas nocturnos aparecen más de una vez por semana.
Las características funcionales son: FEM o FEV1 entre el 60 y el 80% del valor de referencia y variabilidad del FEM superior al 30%.
Asma grave
Los síntomas son continuos con importante necesidad de utilización de ß adrenérgicos de acción rápida, cursa con agudizaciones frecuentes y actividad diaria francamente limitada. Los síntomas nocturnos son frecuentes (casi diarios).
Las características funcionales son: FEM o FEV1 inferior al 60% del valor de referencia y variabilidad del FEM superior al 30%.
Una vez se ha valorado a un paciente con asma, éste será ubicado en el grado correspondiente, con la utilidad de permitirnos diseñar un plan de actuación y teniendo en cuenta las siguientes consideraciones:
La clasificación debe de ser dinámica, ya que la variabilidad de los pacientes hace que pueda cambiar su situación en breves espacios de tiempo. Es importante, pues, una revaluación periódica, cada 3-6 meses, en el asma controlada.
En caso de duda a la hora de clasificar un paciente o bien en caso de control insuficiente de la enfermedad, se ubicará al paciente en el grado de gravedad inmediatamente superior.
Un control sostenido a lo largo de 3 meses permite el descenso a un grado inferior.
Un paciente del grado 1 (asma leve intermitente) también debe seguir controles regulares, ya que no está exento de poder presentar un empeoramiento de la enfermedad o incluso una agudización grave aunque entre períodos quede asintomático.
Medicamentos empleados en el control del asma a largo plazo
Los principales son antiinflamatorios (corticoides, cromonas), broncodilatadores (ß2-adrenérgicos, anticolinérgicos y metilxantinas) y otros como los moduladores de los leucotrienos.
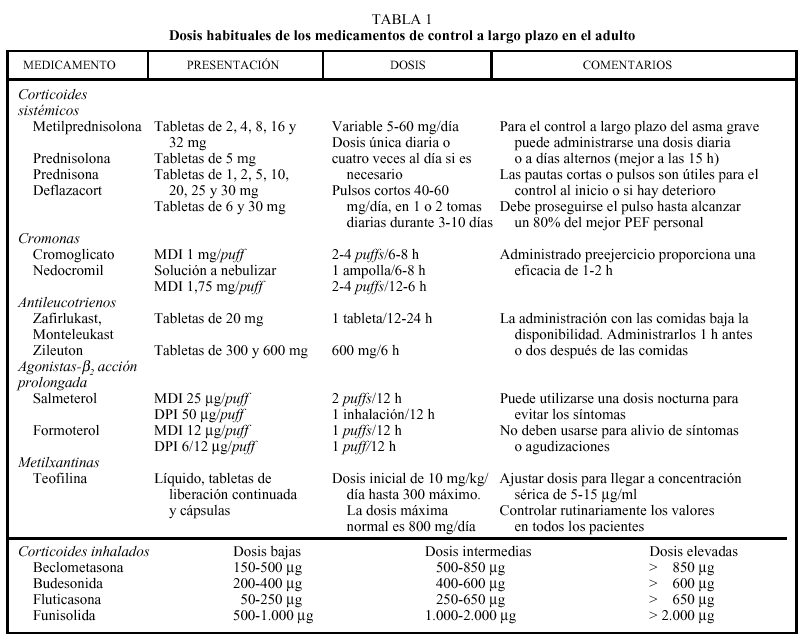
Las dosis habituales de estos medicamentos están reflejadas en la tabla 1.
Corticoides (glucocorticoides)
Constituyen los agentes terapéuticos antiinflamatorios más potentes y eficaces disponibles contra el asma, pueden administrarse de forma inhalada o sistémica.
Inhalados (dipropionato de beclometasona, budesonida, propionato de fluticasona)
Indicaciones. Asma persistente. Prevención a largo plazo de los síntomas. Control e inhibición de la inflamación. Disminución de la necesidad de corticoides sistémicos.
Mecanismos de acción. Antiinflamatorio (disminución de citocinas, inhiben la adhesión, activación y migración celular, etc.). Intervienen en la regulación de los receptores ß2.
Efectos secundarios. Locales: tos, disfonía, Muguet. La repercusión sistémica (p. ej., osteoporosis, equímosis, retraso crecimiento infantil, bloqueo suprarrenal) todavía es controvertida, no obstante, y teniendo en cuenta que está relacionada con la dosis y la propia susceptibilidad individual, debe sopesarse siempre ante dosis elevadas.
Otros aspectos. Los nuevos sistemas de inhalación han disminuido la absorción sistémica y los efectos secundarios locales y han mejorado la eficacia y la llegada del fármaco a las vías aéreas bajas.
Sistémicos (metilprednisolona, prednisona, prednisolona, deflazacort)
Indicaciones. «Pulsos» a corto plazo (pautas cortas de 3-10 días, que suele ser lo necesario para alcanzar el 80% del mejor FEM personal) para conseguir el control de agudizaciones graves o asma no controlada. Prevención a largo plazo en el asma persistente grave.
Mecanismos. Igual que los corticoides inhalados.
Efectos secundarios. A corto plazo: alteraciones en el metabolismo de la glucosa, apetito, retención hídrica, aumento de peso, alteración del humor, hipertensión, úlcera péptica. A largo plazo: osteoporosis, bloqueo del eje suprarrenal, inhibición del crecimiento, adelgazamiento dérmico, hipertensión, diabetes, síndrome de Cushing iatrogénico, cataratas, miopatía, alteraciones inmunológicas (más infrecuente).
Otros aspectos. Se deben utilizar en la mínima dosis eficaz y, a ser posible, en monodosis diaria (su administración a las 15 h mejora la eficacia y disminuye el bloqueo suprarrenal). Considerar otros fármacos (rifampicina, anticonvulsionantes, etc.) que pueden interferir en su metabolismo. Considerar enfermedades que pueden empeorar con su uso (herpes-varicela, tuberculosis, hipertensión, diabetes, úlcera péptica).
Cromoglicato sódico y nedocromil (cromonas)
En la actualidad cada vez están más en desuso.
Indicaciones. Tratamiento profiláctico de los síntomas, especialmente antes de la exposición a alergenos conocidos o a la realización de ejercicio físico.
Mecanismos. Este AINE estabiliza la membrana de los mastocitos y bloquea los mediadores inflamatorios, inhibiendo la reacción ante el estímulo alergénico.
Efectos secundarios. Son muy escasos (mal sabor de boca, etc.). La seguridad es su principal ventaja.
Otros aspectos. Su administración es de forma inhalada. Suelen tener eficacia terapéutica a partir de las 2-3 semanas.
Agonistas ß2-adrenérgicos
De acción prolongada (salmeterol, formoterol)
Indicaciones. Prevención sintomática a largo plazo. Son especialmente útiles en el control de los síntomas nocturnos y los inducidos por el ejercicio. Asimismo, son muy eficaces en combinación con corticoides inhalados para el control de los síntomas.
Mecanismos. Broncodilatación (relajan el músculo liso bronquial). In vitro, inhiben la liberación de media-
dores inflamatorios.
Efectos secundarios. Taquicardia, ansiedad, temblor muscular, cefalea y más raramente hipopotasemia y aumento del intervalo QT.
Otros aspectos. En la actualidad ya se acepta el formoterol para el tratamiento de síntomas agudos. La aparición de tolerancia, aunque cierta, parece tener poca repercusión clínica. No deben sustituir al tratamiento antiinflamatorio de base. En combinación con corticoides inhalados, son de una gran eficacia en el control de los síntomas. Existe poca experiencia en su utilización por vía oral. Su acción se inicia a los pocos minutos (más rápida para el formoterol), es máxima a las 2 h y dura unas 12 h.
De acción corta (salbutamol, terbutalina, albuterol, bitolterol, pirbuterol)
Indicaciones. Alivio rápido de los síntomas agudos. También se pueden usar antes del ejercicio para el broncospasmo inducido por éste.
Mecanismos. Igual que los de acción prolongada.
Efectos secundarios. Equivalentes a los de acción prolongada. Se debe tener especial precaución en pacientes ancianos y con cardiopatía previa.
Otros aspectos. Es el fármaco de elección para el broncospasmo agudo. La vía inhalatoria es más rápida y segura que la sistémica. Un incremento en su utilización o bien la ausencia del efecto esperado indican un control inadecuado del asma. Su acción se inicia rápidamente y dura 5-6 h.
Anticolinérgicos (bromuro de ipratropio)
Indicaciones. Alivio del broncospasmo agudo, son una alternativa cuando no se pueden usar los ß2 o en el broncospasmo debido a medicación betabloqueadora.
Mecanismos. Broncodilatación por inhibición de los receptores muscarínicos. Disminuyen el tono vagal. Pueden disminuir la secreción glandular de moco.
Efectos secundarios. Sequedad bucal.
Otros aspectos. Se utilizan por vía inhalatoria y revierten sólo el broncospasmo colinérgico. No bloquean el broncospasmo inducido por el ejercicio. Tienen un inicio de acción más lento (30 min) que los agonistas ß2 de acción rápida pero también algo más duradero (4-5 h). En la actualidad, su principal papel está en la EPOC.
Metilxantinas (teofilina a modo de tabletas y cápsulas de liberación continuada)
Es otro grupo farmacológico cuya importancia en el tratamiento del asma ha ido decreciendo durante los últimos años.
Indicaciones. Prevención y control a largo plazo de los síntomas (especialmente los nocturnos). Tratamiento de las agudizaciones (por vía intravenosa).
Mecanismos. Broncodilatación mediante inhibición de la fosfodiesterasa. Influye en la infiltración linfocitaria y eosinofílica. Aumenta la contractilidad diafragmática y el aclaramiento mucociliar.
Efectos secundarios. En dosis terapéuticas pueden aparecer insomnio, alteraciones gastrointestinales, dificultad en la micción especialmente en ancianos con prostatismo. A dosis tóxicas puede ocasionar taquicardia, vómitos, arritmias, estimulación del sistema nervioso central, cefalea, convulsiones, hiperglucemia e hipopotasemia.
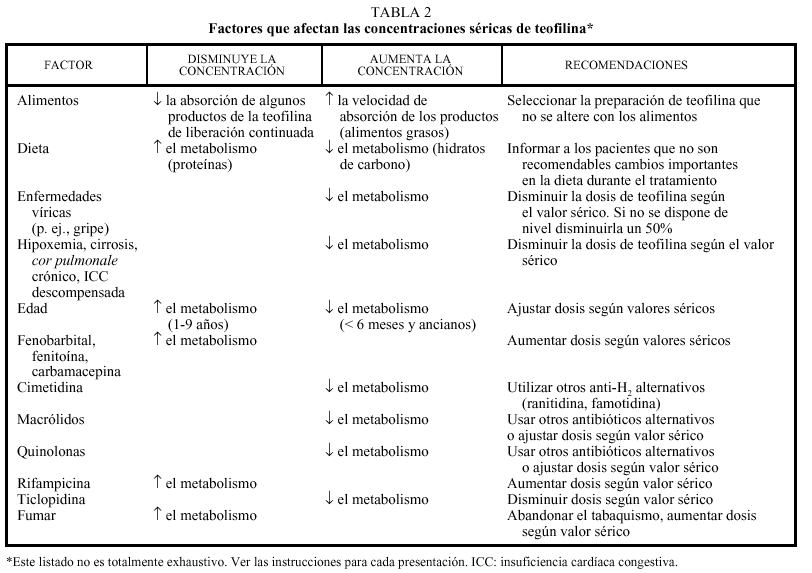
Otros aspectos. Su gran inconveniente es el escaso índice terapéutico (diferencia entre valores terapéuticos y tóxicos), por lo que se debe determinar su concentración sérica de forma sistemática. Además existe una gran variabilidad en cuanto a su aclaramiento metabólico entre individuos y ante la presencia de múltiples factores (tabla 2).
Moduladores de los leucotrienos (zafirlukast, montelukast, panlukast, zileuton)
Constituyen la línea más novedosa de tratamiento del asma. Se administran en tabletas o comprimidos.
Indicaciones. Prevención y control a largo plazo de los síntomas en el asma persistente.
Mecanismos. Inhiben la acción de los leucotrienos (LC4 y LD4), que son mediadores celulares que actúan como potentes broncoconstrictores y productores de moco. Realizan la acción antagonizando el receptor del leucotrieno (zafirlukast, montelukast, panlukast) o inhibiendo la 5-lipooxigenasa (zileuton).
Efectos secundarios. Constituyen un nuevo grupo de fármacos y hasta la fecha no se han detectado efectos secundarios específicos. Se ha descrito un caso de hepatitis hiperbilirrubinémica reversible y, en algunos casos, elevación de las enzimas hepáticas. En trabajos recientes, se ha suscitado polémica en torno a la aparición de algunos casos aislados de síndrome de Churg-Strauss en pacientes con asma dependiente de corticoides que habían empezado tratamiento con alguno de los antagonistas del receptor leucotrieno. Este hecho se ha atribuido a que la reducción en las necesidades de glucocorticoides permitió aflorar la vasculopatía subyacente. En cualquier caso, está pendiente la realización de nuevos estudios de casos y controles3.
Dispositivos de administración inhalada de los fármacos
Inhaladores dosificadores (MDI)
Se emplean con agonistas ß2, anticolinérgicos, corticoides y cromonas. Se administran pulsando el dispositivo durante una inhalación profunda y lenta, manteniendo, posteriormente, la respiración durante 10 s. En condiciones de laboratorio, se encontró que la técnica de la boca abierta (manteniendo el MDI a unos 3 cm de la boca abierta) aumentaba la distribución pulmonar del fármaco; no obstante, no se ha demostrado un beneficio clínico de esta forma respecto a la administración con boca cerrada (cerrando los labios alrededor de la pieza bucal del MDI).
El principal inconveniente que tienen es que la inha lación lenta es difícil y la coordinación de la administración y la maniobra respiratoria complicada, sobre todo en niños y ancianos, por lo que es frecuente su utilización incorrecta, perdiendo así eficacia de absorción pulmonar y aumentando la absorción sisté mica por depósitos orofaríngeos (esto último puede minimizarse parcialmente con lavado bucal postadministración).
MDI activados por la respiración (autohaler)
Se emplea con agonistas ß2. La maniobra de inhalación, que debe ser semejante a la del MDI convencional, aunque algo más rápida, dispara el mecanismo de forma automática. Esto es especialmente útil en aquellos pacientes incapaces de coordinar la administración y la inhalación del MDI convencional. Como desventaja, cabe destacar que no puede utilizarse con las cámaras de inhalación existentes.
Cámaras espaciadoras de inhalación (volumatic, nebuhaler, fisonair, aerocámaras, etc.)
Se realiza una respiración normal o lenta tras la administración del fármaco en la cámara. Se debe realizar un solo puff por inhalación para las cámaras con boquilla, mientras que las que tienen mascarilla permiten de 3 a 5 puffs por administración.
Son más sencillas de usar que los MDI solos, facilitando así la administración a niños y personas con dificultad para coordinar las maniobras, pudiendo llegar a ser tan eficaces como las nebulizaciones para las agudizaciones. Además, disminuyen el depósito orofaríngeo de corticoides.
Inhaladores de polvo seco (DPI)
Se emplean con agonistas ß2, corticoides. En general requieren una inhalación profunda y rápida, aunque el flujo inspiratorio mínimo necesario puede variar en función del tipo de dispositivo.
La distribución puede ser mayor o igual que en los MDI, dependiendo del dispositivo y de la técnica, y en general son sencillos de utilizar y de efecto constante. Entre los inconvenientes destaca que requieren un flujo inspiratorio mínimo y si el paciente espira la dosis se pierde. El lavado bucal es eficaz para reducir la absorción sistémica.
Existen diferentes tipos de dispositivos de polvo seco. La industria farmacéutica realiza un esfuerzo continuado para el diseño de nuevos dispositivos o el perfeccionamiento de los existentes, hasta el momento existen los siguientes:
Accuhaler: salmeterol, fluticasona (solos o combinados en el mismo producto).
Aerolizador: formoterol.
Easyhaler: salbutamol, beclometasona.
Rotahaler: salbutamol, beclometasona.
Turbuhaler: terbutalina, budesonida, formoterol.
Nebulizadores
Se emplea con agonistas ß2, cromonas, anticolinérgicos y corticoides.
Puede usarse en niños de menos de 2 años, en personas que no pueden utilizar ningún otro sistema de inhalación y, especialmente, para administrar broncodilatadores durante las agudizaciones moderadas o graves, aunque por su tamaño y consumo de tiempo se utiliza principalmente en el ámbito hospitalario.
Es importante ajustar bien las mascarillas, para que el paciente pueda respirar normalmente sin preocuparse de la coordinación o cooperación.
Esquema terapéutico a largo plazo del asma
Basado en la clasificación por escalones de gravedad expuesta anteriormente, se puede establecer un plan terapéutico farmacológico gradual1,2, lo más simple posible, enfocado para ayudar en el tratamiento del asma a largo plazo, aplicable en adultos y niños de más de 5 años, y que controle aspectos clínicos, funcionales y proporcione, como se ha demostrado en algunos trabajos, mejoras en la calidad de vida4. Se describe a continuación.
Nivel 1. Asma leve intermitente
No se precisa medicación diaria. Se deben prescribir agonistas ß2 inhalados de acción rápida a demanda, para el control de los síntomas cuando aparezcan o de forma preventiva en el broncospasmo inducido por el ejercicio.
Nivel 2. Asma persistente leve
Se deben prescribir corticoides inhalados (dosis bajas o intermedias) diariamente más agonistas ß2 inhalados de acción rápida a demanda.
Las cromonas y la teofilina son otras alternativas terapéuticas diarias, aunque no las preferidas.
Nivel 3. Asma persistente moderada
Se deben prescribir corticoides inhalados (diarios, dosis intermedias) más agonistas ß2 inhalados de acción prolongada (diarios, especialmente útiles para los síntomas nocturnos) más agonistas ß2 inhalados de acción rápida a demanda.
En caso de un control deficiente de los síntomas, se pueden también considerar como alternativa a los agonistas ß2 de acción prolongada la utilización diaria de antagonistas de los leucotrienos o teofilina de liberación continuada, así como incrementar las dosis del corticoide inhalado.
Nivel 4. Asma persistente grave
Se deben prescribir corticoides inhalados (diarios, dosis elevadas) más agonistas ß2 inhalados de acción prolongada (diarios) más corticoides orales más agonistas ß2 inhalados de acción rápida a demanda.
Se pueden emplear otros broncodilatadores (teofilina, ipratropio), así como, también, antagonistas de los leucotrienos. En este punto es importante la valoración por un especialista y la orientación individualizada de cada caso.
Consideraciones no farmacológicas y puntos clave del tratamiento
El plan terapéutico gradual descrito presenta unas pautas generales de ayuda en la toma de decisiones clínicas. No pretende ser una prescripción específica, ya que el asma es un trastorno variable y los médicos deben adecuar los tratamientos según las necesidades y circunstancias de cada paciente.
Se debe conseguir el control clínico lo más rápidamente posible; por esto, es recomendable iniciar el tratamiento en un nivel superior (p. ej., con un ciclo de corticoides orales o dosis elevadas de corticoides inhalados), para después disminuir de forma paulatina el tratamiento hasta la dosis mínima necesaria.
Son importantes las visitas regulares de seguimiento, en las que se debe monitorizar la gravedad del asma con medidas clínicas objetivas y de función pulmonar. Incluso en el asma clínicamente controlada se aconseja una evaluación cada 3-6 meses.
Es fundamental enseñar al paciente y su familia los rasgos básicos de la enfermedad y su tratamiento, y mejorar, entre otras cosas, la ansiedad que la enfermedad provoca. También es importante educar en las técnicas de utilización de inhaladores (que se deben revisar periódicamente) y en el autotratamiento.
Se deben estudiar e identificar los posibles factores desencadenantes así como las medidas de control ambiental para evitar alergenos e irritantes.
Se debe desarrollar un plan de actuación en caso de agudización, especialmente en aquellos pacientes con el antecedente de exacerbaciones graves.
Es importante destacar que el aumento de las necesidades del agonista ß2 de acción rápida indica que se debe subir un nivel e iniciar tratamiento adicional a largo plazo.
En cualquier momento y nivel terapéutico puede ser necesario un tratamiento de rescate con un ciclo de corticoides sistémicos, que se deben iniciar de forma temprana. Se debe prestar especial atención a algunos pacientes que presentan agudizaciones graves potencialmente letales separadas por períodos sin o con pocos síntomas y con función pulmonar normal.
Se deben vigilar los posibles efectos secundarios e interacciones farmacológicas de los medicamentos utilizados para el asma.
Siempre que existan dificultades para alcanzar o mantener el control del asma, especialmente en los niveles 3 y 4, es recomendable la derivación del paciente a un especialista en asma.
Formas y situaciones especiales de asma
Asma y ejercicio físico
Es frecuente que, con el ejercicio físico, especialmente si es prolongado e intenso, los asmáticos presenten broncospasmo. No obstante, es muy importante hacer una valoración correcta individualizada, ya que sería una mala orientación apartar de forma rutinaria a los pacientes de los deportes. Por el contrario, sí se debe encaminar a los pacientes hacia la integración máxima en las actividades deportivas. De hecho, son conocidos numerosos casos de grandes deportistas asmáticos (p. ej., un 9% de la selección olímpica norteamericana de Los Ángeles en 1994 tenían asma inducida por el ejercicio). El diagnóstico suele ser clínico, aunque se puede confirmar con estudios espirométricos tras la realización de un esfuerzo.
La alteración fisiopatológica implicada es la pérdida de calor y humedad del epitelio bronquial durante la hiperventilación secundaria al ejercicio, aunque también se han descrito otros mecanismos relacionados, como cambios vasculares, cambios en la osmolaridad e incluso hipocapnia.
El tratamiento pasa, en primer lugar, por intentar tomar algunas medidas no farmacológicas, como un buen precalentamiento en una atmósfera caliente y húmeda (p. ej., el deporte de mayor incidencia es el patinaje sobre hielo, y el de menor la natación), respirar por la nariz, valorar el contexto alergológico, evitar ejercicios intensos tras una agudización reciente. En cuanto a los fármacos, la medida más eficaz es la prevención con inhalación previa al ejercicio de agonistas ß2, que se pueden complementar con la administración de cromonas y/o antagonistas de los leucotrienos. Es importante, dada la potencia de los agonistas ß2, aconsejar las dosis adecuadas.
Asma y embarazo
El embarazo comporta una serie de cambios anatómicos y endocrinológicos que repercuten en la función respiratoria de una mujer normal, y por tanto también de una mujer asmática. Tradicionalmente se ha dicho que el embarazo puede influir en el asma en cualquier sentido (mejorarlo, agravarlo o no modificarlo).
El médico que trate el asma de una mujer embarazada se puede encontrar con una serie de dificultades psicológicas y medicamentosas que pueden influir en la decisión terapéutica. No obstante, se debe destacar que, aunque la mayoría de los fármacos antiasmáticos atraviesan la barrera placentaria, los que constituyen el pilar terapéutico del asma, es decir, los agonistas ß2 adrenérgicos y los corticoides, son seguros durante el embarazo y el beneficio que producen supera el riesgo potencial que pudieran tener.
En este sentido, el principal riesgo de una embarazada asmática es ser tratada por debajo de sus posibilidades farmacológicas. Se debe transmitir tranquilidad y seguridad a la mujer, y hay que hacerle saber que la situación que comporta mayor riesgo es la de tener el asma mal controlada, ya que las agudizaciones graves y la hipoxia sí pueden suponer riesgo fetal5. Por otro lado, las indicaciones de cesárea urgente son las mismas que para la embarazada no asmática, y tan sólo en algunos casos muy determinados de asma grave se puede considerar una cesárea electiva con la gestación a término.
Asma e intolerancia al ácido acetilsalicílico
Aunque variable, la cifra de prevalencia de intolerancia a la aspirina (AAS) en la población asmática general se sitúa en torno al 5%, aunque probablemente esta cifra sea mayor (20-30%) en los asmáticos graves. El cuadro clínico se suele presentar de forma aguda, minutos después de la ingesta, y provoca rinitis, conjuntivitis, y broncospasmo, a menudo intenso, y en algunas ocasiones puede ser muy grave y con desenlace fatal. Se puede presentar en cualquier edad, incluso después de haber tolerado el AAS en ocasiones anteriores. Aunque la dosis que puede provocar una crisis es individual, en general, la reacción de intolerancia es dependiente de la dosis.
La teoría etiopatogénica de este fenómeno hace referencia a la interferencia que realiza el AAS en el metabolismo del ácido araquidónico, ya que inhibe la acción de una enzima denominada ciclooxigenasa (bloqueando la síntesis de prostaglandinas y tromboxanos), y reconduce su acción a través de otra enzima, la lipooxigenasa, favoreciendo la síntesis de leucotrienos, que tienen una potente acción broncoconstrictora. También se han implicado otros fenómenos, como sería una reacción anormal de las plaquetas que favorecería la producción de radicales libres.
Debido a la similitud en la estructura química y el mecanismo de acción, la mayoría de pacientes asmáticos con intolerancia a la aspirina también presentan reacciones frente a otros AINE y también suelen ser dependientes de la dosis, siendo la indometacina el más potente inhibidor de la ciclooxigenasa. Los fármacos más seguros para los pacientes con este tipo de asma son: paracetamol, dextropropoxifeno, salicilatos sin actividad anticiclooxigenasa (salicilato sódico, salicilamida, trisalicilato magnésico), y los nuevos inhibidores selectivos de la COX-2 (nimesulide, meloxicam, rofecoxib, celecoxib).
Para el diagnóstico de intolerancia al AAS, la anamnesis es orientativa pero no es segura, y tampoco existen pruebas in vitro; así las pruebas de provocación constituyen el diagnóstico de certeza. Deben realizarse por personal experimentado, y se puede usar una provocación por vía oral, inhalada (bronquiales) o nasal, valorándose la respuesta espirométrica y rinomanométrica respectivamente.
El tratamiento comprende los siguientes puntos:
Prevención de la exposición, especialmente en los pacientes con sospecha de crisis provocadas por AINE, asma moderada-grave o historia de rinosinusitis poliposa. Los glucocorticoides y los nuevos inhibidores selectivos de la COX-2 son los mejores tratamientos antiinflamatorios de corta duración para estos pacientes.
Desensibilización o tolerancia con pruebas de provocación sucesivas con dosis progresivas, según los individuos y respuestas. Este tratamiento está especialmente indicado en aquellos casos que precisan tratamientos continuados con estos fármacos (p. ej., enfermedades reumáticas, en la cardiopatía isquémica como antiagregante, etc.).
Asma corticorresistente
En la mayoría de los pacientes con asma, los corticoides son muy efectivos. De todos modos, existe una variabilidad en la respuesta biológica y clínica, y algunos pacientes presentan síntomas persistentes y no mejoran lo esperado a pesar del uso de dosis altas de corticoides inhalados y orales. Debido, precisamente, a este espectro continuado de respuesta no existe una definición universal de corticorresistencia, aunque de una forma pragmática se acepta que la mejora del FEV1 inferior al 15%, y que sí responde a agonistas ß2, tras un tratamiento con 40 mg/día de prednisona durante 2 semanas es indicativa de resistencia a los corticoides. Este problema dificulta de un modo importante el control de estos pacientes por la falta de un tratamiento alternativo adecuado.
En primer lugar, se deben descartar los factores asociados que puedan contribuir a esta resistencia al tratamiento (diagnóstico o tratamiento inadecuado, mal cumplimiento del tratamiento, reflujo gastroesofágico, sinusitis crónica, alergenos, factores psicológicos, etc.).
De las formas primarias de origen genético existen pocos datos debido a su baja frecuencia. Probablemente, la mayoría de los pacientes con resistencia a los corticoides presentan alteraciones en la configuración del receptor intracelular por el que realiza su acción el glucocorticoide, dichas alteraciones podrían estar inducidas por el mismo proceso inflamatorio6.
En cualquier caso, cuando una vez estudiado debidamente un paciente, se detecte una resistencia importante o completa a los corticoides está indicado reducir estos medicamentos, a fin de evitar los posibles efectos secundarios y valorar otras alternativas terapéuticas (broncodilatadores, otros antiinflamatorios, etc.).
Asma y reflujo gastroesofágico
El reflujo gastroesofágico (RGE) aparece cuando se produce una relajación transitoria del esfínter de la unión gastroesofágica y disminuye la presión intraluminal, permitiendo así el movimiento retrógrado del contenido gástrico. La mayoría de pacientes con RGE presentan también hernia de hiato, condición patológica que favorece su existencia, aunque no necesariamente vayan siempre unidas. El síntoma guía del RGE es la pirosis, aunque no es específico. Con el tiempo puede dar lugar a una esofagitis.
La prevalencia de RGE en la población general es del 5%, y aumenta mucho en la población asmática que, aunque es variable según diferentes estudios con diferentes métodos diagnósticos y selección de pacientes, se cifra alrededor del 50-60%, teniendo especial relevancia en los asmáticos de difícil control7.
En la relación entre la presencia de RGE y la aparición de síntomas asmáticos se han implicado principalmente dos mecanismos patogénicos: la estimulación vagal por excitación neuronal esofágica y las microaspiraciones. En algunos trabajos se han encontrado caídas del pH esofágico asociadas a caídas del pH traqueal y esto, a su vez, relacionado con disminuciones del peak flow.
Aunque el abanico de exploraciones complementarias con finalidad diagnóstica es muy amplio, en la actualidad existe un consenso generalizado de considerar la pH-metría ambulatoria como la técnica de elección para el cribado diagnóstico, y otras técnicas como la endoscopia han quedado reservadas a pacientes con sintomatología franca, disfagia o ausencia de respuesta al tratamiento.
En cuanto al tratamiento para el RGE, principalmente, se considerarán tributarios de realizarlo principalmente dos grupos de pacientes: por un lado, aquellos que, independientemente de la gravedad del asma, presenten clínica franca de enfermedad por RGE, y por otro, los asmáticos de difícil control ya que constituyen un grupo de elevada prevalencia de RGE aunque a menudo sea asintomático.
El tratamiento pasa, en primer lugar, por medidas dieteticoposturales, como la reducción de la ingesta de grasas, evitar el decúbito supino dos horas tras la ingesta y levantar unos 10-15 cm el cabezal de la cama. Los fármacos de elección son los antisecretores como los anti-H2 o el omeprazol en casos más graves. También se pueden emplear medicamentos procinéticos como la cisaprida. En casos rebeldes al tratamiento médico o en caso de necesidad de tratamiento de por vida, es aconsejable la valoración de la cirugía. En este caso la técnica de elección es la fundoplicatura de Nissen. La utilización de una técnica quirúrgica de entrada no ha mostrado efectos beneficiosos sobre el asma con respecto al tratamiento farmacológico8.