La tuberculosis es una infección bacteriana, transmisible y prevenible, con una amplia variedad de manifestaciones, cuyo agente etiológico es el denominado bacilo de Koch.
Es una enfermedad que ha afectado al hombre desde la más remota antigüedad. Existen evidencias del padecimiento humano desde 3.700 años a.C., y se cree que la tuberculosis humana se desarrolló en Europa y en el Cercano Oriente en el período Neolítico, entre 6.000-8.000 años a.C.
A lo largo de la historia, la tuberculosis ha tenido diferentes denominaciones, entre las cuales la más popular fue la de tisis, pero también se llamó peste blanca, enfermedad del mal de vivir, consunción o proceso fímico.
La epidemia actual1 comenzó en Inglaterra durante el siglo xvi y quizá alcanzó su momento álgido alrededor de 1780, como consecuencia de la Revolución Industrial y el crecimiento de las ciudades, lo cual permitió la diseminación de la enfermedad de persona a persona. La enfermedad se transmitió con rapidez desde Inglaterra hacia Europa occidental, alcanzando su momento álgido a principios del siglo xix. En Europa del este, el valor máximo se hizo evidente a finales del siglo xix y a principios del xx en Norteamérica y Sudamérica. En los países en desarrollo de Asia y África, la onda epidémica aún no ha alcanzado su álgido. Como fenómeno mundial, la epidemia disminuye en una zona geográfica, mientras que permanece, aumenta o apenas alcanza su máximo en otras regiones.
Durante la primera mitad del siglo xx, con la mejora de las condiciones de vida comenzó un declive, fundamentalmente en los países desarrollados, alcanzándose una disminución promedio anual del 5%. Este descenso se aceleró hasta el 15% anual a partir de 1950 con la aparición de fármacos eficaces para el tratamiento de la enfermedad. Es a partir de la década de los ochenta cuando comienza lo que se ha denominado «resurgimiento» de la enfermedad, como grave problema de salud pública.
Agente causal
El descubrimiento del agente etiológico de la tuberculosis y la publicación en el año 1882 de Die Aetiologie der Tuberculose2, en la que Koch describía el bacilo tuberculoso, causó gran conmoción en el mundo científico de la época.
El llamado bacilo de Koch pertenece al genero Mycobacterium, el cual comprende más de 50 especies. Las micobacterias capaces de producir enfermedad tuberculosa son las que pertenecen al denominado complejo tuberculosis: M. tuberculosis, M. bovis, M. africanun y M. microtti. Con mucho, el agente causal más frecuente es M. tuberculosis, un bacilo ácido-alcohol resistente, aerófilo, de división lenta, sensible a la luz solar, a la ultravioleta y al calor, así como a algunos desinfectantes de elevado y mediano nivel. Resistente a la desecación, puede persistir durante largos períodos de tiempo en esputos desecados que no estén expuestos a la luz solar.
Transmisión
Vía aérea
La vía aérea es, con mucho, la más importante en la transmisión de la enfermedad. Aunque la tuberculosis puede afectar a cualquier órgano, el pulmón es la vía de entrada en prácticamente todos los casos. El contagio suele producirse a partir de un enfermo de tuberculosis pulmonar, bronquial o laríngea, que al hablar, reír, cantar, toser o estornudar expulsa al aire pequeñas partículas de secreciones respiratorias que contienen bacilos. Estas gotitas respiratorias tienen un tamaño variable, desde partículas relativamente grandes de tamaño superior a 10 µ (gotas de Pfluger), que no son operativas puesto que sedimentan sobre las superficies vecinas y, aún en el caso de ser inhaladas, quedan atrapadas en las vías respiratorias altas o bien son deglutidas, por tanto no pueden considerarse infecciosas, aunque contengan bacilos tuberculosos. Sin embargo, algunas de las gotitas respiratorias exhaladas se evaporan casi completamente antes de sedimentarse y forman núcleos que se desplazan en el aire ambiental1. Son partículas pequeñas (1-5 µ) que contienen 1-3 bacilos tuberculosos y son capaces de iniciar la infección, ya que se mantienen suspendidas en el aire y pueden ser inhaladas y alcanzar el alvéolo pulmonar, donde encuentran las condiciones idóneas para implantarse3,4. Los pacientes con tuberculosis generalmente tosen de manera enérgica y expulsan gran cantidad de gotitas que contienen bacilos tuberculosos infecciosos en potencia. El contacto íntimo con personas enfermas de tuberculosis respiratoria (baciloscopia positiva) aumenta al máximo el riesgo de infección. La capacidad del bacilo para ocasionar infección en nuevos contactos expuestos depende de las defensas del huésped. Los diferentes estudios demuestran que la tasa de infección de los contactos íntimos varía del 25 al 50%, aun en casos de gran hacinamiento y condiciones de miseria5.
Vía digestiva
Actualmente, en nuestro medio es poco importante debido al consumo mayoritario de leche pasteurizada. La transmisión se produce al ingerir leche de vaca enferma sin higienizar.
Otras vías
La vía transplacentaria puede considerarse extremadamente rara, y la transmisión por inoculación puede ocurrir en personas que manejan muestras, como trabajadores de laboratorios de microbiología, etc.
Factores que condicionan la transmisión6-8
La contagiosidad del foco depende de la fuente contagiante, de la intimidad del contacto y del tratamiento que recibe el foco.
Fuente contagiante
Fundamentalmente transmiten la enfermedad los enfermos bacilíferos (frotis positivo en esputo), que son los responsables del 50% de las infecciones en sus convivientes menores de 15 años.
Intimidad del contacto y su duración en el tiempo
Se ha demostrado que la intimidad del contacto y el tiempo de exposición son factores fundamentales en la transmisión de la enfermedad. Incluso en contactos de enfermos bacilíferos, sólo se infectan el 4% de los contactos extrafamiliares. En la patogenia de la enfermedad tiene más importancia la exposición reiterada a enfermos, aunque sea menos intensa que la exposición ocasional a fuentes con gran capacidad de contagio.
Tratamiento que recibe el foco
Se estima que bastan 15 días de tratamiento con una pauta que incluya isoniacida y rifampicina para extinguir el riesgo de contagio, aunque persistan bacilos en el esputo demostrables mediante frotis positivo.
En cuanto a la localización de la enfermedad, el riesgo de contagio se incrementa en presencia de cavitación pulmonar y laringitis tuberculosa.
El máximo riesgo de infección se presenta durante los primeros 4 años de vida, disminuye entre los 5 años y la pubertad y es muy reducido a partir de los 25 años. Dado que la inmunidad celular no se desarrolla completamente hasta pasados los primeros 6 meses de vida, la infección puede no ser revelada por la reacción tuberculínica.
Respecto a los factores ambientales, la transmisión se facilita por habitaciones reducidas, mal ventiladas, aire recirculante y aire acondicionado en circuitos cerrados sin control sanitario. Al aire libre la transmisión es mucho más difícil.
Otros factores relacionados con la infección son: a) la frecuencia de la tos, ya que son más contagiosos los enfermos que más tosen, pues éstos son los que exhalan un mayor número de partículas infecciosas; b) el volumen y la viscosidad del esputo: cuando el esputo es poco viscoso resulta más fácil la formación de aerosoles y, por tanto, facilita la transmisión de bacilos; c) la educación: aspectos importantes para prevenir la transmisión son derivados de la conducta del paciente en lo que se refiere a cubrirse la boca al toser o estornudar, la utilización de mascarillas, etc., y d) los factores genéticos, el estado inmunológico y nutricional o las enfermedades inmunodepresoras no se ha demostrado que aumenten el riesgo de infección.
Patogenia
Los pequeños núcleos goticulares portadores de M. tuberculosis alcanzan los alvéolos pulmonares por inhalación, donde ocasionan una reacción inflamatoria. Como es característico del bacilo de Koch, no produce toxinas y, por tanto, la respuesta inmunológica es tardía (es fundamentalmente de tipo celular y puede tardar en aparecer 4-10 semanas), lo cual provoca que la multiplicación bacilar se realice en un principio sin trabas. A partir de este primer foco se puede producir una diseminación, algunos bacilos son transportados por la circulación linfática o dentro de los macrófagos a los ganglios hiliares y del mediastino, desde allí pueden pasar a la sangre, diseminándose por todo el organismo y produciendo las llamadas siembras orgánicas de la tuberculosis. Una vez establecida la respuesta inmunológica, si es insuficiente se produce una enfermedad local, o bien progresa hacia una diseminación de la enfermedad (TB diseminada, TB miliar, meningitis TB). Por el contrario, si la respuesta inmunitaria es adecuada y capaz de controlar la multiplicación bacilar, los bacilos pueden quedar encapsulados en pequeños focos que no progresan a enfermedad (infección tuberculosa),
que sólo se pone en evidencia por una reacción tuberculínica positiva.
En función de la inmunidad del individuo, los bacilos pueden permanecer latentes en estos pequeños focos sin causar manifestaciones clínicas (infección latente) en alrededor del 90% de las personas infectadas. Del 10% restante, el 5% tendrá manifestaciones «tempranas» de la enfermedad en los 5 años siguientes a la exposición, mientras que el otro 5% puede presentar una enfermedad tardía incluso varias décadas después de haberse infectado9,10. Ésta es la denominada tuberculosis secundaria, que está en función de la integridad del sistema inmunitario del infectado y del potencial riesgo de superinfección exógena.
En el caso de personal sanitario que tenga exposición importante, el riesgo de adquirir tuberculosis es de 15% en el primer año si no se administra tratamiento preventivo11 .
El riesgo de enfermar tras la infección tuberculosa está condicionado por una serie de factores, que exponemos a continuación.
Factores que condicionan el riesgo de enfermar1,6,8,12
Factores dependientes del bacilo
Fundamentalmente los que se derivan de su número y virulencia. La virulencia del bacilo tuberculoso resulta variable, tanto por determinación genética como fenotípica.
Factores dependientes del huésped
Resistencia natural, consecuencia de la selección de los individuos más resistentes producida por exposición histórica y repetida de una comunidad a la enfermedad.
Resistencia adquirida, por la infección previa con M. tuberculosis.
Edad: el riesgo mayor de enfermar se sitúa en los primeros 2 años de vida, y en los cuatro primeros la enfermedad puede ser de mayor gravedad, pudiendo cursar entre el 1-3% de los casos con diseminaciones graves. Entre los 6 años y la pubertad disminuye el riesgo de enfermar, incrementándose de nuevo la probabilidad
de enfermar en un 20% en el adulto joven. Posteriormente, el riesgo se mantiene hasta los 65-70 años, en que aumenta de nuevo la susceptibilidad de padecer la enfermedad.
Sexo: la tuberculosis es más frecuente en la edad adulta en los varones.
La raza: no está claro que algunas razas tengan mayor predisposición a padecer enfermedad tuberculosa. Sin embargo, existen estudios que evidencian un mayor riesgo individual en algunas razas. En estudios realizados tanto en asilos como en cárceles se concluye que los individuos de raza negra poseen un riesgo 2 veces mayor de ser infectados que la población de raza blanca ante la misma intensidad de exposición.
Enfermedades asociadas: silicosis, diabetes mellitus grave, neoplasias, pacientes gastrectomizados, en hemodiálisis o trasplantados y todas aquellas enfermedades que cursen con inmunodepresión, fundamentalmente la infección por el virus de la inmunodeficiencia humana (VIH).
Indicadores epidemiológicos
Mortalidad
Se define como la tasa de muertes por tuberculosis (pulmonar y extrapulmonar) por 100.000 habitantes y año. Se diferencia de la mortalidad que se refiere al porcentaje de enfermos que fallecen por causas ajenas a su proceso tuberculoso.
Se estima que, sin tratamiento, alrededor del 50-60% de los pacientes con tuberculosis fallecen en los 5 años siguientes al diagnóstico. Antes de la introducción de la quimioterapia, las tasas de mortalidad eran suficientes para conocer la situación de la endemia en una comunidad. Había una relación entre los distintos índices epidemiológicos, de modo que la incidencia correspondía al doble de la mortalidad, en tanto que la prevalencia era el doble de la incidencia.
Desde la aparición de pautas terapéuticas eficaces contra la enfermedad, la mortalidad se considera un mal indicador de la situación de la tuberculosis en una comunidad, dado que disminuye mucho más rápidamente que la transmisión de la enfermedad.
Una elevada tasa de mortalidad indica la existencia de un sistema de salud defectuoso y una escasa o nula eficiencia de los programas de control de la enfermedad.
Morbilidad
Es la tasa de enfermos por 100.000 habitantes y año. Se debe distinguir dos variables: a) incidencia: número de casos nuevos anuales por 100.000 habitantes, y b) prevalencia: número total de casos existentes durante el año por 100.000 habitantes. Son los enfermos de los años anteriores más la incidencia anual, menos las altas por curación y las muertes.
Infección
La infección tuberculosa revelada por la reacción tuberculínica constituye en la actualidad el índice más representativo para valorar la situación de la tuberculosis en una comunidad. Refleja el pasado y el presente y permite predecir el futuro, ya que permite detectar a los individuos infectados, que son el reservorio endógeno de la enfermedad.
Los índices de infección son:
Incidencia o tasa anual de infección: determina el porcentaje de nuevos infectados o conversores durante un año en un determinado grupo de edad. Para ello se requiere la realización de repetidos tests tuberculínicos sobre un mismo grupo a examen.
Prevalencia: es el porcentaje de la infección acumulada durante los años precedentes.
Riesgo anual de infección (RAI): expresa el porcentaje de la población que será infectada o reinfectada en el transcurso de un año. Puede estimarse directamente en un determinado grupo de edad observando el porcentaje de conversiones durante un determinado período.
La tuberculosis se podrá considerar en fase de eliminación cuando la incidencia (todas las localizaciones de TB) sea inferior a un caso por 100.000 habitantes, y se aceptará su erradicación cuando la tasa de enfermos bacilíferos (tinción positiva en esputo) sea inferior a un caso por 1.000.000 habitantes o cuando la prevalencia de infectados en la población general se sitúe por debajo del 1%. Esta situación tardará aún muchos años en ser alcanzada, incluso en aquellos países en los que la incidencia puede considerarse baja (inferior a 10/100.000 habitantes).
Situación actual de la tuberculosis
La situación epidemiológica de la tuberculosis no es igual en todo el mundo; existen grandes diferencias entre los países subdesarrollados y los industrializados en cuanto al control de la enfermedad.
En el ámbito mundial, la tuberculosis constituye un grave problema de salud pública. En 1993, la Organización Mundial de la Salud (OMS) declaró la tuberculosis como «emergencia mundial», una situación que no se había producido nunca con anterioridad. El objetivo de esta medida fue llamar la atención sobre una enfermedad que, a pesar de ser bien conocida desde antiguo y de tener un tratamiento eficaz, aún no ha podido ser controlada.
El porcentaje de infección en la población mundial es importante y se calcula que alrededor de un tercio de la población mundial está infectada por el bacilo de Koch, un reservorio que seguirá generando casos durante muchos años. En los países subdesarrollados, la situación es mucho mas grave, ya que se encuentra infectada la gran mayoría de la población y el 80% son menores de 50 años. Al afectar fundamentalmente a adultos jóvenes, es fácil comprender que el tributo que cobra la tuberculosis tanto en términos económicos como humanos es enorme.
Se estima que en 1999 se produjeron en todo el mundo 8,4 millones de casos nuevos, frente a los 8 millones de 1997. De continuar esta tendencia, en el año 2005 se producirán 10,2 millones de casos nuevos13.
La tuberculosis es la enfermedad a la que se atribuye el mayor número de muertes causadas por un solo agente. Es la causa del 7% de todas las defunciones y del 26% de las que se pueden prevenir en el mundo14.
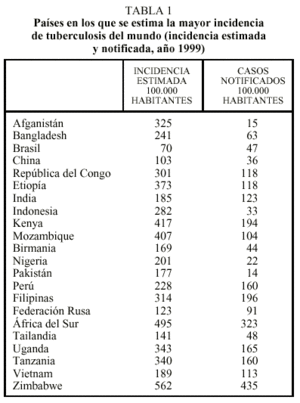
Resulta difícil establecer las tasas de incidencia reales en el ámbito mundial. En los países que disponen de programas de control efectivos, la notificación de casos es muy cercana a la incidencia real de la enfermedad. Sin embargo, en muchos países, fundamentalmente en los países en desarrollo, donde sólo una minoría de la población tiene acceso a los sistemas de salud, la notificación de casos con frecuencia representa sólo una pequeña parte de la verdadera incidencia de la enfermedad. A pesar de ello, la notificación de estos casos bajo condiciones estables dentro de un programa en cualquier país constituye una fuente de información útil acerca del comportamiento de la incidencia y permite obtener las tasas por edad, sexo y grupos de riesgo15.
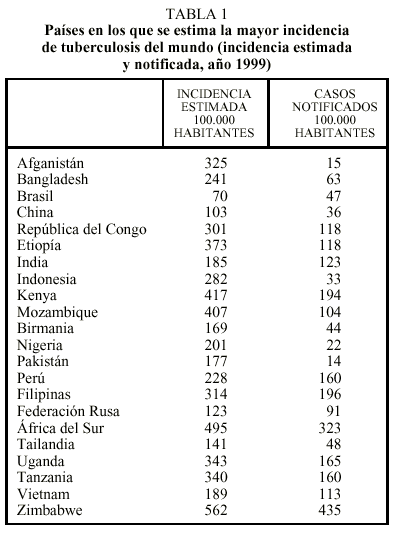
En la tabla 1 se expone la incidencia de casos notificados y de casos estimados de los 22 países con mayor incidencia de tuberculosis del mundo16. Puede comprobarse que existen importantes deficiencias en cuanto a la notificación de casos.
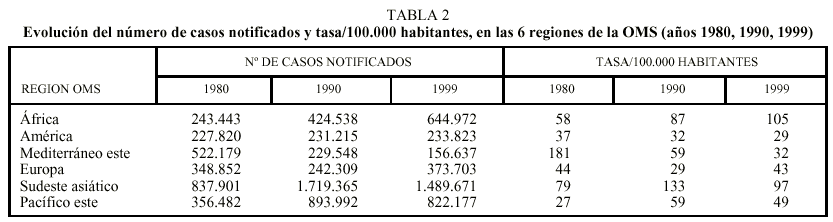
La situación epidemiológica de la enfermedad y la evolución en cuanto al número total de casos y a la incidencia no se comportan de forma homogénea en todas las partes del mundo. En la tabla 2 se observa la evolución del número de casos e incidencia de la enfermedad en 1980, 1990 y 1999 en las 6 regiones de la OMS16.
África es el continente donde la epidemia de tuberculosis continúa incrementándose año tras año, en cuanto al número de casos. En 1999 se notificó un incremento del 37,7% con respecto a 1980. La OMS estimó que a mediados de 1996 había 22 millones de personas en todo el mundo infectadas por el VIH, de las cuales 14 millones (64%) habitaban en África subsahariana. La pandemia del VIH ocasionó un incremento considerable de casos de tuberculosis en una población en la que la infección por M. tuberculosis es importante. Es conocido que el VIH es el factor de riesgo más importante para la evolución de la tuberculosis latente, debido a la intensa inmunodepresión que produce.
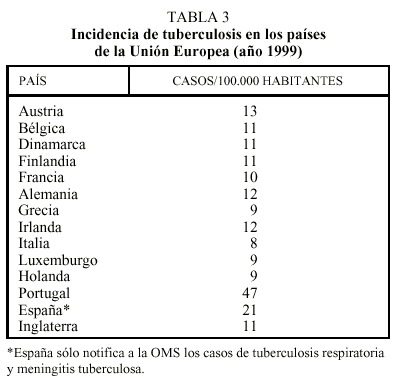
La situación epidemiológica de la tuberculosis en los países industrializados es muy diferente a la de los países en desarrollo. Las tasas de incidencia de la enfermedad presentaron un importante descenso entre los años 1960-1980, evidenciándose lo que se ha denominado «resurgimiento» de la enfermedad entre 1985-1992 en los EE.UU. y Europa17,18. Para justificar este incremento se han argumentado varias razones, como el aumento de la pobreza y de las poblaciones marginales de las grandes ciudades, la inmigración desde países con alta endemia, la aparición de la epidemia por el VIH, etc. Pero, probablemente, la subestimación de esta enfermedad y la creencia de que estábamos ante una afección perfectamente controlada y prácticamente erradicada, que conllevó un descuido en los programas de control, sean la causa más importante del llamado resurgimiento de la tuberculosis en los países industrializados. Hoy día, en Europa existe el modelo epidemiológico habitual de la tuberculosis: los países de la Unión Europea (UE) presentan tasas de morbilidad bajas, entre 5-15 casos por 100.000 habitantes, con excepción de España y Portugal (tabla 3)16, mientras que en los países del este de Europa se presentan tasas que oscilan entre 50-80 por 100.000 habitantes y muchos sobrepasan los 100 casos por 100.000 habitantes. EE.UU. notificó a la OMS en 1999 una tasa de incidencia de 6 casos por 100.000 habitantes.
La situación epidemiológica de España con respecto a la tuberculosis es mala, al presentar tasas muy superiores al resto de los países desarrollados. Esta situación se debe, entre otros factores, a que el control de la tuberculosis en nuestro país ha sido inadecuado19,20.
Se estima que cada año se producen entre 15.600 y 17.500 nuevos casos de tuberculosis (40-45/100.000 habitantes), aunque sólo se contabiliza la mitad al existir una importante infradeclaración16,21,22.
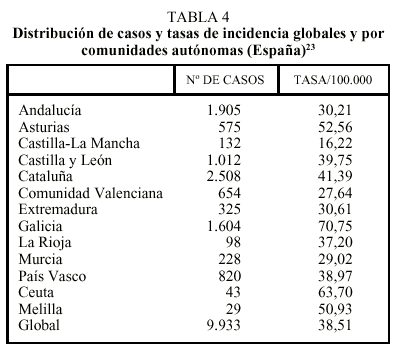
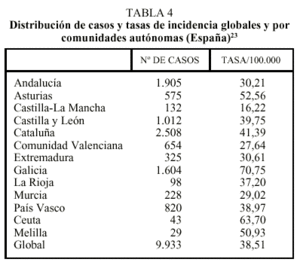
Entre 1996 y 1997 se realizó un estudio en 13 comunidades autónomas (CCAA)23 que abarcaba al 67% de la población española, observándose una incidencia de la enfermedad tuberculosa de 38,51 casos/100.000 habitantes. Se demuestran variaciones importantes de la incidencia de la enfermedad entre las CCAA participantes, en un rango que oscila desde 16,22 casos en Castilla-La Mancha a 70,75 casos en Galicia (tabla 4). Con respecto al sexo, el 67% correspondía a varones y el 33% a mujeres; el 61% de los casos era menor de 45 años, lo que refleja que en nuestro país es todavía una enfermedad de jóvenes. En cuanto a la localización de la enfermedad, fue pulmonar en el 70% de los casos. El factor de riesgo que con más frecuencia se documentó asociado fue la infección por el VIH en un 17,7% del total de enfermos, existiendo amplias variaciones entre las CCAA en un rango que se sitúa entre el 7% de Ceuta y el 8,7% de Galicia o el 27,2% de Andalucía. En cuanto a los casos con localización pulmonar, se documenta confirmación bacteriológica del diagnóstico (cultivo para M. tuberculosis positivo) en el 65,1% de los casos.
La incidencia de enfermedad tuberculosa que demuestra este estudio es similar a la comunicada por la Sociedad Española de Neumología y Cirugía Torácica (SEPAR), que estimaba la incidencia de la tuberculosis en alrededor de 40 casos/100.000 habitantes21.
Actualmente no existe un programa de prevención y control de la tuberculosis en el estado español. El control de la enfermedad es competencia de las CCAA, aunque algunas aún no tienen programas o éstos se encuentran poco desarrollados. Además, la mayoría no conoce las tasas de cumplimentación terapéutica o no plantea estrategias de tratamientos directamente observados24. Estos programas no pueden considerarse homogéneos ni en su estructura ni desarrollo, planteándose importantes problemas en cuanto al registro y comparación de resultados.
Factores que influyen en la falta de control de la tuberculosis
Resulta difícil comprender cómo esta enfermedad que ha acompañado al hombre desde la más remota antigüedad, cuyo agente etiológico es conocido desde hace más de un siglo (descubierto por Koch, en 1882) y para la que existe un tratamiento eficaz, continúa siendo un importantísimo problema de salud pública a comienzos del siglo xxi.
Entre los factores que han impedido el control de la enfermedad se encuentran:
Falta de financiación para programas de control de la tuberculosis debida al escaso apoyo gubernamental a los programas de control de la enfermedad, en cuanto
a la falta de financiación y/o a la mala planificación de los mismos.
El deterioro de las condiciones de vida en amplios sectores de la población, fundamentalmente en los países subdesarrollados, que presentan una precaria situación económica, agravada por las guerras y hambrunas, ha influido de forma negativa en el control de la tuberculosis.
La consideración por parte de los profesionales sanitarios de que la tuberculosis era una enfermedad del pa-
sado y que estaba controlada y prácticamente erradicada.
El fenómeno de la emigración de países endémicos a países desarrollados hace que la tuberculosis mantenga su presencia en todo el mundo. Este fenómeno ha influido de forma importante en la situación de la enfermedad en los países desarrollados, constituyendo uno de los factores más importantes que ha modificado la tendencia a la disminución de la enfermedad25. La tuberculosis es y ha sido una afección ligada al fenómeno de la emigración y, de forma paradójica, la gran mayoría de los inmigrantes de los países industrializados proceden de las antiguas colonias de la «vieja Europa» que en su día recibieron a emigrantes europeos, quienes diseminaron la enfermedad y condicionaron que años más tarde tuvieran las peores tasas de tuberculosis del planeta26.
La aparición de formas de tuberculosis resistente a fármacos: los casos de tuberculosis resistente a fármacos no son un fenómeno nuevo. En 1944, recién introducida la estreptomicina como fármaco esencial en el tratamiento, se describieron cepas resistentes a la misma.
En toda colonia bacilar virgen, es decir, que nunca haya estado en contacto con fármacos antituberculosos, los bacilos se multiplican y se comportan como sensibles en su totalidad hasta alcanzar un número determinado (que varía para cada fármaco), momento en que de forma espontánea y por causas desconocidas empiezan a aparecer mutantes resistentes27. Esta mutación es un azar accidental independiente del medio, pero que está en función del número de población bacilar, del tipo de fármaco administrado y de su concentración. Existe para cada fármaco un mayor número de mutantes cuando se utilizan concentraciones bajas que cuando éstas son elevadas28,29. La resistencia natural (que aparece en cualquier colonia bacilar) es la que obliga a utilizar en el tratamiento 3 fármacos, para evitar la monoterapia, que eliminaría los bacilos sensibles pero seleccionaría los resistentes al medicamento administrado. Si se utilizan fármacos en monoterapia, inexorablemente aparecerán resistencias y, aunque en un principio la respuesta clínica y bacteriológica sea satisfactoria, con posterioridad se producirá un aumento de la población bacilar a costa de los mutantes resistentes. Por tanto, al administrar 2 o 3 fármacos, la probabilidad de aparición de resistencias es prácticamente nula, ya que se necesitaría una población bacilar tan elevada que no existe lesión capaz de albergarla8. A esto se debe añadir que la resistencia a fármacos antituberculosos es cromosómica, definitiva e irreversible, por lo que la sustancia queda invalidada para el resto de la vida del enfermo.
La tuberculosis resistente a fármacos se puede presentar en pacientes con tuberculosis inicial (nunca tratada anteriormente) o en pacientes con antecedentes de tratamientos antituberculosos anteriores:
1. Tuberculosis resistente en pacientes nunca tratados: consiste en el aislamiento de cepas de M. tuberculosis resistentes a uno o varios fármacos antituberculosos en un paciente que con anterioridad no había recibido tratamiento. El estudio y seguimiento de estas resistencias tiene gran interés epidemiológico, ya que mide y alerta sobre las cepas circulantes resistentes con capacidad contagiante en una comunidad2,4. Estudios realizados en zonas urbanas de todo el mundo30,31 confirman una tasa muy elevada de transmisión reciente, sobre todo entre personas con tuberculosis multirresistente (TBMR) (se define TBMR como aquel caso que presenta resistencias a dos o más fármacos entre los que se encuentran al menos la isoniacida y la rifampicina). En la ciudad de Nueva York se ha descrito la diseminación de la denominada cepa W, resistente a 6 o 7 fármacos. Esta transmisión se atribuye a un mal control de la enfermedad33.
2. Resistencia a fármacos en pacientes previamente tratados: se refiere a la aparición de resistencias en un paciente en el curso del tratamiento, en el que previamente se había diagnosticado una cepa de M. tuberculosis sensible. Esto sucede como consecuencia de: a) mala adhesión al tratamiento: el paciente cumple incorrectamente el tratamiento, b) indicación de pautas de tratamiento incorrectas y/o dosificación inadecuada, y c) problemas de malabsorción a fármacos34,35.
El estudio de este tipo de resistencias tiene un interés fundamentalmente clínico ya que puede proporcionar una idea aproximada del grado de idoneidad con que se realizan los tratamientos antituberculosos en el ámbito poblacional estudiado31.
De forma general podríamos decir que la aparición de resistencias en pacientes diagnosticados por primera vez de tuberculosis (no tratados con anterioridad) es el resultado de un fallo en las estrategias de prevención de un programa, mientras que la aparición de resistencias en pacientes en los que se instaura un retratamiento (previamente tratados) se puede considerar como un fracaso de los mecanismos de control del programa.
La situación mundial en cuanto a la tuberculosis resistente no es bien conocida debido a la carencia de medios (técnicas de laboratorio estandarizadas), fundamentalmente en los países subdesarrollados, que son los que acumulan la mayor parte de los casos. Por otra parte, los estudios realizados han incluido muestras reducidas y poco representativas de la amplia población de enfermos tuberculosos y, por lo general, los resultados no diferencian entre resistencia primaria y secundaria.
La OMS y la Unión Internacional contra la Tuberculosis (UICT) han desarrollado un proyecto de vigilancia de la tuberculosis resistente en el mundo. En el informe del año 200013 se documenta la prevalencia de los casos de tuberculosis resistente en 54 zonas geográficas. Globalmente, el mayor porcentaje de resistencias lo presenta Estonia (36,9%), seguida de la provincia Henan de China (35%), Ivanovo Oblast (Federación Rusa) (32,4%) y Latvia (29,9%). Los porcentajes menores se observan en Uruguay (1,7%), New Caledonia (2,2%), Slovkia (2,9%) y Suiza (3,1%). La media de la prevalencia es del 10% (rango, de 1,7-36,9%). En cuanto a España, tan sólo aporta datos a este estudio la ciudad de Barcelona (prevalencia 3%); el resto del estado español no dispone de datos documentados de la situación de la prevalencia de los casos de tuberculosis resistente. Actualmente, en Galicia se está realizando un estudio de resistencias en el ámbito de la OMS.
La infección VIH/sida
Los pacientes con serología VIH que se infecten por M. tuberculosis tienen un riesgo muy alto de desarrollar una tuberculosis activa en muy breve espacio de tiempo36,37. Se puede considerar la infección por el VIH como el factor de riesgo más importante para la evolución de la tuberculosis latente (infección) a enfermedad tuberculosa, debido a la intensa inmunodepresión que se produce en los pacientes infectados por el VIH. El riesgo anual de infección en un paciente infectado por ambos microorganismos es del 5-15%, dependiendo del grado de inmunodepresión38. No se ha demostrado el impacto de la infección por el VIH en la transmisión de la enfermedad. En una revisión de 17 casos sobre la contagiosidad de los pacientes coinfectados VIH-TB, sólo en dos se les imputa una mayor capacidad de transmisión39 y 14 no la demuestran40, criterio apoyado por un extenso trabajo de los CDC41.
En 1996, la OMS estimó que 22 millones de personas estaban infectadas por el VIH en todo el mundo, de las cuales 14 millones (64%) habitaban en África subsahariana. En esta zona la coinfección VIH-TB alcanza cifras del 30-60%.
En cuanto a nuestro país, los resultados del estudio multicéntrico sobre tuberculosis23, referidos a 13 CCAA (66,5% de la población estatal) evidencian un importante porcentaje coinfección VIH-TB, de casi un 20%. Aunque el dato es elevado, no es sorprendente debido a que España es el país europeo que presenta una mayor incidencia anual de sida y que el grupo de riesgo más representado es el de los usuarios de drogas por vía parenteral (UDVP), que también presenta una elevada tasa de infección por M. tuberculosis. Se evidencian importantes diferencias de coinfección VIH-TB entre CCAA: desde el 7% de Ceuta al 27,2% de Andalucía. En algunas, como Galicia, la coinfección VIH-TB no parece tener excesiva incidencia en la epidemiología de la tuberculosis, presentando unos porcentajes de coinfección VIH-TB durante los años 1996,1997,1998,1999 y 2000 del 9,7, 7,8, 5,4, 5,842 y 4,9%, respectivamente.
Control de la tuberculosis
Estrategia de la Organización Mundial de la Salud (OMS)43
La epidemia de tuberculosis se encuentra fuera de control en una gran parte del mundo, lo cual requiere mayor atención mundial y financiación de programas específicos para controlarla.
Los objetivos generales del control de la tuberculosis consisten en: a) disminuir la mortalidad; b) disminuir la morbilidad y la transmisión de la enfermedad, y c) prevenir el desarrollo de resistencias.
Los principios que deben regir el diseño de los programas de prevención y control de la tuberculosis en los países en desarrollo fueron emitidos en 1974 por el Expert Committee on Tuberculosis de la OMS, y son cuatro: a) debe integrarse en los servicios de salud; b) debe ser nacional y permanente; c) adecuarse a las necesidades de la población, y d) debe facilitarse el acceso de la población a los servicios médicos.
La OMS, tras declarar la tuberculosis como emergencia mundial, estableció la denominada «estrategia DOTS» (DOTS son los denominados tratamientos directamente observados [TDO], que se definen como un método que asegura la adhesión al tratamiento y requiere que un trabajador sanitario u otra persona designada para ello presencie la ingesta de la medicación por parte del paciente), como base de una intervención a ejecutar en el mayor número de países. Esta estrategia basada en los trabajos de la Unión Internacional contra la Tuberculosis (UICT) contenía, además de la instauración de tratamiento directamente observado, cinco grandes puntos44:
Voluntad política de los gobiernos para comprometerse en la lucha antituberculosa en cada país.
Establecer una red mínima de laboratorios con capacidad de realizar baciloscopias (se establece la baciloscopia como base del diagnóstico).
Administrar pautas cortas de tratamiento y TDO a todos los enfermos, al menos durante la primera fase del mismo.
Asegurar el abastecimiento de medicamentos.
Elaborar e implantar un sistema de información que permita evaluar el programa periódicamente.
La implantación de esta nueva estrategia pretende alcanzar el 85% de curaciones, al menos en aquellos pacientes con tuberculosis pulmonar bacilífera. El programa de tuberculosis que alcance esta tasa de curación tendrá el siguiente impacto en la epidemia de la tuberculosis45: a) disminuirán rápidamente la prevalencia y la transmisión de la enfermedad; b) la incidencia disminuirá de manera gradual; y c) menor riesgo de aparición de resistencias.
El éxito de la estrategia TDO exige: a) voluntad y compromiso político; b) posibilidad de realización de baciloscopias ante la sospecha de tuberculosis en atención primaria de salud; c) posibilidad de instaurar tratamientos con pautas cortas; d) abastecimiento adecuado de fármacos, y e) sistema de registro e información que permita una evaluación regular del programa.
En 199916, de los 211 países que envían información a la OMS, se estableció la estrategia DOTS en 127 (60,1%).